Слайд 5
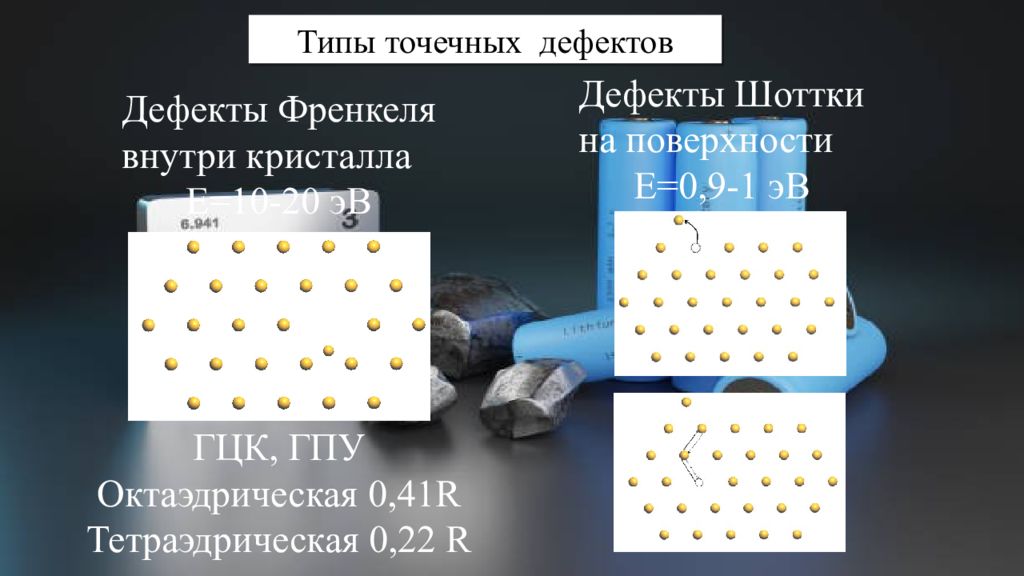
Дефекты Френкеля в нутри кристалла Е=10-20 эВ ГЦК, ГПУ Октаэдрическая 0,41 R Тетраэдрическая 0,22 R Дефекты Шоттки н а поверхности Е=0,9-1 эВ Типы точечных дефектов
Слайд 6
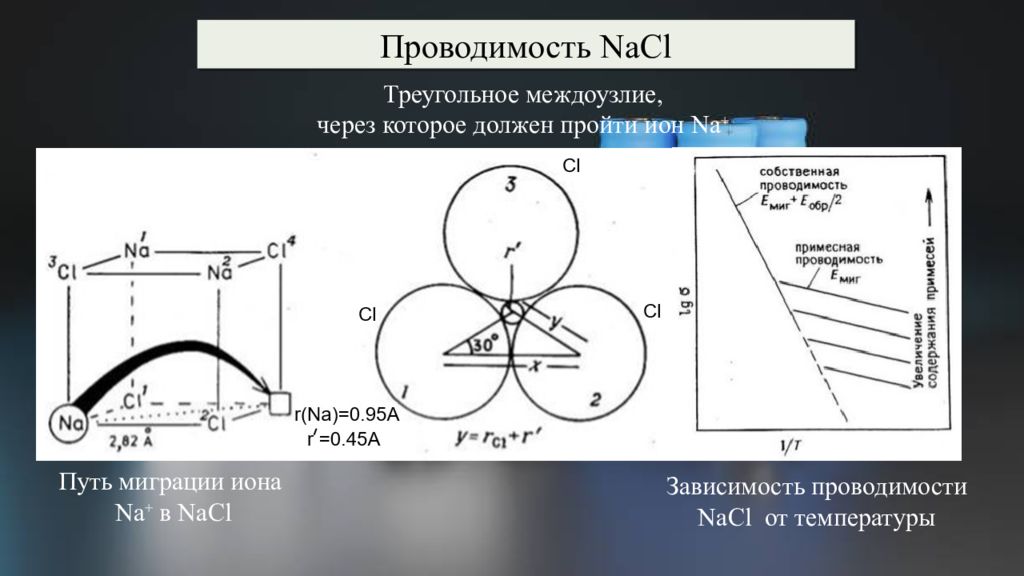
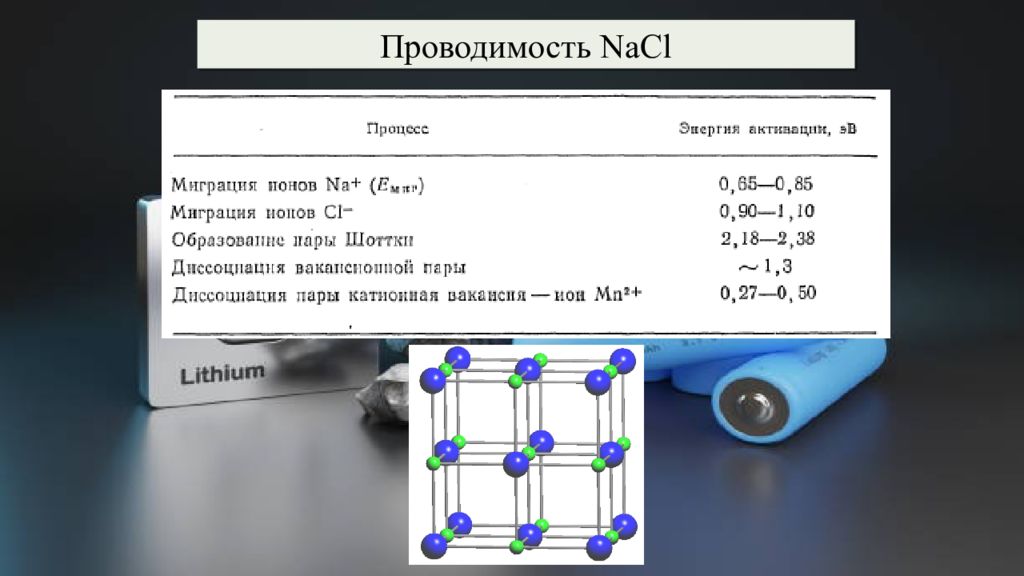
Проводимость NaCl Путь миграции иона Na + в NaCl Треугольное междоузлие, через которое должен пройти ион Na + Зависимость проводимости NaCl от температуры
Слайд 9
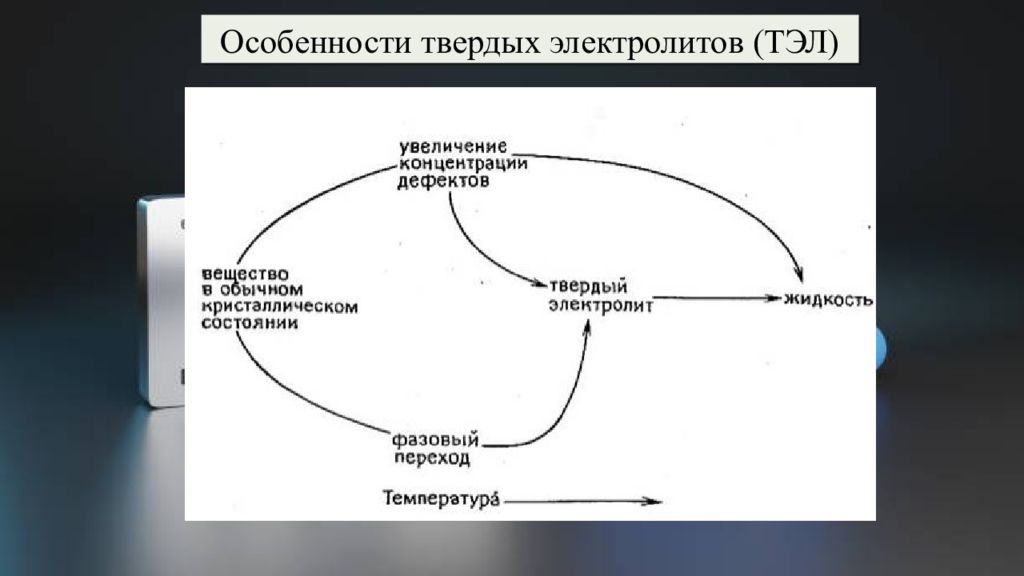
Особенности твердых электролитов (ТЭЛ) Энергетически эквивалентных кристаллографических позиций (в элементарной ячейке) для размещения потенциально подвижных ионов должно быть больше, чем самих ионов. Энергия разупорядочения ионов по позициям и энергия, затрачиваемая на движение, должны быть малыми. Необходимо существование связной сетки "каналов" для движения ионов, в противном случае быстрым будет лишь "локальное" движение частиц (в пределах одной или нескольких элементарных ячеек).
Слайд 11
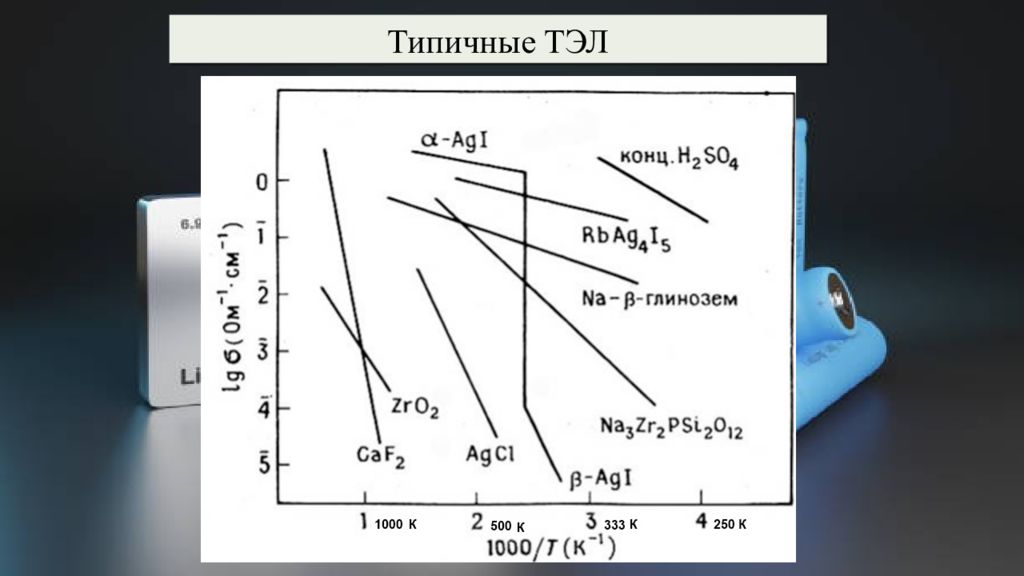
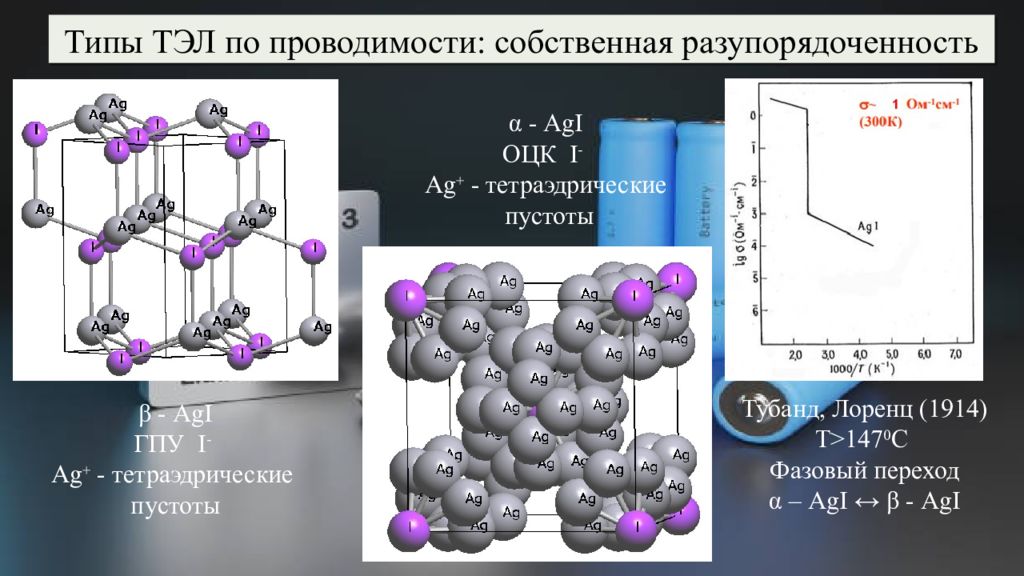
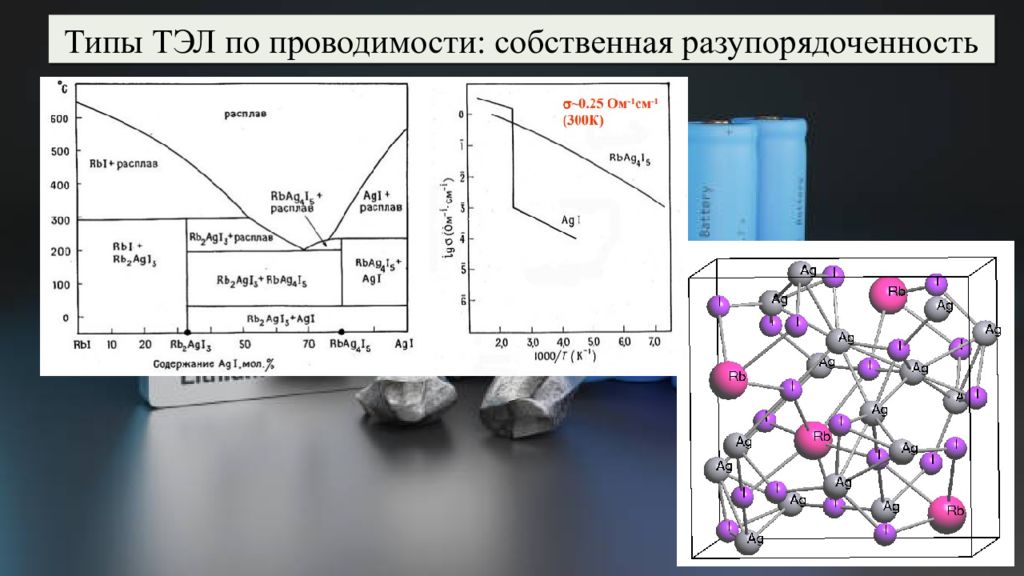
Типы ТЭЛ по проводимости: собственная разупорядоченность β - AgI ГПУ I - Ag + - тетраэдрические пустоты α - AgI ОЦК I - Ag + - тетраэдрические пустоты Тубанд, Лоренц (1914) T>147 0 C Фазовый переход α – AgI ↔ β - AgI
Слайд 13
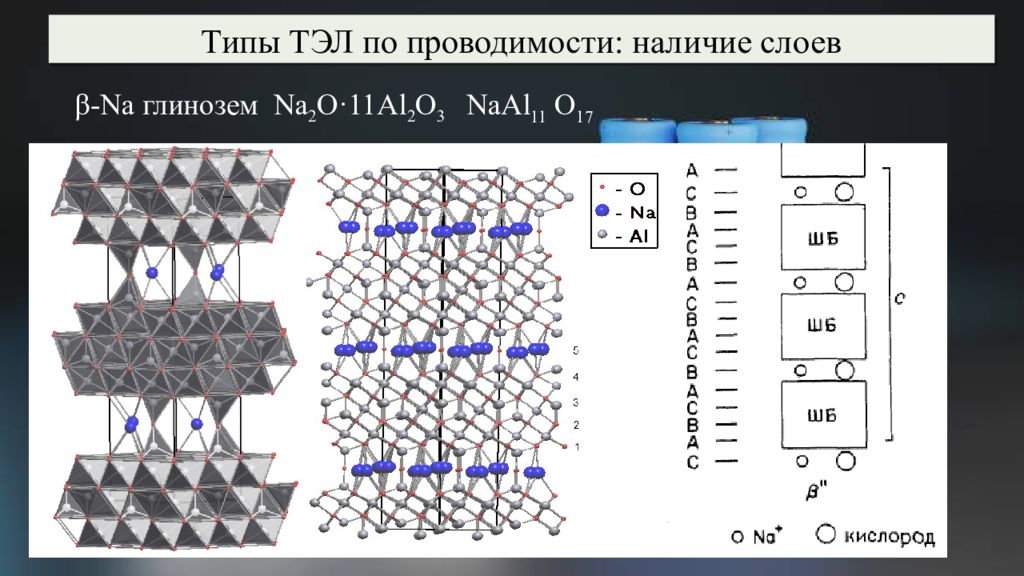
Типы ТЭЛ по проводимости: наличие слоев β - Na глинозем Na 2 O·11Al 2 O 3 NaAl 11 O 17
Слайд 16
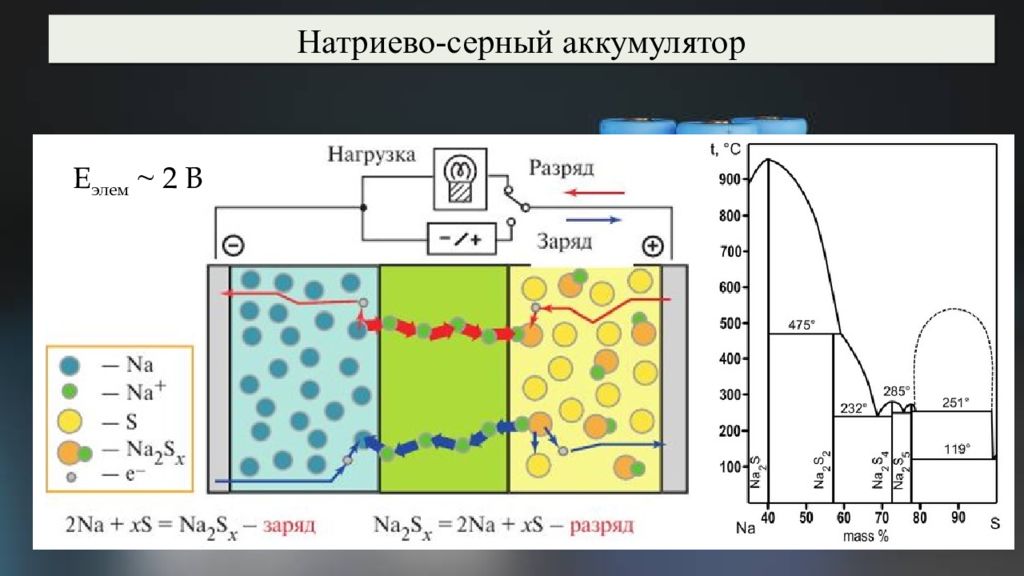
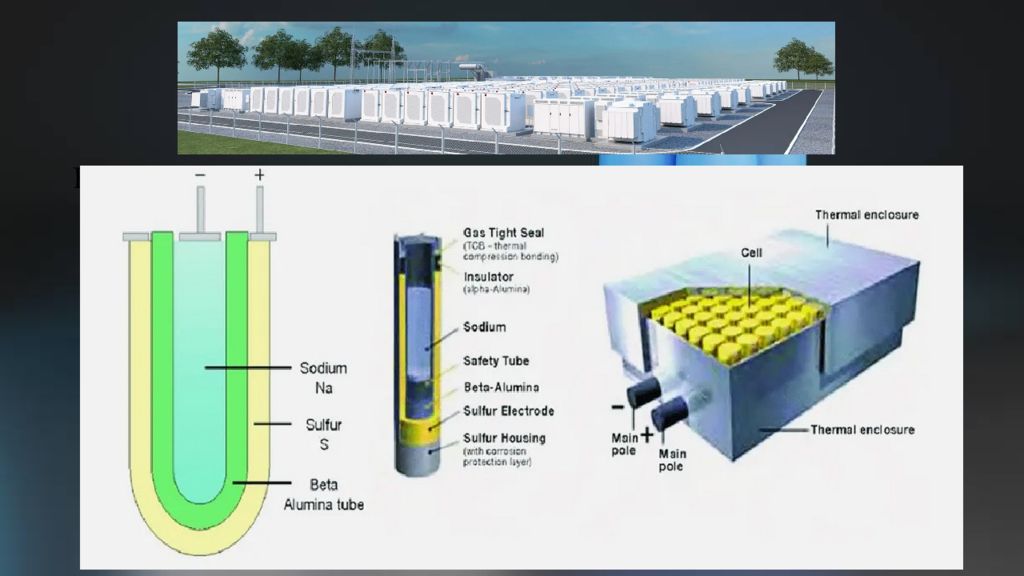
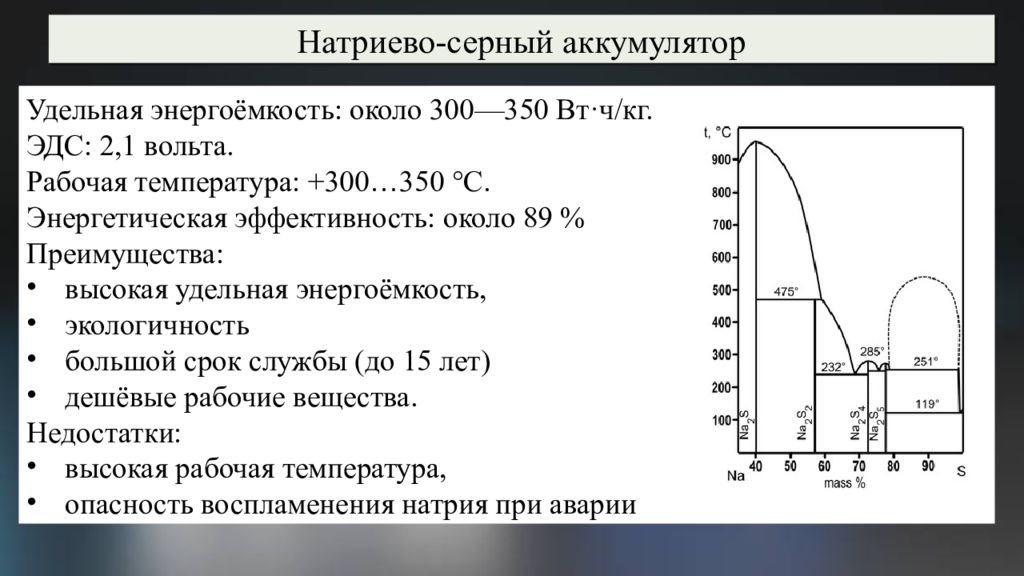
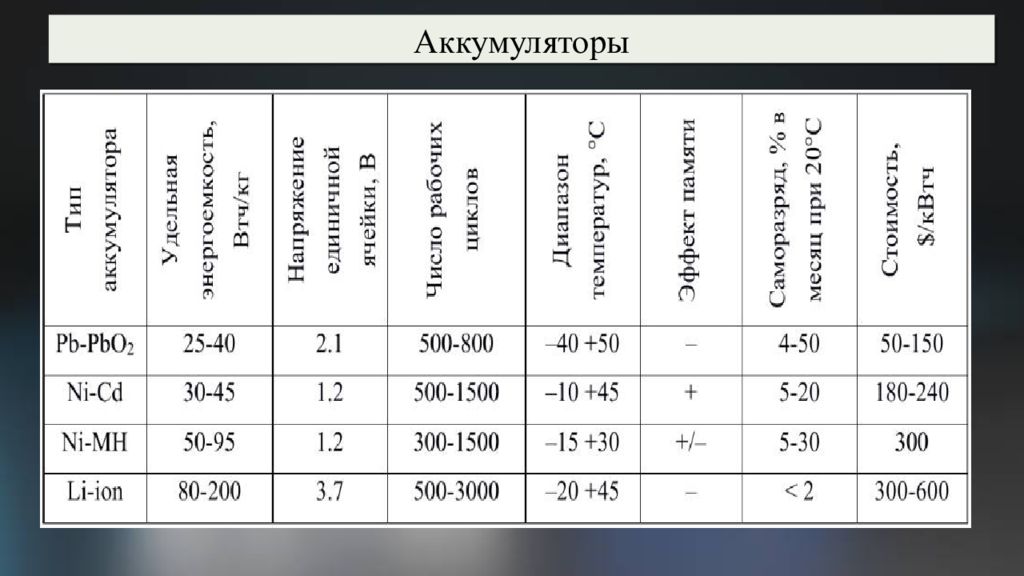
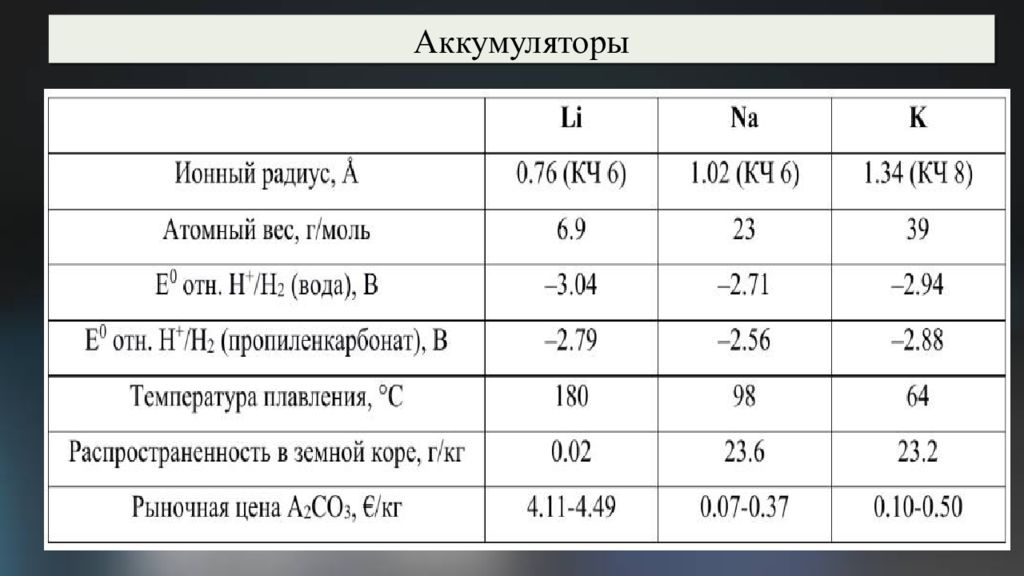
Натриево-серный аккумулятор Удельная энергоёмкость: около 300—350 Вт·ч /кг. ЭДС : 2,1 вольта. Рабочая температура: +300…350 °C. Энергетическая эффективность: около 89 % Преимущества: в ысокая удельная энергоёмкость, э кологичность б ольшой срок службы (до 15 лет) дешёвые рабочие вещества. Недостатки: высокая рабочая температура, опасность воспламенения натрия при аварии
Слайд 17
Натриево-серный аккумулятор Применение: выравнивания нагрузки, резервного питания и стабилизации возобновляемых источников энергии. Аккумуляторы NAS используются для: Электростанции Подстанции Промышленного производства Жилого фонда Стоимость Na-ion аккумуляторов составляет около 40 долларов за кВтч, стоимость литий-ионных аккумуляторов составляет около 137 долларов за кВтч.
Слайд 18
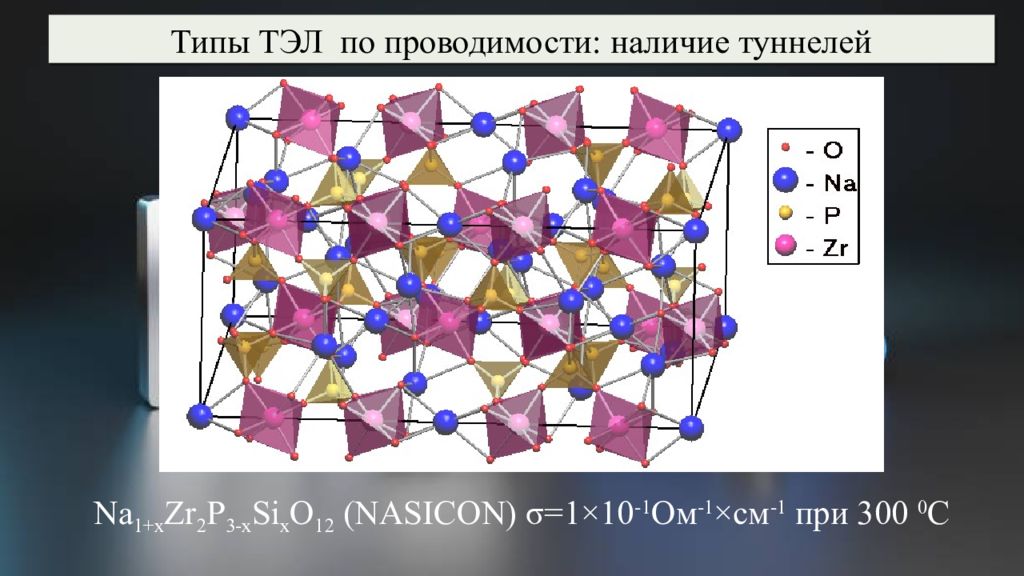
Na 1+x Zr 2 P 3-x Si x O 12 (NASICON) σ =1×10 -1 Ом -1 ×см -1 при 300 0 С Типы ТЭЛ по проводимости: наличие туннелей
Слайд 19
Температурная обработка смеси Na 2 CO 3, NH 4 H 2 PO 4, ZrO 2 и SiO 2 При температуре 440 К происходит удаление газообразных продуктов (NH 3 и H 2 O), при 1170 К происходит разложение карбоната. Образование фазы LiZr 2 (PO 4 ) 3 начинается при температурах синтеза выше 1270 К. Для увеличения содержания продукта проводят многократное повторение отжига с дополнительным перетиранием и прессованием. Золь-гель синтез: P 2 O 5 и SiCl 4 растворяется в дистиллированной воде с образованием растворов фосфорной кислоты (H 3 PO 4 ) и коллоидного раствора SiO 2. Добавляют растворы натриевой и циркониевой солей лимонной в соотношениях, соответствующих составу Na 3 Zr 2 Si 2 PO 12 и нагревают. Насикон получение
Слайд 21
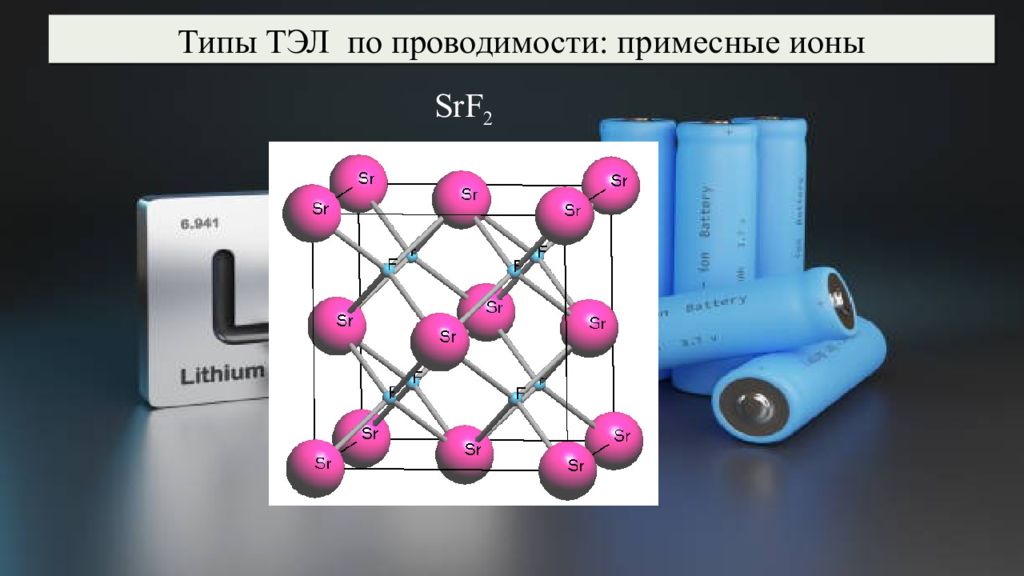
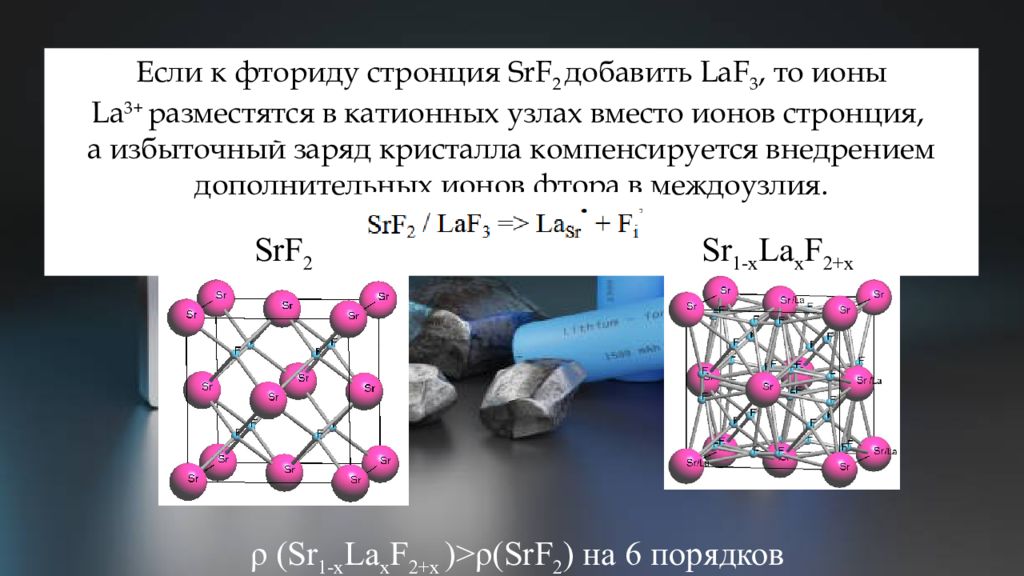
Если к фториду стронция SrF 2 добавить LaF 3, то ионы La 3+ разместятся в катионных узлах вместо ионов стронция, а избыточный заряд кристалла компенсируется внедрением дополнительных ионов фтора в междоузлия. SrF 2 Sr 1-x La x F 2+x ρ ( Sr 1-x La x F 2+x )> ρ ( SrF 2 ) на 6 порядков
Слайд 22
Минерал стронциофлюорит - открыт в 2010 году в Хибинском массиве в ассоциации с ещё одним стронциевым фторидом полежаеваитом -(Се), NaSrCeF 6. В криолитовых копях Гренландии найден минерал ярлит : Na 2 ( Sr,Na ) 14 Al 12 Mg 2 F 64 [(OH), H 2 O] 4. Получение. Взаимодействие оксида или карбоната стронция с плавиковой кислотой: SrCO 3 + 2HF → SrF 2 + H 2 O + CO 2 ↑ Взаимодействие хлорида стронция с фтором: SrCl 2 + F 2 → SrF 2 + Cl 2 ↑ Применение: изготовление твердотельных фторионных аккумуляторных батарей с большой энергоемкостью и энергоплотностью.
Слайд 23
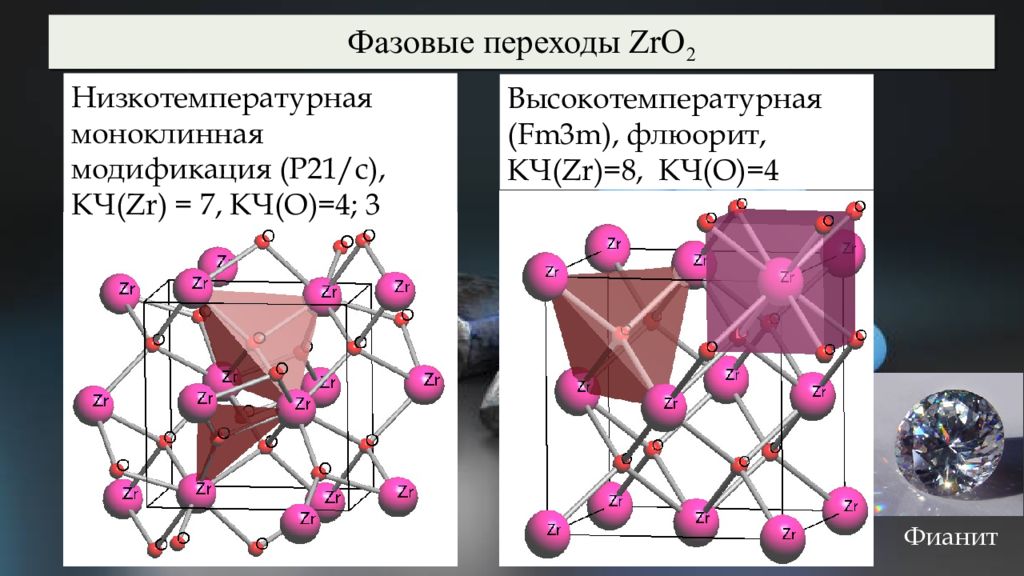
Высокотемпературная ( Fm3m), флюорит, КЧ( Zr )=8, КЧ(О)=4 Фазовые переходы ZrO 2 Фианит Низкотемпературная моноклинная модификация (P21/c ), КЧ( Zr ) = 7, КЧ(О)=4; 3
Слайд 24
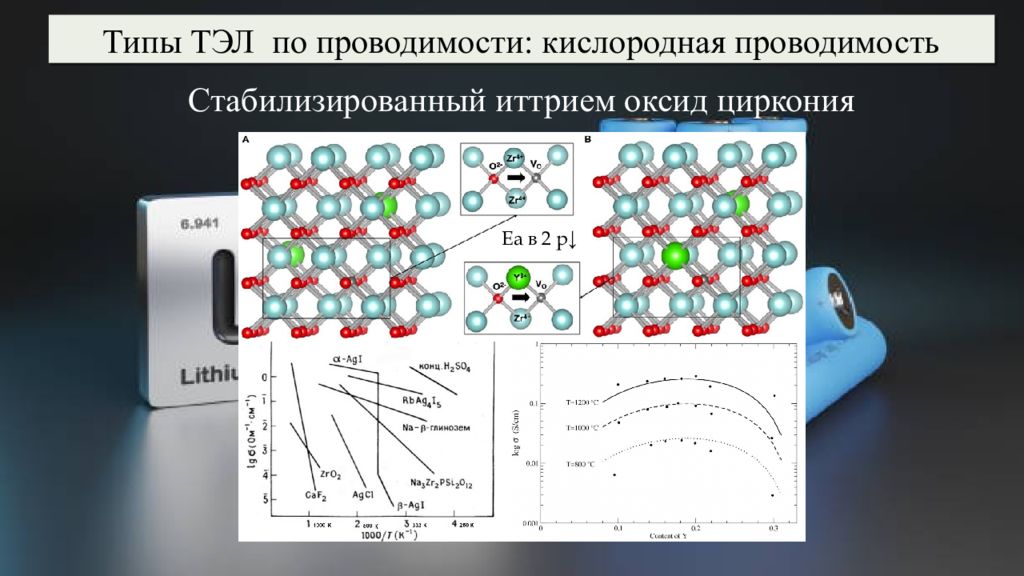
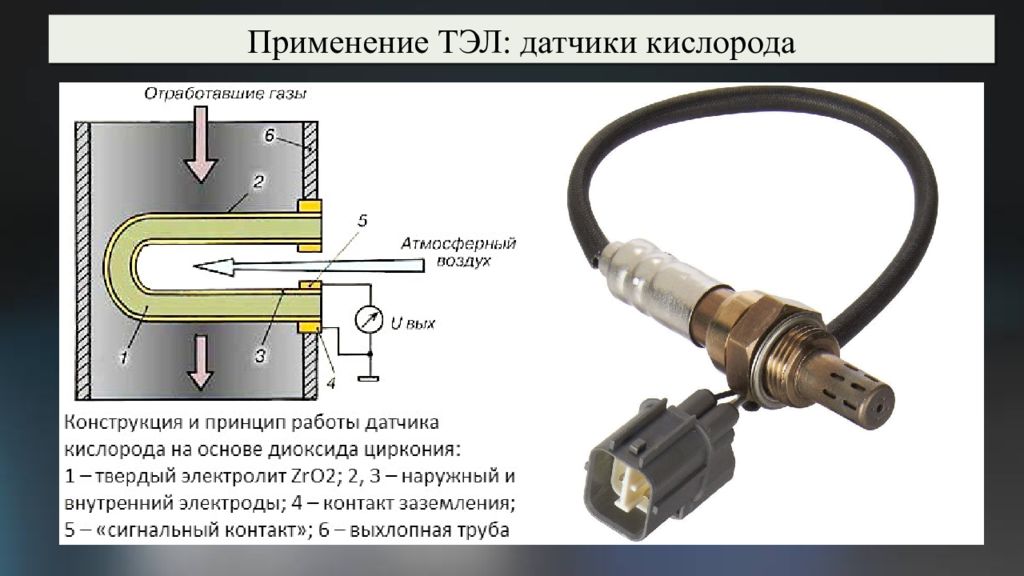
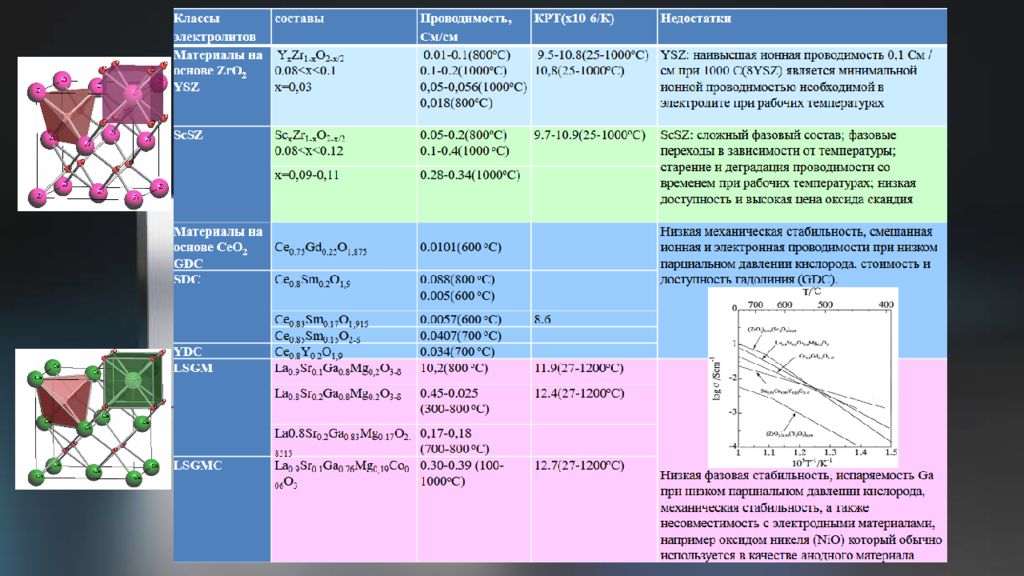
Типы ТЭЛ по проводимости: кислородная проводимость Стабилизированный иттрием оксид циркония Еа в 2 р↓
Слайд 27
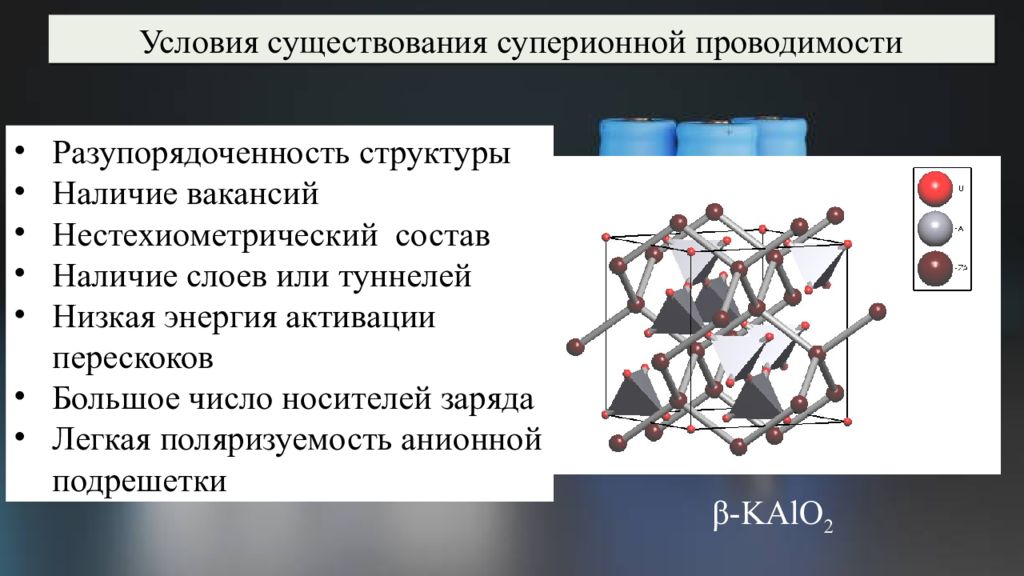
Разупорядоченность структуры Наличие вакансий Нестехиометрический состав Наличие слоев или туннелей Низкая энергия активации перескоков Большое число носителей заряда Легкая поляризуемость анионной подрешетки β- KAlO 2 Условия существования суперионной проводимости
Слайд 28
Методы синтеза ТЭЛ Твердофазный (предотвращение пирогидролиза ) Синтез под высоким давлением: благоприятствует протеканию твердофазной реакции, обеспечивая тесный контакт между частицами реагирующих твердофазных компонент, препятствует разложению нестабильных фаз или возгонке летучих соединений. Золь-гель синтез
Слайд 29
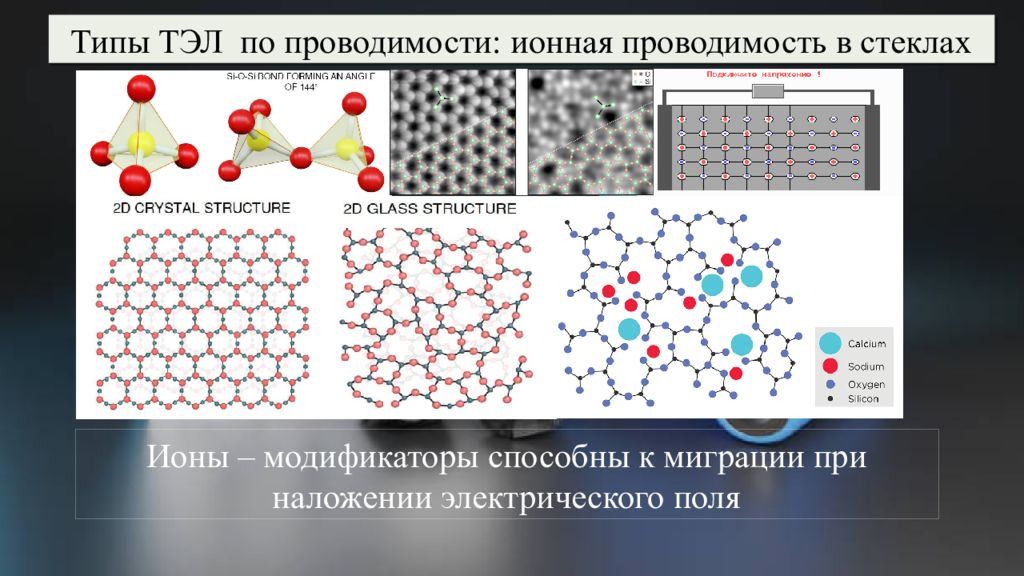
Типы ТЭЛ по проводимости: ионная проводимость в стеклах Ионы – модификаторы способны к миграции при наложении электрического поля
Слайд 30
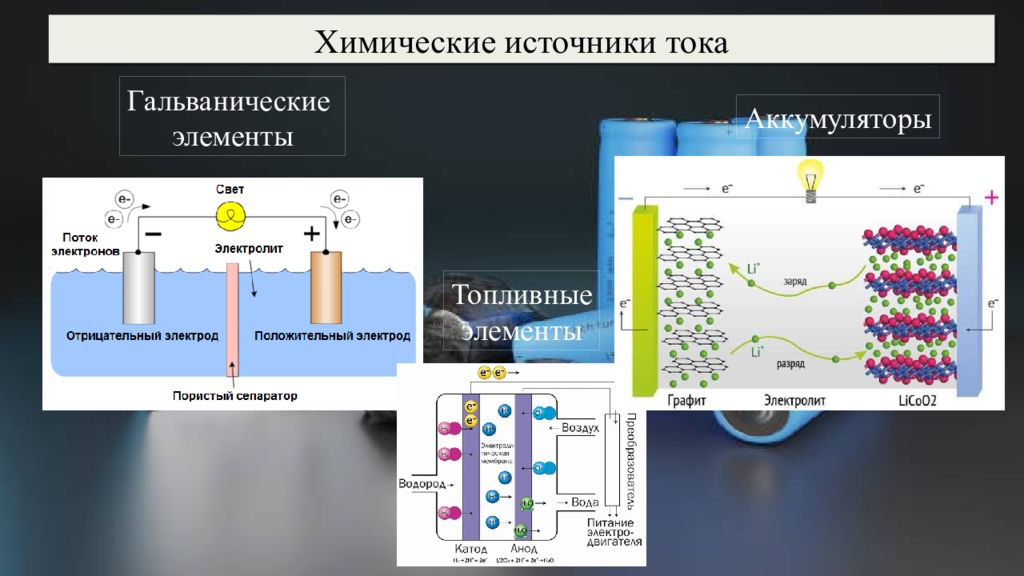
Химические источники тока Гальванические элементы Топливные элементы Аккумуляторы
Слайд 31
Гальванические элементы Солевые батарейки Анод: Zn-2e=Zn 2+ Катод: 2MnO 2 +2H 3 O + +2e=2MnO(OH)+2H 2 O Zn + 2MnO 2 + 2NH 4 Cl → 2MnO (OH) + [Zn (NH 3 ) 2 ]Cl 2 Щелочные ( Alkaline) батарейки Анод: Zn +2OH - - 2e = Zn(OH) 2 Катод: 2MnO 2 +H 2 O+2e=Mn 2 O 3 +2OH - Zn + 2KOH + 2MnO 2 + 2e − → ZnO + 2KOH + Mn 2 O 3
Слайд 33
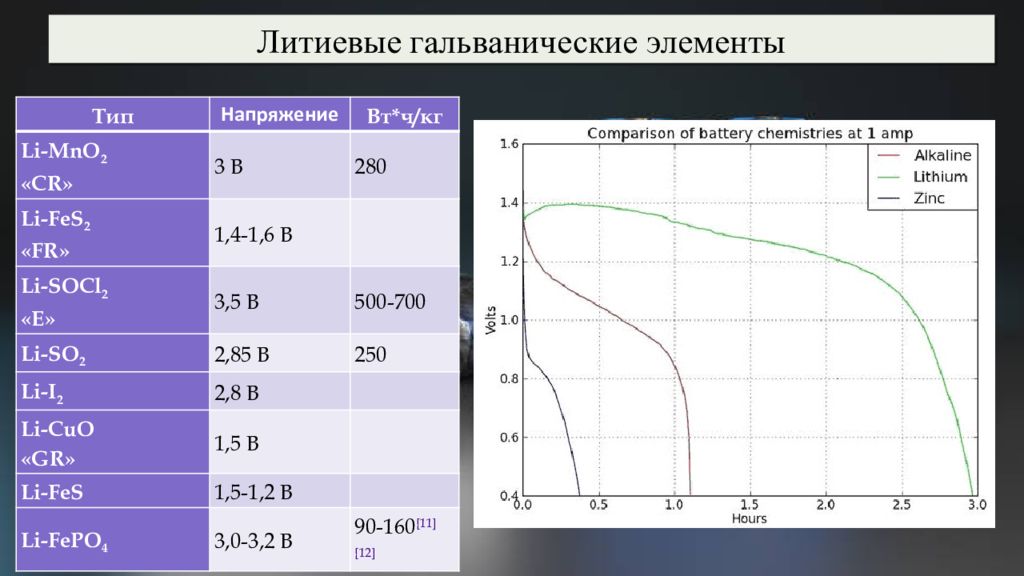
Литиевые гальванические элементы Тип Напряжение Вт*ч/кг Li-MnO 2 «CR» 3 В 280 Li-FeS 2 «FR» 1,4-1,6 В Li-SOCl 2 «E» 3,5 В 500-700 Li-SO 2 2,85 В 250 Li - I 2 2,8 В Li-CuO «GR» 1,5 В Li-FeS 1,5-1,2 В Li-FePO 4 3,0-3,2 В 90-160 [11] [12]
Слайд 34
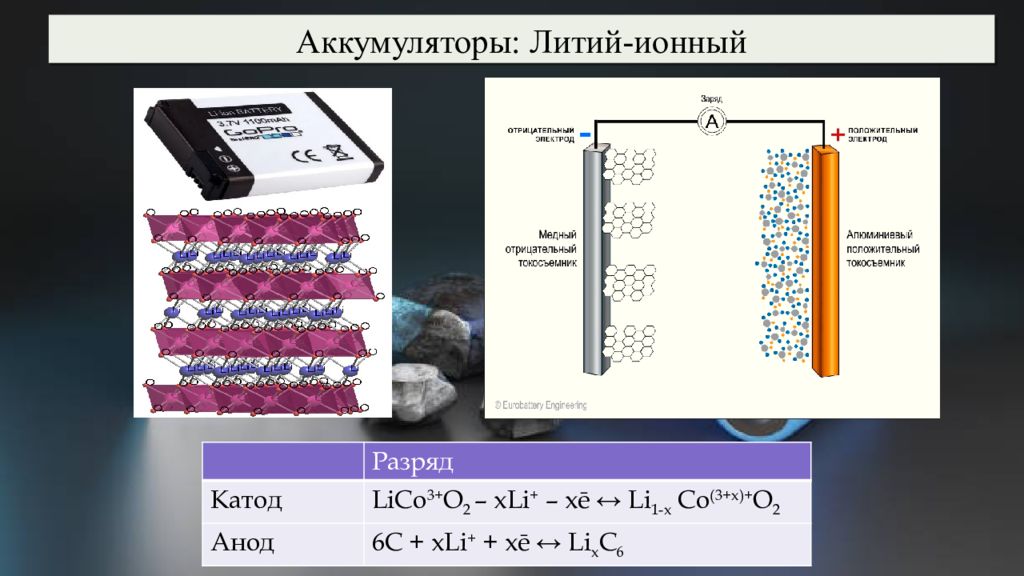
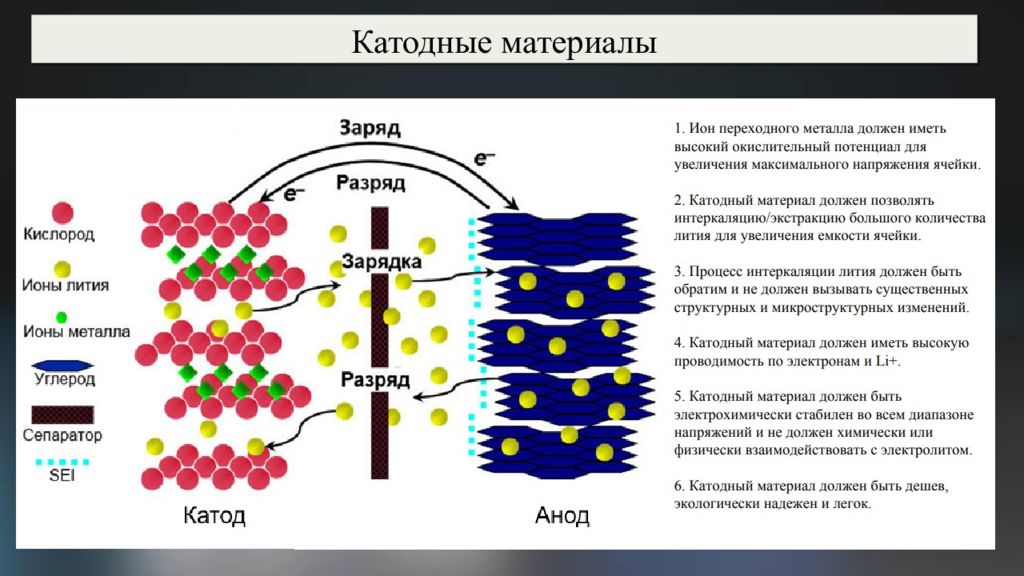
Аккумуляторы: Литий-ионный Разряд Катод LiCo 3+ O 2 – xLi + – x ē ↔ Li 1- x Co (3+ x )+ О 2 Анод 6C + xLi + + xē ↔ Li x C 6
Слайд 35
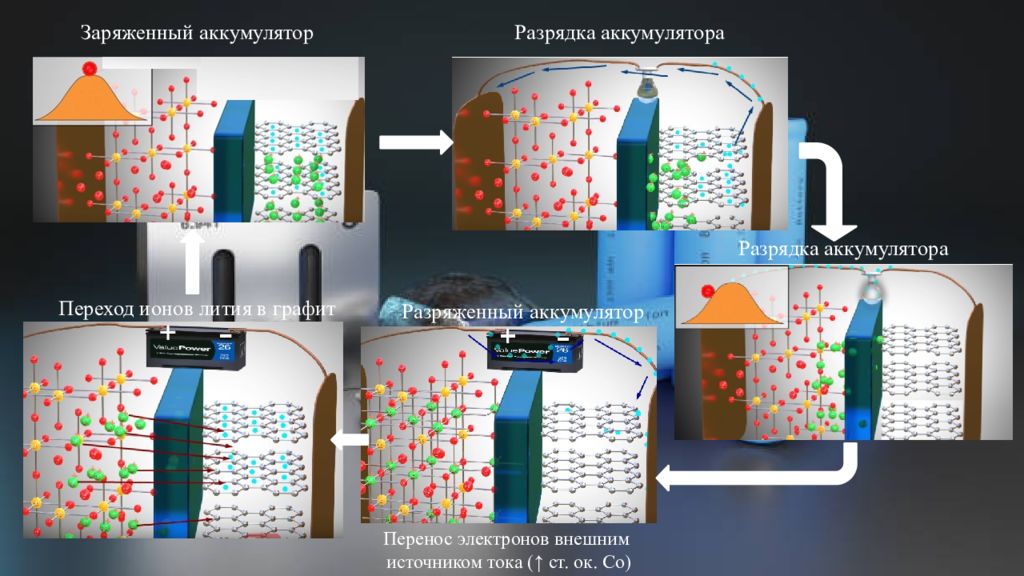
Разрядка аккумулятора Разряженный аккумулятор Перенос электронов внешним источником тока ( ↑ ст. ок. Со) Разрядка аккумулятора Переход ионов лития в графит Заряженный аккумулятор
Слайд 39
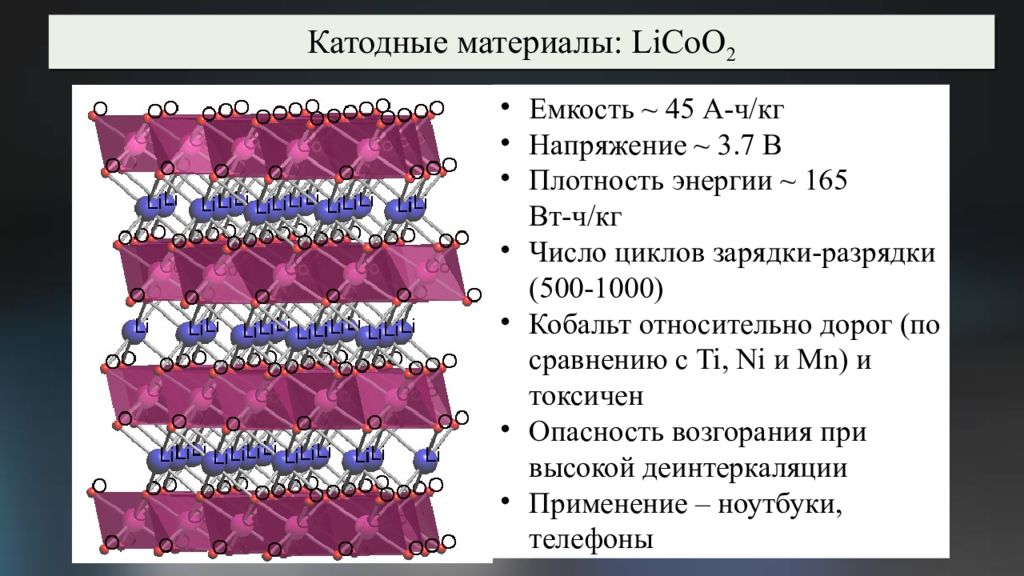
Емкость ~ 45 А-ч/кг Напряжение ~ 3.7 В Плотность энергии ~ 165 Вт-ч/кг Число циклов зарядки-разрядки (500-1000) Кобальт относительно дорог (по сравнению с Ti, Ni и M n) и токсичен Опасность возгорания при высокой деинтеркаляции Применение – ноутбуки, телефоны Катодные материалы: LiCoO 2
Слайд 40
Джон Гуденаф (97 лет), Стэнли Уиттингем, Акира Ёсино Нобелевская премия 2019 Разработка 1985
Слайд 41
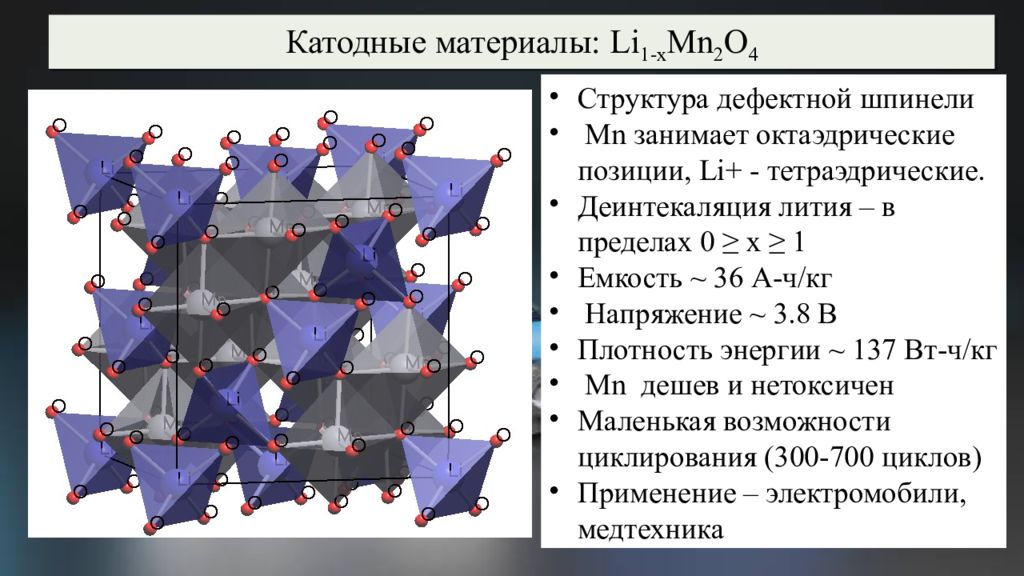
Структура дефектной шпинели Mn занимает октаэдрические позиции, Li + - тетраэдрические. Деинтекаляция лития – в пределах 0 ≥ x ≥ 1 Емкость ~ 36 А-ч/кг Напряжение ~ 3.8 В Плотность энергии ~ 137 Вт-ч/кг Mn дешев и нетоксичен Маленькая возможности циклирования (300-700 циклов) Применение – электромобили, медтехника Катодные материалы: Li 1-x Mn 2 O 4
Слайд 42
Структура оливина : ГПУ кислорода Fe октаэдрические позиции, P - тетраэдрические. Большое количество циклов зарядки-разрядки (1000-2000) Емкость 50 Ач /кг Напряжение ~ 3. 2 В Плотность энергии ~ 90-120 Вт-ч/кг Дешев и нетоксичен Безопасен даже при полной зарядке Применение – электромобили, электросамокаты и велосипеды, источники бесперебойного питания Катодные материалы: LiFePO 4
Слайд 46
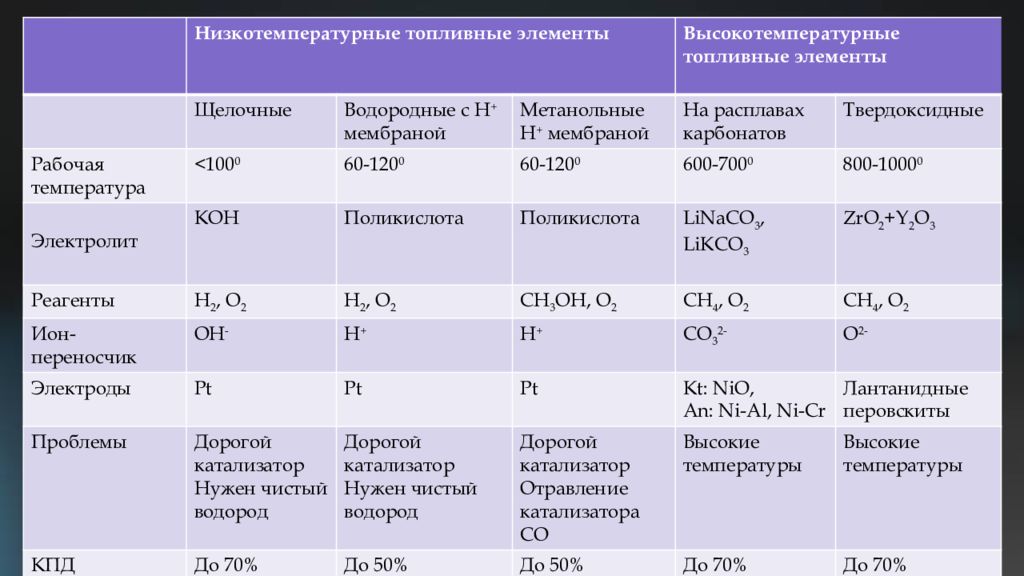
Низкотемпературные топливные элементы Высокотемпературные топливные элементы Щелочные Водородные с Н + мембраной Метанольные Н + мембраной На расплавах карбонатов Твердоксидные Рабочая температура <100 0 60- 1 2 0 0 60- 1 2 0 0 600-70 0 0 800-100 0 0 Электролит КОН Поликислота Поликислота LiNa С O 3, LiK С O 3 ZrO 2 +Y 2 O 3 Реагенты Н 2, О 2 Н 2, О 2 СН 3 ОН, О 2 C Н 4, О 2 C Н 4, О 2 Ион-переносчик ОН - Н + Н + С O 3 2- O 2- Электроды Pt Pt Pt Kt : NiO, An: Ni-Al, Ni-Cr Лантанидные перовскиты Проблемы Дорогой катализатор Нужен чистый водород Дорогой катализатор Нужен чистый водород Дорогой катализатор Отравление катализатора СО Высокие температуры Высокие температуры КПД До 70% До 50% До 50% До 70% До 70%