Слайд 2
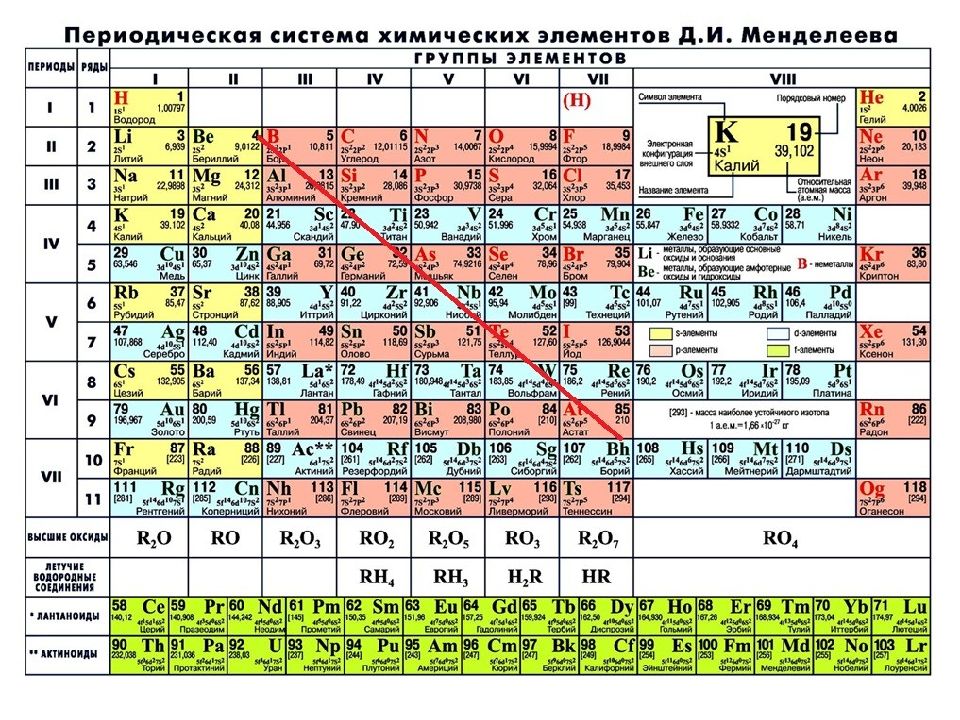
Неметаллы - это химические элементы, которые образуют простые вещества, не обладающие свойствами металлов. В Периодической системе химических элементов Д.И. Менделеева неметаллы находятся только в главных подгруппах
Слайд 4
ОСОБЕННОСТИ СТРОЕНИЯ АТОМОВ НЕМЕТАЛЛОВ: Б ольшое число электронов (4-8) на внешнем энергетическом уровне Исключения: H - 1, He - 2, B - 3. Небольшой атомный радиус, электроны внешнего энергетического уровня прочно связаны с ядром. Высокая электроотрицательность. Валентные электроны располагаются только на внешнем энергетическом уровне. Ковалентная и ионная химическая связь. Атомы некоторых неметаллов образуют аллотропные модификации
Слайд 6
ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ Свойства Характеристика Агрегатное состояние твёрдое (сера, фосфор, кремний, углерод), жидкое (только бром), газообразное (водород, кислород, азот, фтор, хлор ) Цвет различный (сера - жёлтый, бром - красно-бурый, фтор - зелёный, хлор - жёлто-зелёный, иод - фиолетовый, азот, кислород и водород - бесцветные) Блеск отсутствует (исключение - кристаллический иод, кремний и графит) Ковкость отсутствуют, неметаллы в твёрдом агрегатном состоянии хрупкие Пластичность Теплопроводность отсутствует (исключение - графит) Электропроводность отсутствует (исключение - графит и чёрный фосфор, селен и кремний являются полупроводниками)
Слайд 8
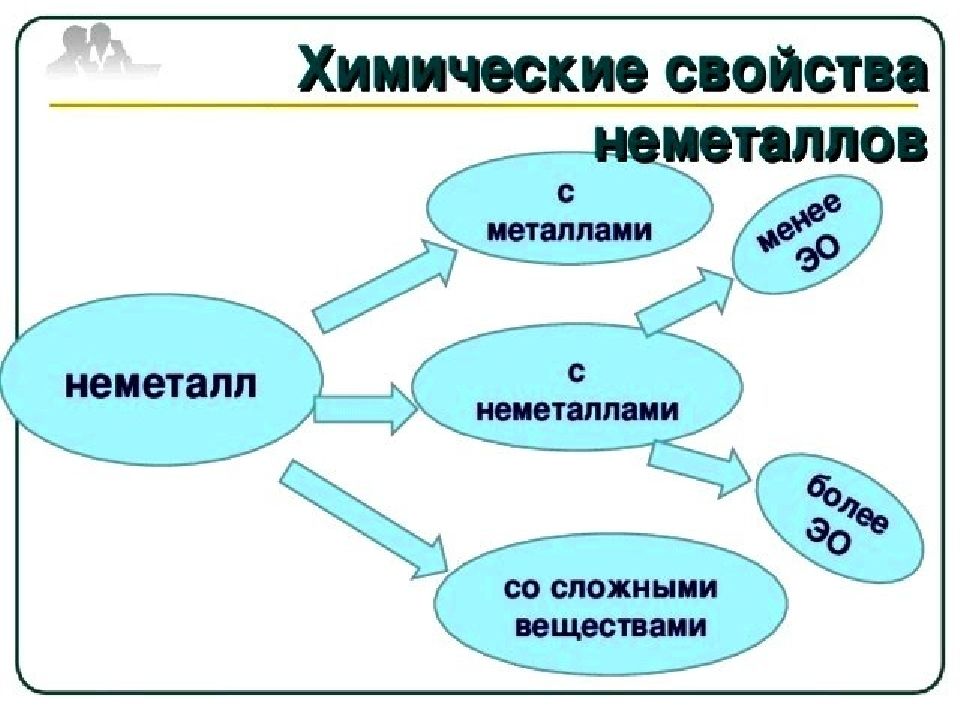
ВЗАИМОДЕЙСТВИЕ НЕМЕТАЛЛОВ С ПРОСТЫМИ ВЕЩЕСТВАМИ Неметаллы + галогены → галогениды: 3 P + 5Cl 2 = 2PCl 5 S + 3F 2 = SF 6 Si + 2F 2 = SF 4 3Cl 2 + I 2 = 2ICl 3 ! Углерод и азот с галогенами не реагируют
Слайд 9
2. Неметаллы + кислород → оксиды: 4 P + 5O 2 = 2P 2 O 5 N 2 + O 2 = 2NO↑ S + O 2 = SO 2 ↑ Si + O 2 = SiO 2 ↓ ! Галогены с кислородом и азотом не реагируют (исключение - фтор): 2 F 2 + O 2 = 2OF 2 ↑
Слайд 10
3. Неметаллы + сера → сульфиды: 2 P + 5S = P 2 S 5 C + 2S = CS 2 Br 2 + S = SBr 2 ! Азот и иод с серой не реагируют
Слайд 11
4. Неметаллы + водород → летучие водородные соединения: Cl 2 + H 2 = 2HCl↑ S + H 2 = H 2 S↑ N 2 + 3H 2 = 2NH 3 ↑ ! Бор с водородом не реагирует ! Фосфор, кремний, водород друг с другом не реагируют !Азот реагирует только с кислородом, водородом и фтором
Слайд 13
РЕАКЦИИ ДИСПРОПОРЦИОНИРОВАНИЯ НЕМЕТАЛЛОВ Хлор, бром и иод (иод в гораздо меньшей степени) диспропорционируют в воде по схеме: Hal + H 2 O = HHal + HHalO Cl 2 + H 2 O = HCl + HClO
Слайд 15
ВЗАИМОДЕЙСТВИЕ НЕМЕТАЛЛОВ (C, P, B, S) С КИСЛОТАМИ-ОКИСЛИТЕЛЯ М И ! Образуется кислота, в которой неметалл находится в высшей степени окисления: неметалл + H 2 SO 4 конц = к-та + SO 2 ↑ + H 2 O 3P + 5 H 2 SO 4 конц = 2 H 3 PO 4 + 5SO 2 ↑ + 2H 2 O S + 2 H 2 SO 4 конц = 3SO 2 ↑ + 2H 2 O неметалл + HNO 3 конц = к-та + NO 2 ↑ + H 2 O C + 4 HNO 3 конц = CO 2 ↑ + 4NO 2 ↑ + 2H 2 O неметалл + HNO 3 разб + H 2 O = к-та + NO↑ B + HNO 3 разб + H 2 O = H 3 BO 3 + NO↑ S + 2 HNO 3 разб = H 2 SO 4 + 2NO↑
Слайд 16
СОЕДИНЕНИЯ НЕМЕТАЛЛОВ Оксиды: безразличные ( N 2 O, NO, CO, SiO ) кислотные ( CO 2, NO 2, SO 3, P 2 O 5 и др.). Гидроксиды : кислоты ( H 2 CO 3, HNO 3, HNO 2, H 2 SO 4, H 3 PO 4 и др.). Летучие водородные соединения: HCl, H 2 S, NH 3, PH 3 и др. (и кислотные и основные свойства)
Последний слайд презентации: НЕМЕТАЛЛЫ И ИХ СОЕДИНЕНИЯ
Вопросы для самоконтроля: Что такое неметаллы? Положение неметаллов в Периодической системе химических элементов Д.И. Менделеева? Особенности строения атомов неметаллов? Физические свойства неметаллов? Какие свойства - окислительные или восстановительные характерны для металлов? Почему? Соединения неметаллов? Нахождение неметаллов в природе?