Первый слайд презентации: ПНИКТОГЕНЫ (элементы V А - группы)
ФОСФОР Подгруппа мышьяка ПНИКТОГЕНЫ (элементы V А - группы)
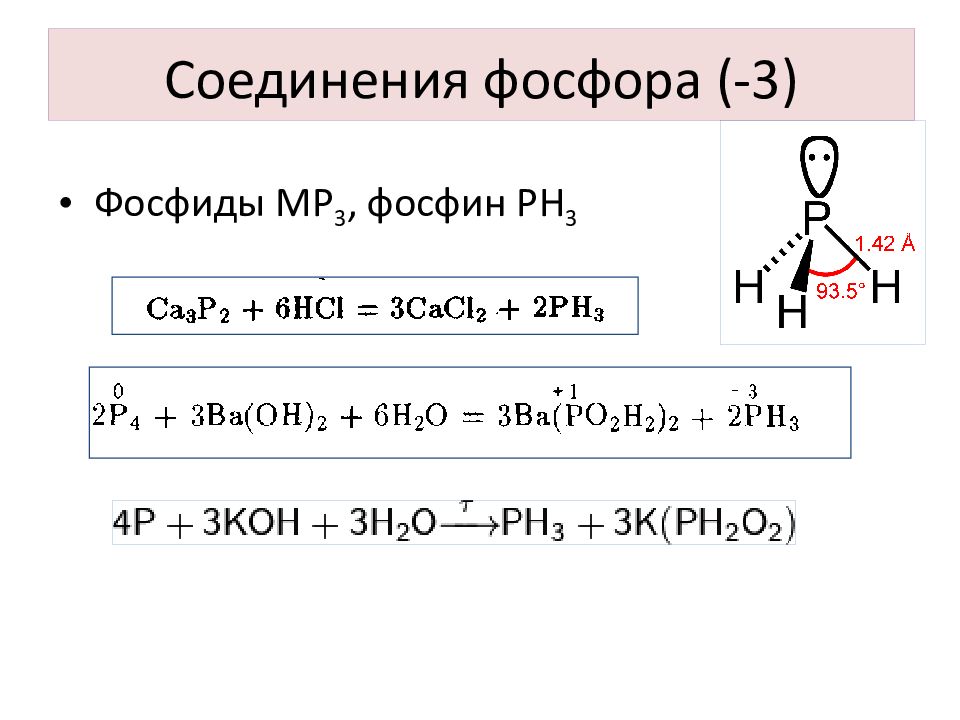
Слайд 6: Соединения фосфора (-3)
Фосфиды МР 3, фосфин РН 3 Соединения фосфора (-3)
Слайд 7: фосфин РН 3
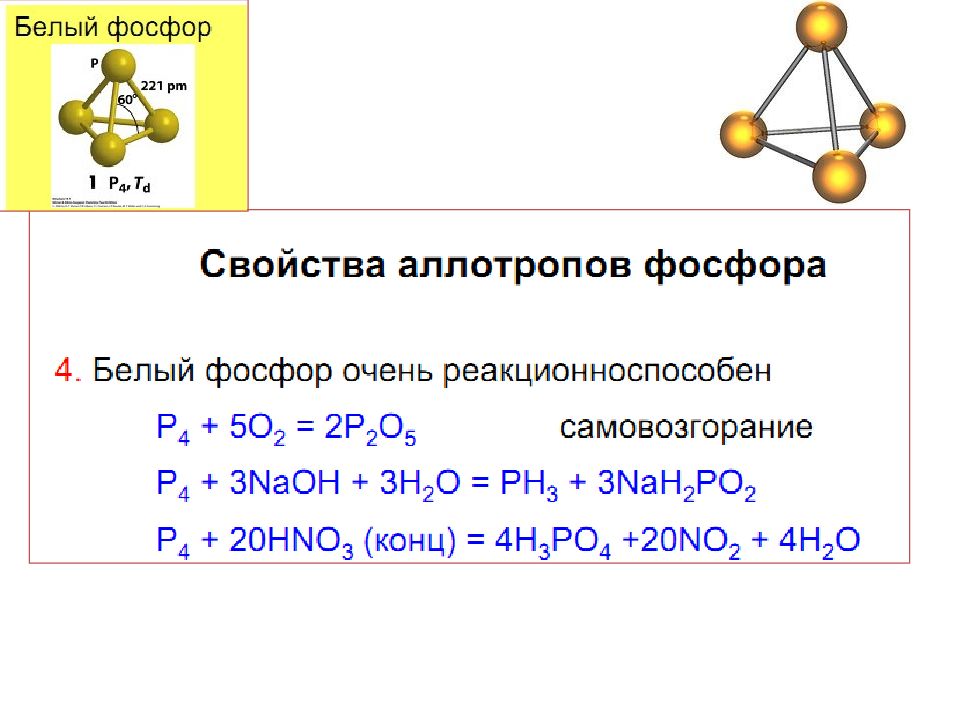
В отсутствие кислорода при нагревании разлагается на элементы: на воздухе самопроизвольно воспламеняется (при температуре свыше 100 °C): Проявляет сильные восстановительные свойства:
Слайд 8
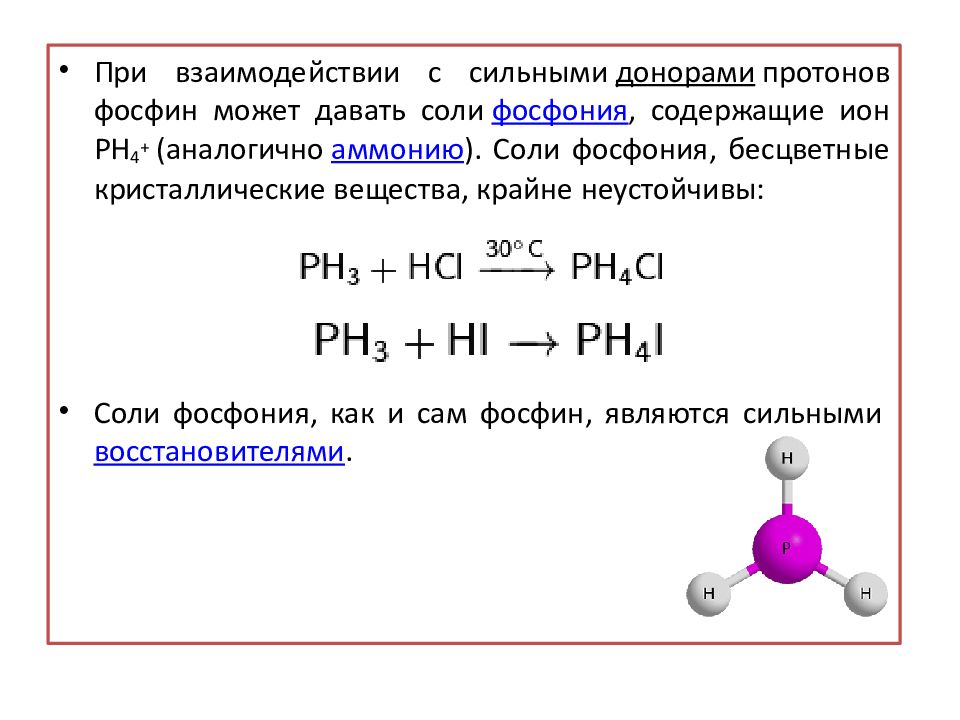
При взаимодействии с сильными донорами протонов фосфин может давать соли фосфония, содержащие ион PH 4 + (аналогично аммонию ). Соли фосфония, бесцветные кристаллические вещества, крайне неустойчивы: Соли фосфония, как и сам фосфин, являются сильными восстановителями.
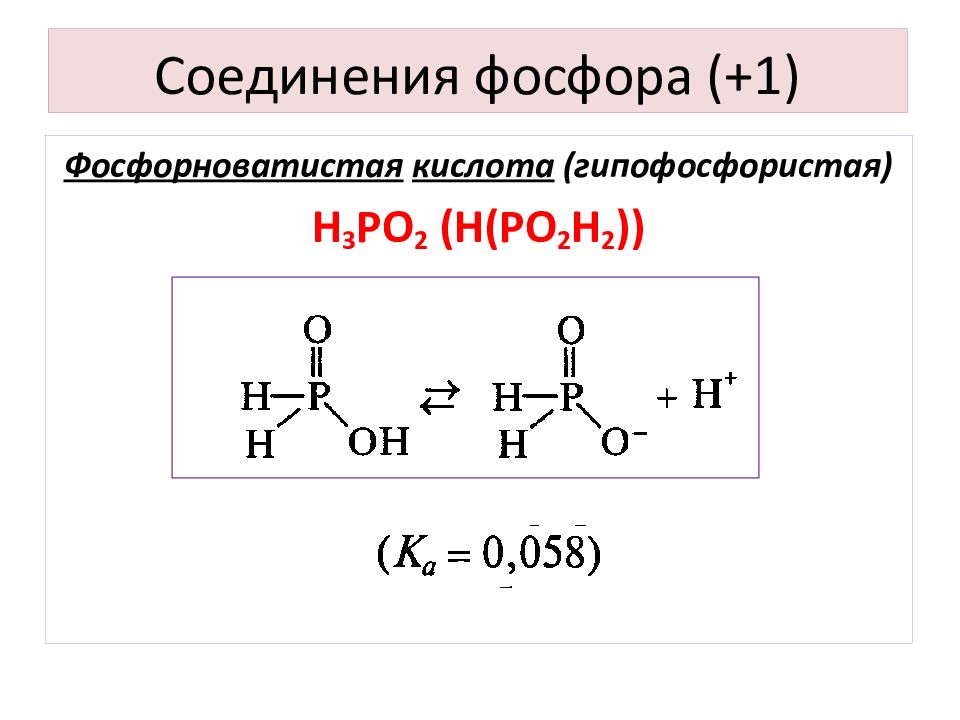
Слайд 10: Соединения фосфора (+1)
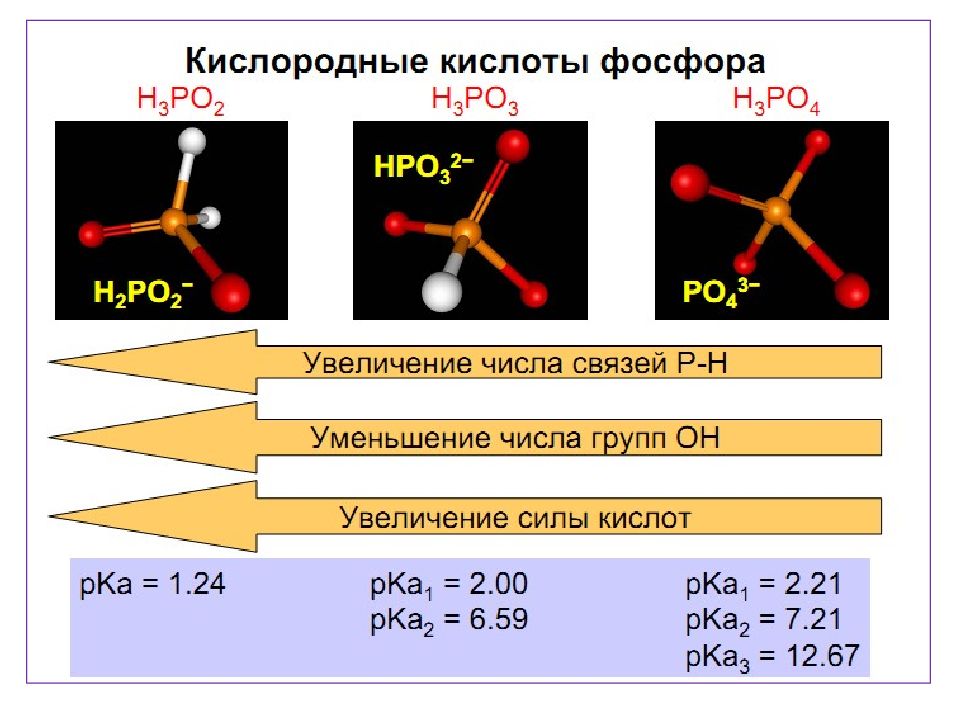
Фосфорноватистая кислота ( гипофосфористая ) Н 3 PO 2 (H(PO 2 H 2 ))
Слайд 11: Соединения фосфора (+1)
Гипофосфит натрия используют при никелировании металлических и неметаллических поверхностей Соединения фосфора (+1)
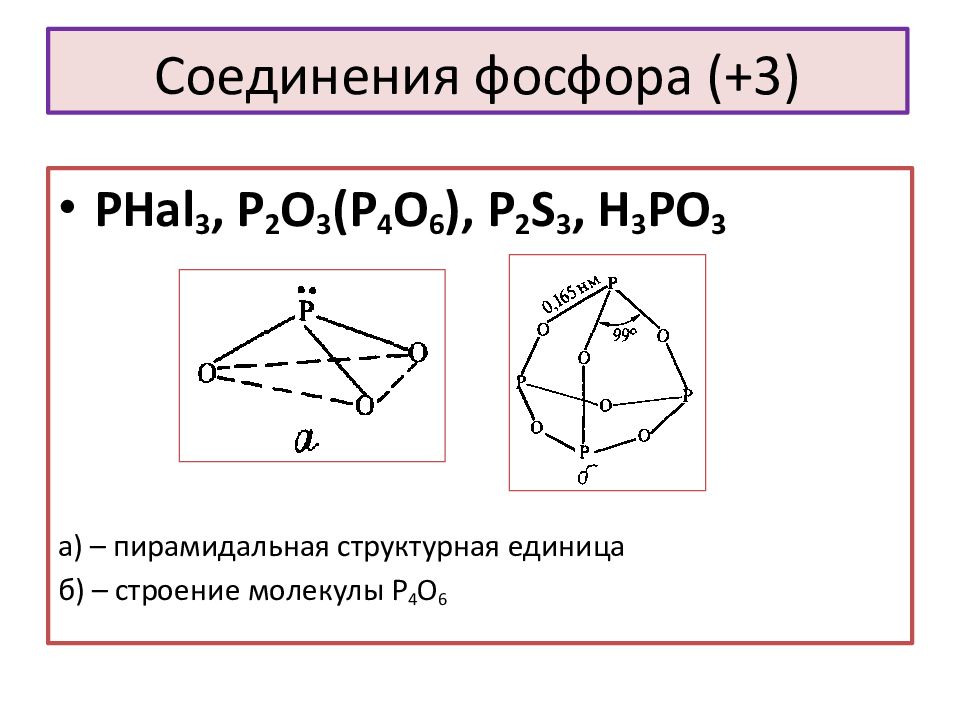
Слайд 12: Соединения фосфора (+3)
PHal 3, P 2 O 3 (P 4 O 6 ), P 2 S 3, H 3 PO 3 а) – пирамидальная структурная единица б) – строение молекулы Р 4 О 6 Соединения фосфора (+3)
Слайд 13
Соединения фосфора ( III ) имеют кислотную природу Гидролиз: Взаимодействие с основными соединениями:
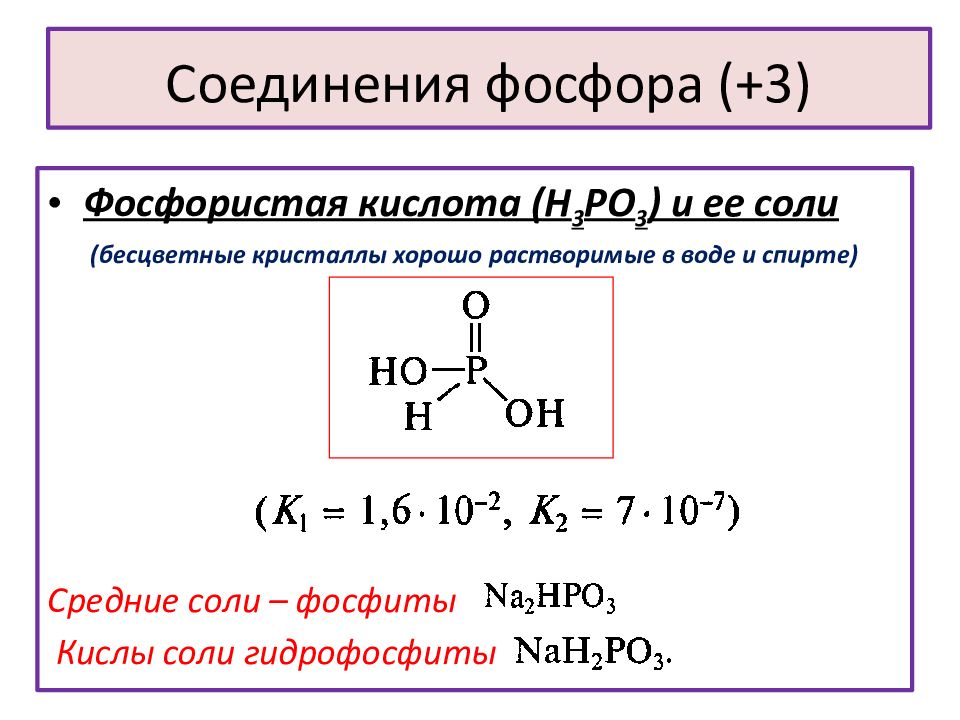
Слайд 14: Соединения фосфора (+3)
Фосфористая кислота (Н 3 РО 3 ) и ее соли (бесцветные кристаллы хорошо растворимые в воде и спирте) Средние соли – фосфиты Кислы соли гидрофосфиты Соединения фосфора (+3)
Слайд 15
Восстанавливает малоактивные металлы из растворов их солей: HgCl 2 + H 3 PO 3 + H 2 O = H 3 PO 4 + Hg + 2HCl
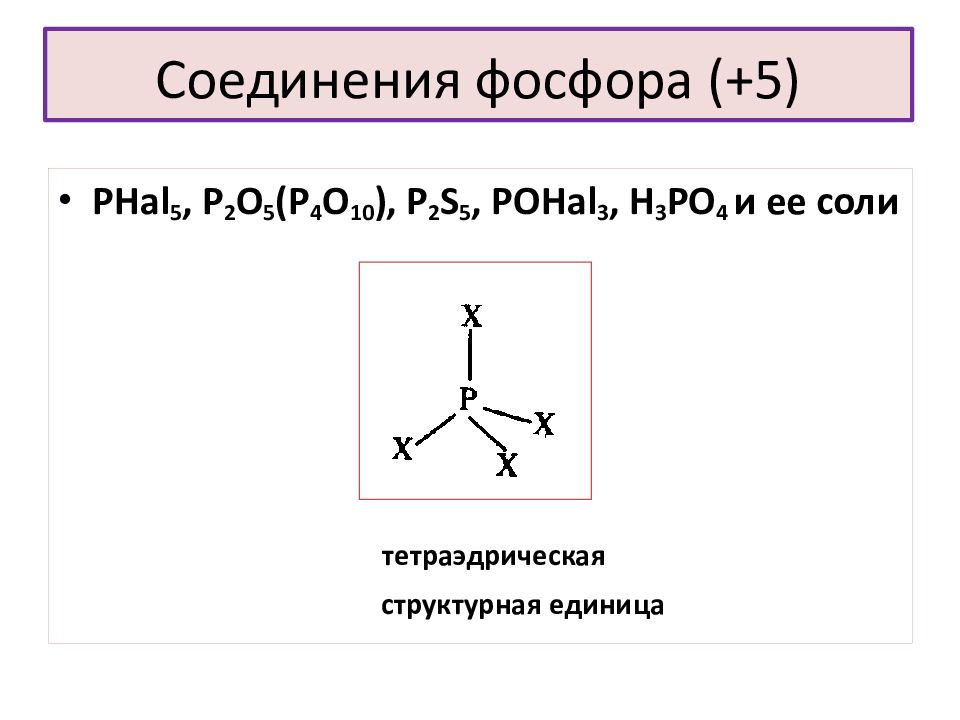
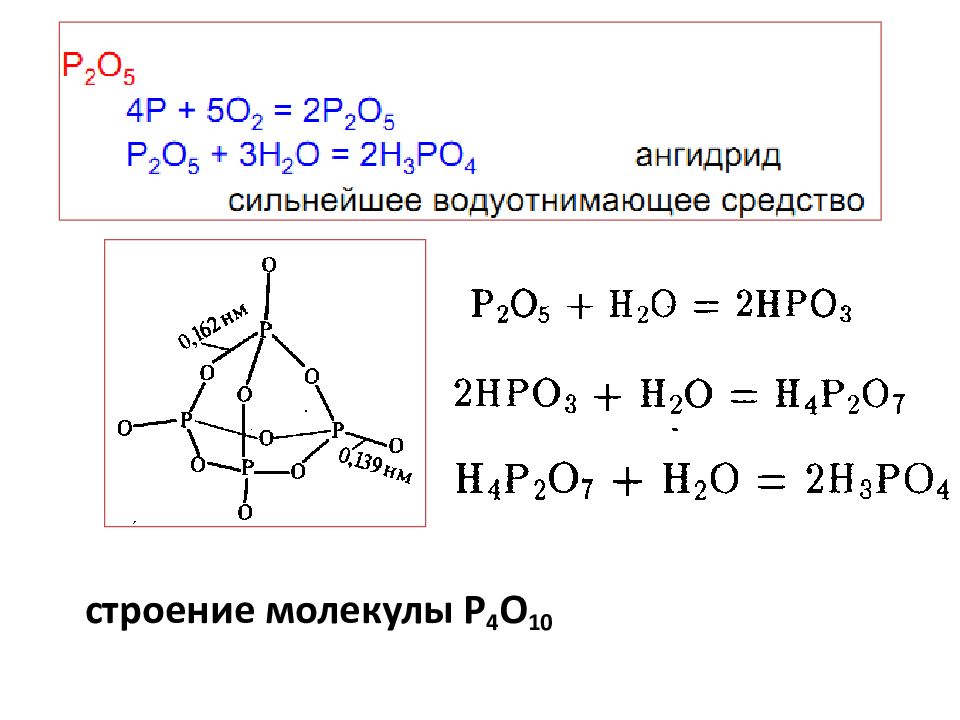
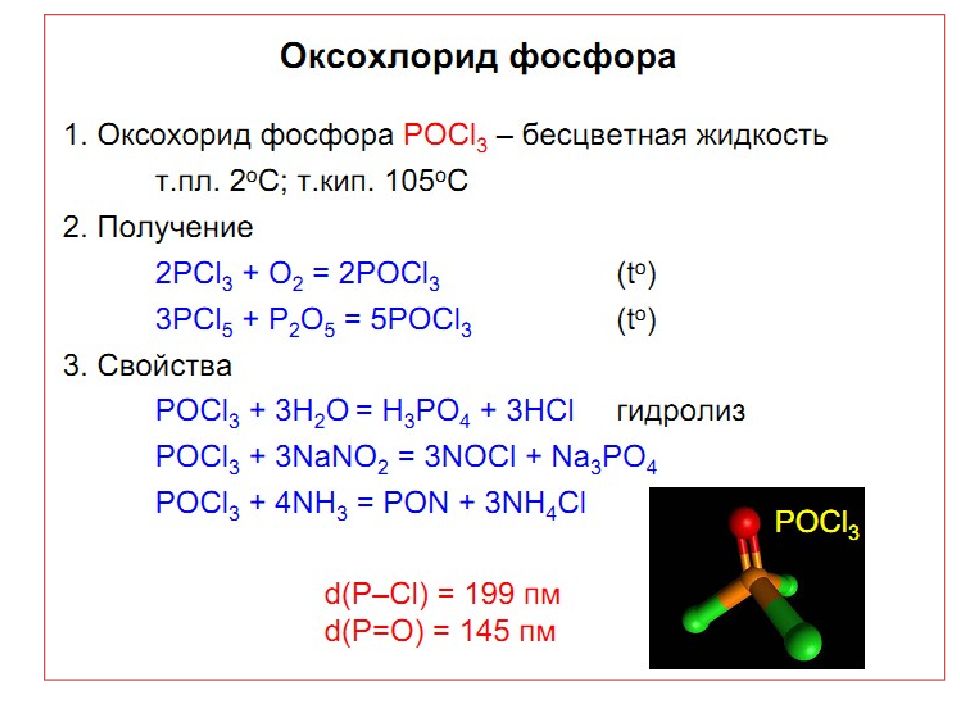
Слайд 16: Соединения фосфора (+ 5 )
PHal 5, P 2 O 5 (P 4 O 10 ), P 2 S 5, РО Hal 3, H 3 PO 4 и ее соли тетраэдрическая структурная единица Соединения фосфора (+ 5 )
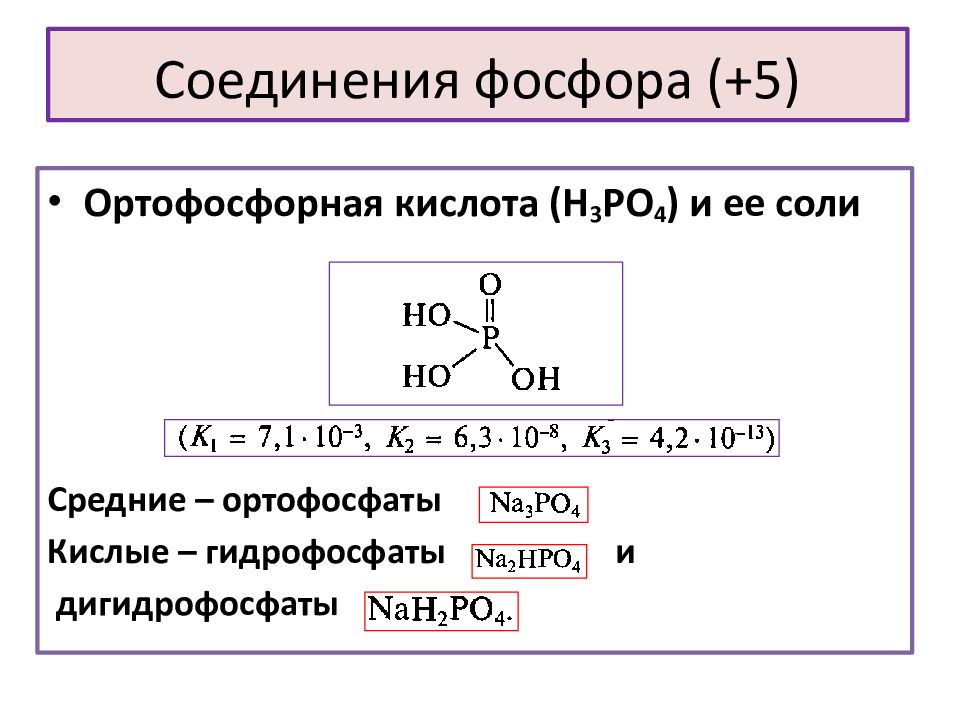
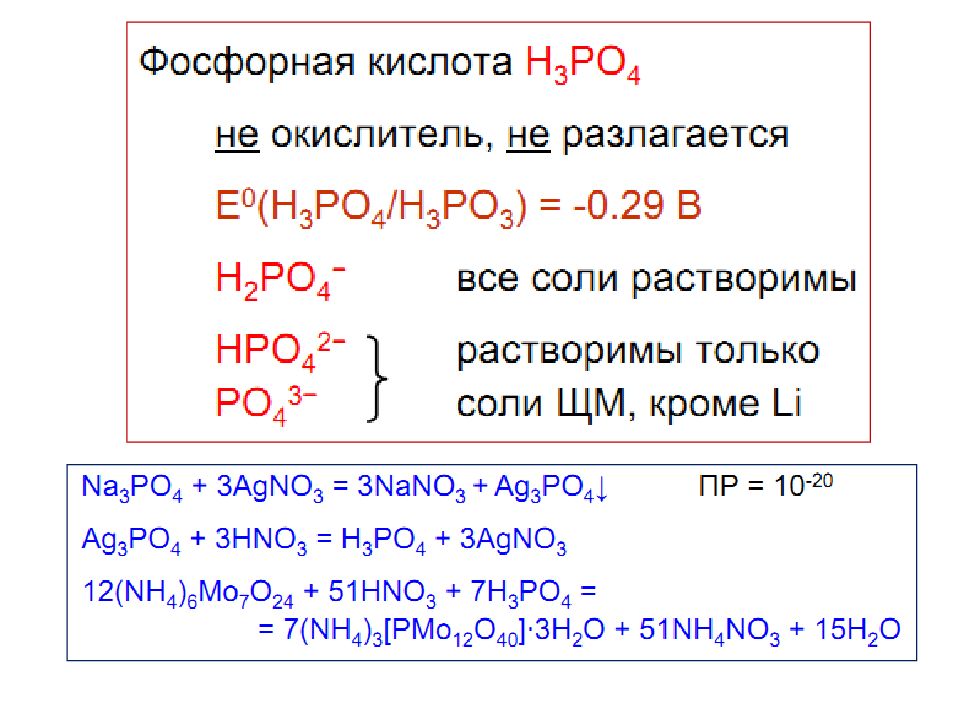
Слайд 19: Соединения фосфора (+ 5 )
Ортофосфорная кислота (Н 3 РО 4 ) и ее соли Средние – ортофосфаты Кислые – гидрофосфаты и дигидрофосфаты Соединения фосфора (+ 5 )
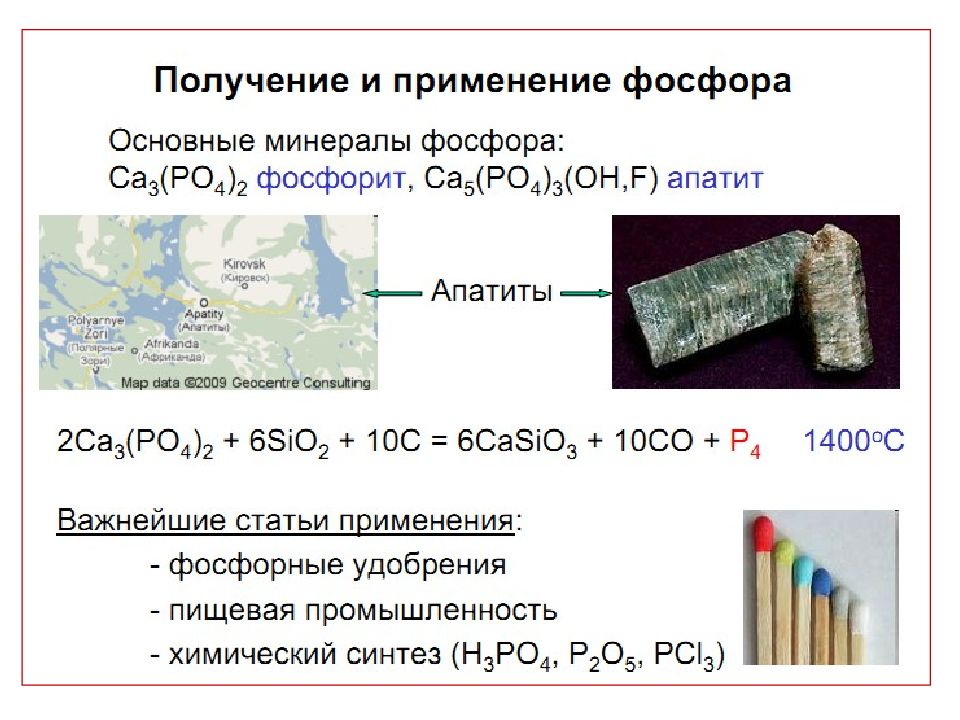
Слайд 20: Получение Н 3 РО 4
1) экстракционный метод (для получения минеральных удобрений ) из апатитов: 2) термический : получают фосфор (восстановлением природного фосфора в электропечи), затем его окисляют до оксида Р 2 О 5, соединяют с водой – Н 3 РО 4 ( = 80% ); 3) Н 3 РО 4 – конечный продукт гидролиза всех соединений фосфора (+5):
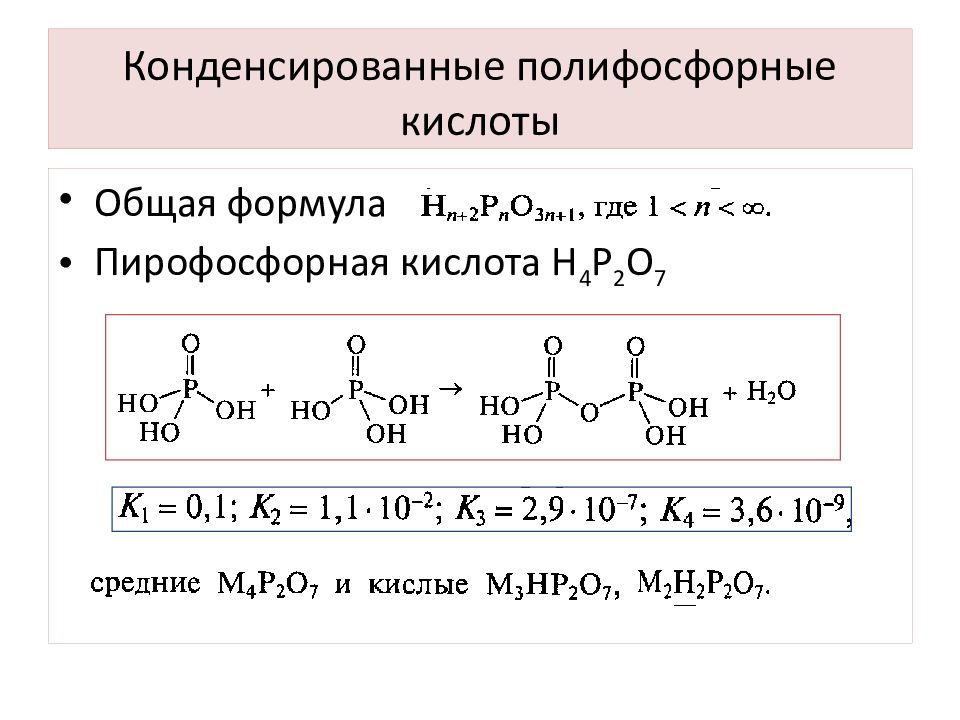
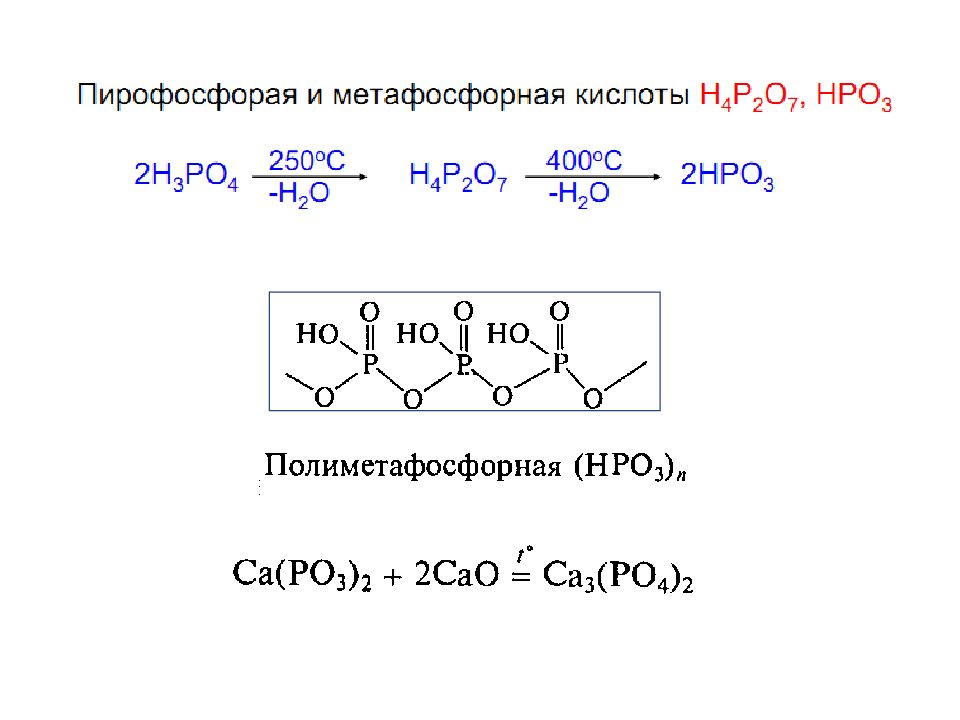
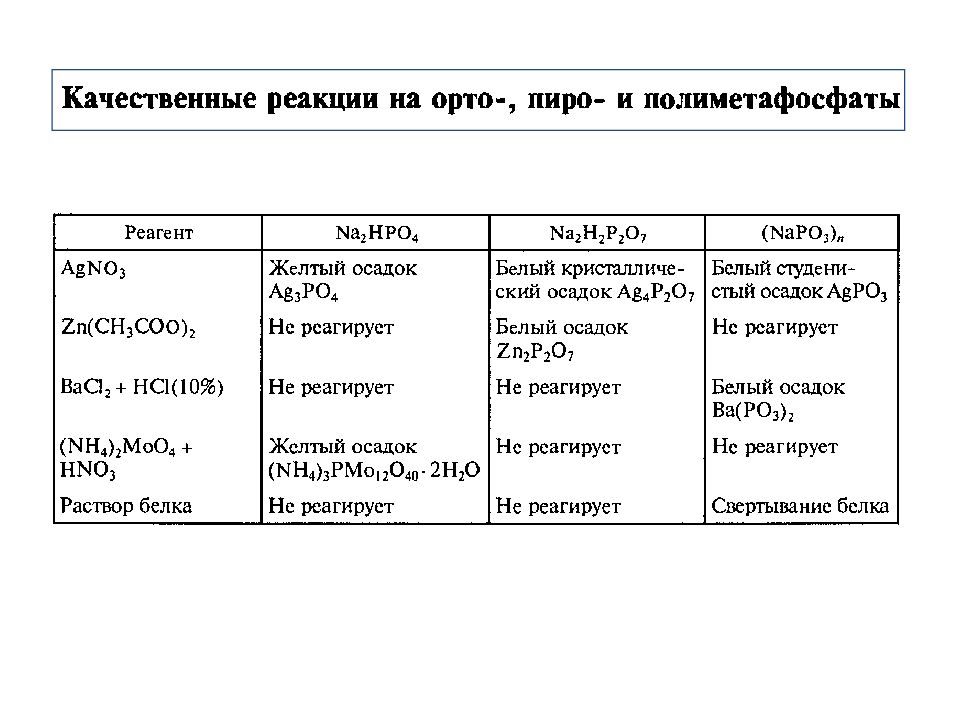
Слайд 23: Конденсированные полифосфорные кислоты
Общая формула Пирофосфорная кислота Н 4 Р 2 О 7