Первый слайд презентации: при опухолях МПС
Работу выполнила: Мамишова Г.А. 4 ПФ 8 группа
Слайд 2
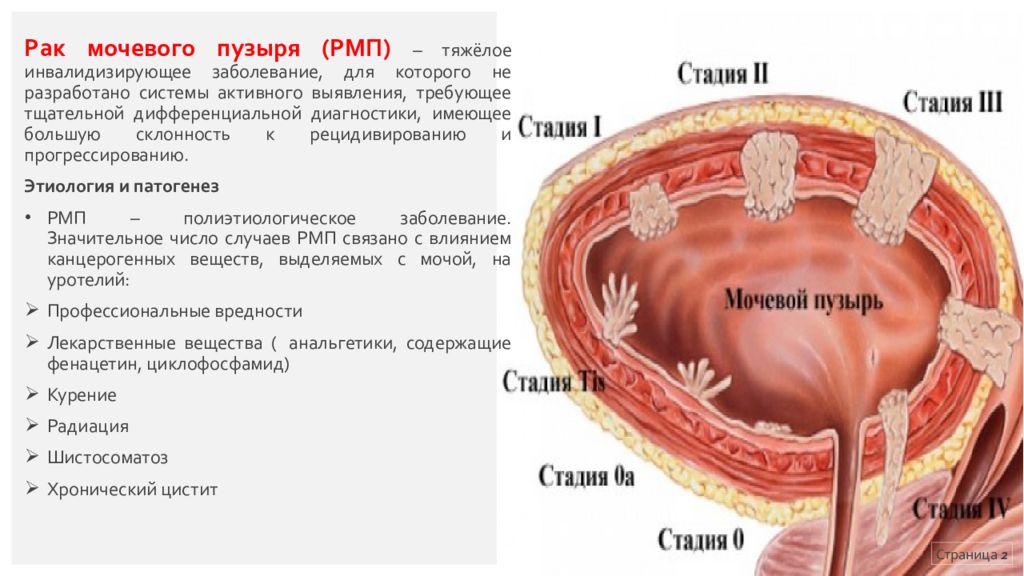
Рак мочевого пузыря (РМП) – тяжёлое инвалидизирующее заболевание, для которого не разработано системы активного выявления, требующее тщательной дифференциальной диагностики, имеющее большую склонность к рецидивированию и прогрессированию. Этиология и патогенез РМП – полиэтиологическое заболевание. Значительное число случаев РМП связано с влиянием канцерогенных веществ, выделяемых с мочой, на уротелий : Профессиональные вредности Лекарственные вещества ( анальгетики, содержащие фенацетин, циклофосфамид ) Курение Радиация Шистосоматоз Хронический цистит Страница 2
Слайд 3
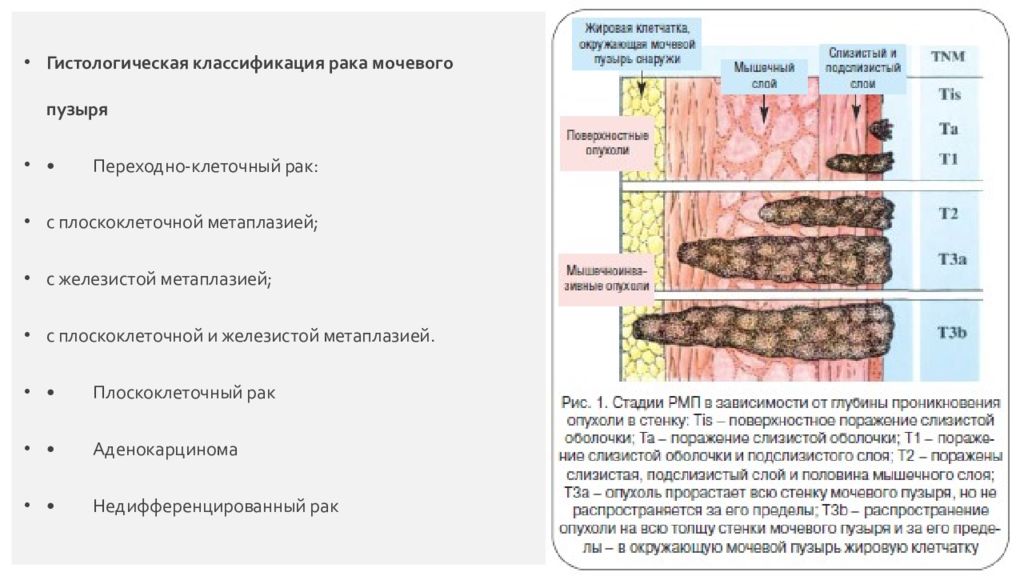
Гистологическая классификация рака мочевого пузыря • Переходно-клеточный рак: с плоскоклеточной метаплазией; с железистой метаплазией; с плоскоклеточной и железистой метаплазией. • Плоскоклеточный рак • Аденокарцинома • Недифференцированный рак Страница 3
Слайд 4: Лучевая терапия
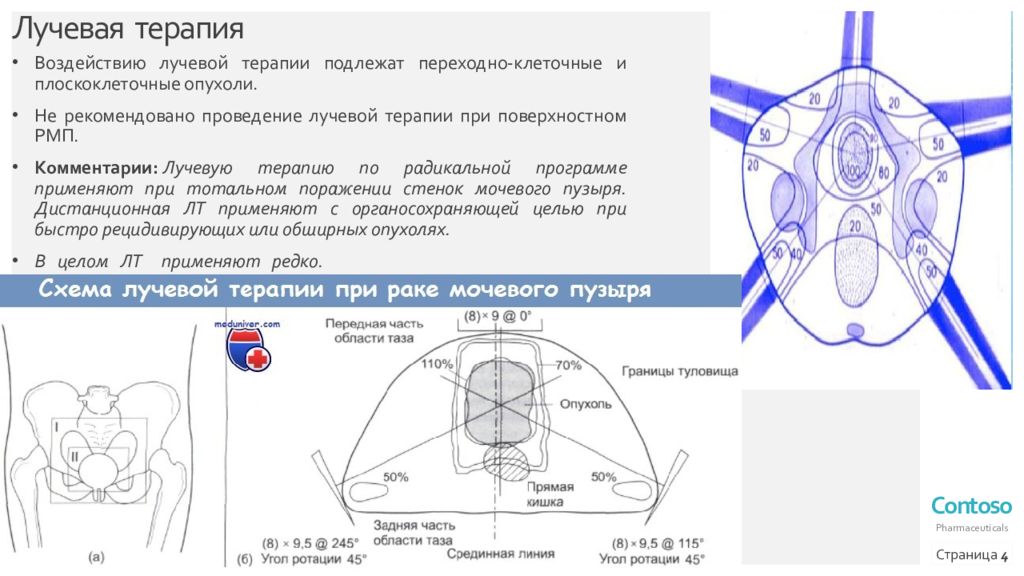
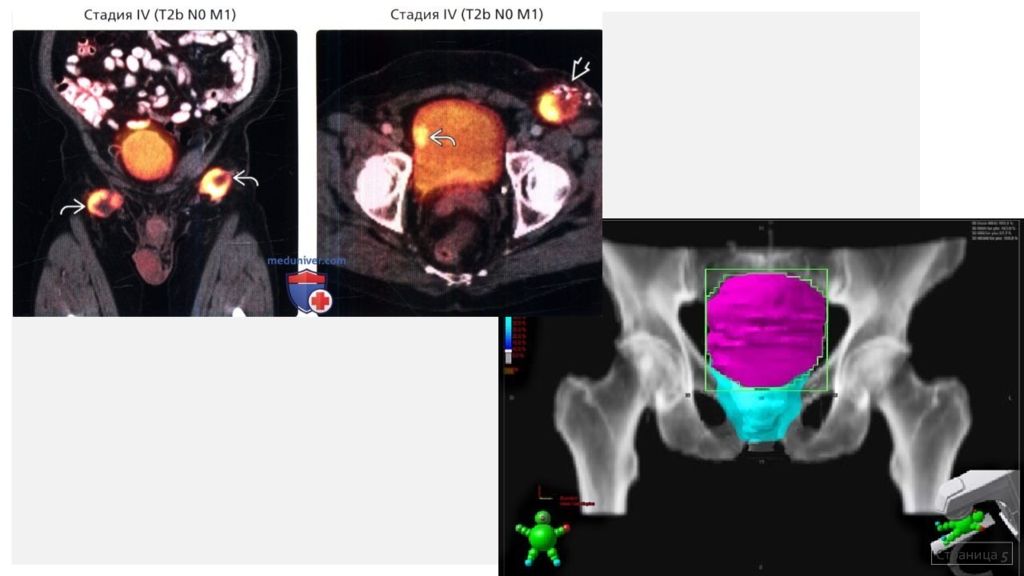
Воздействию лучевой терапии подлежат переходно-клеточные и плоскоклеточные опухоли. Не рекомендовано проведение лучевой терапии при поверхностном РМП. Комментарии: Лучевую терапию по радикальной программе применяют при тотальном поражении стенок мочевого пузыря. Дистанционная ЛТ применяют с органосохраняющей целью при быстро рецидивирующих или обширных опухолях. В целом ЛТ применяют редко. Страница 4
Слайд 7: Рак почки
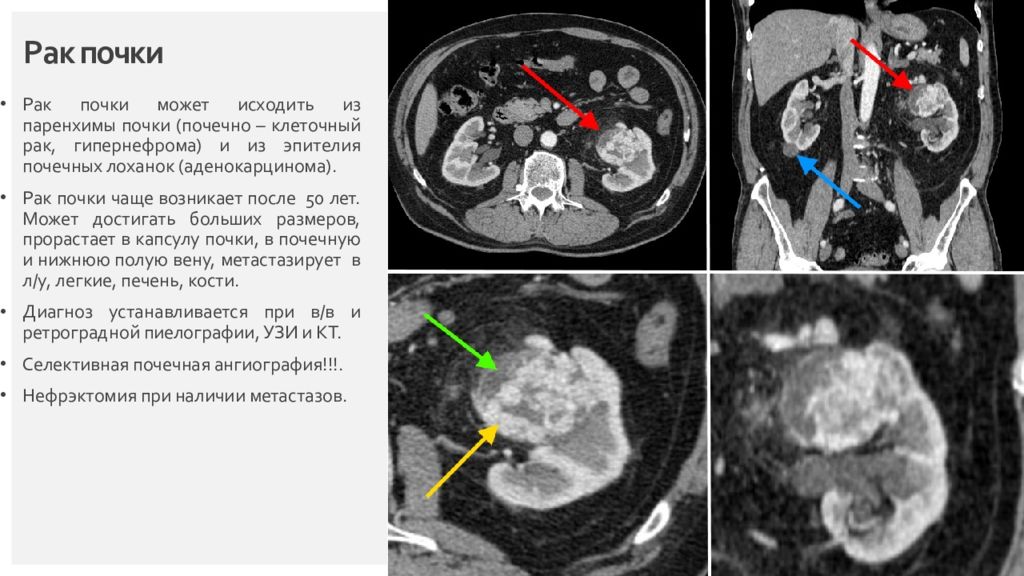
Рак почки может исходить из паренхимы почки ( почечно – клеточный рак, гипернефрома) и из эпителия почечных лоханок (аденокарцинома). Рак почки чаще возникает после 50 лет. Может достигать больших размеров, прорастает в капсулу почки, в почечную и нижнюю полую вену, метастазирует в л/у, легкие, печень, кости. Диагноз устанавливается при в/в и ретроградной пиелографии, УЗИ и КТ. Селективная почечная ангиография!!!. Нефрэктомия при наличии метастазов. Страница 7
Слайд 8: Лучевая терапия
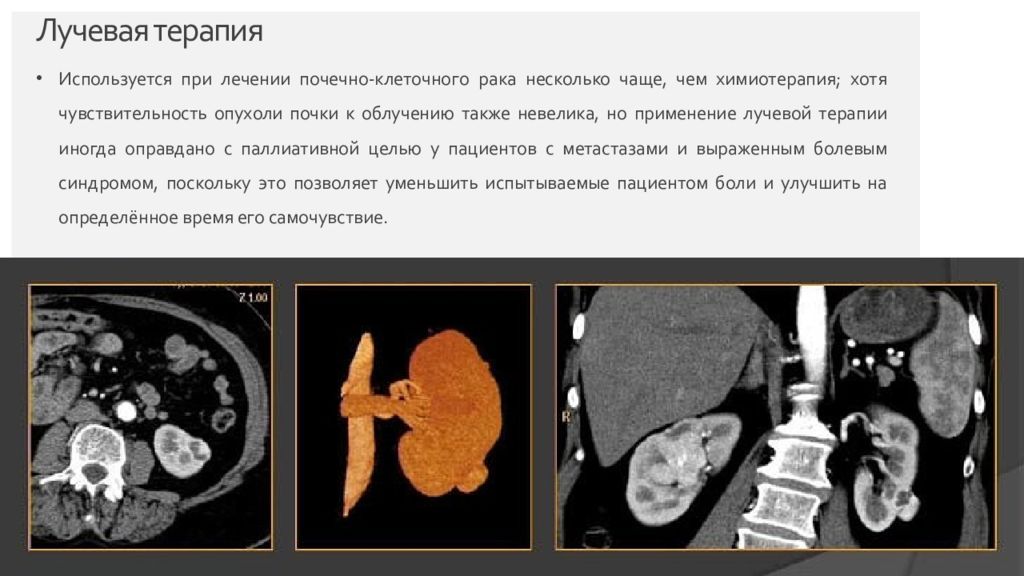
Используется при лечении почечно-клеточного рака несколько чаще, чем химиотерапия; хотя чувствительность опухоли почки к облучению также невелика, но применение лучевой терапии иногда оправдано с паллиативной целью у пациентов с метастазами и выраженным болевым синдромом, поскольку это позволяет уменьшить испытываемые пациентом боли и улучшить на определённое время его самочувствие. Страница 8
Слайд 9
Рак мочеточника — это злокачественная опухоль, которая развивается из многослойного переходного эпителия, или уротелия, выстилающего лоханки почек и мочеточники. Уротелий легко подвергается воздействию агрессивных химических веществ, в том числе канцерогенов, которые его повреждают, вызывают мутации и пролиферации. Группа риска по заболеваемости раком мочеточника в России — пожилые люди, но он может возникнуть и у лиц среднего возраста, у мужчин чаще, и составляет 4% от всех опухолей верхних мочевых путей, в том числе и доброкачественных. По цитологической картине различают следующие виды : • переходноклеточный ; • плоскоклеточный; • аденокарцинома; • папиллярный (растет медленно, обычно расположен в лоханке). Экзофитная и эндофитная (инфильтрирующая) формы рака указывают на тип роста новообразования. Широко используется и международная классификация TNM, которая позволяет установить распространение процесса и тактику лечения. Страница 9
Слайд 10
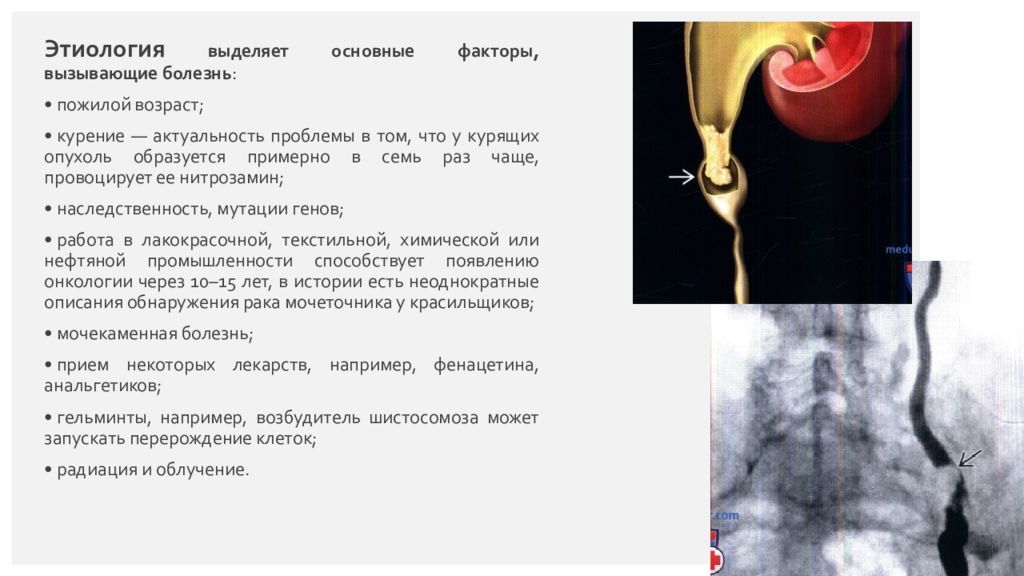
Этиология выделяет основные факторы, вызывающие болезнь : • пожилой возраст; • курение — актуальность проблемы в том, что у курящих опухоль образуется примерно в семь раз чаще, провоцирует ее нитрозамин ; • наследственность, мутации генов; • работа в лакокрасочной, текстильной, химической или нефтяной промышленности способствует появлению онкологии через 10–15 лет, в истории есть неоднократные описания обнаружения рака мочеточника у красильщиков; • мочекаменная болезнь; • прием некоторых лекарств, например, фенацетина, анальгетиков; • гельминты, например, возбудитель шистосомоза может запускать перерождение клеток; • радиация и облучение. Страница 10
Слайд 11
Из клинических исследований, которые способны определить новообразование, используются : • развернутый анализ мочи с цитологией; • ультразвуковое исследование; • экскреторная или ретроградная урография; • почечная ангиография; • цистоскопия; • тест на онкомаркеры ; • компьютерная или магнитно-резонансная томография; • ПЭТ-КТ. Страница 11
Слайд 12: Лечение рака мочеточника
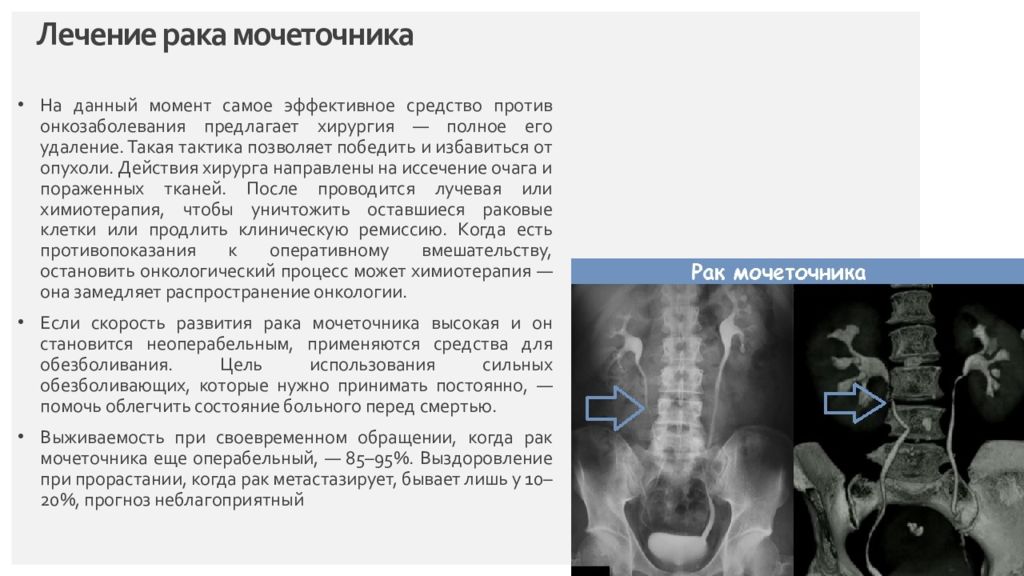
На данный момент самое эффективное средство против онкозаболевания предлагает хирургия — полное его удаление. Такая тактика позволяет победить и избавиться от опухоли. Действия хирурга направлены на иссечение очага и пораженных тканей. После проводится лучевая или химиотерапия, чтобы уничтожить оставшиеся раковые клетки или продлить клиническую ремиссию. Когда есть противопоказания к оперативному вмешательству, остановить онкологический процесс может химиотерапия — она замедляет распространение онкологии. Если скорость развития рака мочеточника высокая и он становится неоперабельным, применяются средства для обезболивания. Цель использования сильных обезболивающих, которые нужно принимать постоянно, — помочь облегчить состояние больного перед смертью. Выживаемость при своевременном обращении, когда рак мочеточника еще операбельный, — 85–95%. Выздоровление при прорастании, когда рак метастазирует, бывает лишь у 10–20%, прогноз неблагоприятный Страница 12
Слайд 13
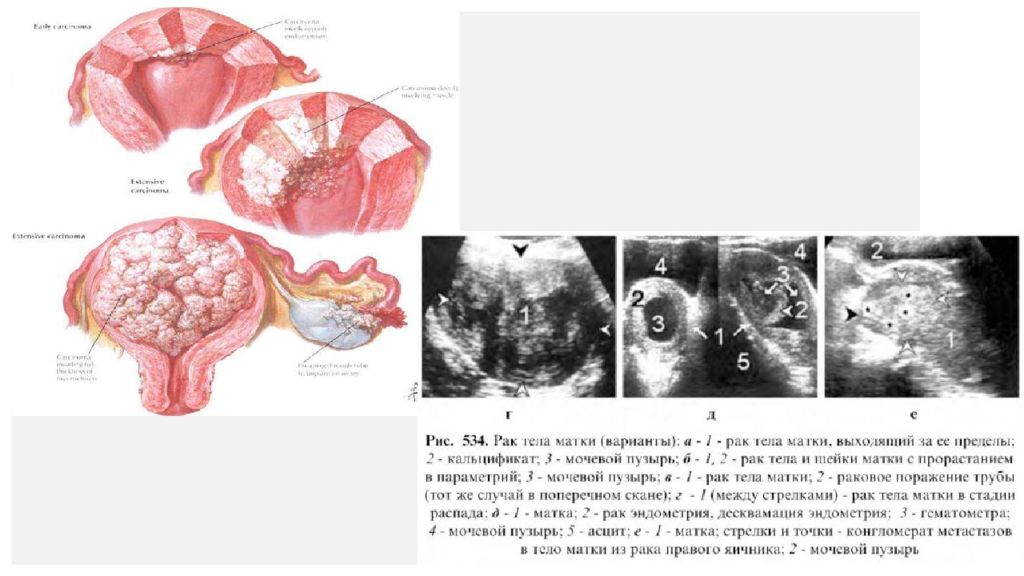
Рак тела матки (РТМ ) – злокачественная опухоль, исходящая из слизистой оболочки тела матки (эндометрия). Этиология и патогенез У большинства пациенток РТМ носит спорадический характер. Только примерно в 5% случаев РТМ ассоциирован с наследственными синдромами, в частности с синдромом Линча (наследственное заболевание, сопровождающееся развитием злокачественных новообразований в толстом кишечнике.) В качестве факторов риска развития данной патологии рассматриваются: гиперэстрогения, ранние менархе, отсутствие родов в анамнезе, поздняя менопауза, возраст старше 55 лет, применение тамоксифена. Выделяют два патогенетических типа РТМ : I тип (более частый). Опухоль развивается в более молодом возрасте, в отличие от пациенток II патогенетического варианта, на фоне длительной гиперэстрогении и гиперплазии эндометрия. У больных РТМ I патогенетического типа часто наблюдаются ожирение, сахарный диабет и гипертоническая болезнь, возможны эстрогенсекретирующие опухоли яичников или синдром склерокистозных яичников. Опухоли I патогенетического варианта, как правило, высокодифференцированные, имеют более благоприятный прогноз. II тип. Опухоли эндометрия обычно низкодифференцированные, имеют менее благоприятный прогноз. Опухоли II патогенетического типа возникают в более старшем возрасте, в отсутствие гиперэстрогении, на фоне атрофии эндометрия. Примерно у 80% больных РТМ диагностируют эндометриоидную аденокарциному. Страница 13
Слайд 15
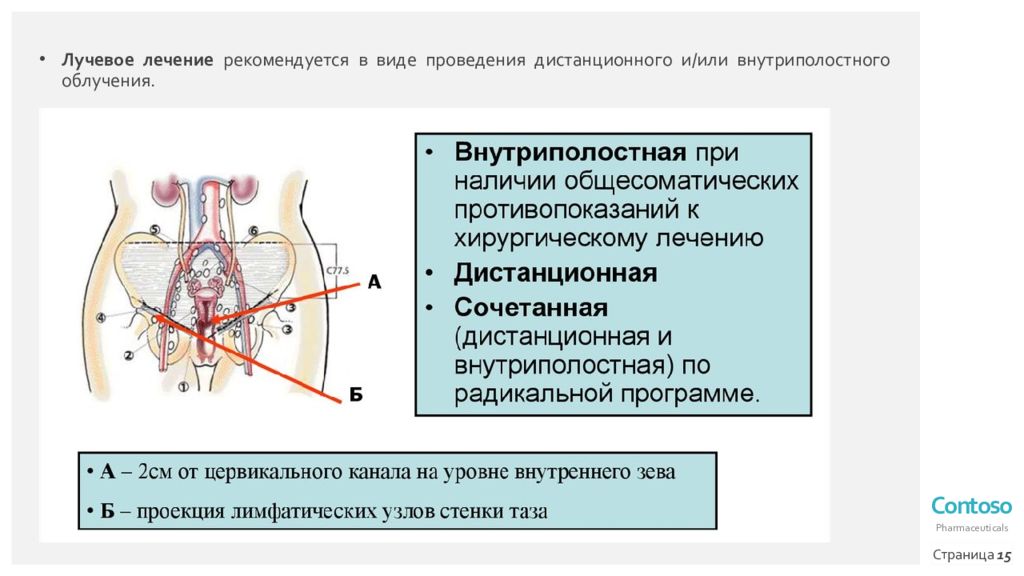
Лучевое лечение рекомендуется в виде проведения дистанционного и/или внутриполостного облучения. Страница 15
Слайд 16
Возможно применение ЛТ и ХТ в плане адьювантного лечения при распространенном опухолевом процессе. Паллиативную ЛТ рекомендуется рассматриваеть с учетом степени распространенности опухолевого процесса и общего состояния больной. Суммарные дозы могут достигать 40-50 Гр. При рецидиве РТМ в культе влагалища или наличии метастаза во влагалище как единственного проявления заболевания, рекомендовано проведение внутритканевой ЛТ. Комментарии: Суммарные дозы подводятся с учетом ранее проведенного лечения на планируемый объем опухолевого образования и достигают 30-40 иГр (проводится в высокотехнологических клиниках и при наличии опыта лечения). Страница 16
Слайд 17
Рак шейки матки (РШМ) – злокачественная опухоль, исходящая из слизистой оболочки шейки матки ( эктоцервикса или цервикального канала). Этиология РШМ имеет спорадический характер. Развитие этого заболевания не связано с наличием известных наследственных синдромов. Причиной развития РШМ является ВПЧ. В странах с высоким уровнем заболеваемости РШМ, персистирующий ВПЧ встречается у 10-20% женщин, в то время как в странах с низким уровнем заболеваемости – только у 5-10%. В качестве факторов риска развития данной патологии рассматриваются: раннее начало половой жизни и ранние первые роды, частая смена половых партнеров, отказ от контрацептивов «барьерного» типа, курение, иммуносупрессия, Дискутируется вопрос о влиянии различных инфекций, передаваемых половым путем. Страница 17
Слайд 18
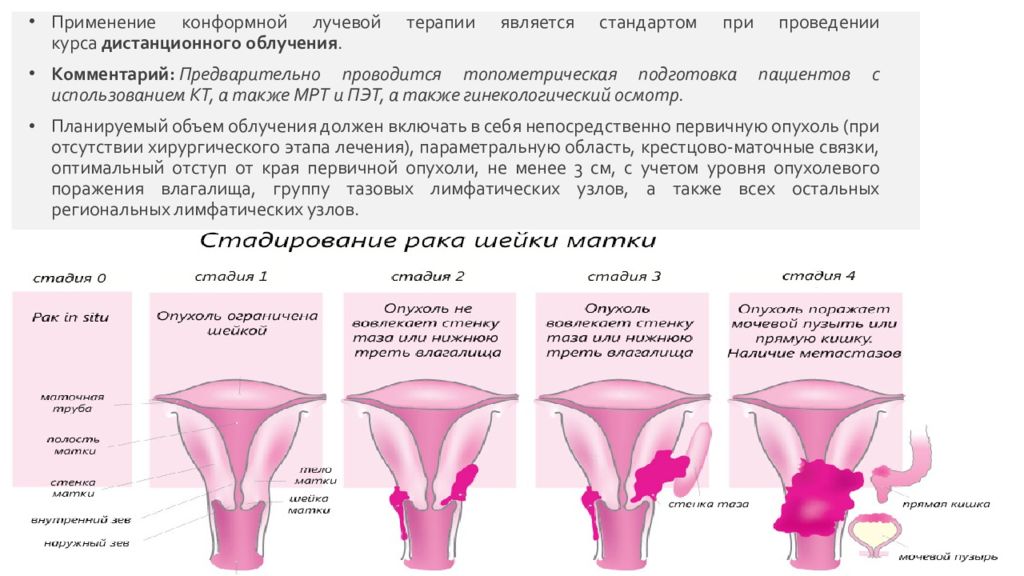
Применение конформной лучевой терапии является стандартом при проведении курса дистанционного облучения. Комментарий: Предварительно проводится топометрическая подготовка пациентов с использованием КТ, а также МРТ и ПЭТ, а также гинекологический осмотр. Планируемый объем облучения должен включать в себя непосредственно первичную опухоль (при отсутствии хирургического этапа лечения), параметральную область, крестцово-маточные связки, оптимальный отступ от края первичной опухоли, не менее 3 см, с учетом уровня опухолевого поражения влагалища, группу тазовых лимфатических узлов, а также всех остальных региональных лимфатических узлов. Страница 18
Слайд 19
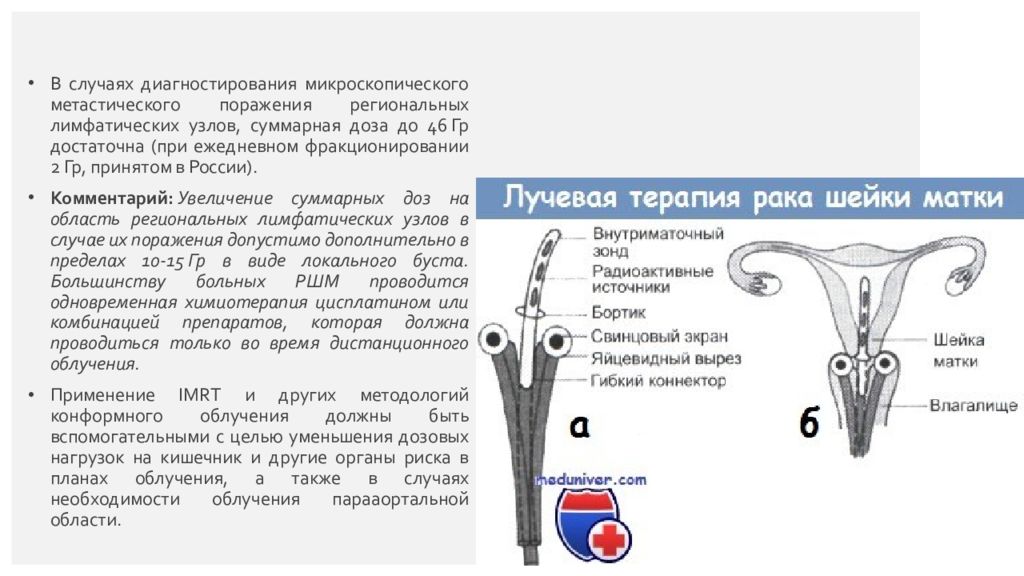
В случаях диагностирования микроскопического метастического поражения региональных лимфатических узлов, суммарная доза до 46 Гр достаточна (при ежедневном фракционировании 2 Гр, принятом в России). Комментарий: Увеличение суммарных доз на область региональных лимфатических узлов в случае их поражения допустимо дополнительно в пределах 10-15 Гр в виде локального буста. Большинству больных РШМ проводится одновременная химиотерапия цисплатином или комбинацией препаратов, которая должна проводиться только во время дистанционного облучения. Применение IMRT и других методологий конформного облучения должны быть вспомогательными с целью уменьшения дозовых нагрузок на кишечник и другие органы риска в планах облучения, а также в случаях необходимости облучения парааортальной области. Страница 19
Слайд 20
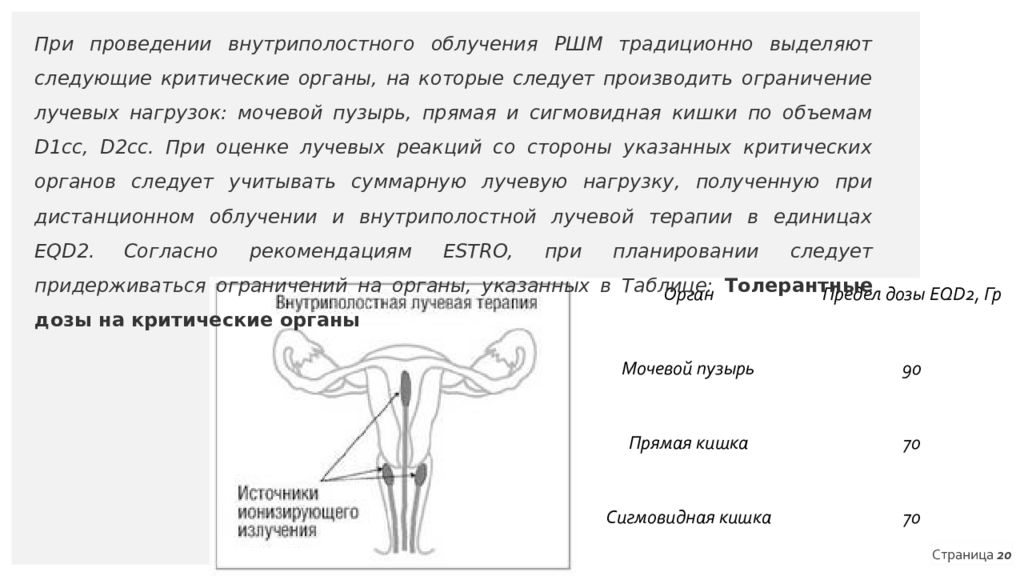
Орган Предел дозы EQD2, Гр Мочевой пузырь 90 Прямая кишка 70 Сигмовидная кишка 70 Страница 20 При проведении внутриполостного облучения РШМ традиционно выделяют следующие критические органы, на которые следует производить ограничение лучевых нагрузок: мочевой пузырь, прямая и сигмовидная кишки по объемам D1cc, D2cc. При оценке лучевых реакций со стороны указанных критических органов следует учитывать суммарную лучевую нагрузку, полученную при дистанционном облучении и внутриполостной лучевой терапии в единицах EQD2. Согласно рекомендациям ESTRO, при планировании следует придерживаться ограничений на органы, указанных в Таблице: Толерантные дозы на критические органы
Слайд 21
Плоскоклеточный рак влагалища – злокачественное новообразование, возникающие из покровного плоского эпителия влагалища женщины. Этиология и патогенез рака влагалища во многом остаются неясными, в первую очередь из-за низких показателей заболеваемости. С учетом единого эмбриогенеза вульвы, влагалища и шейки матки из урогенитального синуса предполагается, что они имеют общие этиологию и патогенез. Однако абсолютно отождествлять эти опухоли нельзя. Исключение составляет светлоклеточная аденокарциномы влагалища — её возникновение связано с воздействием ДЭС. ДЭС применяли в 40–50 - х годах для сохранения беременности у женщин группы высокого риска. В патогенезе РВл возможную отрицательную роль играют следующие факторы: инфицирование женщины в течение жизни вирусами HPV, HSV–2 и HIV с проявлением в виде остроконечной кондиломы; постменопаузальная гипоэстрогения ; тяжелые хронические сенильные кольпиты ; инволютивные, дистрофические посткастрационные и возрастные процессы; хронические неспецифические вагиниты; канцерогенный эффект лучевой терапии в развитии рака влагалища подтверждается многочисленными сообщениями о возникновении плоскоклеточного рака влагалища через 10-30 лет после сочетанной лучевой терапии рака шейки матки; светлоклеточный рак влагалища у девочек и молодых женщин связывают с трансплацентарным карциногенезом (использованием 17 -эстрадиола и диэтилстильбэстрола их матерями для лечения различных осложнений беременности). Страница 21
Слайд 22: Лечение
Страница 22 Рекомендуется лучевая терапия как основной метод радикального лечения больных раком влагалища. Хирургическое лечение возможно при небольшом размере первичной опухоли. Рекомендуется при плоскоклеточном рака влагалища TisN0M0 стадии: лечение VAIN I – мониторинг; лечение VAIN II и III зависит от распространенности процесса. Комментарий: лазерная хирургия; или широкая локальная эксцизия с/без пересадкой кожного лоскута; или частичная/полная вагинэктомия с/без пересадки кожного лоскута; или химиотерапия; или внутриполостная ЛТ. Рекомендуется при плоскоклеточном раке влагалища T1N0M0 (I) стадии проведение сочетанной ЛТ; проведение внутриполостной ЛТ (брахитерапия) в самостоятельном варианте - преимущественно при локальных опухолях.
Слайд 23
вид брахитерапии выбирается с учетом распространения опухолевого процесса и локализации; внутриполостная лучевая терапия проводится в случаях поверхностного роста опухоли влагалища (< 0,5 см), все остальные варианты распространения опухолевого процесса предполагают проведение внутритканевого облучения; возможно рассматривать варианты хирургического лечения: широкая локальная эксцизия или вагинэктомия с реконструкции влагалища, по показаниям - неоадъювантная лучевая терапия; вагинэктомия и лимфодиссекция, с/без реконструкции влагалища, по показаниям - неоадъювантная лучевая терапия рекомендуется рассматривать адьювантную ЛТ при положительных краях резекции. Рекомендуется при плоскоклеточном раке влагалища T2N0M0 (II) стадии проведение сочетанной ЛТ Рекомендуется при плоскоклеточном раке влагалища III стадии (T3N0M0; T1N1M0; T2N1M0; T3N1M0) дистанционная лучевая терапия в комбинации с/без внутриполостной лучевой терапии Комментарий: возможны варианты хирургического лечения в комбинации с дистанционной лучевой терапией, показаниям дополняется внутриполостной лучевой терапией. Рекомендуется при плоскоклеточном раке влагалища IVA стадии (T4, любая N, M0) сочетанная ЛТ. Рекомендуется при плоскоклеточном раке влагалища IVB стадии (любая T, любая NM1) (отдаленные метастазы) лучевая терапия как паллиативное лечение для облегчения симптомов и улучшения качества жизни больной; или варианты химиотерапевтического лечения, применяемого при плоскоклеточном раке других локализаций. Страница 23
Слайд 24
Брахитерапия: применяются вагинальные аппликаторы при вагинальной интраэпителиальной неоплазии или поверхностных образованиях глубиной инвазии до 5 мм. При инвазии более 5 мм – проводится внутритканевая лучевая терапия (как правило после дистанционной лучевой терапии). При локализации опухоли в верхней 2/3 влагалища проводится внутриполостная лучевая терапия по аналогии лечения рака шейки матки. При локализации опухоли в средней и нижней трети влагалища, ограниченная задней его стенкой возможно применение цилиндрического аппликатора как вагинально, так и ректально. Дозы-фракционирование: дистанционное облучение первичной опухоли и зоны региональных лимфатических узлов РД 2 Гр 5 дней в неделю СД 46 – 50 Гр. Брахитерапия: самостоятельная на глубину 5 мм от слизистой РД 5,5 Гр СД 33 Гр в течение10 – 19 дней; внутриполостная лучевая терапия РД 7 Гр 3-4 фракции 1 раз в 5-6 дней; внутритканевая лучевая терапия 20 - 30 Гр. Страница 24
Слайд 25
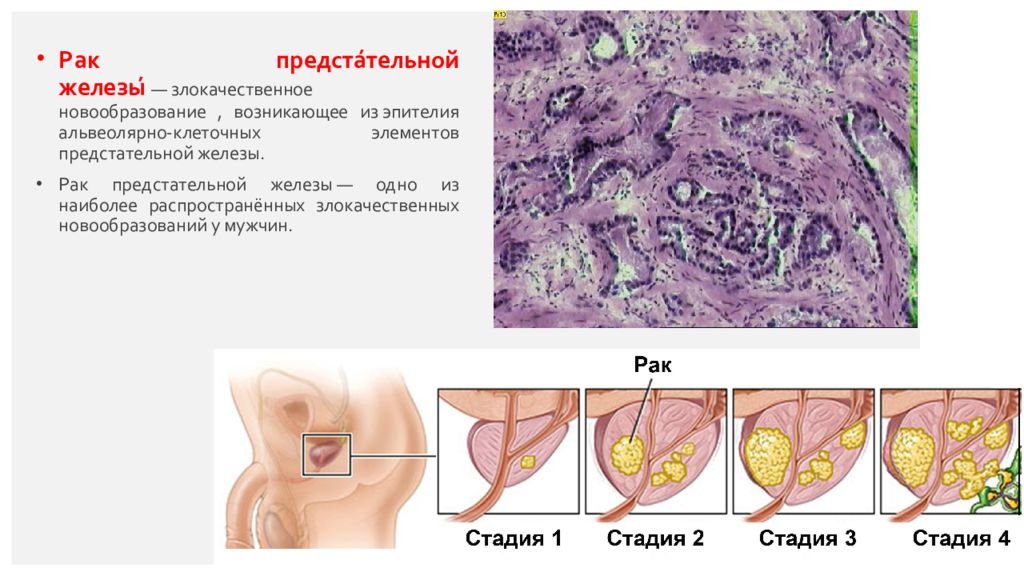
Рак предста́тельной железы́ — злокачественное новообразование, возникающее из эпителия альвеолярно-клеточных элементов предстательной железы. Рак предстательной железы — одно из наиболее распространённых злокачественных новообразований у мужчин. Страница 25
Слайд 26
К факторам риска, увеличивающим шансы заболеть раком предстательной железы, относятся: пожилой возраст (более 75 % случаев рака простаты диагностируется у мужчин старше 65 лет, а на мужчин моложе 60 лет падает лишь 7 % случаев заболевания); связанные с возрастом нарушения гормонального фона; особенности питания (у мужчин, употребляющих жирную пищу, риск возникновения рака простаты возрастает в 2 раза, поскольку обилие в пище животных жиров ведёт к ухудшению всасывания витамина A и, как следствие, β-каротина — фактора защиты от возникновения некоторых злокачественных опухолей; наследственная предрасположенность (так, риск заболеть раком предстательной железы повышается в 10 раз у мужчины, трое родственников которого больны данным заболеванием; в США самый высокий риск заболеть раком предстательной железы имеют афроамериканцы— в три раза выше, чем белые американцы, а у иммигрантов из Азии рак предстательной железы встречается редко); факторы внешней среды (например, облучение ультрафиолетовыми лучами ); вирусные инфекции (в частности, обсуждалась гипотеза о вирусе XMRV из семейства ретровирусов как о факторе риска при заболевании раком простаты); вредные условия труда (работа с кадмием, в резиновой промышленности). Страница 26
Слайд 27: Диагностика
исследование уровня простатического специфического антигена (ПСА) в крови; пальцевое ректальное обследование простаты; трансректальная эхография ( трансректальное ультразвуковое исследование) простаты. Используются также следующие методы диагностики: ультразвуковое исследование брюшной полости; биопсия предстательной железы, проводимая — как правило — по результатам ультразвукового исследования и сопровождающаяся оцениванием степени дифференцировки опухоли путём вычисления «суммы Глисона ». Раннее биопсия являлась главным методом подтверждения диагноза рака простаты; магнитно-резонансная томография; радиоизотопные исследования; рентгенологические обследования (включая компьютерную томографию); исследование образцов мочи на специфические маркеры опухоли предстательной железы, например длинные некодирующие РНК - маркер PCA3; урофлоуметрия. Страница 27
Слайд 28: На ранних стадиях
При локальных формах (1-я или 2-я стадия, без метастазов) рака предстательной железы применяются следующие виды лечения: удаление предстательной железы (радикальная простатэктомия, при которой простата удаляется вместе с семенными пузырьками); дистанционная лучевая терапия (обычно предусматривает облучение предстательной железы и находящихся рядом лимфатических узлов в дозе около 40 Грей; позже направленное на опухоль излучение наращивают до 70 Грей); ультразвуковая абляция опухолей фокусированным высокоинтенсивным ультразвуком; брахитерапия, или интерстициальная лучевая терапия (основана на введении в опухоль зёрен с радиоактивными препаратами); Криоабляция опухоли (процесс локального замораживания и девитализации тканей, позволяющий выполнить прицельную деструкцию поражённой ткани и прилежащих к ней по краю здоровых клеток); монотерапия антиандрогенами (наиболее редкий вид лечения). Страница 28
Слайд 29: На поздних стадиях
Страница 29 При 3-й и 4-й стадиях (характеризующихся наличием метастазов) применяются следующие виды лечения: дистанционная лучевая терапия в сочетании с гормональной терапией, предполагающая облучение предстательной железы и находящихся рядом лимфатических узлов в комбинации с терапией антагонистами (то есть блокаторами) гонадолиберина (такими, как дегареликс, известный под названием фирмагон ); монотерапия антагонистами гонадолиберина или антиандрогенами (возможно также назначение агонистов — то есть аналогов — гонадолиберина, например, трипторелина, хотя они имеют существенно меньшую эффективность в поддержании уровня тестостерона ниже 0,2 нг /мл по сравнению с антагонистами): - монотерапия, предполагающая пожизненное назначение препарата (отмена возможна только по решению врача, например, в случае выздоровления или непереносимости) и означающая медикаментозную кастрацию (в отличие от обычной, такая кастрация обратима в случае отмены препарата; - интермиттирующая терапия (терапия, предусматривающая чередование периодов назначения и отмены препарата), применяемая только для отдельных, относительно нетяжёлых пациентов (недостаток — отсутствие утверждённых схем, в результате чего врач должен сам подбирать допустимую схему терапии индивидуально для каждого пациента); оперативная (хирургическая) кастрация (её эффективность сопоставима с медикаментозной кастрацией антагонистами гонадолиберина, но операция необратима и пагубно влияет на настрой пациента, так что большинство пациентов выбирают — при наличии финансовых возможностей — медикаментозную кастрацию); Иммунотерапия