Слайд 2
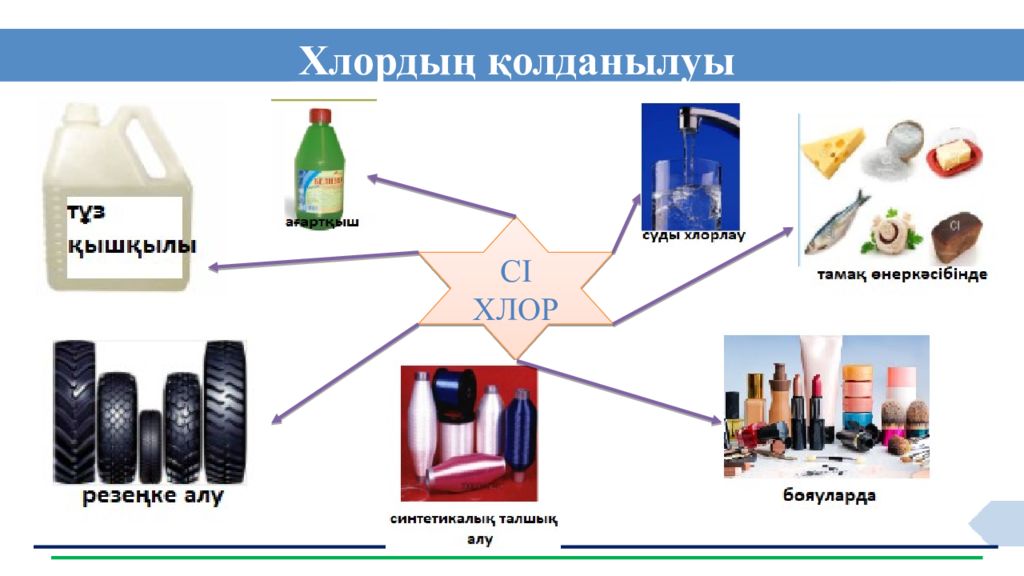
9.2.1.9 хлордың химиялық қасиеттерін сипаттау: металдармен, сутекпен және галогенидтермен әрекеттесуі хлордың молекулалық, электрондық және құрылымдық формуласын сипаттайды; өндірісте және зертханада хлорды алу жолдары мен хлордың физикалық және химиялық қасиеттерін анықтайды; хлорды алу жолдарын және қолданылуын сипаттайды. Оқу мақсаты Ба ғалау критерийлері
Слайд 3: Хлордың ашылуы 1774 жылы Швед ғалымы К. Шееле хлорды алғаш рет алды. Ол бұл затты күрделі затқа санап, «флогистиндірілмеген» тұз қышқылы деп атады. 1807 жылы ағылшын химигі Гемфри Дэви дәл осы газды алды. Ол бұл элементті «хлорин» деп атады. Мағынасы «хлорос» - сары-жасыл деген мағынаны білдіреді. 1812 жылы Гей-Люссак газға хлор деген атау берді
Слайд 4
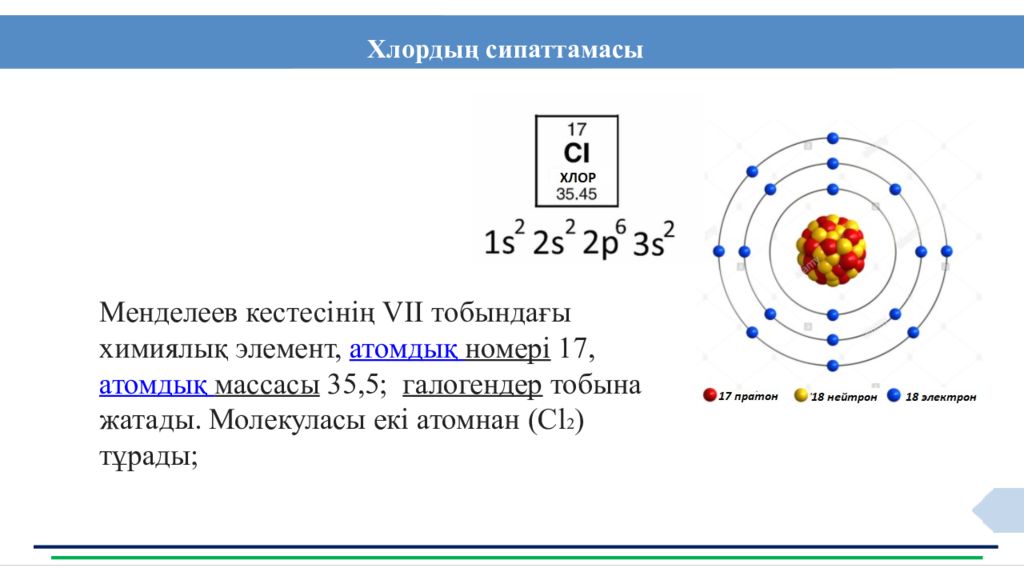
Хлордың сипаттамасы Менделеев кестесінің V ІІ тобындағы химиялық элемент, атомдық номері 17, атомдық массасы 35,5; галогендер тобына жатады. Молекуласы екі атомнан ( Cl 2 ) тұрады ;
Слайд 7
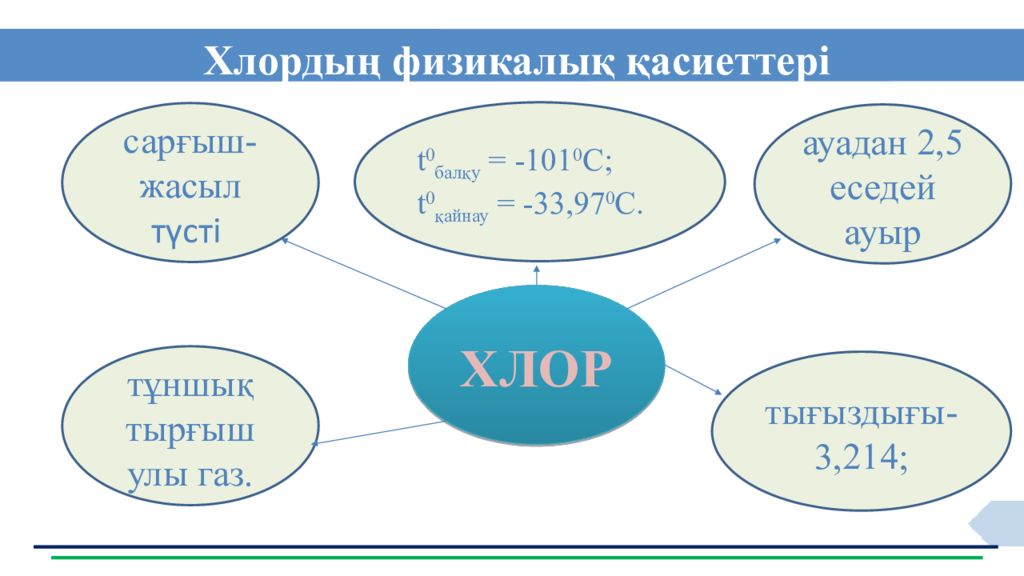
Хлордың физикалық қасиеттері ХЛОР тұншық тырғыш улы газ. ауадан 2,5 еседей ауыр сарғыш-жасыл түсті тығыздығы-3,214; t 0 балқу = -101 0 С; t 0 қайнау = -33,97 0 С.
Слайд 8
8 Өндірісте хлорды ас тұзының ерітіндісі мен балқымасын электролиздеу әдісімен алады: 2NaCl → 2 Na + Cl 2 ↑ Зертханада марганец диоксиді (қыздырып), калий перманганаты КMnO 4 немесе КСІО 3 (бертолле тұзы) концентрлі тұз қышқылымен әсер етіп алады: MnO 2 +4HCl = Cl 2 ↑ + MnCl 2 + 2H 2 O 2 КMnO 4 + 16HCl = 5Cl 2 ↑ +2KCl +2MnCl 2 +8H 2 O К cl O 3 + 6HCl = 3Cl 2 ↑ + KCl +3H 2 O Хлордың алынуы
Слайд 9
Хлордың химиялық қасиеттері Мыстың алдын ала қыздырылған ұнтақтары хлорда тұтанып, қоңыр түтін пайда болады: С u 0 + Cl 0 2 = Cu +2 Cl - 2 Сутек хлорда жанады: H 0 2 + Cl 0 2 = 2H + Cl - ↑ Хлор кремний мен фосформен әрекеттеседі: Si 0 +2Cl 0 2 =Si +4 Cl - 4 2P 0 + 5Cl 0 2 = 2P +5 Cl - 5 Оттекпен, көміртекпен және азотпен хлор тікелей әрекеттеспейді. Хлор сумен әрекеттесіп, орынбасу реакциясы жүреді: 2Cl 0 2 +2H + 2 O 2- = 4H + Cl - + O 2 0 ↑ Хлор – күшті тотықтырғыш, сондықтан жоғары тотығу дәрежесіне жеткенге дейін тотығуға бейім элементтер кіретін күрделі заттармен оңай әрекеттеседі: 2 Fe +2 Cl - 2 +Cl 0 2 = 2Fe +3 Cl - 3
Слайд 10
Хлордың химиялық қасиеттері Құрғақ жерде хлор енжар келеді, ал азғана ылғалды ортада оның белсенділігі артады. Хлор металдармен қосылып, тотықтырғыш қасиет көрсетеді. 2 Fe 0 + 3 Cl 0 2 = 2Fe +3 Cl - 3
Слайд 13
1-тапсырма Берілген сөйлемдерде қойылған көп нүктенің орнына тиісті сөздерді жазыңыз. Өнеркәсіпте ………… ас тұзының ерітіндісі мен балқымасын ………… арқылы алады. Хлор металдармен, сутекпен және фосформен ………… ретінде әрекеттеседі. Хлор сумен әрекеттескенде ………… және ………… түзіледі. Бекіту тапсырмасы Дескриптор: Хлордың өнеркәсіпте алынуын көрсетеді. Хлордың химиялық қасиеттерін анықтайды.
Слайд 14
Дұрыс жауап Дескриптор: Хлордың өнеркәсіпте алынуын көрсетеді. Хлордың химиялық қасиеттерін анықтайды. Өнеркәсіпте хлорды ас тұзының ерітіндісі мен балқымасын электролиздеу арқылы алады. Хлор металдармен, сутекпен және фосформен тотықтырғыш ретінде әрекеттеседі. Хлор сумен әрекеттескенде хлорсутек және оттек түзіледі.
Слайд 15
Бекіту тапсырмасы Дескриптор: Айналымды жүзеге асырып, тиісті реакция теңдеулерін жазады. Мына айналымды жүзеге асырып, тиісті реакция теңдеулерін жазыңыз: СІ 2 →НСІ→СuCl 2 →NaCl→AgCl
Слайд 16
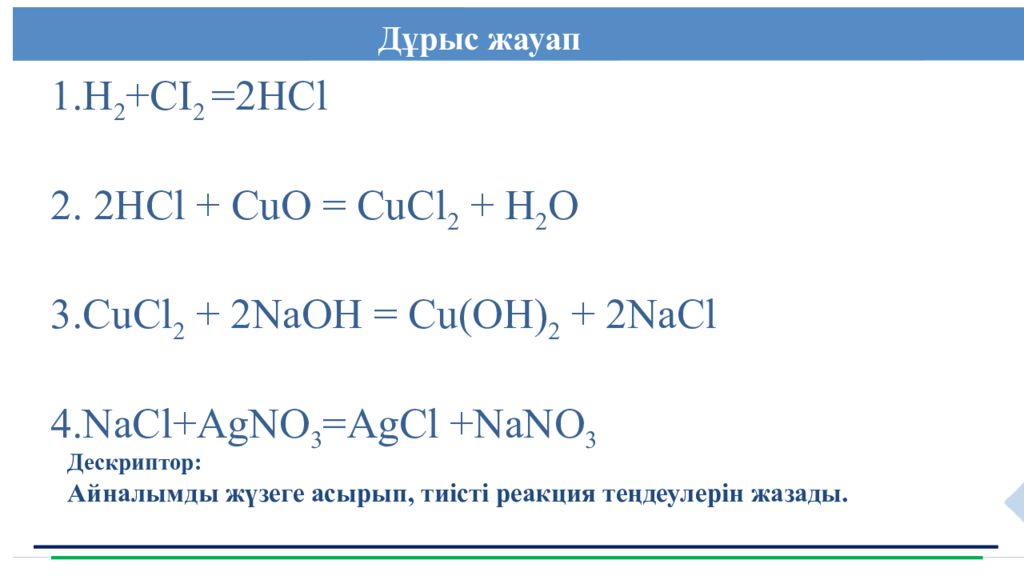
Дұрыс жауап Дескриптор: Айналымды жүзеге асырып, тиісті реакция теңдеулерін жазады. 1.Н 2 +СІ 2 =2HCl 2. 2HCl + CuO = CuCl 2 + H 2 O 3. CuCl 2 + 2NaOH = Cu(OH) 2 + 2NaCl 4.NaCl+AgNO 3 = AgCl +NaNO 3
Слайд 17
Қорытынды хлордың молекулалық, электрондық және құрылымдық формуласын түсіндім; өндірісте және зертханада хлорды алу жолдарымен таныстым; хлордың физикалық және химиялық қасиеттерін және хлорды алу жолдары мен қолданылуын білемін.