Слайд 2
2 УГЛЕВОДЫ Важнейшие химические соединения растительного и животного мира ( 12% сухого веса организма ) МОНОСАХАРИДЫ – не гидролизуются Общая формула: С n (H 2 O) n, где n 4 Пример: глюкоза С 6 Н 12 О 6 = С 6 (Н 2 О) 6 2. ОЛИГОСАХАРИДЫ – при гидролизе образуется от 2 до 10 моносахаридов Общая формула: С n (H 2 O) m, где n m Пример: сахароза С 12 Н 22 О 11 = С 12 (Н 2 О) 11 КАРЛ ШМИДТ (1822-1894) автор слова «углеводы» По способности к гидролизу бывают: конденсационные полимеры моносахаридов 3. ПОЛИСАХАРИДЫ – при гидролизе образуется более 10 моносахаридов Общая формула: С n (H 2 O) m, где n m Пример: крахмал [ С 6 ( H 2 O) 5 ] x
Слайд 3
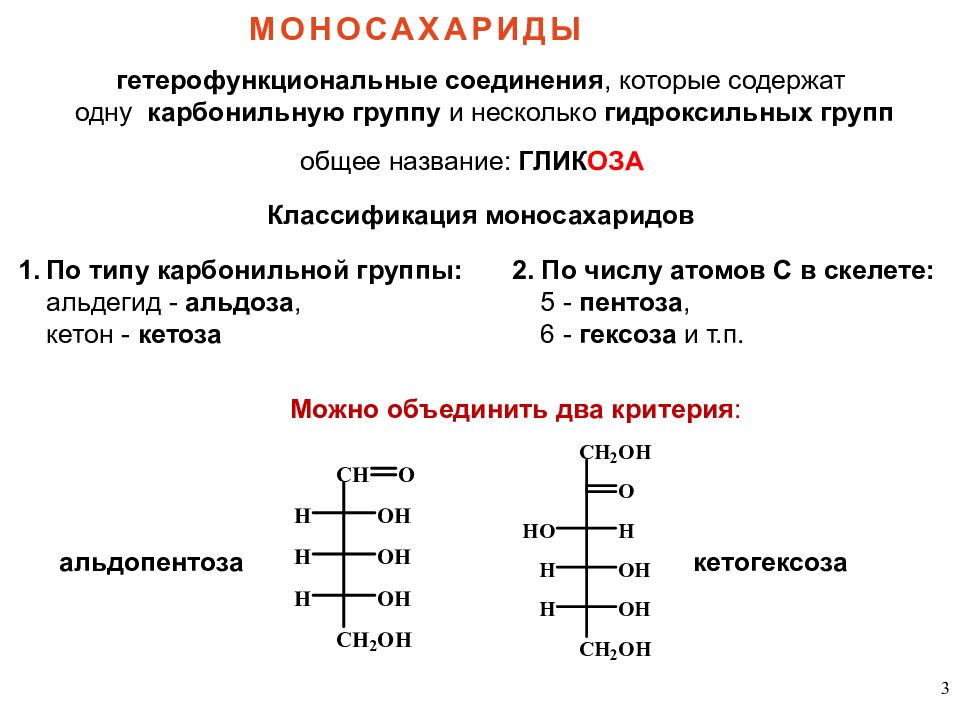
3 гетерофункциональные соединения, которые содержат одну карбонильную группу и несколько гидроксильных групп общее название: ГЛИК ОЗА МОНОСАХАРИДЫ Классификация моносахаридов По типу карбонильной группы: альдегид - альдоза, кетон - кетоза 2. По числу атомов С в скелете: 5 - пентоза, 6 - гексоза и т.п. Можно объединить два критерия : альдопентоза кетогексоза
Слайд 4
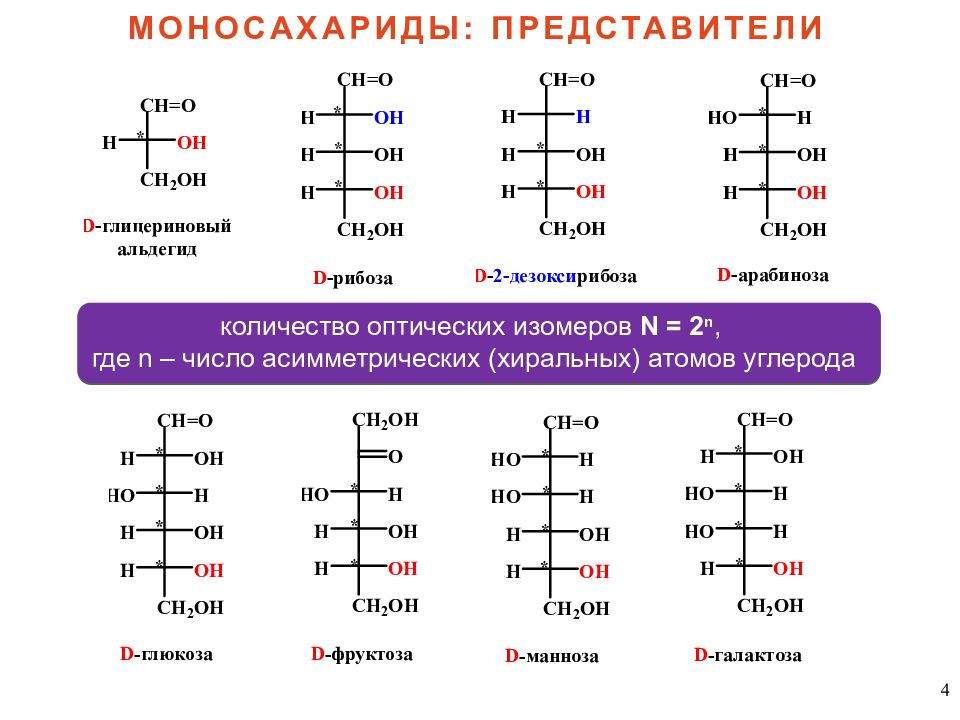
4 МОНОСАХАРИДЫ: ПРЕДСТАВИТЕЛИ количество оптических изомеров N = 2 n, где n – число асимметрических ( хиральных ) атомов углерода
Слайд 5
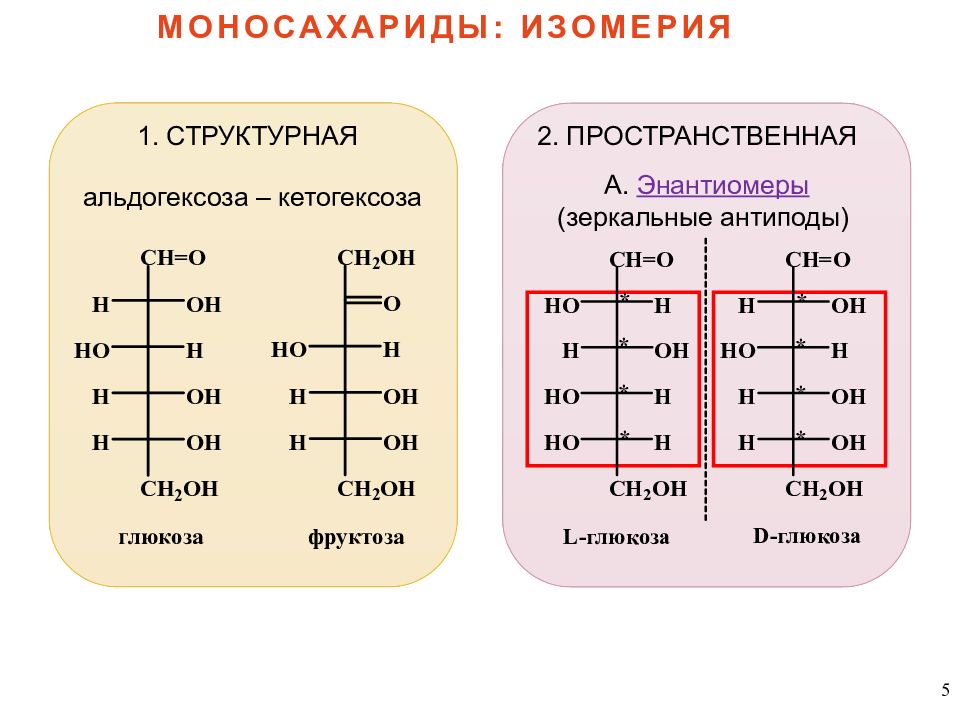
5 МОНОСАХАРИДЫ: ИЗОМЕРИЯ 1. СТРУКТУРНАЯ альдогексоза – кетогексоза 2. ПРОСТРАНСТВЕННАЯ А. Энантиомеры (зеркальные антиподы)
Слайд 6
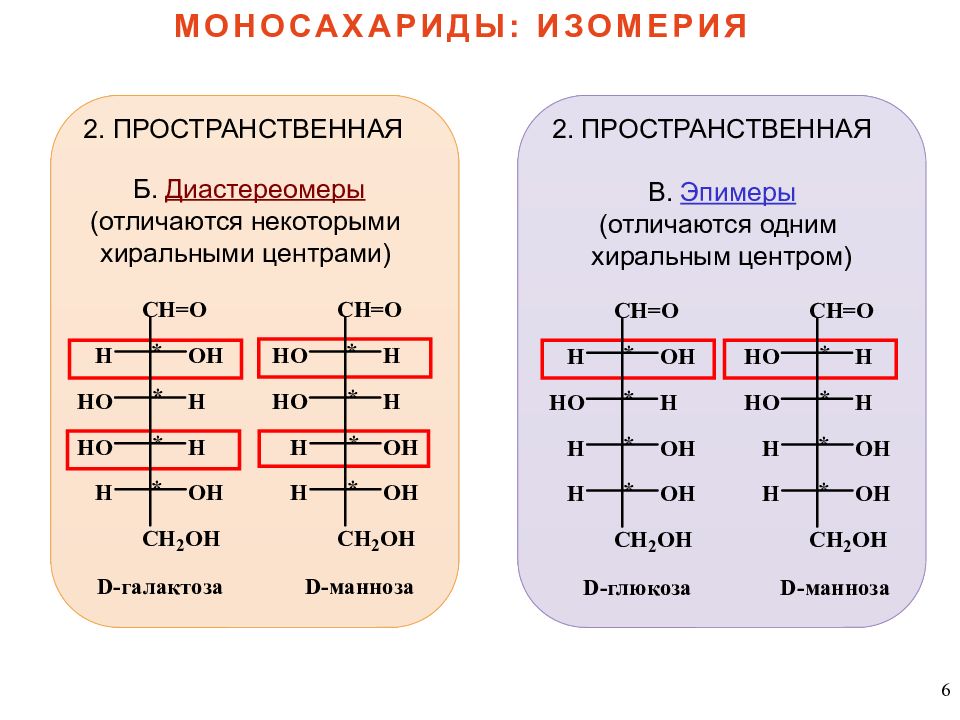
6 МОНОСАХАРИДЫ: ИЗОМЕРИЯ 2. ПРОСТРАНСТВЕННАЯ Б. Диастереомеры (отличаются некоторыми хиральными центрами) 2. ПРОСТРАНСТВЕННАЯ В. Эпимеры (отличаются одним хиральным центром)
Слайд 7
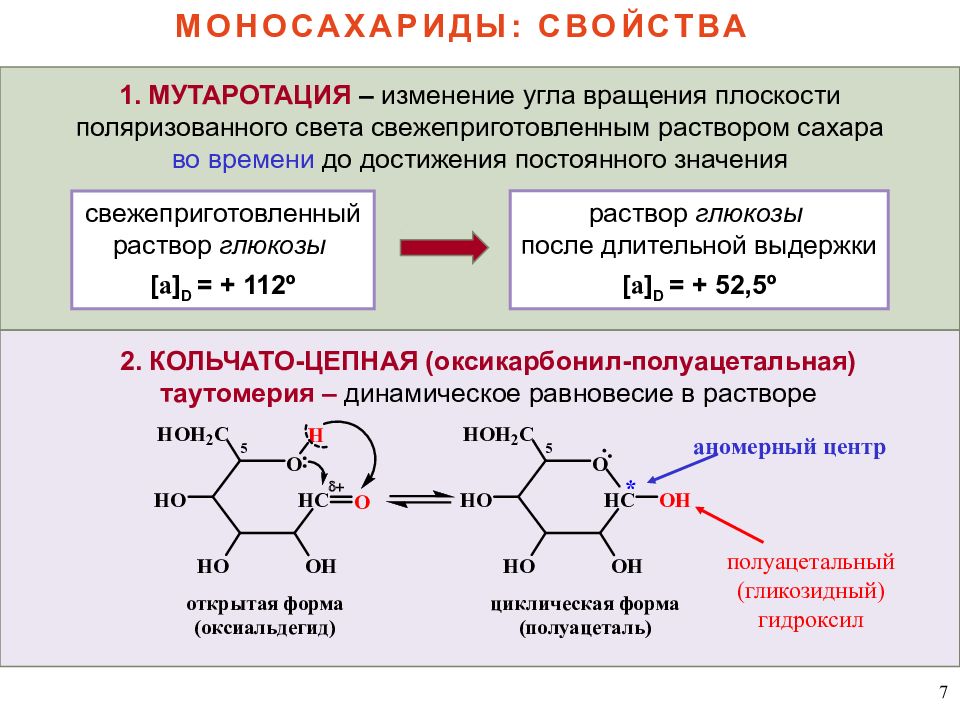
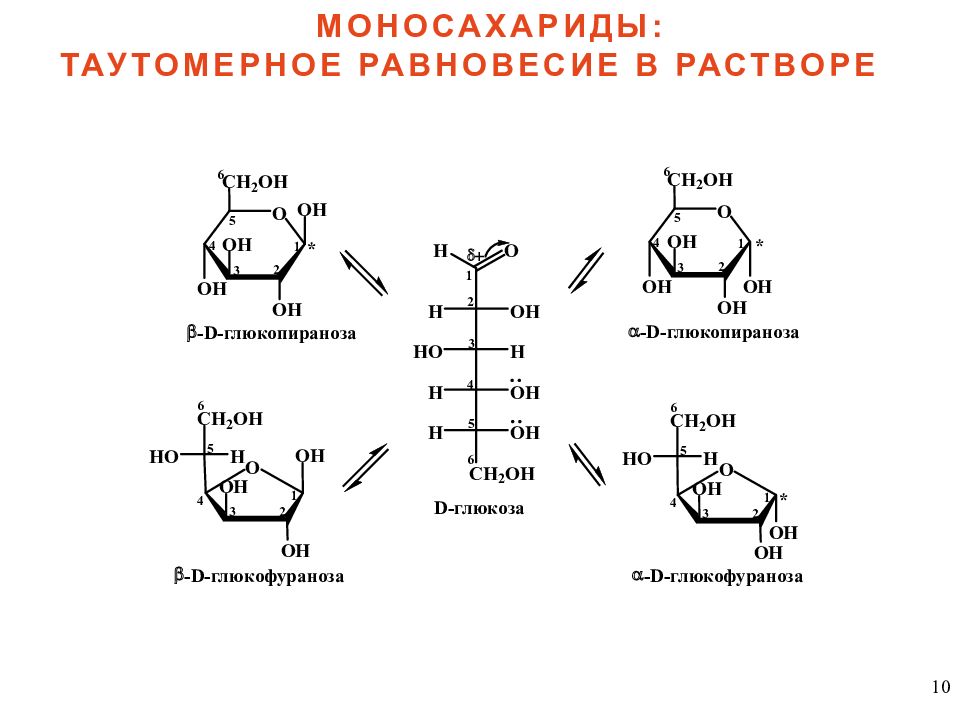
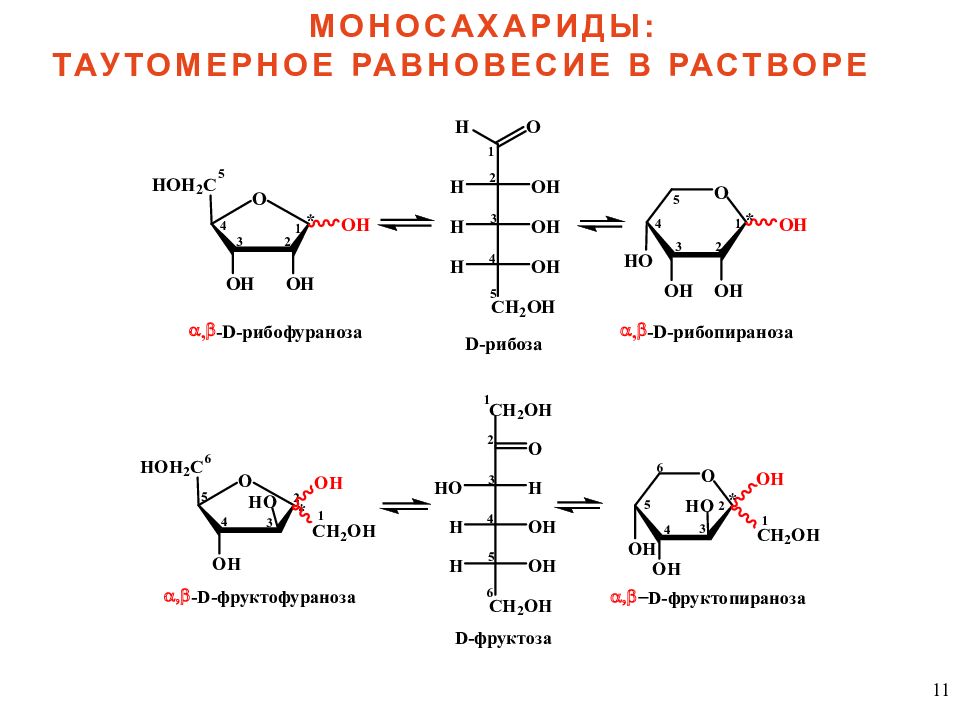
7 свежеприготовленный раствор глюкозы [ a ] D = + 11 2 º 1. МУТАРОТАЦИЯ – изменение угла вращения плоскости поляризованного света свежеприготовленным раствором сахара во времени до достижения постоянного значения МОНОСАХАРИДЫ: СВОЙСТВА раствор глюкозы после длительной выдержки [ a ] D = + 52,5 º 2. КОЛЬЧАТО-ЦЕПНАЯ (оксикарбонил-полуацетальная) таутомерия – динамическое равновесие в растворе полуацетальный ( гликозидный ) гидроксил аномерный центр
Слайд 8
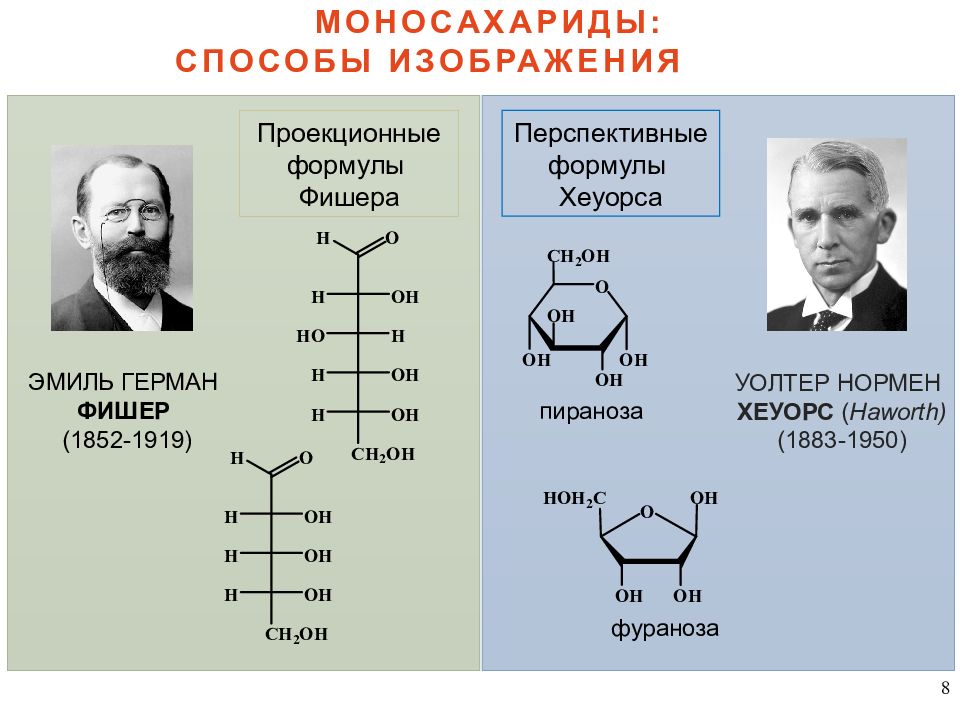
8 МОНОСАХАРИДЫ: СПОСОБЫ ИЗОБРАЖЕНИЯ Проекционные формулы Фишера Перспективные формулы Хеуорса ЭМИЛЬ ГЕРМАН ФИШЕР (1852-1919) УОЛТЕР НОРМЕН ХЕУОРС ( Haworth ) (1883-1950) пираноза фураноза
Слайд 9
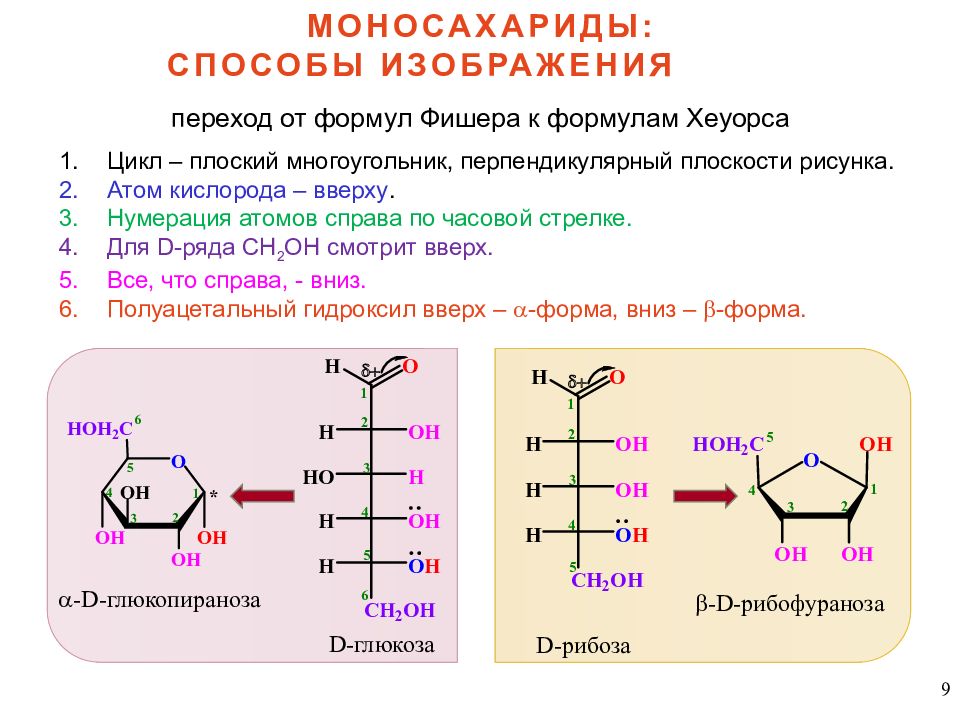
9 МОНОСАХАРИДЫ: СПОСОБЫ ИЗОБРАЖЕНИЯ переход от формул Фишера к формулам Хеуорса Цикл – плоский многоугольник, перпендикулярный плоскости рисунка. Атом кислорода – вверху. Нумерация атомов справа по часовой стрелке. Для D -ряда CH 2 OH смотрит вверх. Все, что справа, - вниз. Полуацетальный гидроксил вверх – -форма, вниз – -форма. -D- глюкопираноза D- рибоза D- глюкоза - D- рибофураноза
Слайд 12
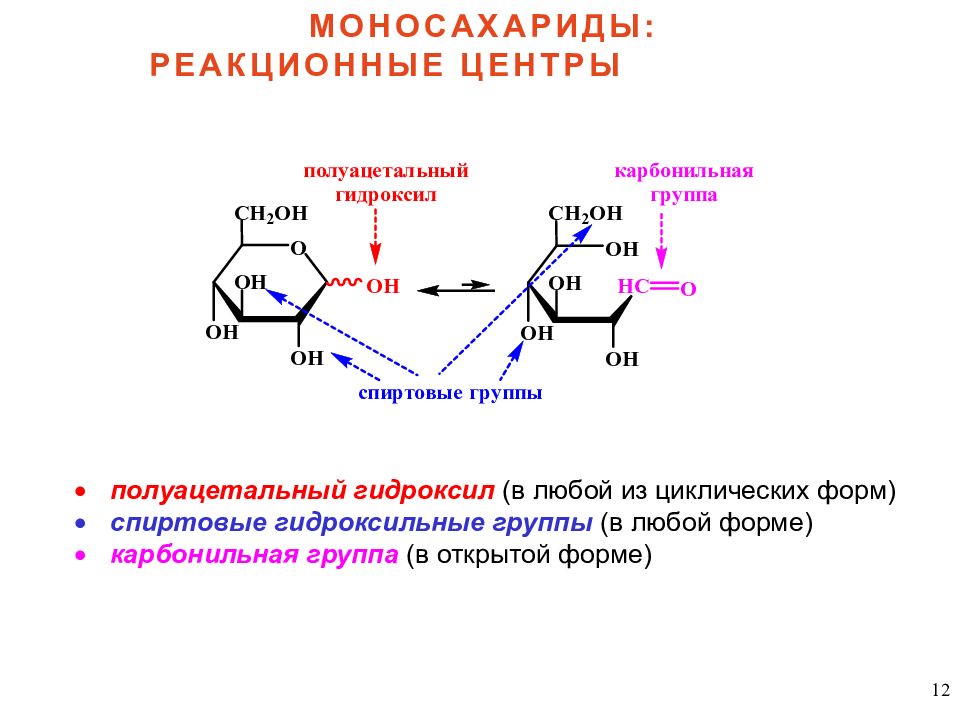
12 полуацетальный гидроксил (в любой из циклических форм) спиртовые гидроксильные группы (в любой форме) карбонильная группа (в открытой форме) МОНОСАХАРИДЫ: РЕАКЦИОННЫЕ ЦЕНТРЫ
Слайд 13
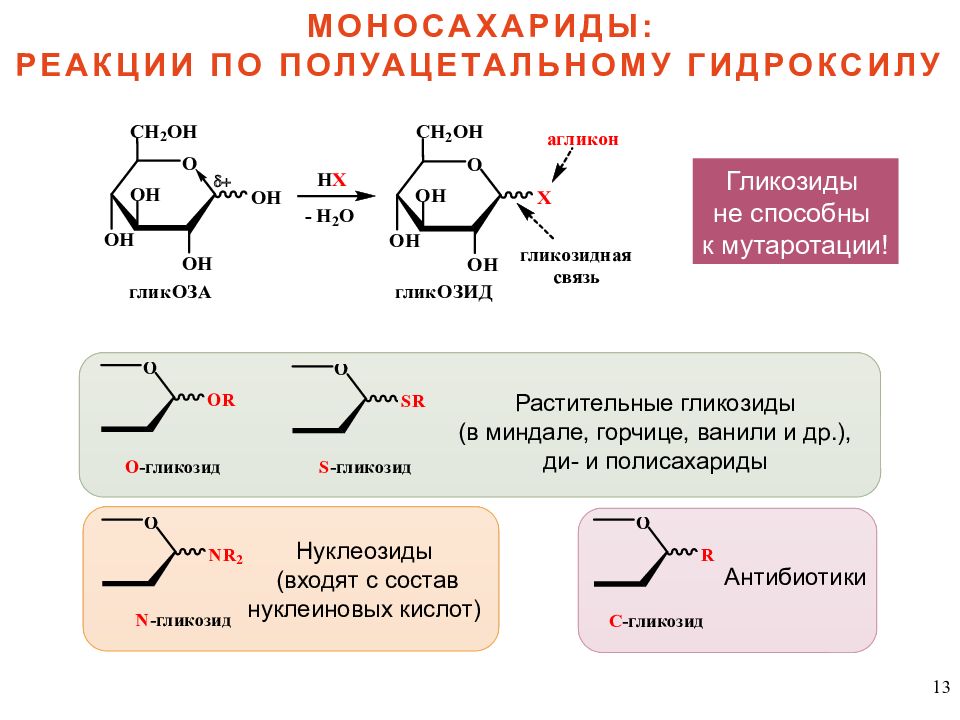
13 МОНОСАХАРИДЫ: РЕАКЦИИ ПО ПОЛУАЦЕТАЛЬНОМУ ГИДРОКСИЛУ Растительные гликозиды (в миндале, горчице, ванили и др.), ди- и полисахариды Нуклеозиды (входят с состав нуклеиновых кислот) Антибиотики Гликозиды не способны к мутаротации!
Слайд 14
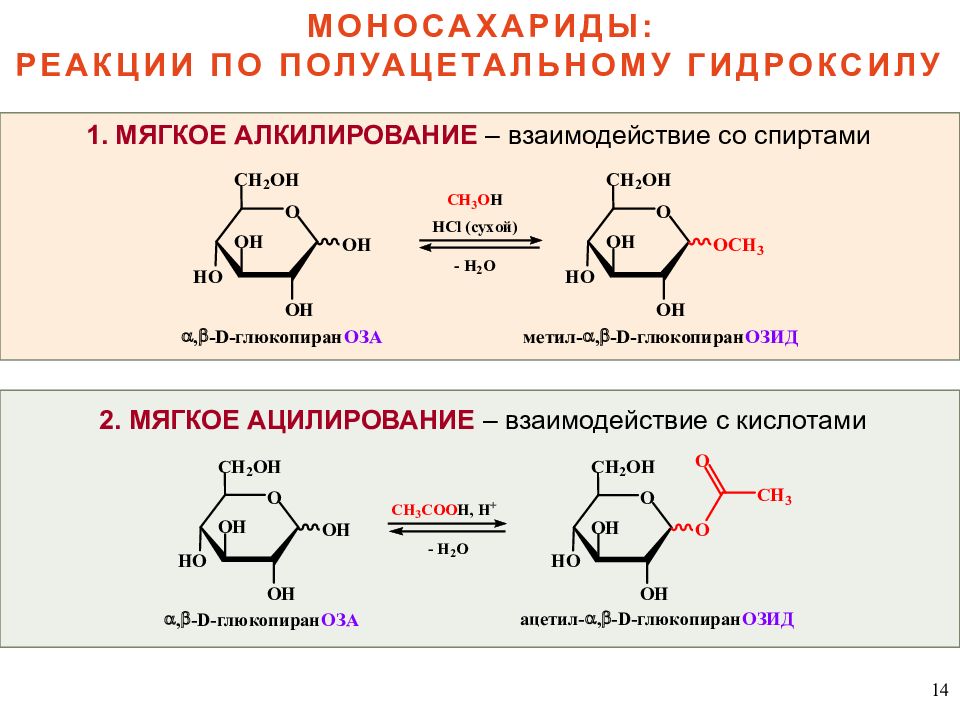
14 МОНОСАХАРИДЫ: РЕАКЦИИ ПО ПОЛУАЦЕТАЛЬНОМУ ГИДРОКСИЛУ 1. МЯГКОЕ АЛКИЛИРОВАНИЕ – взаимодействие со спиртами 2. МЯГКОЕ АЦИЛИРОВАНИЕ – взаимодействие с кислотами
Слайд 15
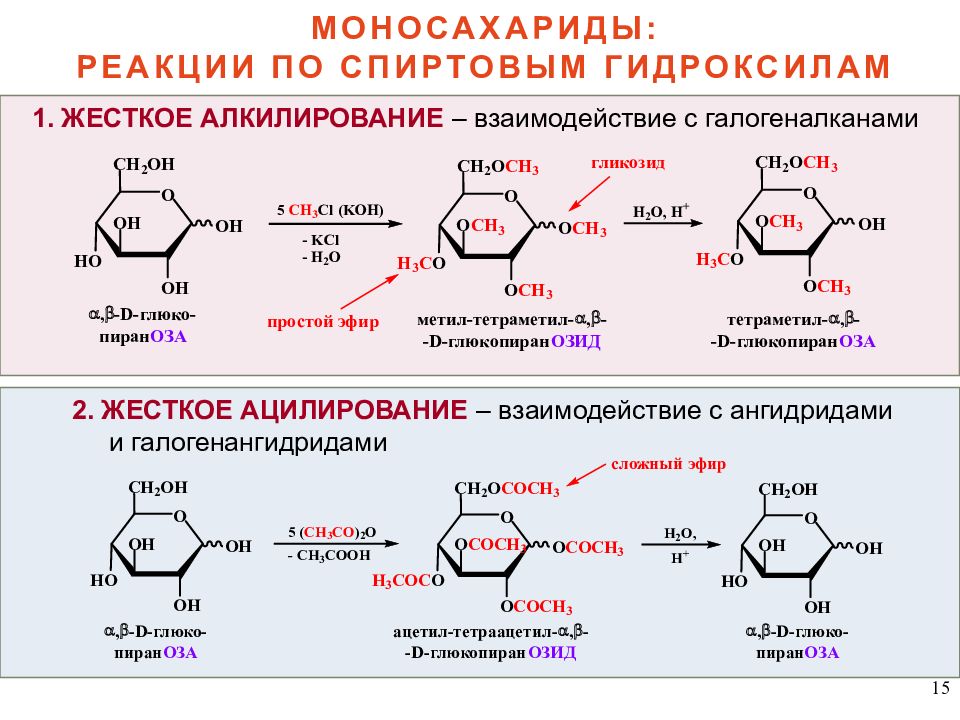
15 МОНОСАХАРИДЫ: РЕАКЦИИ ПО СПИРТОВЫМ ГИДРОКСИЛАМ 1. ЖЕСТКОЕ АЛКИЛИРОВАНИЕ – взаимодействие с галогеналканами 2. ЖЕСТКОЕ АЦИЛИРОВАНИЕ – взаимодействие с ангидридами и галогенангидридами
Слайд 16
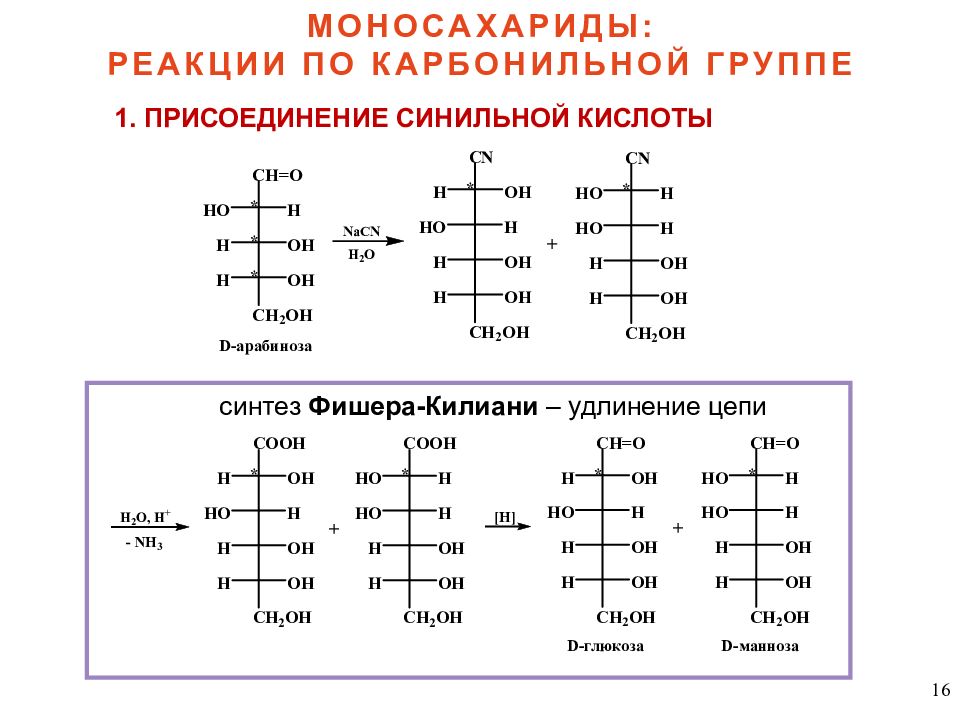
16 МОНОСАХАРИДЫ: РЕАКЦИИ ПО КАРБОНИЛЬНОЙ ГРУППЕ 1. ПРИСОЕДИНЕНИЕ СИНИЛЬНОЙ КИСЛОТЫ синтез Фишера-Килиани – удлинение цепи
Слайд 17
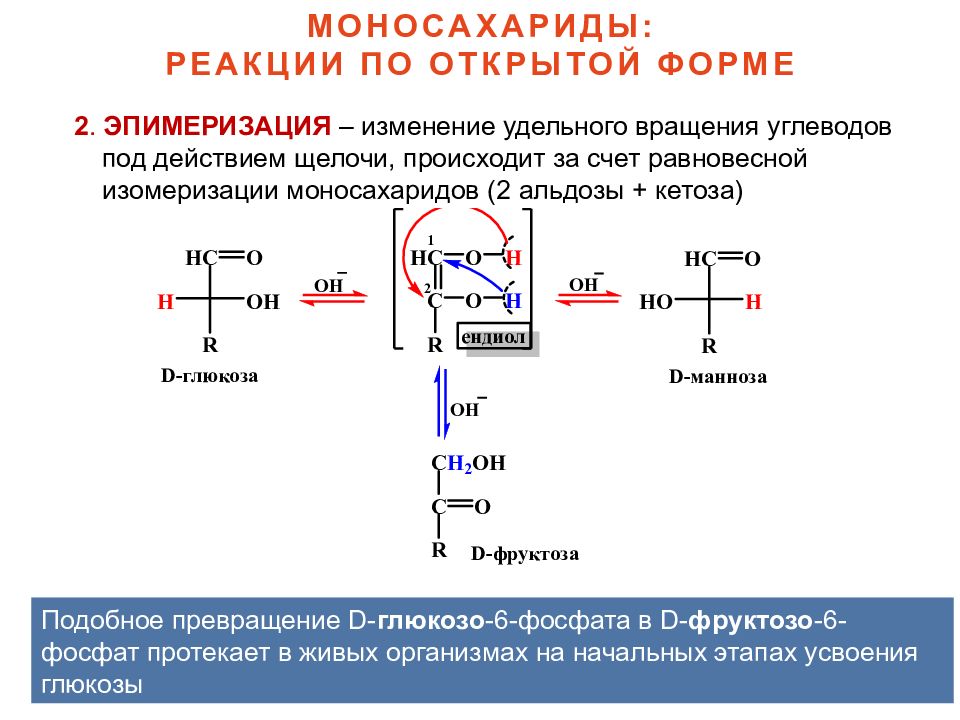
17 МОНОСАХАРИДЫ: РЕАКЦИИ ПО ОТКРЫТОЙ ФОРМЕ 2. ЭПИМЕРИЗАЦИЯ – изменение удельного вращения углеводов под действием щелочи, происходит за счет равновесной изомеризации моносахаридов ( 2 альдозы + кетоза) Подобное превращение D - глюкозо -6-фосфата в D - фруктозо -6-фосфат протекает в живых организмах на начальных этапах усвоения глюкозы
Слайд 18
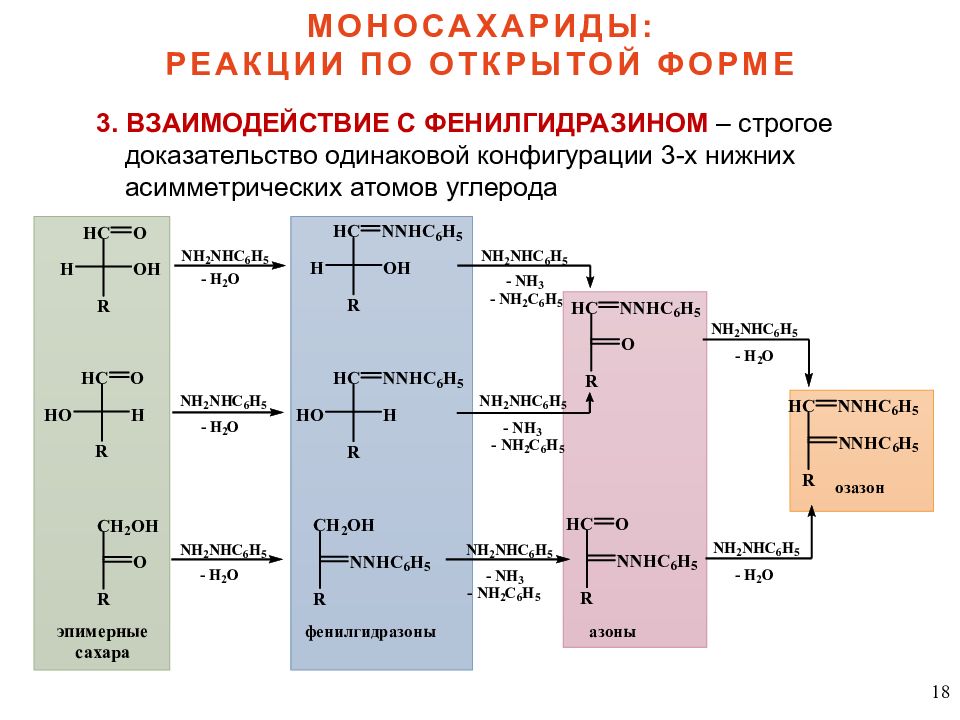
18 МОНОСАХАРИДЫ: РЕАКЦИИ ПО ОТКРЫТОЙ ФОРМЕ 3. ВЗАИМОДЕЙСТВИЕ С ФЕНИЛГИДРАЗИНОМ – строгое доказательство одинаковой конфигурации 3-х нижних асимметрических атомов углерода
Слайд 19
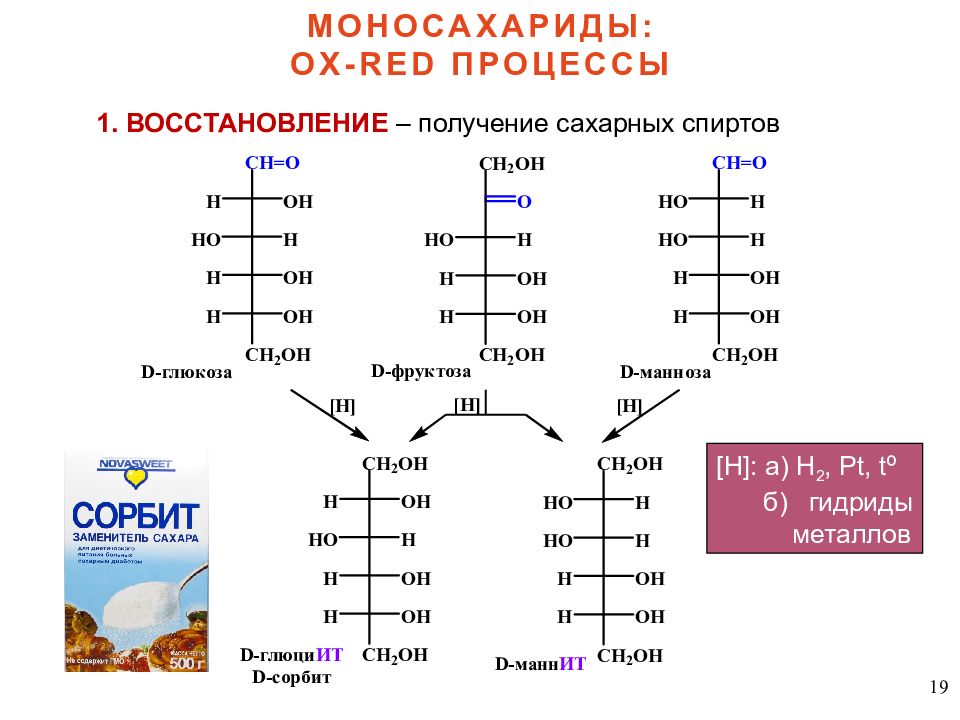
19 МОНОСАХАРИДЫ: OX-RED ПРОЦЕССЫ 1. ВОССТАНОВЛЕНИЕ – получение сахарных спиртов [H] : а) Н 2, Pt, tº б) гидриды металлов
Слайд 20
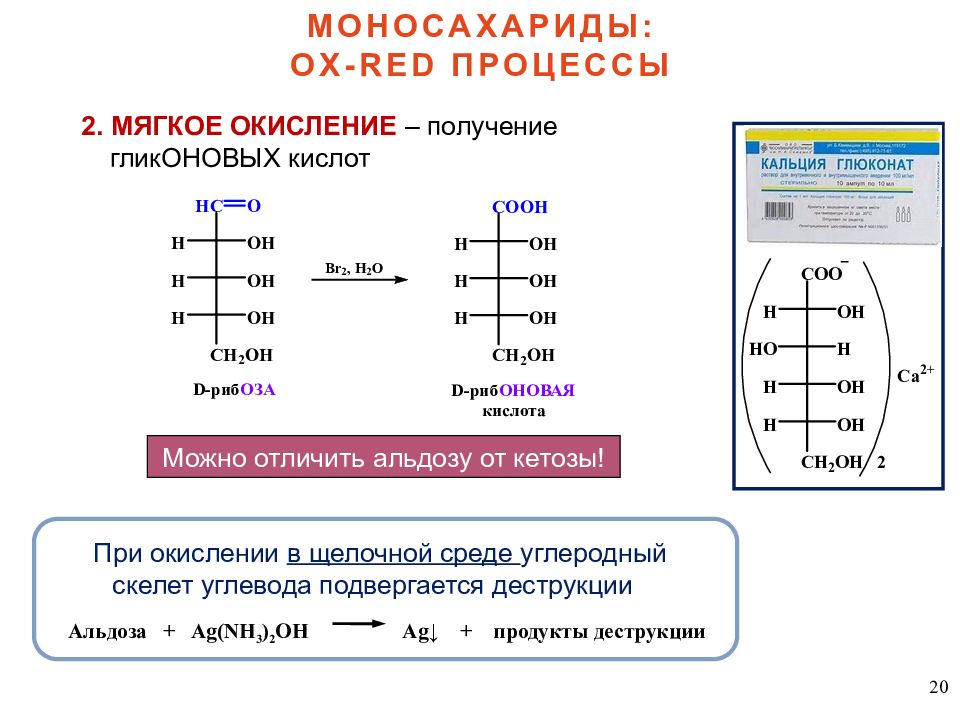
20 2. МЯГКОЕ ОКИСЛЕНИЕ – получение гликОНОВЫХ кислот Можно отличить альдозу от кетозы ! При окислении в щелочной среде углеродный скелет углевода подвергается деструкции Альдоза + Ag(NH 3 ) 2 OH Ag ↓ + продукты деструкции МОНОСАХАРИДЫ: OX-RED ПРОЦЕССЫ
Слайд 21
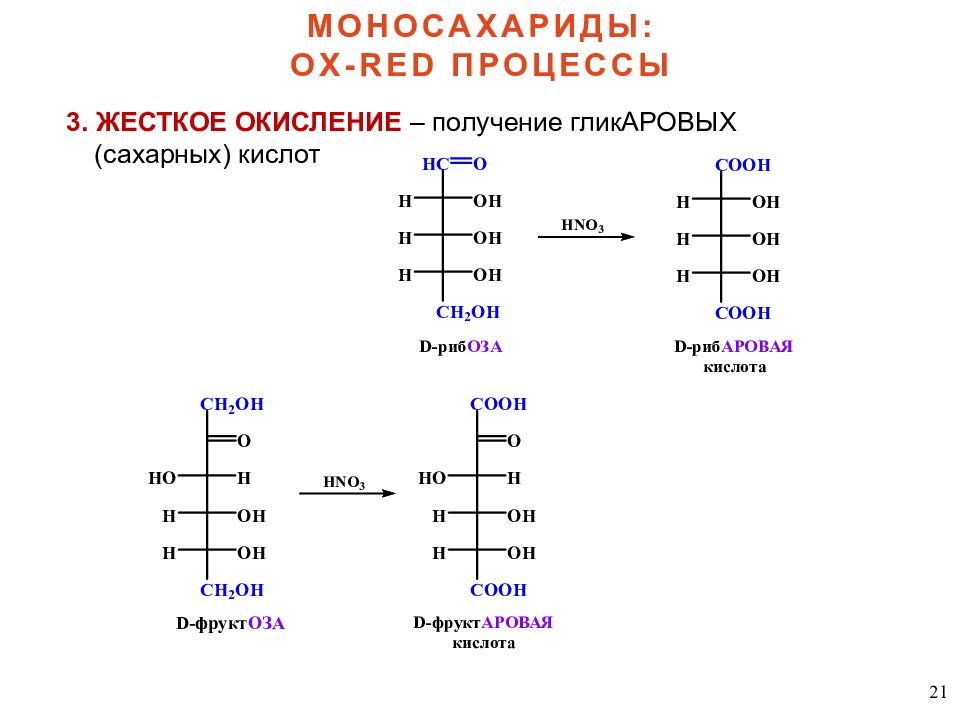
21 3. ЖЕСТКОЕ ОКИСЛЕНИЕ – получение гликАРОВЫХ (сахарных) кислот МОНОСАХАРИДЫ: OX-RED ПРОЦЕССЫ
Слайд 22
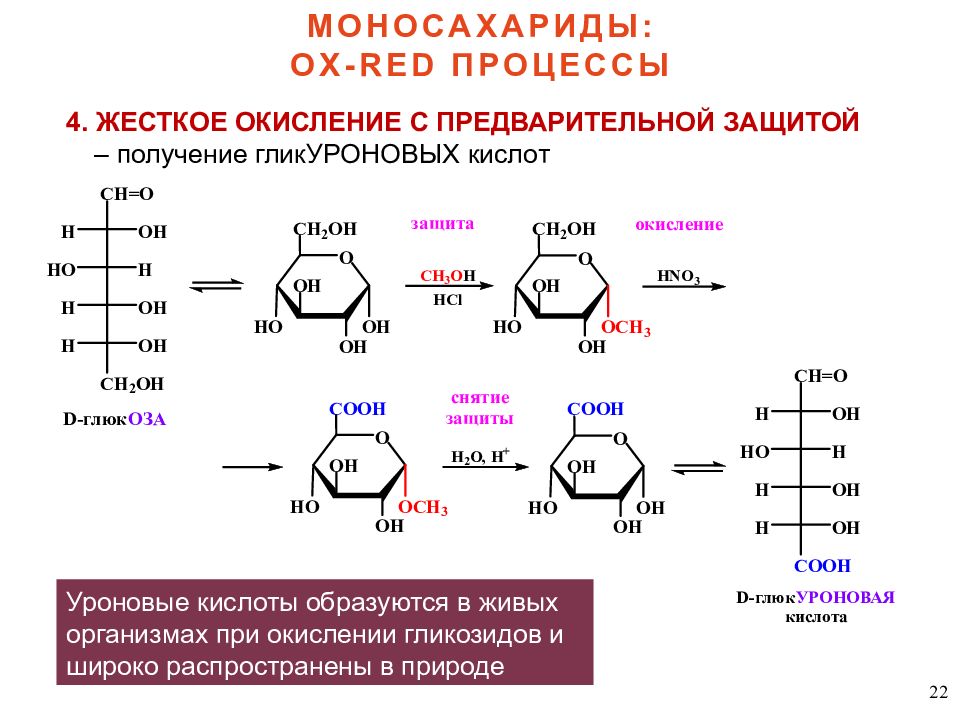
22 4. ЖЕСТКОЕ ОКИСЛЕНИЕ С ПРЕДВАРИТЕЛЬНОЙ ЗАЩИТОЙ – получение гликУРОНОВЫХ кислот МОНОСАХАРИДЫ: OX-RED ПРОЦЕССЫ Уроновые кислоты образуются в живых организмах при окислении гликозидов и широко распространены в природе
Слайд 23
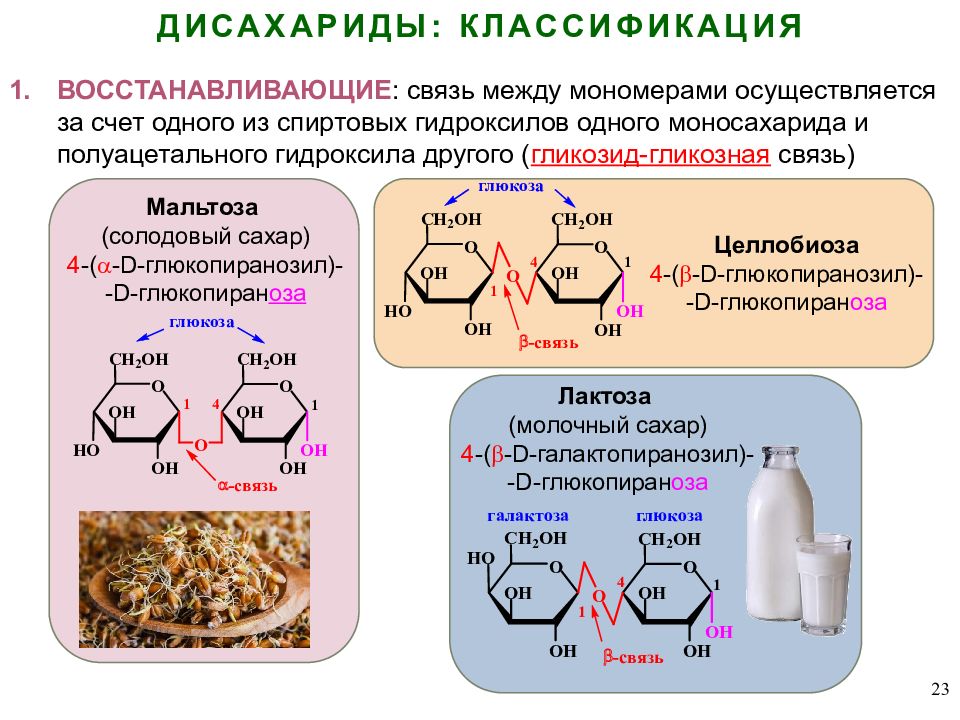
23 ДИСАХАРИДЫ: КЛАССИФИКАЦИЯ ВОССТАНАВЛИВАЮЩИЕ : связь между мономерами осуществляется за счет одного из спиртовых гидроксилов одного моносахарида и полуацетального гидроксила другого ( гликозид- гликозная связь) Мальтоза (солодовый сахар) 4 -( -D-глюкопиранозил)- -D-глюкопиран оза Целлобиоза 4 -( -D-глюкопиранозил)- -D-глюкопиран оза Лактоза (молочный сахар) 4 -( -D-галактопиранозил)- -D-глюкопиран оза
Слайд 24
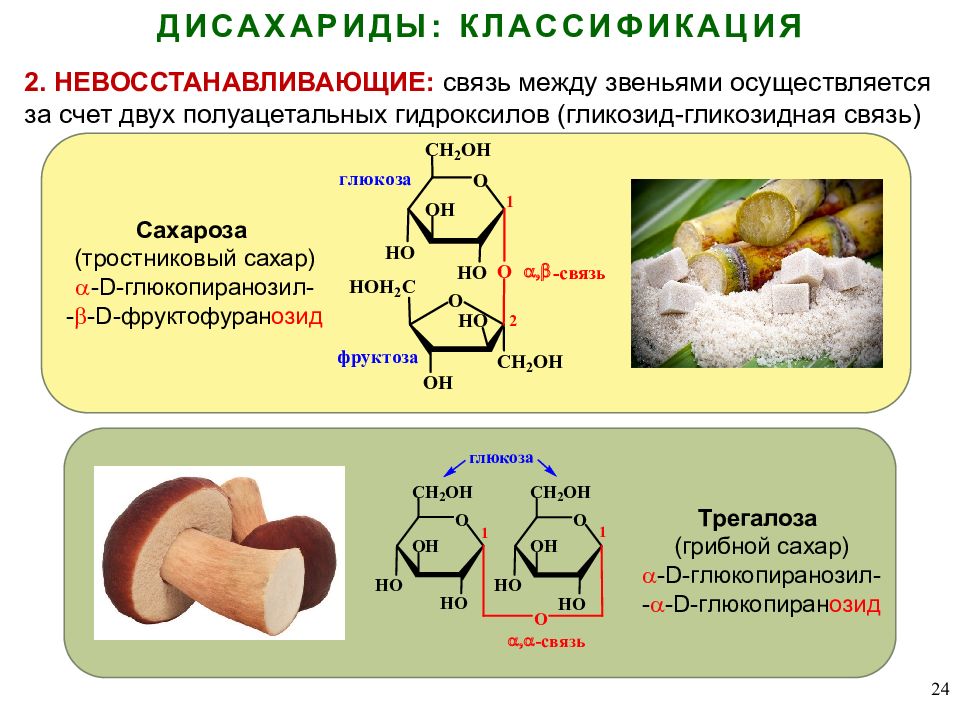
24 ДИСАХАРИДЫ: КЛАССИФИКАЦИЯ Трегалоза (грибной сахар) -D-глюкопиранозил- - -D-глюкопиран озид 2. НЕВОССТАНАВЛИВАЮЩИЕ: связь между звеньями осуществляется за счет двух полуацетальных гидроксилов (гликозид- гликозидная связь) Сахароза (тростниковый сахар) -D-глюкопиранозил- - -D-фруктофуран озид
Слайд 25
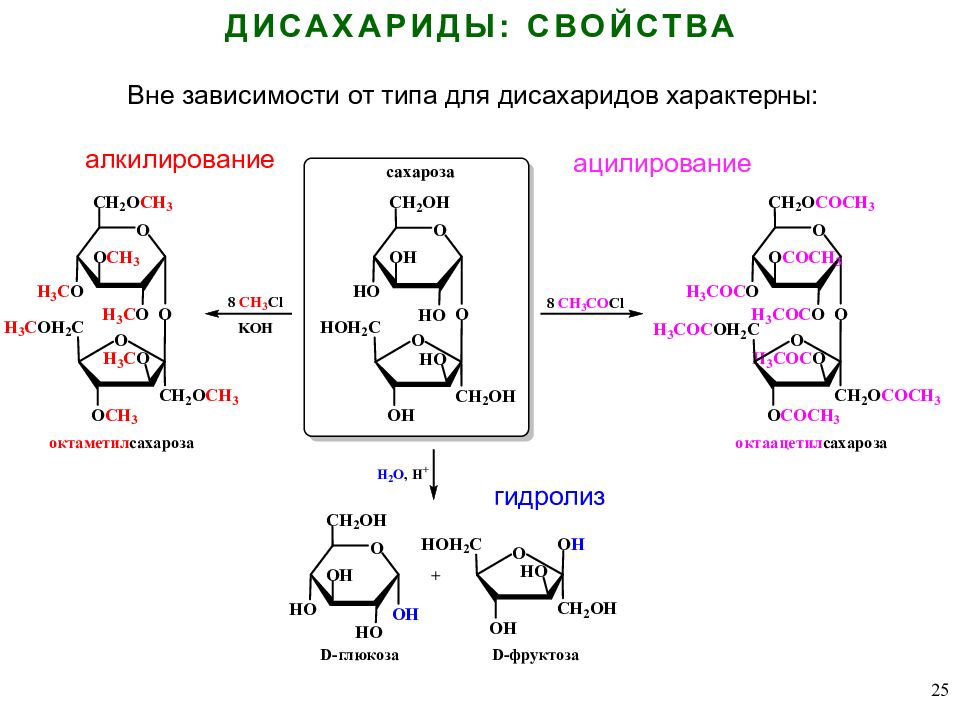
25 ДИСАХАРИДЫ: СВОЙСТВА алкилирование ацилирование гидролиз Вне зависимости от типа для дисахаридов характерны:
Слайд 26
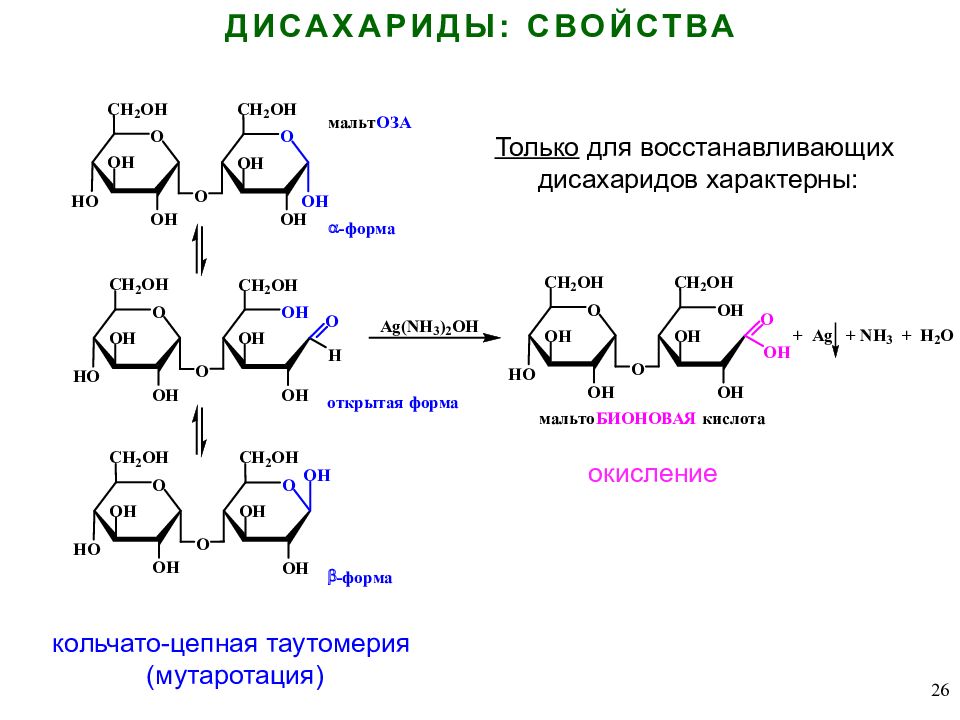
26 ДИСАХАРИДЫ: СВОЙСТВА окисление кольчато-цепная таутомерия (мутаротация) Только для восстанавливающих дисахаридов характерны:
Слайд 27
27 ГОМОПОЛИСАХАРИДЫ ЦЕЛЛЮЛОЗА (клетчатка) – полимер D -глюкозы, остатки которой соединены -(1-4) - гликозидными связями. Имеет строго линейное нитевидное строение. Структурный полисахарид. Не переваривается большинством живых организмов.
Слайд 28
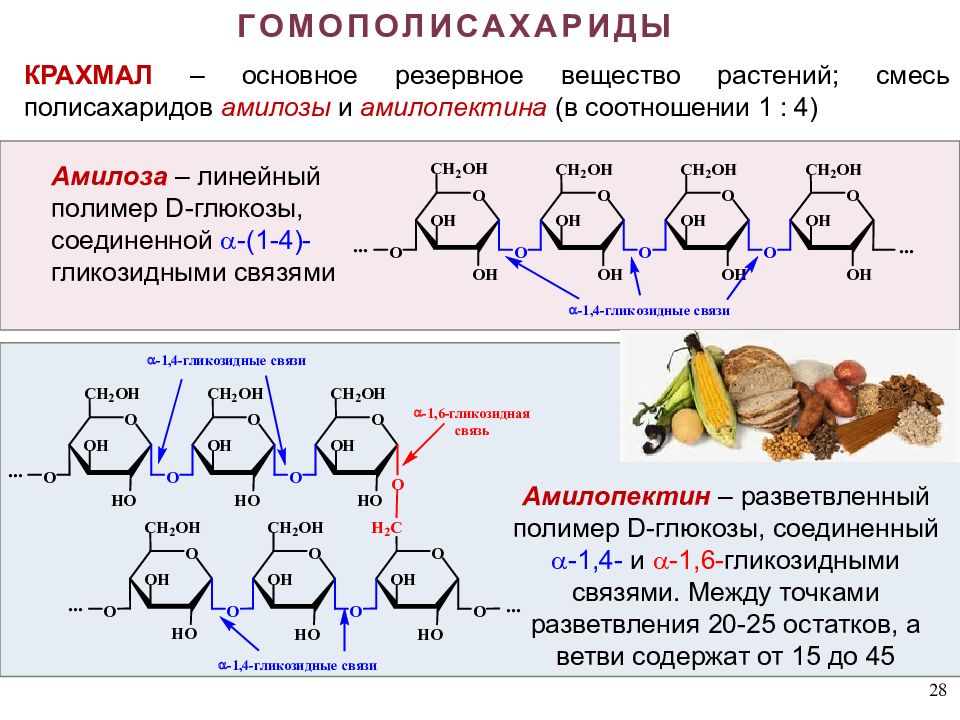
28 ГОМОПОЛИСАХАРИДЫ КРАХМАЛ – основное резервное вещество растений; смесь полисахаридов амилозы и амилопектина (в соотношении 1 : 4 ) Амилопектин – разветвленный полимер D -глюкозы, соединенный -1,4- и -1,6- гликозидными связями. Между точками разветвления 20-25 остатков, а ветви содержат от 15 до 45 Амилоза – линейный полимер D -глюкозы, соединенной -(1-4)- гликозидными связями
Последний слайд презентации: 1 Кафедра химии Тема лекции : УГЛЕВОДЫ
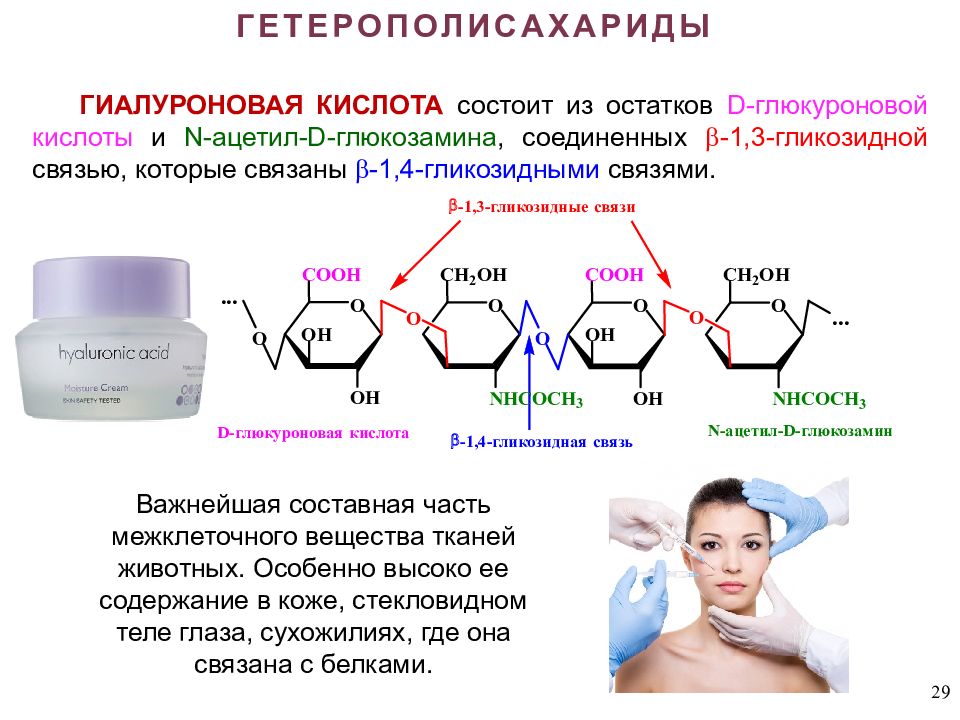
29 ГЕТЕРОПОЛИСАХАРИДЫ Важнейшая составная часть межклеточного вещества тканей животных. Особенно высоко ее содержание в коже, стекловидном теле глаза, сухожилиях, где она связана с белками. ГИАЛУРОНОВАЯ КИСЛОТА состоит из остатков D - глюкуроновой кислоты и N -ацетил- D -глюкозамина, соединенных -1,3-гликозидной связью, которые связаны -1,4-гликозидными связями.