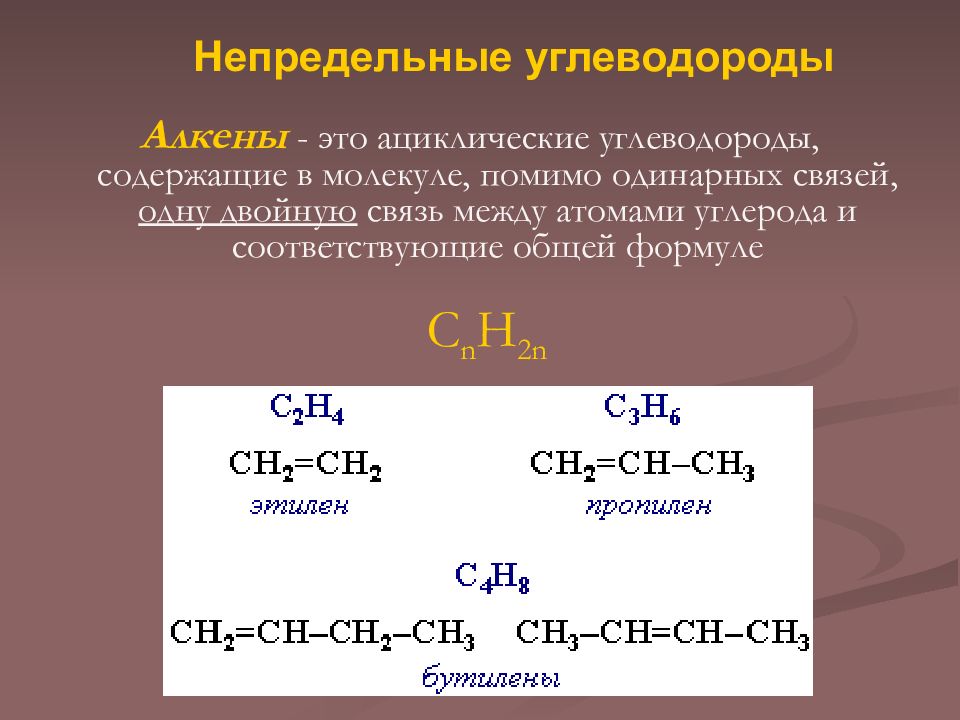
Слайд 2: Непредельные углеводороды
Алкены - это ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле C n H 2n
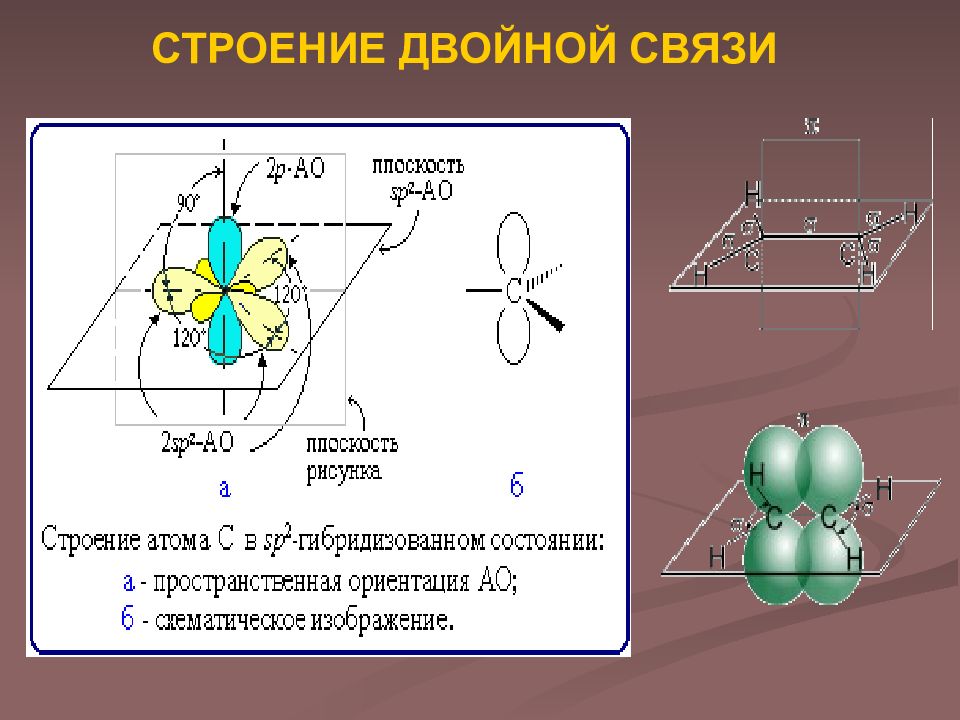
Слайд 3: СТРОЕНИЕ ДВОЙНОЙ СВЯЗИ
В отличие от предельных углеводородов, алкены содержат двойную связь С=С, которая осуществляется 4-мя общими электронами: δ -связь возникает при осевом перекрывании sp 2 -гибридных орбиталей, а π -связь – при боковом перекрывании р-орбиталей соседних sp 2 -гибридизованных атомов углерода По своей природе π -связь резко отличается от δ -связи: π -связь менее прочная вследствие меньшей эффективности перекрывания р-орбиталей Модели молекулы этилена:
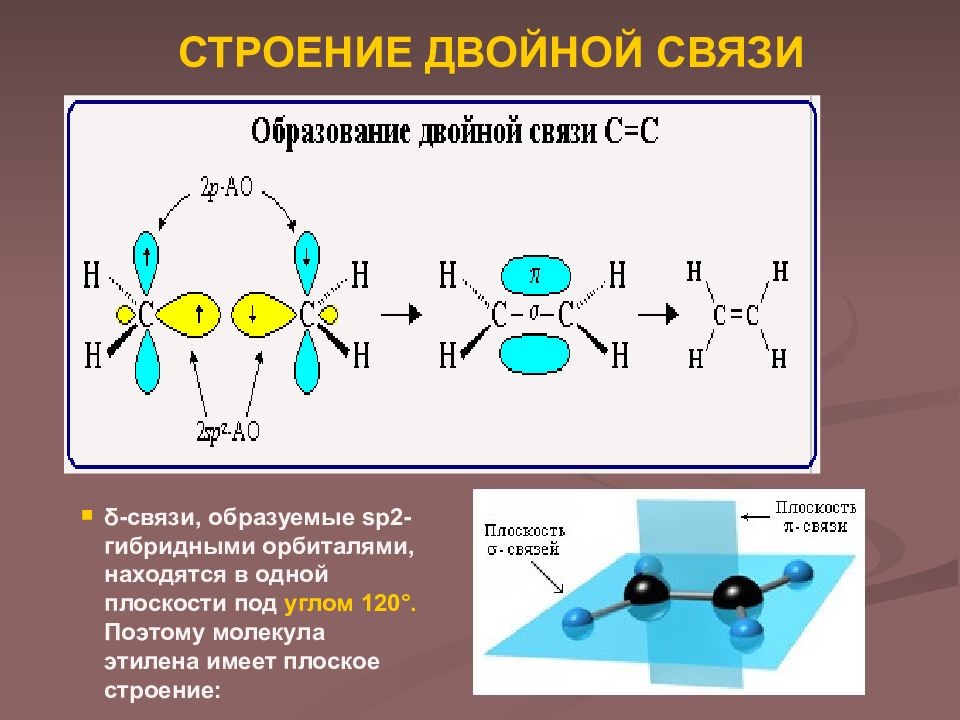
Слайд 5: СТРОЕНИЕ ДВОЙНОЙ СВЯЗИ
δ -связи, образуемые sp2-гибридными орбиталями, находятся в одной плоскости под углом 120°. Поэтому молекула этилена имеет плоское строение:
Слайд 6: Номенклатура алкенов
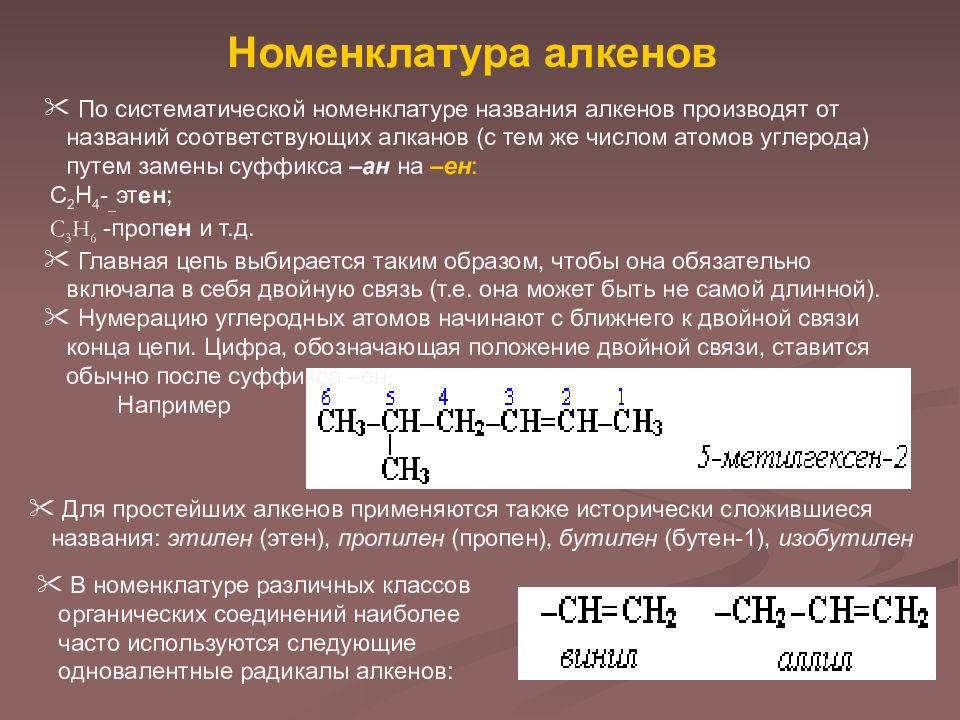
По систематической номенклатуре названия алкенов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ен : С 2 Н 4 - _ эт ен ; С 3 Н 6 -проп ен и т.д. Главная цепь выбирается таким образом, чтобы она обязательно включала в себя двойную связь (т.е. она может быть не самой длинной). Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится обычно после суффикса –ен. Например Для простейших алкенов применяются также исторически сложившиеся названия: этилен (этен), пропилен (пропен), бутилен (бутен-1), изобутилен В номенклатуре различных классов органических соединений наиболее часто используются следующие одновалентные радикалы алкенов:
Слайд 7: Изомерия алкенов
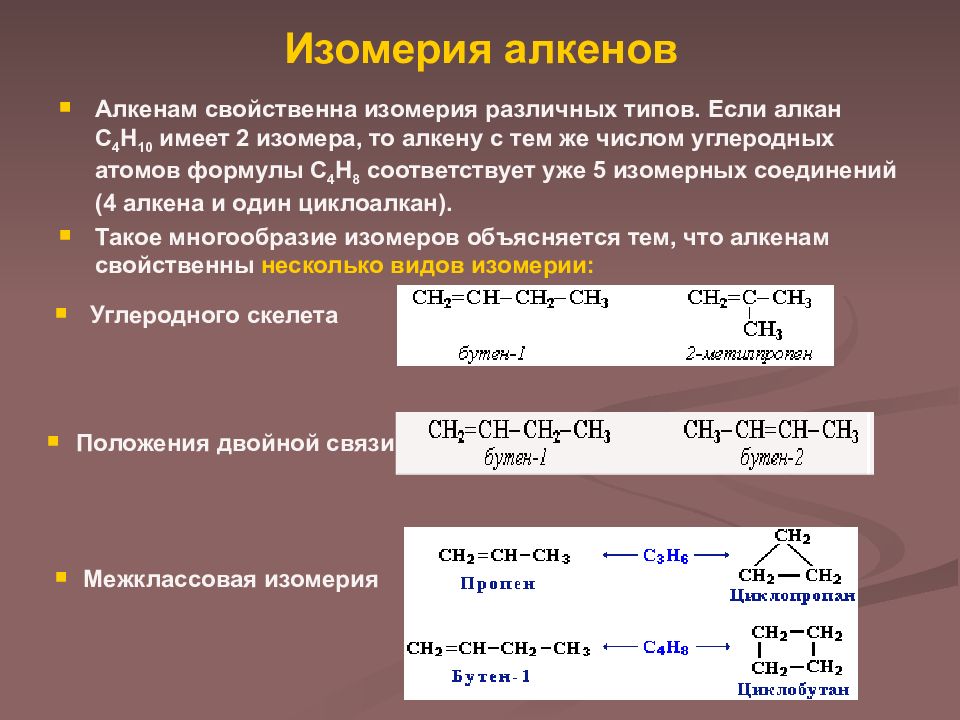
Алкенам свойственна изомерия различных типов. Если алкан С 4 Н 10 имеет 2 изомера, то алкену с тем же числом углеродных атомов формулы С 4 Н 8 соответствует уже 5 изомерных соединений (4 алкена и один циклоалкан). Такое многообразие изомеров объясняется тем, что алкенам свойственны несколько видов изомерии: Межклассовая изомерия Положения двойной связи Углеродного скелета
Слайд 8: Пространственная изомерия
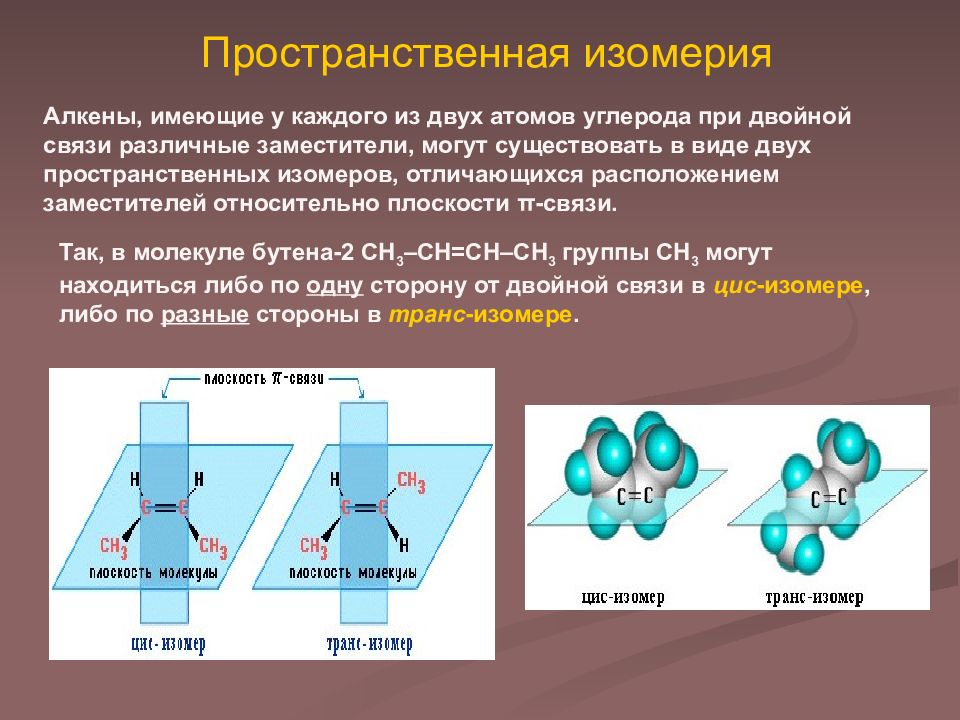
Алкены, имеющие у каждого из двух атомов углерода при двойной связи различные заместители, могут существовать в виде двух пространственных изомеров, отличающихся расположением заместителей относительно плоскости π -связи. Так, в молекуле бутена-2 СН 3 –СН=СН–СН 3 группы СН 3 могут находиться либо по одну сторону от двойной связи в цис -изомере, либо по разные стороны в транс -изомере.
Слайд 9: ФИЗИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ
Закономерно изменяются в гомологическом ряду: от С 2 Н 4 до С 4 Н 8 – газы начиная с С 5 Н 10 – жидкости с С 18 Н 36 – твердые веществ а Температура их плавления и кипения, а также плотность увеличиваются с ростом молекулярной массы Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях По физическим свойствам этиленовые углеводороды близки к алканам:
Слайд 10: ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ
Алкены вступают в разнообразные реакции присоединения: Гидрирование - реакции с водородом образуются алканы Галогенирование – реакции с галогенами образуются дигалогенопроизводные алканов Гидратации – реакции с водой образуются спирты Гидрогалогенирование – реакции с галогеноводородами образуются моногалогенопроизводные алканов
Слайд 11
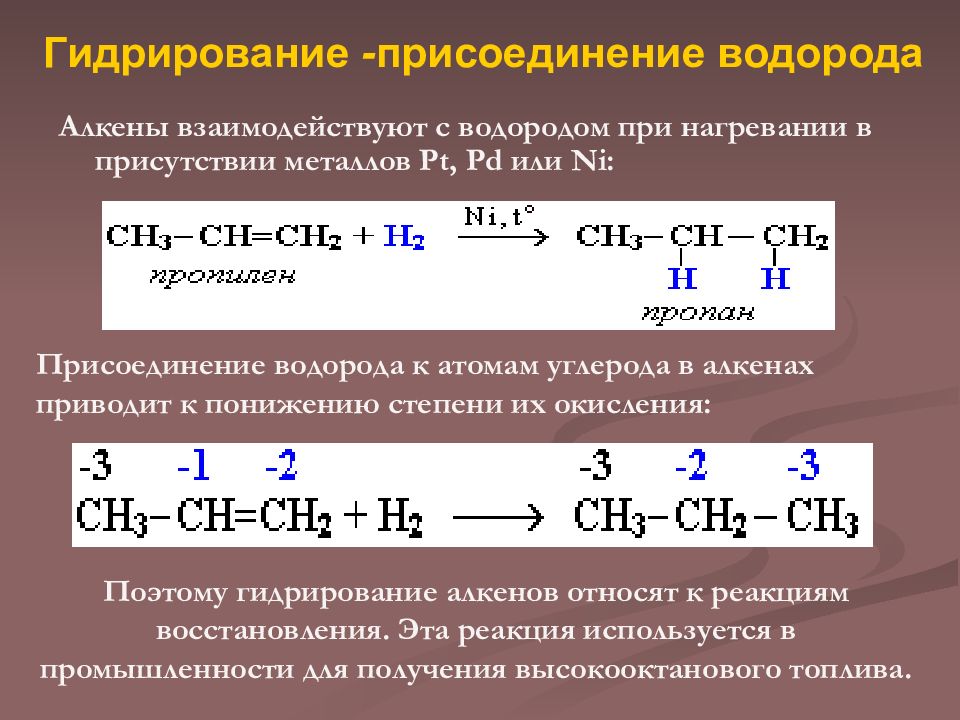
Алкены взаимодействуют с водородом при нагревании в присутствии металлов Pt, Pd или Ni: Гидрирование - присоединение водорода Присоединение водорода к атомам углерода в алкенах приводит к понижению степени их окисления: Поэтому гидрирование алкенов относят к реакциям восстановления. Эта реакция используется в промышленности для получения высокооктанового топлива.
Слайд 12
Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной температуре, без катализатора)Например, быстрое обесцвечивание красно-бурой окраски раствора брома в воде (бромной воды) служит качественной реакцией на наличие двойной связи Галогенирование - присоединение галогенов Эта реакция протекают по механизму электрофильного присоединения с гетеролитическим разрывом связей в молекуле галогена Еще легче происходит присоединение хлора:
Слайд 16: Гидратация - присоединение воды
Гидратация происходит в присутствии минеральных кислот по механизму электрофильного присоединения: В реакциях несимметричных алкенов соблюдается правило Марковникова:
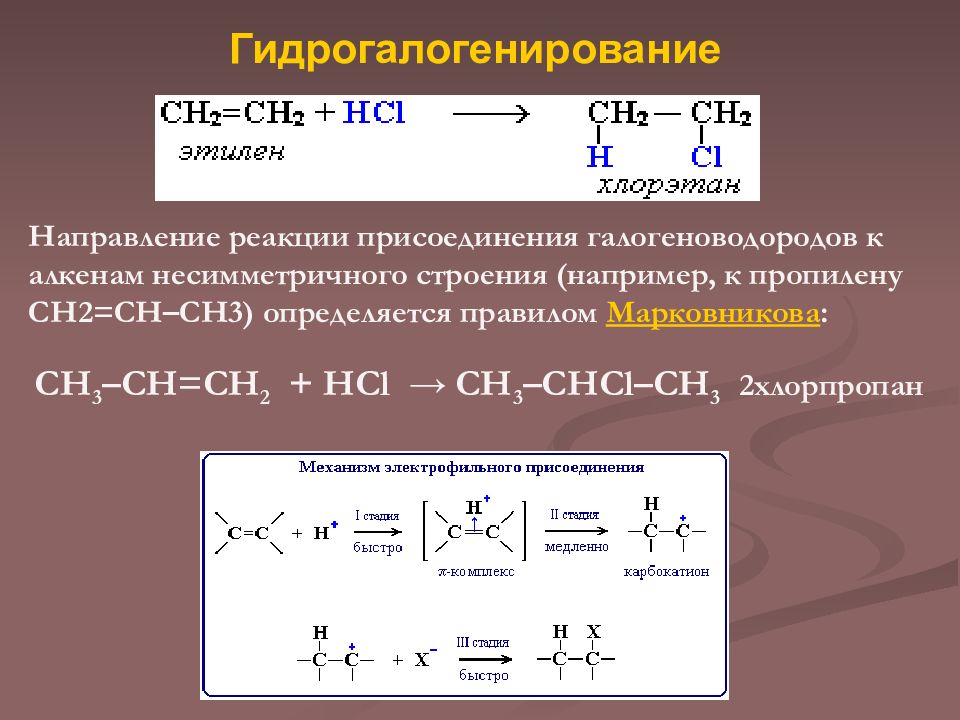
Слайд 17: Гидрогалогенирование
Направление реакции присоединения галогеноводородов к алкенам несимметричного строения (например, к пропилену CH2=CH–СН3) определяется правилом Марковникова : CH 3 –CH=CH 2 + H С l → CH 3 –CHCl–CH 3 2хлорпропан
Слайд 18: ОКИСЛЕНИЕ АЛКЕНОВ
Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакция Вагнера): В ходе этой реакции происходит обесцвечивание фиолетовой окраски водного раствора KMnO4. Поэтому она используется как качественная реакция на алкены Полное уравнение реакции:
Слайд 19: ИЗОМЕРИЗАЦИЯ АЛКЕНОВ
Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al 2 O 3 ) ИЗОМЕРИЗАЦИЯ АЛКЕНОВ Изомеризация алкенов приводит или к перемещению π –связи: или к перестройке углеродного скелета:
Слайд 20: ПОЛИМЕРИЗАЦИЯ АЛКЕНОВ
процесс образования высокомолекулярного соединения (полимера) путем соединения друг с другом молекул исходного низкомолекулярного соединения (мономера) При полимеризации двойные связи в молекулах исходного непредельного соединения "раскрываются", и за счет образующихся свободных валентностей эти молекулы соединяются друг с другом nCH 2 =CH 2 →( - CH 2 -CH 2 ) - n этилен полиэтилен
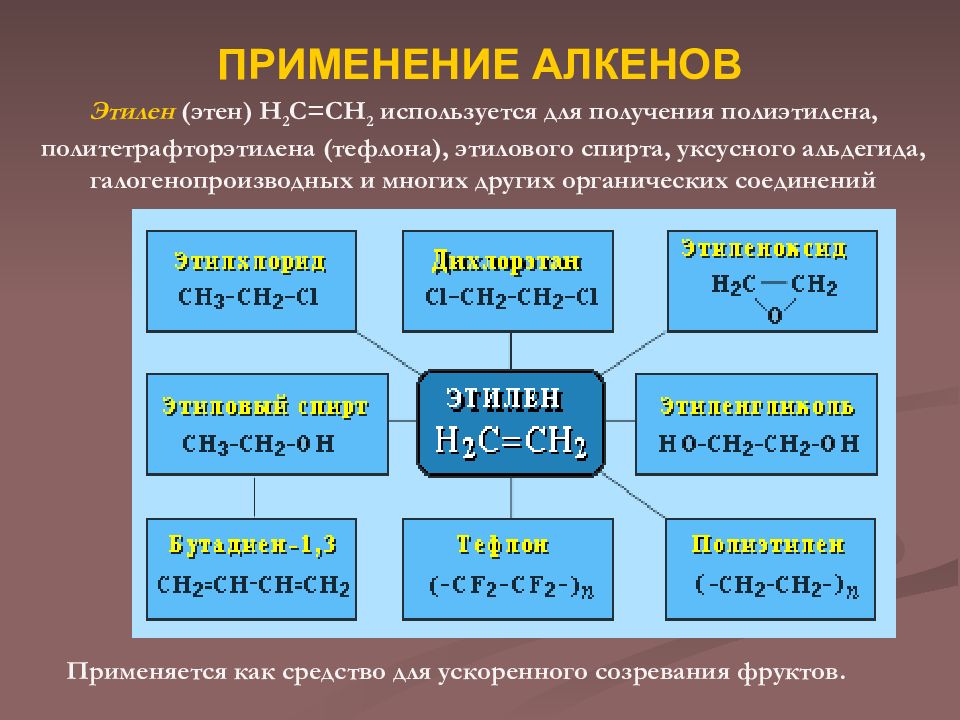
Слайд 21: ПРИМЕНЕНИЕ АЛКЕНОВ
Этилен (этен) Н 2 С=СН 2 используется для получения полиэтилена, политетрафторэтилена (тефлона), этилового спирта, уксусного альдегида, галогенопроизводных и многих других органических соединений Применяется как средство для ускоренного созревания фруктов.
Слайд 22: ПРИМЕНЕНИЕ АЛКЕНОВ
в качестве исходных продуктов в производстве полимерных материалов (пластмасс, каучуков, пленок) и других органических веществ Пропилен (пропен) Н2С=СН2–СН3 и бутилены (бутен-1 и бутен-2) используются для получения спиртов и полимеров Изобутилен (2-метилпропен) Н2С=С(СН3)2 применяется в производстве синтетического каучука
Слайд 23
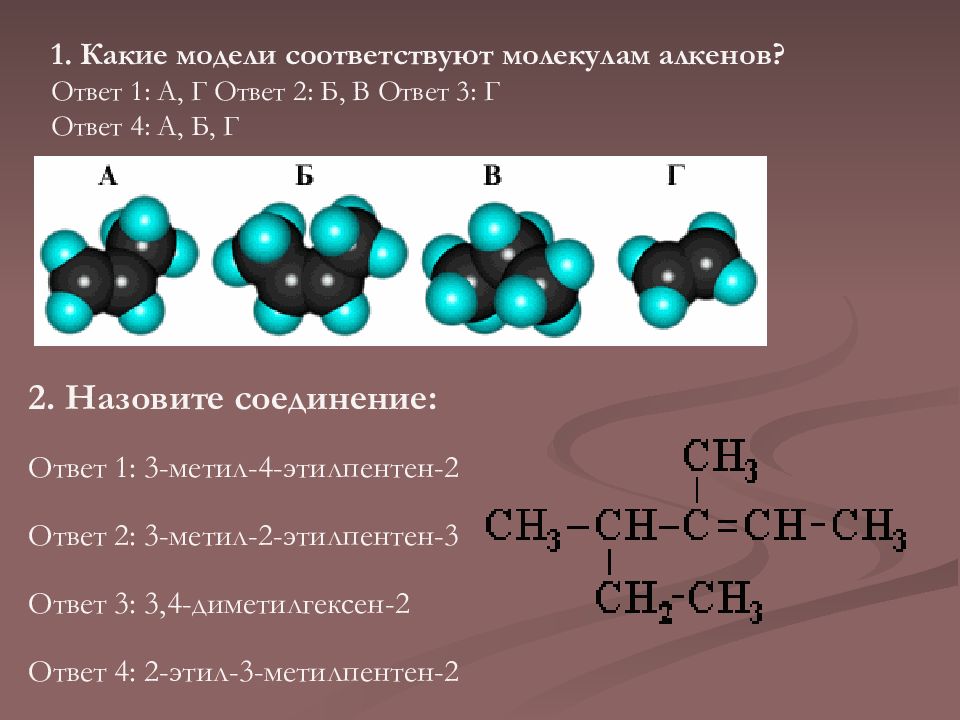
1. Какие модели соответствуют молекулам алкенов? Ответ 1 : А, Г Ответ 2 : Б, В Ответ 3 : Г Ответ 4 : А, Б, Г 2. Назовите соединение: Ответ 1 : 3-метил-4-этилпентен-2 Ответ 2 : 3-метил-2-этилпентен-3 Ответ 3 : 3,4-диметилгексен-2 Ответ 4 : 2-этил-3-метилпентен-2
Слайд 24
3. Сколько изомерных алкенов соответствует формуле С4Н8 ? Ответ 1 : изомеров нет Ответ 2 : два Ответ 3 : три Ответ 4 : четыре 4. Двойная связь является сочетанием... Ответ 1 : двух σ-связей Ответ 2 : двух π-связей Ответ 3 : одной σ-связи и одной π-связи Ответ 4 : ионной связи и ковалентной связи 5. Какова гибридизация атомов углерода в молекуле алкена: Ответ 1 : 1 и 4 – sp2, 2 и 3 – sp3 Ответ 2 : 1 и 4 – sp3, 2 и 3 – sp2 Ответ 3 : 1 и 4 – sp3, 2 и 3 – sp Ответ 4 : 1 и 4 – не гибридизованы, 2 и 3 – sp2
Слайд 25
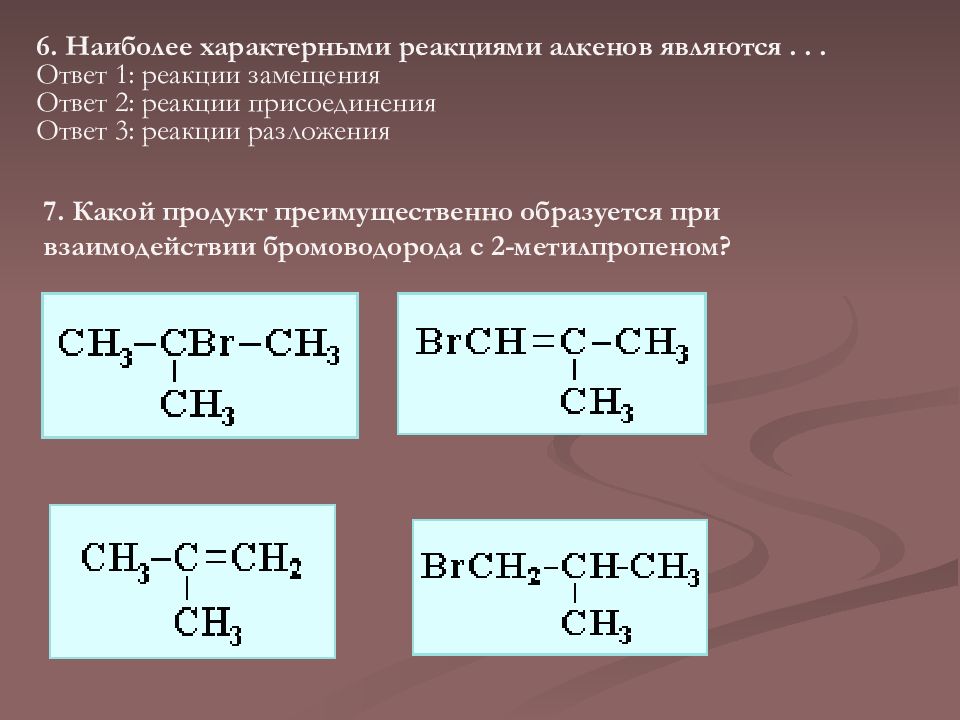
6. Наиболее характерными реакциями алкенов являются... Ответ 1 : реакции замещения Ответ 2 : реакции присоединения Ответ 3 : реакции разложения 7. Какой продукт преимущественно образуется при взаимодействии бромоводорода с 2-метилпропеном?
Слайд 26
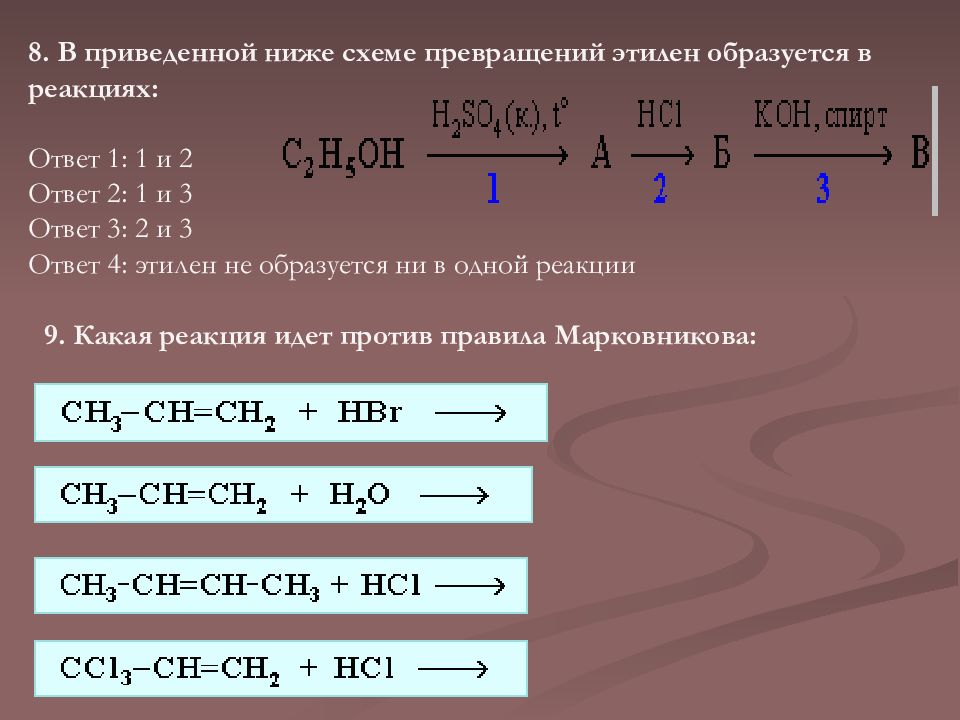
8. В приведенной ниже схеме превращений этилен образуется в реакциях: Ответ 1 : 1 и 2 Ответ 2 : 1 и 3 Ответ 3 : 2 и 3 Ответ 4 : этилен не образуется ни в одной реакции 9. Какая реакция идет против правила Марковникова:
Последний слайд презентации: Алкены: Кроссворд АЛКEНЫ для учащихся 10–11 классов
1. Буква греческого алфавита, которой обозначают более прочную связь, образующуюся при перекрывании атомных орбиталей вдоль оси, соединяющей центры атомов. 2. Бесцветный газ, немного легче воздуха, почти не имеющий запаха, плохо растворим в воде, простейший алкен. В смеси с кислородом используется в медицине для общего наркоза при хирургических операциях. 3. Предельный углеводород – бесцветная жидкость, нерастворимая в воде. 4. Название химического процесса соединения одинаковых молекул в более крупные молекулы с большой молекулярной массой. 5. Термин для обозначения химической связи в молекуле этилена. 6. Один из переводов греческого слова makros, от которого произошел термин «макромолекула».