Первый слайд презентации: Периодическая система Д.И. Менделеева
8 класс учитель Серегина Е.Н.
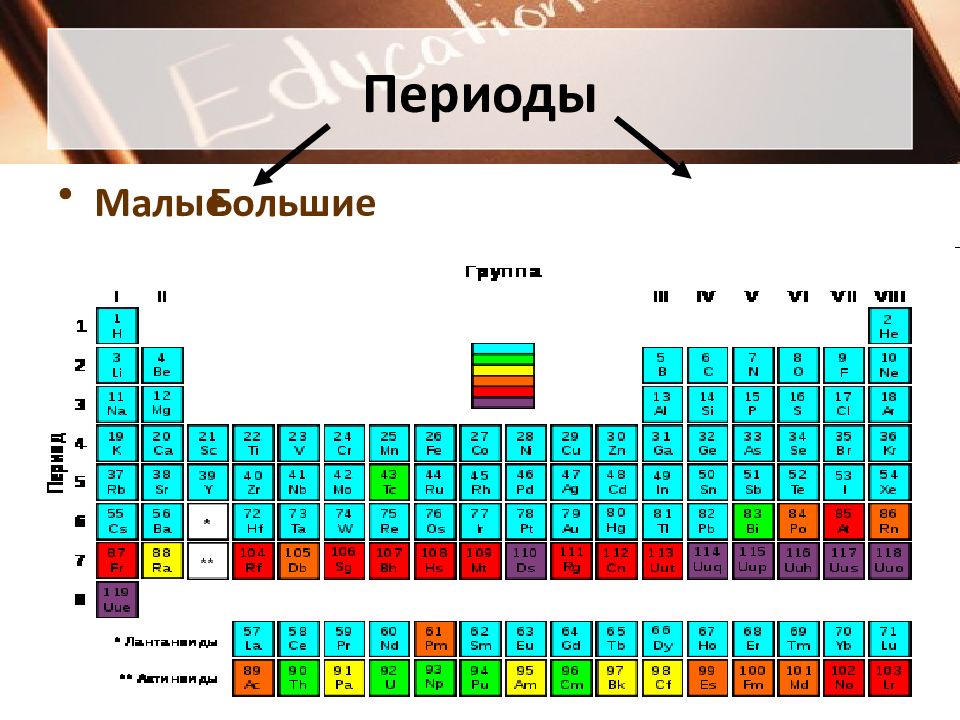
Слайд 4: Период
Горизонтальный ряд элементов, расположенных в порядке возрастания заряда ядра их атомов Номер периода показывает число занятых электронами энергетических уровней Каждый период начинается элементом, атомы которого образуют активные металлы и заканчивается элементом, атомы которого образуют благородные газы
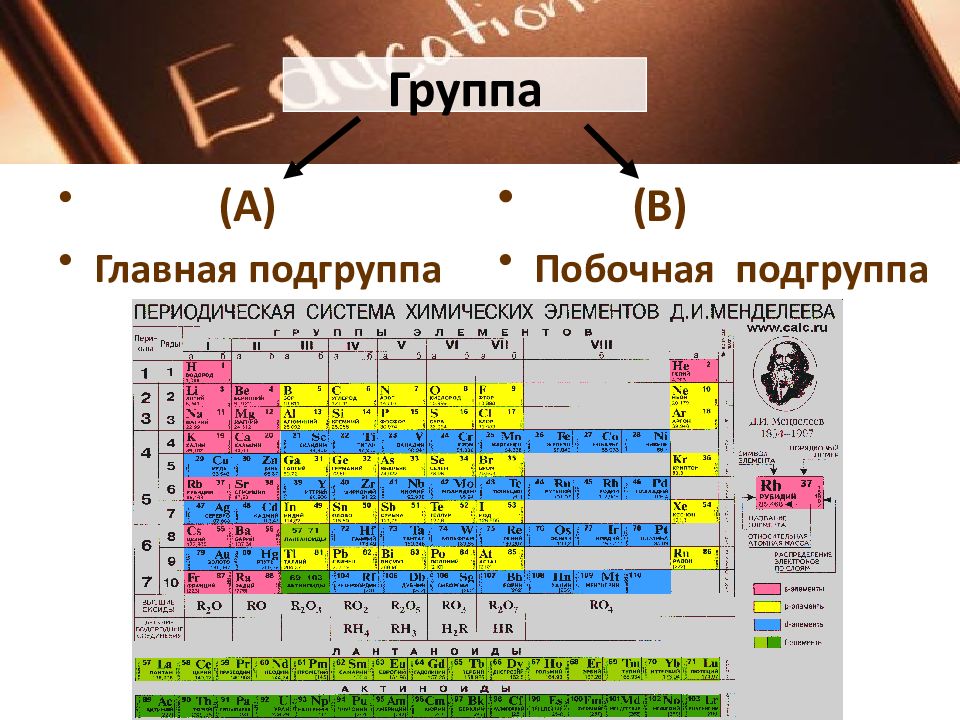
Слайд 7: Группы
Это вертикальный столбец элементов, атомы которых имеют одинаковое количество валентных электронов. Номер группы показывает число валентных электронов в атомах О 2е, 6е ; S 2e,8e, 6e 8 32
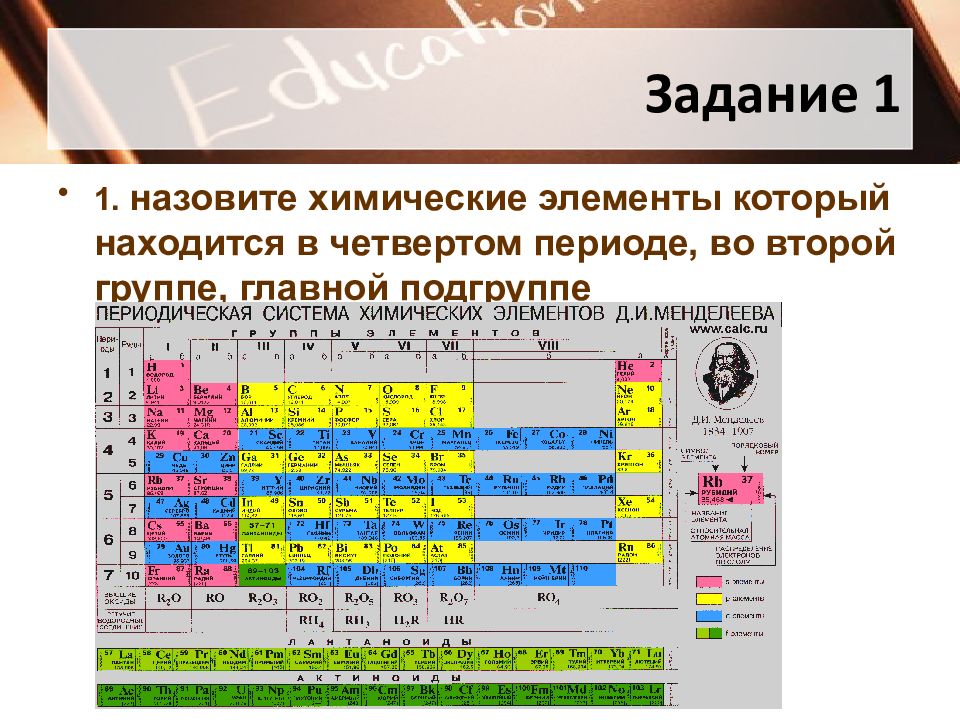
Слайд 9: Задание 1
1. назовите химические элементы который находится в четвертом периоде, во второй группе, главной подгруппе
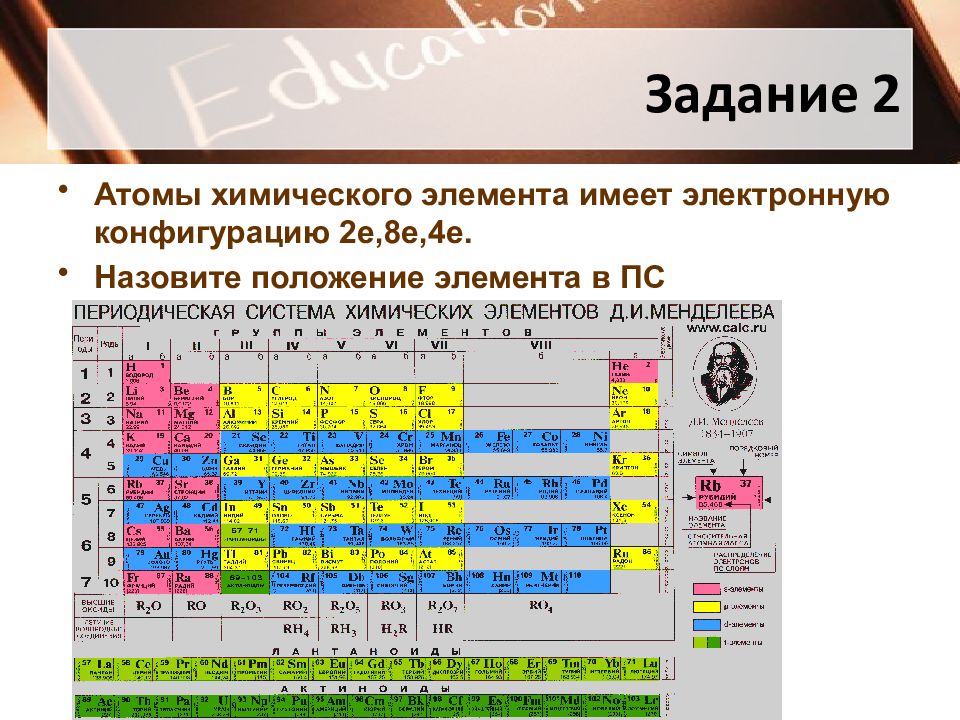
Слайд 10: Задание 2
Атомы химического элемента имеет электронную конфигурацию 2е,8е,4е. Назовите положение элемента в ПС
Слайд 11: Задание 3
Охарактеризуйте элемент № 16 Положение в ПС Строение атома Схема строения атома
Слайд 12
Как изменяются свойства атомов химических элементов в группах и в периодах Периодической системы?
Слайд 14
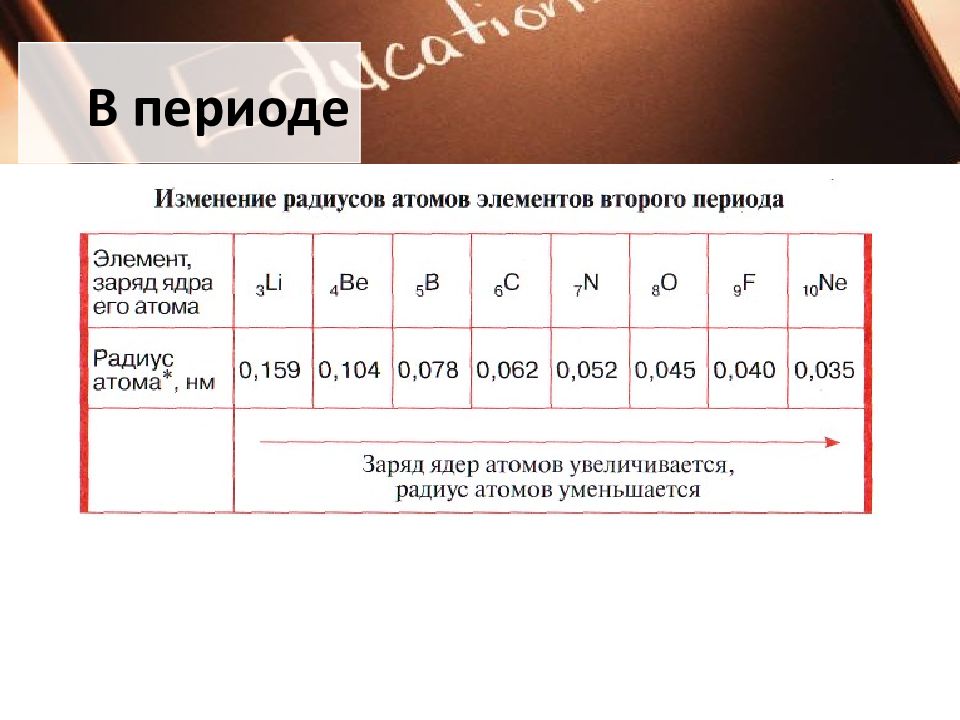
В периодах слева направо: Заряд ядер атомов увеличивается; число занятых электронами энергетических уровней в атомах не изменяется; число электронов на внешнем энергетическом уровне атомов (валентных) увеличивается от 1 до 8; радиус атомов уменьшается; прочность связи электронов внешнего уровня (валент ных) с ядром увеличивается ; металлические свойства атомов элементов убывают ; неметаллические свойства атомов элементов усиливаются. Начало каждого периода совпадает с началом заполнения нового электронного слоя. Каждый период начинается элементом, атомы которого образуют вещество — металл, а заканчивается элементом, атомы которого образуют вещество — благородный газ. В периоде
Слайд 16: В группе (А)
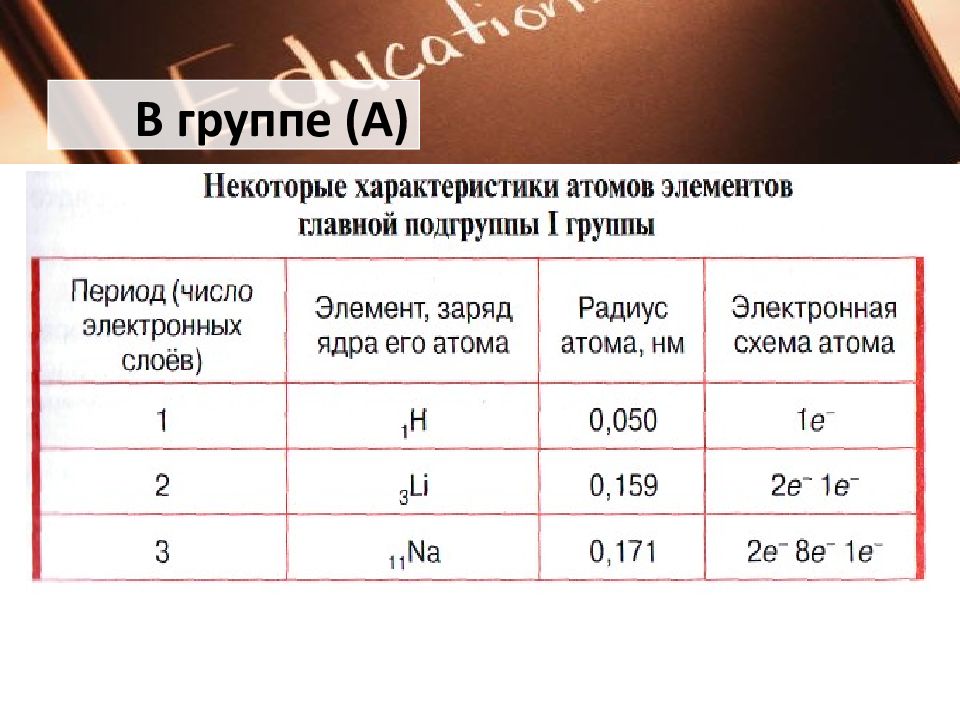
В главных подгруппах сверху вниз: заряд ядер атомов возрастает; число занятых электронами энергетических уровней увеличивается; радиус атомов растёт; число электронов на внешнем уровне не изменяется, оно равно номеру группы; 5. прочность связи электронов внешнего уровня с ядром уменьшается ; 6. металлические свойства атомов элементов усиливаются ; 7. неметаллические свойства атомов элементов ослабевают. В группе (А)
Слайд 17
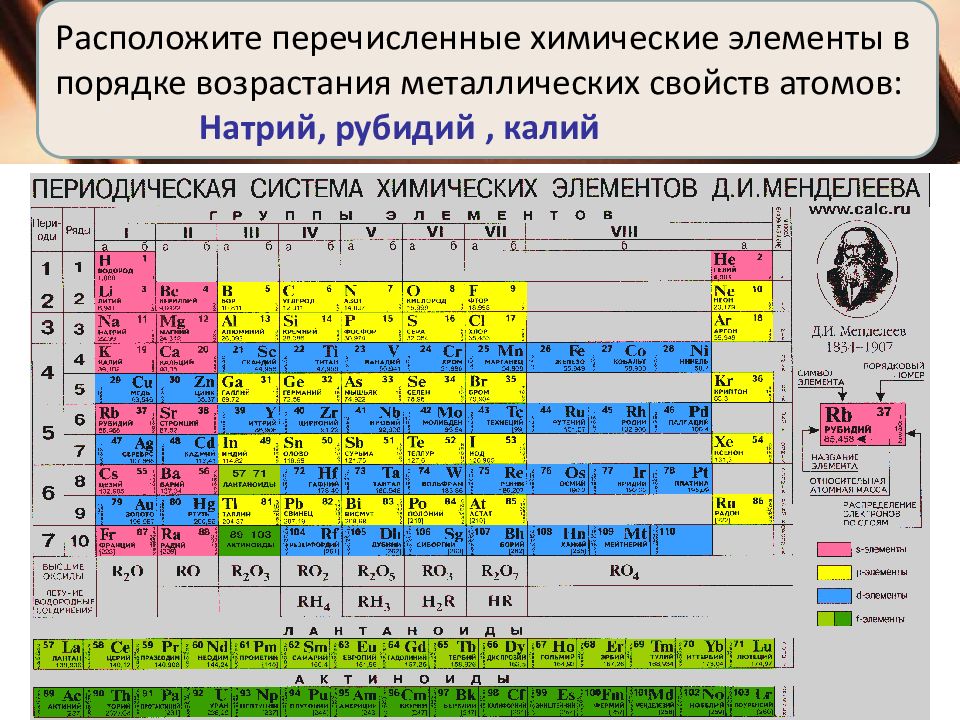
Расположите перечисленные химические элементы в порядке возрастания металлических свойств атомов: Натрий, рубидий, калий
Слайд 18
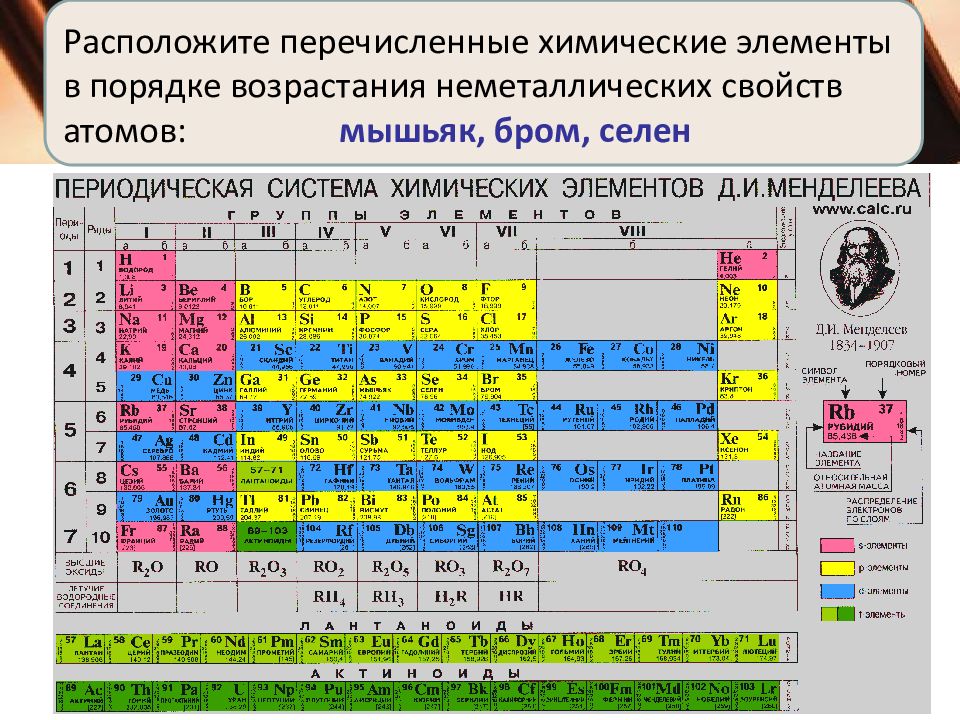
Расположите перечисленные химические элементы в порядке возрастания неметаллических свойств атомов: мышьяк, бром, селен