Слайд 2
РАСТВОР – гомогенная (однородная) система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия Растворитель – вещество, агрегатное состояние которого не изменяется при образовании раствора Растворенное вещество – вещество, агрегатное состояние которого изменяется при образовании раствора
Слайд 3
по количеству растворенного вещества ненасыщенные насыщенные пересыщенные Раствор, находящийся в равновесии с растворяющимся веществом Раствор, в котором содержание растворенного вещества значительно превышает содержание растворителя Раствор, в котором содержание растворенного вещества значительно меньше содержания растворителя
Слайд 4: ОПЕРАЦИИ, ПРОИЗВОДИМЫЕ С РАСТВОРАМИ
ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ РАСТВОРА ПРИГОТОВЛЕНИЕ РАСТВОРА РАЗБАВЛЕНИЕ РАСТВОРА КОНЦЕНТРИРОВАНИЕ РАСТВОРА СМЕШИВАНИЕ РАСТВОРОВ
Слайд 5: ХАРАКТЕРИСТИКА РАСТВОРА
КАЧЕСТВЕННАЯ (ИЗ КАКИХ ВЕЩЕСТВ СОСТОИТ РАСТВОР) КОЛИЧЕСТВЕННАЯ (СКОЛЬКО? В КАКОМ СООТНОШЕНИИ?)
Слайд 6: МАССОВАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА
Отношение массы растворенного вещества к общей массе раствора Выражают в долях или процентах ω = m в- ва m р-ра m р- ра = m в- ва + m р-ля.
Слайд 7: МОЛЯРНАЯ КОНЦЕНТРАЦИЯ
ПОКАЗЫВАЕТ КОЛИЧЕСТВО ВЕЩЕСТВА, СОДЕРЖАЩЕГОСЯ В 1 ЛИТРЕ РАСТВОРА Выражается в [ моль / л ] С = V р-ра n
Слайд 9
Задача № 1 Какую массу ортофосфата калия и воды необходимо взять для приготовления 250 граммов раствора с массовой долей ортофосфата калия 15 % ? Дано: ω ( K 3 PO 4 ) = 15 % =0,15 m р - ра = 250 гр Найти: m ( K 3 PO 4 ) = ? m ( H 2 O) = ? Решение: ω = m р.в m р-ра m р-ра = m р.в + m р-ля Вычисление: m р.в. = 0,15 * 250 гр = 37,5 гр m воды = 250 – 37,5 = 212,5 гр
Слайд 10
Задача № 2 В бензоле объемом 176 мл растворили 18 гр серы. Определите массовую долю серы в полученном растворе (плотность бензола 0,8 г/мл). Задача № 3 Определите массу воды и формальдегида, необходимых для приготовления 40 г 40 % - ого раствора формалина. Задача № 4 Смешали 200 г 10 % - o го раствора и 350 г 15 % - ого раствора. Определите массовую долю полученного раствора. Задача № 5 К 350 г 25 % - ого раствора добавили 50 г воды. Определите массовую долю полученного раствора. Задача № 6 Определите молярную концентрацию раствора гидроксида натрия, в 2 – х литрах которого содержится 10 г NaOH
Слайд 11
Домашнее задание: Сколько граммов соли нужно добавить к 250 г 4 % раствора, чтобы раствор стал 10 % ? 2. Какова молярная концентрация 40 % раствора гидроксида натрия, если его плотность 1,43 г/мл?
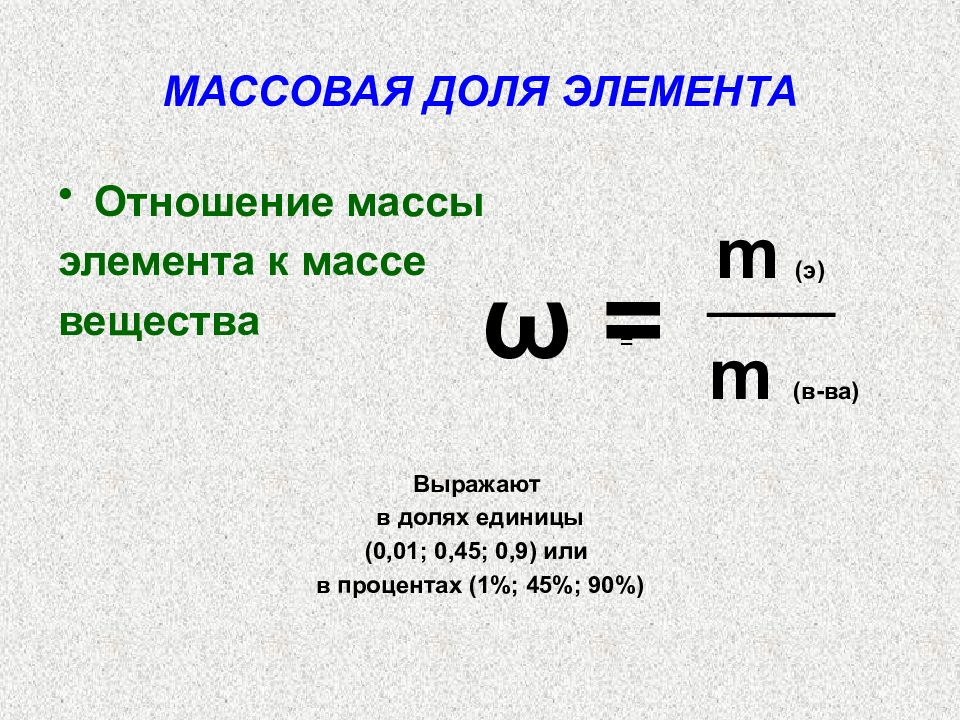
Слайд 12: МАССОВАЯ ДОЛЯ ЭЛЕМЕНТА
Отношение массы элемента к массе вещества Выражают в долях единицы (0,01; 0,45; 0,9) или в процентах (1 % ; 45 % ; 90 % ) ω = = m ( э) m ( в-ва)