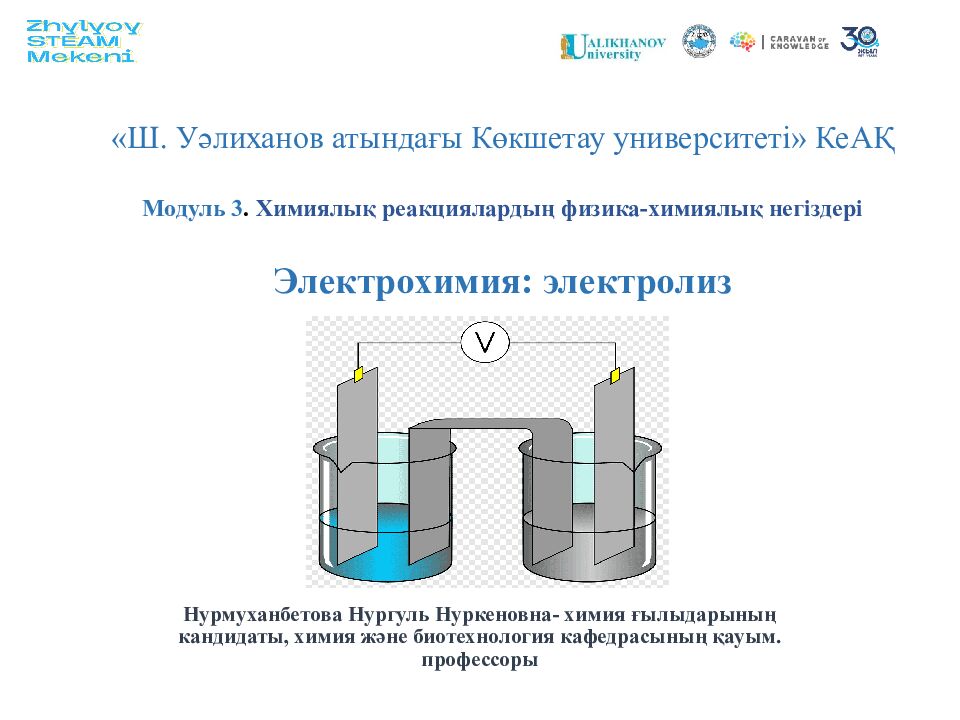
Первый слайд презентации: Ш. Уәлиханов атындағы Көкшетау университеті » КеАҚ Модуль 3. Химиялық реакциялардың физика-химиялық негіздері Электрохимия: электролиз
Нурмуханбетова Нургуль Нуркеновна- химия ғылыдарының кандидаты, химия және биотехнология кафедрасының қауым. профессоры
Слайд 2: Дәріс жоспары :
1. Электролиз : н егізгі түсініктер, механизм 2. Электродтардағы иондардың разрядтану ережелері; 3. Сандық есептер шығару;
Слайд 3
ЭЛЕКТРОХИМИЯЛЫҚ ПРОЦЕСТЕР Ехим Еэлектр (ГАЛЬВАНИКАЛЫҚ ЭЛЕМЕНТТЕР) Нернст теңдуін қолдануға негізделген Еэлектр Ехим (ЭЛЕКТРОЛИЗ) Фарадей заңын қолдануға негізделген
Слайд 5
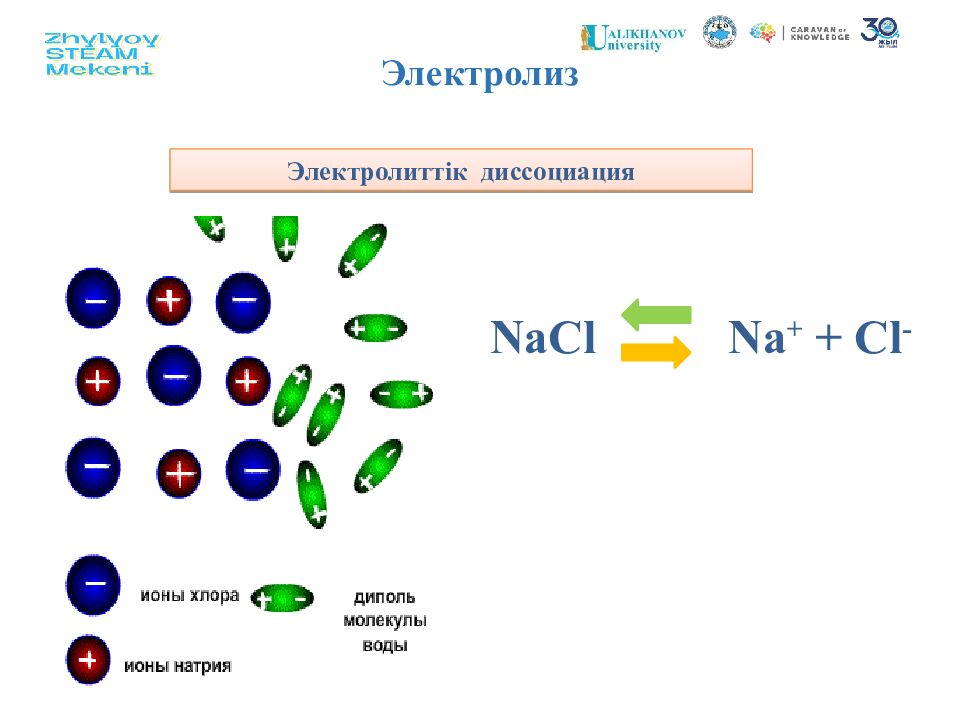
Na Cl Na + Cl - Ас тұзының электролиттік диссоциациясы NaCl Na + + Cl - Диссоциация других веществ: CuSO 4 Cu 2+ + SO 4 2- HCl H + + Cl - H 2 SO 4 H + + H + + SO 4 2- CaCl 2 Ca 2+ + Cl - + Cl - Диссоциация кезінде металл және сутек иондары үнемі оң зарядталады, ал қышқыл қалдықтары радикалдары мен ОН тобы - теріс зарядталады
Слайд 6
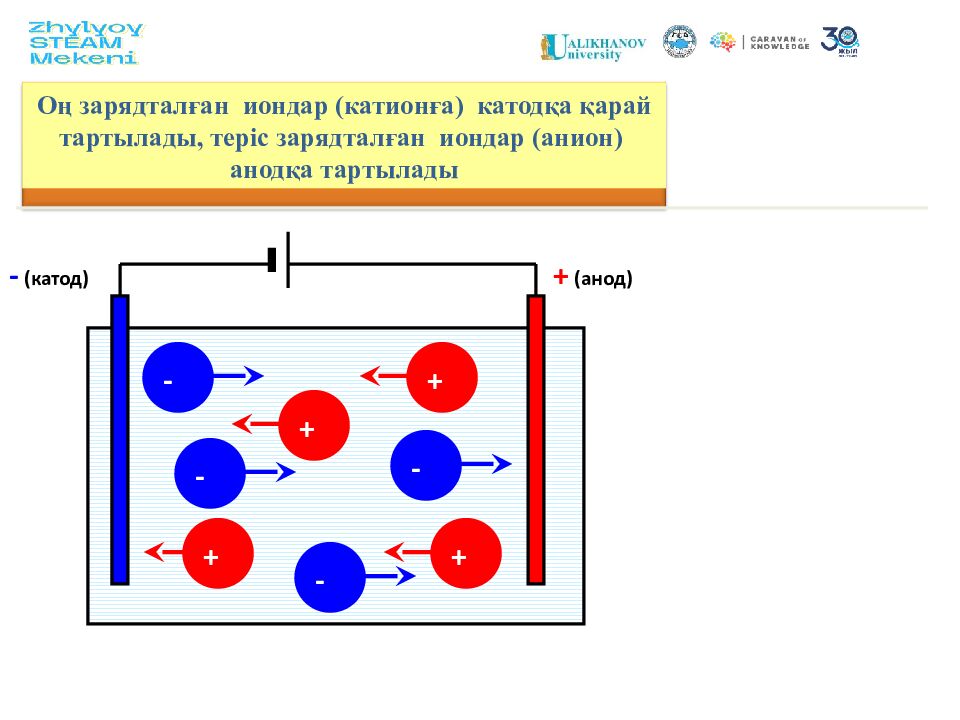
Оң зарядталған иондар ( катионға ) катодқа қарай тартылады, теріс зарядталған иондар (анион) анодқа тартылады + (анод) - (катод) + + + - - - + -
Слайд 7: Электролиз
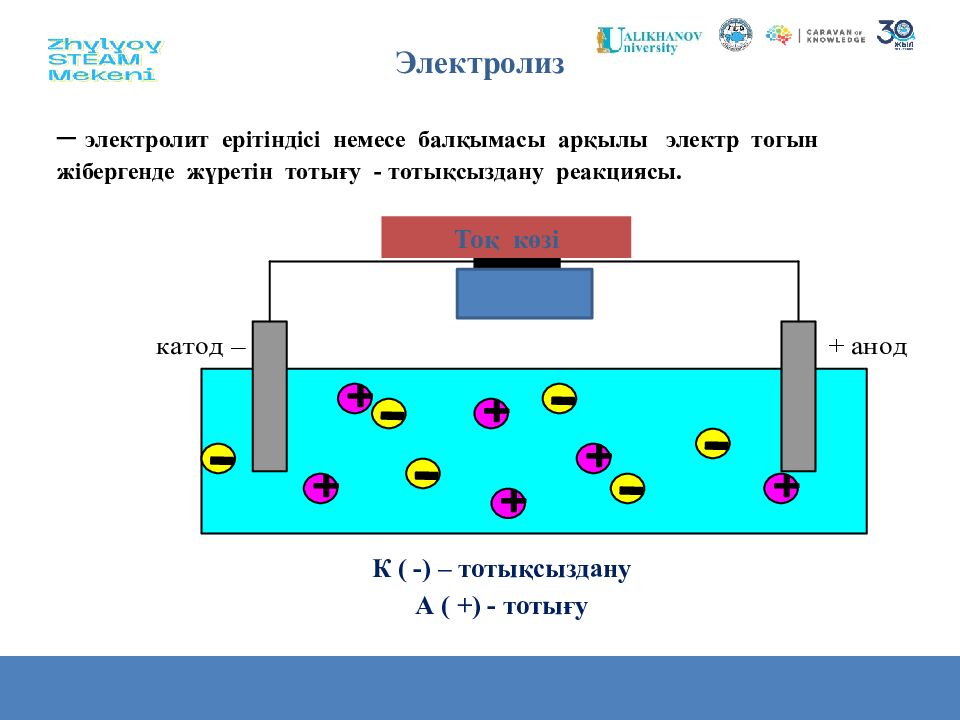
– э лектролит ерітіндісі немесе балқымасы арқылы электр тогын жібергенде жүретін тотығу - тоты қсыздану реакциясы. То қ көзі К ( -) – тотықсыздану А ( +) - тотығу
Слайд 8: Балқыма электролизі
t 0 NaCI ↔ Na + + CI - K (-) (Na ) Na + + e → Na 0 ттғш - тотықсыздану A (+) (CI ) 2 CI - -2 e → CI 2 0 ттсғш – тотығу 2 NaCI ↔ 2 Na + CI 2
Слайд 9: Катодтық үдерістер
1)Егер, сутектен кейін тұрған металл иондары мен сутек иондары бәсекелес болса, онда металл иондары бірінші тотықсызданады - Me n+ + ne - → Me 0 2) Li -ден АІ-ге дейін орналасқан металл иондары мен су молекулалары бәсекелес болса, онда су молекулалары бірінші тотықсызданады - 2H 2 O + 2e - → H 2 0 ↑+ 2OH - 3)Егер АІ-ден сутеккке дейін орналасқан металл иондары мен су молекулалары бәсекелес болса, онда катодта екеуі қатар тотықсызданады – Me n + + ne - → Me 0 2H 2 O + 2e - → H 2 0 ↑+ 2OH -
Слайд 10: Анодтық үдерістер
Анодқа қышқыл қалдығы мен су молекулалары не оның иондары келеді. Аниондар Оттексіз аниондар : 2 Hal - -2e - → Cl 0 2 ↑ Оттект і аниондар : 2 H 2 O - 4e - → О 2 0 ↑ + 4H + 4ОН - - 4 e - → О 2 0 ↑ + 2Н 2 О Анодта тотығу мына ретпен жүреді. S 2-, I -, Br -, CI -, OH-, SO 4 2-, NO 3 -, CO 3 2-, PO 4 3-, MnO 4 -, F -
Слайд 11: Тұз ерітіндісінің электролизі
NaCI → Na + + CI - (-) K (Na +, H 2 O) 2H 2 O + 2e → H 2 + 2OH - тотықсыздану (+) A ( CI -, H 2 O) 2CI - - 2e → CI 2 тотығу Жалпы реакция теңдеуі: 2 NaCI + 2H 2 O = CI 2 ↑ + H 2 ↑ + 2NaOH
Слайд 12
ЭЛЕКТРОЛИЗДІҢ ҚОЛДАНЫЛУЫ Химиялық таза заттар алу үшін Гальваностегия Гальванопластика
Слайд 13: Гальваностегия
Бұйымды коррозиядан қорғап, ұзақ бойы қолдану үшін асыл металдан жасалған қорғаныш ( жұқа қабықпен ) қабықпен қаптайды. Гальваникалық цехтар көптеген металлургиялық және басқа зауыттарда бар.
Слайд 14
Күміс нитратының сулы ерітіндісінің электролизі кезінде анодта 6 г оттек газы бөлінетін болса, катодта бөлінген күмістің массасын есептеңдер.
Слайд 15
Зауытта массасы 468 кг натрий хлорид інің ерітіндісін электролизге ұшыратты. Алынған газдар хлорсутектің синтезі үшін қолданылады. Алынған хлорсутек газын 708 л суда ерітті. Алынған ерітіндідегі тұз қышқылының массалық үлесін есептеңдер.
Слайд 16
Жатты ғу Сулы ерітінділер электролизында инертті электродтарды қолданған кезде анодта бөлінетін өнім мен электролизге ұшырайтын заттың арасындағы сәйкестікті көрсетіңіз: Заттың формуласы Анодтағы өнімдер А) NaCl 1) Cl 2 B) NaClO 4 2) Cl 2, O 2 C) NaOH 3) O 2 D) NaBr 4) H 2, Br 2 5) O 2, Br 2 6) Br 2
Слайд 17
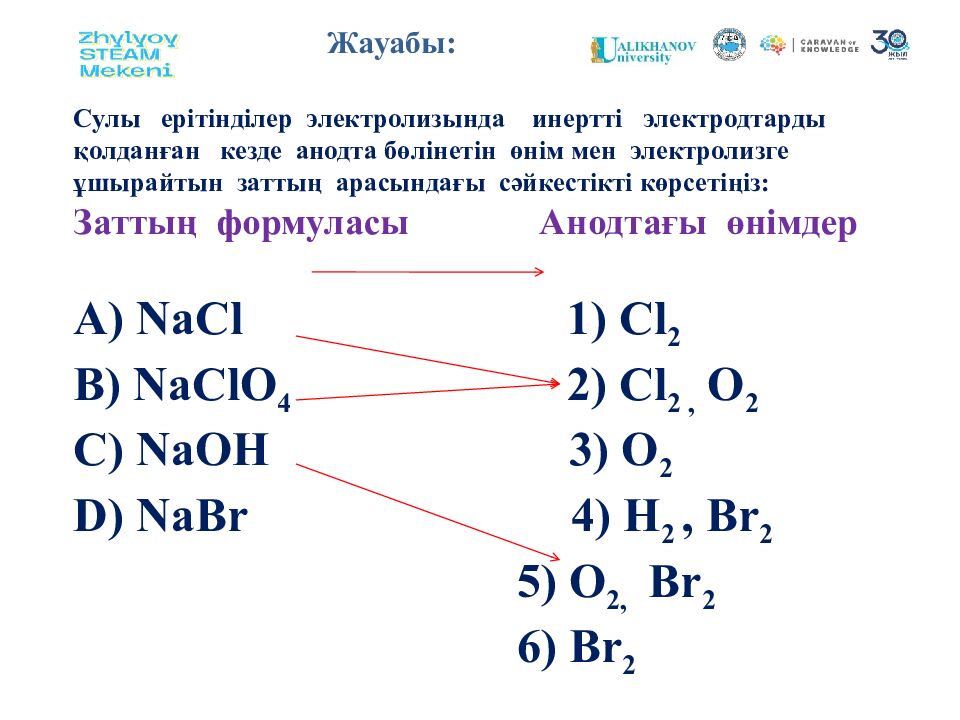
Жа уабы: Сулы ерітінділер электролизында инертті электродтарды қолданған кезде анодта бөлінетін өнім мен электролизге ұшырайтын заттың арасындағы сәйкестікті көрсетіңіз: Заттың формуласы Анодтағы өнімдер А) NaCl 1) Cl 2 B) NaClO 4 2) Cl 2, O 2 C) NaOH 3) O 2 D) NaBr 4) H 2, Br 2 5) O 2, Br 2 6) Br 2
Слайд 18
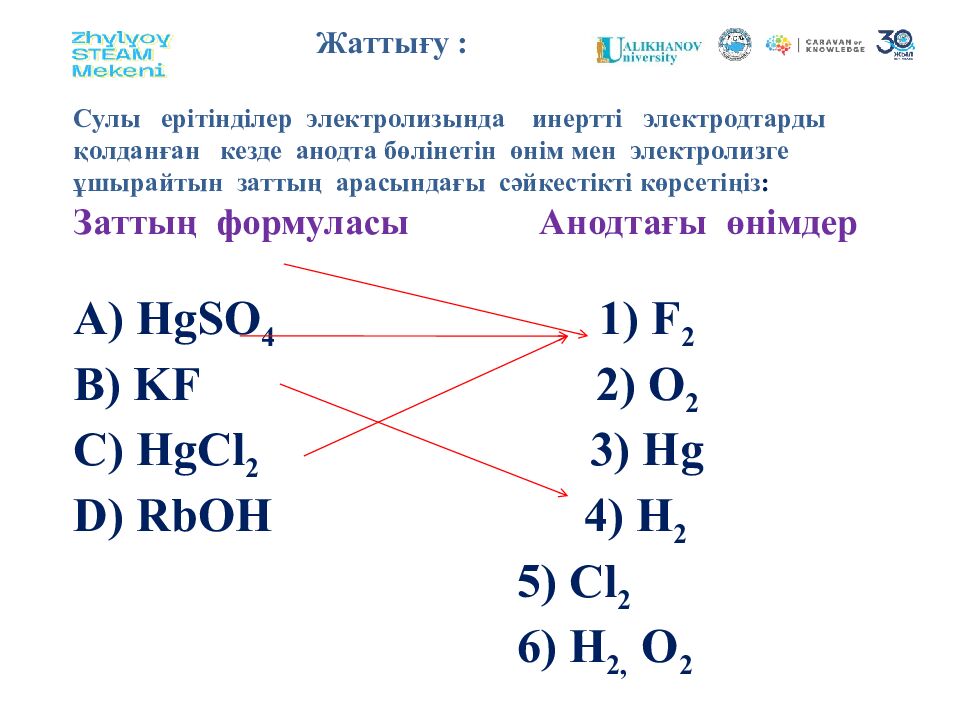
Жа ттығу : Сулы ерітінділер электролизында инертті электродтарды қолданған кезде анодта бөлінетін өнім мен электролизге ұшырайтын заттың арасындағы сәйкестікті көрсетіңіз: Заттың формуласы Анодтағы өнімдер А) HgSO 4 1) F 2 B) KF 2) O 2 C) HgCl 2 3) Hg D) RbOH 4) H 2 5) Cl 2 6) H 2, O 2
Слайд 19
Жа ттығу : Сулы ерітінділер электролизында инертті электродтарды қолданған кезде анодта бөлінетін өнім мен электролизге ұшырайтын заттың арасындағы сәйкестікті көрсетіңіз : Заттың формуласы Анодтағы өнімдер А) HgSO 4 1) F 2 B) KF 2) O 2 C) HgCl 2 3) Hg D) RbOH 4) H 2 5) Cl 2 6) H 2, O 2
Слайд 20: Үй тапсырмасы
1. Кальций хлориді балқымасының электролизі теңдеуін жазып, катод пен анодта бөлінетін өнімдерді көрсетіңіз. 2. Темірдің (ІІ) хлориді ерітіндісінің электролизі теңдеуін жазып, катод пен анодта бөлінетін өнімдерді көрсетіңіз. 3. Электронды баланс әдісін қолданып реакция теңдеуін аяқтаңыз. Есеп Күміс нитратының электролит ерітіндісі арқылы 30 минут уақыт бойы 6 A тоқ күшін жұмсаған кезде ерітіндіден бөлініп шыққан металл күмістің массасын анықтаңыз.
Слайд 21: Есептер
Ерімейтін анод алынып күміс нитратының сулы ерітіндісінің электролизі 25 минут бойы 3А ток күшімен жүрді. Токтың шығымы 95% екендігі белгілі болса, катодта күмістің қандай массасы бөлінеді ? 500 г ерітіндіде мыс (ІІ) және күміс нитраттарының 12,8 г қоспасы ерітілген. Ерітіндіні толық электролиздегенде катодта бөлінген металдардың массаларының қосындысы 5,34 г болған. Бастапқы берілген ерітіндідегі нитраттардың әрқайсысының массалық үлестерін анықтаңдар. Зауытта массасы 468 кг натрий хлоридінің ерітіндісін электролизге ұшыратты. Алынған газдар хлорсутектің синтезі үшін қолданылады. Алынған хлорсутек газын 708 л суда ерітті. Алынған ерітіндідегі тұз қышқылының массалық үлесін есептеңдер.
Последний слайд презентации: Ш. Уәлиханов атындағы Көкшетау университеті » КеАҚ Модуль 3. Химиялық: Т апсырма
1. Темір (Ш) хлориді ерітіндісі мен балқымасының электролизі теңдеуін жазып, катод пен анодта бөлінетін өнімдерді көрсетіңіз. 2. Мыс (ІІ) нитраты балқымасы мен ерітіндісінің электролизі теңдеуін жазып, катод пен анодта бөлінетін өнімдерді көрсетіңіз. 3. Электронды баланс әдісін қолданып реакция теңдеуін аяқтаңыз. Есеп Күміс нитратының электролит ерітіндісі арқылы 30 минут уақыт бойы 6 A тоқ күшін жұмсаған кезде ерітіндіден бөлініп шыққан металл күмістің массасын анықтаңыз.