Первый слайд презентации: Способы получения полимеров
Слайд 2
Способы получения полимеров Синтез полимеров из мономеров основан на реакциях двух типов: полимеризации и поликонденсации. Пoлимеризация цепная реакция образования высокомолекулярных соединений путем последовательного присоединения молекул мономера к растущей цепи. Поликонденсация процесс образования полимеров взаимодействием би - или полифункциональных мономеров и (или) олигомеров, сопровождающийся выделением низкомолекулярного продукта (воды, спирта, NH 3, галогеноводорода, соответствующих солей и др.).
Слайд 3: Полимеризация
Характерные признаки полимеризации 1. В основе полимеризации лежит реакция присоединения. 2. Полимеризация является цепным процессом, т.к. включает стадии свободно-радикального механизма: инициирования, роста и обрыва цепи. 3. Элементный состав мономера и c труктурного звена полимера одинаков.
Как всякая цепная реакция, полимеризация включает три типа элементарных реакций : инициирование цепи с образованием активного центра, рост цепи обрыв цепи
Слайд 5: Инициирование цепи
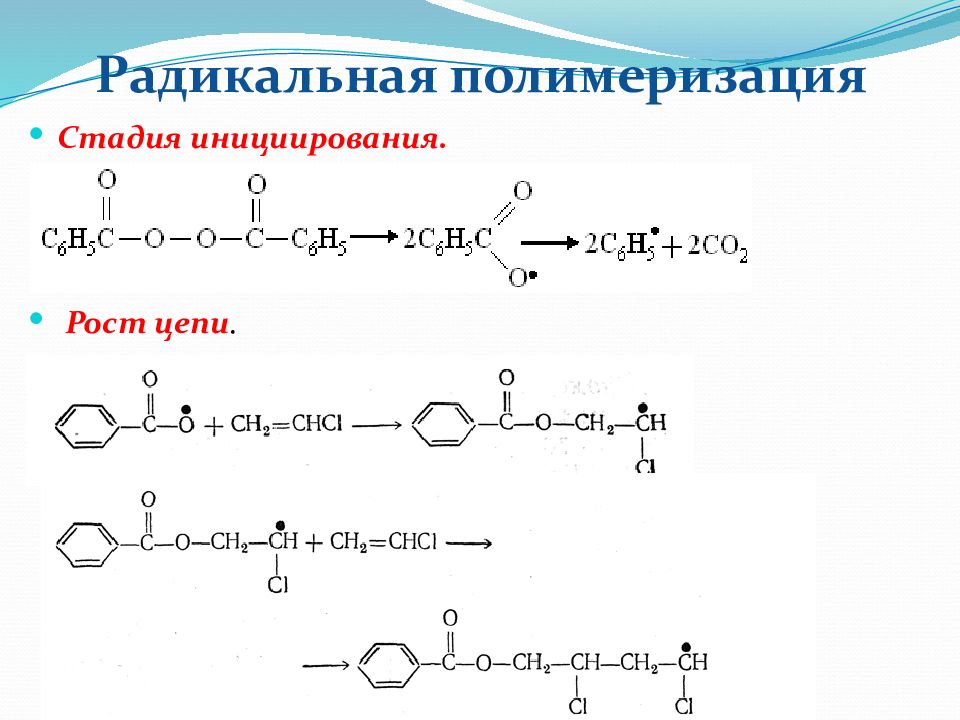
Радикальная полимеризация : гомолитический разрыв и образование радикала : Ионная полимеризация: гетеролитический разрыв и образование иона:
Слайд 6: Рост цепи
представляет собой многократное повторение актов присоединения молекул мономера к активному центру с образованием макромолекулы. Обрыв цепи происходит в результате взаимодействия двух радикалов путём их рекомбинации или диспропорционирования.
Слайд 8: Радикальная полимеризация
Обрыв цепи Насыщение свободных валентностей: Диспропорционирование :
Слайд 9: Ионная полимеризация
Катионная полимеризация протекает под влиянием сильных акцепторов электронов (минеральных кислот, галогенидов AlCl 3, BF 3, SnCl 4, FeCl 3 и т.д. ) В среде сокатализиторов (воды, эфиров, кислот и др.) может образоваться активный каталитический комплекс, инициирующий реакцию катионной полимеризации, например: Н 2 О + BF 3 → (BF 3 · OH) H +
Слайд 10: Карбкатион
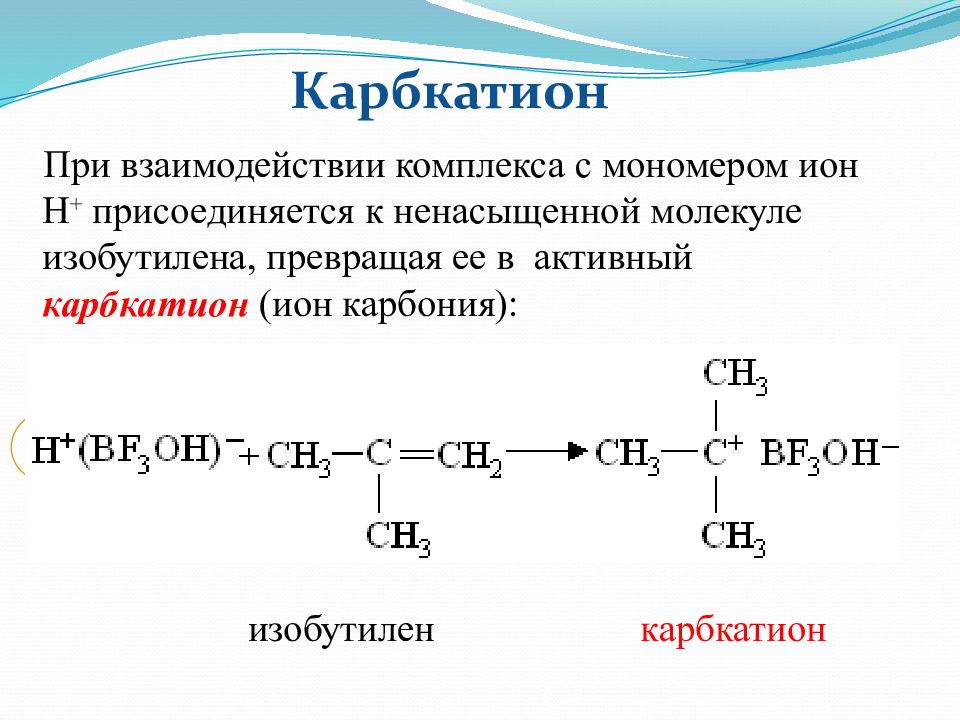
При взаимодействии комплекса с мономером ион Н + присоединяется к ненасыщенной молекуле изобутилена, превращая ее в активный карбкатион (ион карбония): изобутилен карбкатион Карбкатион
Слайд 11: Рост цепи
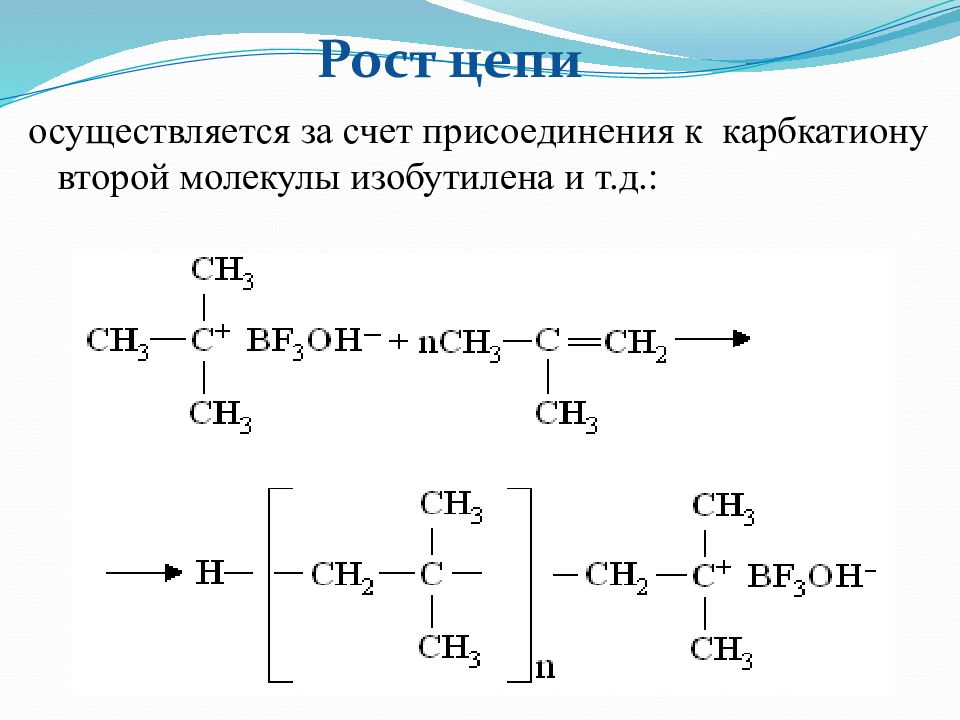
осуществляется за счет присоединения к карбкатиону второй молекулы изобутилена и т.д.: Рост цепи
Слайд 12: Обрыв цепи
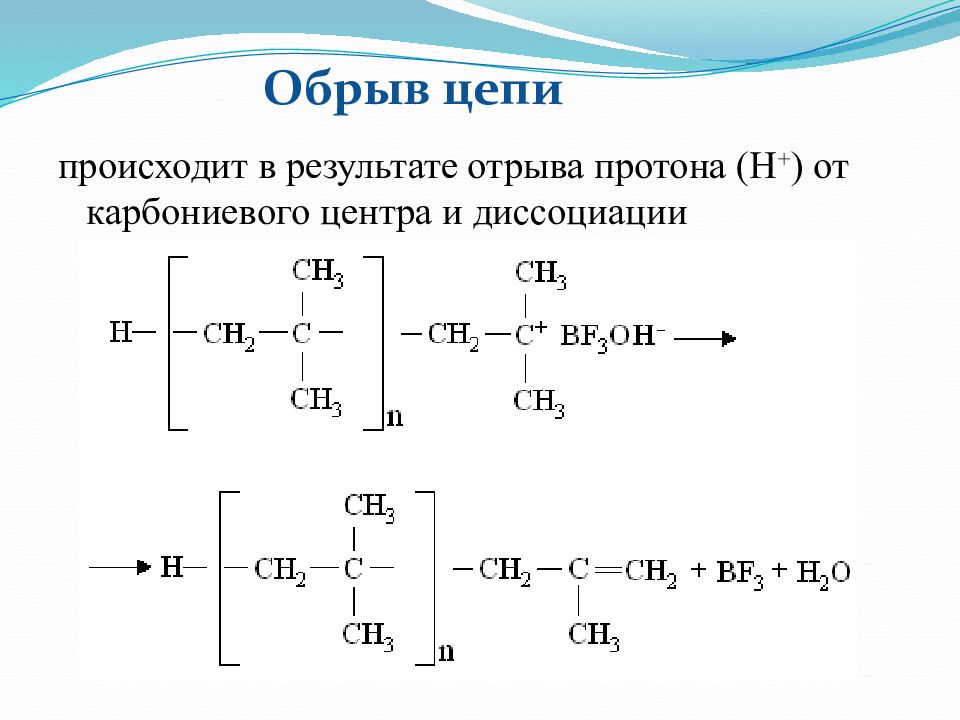
происходит в результате отрыва протона (Н + ) от карбониевого центра и диссоциации каталитического комплекса: Обрыв цепи
Слайд 13: Анионная полимеризация
протекает под влиянием щелочных металлов и их алкоголятов, металлоорганических соединений и других электронодонородных соединений. Например, амид калия полностью диссоциирует на ионы под воздействием жидкого аммиака: KNH 2 K + + NH 2 Анионная полимеризация
Слайд 14: Рост цепи
Амидный ион может взаимодействовать с молекулой мономера СН 2 = СН – CN (акрилонитрил), образуя активный карбанион : Рост цепи который затем вызывает рост цепи:
Слайд 15: Обрыв цепи
Может быть проведён аммиаком, т.к. при взаимодействии его с карбанином образуется амидный анион NH 2 . Получается реакция передачи цепи. Либо протонными кислотами:
Слайд 16: Особенность реакций катионной и анионной полимеризации
они могут протекать с огромной скоростью при очень низких температурах, приводя к образованию высокомолекулярного продукта. полимеризация под действием комбинированных катализаторов особого типа, например смеси алюминийалкилов и хлоридов титана или ванадия (катализаторы Циглера-Натта) во многих случаях приводит к образованию стереорегулярных полимеров.
Слайд 17: Сополимеризация
Процесс образования высокомолекулярных соединений при совместной полимеризации двух или более различных мономеров называют сополимеризацией. Пример. Схема сополимеризации этилена с пропиленом:
Слайд 19: Высокомолекулярные соединения, получаемые методом полимеризации
Полиэтилен Полипропилен Поливинилхлорид Политетрафторэтилен Полимеры производных акриловой и метакриловой кислот Каучук
Слайд 20
ХАРАКТЕРНЫЕ ПРИЗНАКИ РЕАКЦИИ ПОЛИКОНДЕНСАЦИИ В основе поликонденсации лежит реакция замещения. 2. Поликонденсация – процесс ступенчатый, т.к. образование макромолекул происходит в результате ряда реакций последовательного взаимодействия мономеров, димеров или n- меров как между собой, так и друг с другом. 3. Элементные составы исходных мономеров и полимера отличаются на группу атомов, выделившихся в виде низкомолекулярного продукта (H 2 O, спирта, NH 3 и т.п.). Поликонденсация является основным способом образования природных полимеров в естественных условиях. Поликонденсация
Слайд 21: Механизм поликонденсации
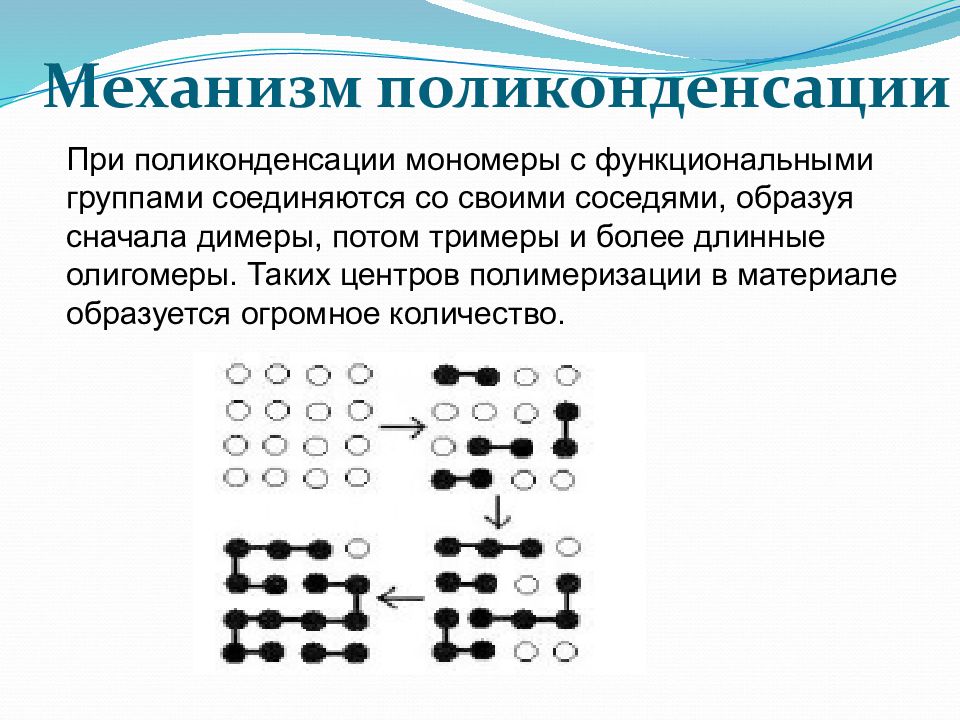
При поликонденсации мономеры с функциональными группами соединяются со своими соседями, образуя сначала димеры, потом тримеры и более длинные олигомеры. Таких центров полимеризации в материале образуется огромное количество. Механизм поликонденсации
Слайд 22: Механизм поликонденсации
При поликонденсации мономеры исчерпываются уже при невысоких степенях завершенности реакции. Рост цепи высокомолекулярного полимера происходит преимущественно в результате многократного взаимодействия между собой олигомерных или полимерных молекул по концевым функциональным группам (принцип многократного удвоения), при этом число молекул в системе уменьшается (в этом ступенчатый характер поликонденсации ). Механизм поликонденсации
Слайд 23: Мономеры, способные к поликонденсации
В поликонденсацию могут вступать соединения, содержащие не менее двух функциональных групп, способных к химическому взаимодействию. Например, соединение с двумя разнородными функциональными группами: аминокислоты H 2 N - R – COOH полиамиды; гидроксикислоты HO - R – COOH полиэфиры; Мономеры, способные к поликонденсации
Слайд 24: Мономеры, способные к поликонденсации
два соединения, каждое из которых содержит одинаковые функциональные группы, способные взаимодействовать с группами другой молекулы: двухатомные спирты и двухосновные (дикарбоновые) кислоты: HO-R-OH + HOOC-R`-COOH полиэфиры; диамины и двухосновные кислоты: H 2 N-R-NH 2 + HOOC-R`-COOH полиамиды. Мономеры, способные к поликонденсации
Последний слайд презентации: Способы получения полимеров: Названия полимеров
Назвать полимер можно если известно химическое строение его макромолекул. Для этого нужно: выделить структурное (мономерное) звено в макромолекуле; по строению этого звена определить, какой мономер использован для получения данного полимера; назвать полимер, добавив приставку "поли" перед названием мономера.