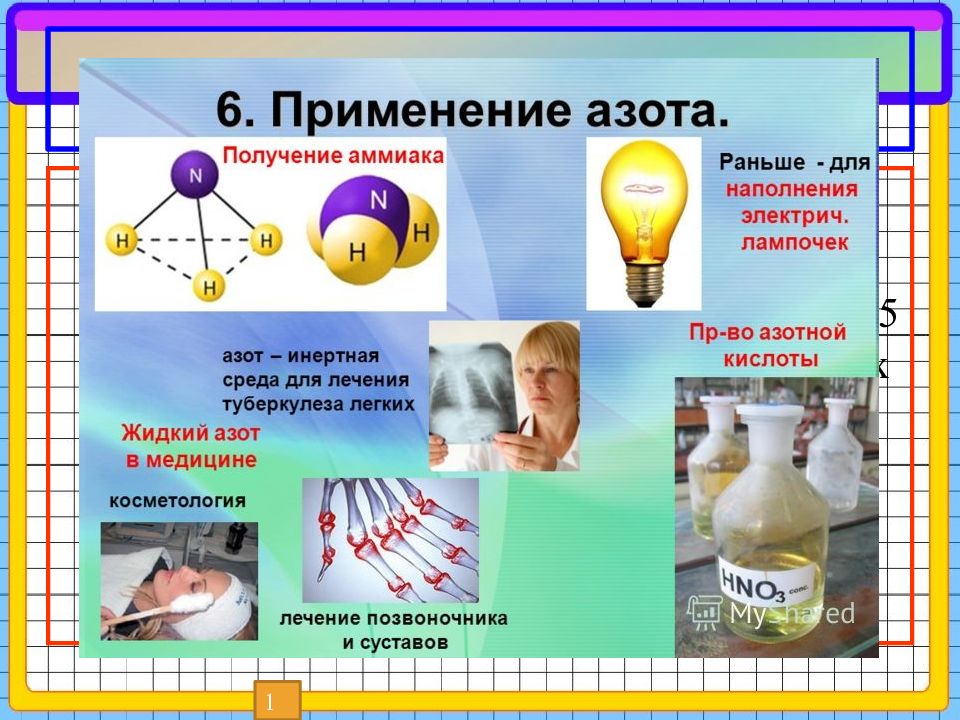
Первый слайд презентации: Внеклассное мероприятие
Сорокина Галина Ивановна ОГАПОУ СПО
Слайд 2: Своя игра Гордись лишь теми победами, какие ты одержал над самим собой. Вольфром
1 2
Слайд 3: Красный раунд
1 2 10 20 30 40 50 10 20 30 40 50 10 20 30 40 50 10 20 30 40 50 10 20 30 40 50 10 20 30 40 50 Химические элементы Галогены Металлы Оксиды Ученые Реакции
Слайд 4: Сектор «Химические элементы»
10 баллов. Этот химический элемент выделен в 1751 году шведским учёным Аксель Фредрик Кронштедтом в металлическом состоянии из никелевого колчедана. 1
Слайд 5: Сектор «Химические элементы»
20 баллов. Данный химический элемент выделен в виде оксида из минерала стронционита. В металлическом состоянии получен в 1808 году Гемфри Деви 1
Слайд 6: Сектор «Химические элементы»
30 баллов Этот химический элемент предсказан Д.И.Менделеевым под названием «экабор». В свободном виде получен в 1937 году В.Фишером 1
Слайд 7: Сектор «Химические элементы»
40 баллов Сплав этого металла и меди (бронза) изготовлялся ещё в третьем тысячелетии до н.э. 1
Слайд 8: Сектор «Химические элементы»
50 баллов Сплав этого металла с медью (латунь) известен с древних времён. В чистом виде, по-видимому, был получен впервые в XII веке. 1
Слайд 9: Сектор «Галогены»
10 баллов Что в переводе с греческого означает слово «галогены»? 1
Слайд 10: Сектор «Галогены»
20 баллов При обычных условиях этот галоген представляет собой газ жёлто-зелёного цвета 1
Слайд 11: Сектор «Галогены»
30 баллов Этот галоген при обычных условиях – тёмно-фиолетовое, почти чёрное кристаллическое вещество. 1
Слайд 12: Сектор «Галогены»
40 баллов При обычных условиях – это газ светло-зелёного цвета 1
Слайд 13: Сектор «Галогены»
50 баллов При обычных условиях этот галоген представляет собой жидкость красно-бурого цвета 1
Слайд 14: Сектор «Металлы»
10 баллов Этот щелочной металл по распространённости в земной коре занимает шестое место. Температурный интервал жидкого состояния достаточно велик, поэтому его используют в ядерной энергетике как теплоноситель. 1
Слайд 15: Сектор «Металлы»
20 баллов Название этого металла произошло от латинского слова, обозначающего утреннюю звезду. В природе он встречается в виде самородков. Это благородный металл жёлтого цвета, обладает высокой ковкостью. 1
Слайд 16: Сектор «Металлы»
30 баллов На некоторых древних языках этот металл именуется «небесным камнем». 1
Слайд 17: Сектор «Металлы»
40 баллов В 1854 г стоимость 1кг этого металла составляла 1200 рублей, т.е. он был в 270 раз дороже серебра, а в 1899г – 1 рубль. 1
Слайд 18: Сектор «Металлы»
50 баллов Он примечателен как всесторонне «нечётный» металл: №19, A r =39, 1 внешний электрон. 1
Слайд 19: Сектор «Оксиды»
10 баллов Летучая жидкость, которая «дымит» на воздухе. «Дым», или, точнее, туман, - это мельчайшие капельки серной кислоты, образовавшиеся при соединении паров этого оксида с присутствующим в воздухе водяным паром. 1
Слайд 20: Сектор «Оксиды»
20 баллов Твёрдое, очень тугоплавкое вещество. В природе встречается в виде включений в гранит и другие породы. Такие включения выглядят как кусочки сплавленного стекла. Освобождаясь при выветривании породы, они скапливаются в руслах рек в виде белого песка. 1
Слайд 21: Сектор «Оксиды»
30 баллов Тугоплавкое вещество, при смешивании с водой оно соединяется с ней с выделением такого большого количества теплоты, что вода закипает. Куски этого оксида, впитывая воду, разбухают и рассыпаются, превращаясь в рыхлый порошок. 1
Слайд 22: Сектор «Оксиды»
40 баллов Бесцветный газ с характерным резким запахом. Обесцвечивает многие органические краски, образуя с ними бесцветные соединения. Так окраска красной розы, опущенной в этот газ, пропадает. Она становится белой. Этот газ убивает микроорганизмы. Применяется для беления соломы, шёлка, шерсти. 1
Слайд 23: Сектор «Оксиды»
50 баллов Соединение чёрного цвета, применяется в стекольной промышленности, а также как окислитель в анализе органических соединений. 1
Слайд 24: Сектор «Учёные»
10 баллов Этот гениальный химик XIX века родился в Тобольске. В его биографии есть примечательный факт: в 1887 г. Он поднялся на аэростате выше облаков наблюдать солнечное затмение, а приземлился в другой губернии. Суеверные люди подумали, что снизошёл на землю Всевышний. 1
Слайд 25: Сектор «Учёные»
20 баллов Итальянский учёный. В 1811 году открыл закон о газах, позже названный его именем. 1
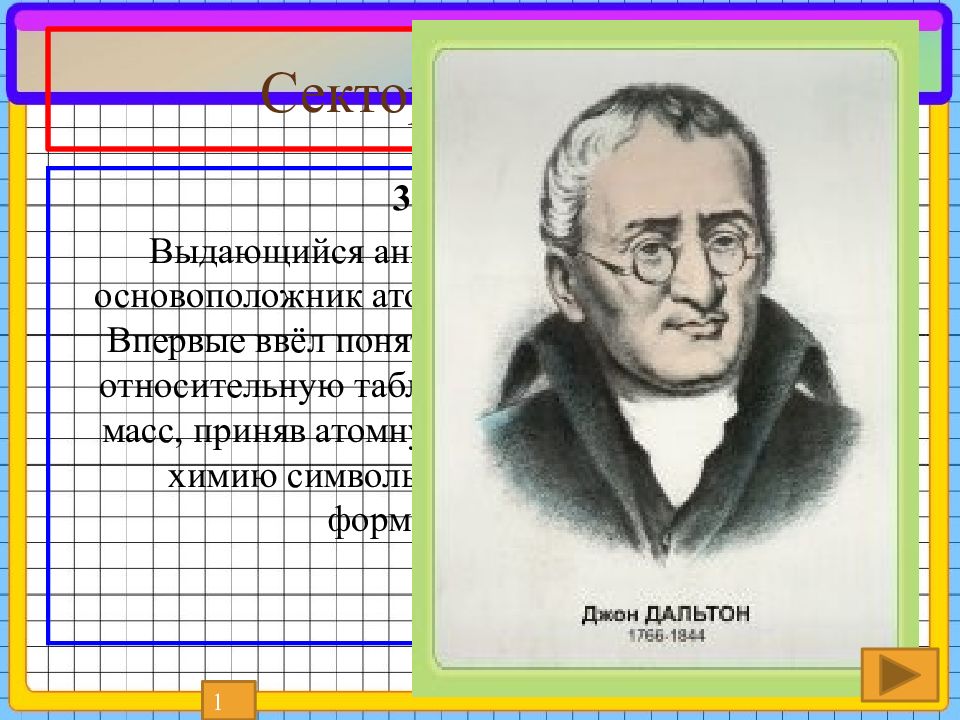
Слайд 26: Сектор «Учёные»
30 баллов Выдающийся английский химик и физик, основоположник атомных представлений в химии. Впервые ввёл понятие «атомный вес» и составил относительную таблицу атомных и молекулярных масс, приняв атомную массу водорода за 1; ввёл в химию символы химических элементов и формулы соединений 1
Слайд 27: Сектор «Учёные»
40 баллов Выдающийся французский химик, родившийся в Париже. Доказал сложность состава воздуха и воды. Правильно объяснил процессы горения, обжига металлов и дыхания участием в них кислорода. 1
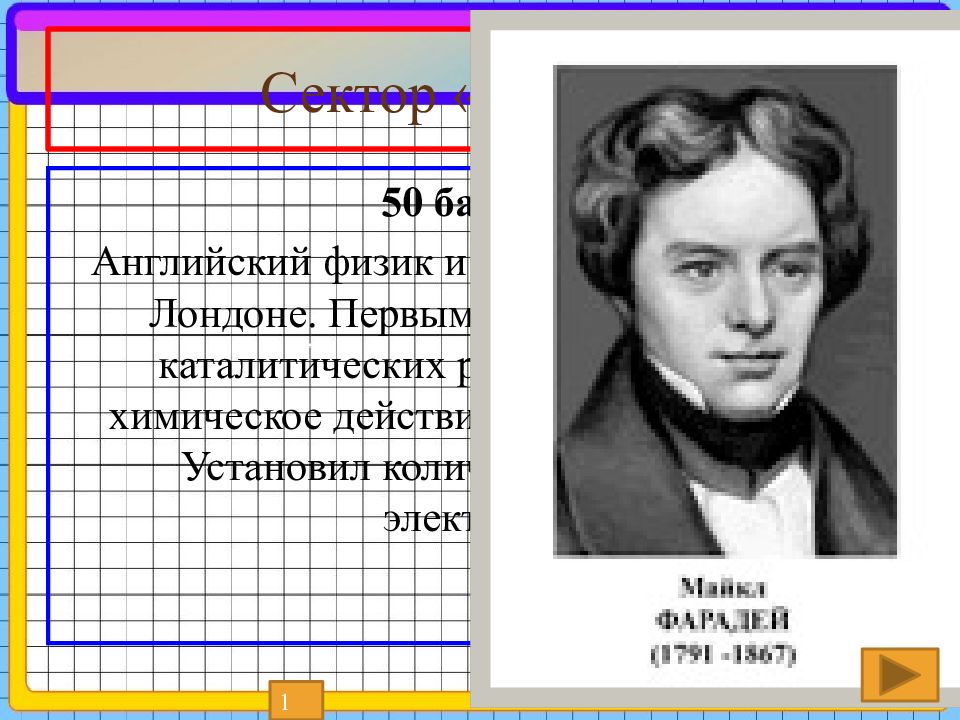
Слайд 28: Сектор «Учёные»
50 баллов Английский физик и химик, родившийся в Лондоне. Первым начал исследование каталитических реакций. Обнаружил химическое действие электрического тока. Установил количественные законы электролиза. 1
Слайд 29: Сектор «Реакции»
10 баллов Реакция, в результате которой из двух или нескольких простых или сложных веществ образуется одно сложное вещество 1
Слайд 31: Сектор «Реакции»
30 баллов Реакция, в результате которой из одного сложного вещества получается несколько простых или сложных веществ 1
Слайд 32: Сектор «Реакции»
40 баллов Реакция, в результате которой происходит ряд последовательных превращений 1
Слайд 33: Сектор «Реакции»
50 баллов Реакция, протекающая между простым и сложным веществами, при которой атомы простого вещества замещают атомы одного из элементов сложного вещества. 1
Слайд 34
Синий раунд 1 2 20 40 60 80 100 20 40 60 80 100 20 40 60 80 100 20 40 60 80 100 20 40 60 80 100 20 40 60 80 100 Открытия Газы Кислоты Соли Неметаллы Строение вещества
Слайд 35: Сектор «Открытия»
20 баллов Первенство открытия этого химического элемента принадлежит китайскому учёному VIII века Маохао, который за 1000 лет до А. Лавуазье установил, что в состав воздуха, входит газ, поддерживающий горение и дыхание. 1
Слайд 36: Сектор «Открытия»
40 баллов Этот химический элемент был обнаружен немецким учёным Парацельсом в XVI веке, когда он погружал железо в серную кислоту. 1
Слайд 37: Сектор «Открытия»
60 баллов Этот английский физик в 1911 году своим знаменитым опытом рассеивания альфа-частиц доказал существование положительно заряженного ядра в атомах элементов 1
Слайд 38: Сектор «Открытия»
80 баллов Впервые этот химический элемент был открыт английским учёным Д.Резерфордом в 1772 году. Его свойства исследовали К. Шееле, Г. Кавендиш, Дж. Пристли, А. Лавуазье. 1
Слайд 39: Сектор «Открытия»
100 баллов В поисках «философского камня», якобы способного превратить неблагородные металлы в золото, гамбургский алхимик Бранд в 1669 году при перегонке сухого остатка от выпаривания мочи впервые получил аллотропное видоизменение одного из химических элементов. Поначалу алхимик думал, что это «философский камень», ибо полученное вещество испускало голубоватый свет. 1
Слайд 40: Сектор «Газы»
20 баллов Бесцветный газ с характерным запахом тухлых яиц, тяжелее воздуха, малорастворим в воде, его водный раствор на свету мутнеет, вследствие выделения серы. В смеси с воздухом взрывоопасен и ядовит. 1
Слайд 41: Сектор «Газы»
40 баллов Бесцветный газ, тяжелее воздуха, при сильном охлаждении превращается в твёрдую массу, похожую на снег. Применяется в пищевой промышленности при производстве сахара, пива, газированной воды, в химической промышленности – для получения соды, мочевины и др. 1
Слайд 42: Сектор «Газы»
60 баллов Газ без цвета, запаха и вкуса, продукт неполного окисления углерода, плохо растворим в воде, ядовит. Имеет большое практическое значение как горючее(генераторный светильный газ) и восстановитель, в смеси с водородом – сырьё для получения метилового спирта. 1
Слайд 43: Сектор «Газы»
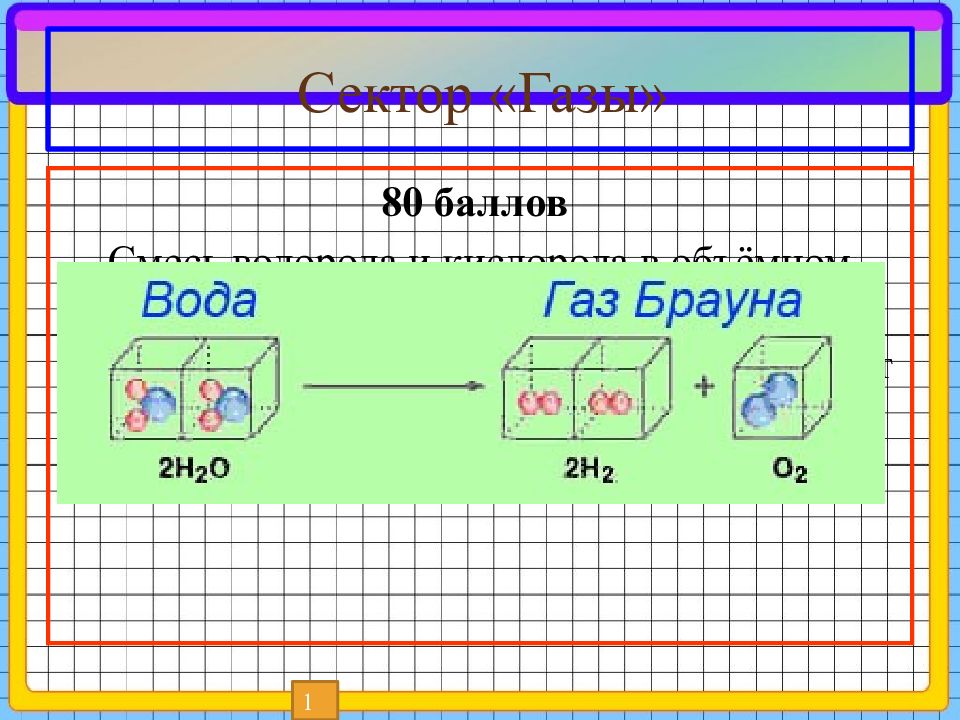
80 баллов Смесь водорода и кислорода в объёмном отношении 2:1. При поджигании они соединяются почти мгновенно, происходит сильный взрыв. 1
Слайд 44: Сектор «Газы»
100 баллов Газ бурого цвета, ядовит, нарушает деятельность сердца и лёгких 1
Слайд 45: Сектор «Кислоты»
20 баллов Бесцветная жидкость с резким запахом, гигроскопична, кипит при 84 º С, хорошо растворима в воде. В концентрированном виде (96-98 %) имеет красно-бурый цвет из-за присутствия в ней оксида. Применяется в производстве удобрений, взрывчатых веществ, лекарств, красителей, пластмасс, искусственных волокон, как окислитель в ракетных двигателях. 1
Слайд 46: Сектор «Кислоты»
40 баллов Бесцветная маслянистая жидкость, очень гигроскопична, растворяется в воде с выделением большого количества теплоты вследствие образования гидратов. Эффективное обезвоживающее средство, применяется для сушки газов, обугливает углеводы, отнимая воду. Применяется в производстве кислот, щелочей, солей, хлора, минеральных удобрений, красок и др. 1
Слайд 47: Сектор «Кислоты»
60 баллов Смесь концентрированных азотной и соляной кислот в объёмном соотношении 1:3, сильный окислитель: растворяет золото, платину и некоторые другие металлы, не растворимые в обычных кислотах. 1
Слайд 48: Сектор «Кислоты»
80 баллов Слабая нерастворимая в воде кислота, в воде образует коллоидный раствор. Гели этой кислоты используют как адсорбенты и отбеливатели. Её соли широко распространены в природе 1
Слайд 49: Сектор «Кислоты»
100 баллов Бесцветная жидкость с запахом горького миндаля, легко испаряется и разлагается, пары её легче воздуха. Содержится в косточках вишни и сливы. Очень слабая одноосновная кислота. Её соли и сама кислота – сильнейшие яды. Применяется для борьбы с насекомыми-паразитами, грызунами и вредителями садовых культур. 1
Слайд 50: Сектор «Соли»
30 баллов Эта соль применяется в производстве соды, едкого натра, хлора, сульфата натрия, а в быту – как консервирующее средство. 1
Слайд 51: Сектор «Соли»
40 баллов Эту соль калия применяют в стекольном и мыловаренном производствах, а также в сельском хозяйстве как калийное удобрение 1
Слайд 52: Сектор «Соли»
60 баллов Эта соль образует синие кристаллы, используется при получении минеральных красок, для пропитки древесины, борьбы с вредителями и болезнями растений 1
Слайд 53: Сектор «Соли»
80 баллов Соль кальция, применяется как наполнитель для бумаги, резины, линолеума, а её природные залежи – как строительный материал. 1
Слайд 54: Сектор «Соли»
100 баллов Эту соль бария используют в стекольной промышленности для изготовления эмалей, глазурей. 1
Слайд 55: Сектор «Неметаллы»
20 баллов Этот неметалл издавна употребляли для отбеливания тканей, изготовления лекарственных препаратов, чернения оружия и приготовления чёрного пороха. 1
Слайд 56: Сектор «Неметаллы»
40 баллов Второй элемент после кислорода по распространённости в земной коре. В свободном виде не встречается. Его соединения входят в состав растительных и животных клеток, некоторые организмы обладают способностью его накапливать. 1
Слайд 57: Сектор «Неметаллы»
60 баллов В природе этот элемент может находиться в виде простого вещества. Он составляет 75,5 % воздуха по массе, содержится во многих органических веществах, в том числе и в белках. 1
Слайд 58: Сектор «Неметаллы»
80 баллов Открыт Д.Рэлеем и У.Рамзаем в 1894 году. В переводе с греческого его название означает «недеятельный, неработающий» 1
Слайд 59: Сектор «Неметаллы»
100 баллов Этот газ нашёл применение в рекламной индустрии (заполненные им рекламные трубки дают ярко-красное свечение). В переводе с греческого его название означает «новый» 1
Слайд 60: Сектор «Строение вещества»
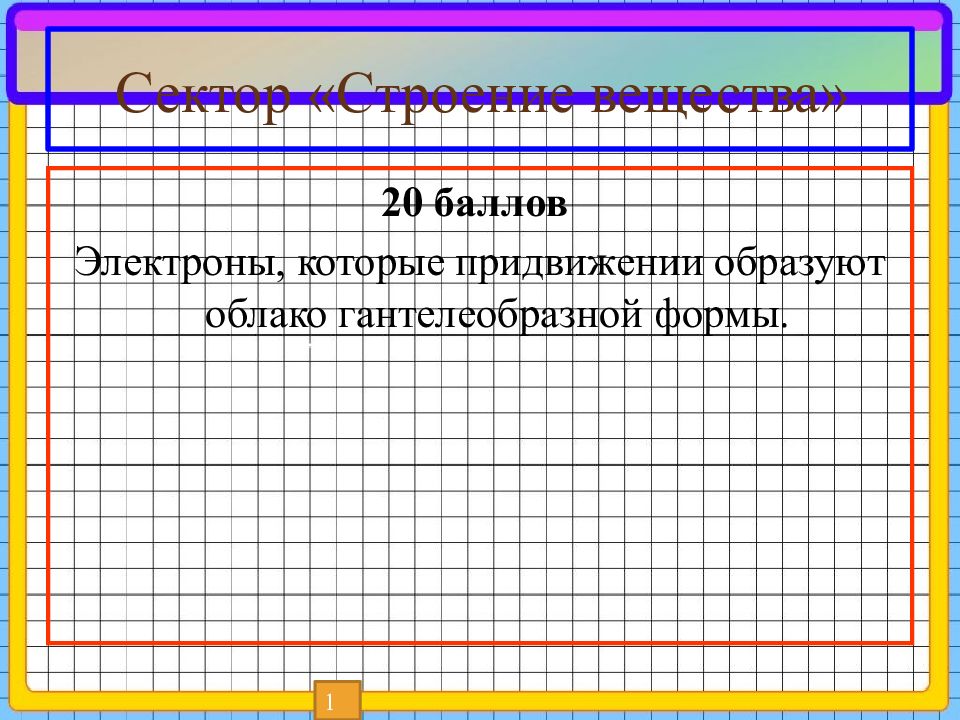
20 баллов Электроны, которые придвижении образуют облако гантелеобразной формы. 1
Слайд 61: Сектор «Строение вещества»
40 баллов Заряженные частицы, в которые превращаются атомы, в результате присоединения или отдачи электронов. 1
Слайд 62: Сектор «Строение вещества»
60 баллов Вид химической связи, образованной атомами элементов, электроотрицательности которых незначительно отличаются. 1
Слайд 63: Сектор «Строение вещества»
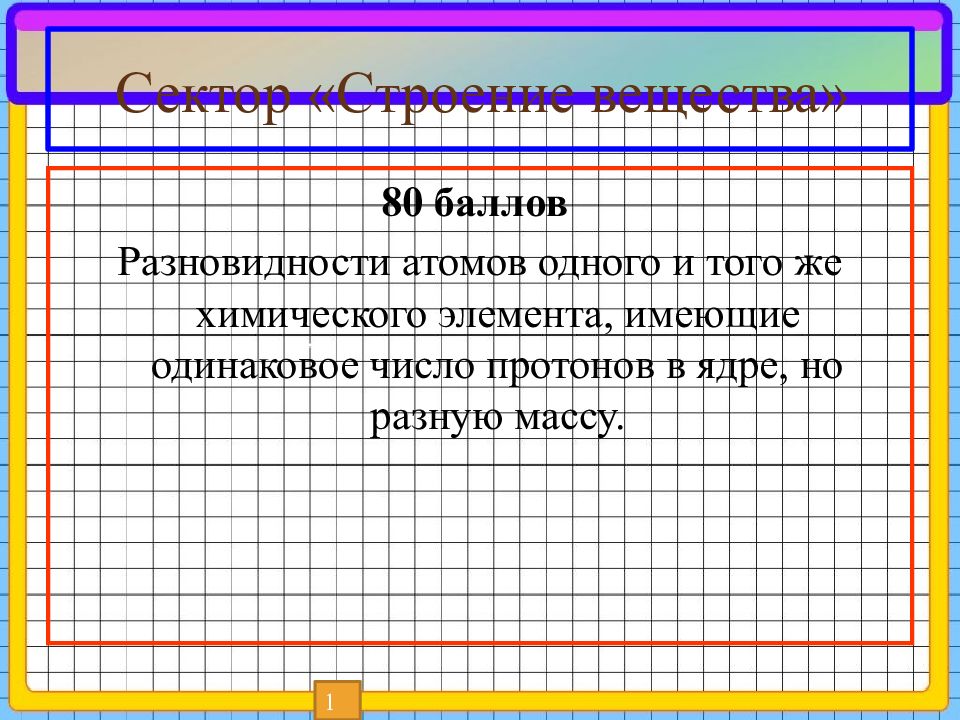
80 баллов Разновидности атомов одного и того же химического элемента, имеющие одинаковое число протонов в ядре, но разную массу. 1
Слайд 64: Сектор «Строение вещества»
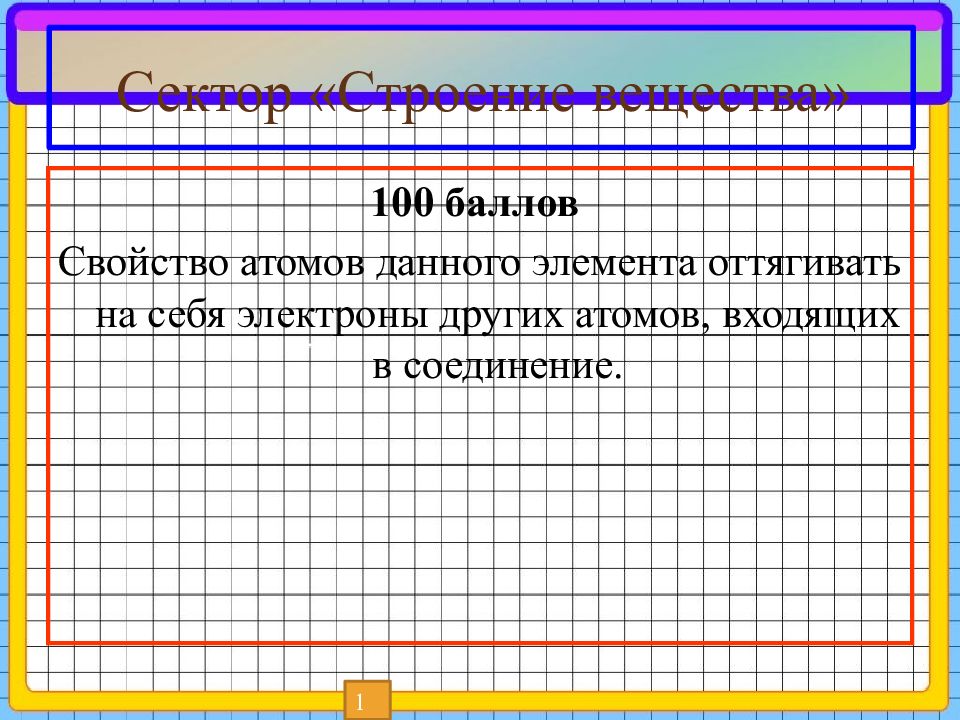
100 баллов Свойство атомов данного элемента оттягивать на себя электроны других атомов, входящих в соединение. 1
Слайд 67
Два животных дружат так, Что в честь их назвали знак. Неметалл он, сероват; Крыс, мышей морить мастак. Стоматологи у нас Очень ценят этот знак.
Слайд 69
Смог с наружи показать Электронов целых пять. И судьбою не обижен, Аллотропии привычен: Красный, белый, чёрный цвет, В рыбе главный элемент.
Слайд 70: Карбонат
Белый зайчик прыгает по черному полю Ответ – мел, черная доска
Слайд 77
Источники: Картинки : https://upload.wikimedia.org/wikipedia/commons/thumb/e/e7/Axel_Fredrik_Cronstedt.JPG/200px-Axel_Fredrik_Cronstedt.JPG https://upload.wikimedia.org/wikipedia/commons/thumb/6/6a/Nickel_electrolytic_and_1cm3_cube.jpg/230px-Nickel_electrolytic_and_1cm3_cube.jpg http://protown.ru/pic/niccolum1.jpg http://img10.proshkolu.ru/content/media/pic/std/4000000/3490000/3489816-5d707488ff383bf1.png http://kristallov.net/strontianite.html http://forum.xumuk.ru/uploads/monthly_12_2011/post-4796-0-35309100-1324844583.jpg https://upload.wikimedia.org/wikipedia/commons/thumb/6/6a/Tin-2.jpg/220px-Tin-2.jpg http://www.detallium.ru/images/stories/metallimg/bronze.jpg http://chemistry-chemists.com/N6_2011/U111/Zinc-2.jpg http://palladium.ru/files/goods/363/363_1_sb.jpg
Слайд 78
Источники: Картинки : http://chemistry-chemists.com/N1_2012/S1/image/chlorine.jpg http://upload.wikimedia.org/wikipedia/commons/c/c2/Iodine-sample.jpg http://ppt4web.ru/images/8/23624/310/img13.jpg http://files.ub.ua/goods/goods-photos/22/549112_bromine-1-92033773.jpg http://chemistry-chemists.com/Video/Sodium-1.jpg http://www.arlan.ru/upload/iblock/330/3302b4ad65f180fa21b3024f0e8fa813.jpg http://www.metatorg.com/upload/iblock/5c3/400_iron_electrolytic.png http://www.periodictable.ru/013Al/slides/Al1.jpg https://upload.wikimedia.org/wikipedia/commons/thumb/b/b3/Potassium.JPG/220px-Potassium.JPG http://www.istu.edu/news/images/2013/01/truba22.jpg http://ligr.ucoz.ru/_ph/1/2/455110205.jpg http://gallery.ykt.ru/galleries/dachniy/2013/06/19/1297183_0.jpg http://900igr.net/datai/ekologija/Dozhdi/0010-032-Sera.jpg http://www.syl.ru/misc/i/ai/97628/196552.jpg http://todnb.ru/content/images/%D0%9C%D0%B5%D0%BD%D0%B4%D0%B5%D0%BB%D0%B5%D0%B5%D0%B2_0005.bmp
Слайд 79
Источники: Картинки : https://upload.wikimedia.org/wikipedia/commons/thumb/3/3d/Avogadro_Amedeo.jpg/240px-Avogadro_Amedeo.jpg http://dou-shkola.ru/local/cache-vignettes/L200xH267/arton1697-22c28.jpg http://www.obzor.lt/images/news/6/2013_08_22/pic.jpg http://saratov-shkola.ru/images/photos/medium/4e159538e8ffc399f6c1e5f1b36fcec9.jpg http://www.teplonositeli.ru/img/truba_kor.gif http://www.tantal-d.ru/img/image/kislorod.jpg http://cdn.fxyz.ru/img/mendeleev/H-splash.jpg http://class-fizika.narod.ru/phys/9.jpg http://gizmod.ru/uploads/posts/2014-09/1411480212_iphone-6-ispytanie-1.jpg http://chemistry-chemists.com/N3_2012/U3/img/white_phosphorus-5.jpg http://eaaab56b-4089-46de-bde0-552351c9bd98.jpeg.beta.cdn.gorod55.ru/fs/ea/a/ab56b-4089-46de-bde0-552351c9bd98_big.jpeg http://upakovka66.ru/images/Suhoy_Led_pic_1.jpg http://www.dishisvobodno.ru/pictures/carbonic%20oxide_2.jpg http://sds-max.com.ua/pic/braun1.jpg http://900igr.net/datai/khimija/Reaktsii-veschestv/0017-023-NO2.png
Слайд 80
Источники: Картинки : http://static.irk.ru/media/img/site/gallery/85/c2920abe-2438-4ae6-8ec5-1003d1d4078f_jpg_460x1000_q85.jpg http://chemistry-chemists.com/Video/eggs-acid-11.JPG http://himege.ru/wp-content/uploads/2013/12/%D0%BA%D0%BE%D0%BD%D1%86%D0%B5%D0%BD%D1%82%D1%80%D0%B8%D1%80%D0%BE%D0%B2%D0%B0%D0%BD%D0%BD%D0%B0%D1%8F-%D1%81%D0%B5%D1%80%D0%BD%D0%B0%D1%8F-%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0-%D0%BE%D0%B1%D1%83%D 0%B3%D0%BB%D0%B8%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5-%D1%81%D0%B0%D1%85%D0%B0%D1%80%D0%B0.jpg http://images.myshared.ru/6/582501/slide_18.jpg http://files.school-collection.edu.ru/dlrstore/90722b3f-edab-6290-3cb1-717eb90115db/index.files/image002.jpg http://images.myshared.ru/4/199472/slide_18.jpg http://img.21food.com/20110609/product/1305777341020.jpg
Слайд 81
Источники: Картинки : http://dic.academic.ru/pictures/wiki/files/80/PotashUSGOV.jpg https://upload.wikimedia.org/wikipedia/commons/thumb/d/d8/Copper_sulfate.jpg/300px-Copper_sulfate.jpg http://raax.ru/wp-content/uploads/2010/07/gemchug.jpg http://chemistry-chemists.com/N3_2012/U3/img/barium_carbonate-1.jpg http://geo.web.ru/druza/a-Dvor_V-141.JPG http://upload.wikimedia.org/wikipedia/commons/thumb/5/59/Polycrystalline_silicon_rod.jpg/150px-Polycrystalline_silicon_rod.jpg http://images.myshared.ru/4/277145/slide_9.jpg http://apeks-m.ru/wp-content/uploads/2011/09/svarka-argonom.jpg http://thumbs.dreamstime.com/t/%D0%BD%D0%B5%D0%BE%D0%BD%D0%BE%D0%B2%D0%B0%D1%8F-%D0%BF%D0%B0-%D1%8C%D0%BC%D0%B0-46193111.jpg http://900igr.net/datas/obg/Profilaktika-vrednykh-privychek/0003-003-Sostav-tabachnogo-dyma.jpg Ребусы: http://www.igraza.ru/images/stories/1500.png
Последний слайд презентации: Внеклассное мероприятие
Источники: 2. Ребусы: http://allforchildren.ru/rebus/rebus15/15-053.gif Солнце: http://img-novosib.fotki.yandex.ru/get/4808/valenta-mog.73/0_63c39_f5b1d1be_orig.jpg 3. Слайды 70 – 75: рисунки выполнили ребята МКОУ СОШ №2 г. Малмыжа. 4. Сценарий «Своя игра»: Научно-методический журнал : Химия в школе, 4 июня 1997г.