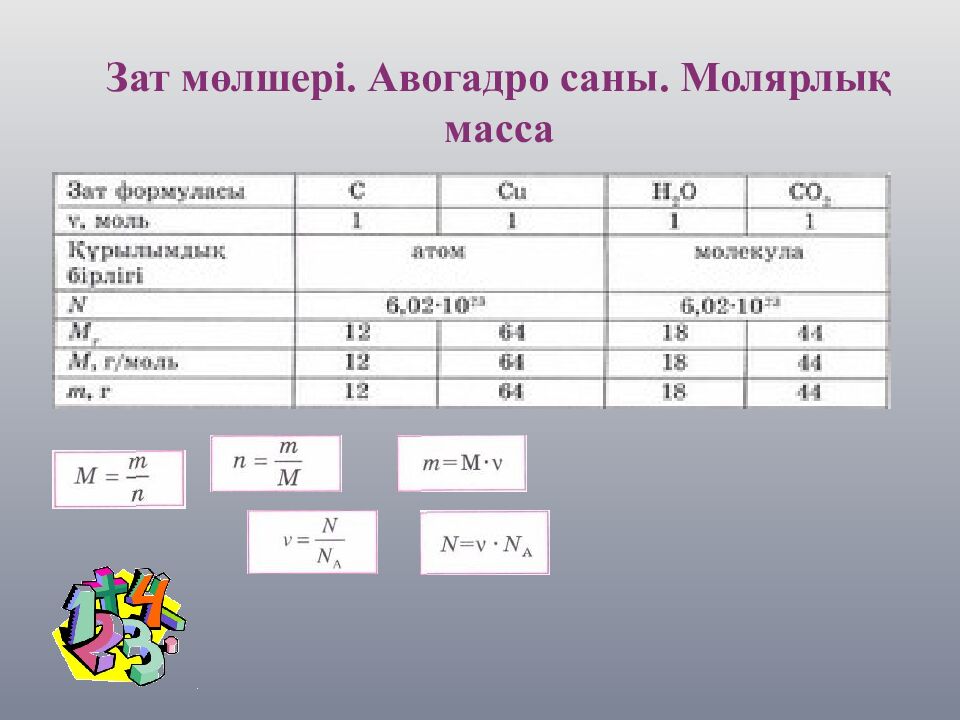
Слайд 2
Сабақтың мақсаты : Тапсырмалар арқылы бағдарлау тәсілдерін зерттеу арқылы оқушылар ұғымын кеңейтеді, реакциялармен жұмыс істеуге топ арқылы дағдыланады Күтілетін нәтиже: Тақырыпты түсіне отырып ойын жеткізе білу арқылы,тақырыпты дұрыс орындауға дағдыланады
Слайд 3: Жигсо» әдісі
1 топ. Жай және күрделі заттар 2 топ. Салыстырмалы молекулалық масса 3 топ. Салыстырмалы атомдық масса
Слайд 5: Спираль” әдісі
325 г мырыш тұз қышқылымен әрекеттескенде бөлінетін сутектің зат мөлшері (моль) Шешуі: Zn + 2НСІ →ZnСІ 2 + Н 2 ↑ М ( Zn ) = 65 г/моль m ( Zn ) = ν · М ( Zn ) = 1 моль · 65 г/моль = 65 г 325 г Zn ----- х моль Н 2 65 г Zn ---- 1 моль Н 2
Слайд 7
4 грамм темір (ІІІ)оксидін толық тотықсыздандыруға жұмсалатын көміртек (ІІ) оксидінің мөлшері (моль) Шешуі: Ғе 2 О 3 + 3СО → 2Ғе + 3СО 2 М (Ғе 2 О 3 ) = 160 г/моль m (Ғе 2 О 3 ) = ν · М (Ғе 2 О 3 ) = 1 моль · 160 г/моль = 160 г 4 г Ғе 2 О 3 ----- х моль СО 160 г Ғе 2 О 3 ---- 3 мольСО
Слайд 8
3,6 г кальций гидрофосфатының зат мөлшері (моль) Шешуі: М ( Са(Н 2 РО 4 ) 2 ) = 234 г/моль
Слайд 9
Судың 45 г сәйкес келетін зат мөлшері (моль) Шешуі: М (Н 2 О) = 18 г/моль m (Н 2 О) = ν · М (Н 2 О) = 1 моль · 18 г/моль = 18 г
Слайд 10
2 моль темірдің зат мөлшеріндегі атом саны Шешуі: N (Ғе) = N А 2 моль · 6,02 · 10 23 = 1 2,04 · 10 24
Слайд 11
1,6 г мыс (ІІ) сульфаты бар ерітіндімен әрекеттескен темір тақташадан ерітіндіге өткен темір атомдарының саны Шешуі: CuSO 4 + Ғе → ҒеSO 4 + Cu М (CuSO 4 ) = 160 г/моль m (CuSO 4 ) = ν · М (CuSO 4 ) = 1 моль · 160 г/моль = 160 г N А = 6,02 · 10 23 х ----- 1,6 г Cu SO 4 6,02 · 10 23 ---- 160 г Cu SO 4
Слайд 12: Бағалау критерийлері мен бағалау шкаласын
Бағалау шкаласы арқылы өз білімдерін топпен жеке бағалау
Слайд 13: Рефлексия
Стикерлерді толтыру Оқушылар бүгінгі сабаққа деген ойынын стикерге жазып, тақтаға іледі