Первый слайд презентации: Алколоиды, производные имидазола. Производные бензимидазола
Выполнила Ковбасюк Р.К.
Слайд 2
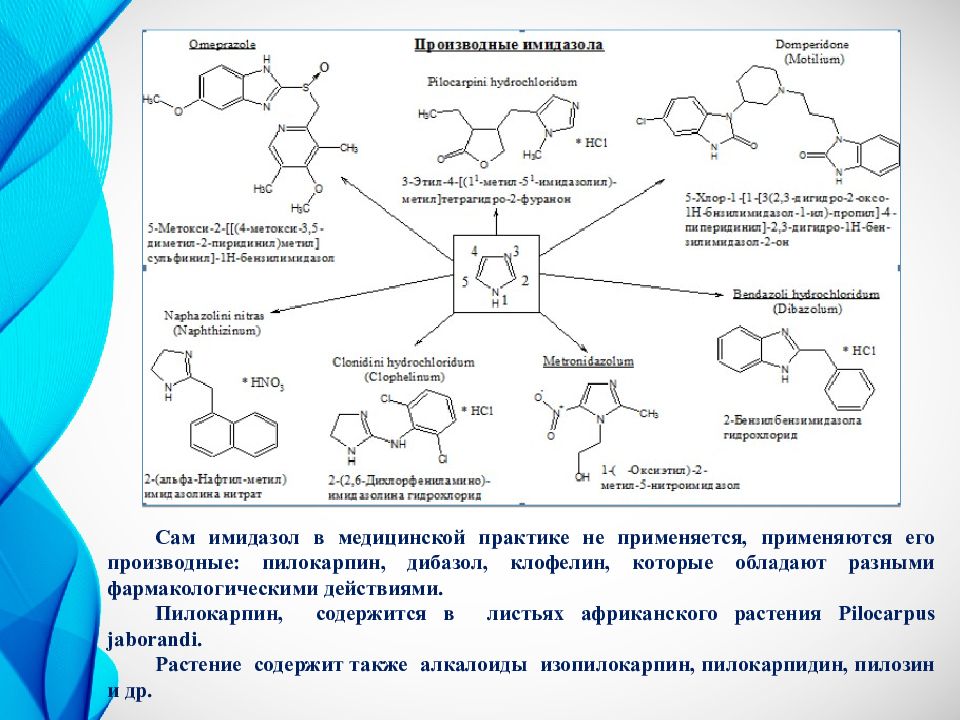
Сам имидазол в медицинской практике не применяется, применяются его производные: пилокарпин, дибазол, клофелин, которые обладают разными фармакологическими действиями. Пилокарпин, содержится в листьях африканского растения Pilocarpus jaborandi. Растение содержит также алкалоиды изопилокарпин, пилокарпидин, пилозин и др.
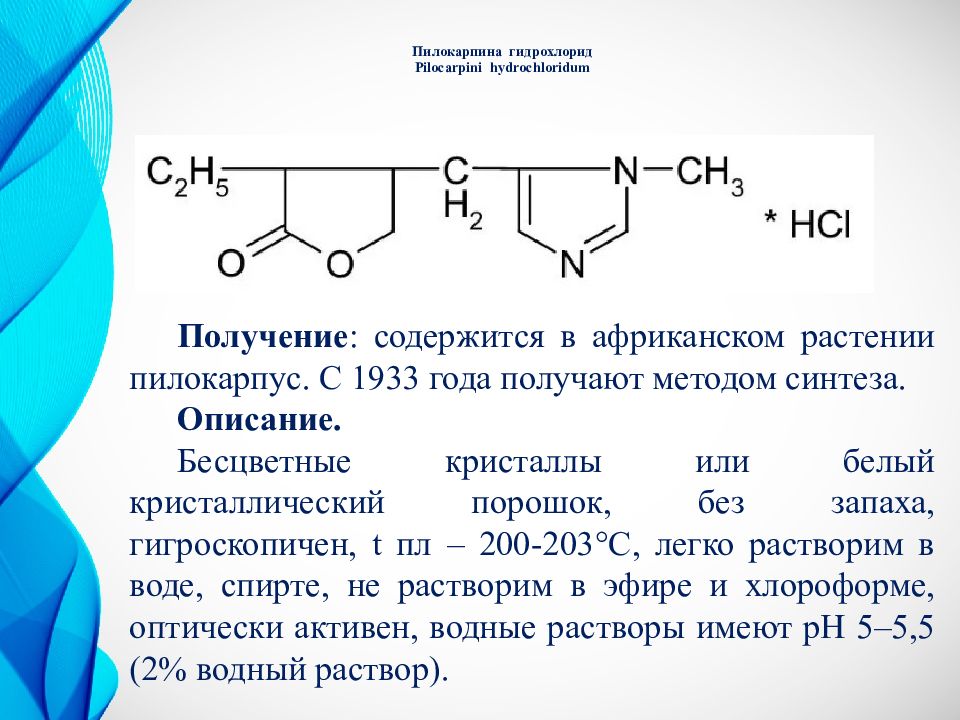
Слайд 3: Пилокарпина гидрохлорид Pilocarpini hydrochloridum
Получение : содержится в африканском растении пилокарпус. С 1933 года получают методом синтеза. Описание. Бесцветные кристаллы или белый кристаллический порошок, без запаха, гигроскопичен, t пл – 200-203°С, легко растворим в воде, спирте, не растворим в эфире и хлороформе, оптически активен, водные растворы имеют pH 5–5,5 (2% водный раствор).
Слайд 4: Подлинность
1. Подлинность пилокарпина гидрохлорида (ФС) устанавливают по наличию хлорид-иона. Обнаружение хлорид-иона. 2. Образование надхромовых кислот Испытание основано на выполнении реакции образования надхромовых кислот в присутствии пилокарпина. Смесь надхромовых кислот и пероксида хрома имеет синюю окраску и растворяется в эфире (эфирный слой синеет), но не растворяется в бензоле и хлороформе. В присутствии пилокарпина смесь извлекается и бензолом, и хлороформом, при этом извлечение имеет сине-фиолетовую окраску.
Слайд 5
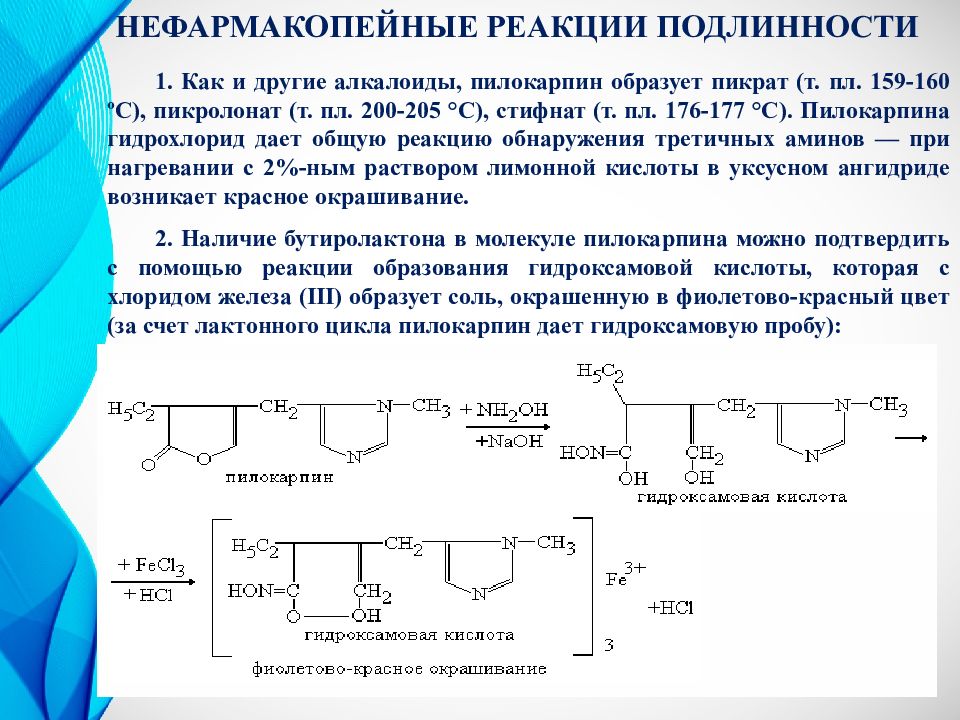
1. Как и другие алкалоиды, пилокарпин образует пикрат (т. пл. 159-160 ºС ), пикролонат (т. пл. 200-205 °C), стифнат (т. пл. 176-177 °C). Пилокарпина гидрохлорид дает общую реакцию обнаружения третичных аминов — при нагревании с 2%-ным раствором лимонной кислоты в уксусном ангидриде возникает красное окрашивание. 2. Наличие бутиролактона в молекуле пилокарпина можно подтвердить с помощью реакции образования гидроксамовой кислоты, которая с хлоридом железа (III) образует соль, окрашенную в фиолетово-красный цвет (за счет лактонного цикла пилокарпин дает гидроксамовую пробу): НЕФАРМАКОПЕЙНЫЕ РЕАКЦИИ ПОДЛИННОСТИ
Слайд 6
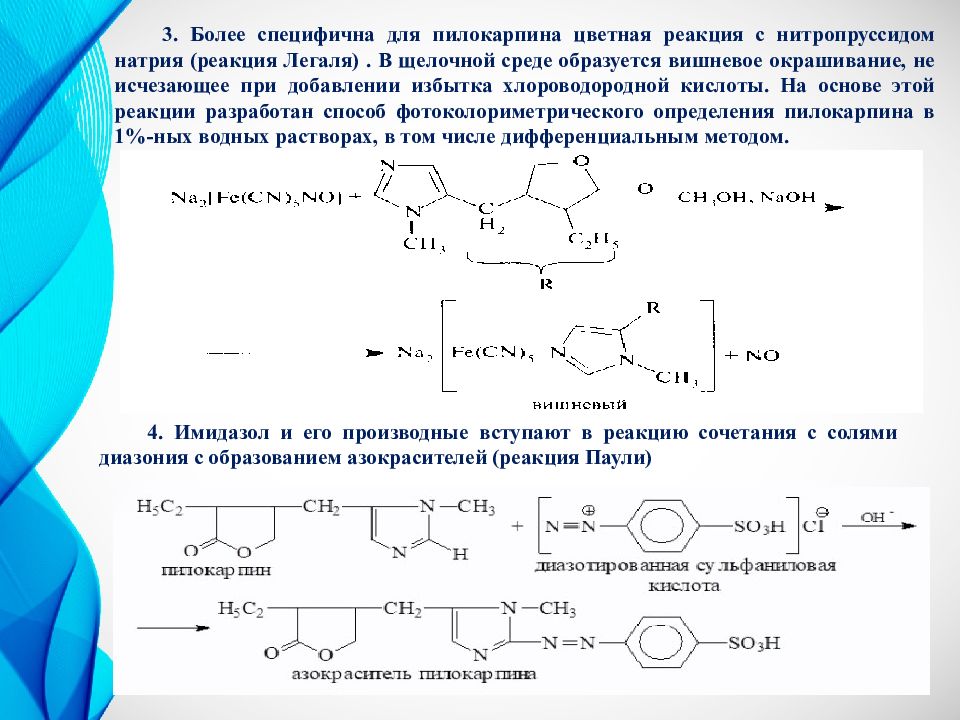
3. Более специфична для пилокарпина цветная реакция с нитропруссидом натрия (реакция Легаля ). В щелочной среде образуется вишневое окрашивание, не исчезающее при добавлении избытка хлороводородной кислоты. На основе этой реакции разработан способ фотоколориметрического определения пилокарпина в 1%-ных водных растворах, в том числе дифференциальным методом. 4. Имидазол и его производные вступают в реакцию сочетания с солями диазония с образованием азокрасителей (реакция Паули)
Слайд 7
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ Количественное определение пилокарпина гидрохлорида выполняют, подобно другим гидрохлоридам алкалоидов, методом титрования в неводных растворителях или используя метод нейтрализации (в спиртовом растворе) по связанной хлороводородной кислоте: C 11 H 16 O 2 N 2 × HCl + NaOH → C 11 H 16 O 2 N 2 + NaCl + H 2 O Известен способ определения, основанный на образовании полииодида пилокарпина. Анализ выполняют в присутствии насыщенного раствора хлорида натрия и ацетатного буферного раствора ( pH около 6,0) методом обратного иодометрического титрования после отделения осадка полииодида. Количественно определить пилокарпина гидрохлорид можно методом УФ-спектрофотометрии. В качестве растворителя используют воду или 0,01 М раствор хлороводородной кислоты. Анализ выполняют при длине волны 215 нм (удельный показатель поглощения 223,7).
Слайд 8
Применяют в глазной практике для лечения глаукомы, готовят глазные капли, мази. М-холиномиметик (антагонист атропина), антиглаукомное средство, понижает внутринлазное давление, улучшает трофику глаза при тромбозе центральной вены сетчатки, а так же при необходимость сужения зрачка после инстилляции мидриатиков. Пилокарпина гидрохлорид хранят в хорошо укупоренной таре, предохраняющей от действия света и влаги. Такие условия хранения необходимо соблюдать ввиду его гигроскопичности, а также возможности гидролиза и окисления. Даже в отсутствии света пилокарпина гидрохлорид разрушается во влажной атмосфере. При повышении температуры разрушение ускоряется. Применение. Хранение
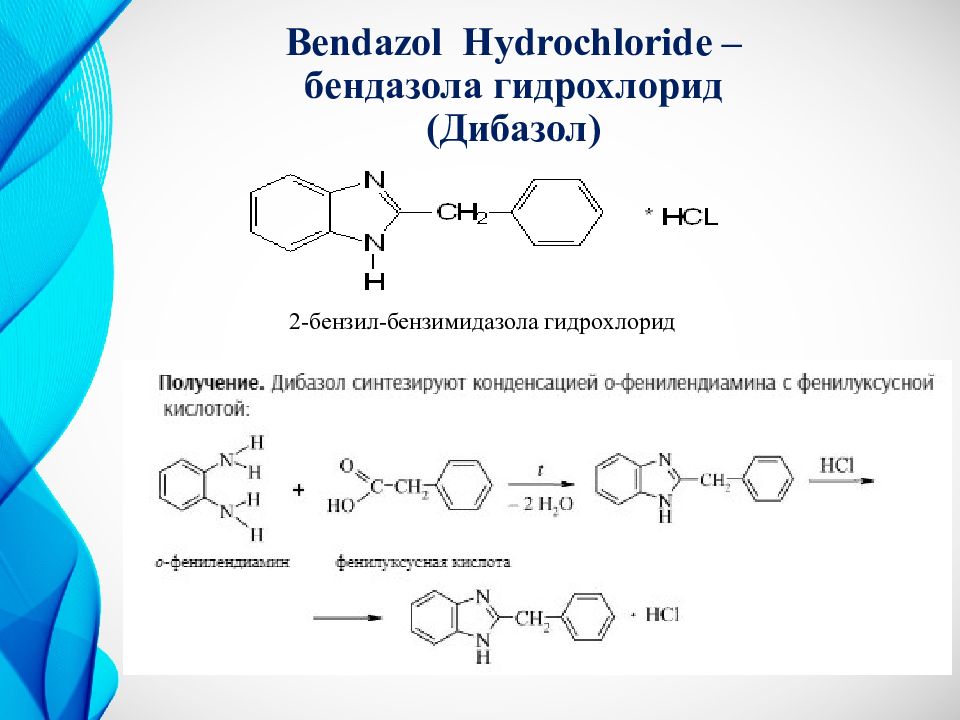
Слайд 9: Bendazol Hydrochloride – бендазола гидрохлорид ( Дибазол)
2-бензил-бензимидазола гидрохлорид
Слайд 10
Bendazoli Hydrochloridum ( Дибазол )- Белый или белый со слегка сероватым или желтоватым оттенком кристаллический порошок, горько-соленого вкуса. Гигроскопичен. Трудно растворим в воде и хлороформе, легко растворим в спирте, мало растворим в ацетоне, практически нерастворим в эфире. Температура плавления 182–186°. Водные растворы имеют рН 2,8-3,5. Подлинность 1. ИК-спектр препарата должен полностью совпадать со спектром стандарта или с рисунком, прилагаемым к фармакопейной статье. 2. УФ-спектр спиртового раствора препарата имеет характерные максимумы и минимумы поглощения. 3. Температура плавления
Слайд 11
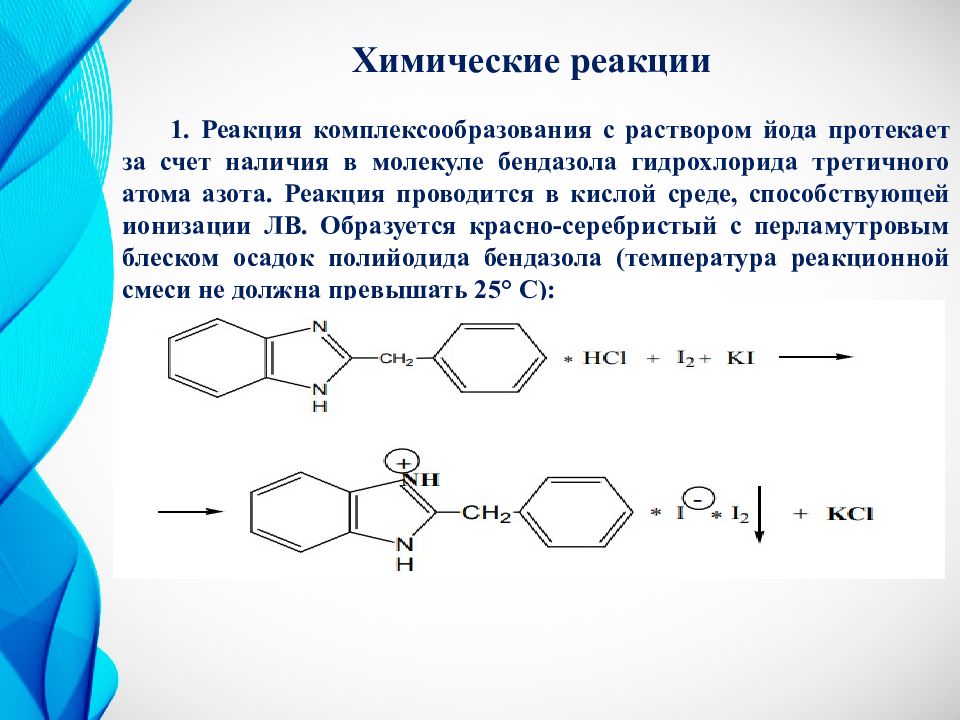
Химические реакции 1. Реакция комплексообразования с раствором йода протекает за счет наличия в молекуле бендазола гидрохлорида третичного атома азота. Реакция проводится в кислой среде, способствующей ионизации ЛВ. Образуется красно-серебристый с перламутровым блеском осадок полийодида бендазола (температура реакционной смеси не должна превышать 25° С):
Слайд 12
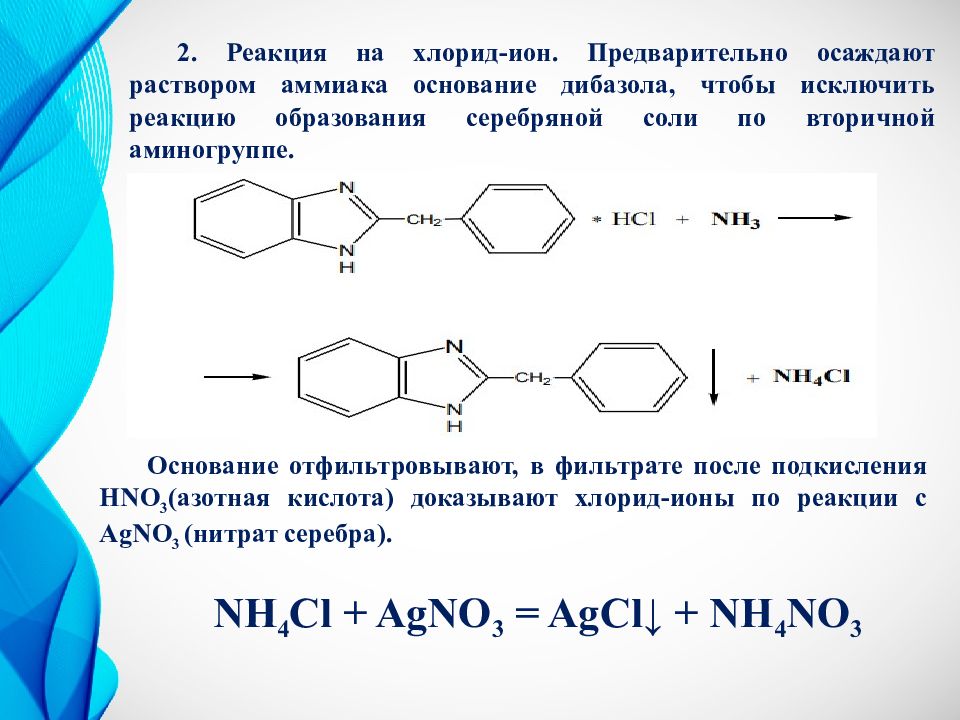
2. Реакция на хлорид-ион. Предварительно осаждают раствором аммиака основание дибазола, чтобы исключить реакцию образования серебряной соли по вторичной аминогруппе. Основание отфильтровывают, в фильтрате после подкисления HNO 3 (азотная кислота) доказывают хлорид-ионы по реакции с AgNO 3 (нитрат серебра). NH 4 Cl + AgNO 3 = AgCl↓ + NH 4 NO 3
Слайд 13
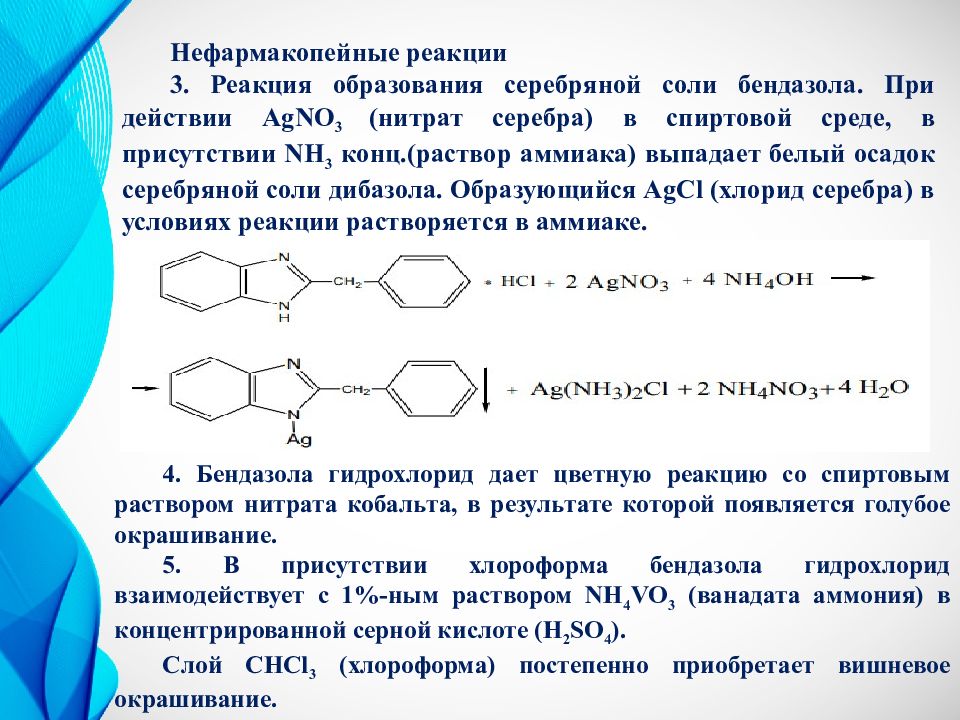
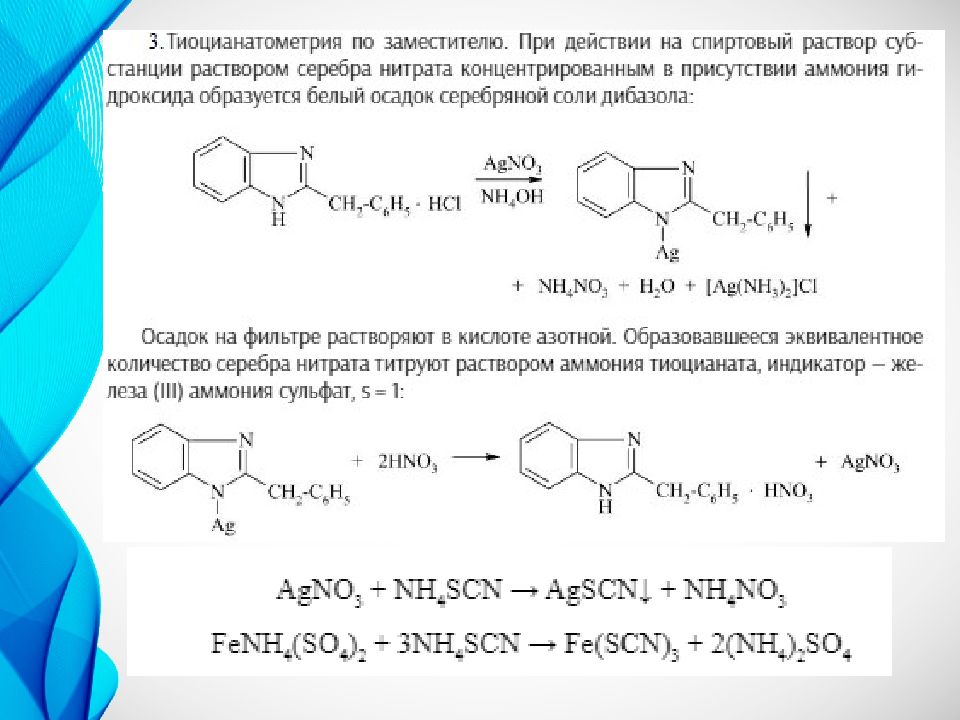
Нефармакопейные реакции 3. Реакция образования серебряной соли бендазола. При действии AgNO 3 ( н итрат серебра ) в спиртовой среде, в присутствии NH 3 конц.(раствор аммиака) выпадает белый осадок серебряной соли дибазола. Образующийся AgCl (хлорид серебра) в условиях реакции растворяется в аммиаке. 4. Бендазола гидрохлорид дает цветную реакцию со спиртовым раствором нитрата кобальта, в результате которой появляется голубое окрашивание. 5. В присутствии хлороформа бендазола гидрохлорид взаимодействует с 1%-ным раствором NH 4 VO 3 (ванадата аммония) в концентрированной серной кислоте ( H 2 SO 4 ). Слой CHCl 3 (хлороформа) постепенно приобретает вишневое окрашивание.
Слайд 14
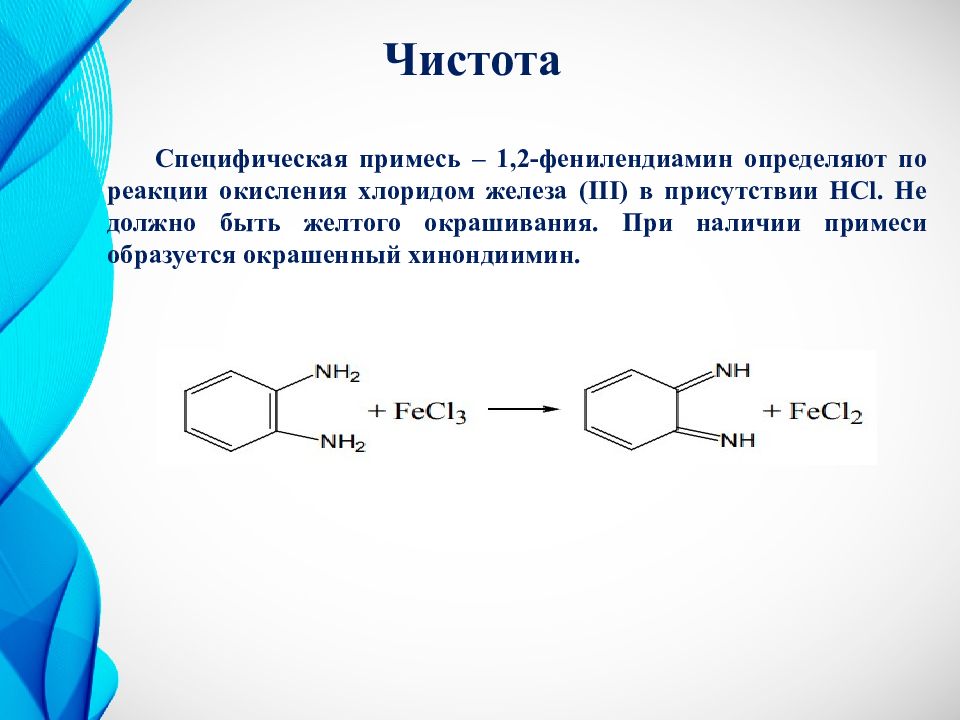
Специфическая примесь – 1,2-фенилендиамин определяют по реакции окисления хлоридом железа (III) в присутствии HCl. Не должно быть желтого окрашивания. При наличии примеси образуется окрашенный хинондиимин. Чистота
Слайд 15: Количественное определение
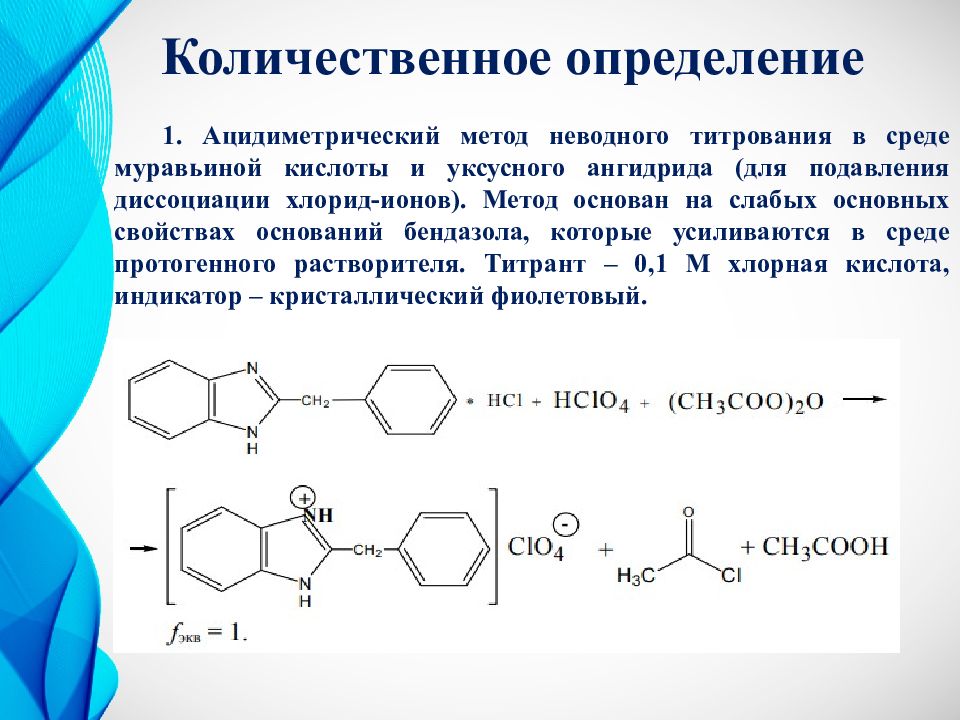
1. Ацидиметрический метод неводного титрования в среде муравьиной кислоты и уксусного ангидрида (для подавления диссоциации хлорид-ионов ). Метод основан на слабых основных свойствах оснований бендазола, которые усиливаются в среде протогенного растворителя. Титрант – 0,1 М хлорная кислота, индикатор – кристаллический фиолетовый.
Слайд 16
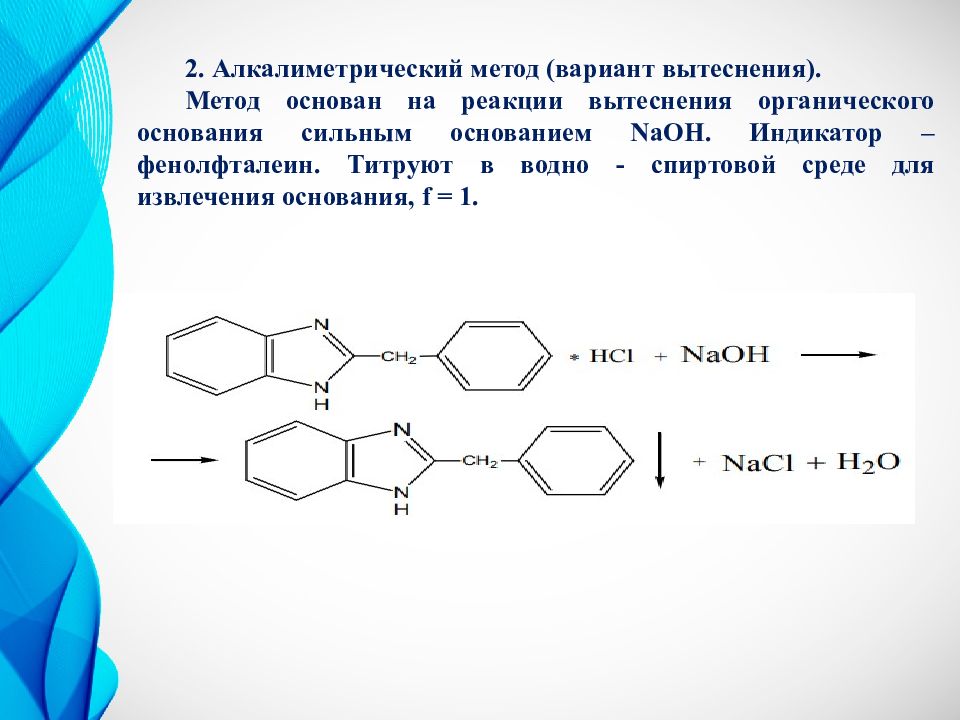
2. Алкалиметрический метод (вариант вытеснения). Метод основан на реакции вытеснения органического основания сильным основанием NaOH. Индикатор – фенолфталеин. Титруют в водно - спиртовой среде для извлечения основания, f = 1.