Слайд 2
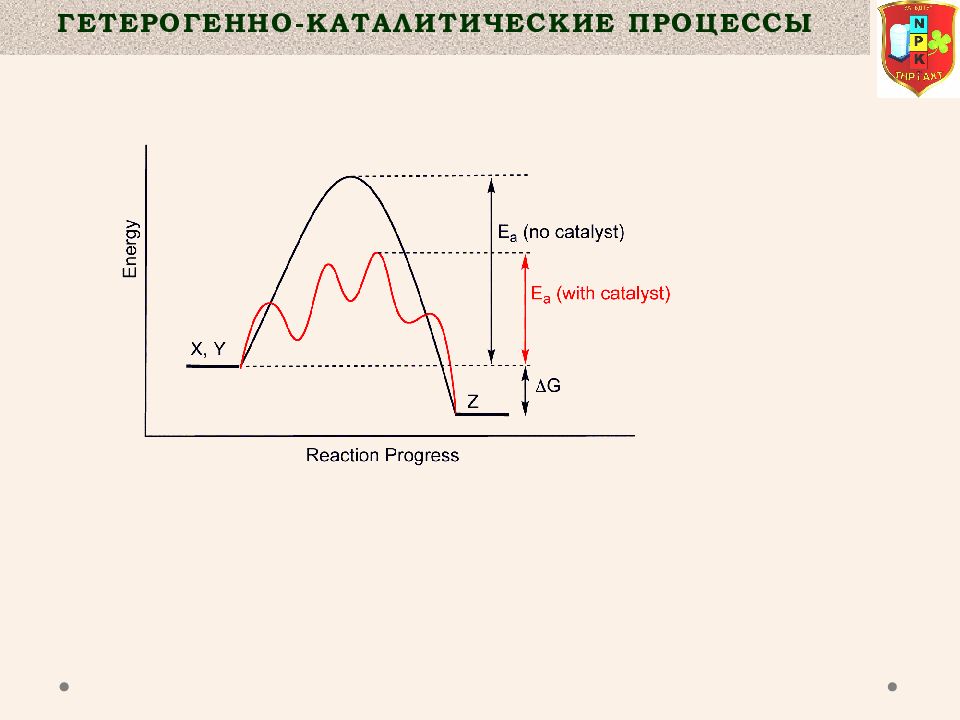
Катализаторы могут находиться в газообразном, жидком и твердом состояниях. По фазовому состоянию реагентов и катализатора каталитические процессы разделяют на две основные группы : - гомогенные - гетерогенные. Гетерогенно– Каталитические процессы Катализом называют изменение скорости химических реакций в результате воздействия веществ — катализаторов, которые участвуют в реакции, вступая в промежуточное химическое взаимодействие с реагентами, но восстанавливают свой химический состав по окончании каталитического акта.
Слайд 4
Гетерогенно - Каталитические процессы Действие катализаторов не влияет на равновесие, а лишь ускоряет достижение равновесия при данной температуре. Сущность катализа одинакова для всех его видов, в частности для гомогенного и гетерогенного. Все каталитические реакции по типу взаимодействия между реагентами и катализатором делят на окислительно-восстановительные и кислотно-основные. Окислительно-восстановительный механизм катализа связан с переносом электронов между реагентами и катализатором, который облегчает электронные переходы в реагирующих молекулах. По этому принципу происходят процессы окисления, дегидрирования, конверсии углеводородов, синтез аммиака, метанола и др. Механизм кислотно-основного катализа заключается в переносе положительно заряженного иона, например протона, или отрицательного иона, например гидроксила, между катализатором и реагентами, в результате чего происходят внутримолекулярные превращения, облегчающие взаимодействия исходных веществ. По такому типу протекают реакции гидратации, дегидратации, гидролиза, этерификации, поликонденсации в растворах и др.
Слайд 5
Гетерогенно– Каталитические процессы Основные требования к катализаторам Выбор катализатора для того или иного процесса определяется в основном технологическими и экономическими соображениями. Катализаторы должны иметь высокую активность, избирательность, низкую температуру зажигания, быть стабильными в работе, малочувствительными к перегреву, к действию контактных ядов, иметь достаточную механическую прочность. При сравнении различных катализаторов для одного процесса используют понятие «активность» катализатора. Активность катализатора — это мера ускоряющего действия его на данную реакцию. Наиболее часто активность выражают разностью или соотношением скоростей каталитической и некаталитической реакций, степенью превращения исходного реагента или выходом целевого продукта при определенном технологическом режиме. Иногда активность представляют соотношением констант скоростей каталитической и некаталитической реакций или отношением энергий активации. Избирательность (селективность) действия катализаторов важна для большинства каталитических процессов органической технологии, в которых термодинамически возможен ряд параллельных и последовательных реакций. Избирательность некоторых катализаторов позволяет сильно ускорять только одну реакцию из ряда возможных, проводить процесс при такой температуре, при которой подавляются другие реакции.
Слайд 6
Гетерогенно-Каталитические процессы Температура зажигания — это минимальная температура, при которой процесс начинает идти с достаточной для практических целей скоростью. Термостойкость катализаторов определяет возможность стабильной работы при высоких температурах. Высокая термостойкость особенно важна при проведении сильно экзотермических процессов. При высоких температурах могут происходить процессы образования неактивных кристаллов, процессы спекания, приводящие к уменьшению внутренней поверхности контакта. Стойкость катализатора к действию контактных ядов — важнейшая характеристика, определяющая возможность отравления катализатора. Отравление катализатора — это частичная или полная потеря активности под действием небольшого количества веществ, называемых контактными ядами.
Слайд 7
Гетерогенно-Каталитические процессы Теплопроводность катализатора является важной характеристикой, т.к. способствует выравниванию температуры в слое контактной массы. При проведении экзотермических процессов катализатор с высокой теплопроводностью применяют для устранения местных перегревов, приводящих к снижению выхода продукта, степени использования сырья, активности контактной массы вследствие спекания или изменения кристаллической структуры и др. В эндотермических процессах крупнозернистый катализатор с низкой теплопроводностью может быть менее активным вследствие снижения температуры в глубине зерна, капиллярной конденсации паров реагентов в порах и др. Повышенная теплопроводность зерен особенно важна для контактных аппаратов с отводом или подводом тепла непосредственно от слоя катализатора. Прочность зерен катализатора. Данное свойство должно обеспечивать эксплуатацию катализатора в течение длительного времени. В неподвижном слое катализатор разрушается вследствие изменения температур, эрозии газовым или жидкостным потоком реагентов, давления слоя вышележащих зерен, высота которого в контактных аппаратах может достигать 5 м. В реакторах с псевдоожиженным или движущимся слоем катализатора под прочностью понимают прежде всего износоустойчивость зерен при ударах и трении их друг о друга, о стенки реактора и теплообменных элементов. Стоимость катализатора – определяющий фактор при его эксплуатации.
Слайд 8
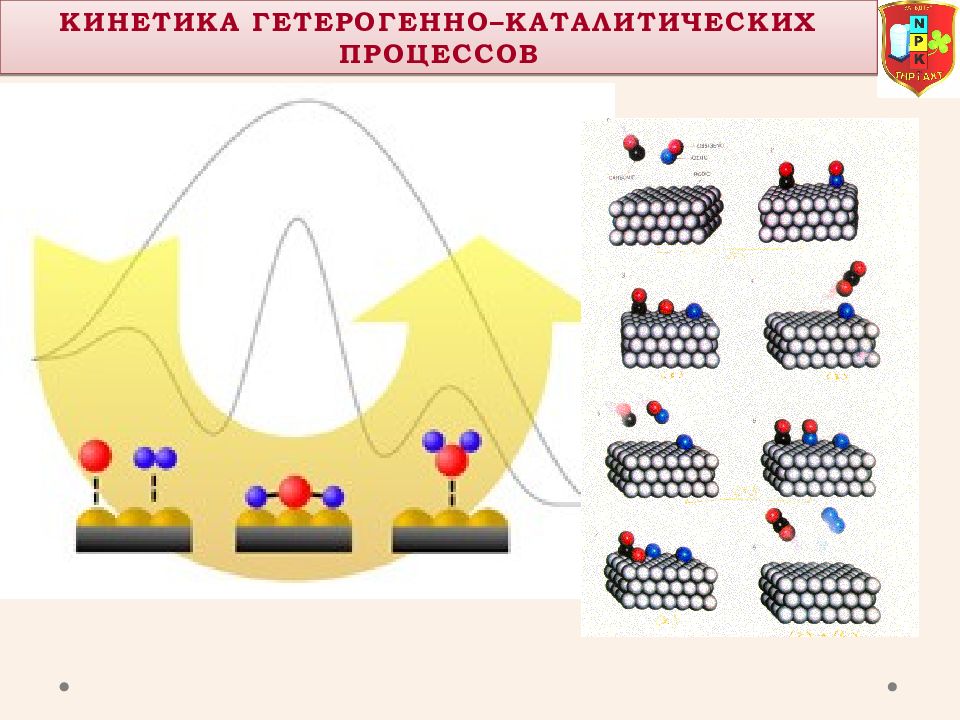
Кинетика Гетерогенно– КаталитическиХ процессОВ Для кинетического моделирования этого сложного превращения его необходимо представить как результат суперпозиции нескольких элементарных процессов: Диффузия реагента из объёма к поверхности катализатора (массоперенос ). Адсорбция реагента на поверхности катализатора. Разрыв связей адсорбированных молекул. Химическое превращение реагента в продукт на поверхности катализатора. Десорбция продукта с поверхности катализатора. Диффузия продукта от поверхности катализатора в объём (массоперенос). Создание новых связей, формирование адсорбированных молекул продукта.
Слайд 9
Кинетика Гетерогенно- КаталитическиХ процессОВ Каталитические процессы как частный случай гетерогенных ХТП в зависимости от технологических условий могут протекать в диффузионных и кинетических областях. В присутствии катализатора К бимолекулярная гомогенная реакция А + В = С + … протекает по следующей схеме: 1) образование промежуточного соединения А К А + К = А К ; 2) образование активированного комплекса А К + В = (АВ ' ) К ; 3) образование конечных продуктов и регенерация катализатора (АВ ' ) К = К + С + …. Если переход от активированного комплекса в отсутствие катализатора к активированному комплексу, возникающему в ходе каталитического процесса, является экзотермическим, т. е. АВ ' + К = (АВ ' ) К, Н < 0,
Слайд 11
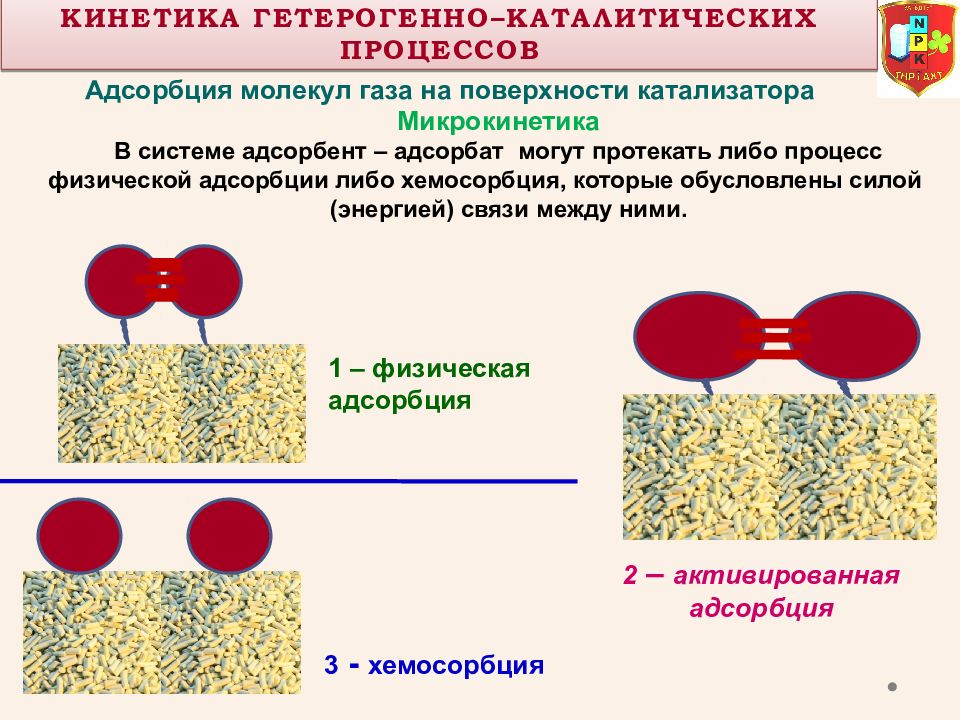
Адсорбция молекул газа на поверхности катализатора 1 – физическая адсорбция 3 - хемосорбция 2 – активированная адсорбция Кинетика Гетерогенно– КаталитическиХ процессОВ Микрокинетика В системе адсорбент – адсорбат могут протекать либо процесс физической адсорбции либо хемосорбция, которые обусловлены силой (энергией) связи между ними.
Слайд 12
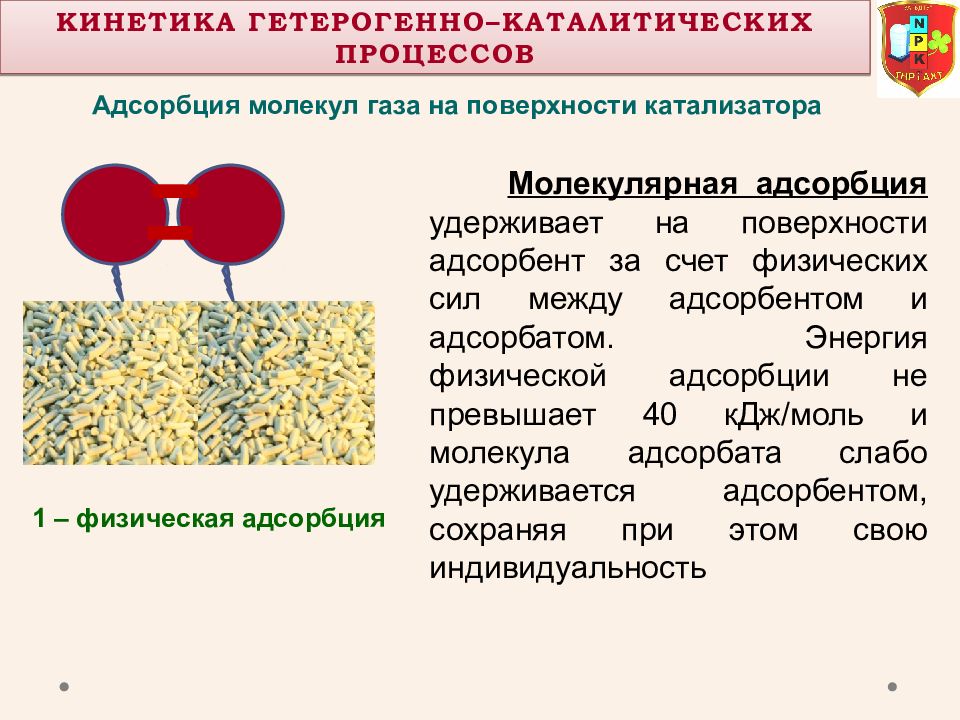
Адсорбция молекул газа на поверхности катализатора 1 – физическая адсорбция Кинетика Гетерогенно– КаталитическиХ процессОВ Молекулярная адсорбция удерживает на поверхности адсорбент за счет физических сил между адсорбентом и адсорбатом. Энергия физической адсорбции не превышает 40 кДж/моль и молекула адсорбата слабо удерживается адсорбентом, сохраняя при этом свою индивидуальность
Слайд 13
Адсорбция молекул газа на поверхности катализатора Кинетика Гетерогенно– КаталитическиХ процессОВ 2 – активированная адсорбция Активированная адсорбция – адсорбция, которая характеризуется наличием химического взаимодействия между адсорбентом и адсорбатом. Энергия связи – свыше 80 кДж/моль. Под воздействием поверхности адсорбента (катализатора) – активного центра – в молекуле газа-адсорбата происходят некоторые изменения, в частности, меняется геометрия молекулы, увеличивается длина связей между атомами, изменяются углы. Молекула ещё сохраняет свою индивидуальность, но за счет изменения геометрии меняются её свойства и она становится реакционоспособной.
Слайд 14
Адсорбция молекул газа на поверхности катализатора Кинетика Гетерогенно– КаталитическиХ процессОВ 3 - хемосорбция Хемосорбция – образование прочных химических связей между поверхностью адсорбента и адсорбатом. Энергия связи – свыше 100 кДж/моль. За счет взаимодействия с поверхностью адсорбента образуются стабильные химические соединения. При этом активность катализатора снижается, т.е. происходит отравление катализатора
Слайд 15
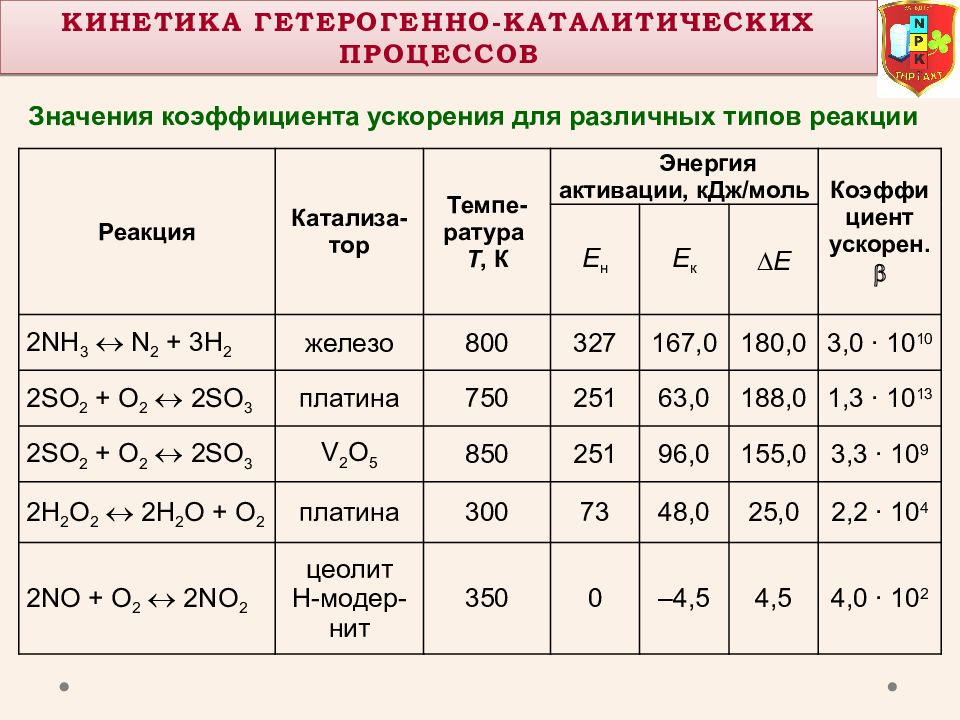
Реакция Катализа- тор Темпе- ратура Т, К Энергия активации, кДж/моль Коэффициент ускорен. Е н Е к Е 2NH 3 N 2 + 3H 2 железо 800 327 167,0 180,0 3,0 ∙ 10 10 2SO 2 + O 2 2SO 3 платина 750 251 63,0 188,0 1,3 ∙ 10 13 2SO 2 + O 2 2SO 3 V 2 О 5 850 251 96,0 155,0 3,3 ∙ 10 9 2H 2 O 2 2H 2 O + О 2 платина 300 73 48,0 25,0 2,2 ∙ 10 4 2NO + O 2 2NO 2 цеолит Н- модер - нит 350 0 –4,5 4,5 4,0 ∙ 10 2 Значения коэффициента ускорения для различных типов реакции Кинетика Гетерогенно- КаталитическиХ процессОВ
Слайд 16
Гетерогенно-Каталитические процессы Основные методы изготовления катализаторов: Осаждение гидроксидов или карбонатов из растворов их солей с последующим формованием и термообработкой контактной массы (осажденные катализаторы). Смешение порошкообразных каталитически активных веществ, промоторов, носителей и связующих с последующим прессованием и термообработкой (смешанные катализаторы). Сплавление нескольких оксидов с последующим восстановлением металлов из оксидов (плавленые катализаторы). Иногда после сплавления одно из веществ удаляют путем выщелачивания (скелетные катализаторы). Пропитка пористого носителя раствором, содержащим соли активных элементов, с их последующей сушкой и термообработкой (нанесенные катализаторы). Катализаторы выпускают в виде таблеток, колец, шариков, цилиндрических гранул, сеток и др.
Слайд 18
Гетерогенно–Каталитические процессы Катализатор процесса окисления орто-ксилола во фталевый ангидрид Катализатор разложения аммиака Катализаторы для процессов: риформинга, изомеризации, гидрокрекинга, гидрирования, гидродеалкилирования