Слайд 2
Тотығу-тотықсыздандырғыш реакциялары табиғатта және өндірісте кең таралған. Табиғатта бұл фотосинтез, тыныс алу, ашыту, ыдырау. Өнеркәсіпте олар металдарды, тыңайтқыштарды өндіру үшін қолданылады. Күнделікті өмірде жанармайды жағу, темірдің тозуы және т.б.
Слайд 4
ЦО 9.2.2.3 тотығу дәрежелерін табу қағидаларын білу және қолдану ЦО 9.2.2.4 тотығу және тотықсыздандыру процестері өзара байланысты екенін және біруақытта болатындығын түсіну
Слайд 5
Сабақтың мақсаты : Барлық оқушылар : « тотығу дәрежесі », « тотығудың тұрақты, айнымалы дәрежесі » ұғымын білуі тиіс ; т отығу дәрежелерін анықтау қағидаларын білуі керек ; бинарлы қосылыстар құру қағидатын және керісіншені, атаулары бойынша заттардың формулаларын құруды білуі қажет ;
Слайд 6: талқылауға арналған сұрақтар
Электрондарын жоғалтқан немесе қосып алған атомдар қандай бөлшектерге айналады ? Атом өзінің сыртқы бір немесе бірнеше электрондарын жоғалтқанда оң, ал сырттан электрон қосып алғанда теріс ионға айналады 2. Атомның электронды жоғалту(беру) процесі қалай аталады? Тоты ғу 3. Атомның электронды қосып алу процесі қалай аталады ? Тотықсыздану
Слайд 7
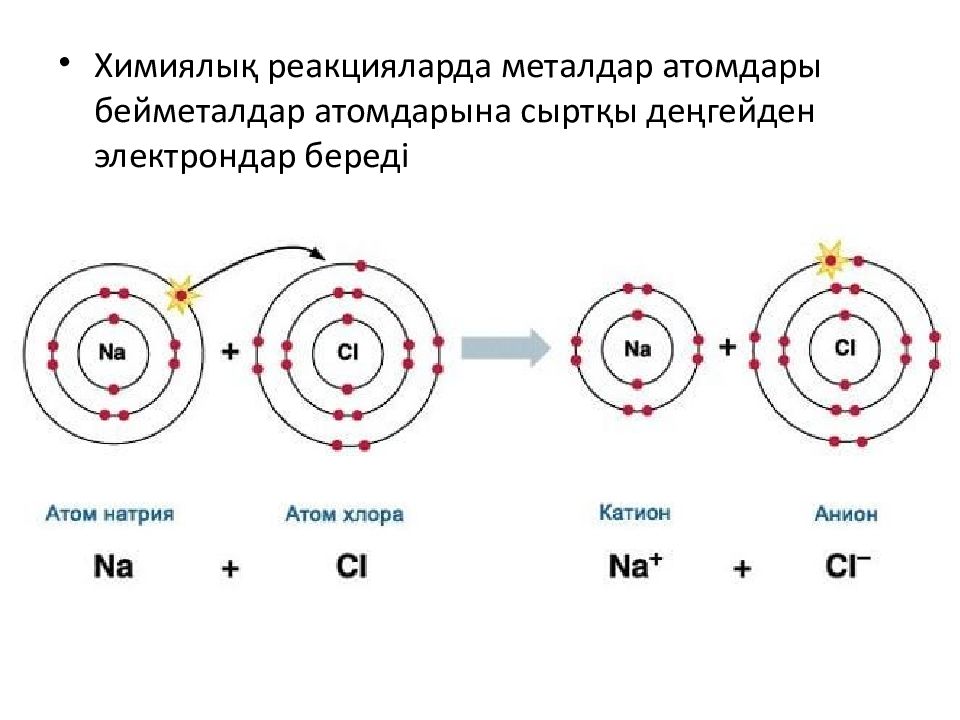
Химиялық реакцияларда металдар атомдары бейметалдар атомдарына сыртқы деңгейден электрондар береді
Слайд 9
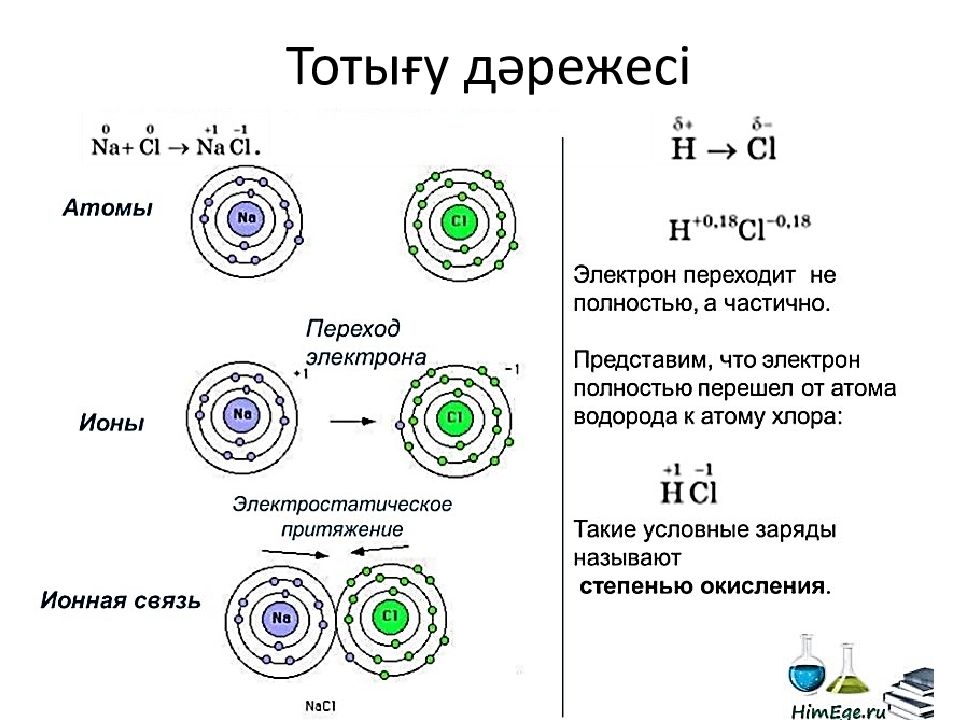
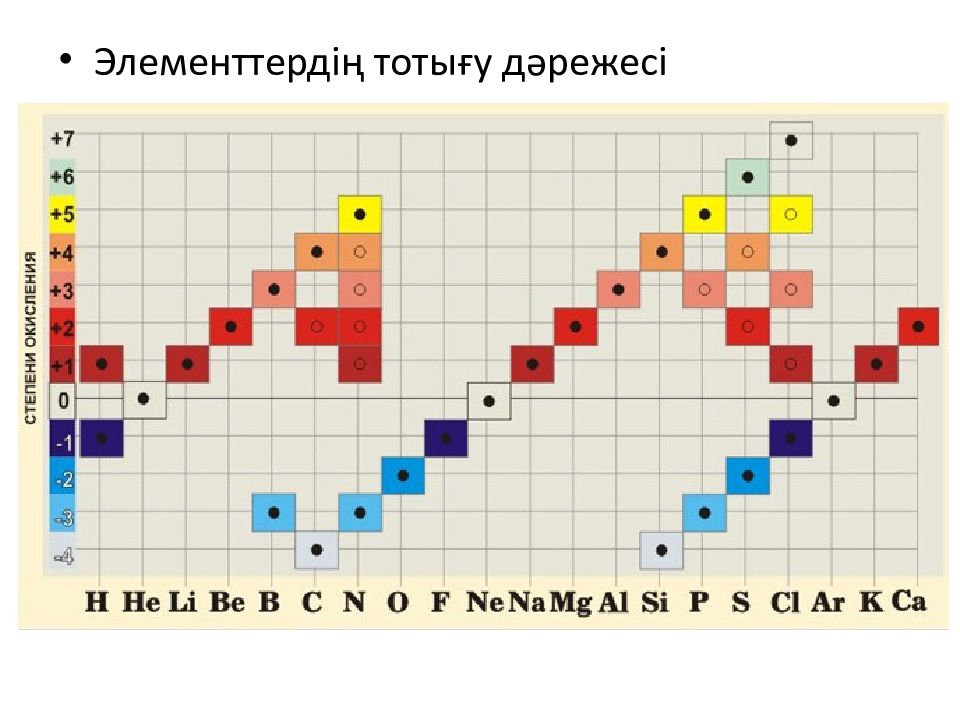
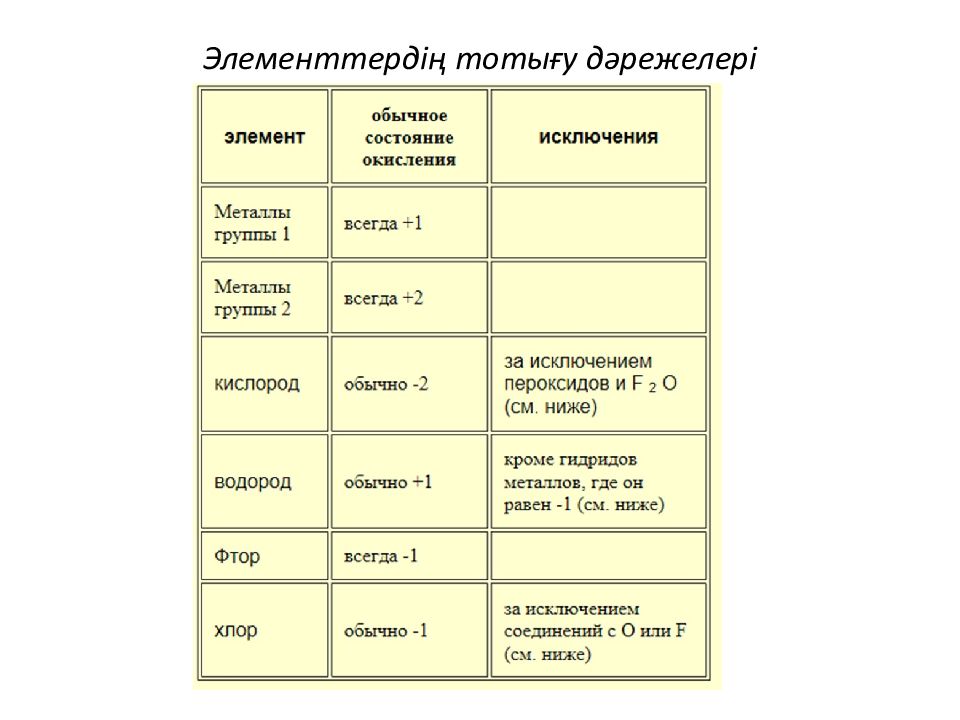
Элементтің тотығу дәрежесі дегеніміз оның шартты электрондық заряды. Атом немесе молекула әрқашан элекртобейтарап, себебі олар да оң таңбалар теріс таңбалар санымен теңеседі; Жай заттардың элементінің тотығу дәрежесі 0-ге тең; Na 0 ; O 0 ; Металдар катионы әрқашан оң зарядталады: Al 3+,Na +,Ca 2+ ; 2
Слайд 10
Химиялық қосылыста атомның тотығу дәрежесін анықтау үшін қажет : 1. Заттың формуласын жазыңыз : P 2 O 5 2. Оттегінің, сутекті немесе басқа тұрақты элементтің тотығу дәрежесінің мәндерін жазыңыз: x P 2 O −2 5 3. Тотығу д әрежелерінің сомасын қосып, мәнді есептеңіз. x: 2⋅x+5⋅(−2)=0 2x−10=0 2x=10x=+5 Фосфордың тотығу дәрежесі +5.
Слайд 12
Тотығу –тотықсыздану реакциялары ( ТТР ) - элементтердің атомдары тотығу күйінде өзгеріс болатын реакция. Тотығу — электрондарды беру процесі. Тотықсыздану – электрондарды қосып алу процесі.
Слайд 13: Есте сақтаңыздар !
Тотықсыздандырғыштар – тотығу дәрежесі жоғары элементтер : Н 2 S О 4, Н N О 3, KMnO 4, K 2 Cr 2 O 7 Cl 2 ( Cl – дейін ), O 2 ( H 2 O немесе OH – ), Br 2 ( Br – дейін ) Бейметалл ( F 2 ) Тотықтырғыштар – төмен тотықтыру күйлеріндегі элементтер. Ме 0 НЭ ( Н 2 S, NH 3, HCl СН 4 ) Барлық органикалық заттар. Тотықтырғыштар мен тотықсыздандырғыштар атомдардың аралық тотығу күйінде элементтер болып табылады.
Слайд 15
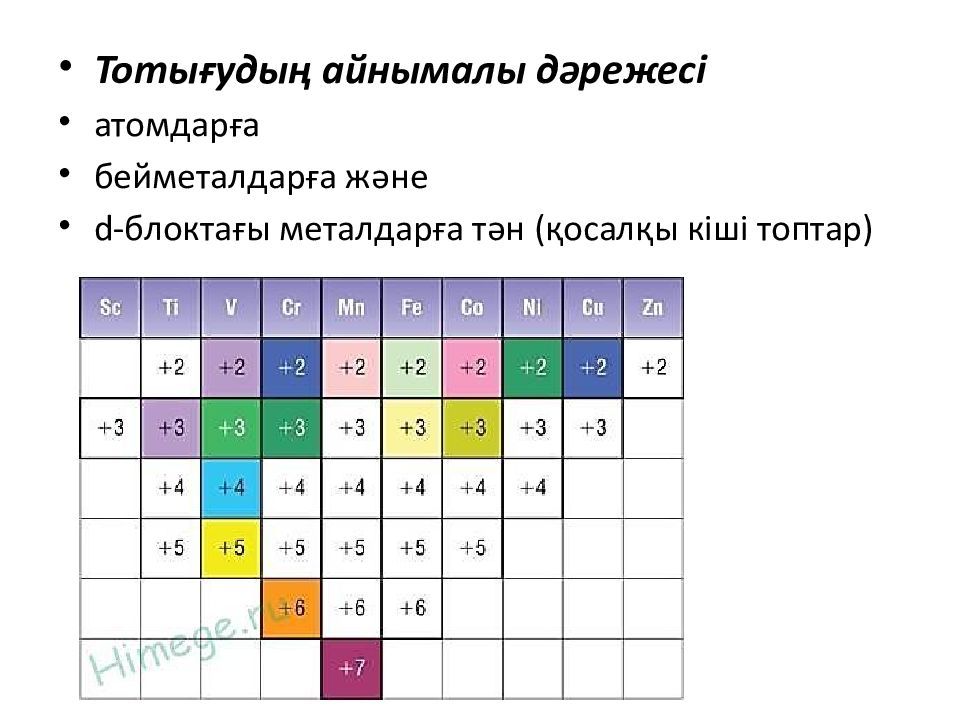
Тотығудың айнымалы дәрежесі атомдарға бейметалдарға және d- блоктағы металдарға тән ( қосалқы кіші топтар )
Слайд 17
1 -тапсырма. Мына қосылыстардағы тотығу дәрежесін анықтаңыз : Mg O Zn Cl 3 О 2 Fe 2 O 3 Ca S P 2 O 5 Si H 4 Na H