Первый слайд презентации: Химиялық реакцияның типтері Пән мұғалімі: Асылова Ляйла
« BAITEREK SCHOOL » ЖЕКЕ МЕКТЕБІ
Слайд 2: Топқа бөлу
4Al + 3O 2 ═ 2 Al 2 O 3 2KBr + H 2 SO 4 ═ K 2 SO 4 + 2HBr MgCl 2 +2AgNO 3 ═ Mg(NO 3 ) 2 + 2AgCl
Слайд 3
ХИМИЯЛЫҚ ДИКТАНТ 1 ) __________________ дегеніміз заттың құрамын химиялық элемент таңбалары және индекстері көмегімен жазу. 2) ______________ заттың құрамындағы элементтердің атом санын көрсетеді. 3) ____________________ заттың молекула санын көрсетеді. 4) Химиялық таңбалар мен формулаларды қолданып, заттардың өзара әрекеттесуін шартты түрде жазуды _______________________________________ деп айтамыз. 5) Химиялық реакциялардың теңдеулерін теңестіру барысында тек __________________ есептелініп қойылады. 6) Ал формулалардағы ______________________ өзгермейді, себебі заттың құрамын өз еркімізбен өзгерте алмаймыз. 7) Зат массасының сақталу заңын _________________ ашты. 8 ) Мына реакцияларды теңестір: а ) __ А l + __ S → Al 2 S 3 ә ) __ С r + __ O 2 → __ Cr 2 O 3 б ) __ LiOH + MgS → Li 2 S + Mg(OH) 2
Слайд 4
ХИМИЯЛЫҚ ДИКТАНТ 1 ) ХИМИЯЛЫҚ ФОРМУЛА дегеніміз заттың құрамын химиялық элемент таңбалары және индекстері көмегімен жазу. 2) ИНДЕКС заттың құрамындағы элементтердің атом санын көрсетеді. 3) КОЭФФИЦЕНТ заттың молекула санын көрсетеді. 4) Химиялық таңбалар мен формулаларды қолданып, заттардың өзара әрекеттесуін шартты түрде жазуды ХИМИЯЛЫҚ ТЕҢДЕУ деп айтамыз. 5) Химиялық реакциялардың теңдеулерін теңестіру барысында тек КОЭФФИЦЕНТ есептелініп қойылады. 6) Ал формулалардағы ИНДЕКСТЕР өзгермейді, себебі заттың құрамын өз еркімізбен өзгерте алмаймыз. 7) Зат массасының сақталу заңын М.В. ЛОМОНОСОВ ашты. 8 ) Мына реакцияларды теңестір: а) 2 А l + 3 S → Al 2 S 3 ә ) 4 С r + 6 O 2 → 2 Cr 2 O 3 б ) 2 LiOH + MgS → Li 2 S + Mg(OH) 2
Слайд 6: Сабақтың мақсаты :
8.2.2.1 -бастапқы және түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктеу
Слайд 7
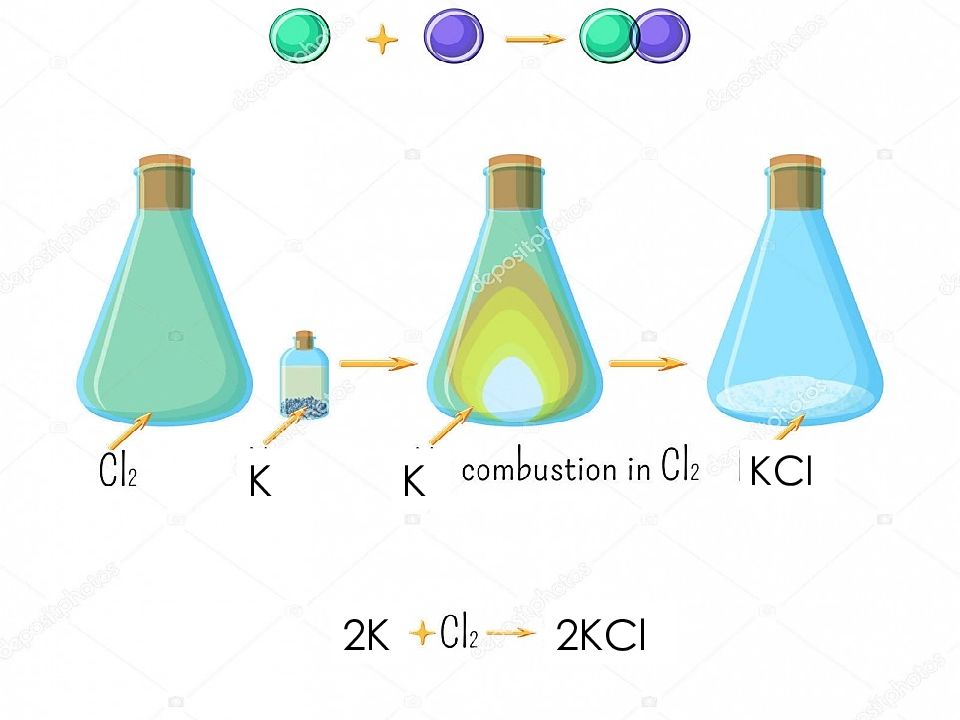
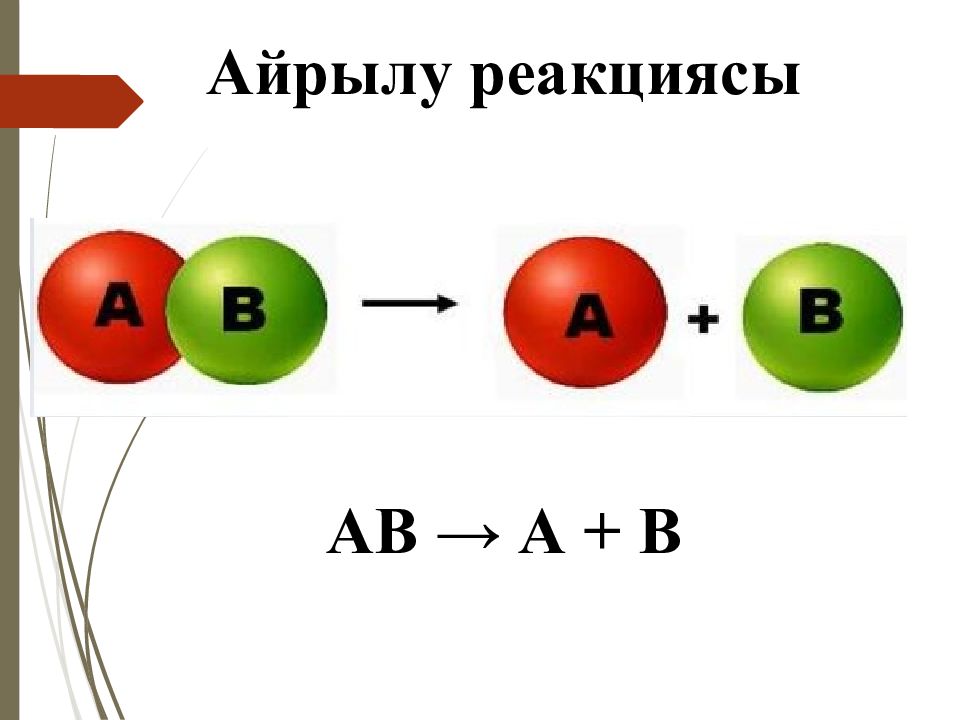
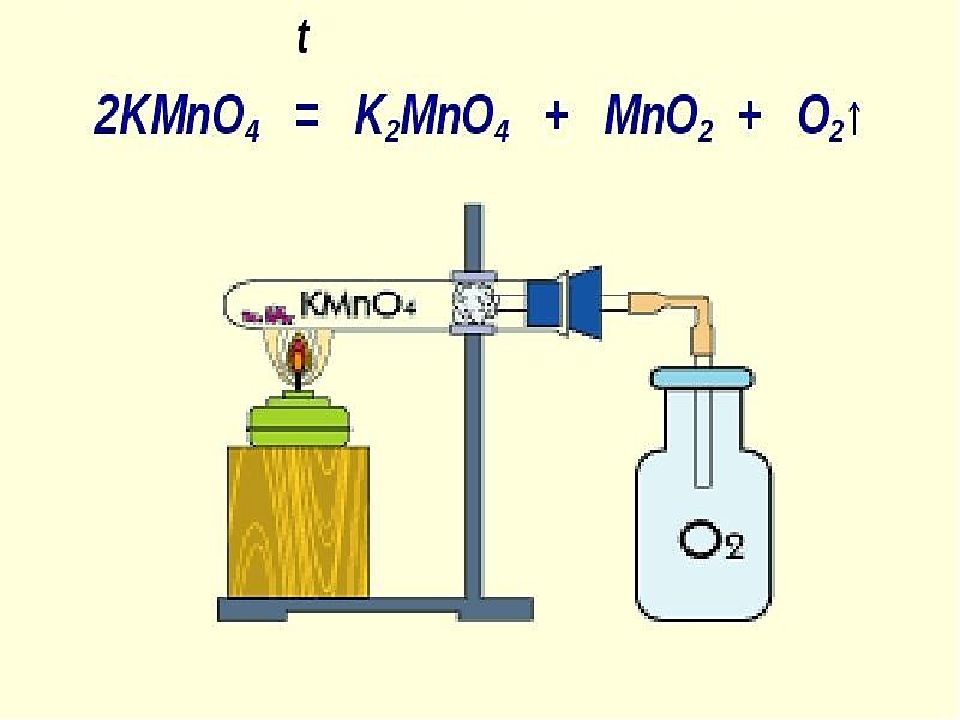
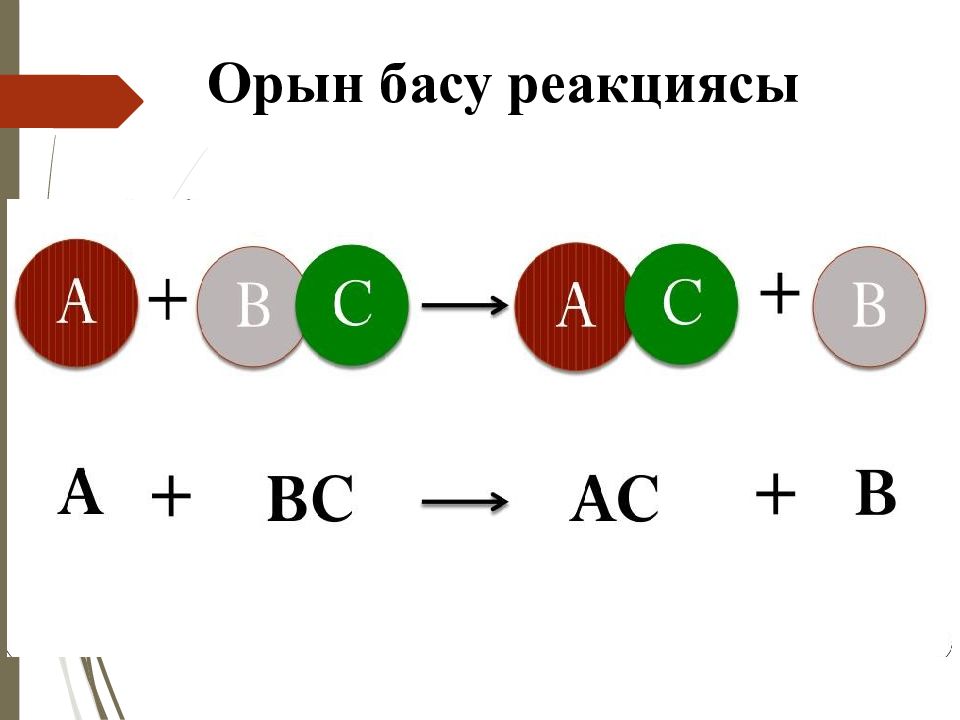
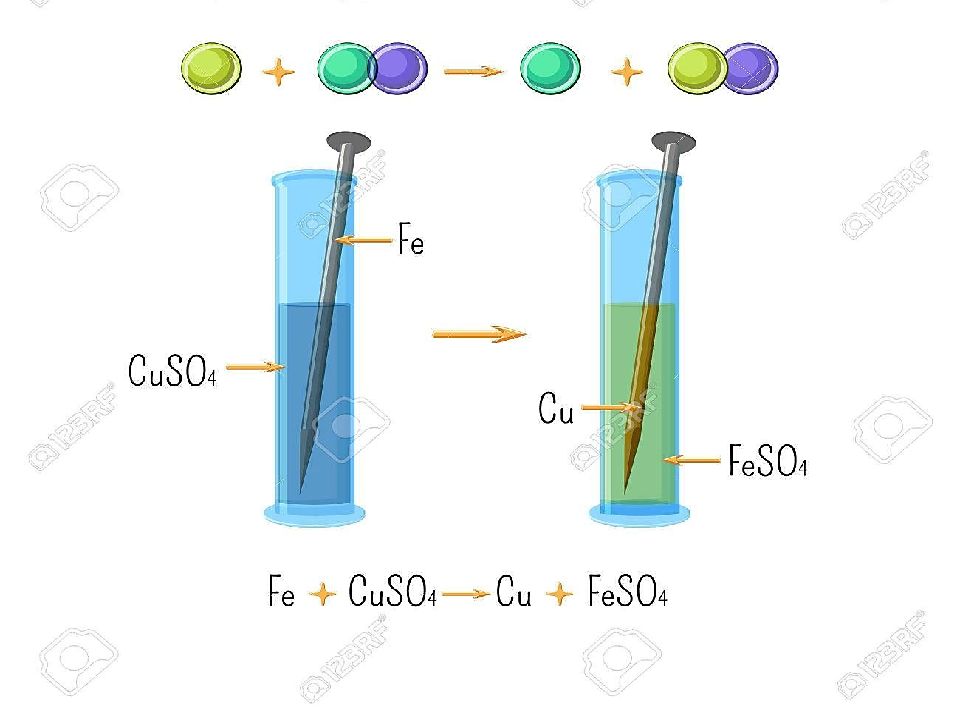
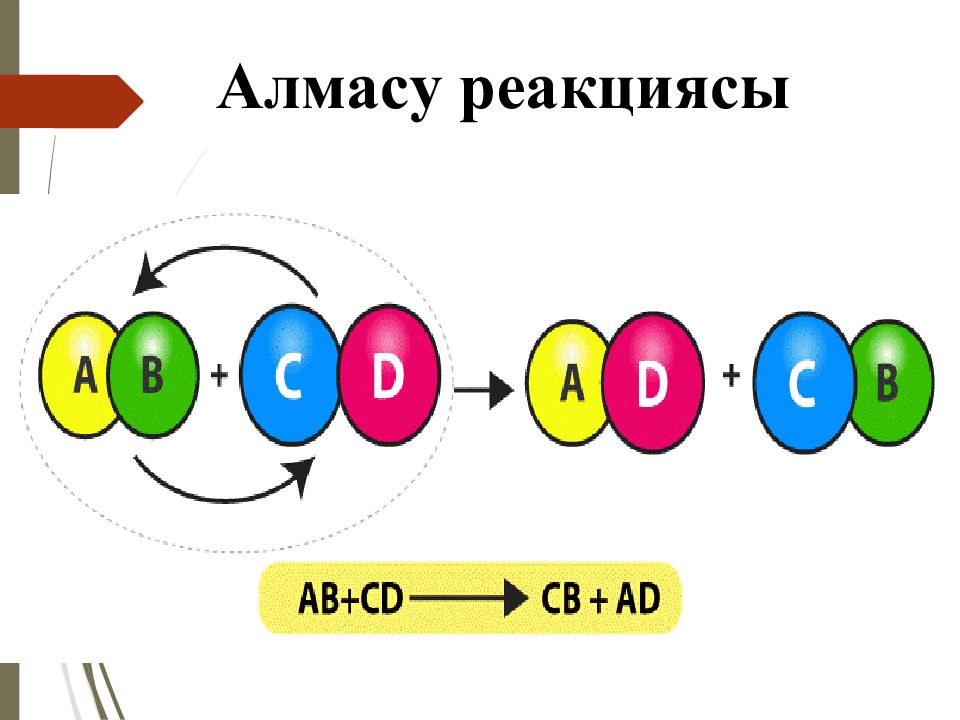
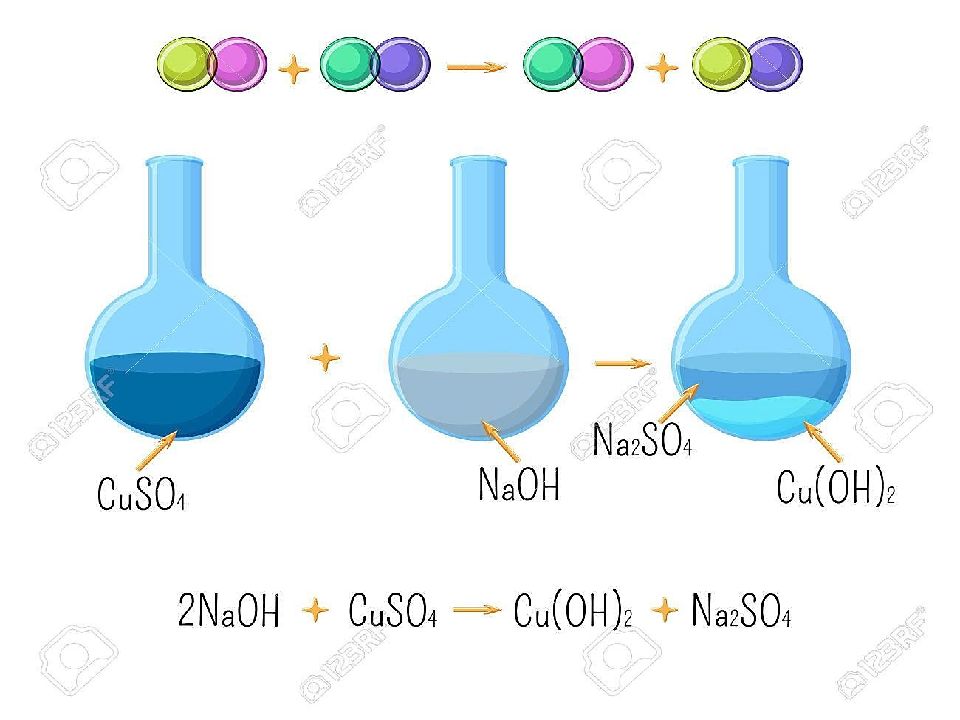
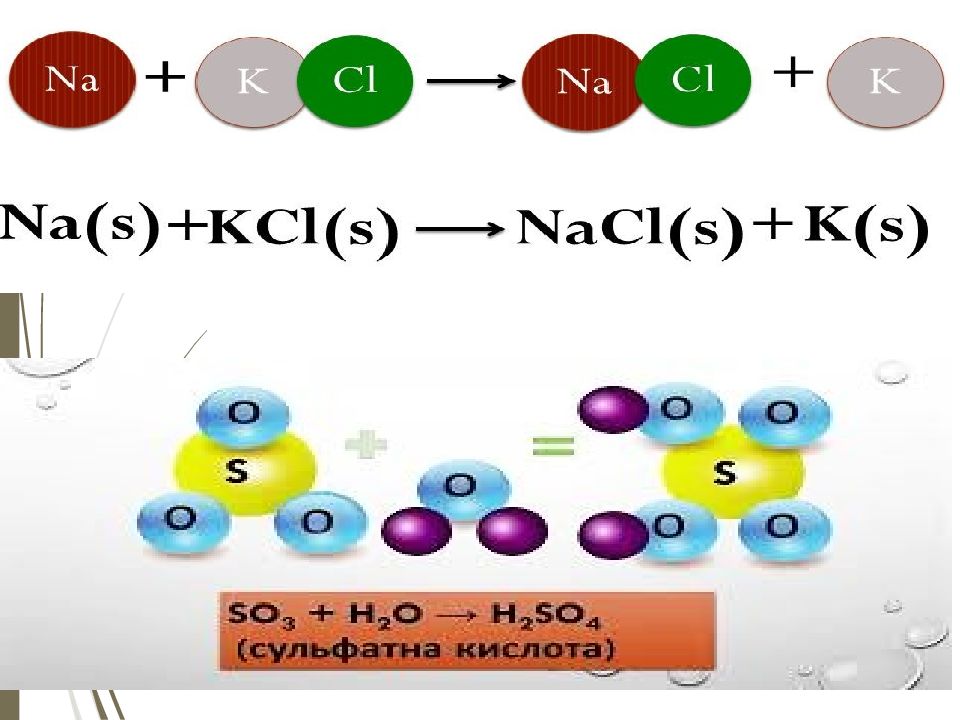
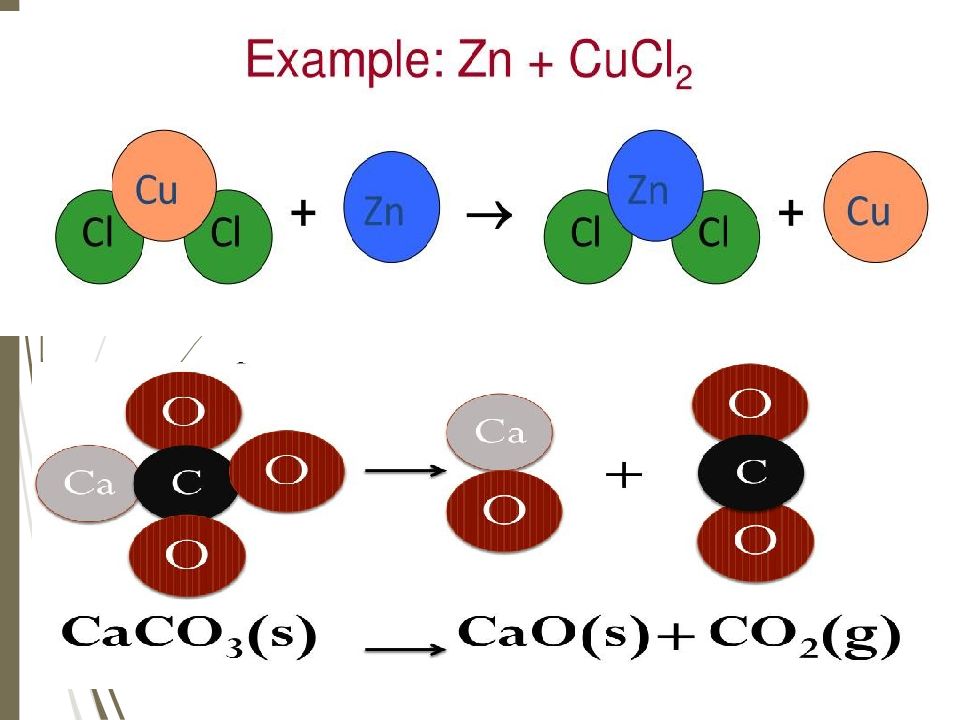
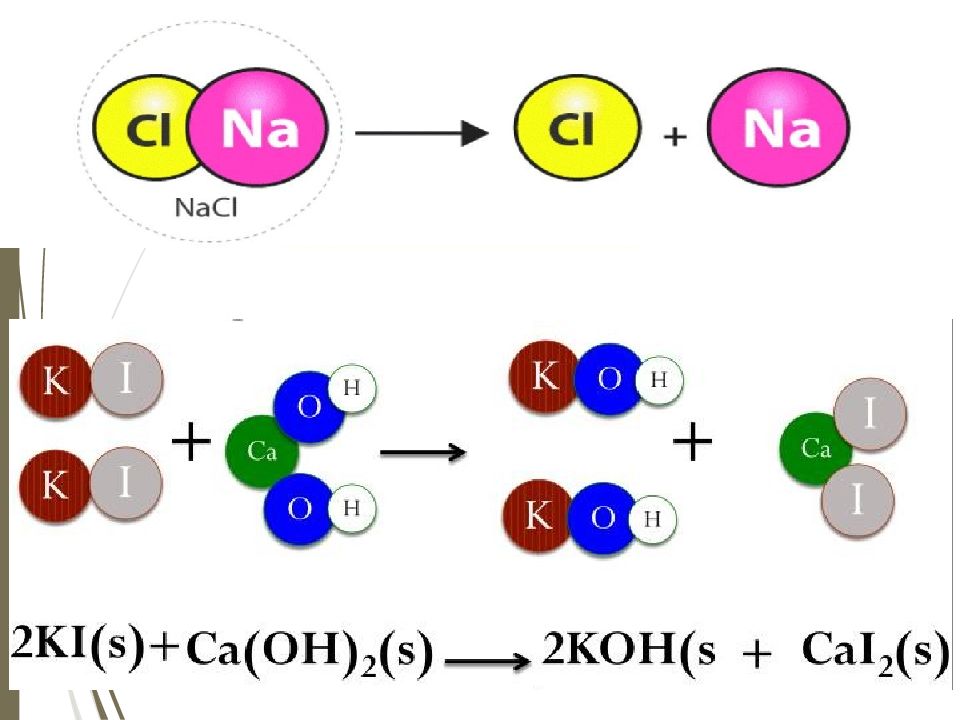
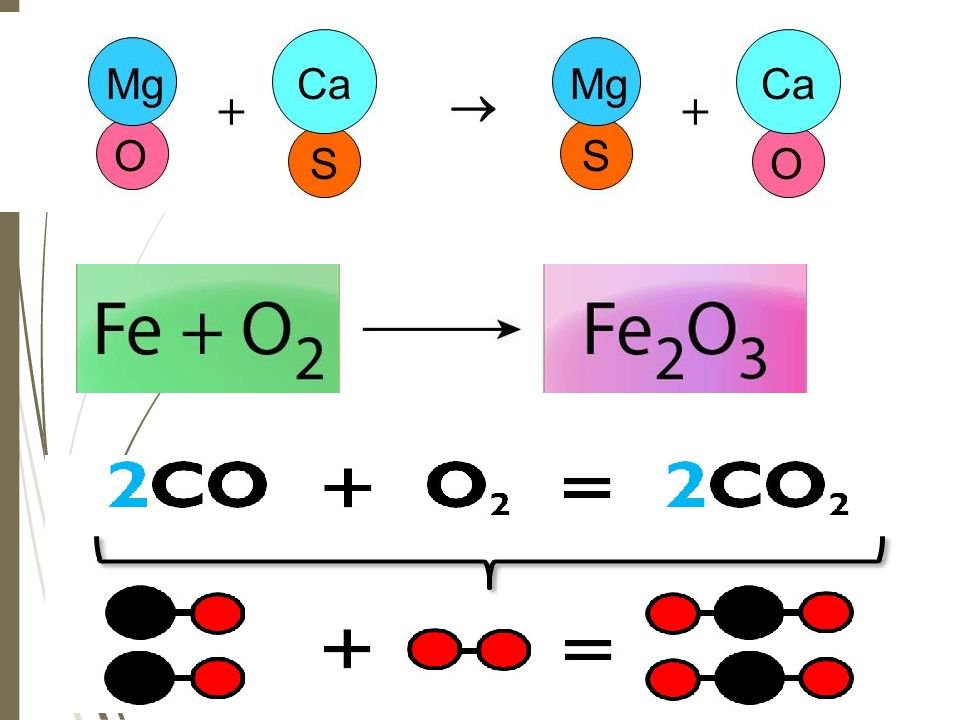
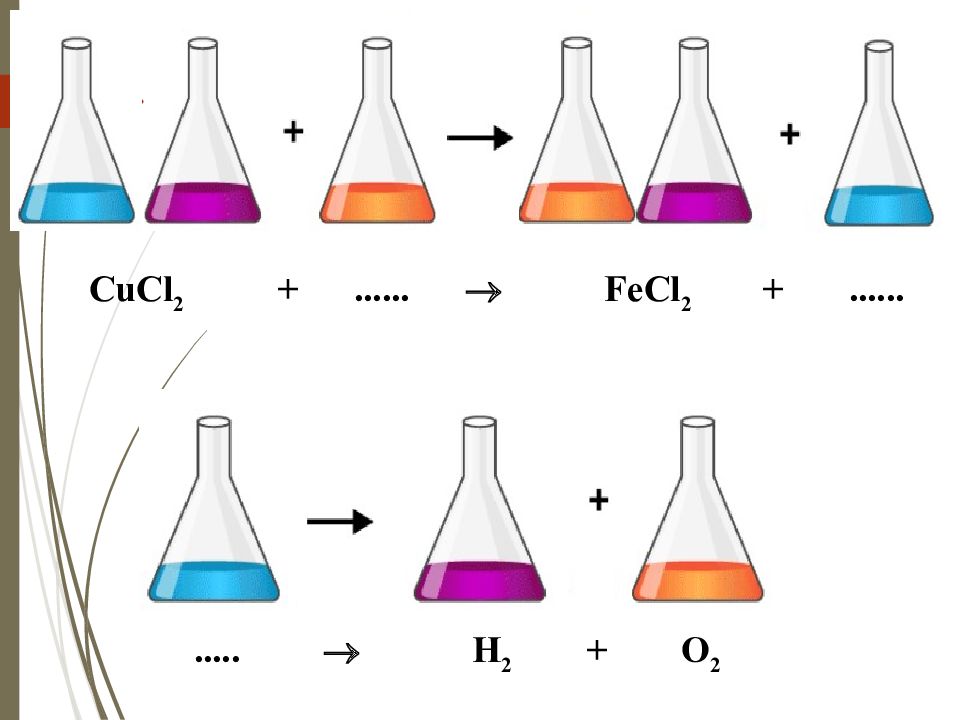
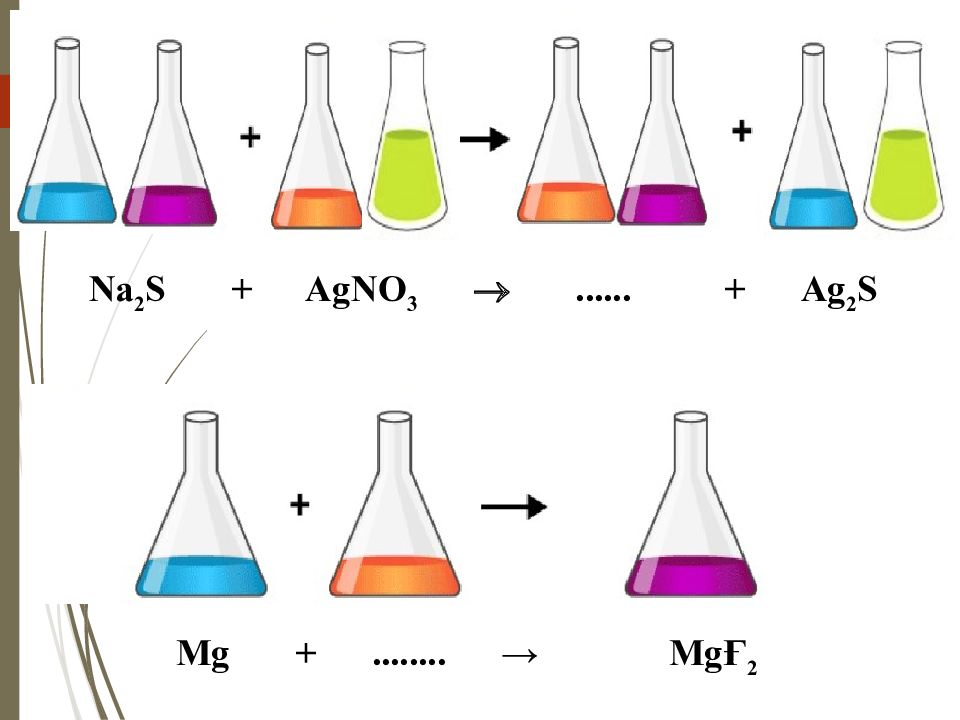
Химиялық реакцияның 4 типі бар: Қосылу реакциясы Айрылу реакциясы Орынбасу реакциясы Алмасу реакциясы
Слайд 16: Инсерт» Берілген мәтінді «Түртіп алу» әдісі арқылы танысып шығу
V білемін - мен үшін түсініксіз + мен үшін жаңа ақпарат ? мені таңғал-дырды
Слайд 17
Натрий мен хлор туралы ертегі Натрийді ешкім жақсы көрмейтін. Ол улы болды. Оның тотығу дәрежесі +1. Натрий мұхитта болды, бірақ та егер ол таза күйінде болса суға күшті әсер ететін. Хлорды да ешкім ұнатпайтын. Ол да улы, түсі де сарғылт жасыл болатын. Тотығу дәрежесі -1 және одан жоғары. Адамдар онымен араласқанда көздерін күйдіріп, тыныс алуы қиындап кететін. Натрий мен хлор өздеріне тең жұпты таба алмаспыз деп, екеуі үйленеді. Сөйтіп, олардың отбасында натрий хлориді пайда болады. Көбісі олардың қызын Ас тұзы деп атады. Қазір бұл өнім адамдар үшін өте маңызды болды. Өйткені, тұздағы хлор ионынан тұз қышқылын алады, ал натрий иондары басқа элементтер иондарымен бірге жүйке импульстерін өткізуге қатысады.
Слайд 31
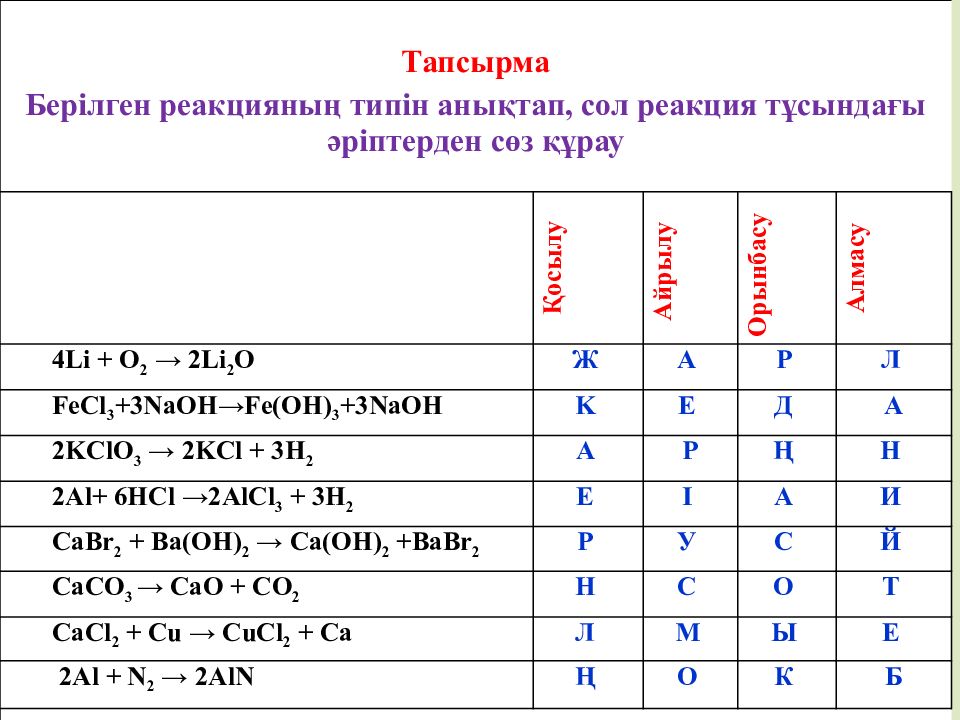
Тапсырма Берілген реакцияның типін анықтап, сол реакция тұсындағы әріптерден сөз құрау Қосылу Айрылу Орынбасу Алмасу 4Li + O 2 → 2Li 2 O Ж А P Л FeCl 3 +3NaOH→Fe(OH) 3 +3NaOH K Е Д А 2KClO 3 → 2KCl + 3H 2 A Р Ң Н 2 Al+ 6 HCl → 2 AlCl 3 + 3 H 2 Е І А И Ca Br 2 + Ba( O H) 2 → Ca (OH) 2 + BaBr 2 Р У С Й CaCO 3 → CaO + CO 2 H С О Т Ca С l 2 + Cu → CuCl 2 + Ca Л М Ы E 2Al + N 2 → 2AlN Ң О К Б