Первый слайд презентации
Внутренняя энергия. Теплопередача. Работа в термодинамике
Слайд 2: Термодинамика-
теория тепловых процессов, в которой не учитывается молекулярное строение тел.
Слайд 3: Одноатомный газ -
газ, состоящий из отдельных атомов, а не молекул( идеальный газ ). Одноатомными являются инертные газы- гелий, неон, аргон и др.
Слайд 5
Внутренняя энергия тела равна сумме кинетической энергии движения молекул и потенциальной энергии взаимодействия молекул. 2. Внутренняя энергия зависит от температуры и от количества частиц. Обозначается U, измеряется в Дж. 3. Т.к. потенциальная энергия идеального газа равна 0, то Выведем формулу для расчета внутренней энергии одноатомного идеального газа :
Слайд 7
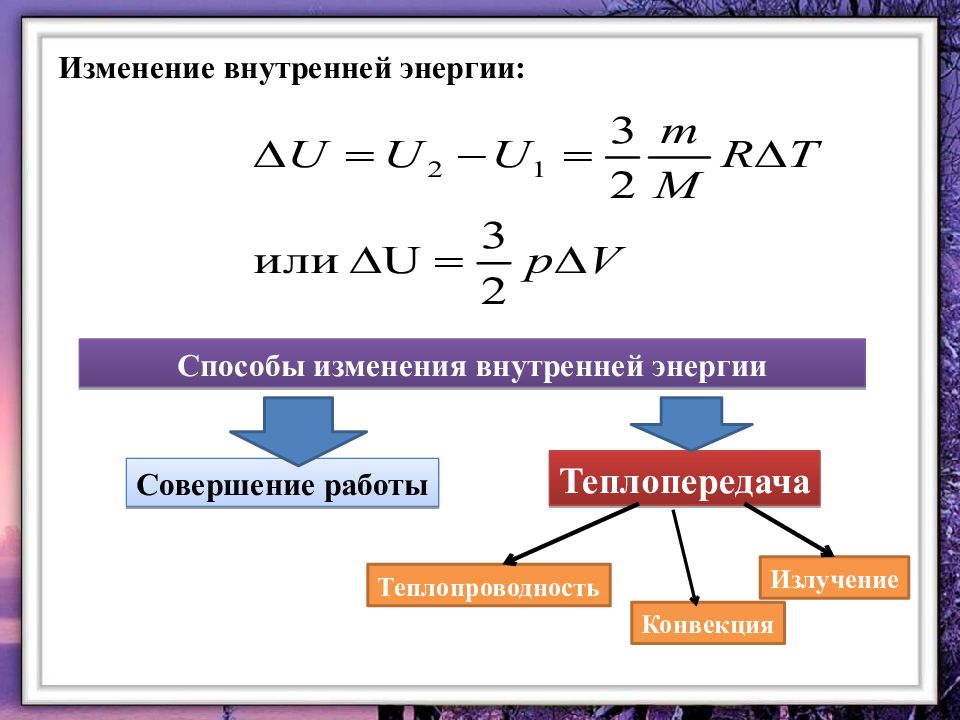
Изменение внутренней энергии: Способы изменения внутренней энергии Совершение работы Теплопередача Теплопроводность Конвекция Излучение
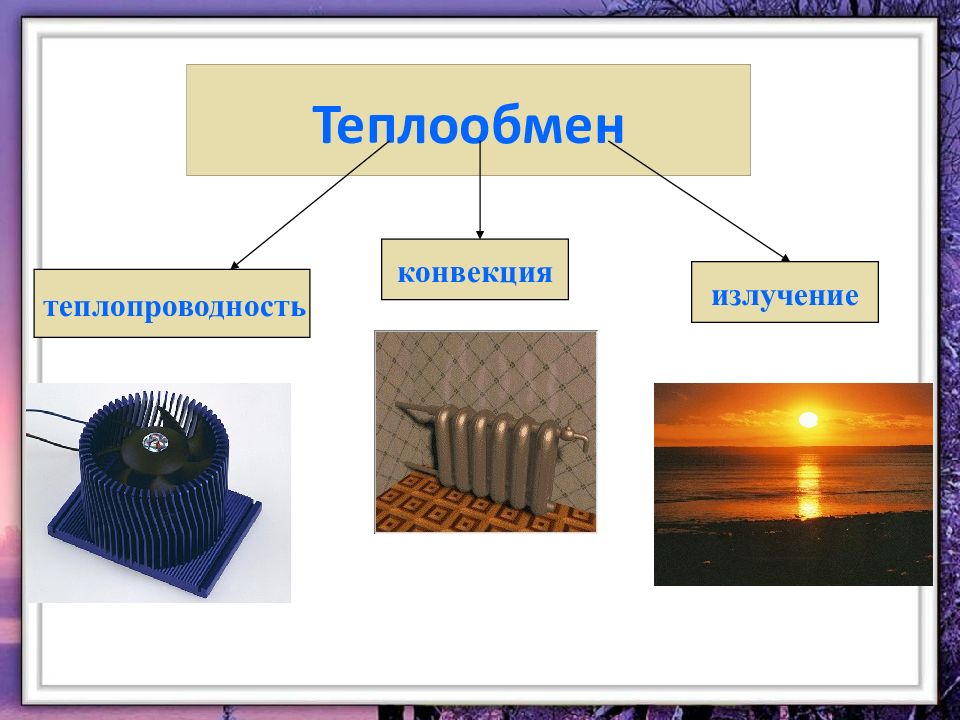
Слайд 9: Теплопроводность
- это такой тип теплообмена, когда тепло передаётся от более нагретых участков тела менее нагретым вследствие теплового движения молекул. Все вещества имеют различную теплопроводность. Лучшие проводники тепла – кристаллы. Те вещества, в которых расстояния между молекулами большие – плохие проводники тепла. Это древесина, кирпич и т.д.
Слайд 10: Конвекция
- это такой тип теплообмена, при котором энергия переносится струями жидкости или газа. Плотность горячего газа или жидкости меньше, чем холодных, поэтому конвекционные потоки поднимаются вверх.
Слайд 11: Лучистый обмен или просто излучение
это перенос энергии в виде электромагнитных волн. Любое нагретое тело является источником излучения. Этот вид теплообмена отличается от предыдущих тем, что может происходить и в вакууме.
Слайд 12
Количество теплоты, Q – это энергия, переданная системе или полученная системой при теплообмене. Процесс Формула, удельные величины Нагревание или охлаждение c- удельная теплоемкость, Дж/(кг*К) m – масса, кг; - изменение температуры, К Кипение или конденсация Q= rm r– удельная теплота парообразования, Дж/кг Плавление или кристаллизация Q= λ m λ – удельная теплота плавления, Дж/кг Сгорание топлива Q= qm q – удельная теплота сгорания, Дж/кг Уравнение теплового баланса:
Слайд 15
Работа в термодинамике – работа сил, приложенных к внешним телам со стороны системы при её деформации. Работа газа численно равна площади фигуры под графиком зависимости давления от объёма в координатах p, V 2 A>0 p V 1 A<0 p V 1 2 p Расширение газа Сжатие газа
Слайд 16
Задача №1. В стальном баллоне находится гелий массой 0,5 кг при температуре 10°С. Как изменится внутренняя энергия гелия, если его температура повысится до 30°С? Дано: Решение: Ответ. 31,2 кДж
Последний слайд презентации: Внутренняя энергия. Теплопередача. Работа в термодинамике
Задачи (самостоятельно ): Определите изменение внутренней энергии кислорода ( ) массой 3 кг при изменении его температуры от 17 º С до 27 º С. 2. Газ, расширяясь изобарно, совершает работу 0,2 кДж при давлении 200 кПа. Определите первоначальный объём газа, если конечный объём стал равен 2,5 л.