Первый слайд презентации: 4.4. Темновая стадия фотосинтеза
Цель: изучить темновую стадию фотосинтеза, механизмы С 3 -, С 4 -пути фотосинтеза и САМ-фотосинтеза, фотодыхания, пути повышения продуктивности фотосинтеза. Вопросы для рассмотрения. С 3 -путь фотосинтеза (цикл Кальвина), его механизмы. Фотодыхание, его биологическое значение. С 4 -путь фотосинтеза. Особенности САМ-фотосинтеза. Продукты фотосинтеза. Пути повышения продуктивности фотосинтеза.
Слайд 2: Темновая фаза фотосинтеза —
это совокупность биохимических реакций, в результате которых происходит усвоение растениями углекислого газа атмосферы (СО 2 ) и образование углеводов. Ферменты, катализирующие темновые реакции растворены в строме.
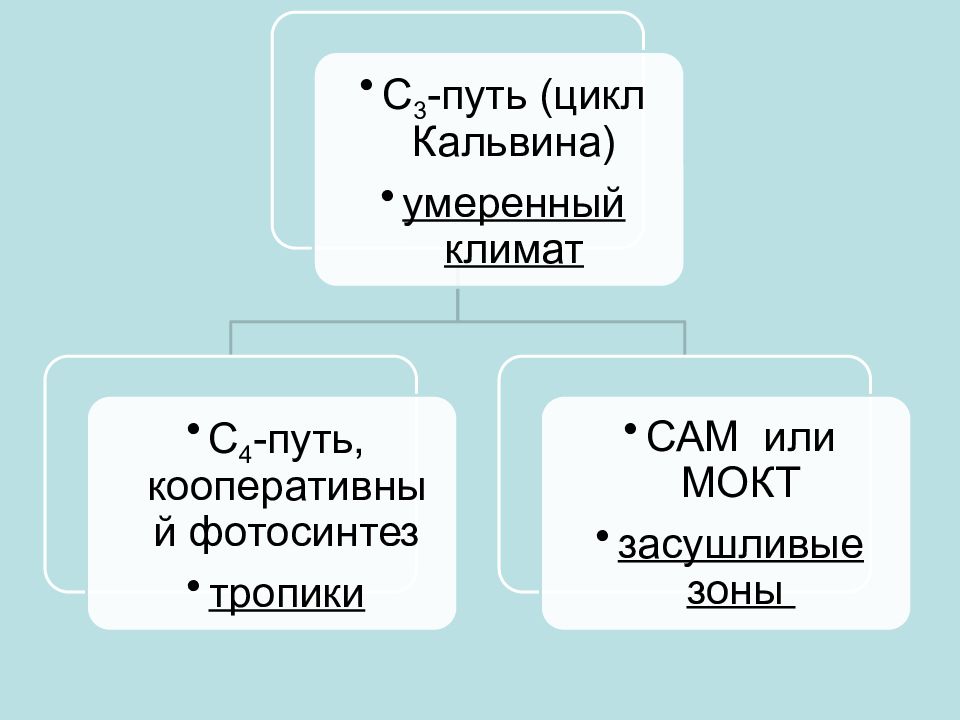
Слайд 4: Отличие темновой стадии у С 3 от С 4 и САМ-растений — С 3 + доп. реакции превращения СО 2 :
временем суток, когда эти реакции происходят, в каких клетках находятся вещества, участвующие в этих реакциях.
Слайд 5
Сущность темновых реакций процесса фотосинтеза была раскрыта: Мельвином Кальвином (Нобелевская премия в 1961г.) с сотрудниками, Бэнсоном, Басхэмом.
Слайд 6: Вопросы, которые поставили и на которые ответили Кальвин и его сотрудники :
какова природа соединения, являющегося первичным акцептором СО 2, какой продукт образуется непосредственно при фиксации СО 2, как этот продукт затем превращается в простые сахара?
Слайд 7: Обстоятельства, способствовавшие успеху эксперимента М. Кальвина:
впервые применили метод меченных атомов (С 14 О 2 ), хроматографический метод разделения продуктов фотосинтеза при коротких экспозициях (освещение 1 с и более), использовали однородный материал – хлореллу. Растения,на которых производили эксперимент— ячмень и шпинат.
Слайд 8: Лоуренсовская лаборатория ( Калифорния, США ) 1946 – 1956 Мелвин Кальвин
Объект: Chlorella Методы: С (14), P(32), Двумерная хроматография
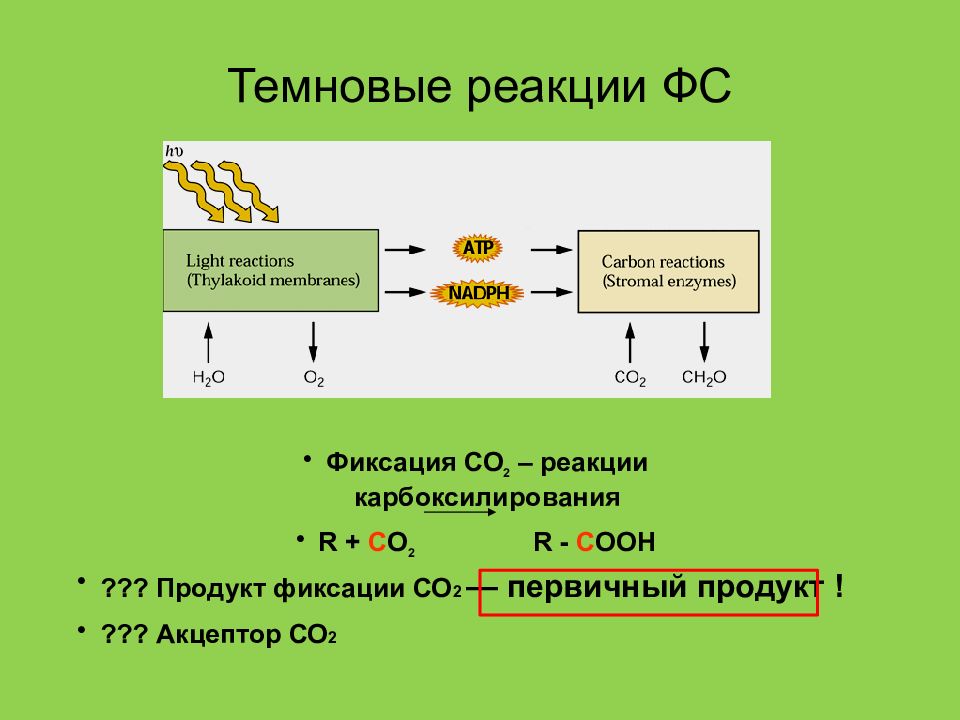
Слайд 9: Темновые реакции ФС
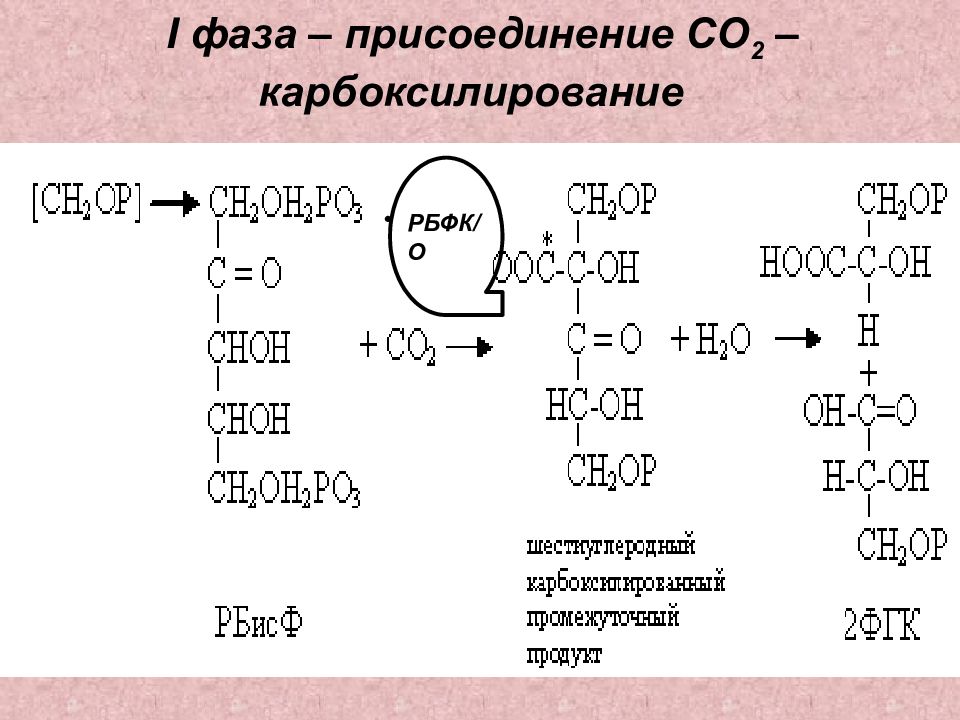
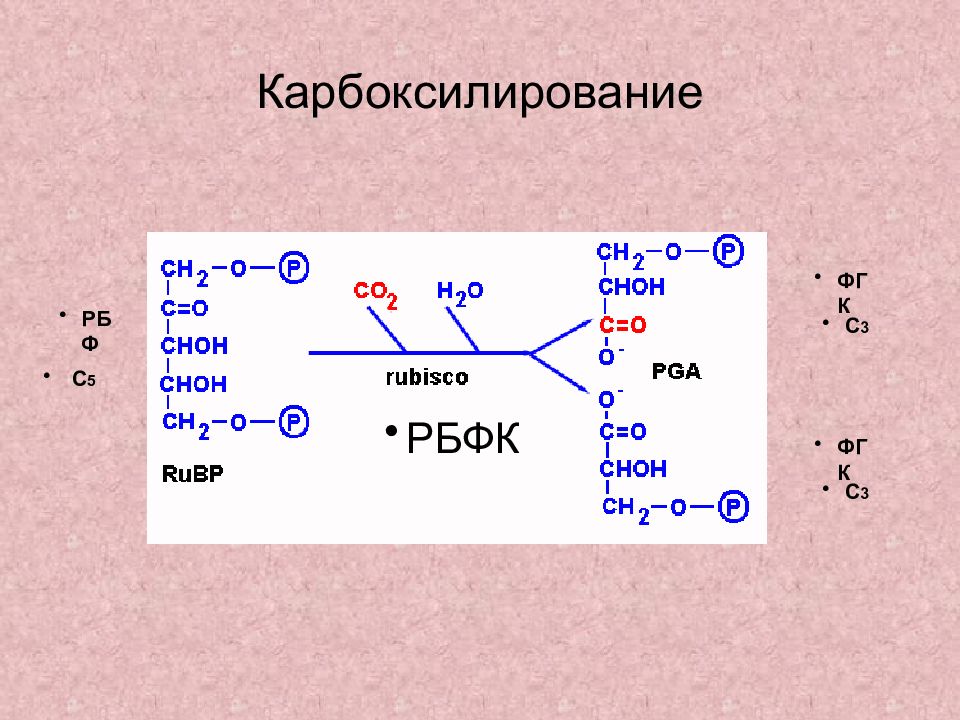
Фиксация СО 2 – реакции карбоксилирования R + C O 2 R - C OOH ??? Продукт фиксации СО 2 — первичный продукт ! ??? Акцептор СО 2
Слайд 10: Зависимость времени инкубации в С 14 О 2 и содержания С 14 -меченых соединений:
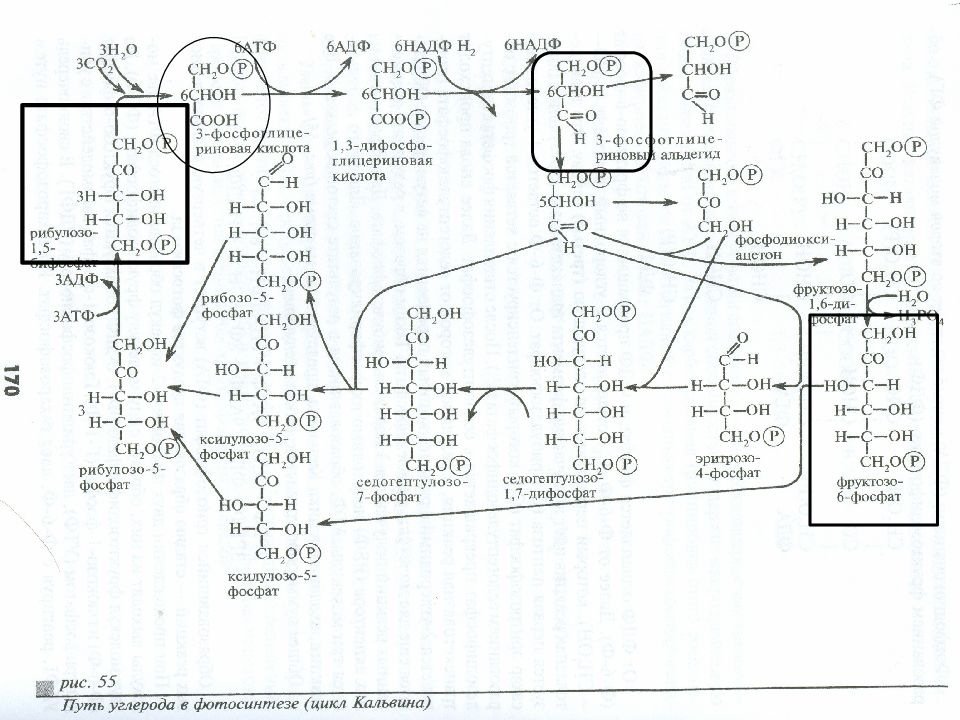
если время экспозиции было 10 мин., то на хроматографии обнаруживается большой набор различных меченых соединений, в том числе простые углеводы (фосфорилированные сахара), некоторые аминокислоты, все основные нуклеотиды и другие соединения; при 30 с экспозиции набор веществ получался меньший – фосфорилированные углеводы – соединения цикла Кальвина – триозы (ФГК, ФГА, ФДА), тетрозы (эритрозо-4-фосфат), пентозы (рибозо-5-фосфат, рибулозо-5-фосфат, рибулозо-1,5-бисфосфат, ксилулозо-5-фосфат), гексозы (фруктозо-1,6-бисфосфат, фруктозо-6-фосфат, глюкозо-6-фосфат), гептозы (седогептулозо-1,7-бисфосфат, седогептулозо-7-фосфат). доли с – одно соединение – фосфоглицериновая кислота ( ФГК ) – трехуглеродное соединение.
Слайд 11: Можно было предположить, что первичным акцептором должно быть С 2 -соединение (С 2 +СО 2 С 3 )
Но Кальвин и сотр. показали – акцепторная молекула – рибулозо-1,5-бисфосфат – С 5 -соединение, т.е. первоначальный процесс соответствует схеме – С 5 +СО 2 2С 3.
Слайд 12: Взаимосвязь акцептор продукт является циклической
Клеточный уровень меченного РБФ снижается в темноте, а уровень ФГК —повышается.
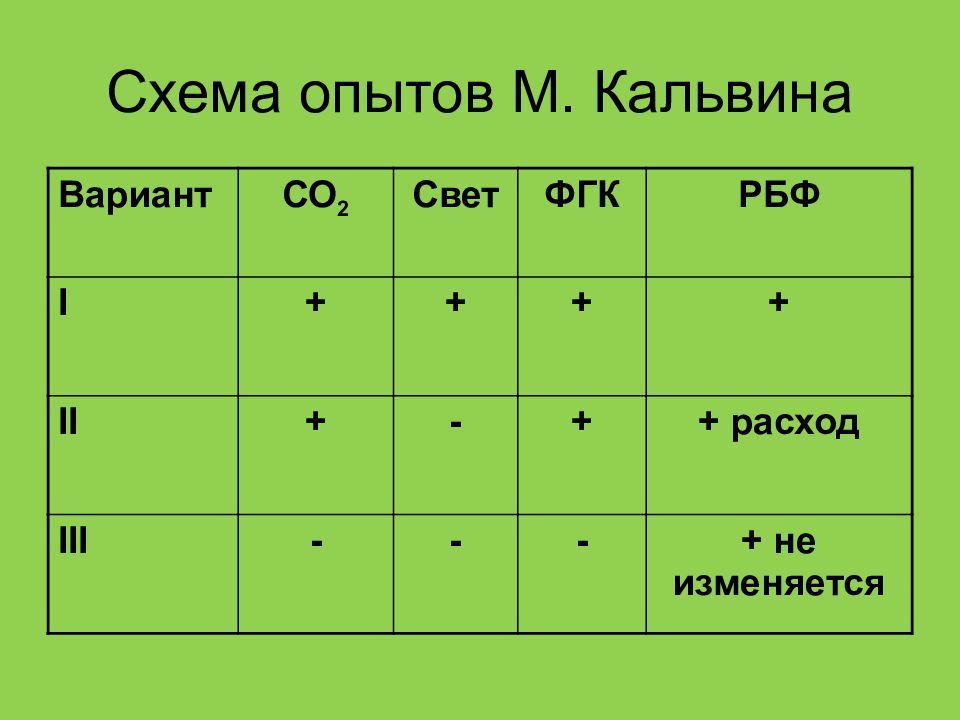
Слайд 13: Схема опытов М. Кальвина
Вариант СО 2 Свет ФГК РБФ I + + + + II + - + + расход III - - - + не изменяется
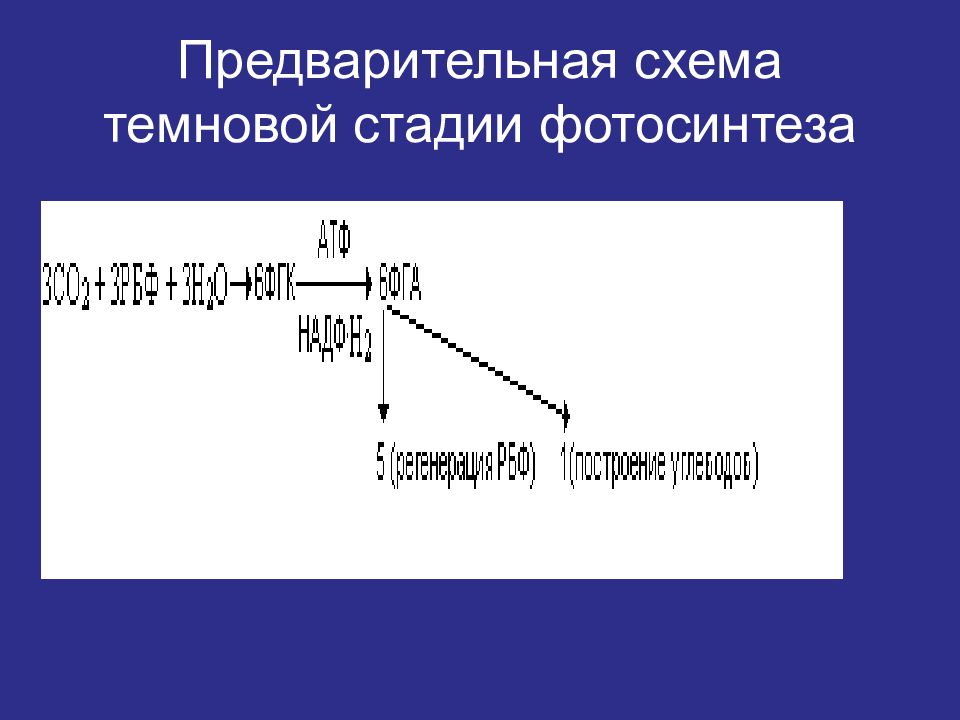
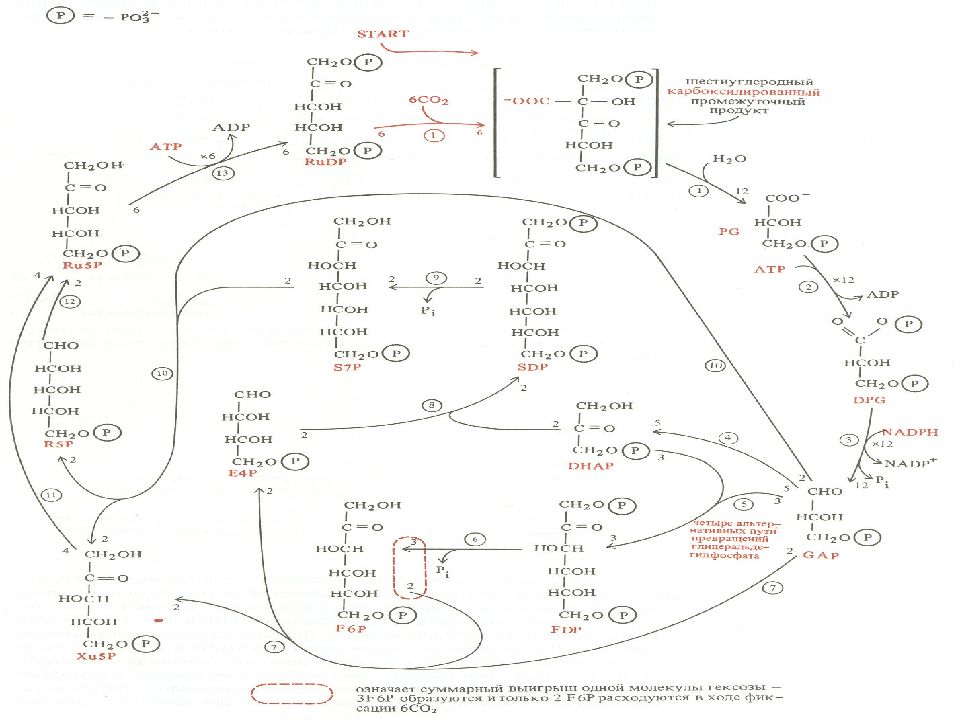
Слайд 14: Цикл можно разделить на 3 фазы:
карбоксилирование (+СО 2 ), восстановление (СО 2 до органических веществ), регенерация (акцепторов).
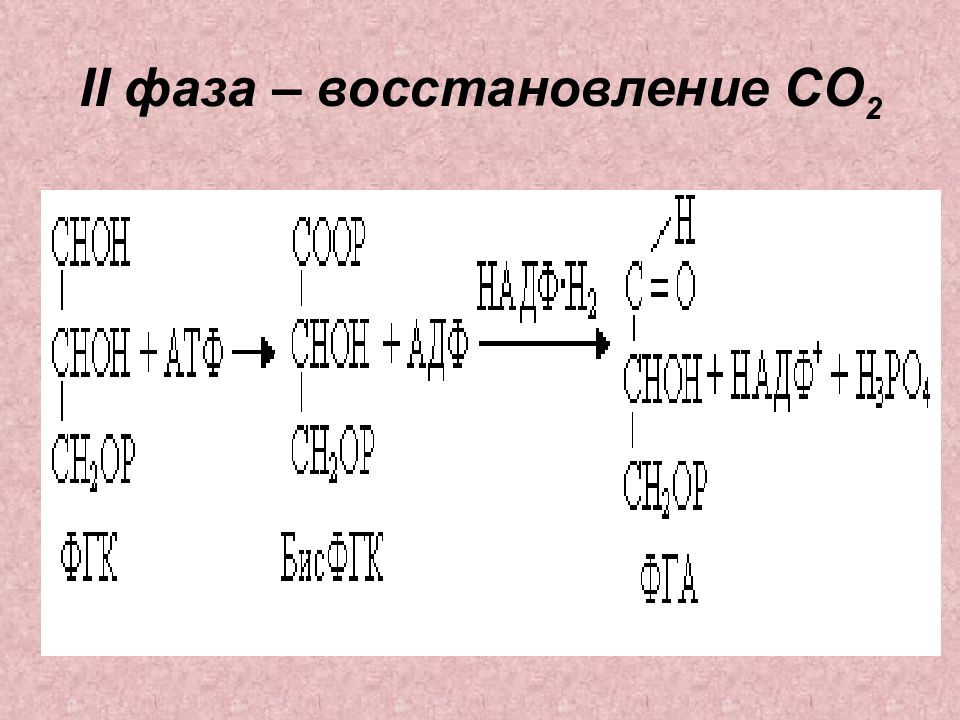
Слайд 22: II фаза – восстановление СО 2
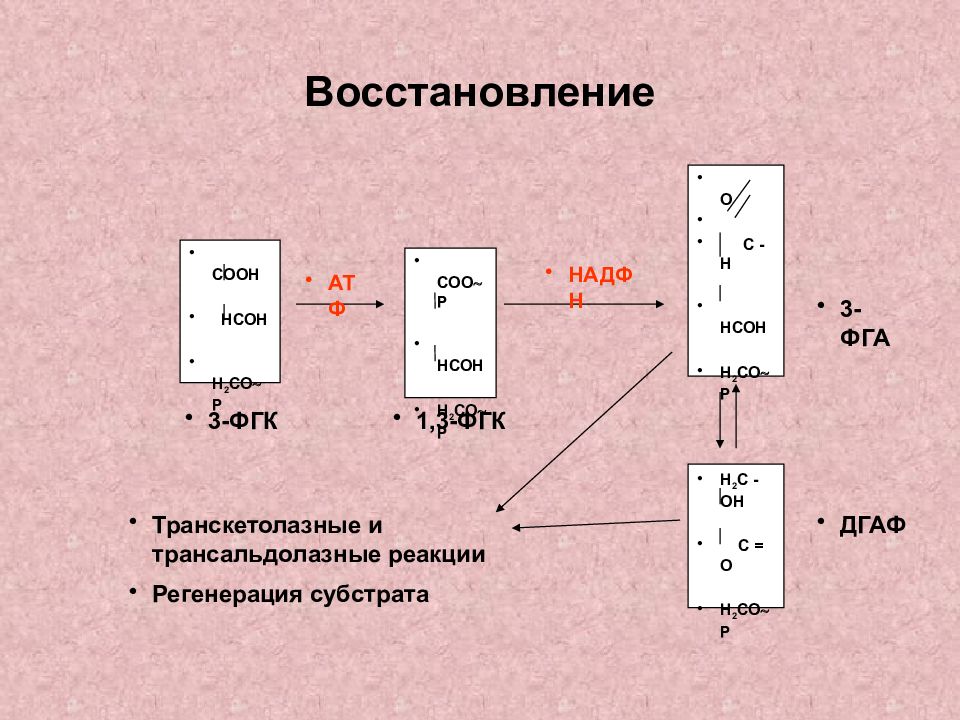
Слайд 23: Восстановление
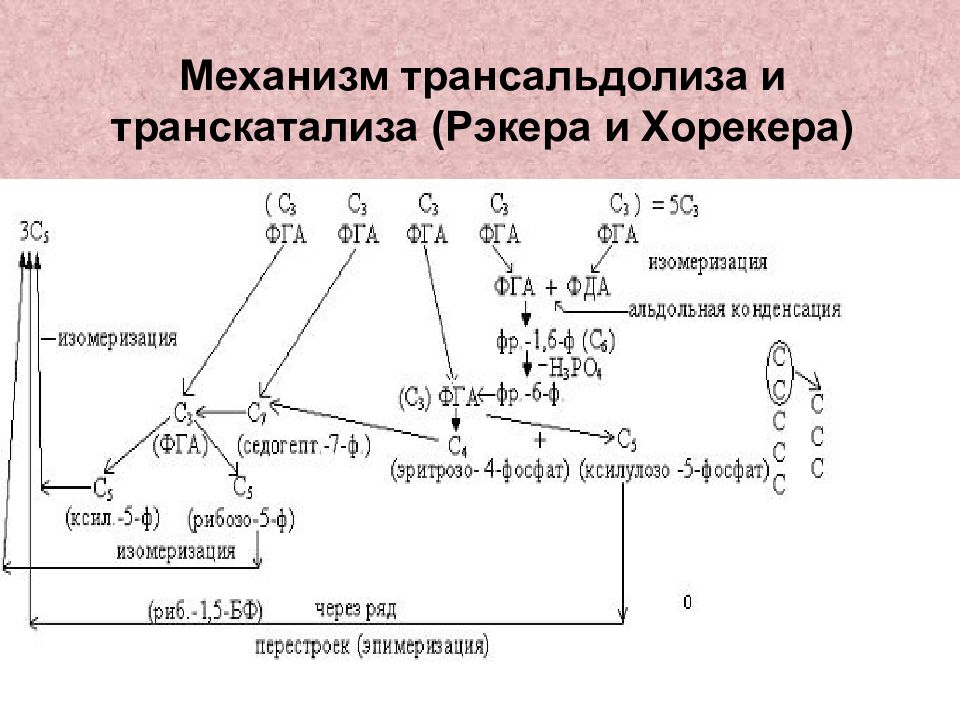
СООН НСОН Н 2 СО Р СОО Р НСОН Н 2 СО Р О С - Н НСОН Н 2 СО Р АТФ НАДФН Н 2 С - ОН С = О Н 2 СО Р 3-ФГК 1,3-ФГК 3-ФГА ДГАФ Транскетолазные и трансальдолазные реакции Регенерация субстрата
Слайд 25
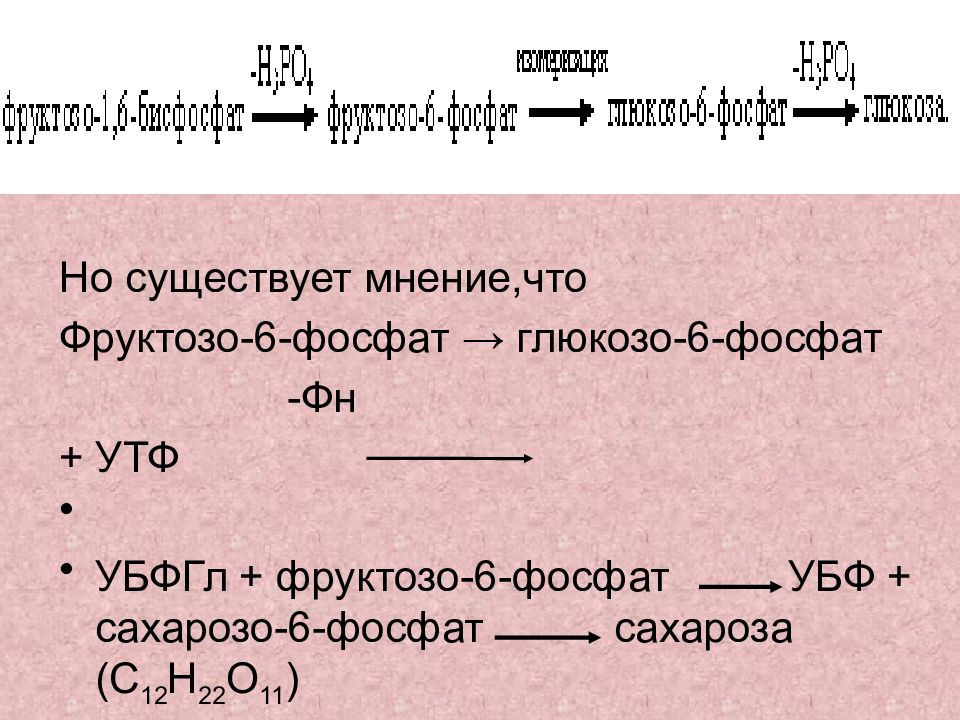
Но существует мнение,что Фруктозо-6-фосфат → глюкозо-6-фосфат -Фн + УТФ УБФГл + фруктозо-6-фосфат УБФ + сахарозо-6-фосфат сахароза (С 12 Н 22 О 11 )
Слайд 28: Для синтеза 1 молекулы гексозы (С 6 ) требуется:
6СО 2 + 6РБФ + 12 НАДФ∙Н + (12+6)АТФ + Н 2 О → фрукт.-6-фосфат + 6РБФ + + 12НАДФ+ + 18АДФ + 17Фн
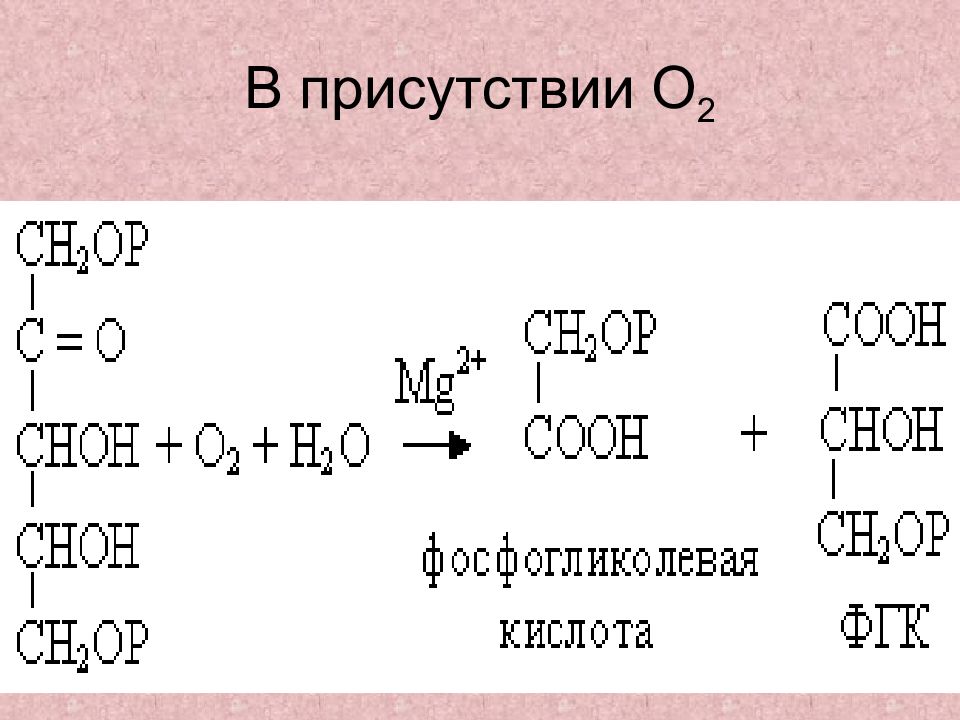
Слайд 29: Эффект Варбурга —
в присутствии большого количества О 2, фотосинтез тормозится.
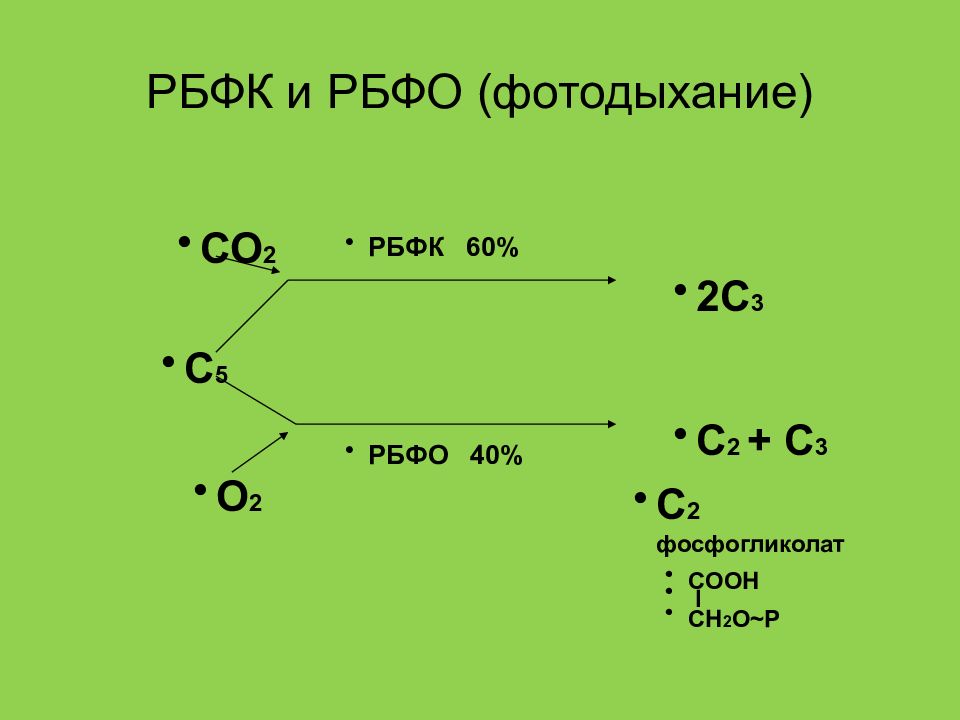
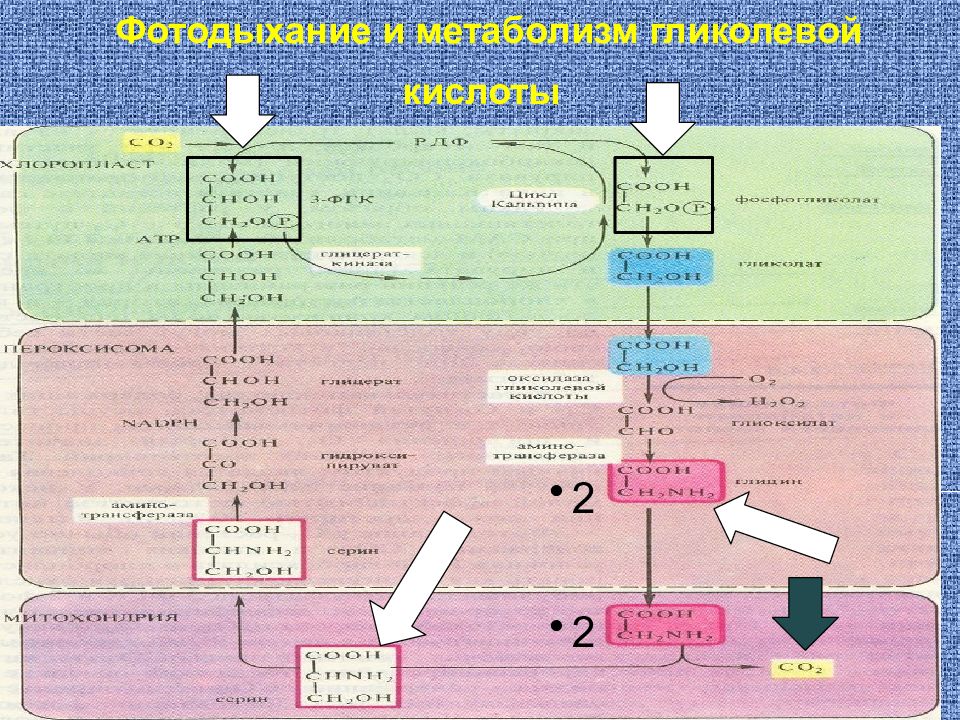
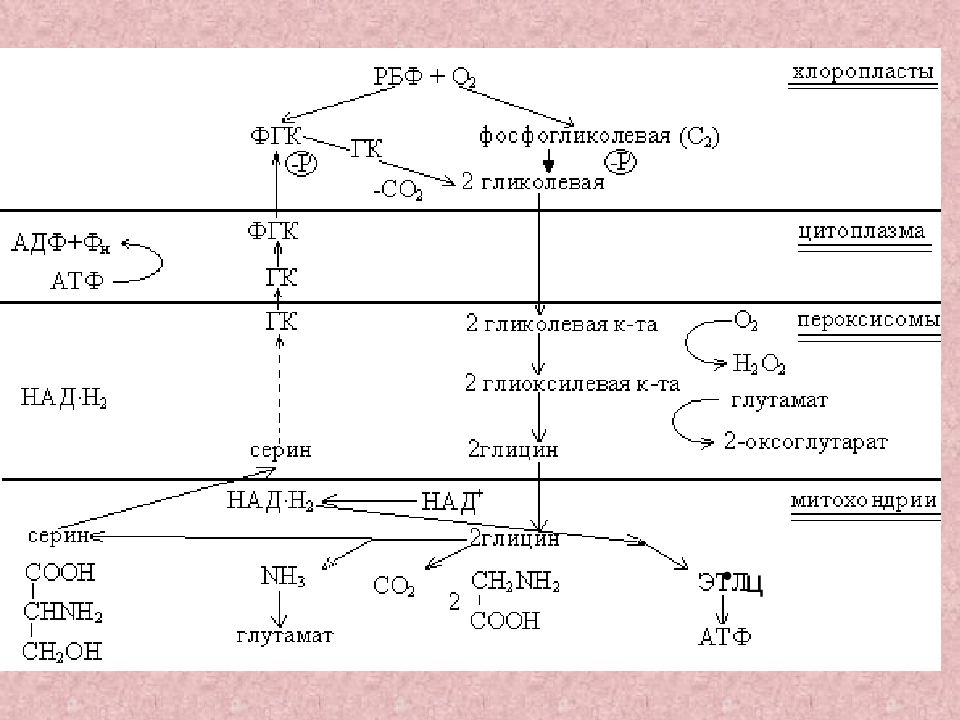
Слайд 30: РБФК и РБФО ( фотодыхание )
С 5 СО 2 О 2 2С 3 С 2 + С 3 РБФК 60% РБФО 40% С 2 фосфогликолат СООН I СН 2 О ~ Р
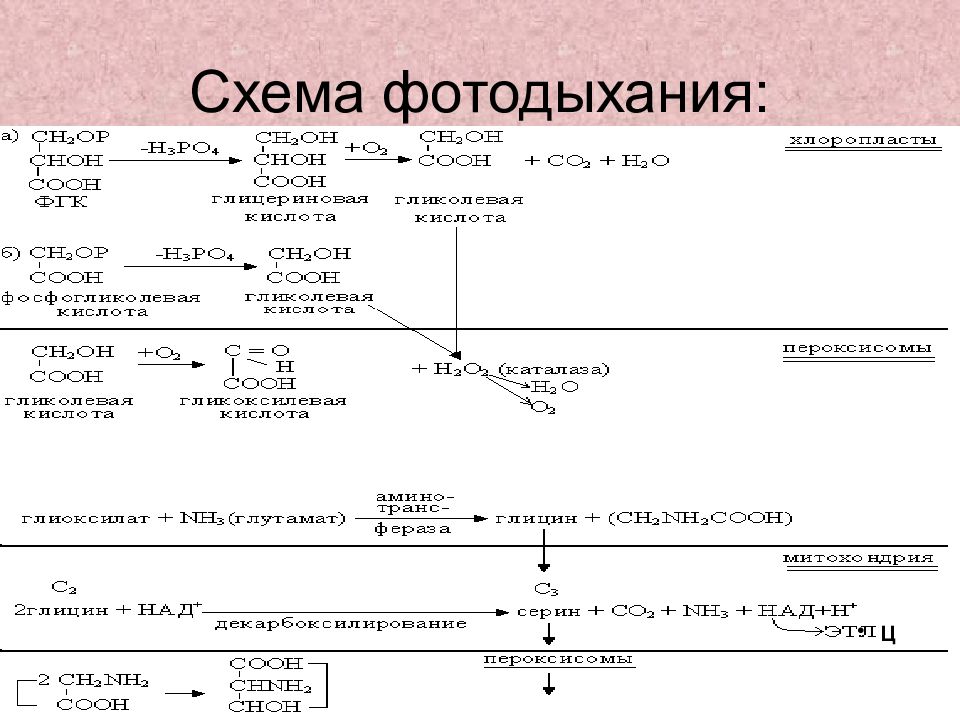
Слайд 34: Сходство фото- и темнового дыхания— только конечные продукты
отличаются по субстратам и локализации: фотодыхание— окисление гликолата в пероксиомах, темновое – углеводы в митохондриях.
Слайд 35: Фотодыхание у С 3 растений составляет 20—40%
Фотодыхание у С 4 -растений составляет 1-3%, их продуктивность в 2 раза выше, чем у С 3 -растений
Слайд 36: Что дает растениям фотодыхание?
1. Так, есть мнение, что фотодыхание – бесполезный процесс, общий выход органических веществ снижается, АТФ не образуется, только когда НАДФН митохондриях →в ЭТЦ приводит к образованию АТФ. АТФ расходуется на фосфорилирование ГК до ФГК. 2. Согласно другого мнения, наоборот, фотодыхание: а) энергетический процесс (в митохондриях – АТФ); б) накапливаются физиологически важные метаболиты – глицин, серин; в) поглощается избыток АТФ и НАДФН, который возникает при повышенном освещении; г) если мало СО 2 и света устанавливается баланс между темновой и световой стадиями фотосинтеза; д) фотодыхание – один из способов защиты от торможения О 2 -ом за счет его дополнительной утилизации и т.д.
Слайд 37: С 4 -путь фотосинтеза
С 4 -путь более эволюционно поздний, встречается у почти 300 видов растений 16 семейств покрытосеменных.
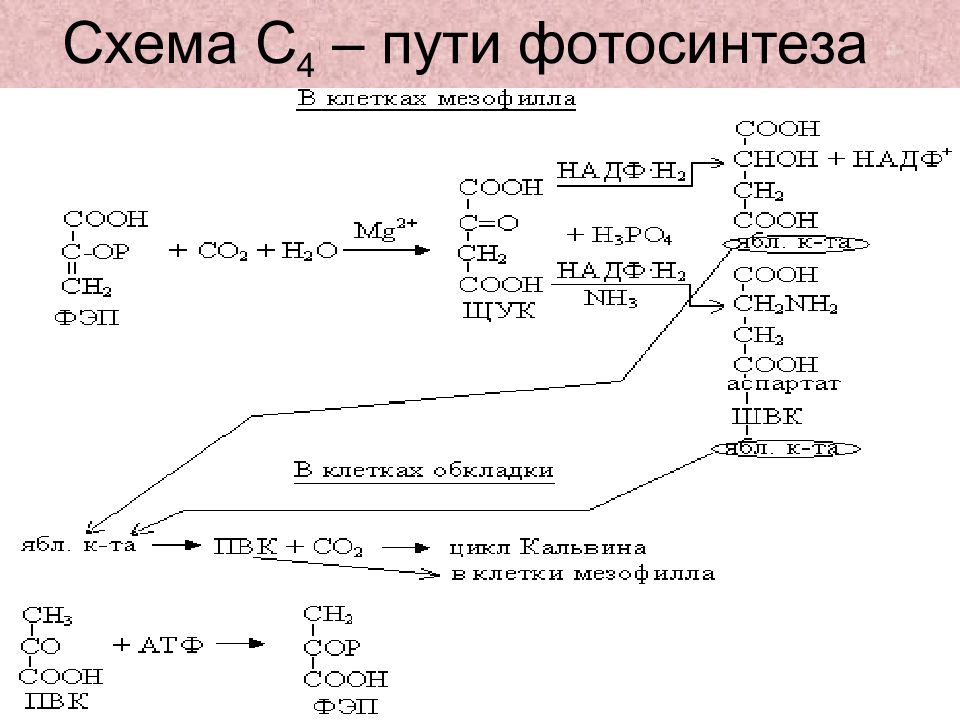
Слайд 38: Цикл Хэтча – Слэка - Карпилова
Незговорова Л.А. 1956 – 1957 Карпилов Ю.С. 1960 кукуруза Тарчевский И.А. 1963 М.Д. Хэтч и К.Р. Слэк 1966 сах. тростник Продукт фиксации С4 – малат ( ЩУК ), аспартат Акцептор С 3 – ФЕП
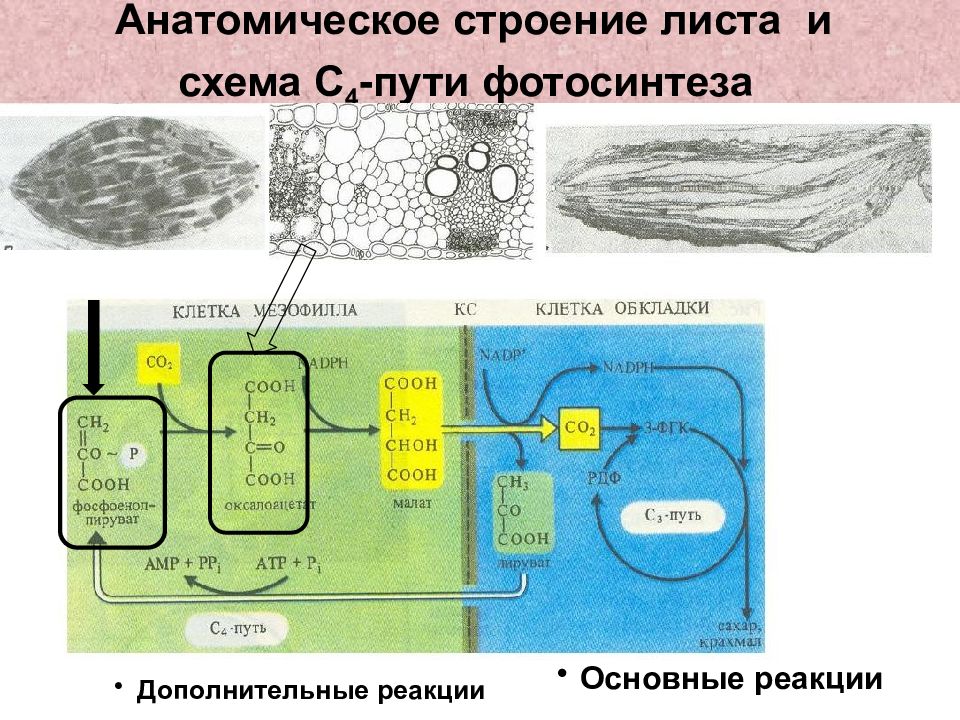
Слайд 39: Анатомические особенности листа –
у С 4 -растений есть клетки обкладки вокруг сосудисто-волокнистых пучков, содержащие большие хлоропласты без гран, а клетки мезофилла расположены рыхло, их хлоропласты более мелкие, с гранами.
Слайд 40: Анатомическое строение листа и схема С 4 -пути фотосинтеза
Дополнительные реакции Основные реакции
Слайд 41: Отличие С 4 -пути от С 3 -пути :
Хэтч и Слэк в 1966г, а еще ранее Карпилов (1960г.), Корчак (1965г.) – установили, что у сахарного тростника и кукурузы в противоположность циклу Кальвина акцептором СО 2 является ФЭП, а не РБФ. ФЭП-карбоксилаза имеет более высокое химическое сродство к СО 2, чем РБФ-карбоксилаза. При концентрации в 100 раз ниже обычной ФЭП-карбоксилаза более активна.
Слайд 42: Преимущество С 4 -растений:
в клетках обкладки СО 2 концентрируется, потому фотодыхание не идет; клетки обкладки находятся вокруг сосудисто-волокнистых пучков, что содействует быстрому оттоку органических веществ, они не накапливаются в хлоропластах; сопротивление устьиц выше у этих растений, СО 2 входит с трудом, что мешает транспирации. Растения более экономно расходуют воду, более устойчивы к засухе.
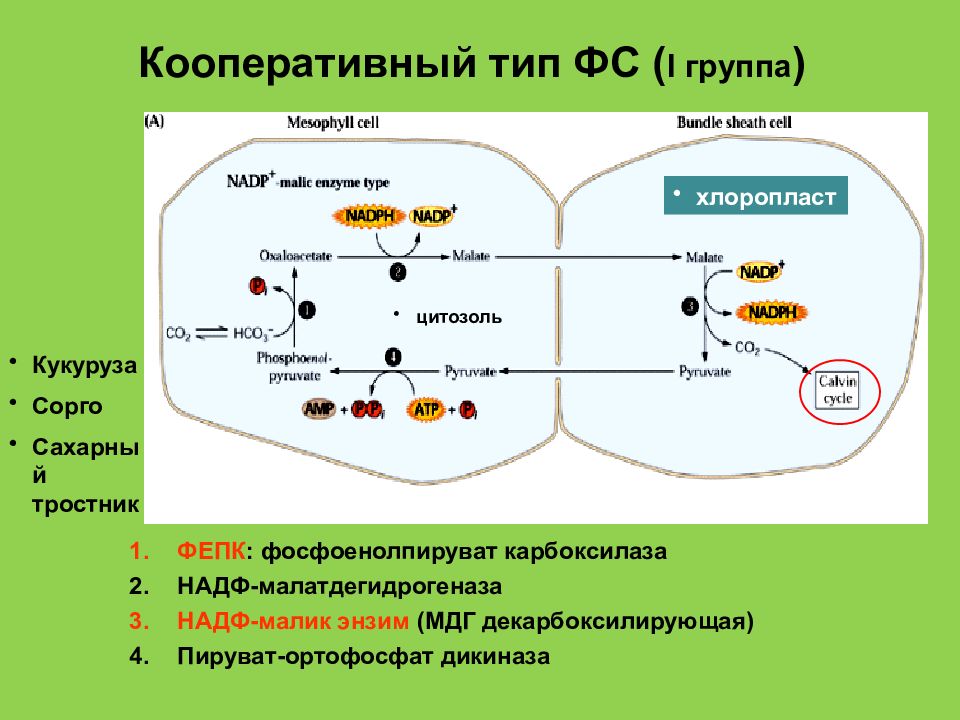
Слайд 45: Кооперативный тип ФС ( I группа )
ФЕПК : фосфоенолпируват карбоксилаза НАДФ-малатдегидрогеназа НАДФ-малик энзим ( МДГ декарбоксилирующая ) Пируват-ортофосфат дикиназа Кукуруза Сорго Сахарный тростник хлоропласт цитозоль
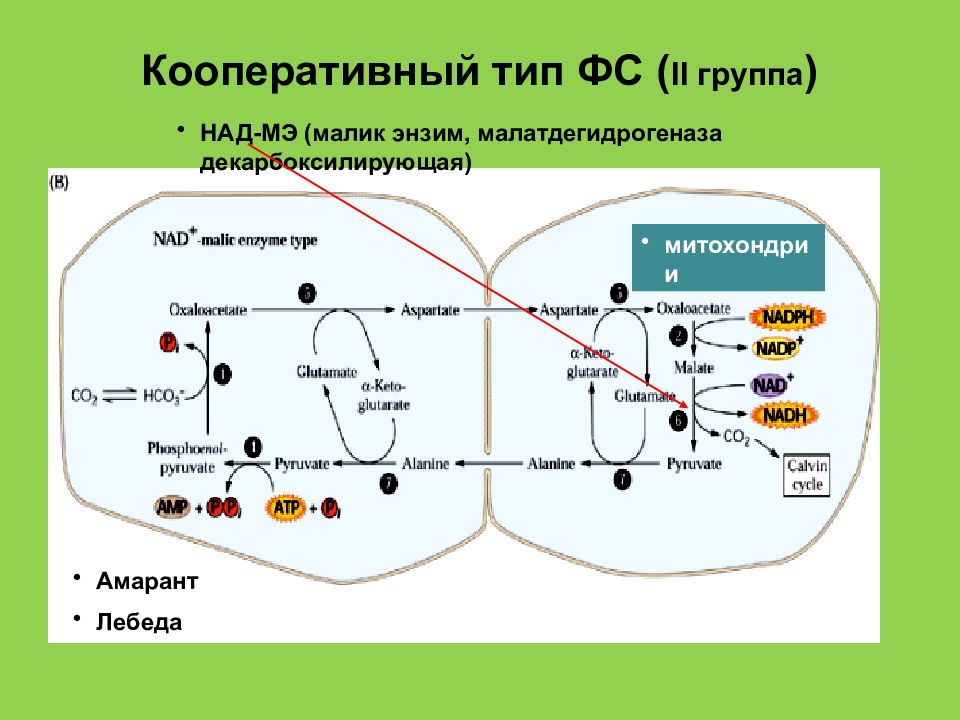
Слайд 46: Кооперативный тип ФС ( II группа )
Амарант Лебеда митохондрии НАД-МЭ ( малик энзим, малатдегидрогеназа декарбоксилирующая )
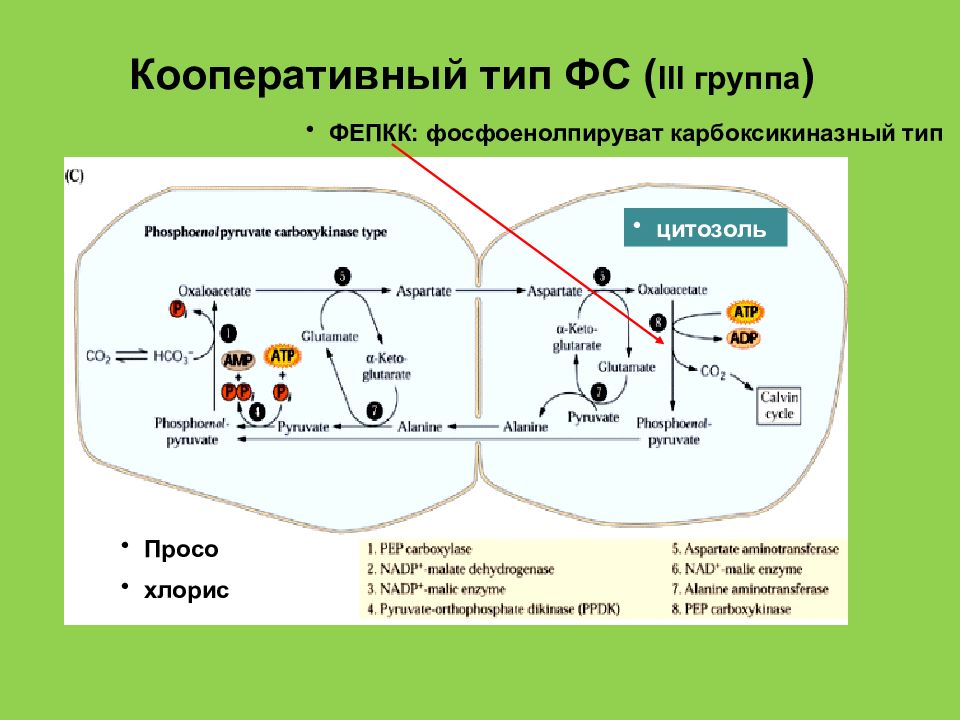
Слайд 47: Кооперативный тип ФС ( III группа )
Просо хлорис ФЕПКК: фосфоенолпируват карбоксикиназный тип цитозоль
Слайд 48: С 4 растения различаются по способам декарбоксилирования
Карбоксилирование у всех одинаково: в цитозоле клеток мезофилла ФЕПК: фосфоенолпируват карбоксилаза Декарбоксилирование трех типов 1. НАДФ-малатдегидрогеназа 2. НАДФ-малик энзим ( МДГ декарбоксилирующая ) 3. ФЕПКК: фосфоенолпируват карбоксикиназа
Слайд 49
Кооперативный тип фотосинтеза ! Морфологические особенности ! Биохимические особенности Фермент декарбоксилирования НАДФ-МЭ НАД-МЭ ФЕП-КК Продукт фиксации СО 2 малат аспартат
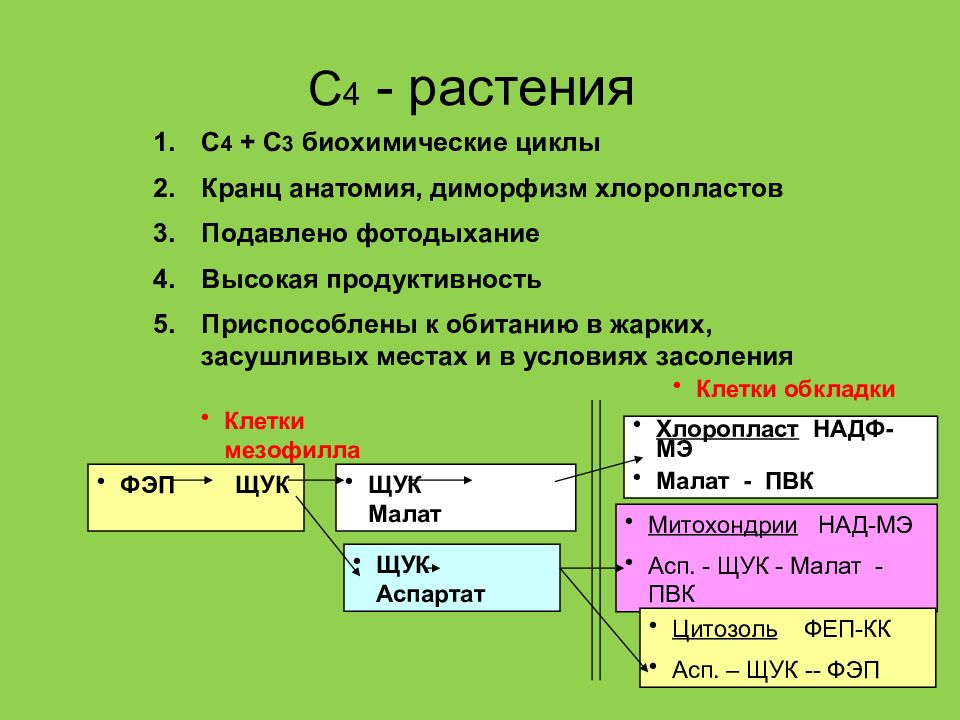
Слайд 50: С 4 - растения
С 4 + С 3 биохимические циклы Кранц анатомия, диморфизм хлоропластов Подавлено фотодыхание Высокая продуктивность Приспособлены к обитанию в жарких, засушливых местах и в условиях засоления ФЭП ЩУК ЩУК Малат Клетки обкладки Хлоропласт НАДФ-МЭ Малат - ПВК Митохондрии НАД-МЭ Асп. - ЩУК - Малат - ПВК Цитозоль ФЕП-КК Асп. – ЩУК -- ФЭП Клетки мезофилла ЩУК Аспартат
Слайд 51
Злаки: 3 типа кранц анатомии, 3 энзиматические группы Маревые: 4 типа кранц анатомии, 3 энзиматические группы C 4 – растения: 18 семейств 90% видов в двух семействах Poaceae (1000) и Chenopodiaceae (250) Пьянков Владимир Иванович, Мокроносов Адольф Трофимович (1993) «Основные тенденции изменения растительности земли в связи с глобальным потеплением климата»// «Физиология растений», том 40, N 4, с. 515 - 531
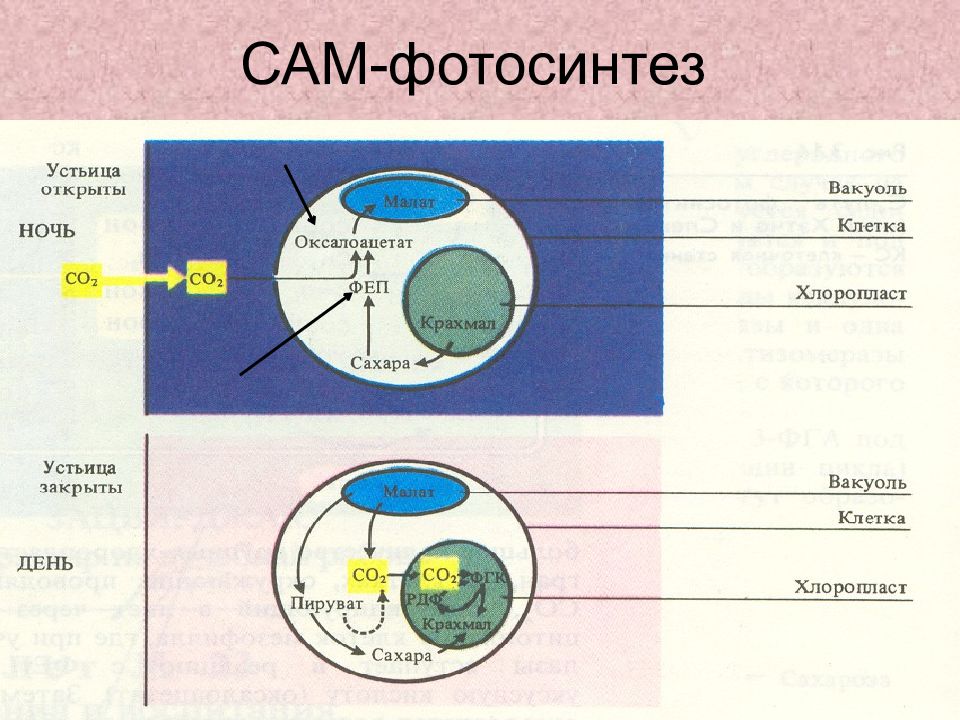
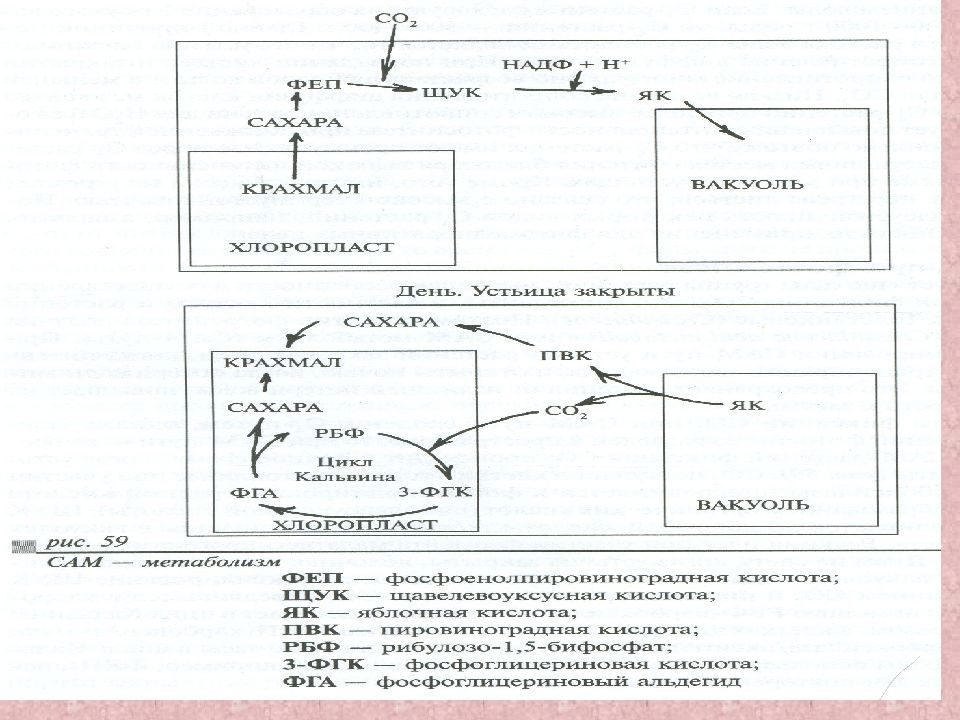
Слайд 52: Ассимиляция СО 2 у толстянковых – САМ – фотосинтез
У обычных С 4 -растеий 1 и 2 карбоксилирование разделены пространством – мезофилл и обкладка; у толстянковых – временем : все реакции идут в мезофилле, ночью образуются органические кислоты при открытых устьицах, днем при закрытых - СО 2 выделяется внутри клеток и происходит цикл Кальвина. Фотосинтез идет на свету при закрытых устьицах (приспособление к засухе).
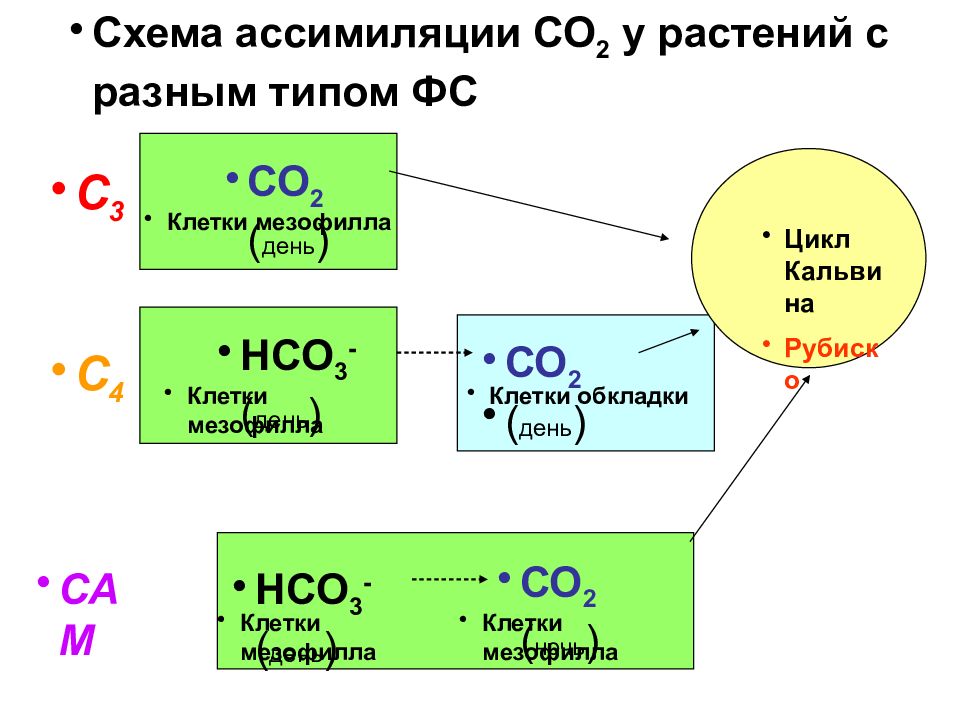
Слайд 55
САМ С 3 С 4 СО 2 ( день ) НСО 3 - ( день ) СО 2 ( ночь ) Клетки мезофилла Клетки мезофилла Клетки обкладки Цикл Кальвина Рубиско Схема ассимиляции СО 2 у растений с разным типом ФС НСО 3 - ( день ) Клетки мезофилла Клетки мезофилла СО 2 ( день )
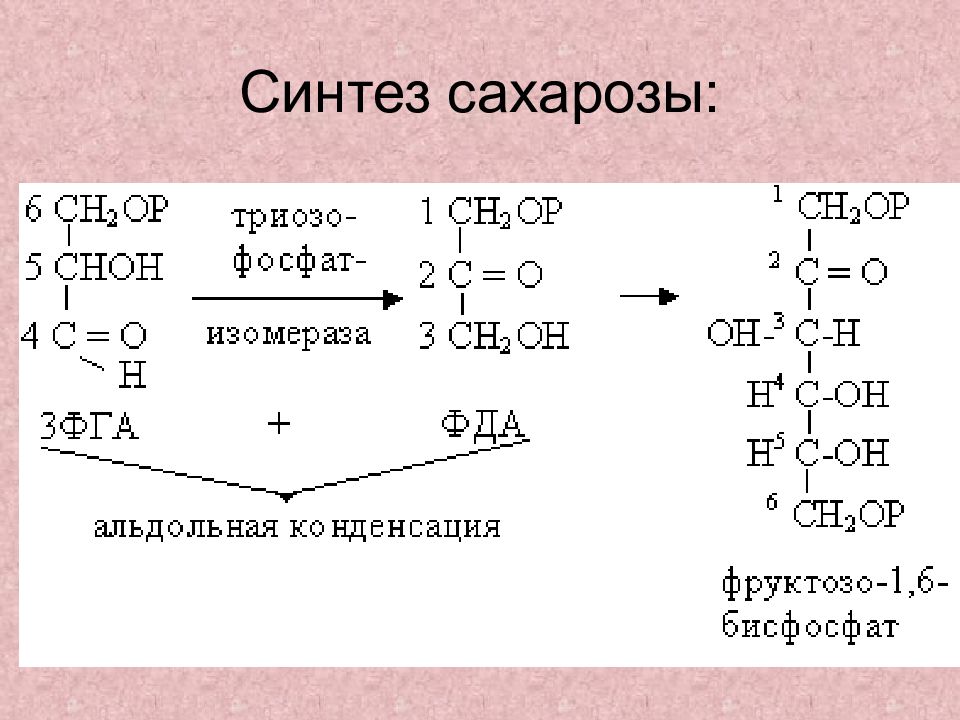
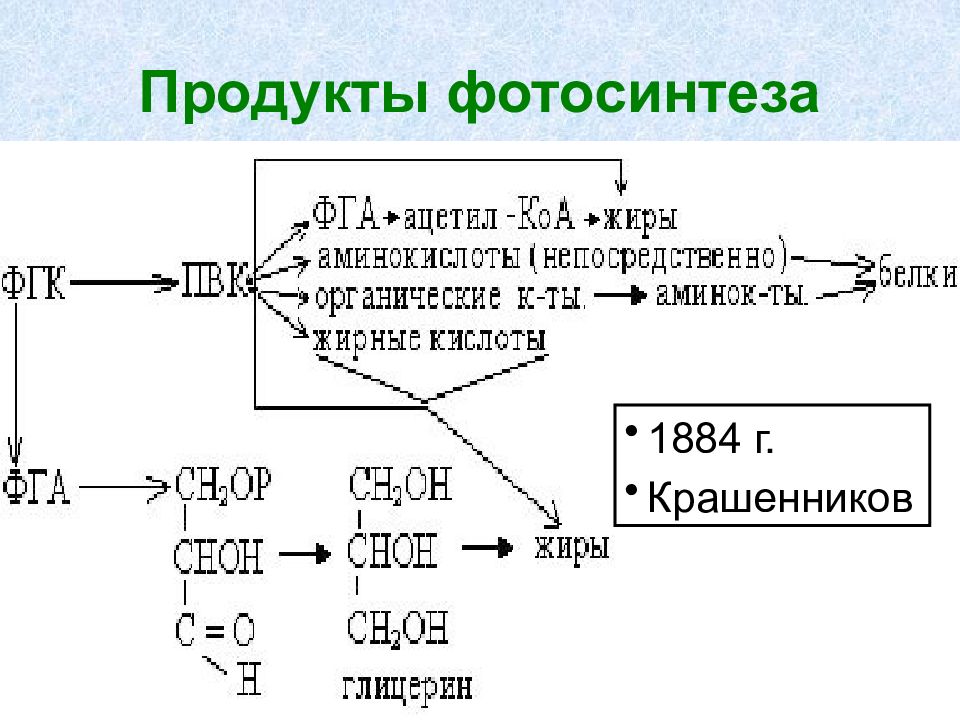
Слайд 57: Из промежуточных продуктов цикла Кальвина могут образовываться жиры, липиды и др.продукты. Состав продуктов, образующихся при фотосинтезе, может быть определен исходя из величин фотосинтетического коэффициента
Под фотосинтетическим коэффициентом понимается отношение выделенного в процессе фотосинтеза кислорода к поглощенному СО 2. ФК = Vo 2 /Vco 2
Слайд 58: Работы Ничипоровича, Андреевой и Воскресенской показали:
Синий свет Красный свет Больше белков больше углеводов
Слайд 59: Нет единства в продуктах фотосинтеза, это является приспособительной реакцией
Есть группы растений, у которых основные продукты фотосинтеза: сахароза и крахмал (90-95%) — картофель, сахарная свекла, ранневесенние эфемеры (тюльпаны) и др. галактозосодержащие углеводы — раффиноза, стахиоза, вербаcкоза- тыквенные. сахароспирты – манит, сорбит — яблоня, ясень, сирень, сельдерей и др. наряду с сахарозой и крахмалом есть глицин, серин и другие аминокислоты — бобовые.
Слайд 60: Таким образом, сущность темновой стадии фотосинтеза —
преобразование химически связанной энергии лабильных промежуточных соединений АТФ и НАДФН в потенциальную энергию химических связей стабильных продуктов – сахаров, аминокислот и др.
Слайд 61
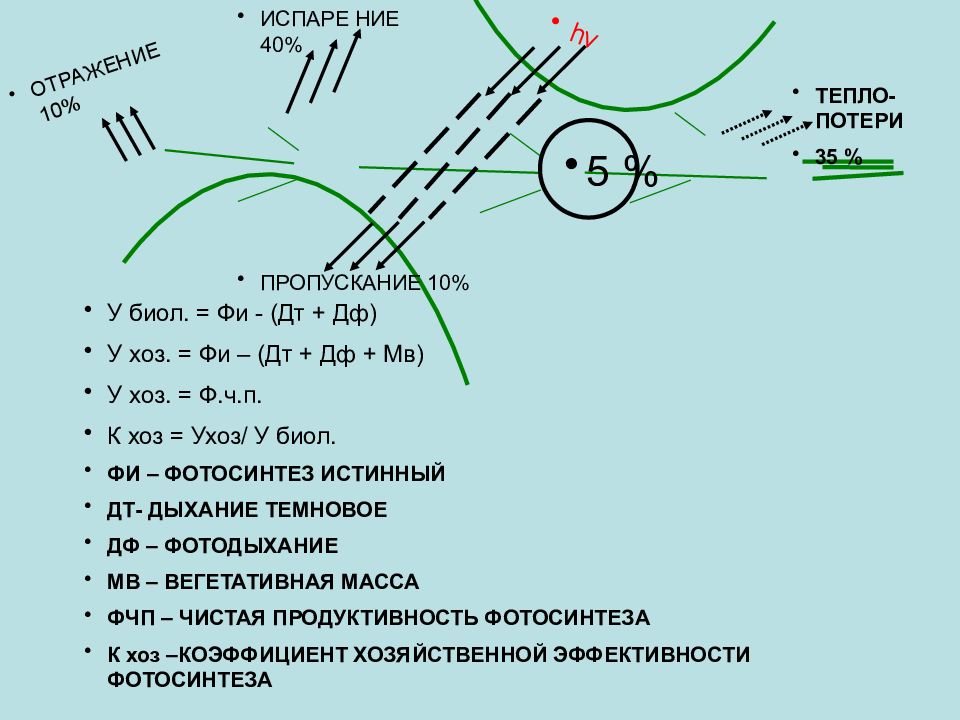
ТЕПЛО-ПОТЕРИ 35 % ПРОПУСКАНИЕ 10% ОТРАЖЕНИЕ 10% ИСПАРЕ НИЕ 40% 5 % hv У биол. = Фи - (Дт + Дф) У хоз. = Фи – (Дт + Дф + Мв) У хоз. = Ф.ч.п. К хоз = Ухоз/ У биол. ФИ – ФОТОСИНТЕЗ ИСТИННЫЙ ДТ- ДЫХАНИЕ ТЕМНОВОЕ ДФ – ФОТОДЫХАНИЕ МВ – ВЕГЕТАТИВНАЯ МАССА ФЧП – ЧИСТАЯ ПРОДУКТИВНОСТЬ ФОТОСИНТЕЗА К хоз –КОЭФФИЦИЕНТ ХОЗЯЙСТВЕННОЙ ЭФФЕКТИВНОСТИ ФОТОСИНТЕЗА
Слайд 62
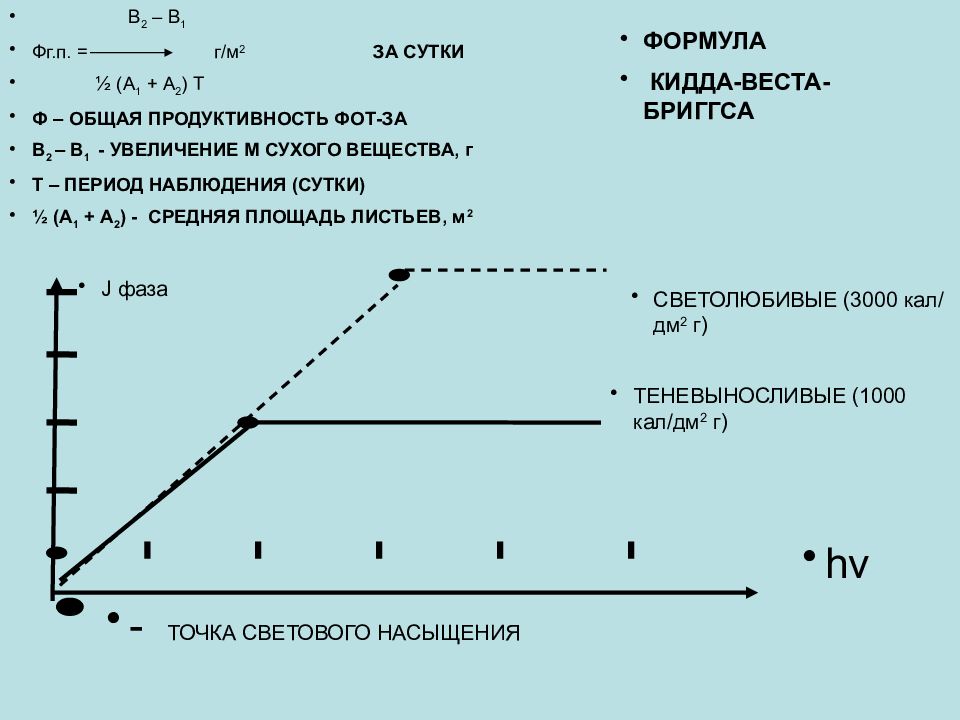
В 2 – В 1 Фг.п. = г/м 2 ЗА СУТКИ ½ (А 1 + А 2 ) Т Ф – ОБЩАЯ ПРОДУКТИВНОСТЬ ФОТ-ЗА В 2 – В 1 - УВЕЛИЧЕНИЕ М СУХОГО ВЕЩЕСТВА, г Т – ПЕРИОД НАБЛЮДЕНИЯ (СУТКИ) ½ (А 1 + А 2 ) - СРЕДНЯЯ ПЛОЩАДЬ ЛИСТЬЕВ, м 2 hv J фаза СВЕТОЛЮБИВЫЕ (3000 кал/дм 2 г) ТЕНЕВЫНОСЛИВЫЕ (1000 кал/дм 2 г) - ТОЧКА СВЕТОВОГО НАСЫЩЕНИЯ ФОРМУЛА КИДДА-ВЕСТА-БРИГГСА
Слайд 63
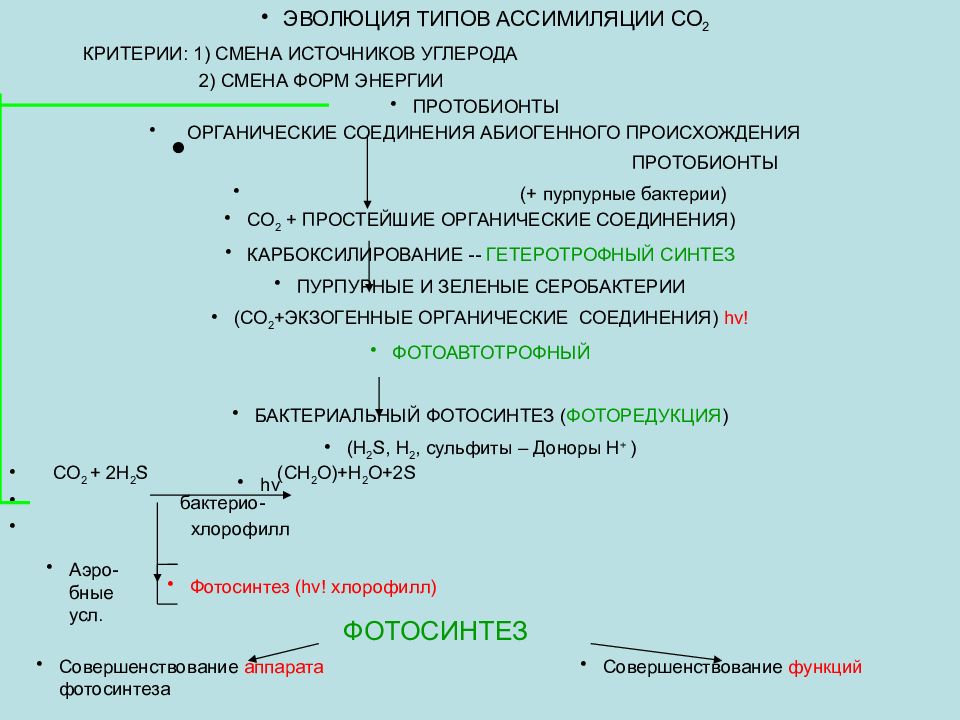
ЭВОЛЮЦИЯ ТИПОВ АССИМИЛЯЦИИ СО 2 КРИТЕРИИ: 1) СМЕНА ИСТОЧНИКОВ УГЛЕРОДА 2) СМЕНА ФОРМ ЭНЕРГИИ ПРОТОБИОНТЫ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ АБИОГЕННОГО ПРОИСХОЖДЕНИЯ ПРОТОБИОНТЫ (+ пурпурные бактерии) СО 2 + ПРОСТЕЙШИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ) КАРБОКСИЛИРОВАНИЕ -- ГЕТЕРОТРОФНЫЙ СИНТЕЗ ПУРПУРНЫЕ И ЗЕЛЕНЫЕ СЕРОБАКТЕРИИ (СО 2 +ЭКЗОГЕННЫЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ) hv! ФОТОАВТОТРОФНЫЙ БАКТЕРИАЛЬНЫЙ ФОТОСИНТЕЗ ( ФОТОРЕДУКЦИЯ ) (Н 2 S, Н 2, сульфиты – Доноры Н + ) СО 2 + 2Н 2 S (CН 2 О)+Н 2 О+2S бактерио- хлорофилл hv Аэро-бные усл. Фотосинтез (hv! хлорофилл) ФОТОСИНТЕЗ Совершенствование аппарата фотосинтеза Совершенствование функций
Слайд 64
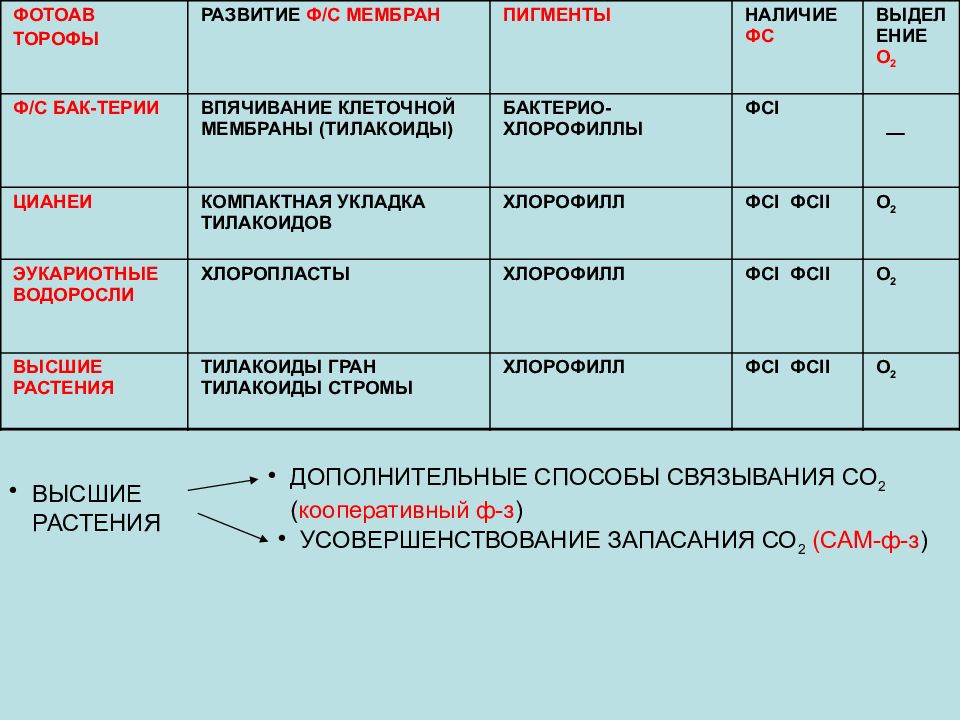
ФОТОАВ ТОРОФЫ РАЗВИТИЕ Ф/С МЕМБРАН ПИГМЕНТЫ НАЛИЧИЕ ФС ВЫДЕЛЕНИЕ О 2 Ф/С БАК-ТЕРИИ ВПЯЧИВАНИЕ КЛЕТОЧНОЙ МЕМБРАНЫ (ТИЛАКОИДЫ) БАКТЕРИО-ХЛОРОФИЛЛЫ ФСI — ЦИАНЕИ КОМПАКТНАЯ УКЛАДКА ТИЛАКОИДОВ ХЛОРОФИЛЛ ФСI ФСII О 2 ЭУКАРИОТНЫЕ ВОДОРОСЛИ ХЛОРОПЛАСТЫ ХЛОРОФИЛЛ ФСI ФСII О 2 ВЫСШИЕ РАСТЕНИЯ ТИЛАКОИДЫ ГРАН ТИЛАКОИДЫ СТРОМЫ ХЛОРОФИЛЛ ФСI ФСII О 2 ВЫСШИЕ РАСТЕНИЯ ДОПОЛНИТЕЛЬНЫЕ СПОСОБЫ СВЯЗЫВАНИЯ СО 2 ( кооперативный ф-з ) УСОВЕРШЕНСТВОВАНИЕ ЗАПАСАНИЯ СО 2 (САМ-ф-з )
Последний слайд презентации: 4.4. Темновая стадия фотосинтеза
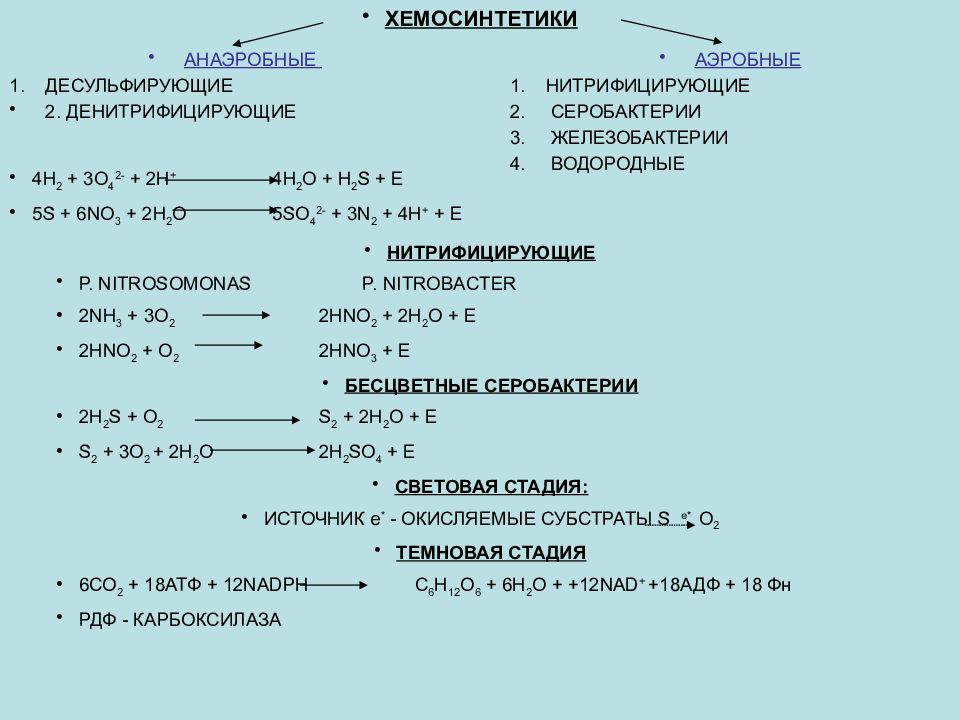
ХЕМОСИНТЕТИКИ АНАЭРОБНЫЕ ДЕСУЛЬФИРУЮЩИЕ 2. ДЕНИТРИФИЦИРУЮЩИЕ АЭРОБНЫЕ НИТРИФИЦИРУЮЩИЕ СЕРОБАКТЕРИИ ЖЕЛЕЗОБАКТЕРИИ ВОДОРОДНЫЕ 4Н 2 + 3О 4 2- + 2Н + 4Н 2 О + Н 2 S + Е 5S + 6NО 3 + 2Н 2 О 5 S О 4 2- + 3N 2 + 4H + + Е НИТРИФИЦИРУЮЩИЕ Р. NITROSOMONAS P. NITROBACTER 2NH 3 + 3O 2 2HNO 2 + 2H 2 O + E 2HNO 2 + O 2 2HNO 3 + E БЕСЦВЕТНЫЕ СЕРОБАКТЕРИИ 2H 2 S + O 2 S 2 + 2H 2 O + E S 2 + 3O 2 + 2H 2 O 2H 2 S O 4 + E СВЕТОВАЯ СТАДИЯ: ИСТОЧНИК е * - ОКИСЛЯЕМЫЕ СУБСТРАТЫ S е* О 2 ТЕМНОВАЯ СТАДИЯ 6СО 2 + 18АТФ + 12NADPH C 6 H 12 O 6 + 6H 2 O + +12NAD + +18АДФ + 18 Фн РДФ - КАРБОКСИЛАЗА