Слайд 2: Актуальность
Расчетное число всех типов энцефалитов – 5-10 случаев на 100.000 населения (для РБ – 500-1000 пациентов ежегодно ?) 40-50 % всех энцефалитов до сих пор остаются нерасшифрованными Распространенность аутоиммунных энцефалитов (13,7 на 100.000 населения) статистически значимо не отличается от распространенности инфекционных (11,6 на 100.000 населения) Число рецидивов заболевания и число повторных госпитализаций существенно выше в группе аутоиммунных энцефалитов RopperA. et al. NEJM 2018; 378; 840
Слайд 3: Аутоиммунный энцефалит
это заболевание, характеризующееся поражением преимущественно серого вещества, в патогенезе которого основную роль играют аутоантитела (АТ) к внутри- и/или внеклеточным структурам нервной системы, выступающих в качестве антигенов.
Слайд 4: Аутоиммунный энцефалит
Среди этих заболеваний выделяют паранеопластические неврологические синдромы, при которых поражение нервной системы связано с текущим онкологическим процессом, и недавно выделенные в отдельную группу идиопатические АЭ, при которых поражение нервной системы может происходить в отсутствие онкологии.
Слайд 5: Разновидности аутоиммунного энцефалита
энцефалит с антителами к NMDA-рецепторам лимбический энцефалит энцефалопатию Хашимото PANDAS- синдром ( Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal infections) Опсоклонусоклонус (СОМ Синдром Опсоклонус-миоклонус) CLIPPERS (Chronic lymphocytic inflammation with pontine perivascular enhancement responsive to steroids) и некоторые другие.
Слайд 7: В настоящее время выделены 3 группы аутоантител при аутоиммунных поражениях ЦНС
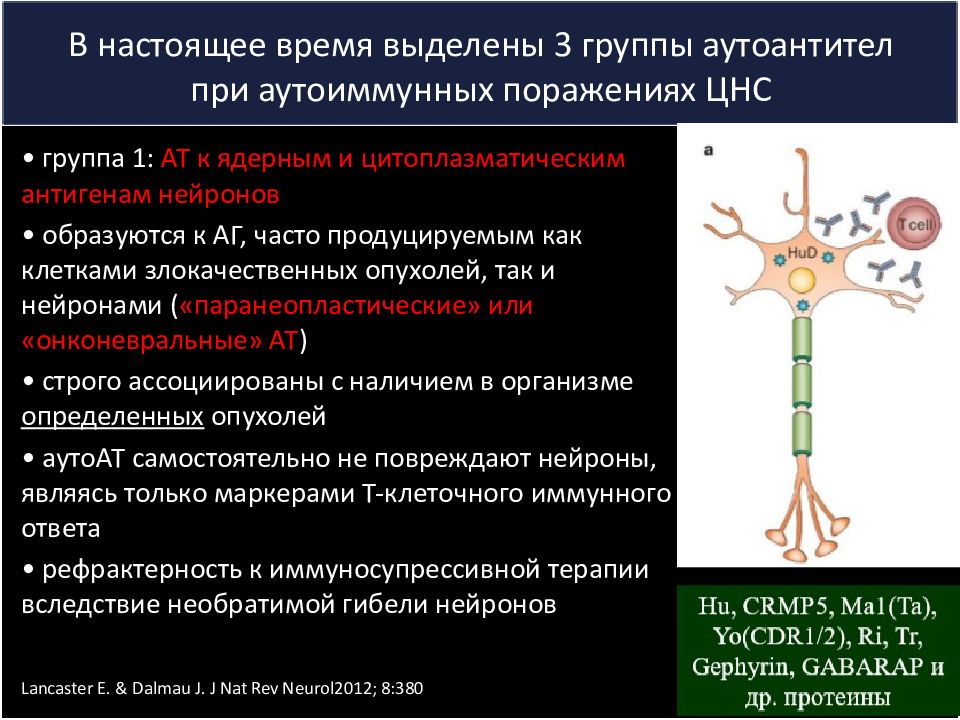
• группа 1: АТ к ядерным и цитоплазматическим антигенам нейронов • образуются к АГ, часто продуцируемым как клетками злокачественных опухолей, так и нейронами ( «паранеопластические» или «онконевральные» АТ ) • строго ассоциированы с наличием в организме определенных опухолей • аутоАТ самостоятельно не повреждают нейроны, являясь только маркерами Т-клеточного иммунного ответа • рефрактерность к иммуносупрессивной терапии вследствие необратимой гибели нейронов Lancaster E. & Dalmau J. J Nat Rev Neurol2012; 8:380
Слайд 8: Основные паранеопластические аутоАТ и проявления, ассоциированные с ними
Слайд 9: В настоящее время выделены 3 группы аутоантител при аутоиммунных поражениях ЦНС
• группа 2: АТ к внутриклеточным синаптическим антигенам нейронов • АТ к GAD 65 крайне редко ассоциированы с новообразованиями, АТ к амфифизину часто выявляются при раке молочной железы • АТ к GAD65: синдром ригидного человека или церебеллит, редко лимбический энцефалит и эпилепсия, АТ к амфифизину – синдром ригидного человека • прямые повреждающие факторы нейронов как аутоАТ, так и Т-клеточный иммунный ответ, что преобладает–пока неясно • вариабельный ответ на иммуносупрессивную терапию
Слайд 10: В настоящее время выделены 3 группы аутоантител при аутоиммунных поражениях ЦНС
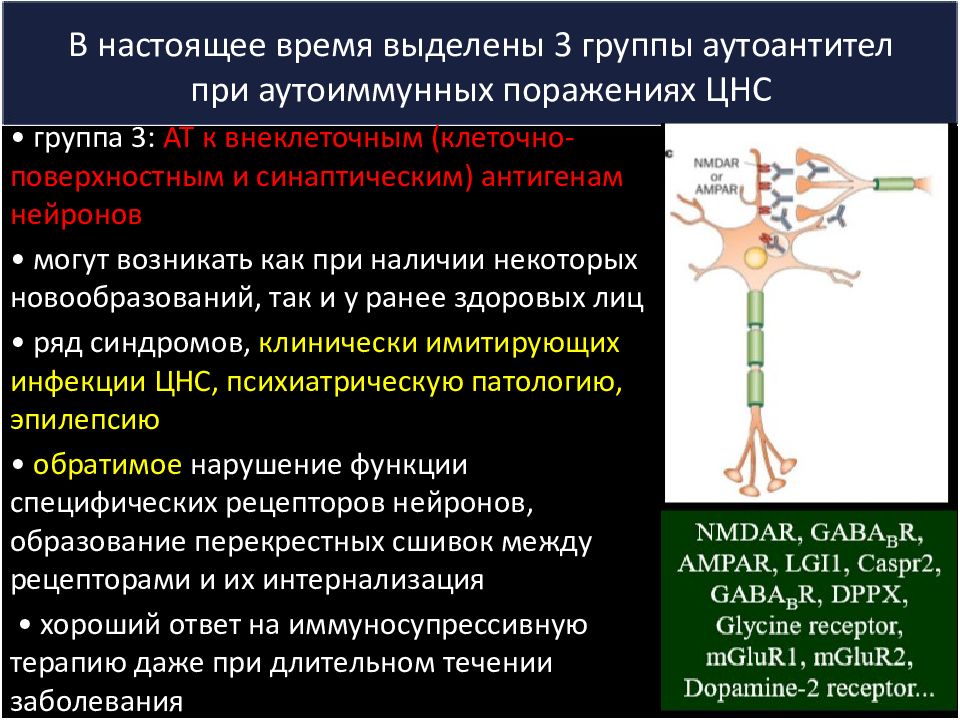
• группа 3: АТ к внеклеточным (клеточно- поверхностным и синаптическим) антигенам нейронов • могут возникать как при наличии некоторых новообразований, так и у ранее здоровых лиц • ряд синдромов, клинически имитирующих инфекции ЦНС, психиатрическую патологию, эпилепсию • обратимое нарушение функции специфических рецепторов нейронов, образование перекрестных сшивок между рецепторами и их интернализация • хороший ответ на иммуносупрессивную терапию даже при длительном течении заболевания
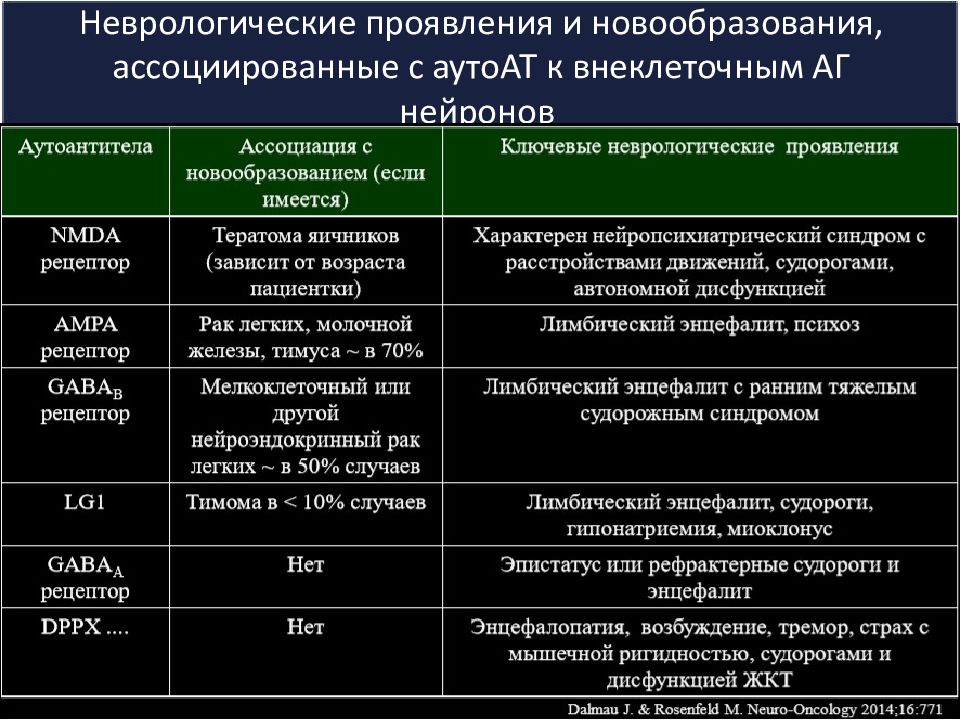
Слайд 11: Неврологические проявления и новообразования, ассоциированные с аутоАТ к внеклеточным АГ нейронов
Слайд 12: Механизмы развития нейрональной дисфункции
АТ к внутриклеточным антигенам наиболее вероятно вызывают повреждение путем активации цитотоксического Т-клеточного механизма. В патологический процесс вовлекаются цитоплазма и ядро. Морфологически при этом виде повреждения отмечаются гибель нейронов преимущественно по механизму некроза, дегенеративные изменения в аксонах, реактивный глиоз и признаки активации микроглии. Апоптотические изменения в нейронах выявляются реже и связываются с хроническим течением заболевания. Важно отметить отсутствие демиелинизации. АТ к мембранным и синаптическим антигенам оказывают непосредственное повреждающее действие на нервную клетку через нарушение функции рецепторов и ионных каналов мембран.
Слайд 13
Как клинически проявляются наиболее распространенные аутоиммунные энцефалиты?
Слайд 14: Энцефалит с антителами к NMDA-рецепторам
Впервые антитела к NMDA-рецепторам были описаны в 2007 году у пациенток с тератомами яичников, у которых развилась энцефалопатия с психическими нарушениями. ч асто дебютирует с явлений острого психоза • пациенты могут госпитализироваться в психиатрические отделения и долго причина их состояния интерпретируется неверно.
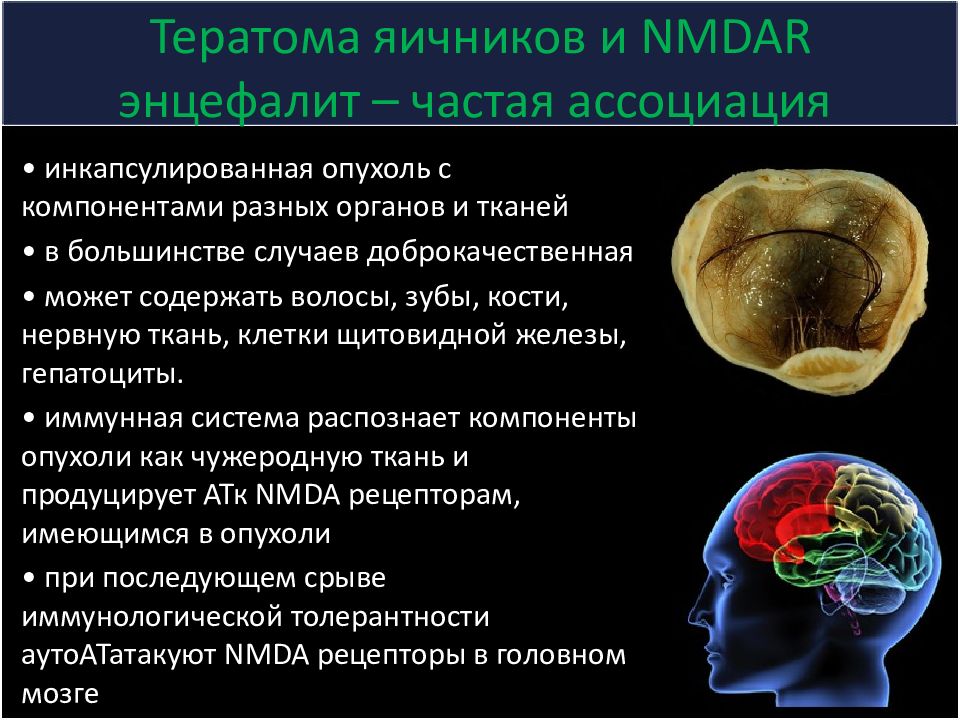
Слайд 15: Тератома яичников и NMDAR энцефалит – частая ассоциация
• инкапсулированная опухоль с компонентами разных органов и тканей • в большинстве случаев доброкачественная • может содержать волосы, зубы, кости, нервную ткань, клетки щитовидной железы, гепатоциты. • иммунная система распознает компоненты опухоли как чужеродную ткань и продуцирует АТк NMDA рецепторам, имеющимся в опухоли • при последующем срыве иммунологической толерантности аутоАТатакуют NMDA рецепторы в головном мозге
Слайд 16: Особенности
преимущественно молодой возраст ( подростки или молодые взрослые), средний возраст – 21 год (от 2 месяцев до 85 лет) • женщины: мужчины = 4:1 • 58% женщин 18-45 лет имеют тератому яичников • стадийное течение • часто дебют с нейропсихиатрических проявлений (судороги, психоз, спутанность сознания, амнезия) • быстрое ухудшение психического статуса в течение 1-14 дней • при прогрессировании - нарушение уровня сознания, автономная дисфункция, расстройства движений, кома • превалирование у детей судорог и дискинезий, у взрослых – психиатрической симптоматики
Слайд 17: Энцефалит с антителами к NMDA-рецепторам
В классическом варианте заболевание представлено эпилептическими приступами, психотическими и двигательными нарушениями, вегетативными расстройствами. В течение болезни выделяют ряд стадий : продромальную, психотическую, ареактивную, гиперкинетическую фазу постепенного регресса симптомов.
Слайд 18: Энцефалит с антителами к NMDA-рецепторам
В продромальной фазе заболевания пациенты страдают от неспецифических ОРВИ-подобных симптомов ( лихорадки, утомляемости, головной боли ). Данная фаза развития болезни длится в среднем около 5 дней. Психотическая фаза знаменует появление психопатологических симптомов. Могут встречаться эмоциональные нарушения ( апатия, недостаточность эмоций, депрессия, замыкание в себе, страх ), когнитивное снижение ( расстройства кратковременной памяти, затруднения в пользовании телефоном, другими электронными средствами ), выраженные шизофреноподобные симптомы ( дезорганизация мышления, компульсивные идеации, бред, зрительные и слуховые галлюцинации ), снижение критики своего состояния. Через 2 недели после психотических симптомов наступает ареактивная фаза болезни. У большинства пациентов (более 70%) перед этим возникают судорожные припадки. Преобладают генерализованные тонико-клонические приступы.
Слайд 19: Энцефалит с антителами к NMDA-рецепторам
Ареактивную фазу характеризуют нарушение сознания, напоминающее кататонию, мутизм, акинезия, отсутствие ответа на вербальные команды при открытых глазах. Гиперкинетическая фаза сопровождается постепенно развивающимися гиперкинезами. Так, к наиболее характерным ее проявлениям относят оролингвальные дискинезии ( облизывание губ, жевание ), атетоидные дискинетические позы пальцев рук. На этой стадии заболевания развиваются симптомы вегетативной нестабильности, среди которых – лабильность артериального давления, брадикардия или тахикардия, гипертермия, потливость. Особую опасность представляет гиповентиляция.
Слайд 20: Энцефалит с антителами к NMDA-рецепторам
Обратное развитие симптомов в первую очередь касается улучшения гиперкинетических нарушений. Регресс их обычно происходит в течение двух месяцев заболевания, однако описаны случаи, когда гиперкинезы персистируют более полугода и резистентны к множеству терапевтических воздействий. Для периода восстановления характерно наличие стойкого амнестического синдрома.
Слайд 21: Диагностика энцефалита с антителами к NMDA-рецепторам
• ЦСЖ: – плеоцитоз, увеличение концентрации белка, нормальная глюкоза • Электроэнцефалография – часто: очаговая или диффузная медленная активность во время эпизодов дискинезий или патологических движений – иногда: эпилептическая активность – «extreme delta brush»(специфичен для анти-NDMAR энцефалита) • МРТ головного мозга – зоны гиперинтенсивности на T2/FLAIR в гиппокампе, коре полушарий или мозжечка, лобно-базальной и островковой областях, базальных ганглиях, стволе мозга (~ 50% случаев) – отклонения на МРТ, как правило, не изменяются во время течения заболевания и не коррелируют с его тяжестью Dalmau J. et al. Lancet Neurol 2011; 10: 63 Gitiaux C. et al. Clinical Neurophysiology 2013; 124:2354
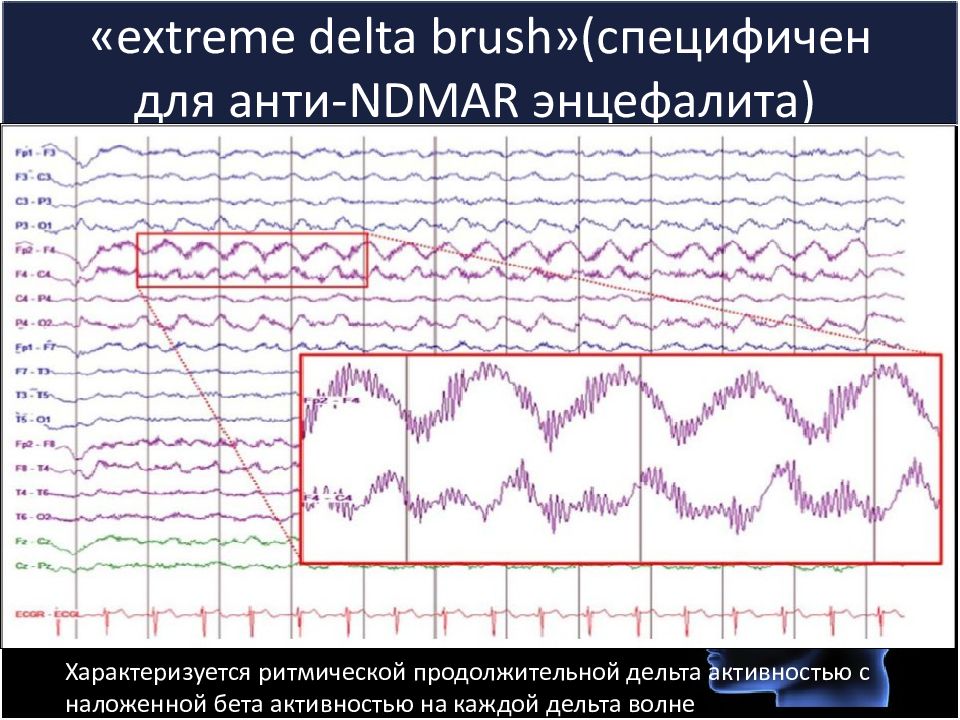
Слайд 22: extreme delta brush»( специфичен для анти- NDMAR энцефалита)
Характеризуется ритмической продолжительной дельта активностью с наложенной бета активностью на каждой дельта волне
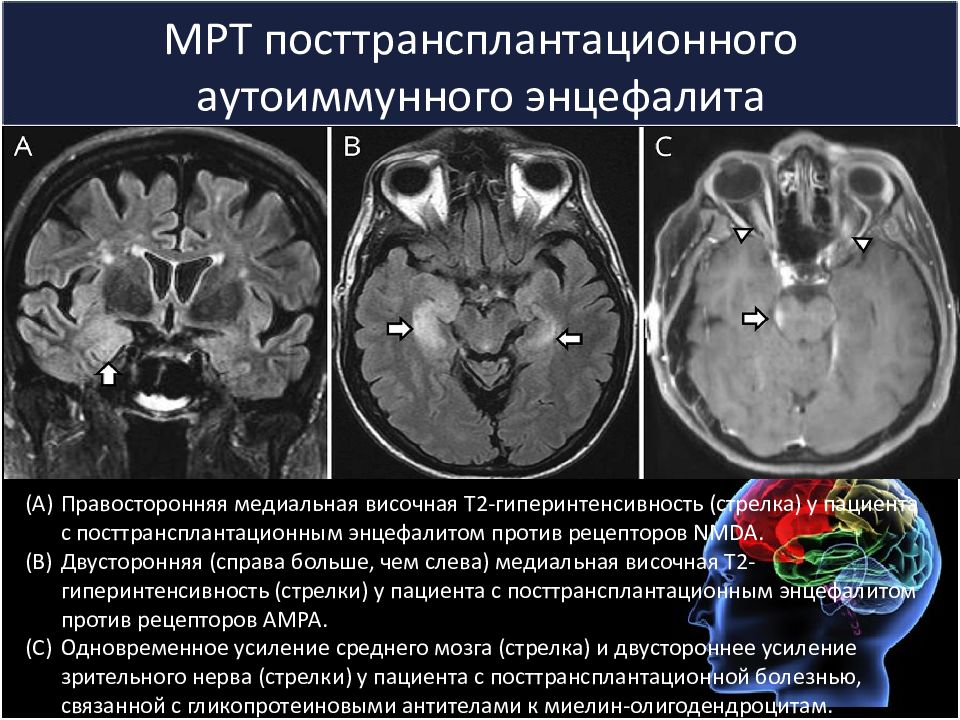
Слайд 23: МРТ посттрансплантационного аутоиммунного энцефалита
Правосторонняя медиальная височная T2-гиперинтенсивность (стрелка) у пациента с посттрансплантационным энцефалитом против рецепторов NMDA. Двусторонняя (справа больше, чем слева) медиальная височная Т2-гиперинтенсивность (стрелки) у пациента с посттрансплантационным энцефалитом против рецепторов AMPA. Одновременное усиление среднего мозга (стрелка) и двустороннее усиление зрительного нерва (стрелки) у пациента с посттрансплантационной болезнью, связанной с гликопротеиновыми антителами к миелин-олигодендроцитам.
Слайд 24: Диагностические критерии предполагаемого antiNMDAR энцефалита
Диагноз может быть установлен, когда имеются все три из нижеперечисленных критериев: 1. Быстрое начало (менее, чем за 3 месяца) по меньшей мере 4 из 6 основных групп симптомов: Психиатрические отклонения или когнитивная дисфункция Нарушения речи Судороги Двигательные расстройства, дискинезиии /или ригидность / аномальные позы Снижение уровня сознания Дисфункция автономной нервной системы или центральная гиповентиляция 2. По меньшей мере, 1 из следующих результатов лабораторного обследования: Отклонения на ЭЭГ (очаговая или диффузная медленная или дизорганизованная активность, эпилептическая активность или « extreme delta brush ») Плеоцитоз ЦСЖ или олигоклональные цепи 3. Исключение альтернативных причин состояния Graus F. et al. Lancet Neurol 2016; 15:391
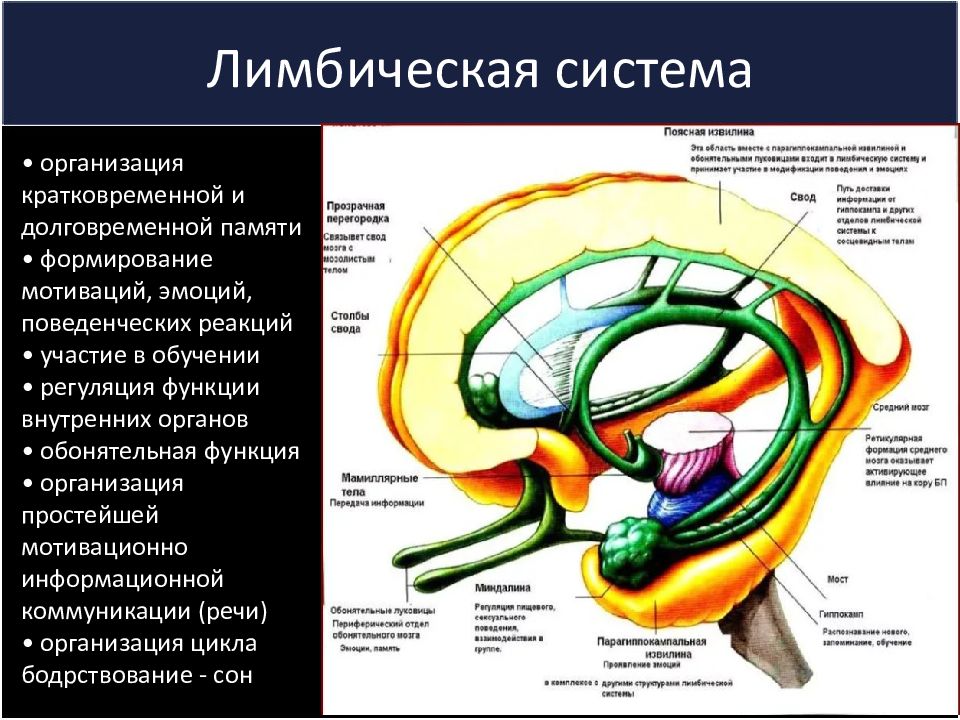
Слайд 25: Лимбическая система
• организация кратковременной и долговременной памяти • формирование мотиваций, эмоций, поведенческих реакций • участие в обучении • регуляция функции внутренних органов • обонятельная функция • организация простейшей мотивационно информационной коммуникации (речи) • организация цикла бодрствование - сон
Слайд 26: Лимбический энцефалит
Лимбический энцефалит – аутоиммунное воспаление в лимбической системе, включая медиальные височные доли, амигдалу и цингулярную извилину. Впервые заболевание было описано Brierley как паранеопластический процесс в 1960 г. Классические варианты описаны преимущественно у взрослых. У детей встречается редко. Клиническая картина лимбического энцефалита складывается из подостро развивающихся когнитивных и поведенческих нарушений, расстройства кратковременной памяти, эпилептических приступов, характерных для височно-долевой локализации эпилептического фокуса, нарушения сна.
Слайд 27: Диагностика ЛЭ
При лимбическом энцефалите возможно обнаружение целого ряда антинейрональных АТ, направленных как к внутриклеточным, так и к внеклеточным антигенам. К внутриклеточным относят АТ к Hu, Ma2, CV2. Именно с внутриклеточными АТ ассоциировано большинство паранеопластических энцефалитов. Повреждение нейронов при выявлении данных АТ является более тяжелым и часто необратимым, плохой ответ на иммуносупрессивную терапию. Внеклеточными антигенами являются вольтаж-зависимые калиевые каналы ( NMDA, AMPA, GABA ). Энцефалиты, ассоциированные с АТ к внеклеточным антигенам, реже имеют связь с онкологическим заболеваниями, характеризуются лучшим прогнозом и хорошим ответом на иммуномодулирующую терапию. При МРТ-исследовании головного мозга определяются явления отека (увеличение сигнала) в режимах Т2 и FLAIR в области медиального виска. В течение нескольких месяцев отек уменьшается и может развиться склероз гиппокампа. На ЭЭГ фиксируется замедление или спайк волновая активность в височных отведениях.
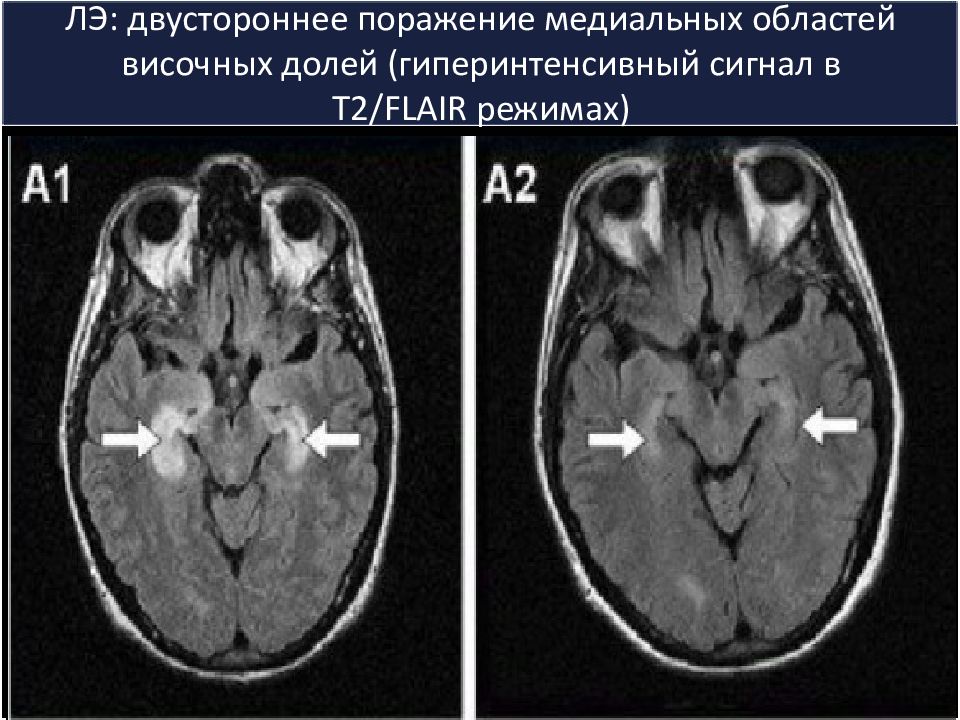
Слайд 28: ЛЭ: двустороннее поражение медиальных областей височных долей (гиперинтенсивный сигнал в Т2/FLAIR режимах)
Слайд 29
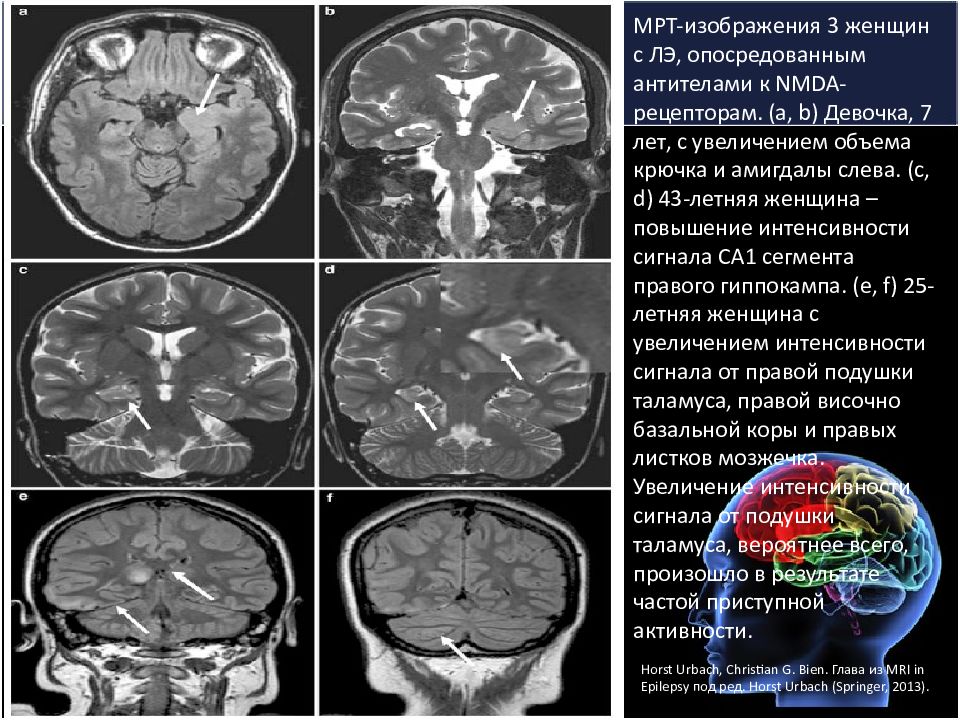
МРТ-изображения 3 женщин с ЛЭ, опосредованным антителами к NMDA-рецепторам. (а, b) Девочка, 7 лет, с увеличением объема крючка и амигдалы слева. (c, d) 43-летняя женщина – повышение интенсивности сигнала СА1 сегмента правого гиппокампа. (e, f) 25-летняя женщина с увеличением интенсивности сигнала от правой подушки таламуса, правой височно базальной коры и правых листков мозжечка. Увеличение интенсивности сигнала от подушки таламуса, вероятнее всего, произошло в результате частой приступной активности. Horst Urbach, Christian G. Bien. Глава из MRI in Epilepsy под ред. Horst Urbach (Springer, 2013).
Слайд 30
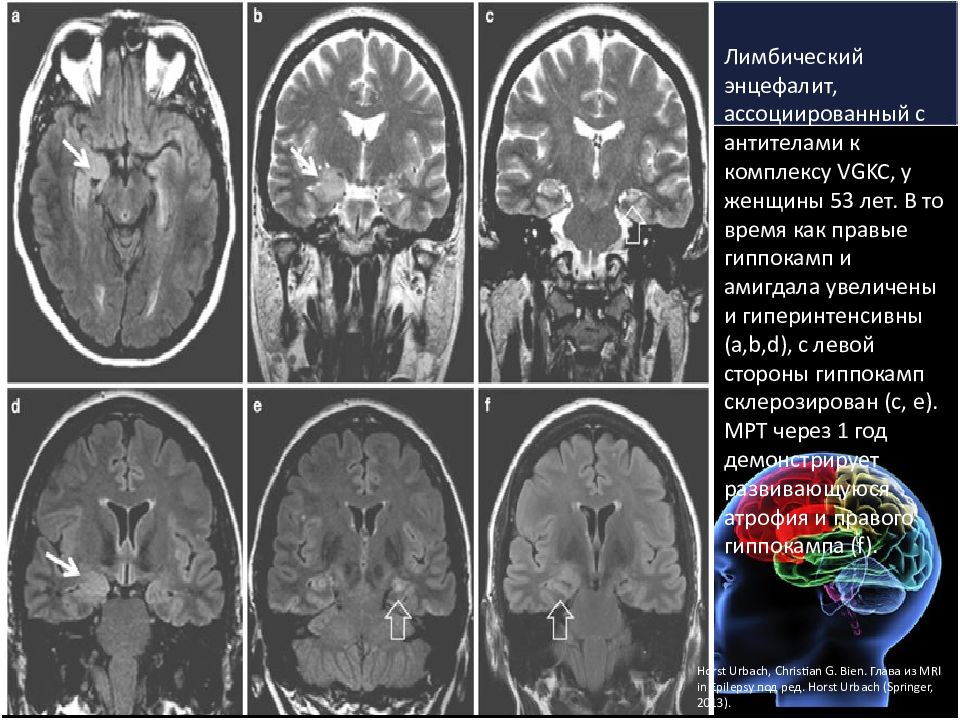
Horst Urbach, Christian G. Bien. Глава из MRI in Epilepsy под ред. Horst Urbach (Springer, 2013). Лимбический энцефалит, ассоциированный с антителами к комплексу VGKC, у женщины 53 лет. В то время как правые гиппокамп и амигдала увеличены и гиперинтенсивны (a,b,d), с левой стороны гиппокамп склерозирован (с, е). МРТ через 1 год демонстрирует развивающуюся атрофия и правого гиппокампа (f).
Слайд 31
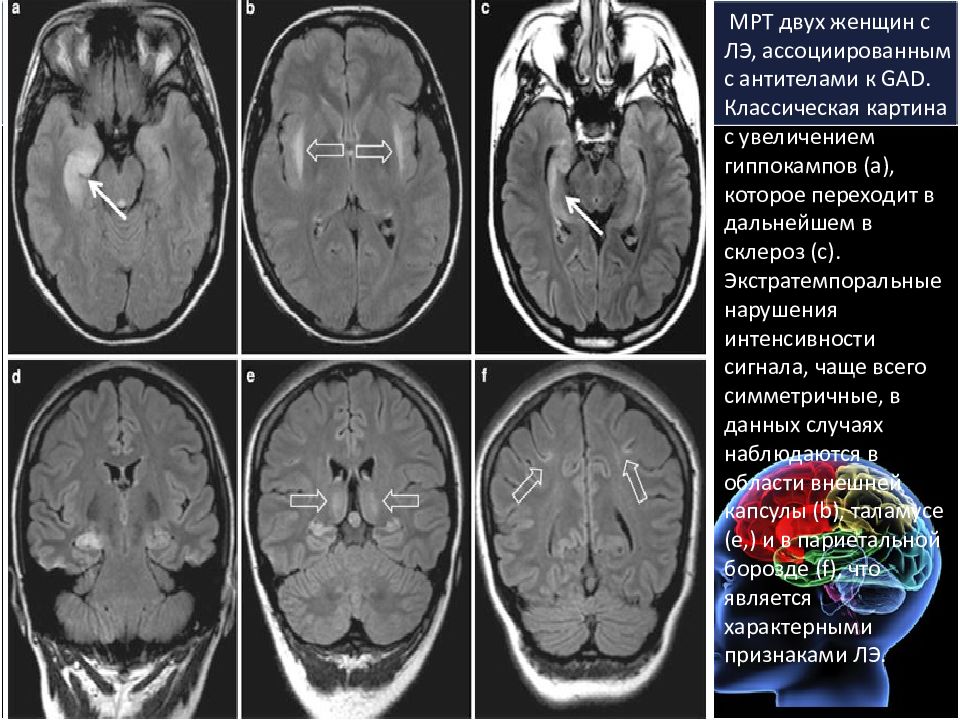
МРТ двух женщин с ЛЭ, ассоциированным с антителами к GAD. Классическая картина с увеличением гиппокампов (а), которое переходит в дальнейшем в склероз (с). Экстратемпоральные нарушения интенсивности сигнала, чаще всего симметричные, в данных случаях наблюдаются в области внешней капсулы (b), таламусе (е,) и в париетальной борозде (f), что является характерными признаками ЛЭ.
Слайд 32: Диагностические критерии установленного ЛЭ
Диагноз ЛЭ может быть установлен, когда имеются все четыре из нижеперечисленных критериев: Подострое начало (быстрое прогрессирование в течение 3 месяцев и менее) нарушений кратковременной памяти, судорог, психиатрических нарушений, предполагающих вовлечение лимбической системы Двусторонние патологические отклонения на Т2/FLAIR режимах МРТ, ограниченные медиальными зонами височных долей По меньшей мере, одно из следующих: Плейоцитоз ЦСЖ ≥5/ мкл Изменения на ЭЭГ с эпилептической или медленно-волновой активностью, вовлекающей височные доли 4. Исключение альтернативных причин состояния (прежде всего, ВПГ-1 энцефалита ). Graus F. et al. Lancet Neurol 2016; 15:391
Слайд 34
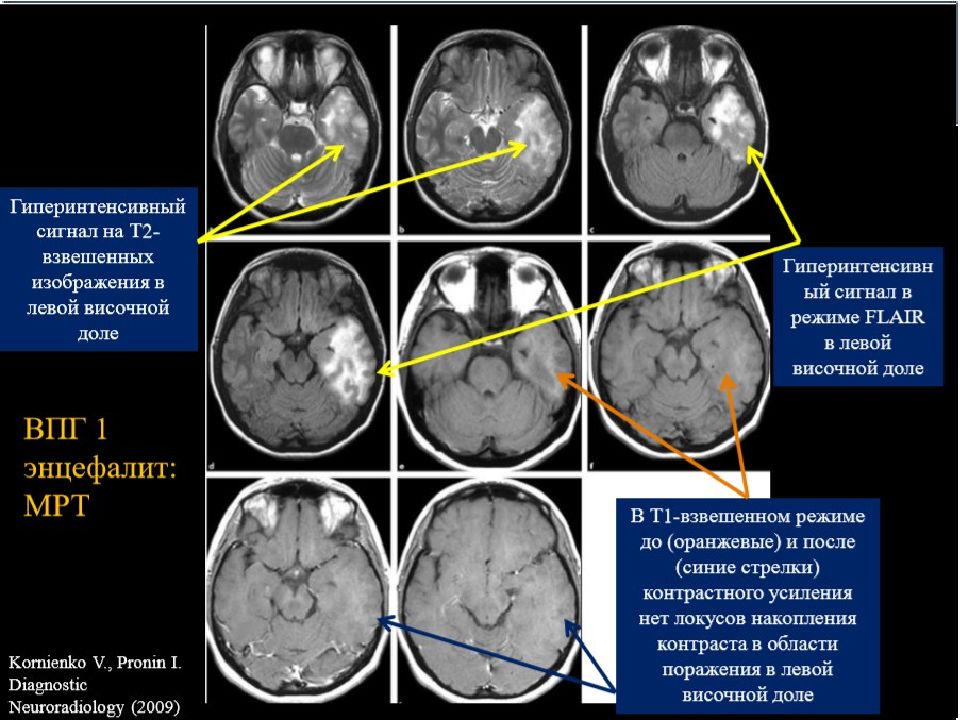
Крайне проблематично (если вообще возможно) дифференцировать между инфекционным и аутоиммунным генезом энцефалита на основании клинических данных и общедоступных параклинических (общеклиническое исследование ЦСЖ, ЭЭГ, МРТ) исследований. При любом синдроме энцефалита / энцефалопатии помним про герпетический энцефалит!
Слайд 36
Шизофрения, так как именно с этим диагнозом пациент изначально попадает в психиатрическую больницу на фоне развивающегося острого психоза.
Слайд 37: Дебют психиатрического заболевания или анти-NMDAR-энцефалит?
У каждого пациента с впервые возникшим эпизодом психоза важно вначале исключить органическое поражение нервной системы. В ноябре 2019 года в журнале Lancet Psychiatry опубликован международный консенсус по подходам к диагностике и лечению психозов аутоиммунного генеза. Для раннего выявления пациентов с аутоиммунным энцефалитом в психиатрической практике предложены две группы критериев: «желтые флаги», когда наличие хотя бы одного признака предполагает включение аутоиммунного энцефалита в дифференциальный диагноз, и «красные флаги», когда наличие даже одного из критериев данной группы предполагает обязательное обследование на антинейрональные антитела у пациентов с психотической симптоматикой.
Слайд 38: Дебют психиатрического заболевания или анти-NMDAR-энцефалит?
Непереносимость / аномальные реакции на применение нейролептиков как возможный признак аутоиммунного энцефалита.
Слайд 39: Подтверждение диагноза аутоиммунного энцефалита
- определение специфических аутоАТ в крови и/или ЦСЖ Скрининг на АТ к глутаматным рецепторам ( анти-NMDAR NR1 АТ IgG ) и АТ VGKC-комплекса ( LG1,CASPR2 ) - наиболее распространены Определение панели онконевральных АТ ( Hu, Ma2 CV2/CRMP5, Ri, amphiphysin и др.) При отрицательном результате либо подозрении на более редкий синдром аутоиммунного поражения ЦНС – дополнительное определение других АТ (оптимально в условиях референс -лаборатории, способной в том числе выявлять ранее не описанные АТ) При недоступности диагностики – иммуносупрессивная терапия с последующей оценкой ее эффективности (диагностика ex juvantibus ). Zuliani L. et al. J Neurol Neurosurg Psychiatry 2012; 83:638
Слайд 40: Подтверждение диагноза аутоиммунного энцефалита
Для выявления АТ к NMDAR оптимально использовать ЦСЖ Титры АТ в ЦСЖ и сыворотке крови выше у пациентов с неблагоприятным исходом заболевания и тератомами Титры АТ в ЦСЖ лучше коррелируют с вероятностью рецидива заболевания по сравнению с титрами АТ в сыворотке крови
Слайд 41: Терапия аутоиммунных поражений ЦНС
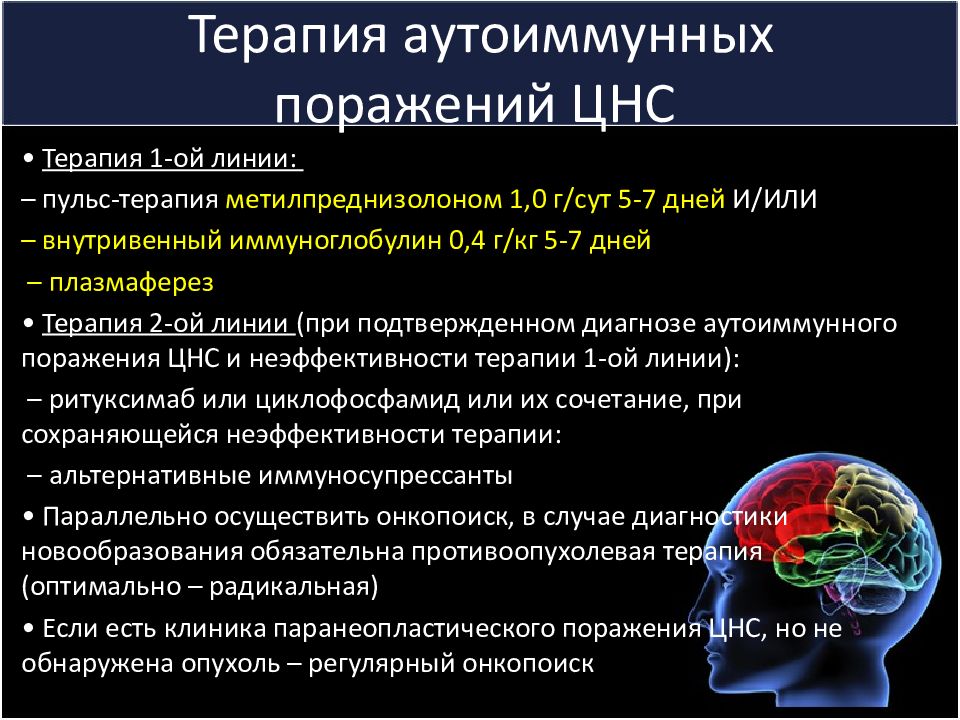
• Терапия 1-ой линии: – пульс-терапия метилпреднизолоном 1,0 г/сут 5-7 дней И/ИЛИ – внутривенный иммуноглобулин 0,4 г/кг 5-7 дней – плазмаферез • Терапия 2-ой линии (при подтвержденном диагнозе аутоиммунного поражения ЦНС и неэффективности терапии 1-ой линии): – ритуксимаб или циклофосфамид или их сочетание, при сохраняющейся неэффективности терапии: – альтернативные иммуносупрессанты • Параллельно осуществить онкопоиск, в случае диагностики новообразования обязательна противоопухолевая терапия (оптимально – радикальная) • Если есть клиника паранеопластического поражения ЦНС, но не обнаружена опухоль – регулярный онкопоиск
Последний слайд презентации: Аутоиммунный энцефалит: Литература
статья «Аутоиммунные энцефалиты: болезнь XXI века на перекрестке неврологии и психиатрии» В.В. Фоминых, Е.А. Фрей, Л.В. Брылев, Н.В. Гуляева; ФГБУН Институт высшей нервной деятельности и нейрофизиологии, Москва; Городская клиническая больница им. В.М. Буянова ДЗМ, Москва; Госпиталь университета г. Осло, Норвегия; ГБУЗ Научно-практический центр психоневрологии ДЗМ, Москва (журнал «Нейрохимия» №4, 2018) статья «Аутоиммунные энцефалиты» М.В. Давыдовская, А.Н. Бойко, И.А. Беляева, М.Ю. Мартынов, Е.И. Гусев; Кафедра неврологии, нейрохирургии и медицинской генетики лечебного факультета ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова», Москва (Журнал неврологии и психиатрии, №4, 2015) презентация «Аутоиммунный энцефалит: что нужно знать психиатру» Доцент Н.В. Соловей, Белорусский государственный медицинский университет, Кафедра инфекционных болезней, 2018 статья «Аутоиммунный энцефалит с антителами к NMDA-рецепторам» Е.Е. Васенина, О.С. Левин, О.А. Ганькина, А.Ш. Чимагомедова, Д.И. Левиков; ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва; ГБУЗ «Городская клиническая больница им. С.П. Боткина», Москва, Россия (Журнал неврологии и психиатрии, №2, 2017) статья «Аутоиммунные энцефалиты. Современные данные об этиологии, патогенезе, особенностях клиники, диагностики и лечения» Кутько И.И., Гусова А.Б., Белозоров А.П. (газета «Новости медицины и фармации», №6 (575), 2016) статья Куликова С.Л., Лихачев С.А. Республиканский научно-практический центр неврологии и нейрохирургии, Минск, Беларусь статья АНТИТЕЛА К NMDA-РЕЦЕПТОРАМ: АУТОИММУННЫЙ ЭНЦЕФАЛИТ И ПСИХОТИЧЕСКИЕ РАССТРОЙСТВА А.А. Мурашко Московский научно-исследовательский институт психиатрии – филиал ФБГУ «НМИЦ ПН им. В.П.Сербского» Минздрава России https://medvestnik.by/konspektvracha/autoimmunnyj-entsefalit Horst Urbach, Christian G. Bien. Глава из MRI in Epilepsy под ред. Horst Urbach (Springer, 2013).