Первый слайд презентации: Испарение и конденсация. Кипение жидкости
Слайд 2: Фазовые переходы
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. Переход из одного состояния в другое называется фазовым переходом. Твердое тело Газ Жидкость
Слайд 3: Парообразование
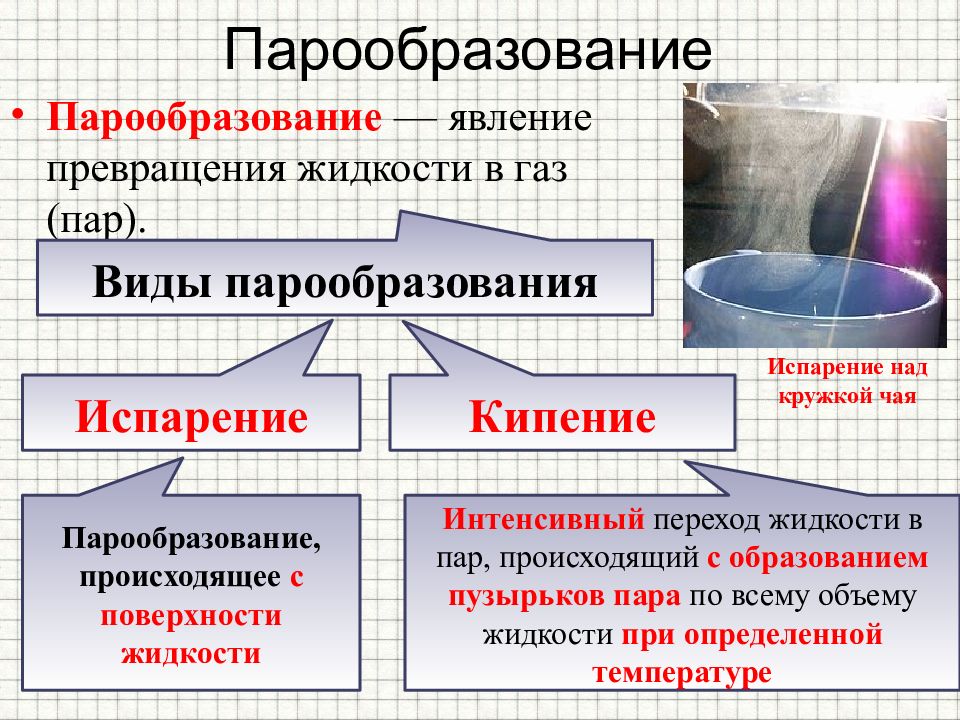
Парообразование — явление превращения жидкости в газ (пар). Испарение над кружкой чая Виды парообразования Испарение Кипение Парообразование, происходящее с поверхности жидкости Интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре
Слайд 4: Испарение
- это парообразование с поверхности жидкости. При испарении жидкость покидают более быстрые молекулы, обладающие большей скоростью. Испарение происходит при любой температуре, т.к. при любой температуре в жидкости находятся такие молекулы, которые обладают достаточной кинетической энергией, чтобы преодолеть силы сцепления между молекулами и совершить работу выхода из жидкости.
Слайд 5: От чего зависит скорость испарения?
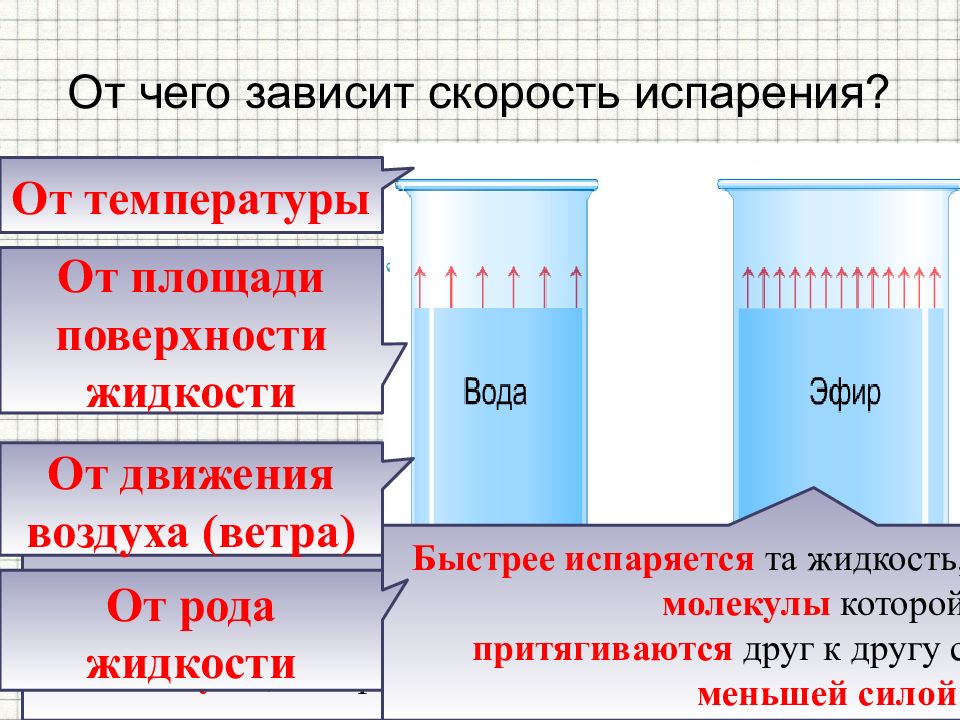
Чем выше температура жидкости, тем больше скорость движения молекул, у которых кинетическая энергия достаточна, чтобы преодолеть притяжение соседних молекул и вылететь с поверхности жидкости. Жидкость могут покинуть только те молекулы, которые находятся у самой поверхности. Чем больше площадь испаряемой поверхности, тем большее число молекул одновременно вылетают из жидкости. Молекула, вылетевшая из жидкости, может вернуться обратно в жидкость. Если дует ветер, который уносит эти молекулы, испарение происходит быстрее От температуры От площади поверхности жидкости От движения воздуха (ветра) Быстрее испаряется та жидкость, молекулы которой притягиваются друг к другу с меньшей силой. От рода жидкости
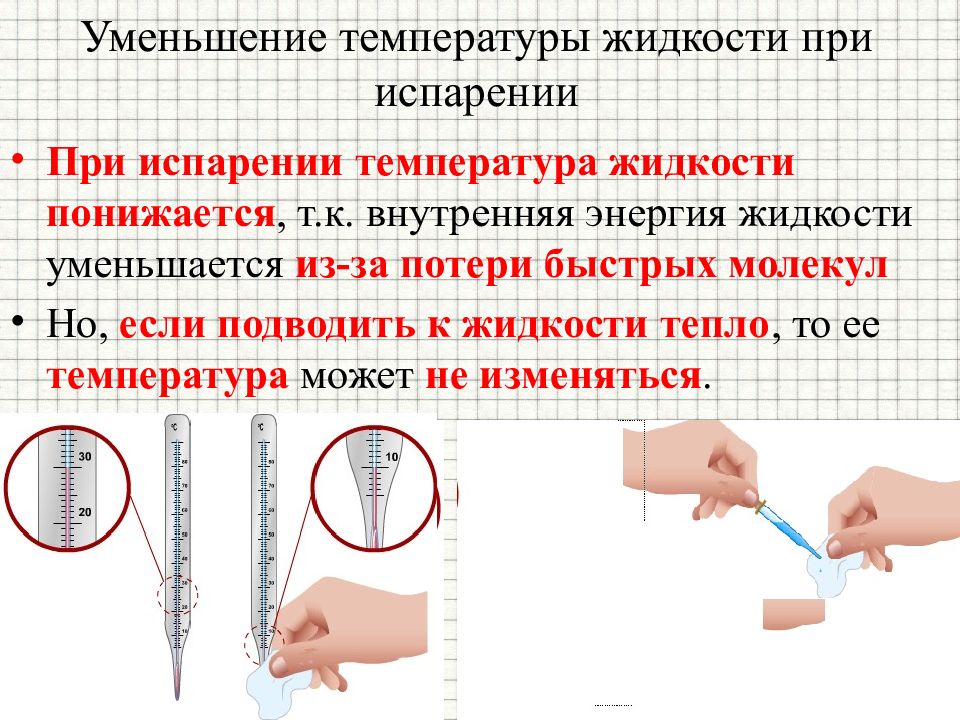
При испарении температура жидкости понижается, т.к. внутренняя энергия жидкости уменьшается из-за потери быстрых молекул Но, если подводить к жидкости тепло, то ее температура может не изменяться.
Слайд 7: Возгонка и сублимация
Существует ещё один интересный вид парообразования, когда твердое тело, минуя жидкое состояние, превращается в газ - возгонка. Такой особенностью обладают, например, кристаллы йода, нафталина, обычного и "сухого" льда. Возгонка льда возможна практически при любой отрицательной температуре в сухом воздухе, что практически бывает при сильном морозе. Обратный процесс превращения газа непосредственно в твердое вещество называется сублимацией (иней на деревьях и снег в тучах). Центрами кристаллизации здесь служат микроскопические пылинки и кристаллики соли, взвешенные в воздухе.
Слайд 8: Конденсация
Процесс превращения пара в жидкость называется конденсацией. Конденсация пара сопровождается выделением энергии ; Пары воды в верхних (холодных) слоях атмосферы превращаются в облака Летним вечером или под утро, когда становится холоднее, выпадает роса
Слайд 9: Кипение жидкости
Кипение - это интенсивное парообразование, которое происходит при нагревании жидкости не только с поверхности, но и внутри неё. Кипение возможно лишь при определенной температуре – температуре кипения; Кипение начинается лишь после того, как давление внутри пузырьков сравнивается с давлением в окружающей жидкости; Во время кипения температура жидкости и пара над ней не меняется.
Слайд 10: Температура кипения
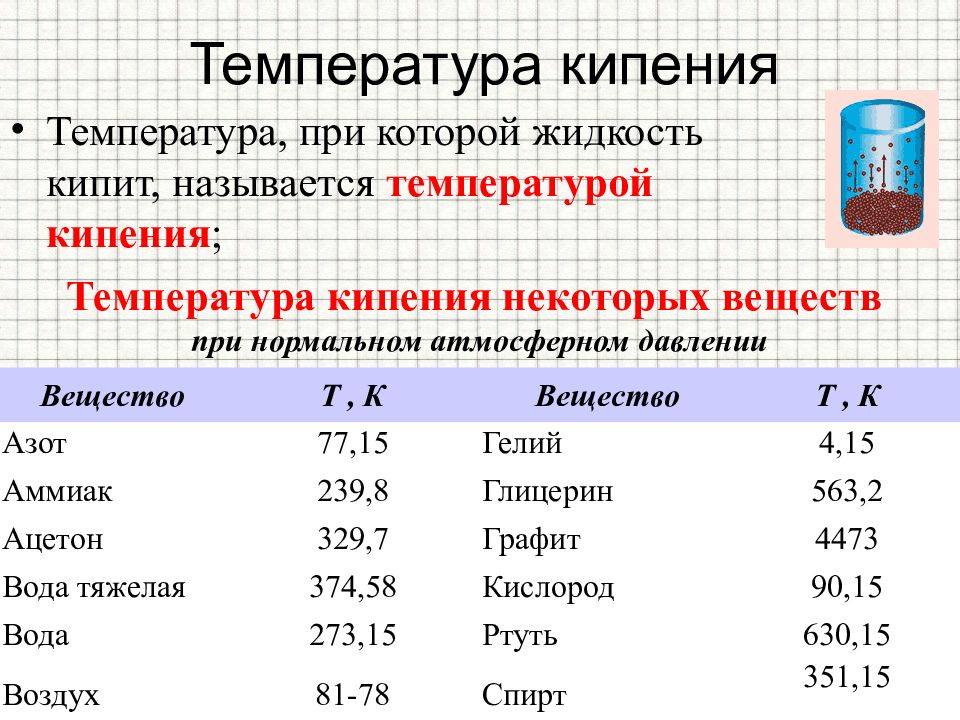
Температура, при которой жидкость кипит, называется температурой кипения ; Температура кипения некоторых веществ при нормальном атмосферном давлении Вещество Т, К Вещество Т, К Азот 77,15 Гелий 4,15 Аммиак 239,8 Глицерин 563,2 Ацетон 329,7 Графит 4473 Вода тяжелая 374,58 Кислород 90,15 Вода 273,15 Ртуть 630,15 Воздух 81-78 Спирт 351,15
Слайд 11: Процесс кипения
Кипение происходит с поглощением теплоты. Жидкость Кипение Пар (газ) Q Большая часть подводимой теплоты расходуется на разрыв связей между частицами вещества, остальная часть - на работу, совершаемую при расширении пара. В результате энергия взаимодействия между частицами пара становится больше, чем между частицами жидкости, поэтому внутренняя энергия пара больше, чем внутренняя энергия жидкости при той же температуре.
Слайд 12: Механизм кипения воды
При нагревании испарение с поверхности воды усиливается. Появление в жидкости многочисленных мелких пузырьков воздуха, растворённого в воде. При нагревании излишек воздуха выделяется в виде пузырьков с насыщенным водяным паром - испарение внутрь жидкости. Пузырьки становятся крупнее и многочисленнее. Архимедова сила, действующая на пузырьки, возрастает и при температуре близкой к кипению они всплывают. С приближением к поверхности объём пузырьков резко возрастает, на поверхности они лопаются, находящийся в них насыщенный пар выходит в атмосферу – слышен характерный шум – вода кипит.
Слайд 13: Удельная теплота парообразования
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования. Единица удельной теплоты парообразования в системе СИ: [ L ] = 1 Дж/ кг С ростом давления удельная теплота парообразования уменьшается и наоборот.
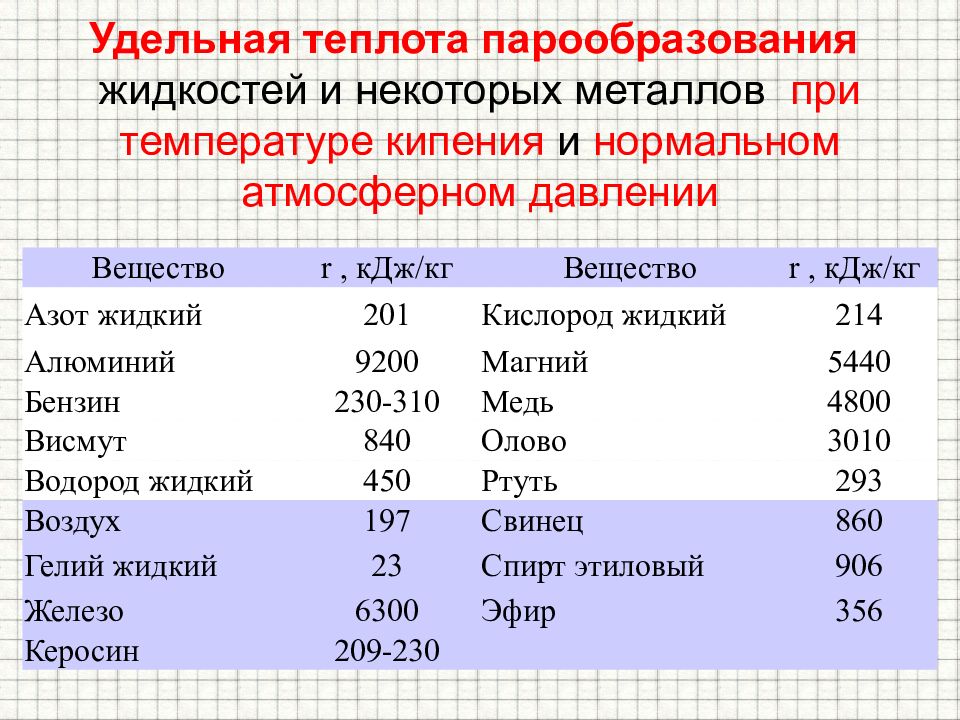
Слайд 14: Удельная теплота парообразования жидкостей и некоторых металлов при температуре кипения и нормальном атмосферном давлении
Вещество r, кДж/кг Вещество r, кДж/кг Азот жидкий 201 Кислород жидкий 214 Алюминий 9200 Магний 5440 Бензин 230-310 Медь 4800 Висмут 840 Олово 3010 Водород жидкий 450 Ртуть 293 Воздух 197 Свинец 860 Гелий жидкий 23 Спирт этиловый 906 Железо 6300 Эфир 356 Керосин 209-230 Удельная теплота парообразования жидкостей и некоторых металлов при температуре кипения и нормальном атмосферном давлении
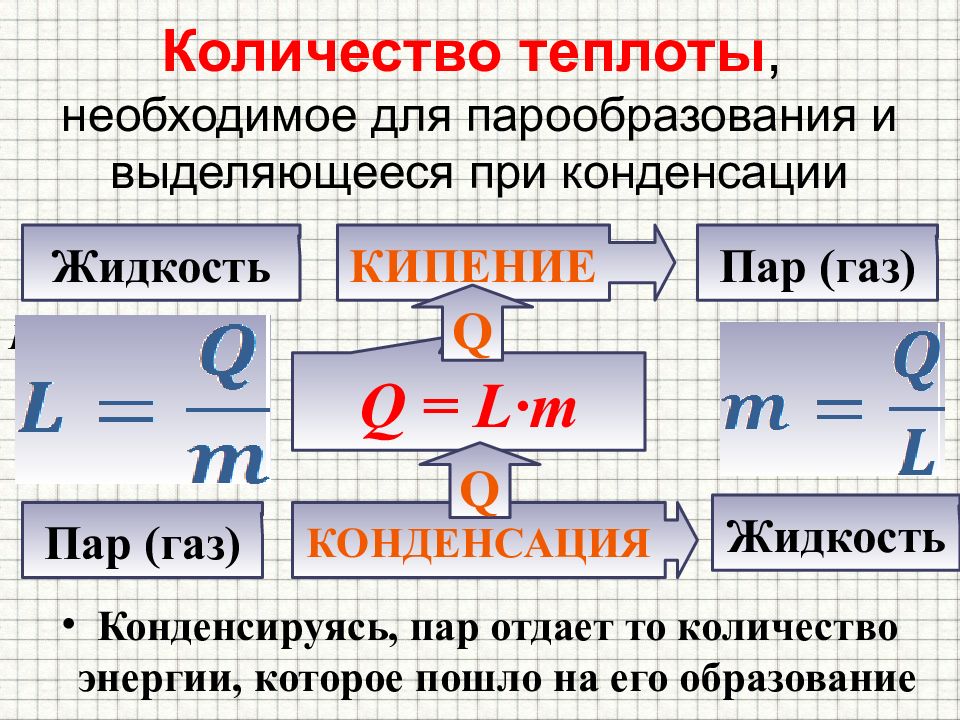
Слайд 15: Количество теплоты, необходимое для парообразования и выделяющееся при конденсации
Конденсируясь, пар отдает то количество энергии, которое пошло на его образование Пар (газ) Конденсация Жидкость Жидкость Кипение Пар (газ) Q = L·m Q Q L – удельная теплота парообразования m – масса вещества
Слайд 16
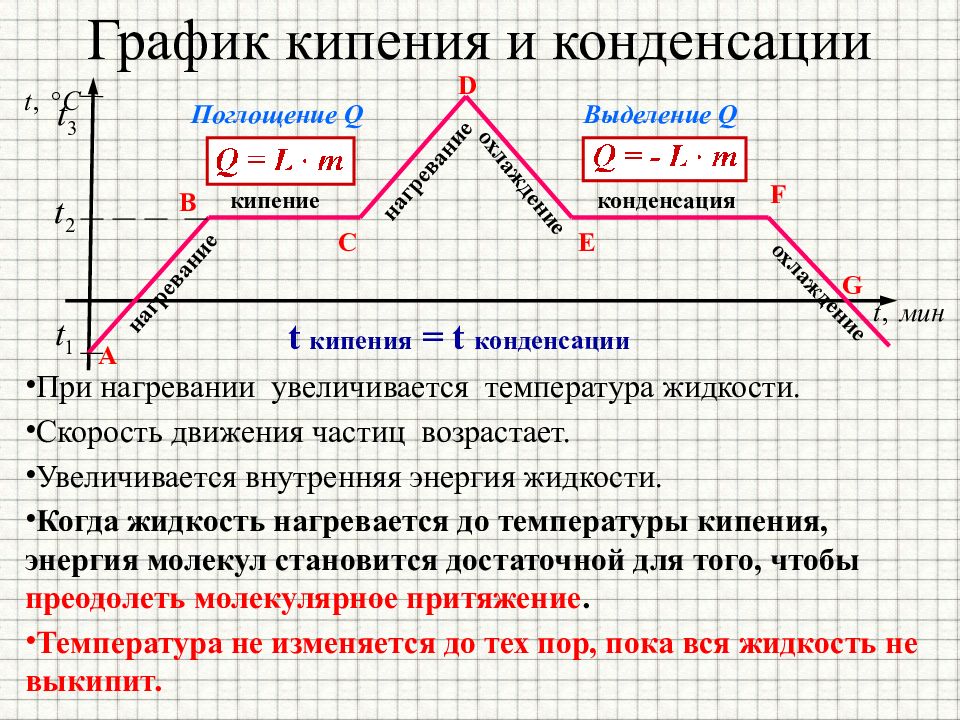
кипение нагревание конденсация охлаждение Поглощение Q Выделение Q t кипения = t конденсации График кипения и конденсации А B C D E F G нагревание охлаждение При нагревании увеличивается температура жидкости. Скорость движения частиц возрастает. Увеличивается внутренняя энергия жидкости. Когда жидкость нагревается до температуры кипения, энергия молекул становится достаточной для того, чтобы преодолеть молекулярное притяжение. Температура не изменяется до тех пор, пока вся жидкость не выкипит.
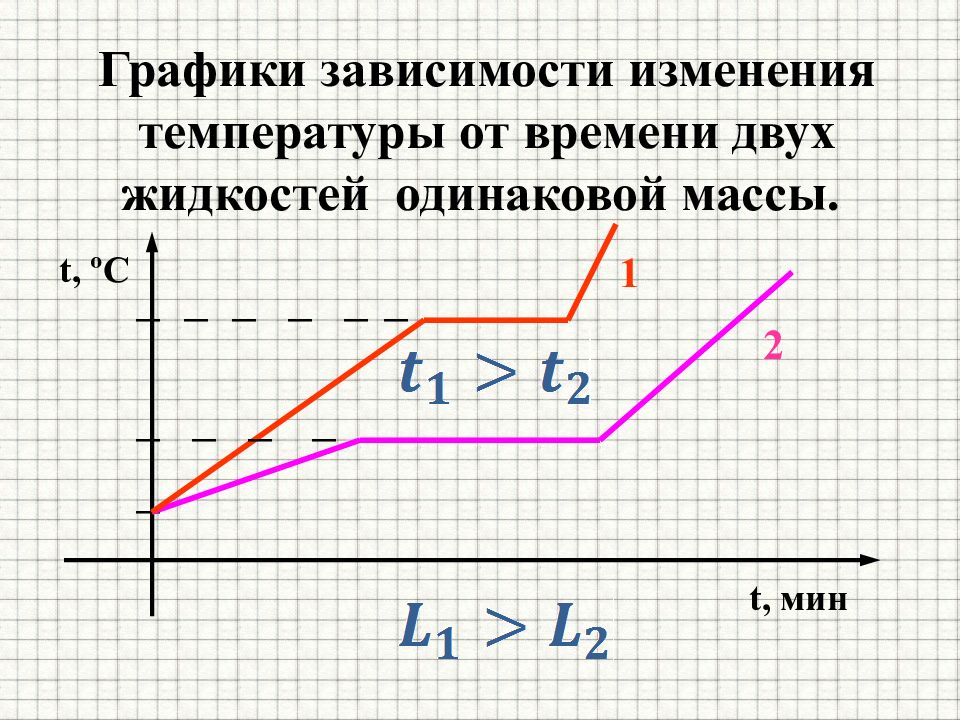
Слайд 17: Графики зависимости изменения температуры от времени двух жидкостей одинаковой массы
t, мин 1 2 t, ºC
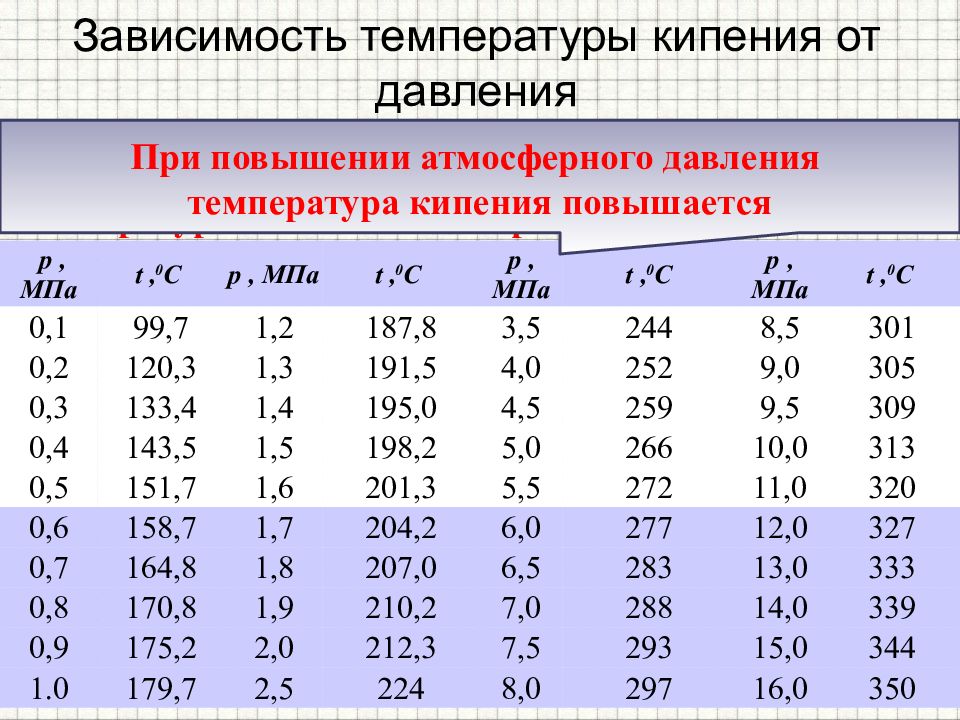
Слайд 18: Зависимость температуры кипения от давления
Температура кипения зависит от давления, оказываемого на свободную поверхность жидкости. Температура кипения воды при различных давлениях. р, МПа t, 0 C р, МПа t, 0 C р, МПа t, 0 C р, МПа t, 0 C 0,1 99,7 1,2 187,8 3,5 244 8,5 301 0,2 120,3 1,3 191,5 4,0 252 9,0 305 0,3 133,4 1,4 195,0 4,5 259 9,5 309 0,4 143,5 1,5 198,2 5,0 266 10,0 313 0,5 151,7 1,6 201,3 5,5 272 11,0 320 0,6 158,7 1,7 204,2 6,0 277 12,0 327 0,7 164,8 1,8 207,0 6,5 283 13,0 333 0,8 170,8 1,9 210,2 7,0 288 14,0 339 0,9 175,2 2,0 212,3 7,5 293 15,0 344 1.0 179,7 2,5 224 8,0 297 16,0 350 При повышении атмосферного давления температура кипения повышается
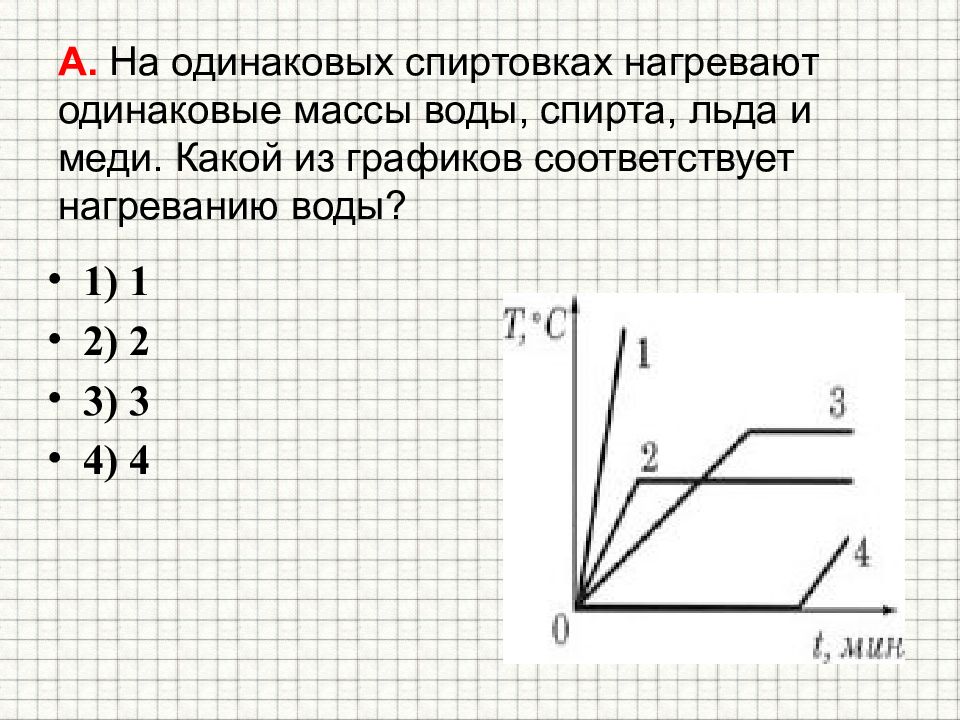
Слайд 20: А. На одинаковых спиртовках нагревают одинаковые массы воды, спирта, льда и меди. Какой из графиков соответствует нагреванию воды?
1) 1 2) 2 3) 3 4) 4
Слайд 21: Б. Жидкости могут испаряться
1) только при температуре кипения 2) только при температуре выше ее температуры кипения 3) только при температуре, близкой к ее температуре кипения 4) при любой температуре
Слайд 22: В. Часть воды частично испарилась из чашки при отсутствии теплообмена с окружающей средой. Температура воды, оставшейся в чашке
1) повысилась 2) понизилась 3) не изменилась 4) повысилась или понизилась, в зависимости от скорости испарения
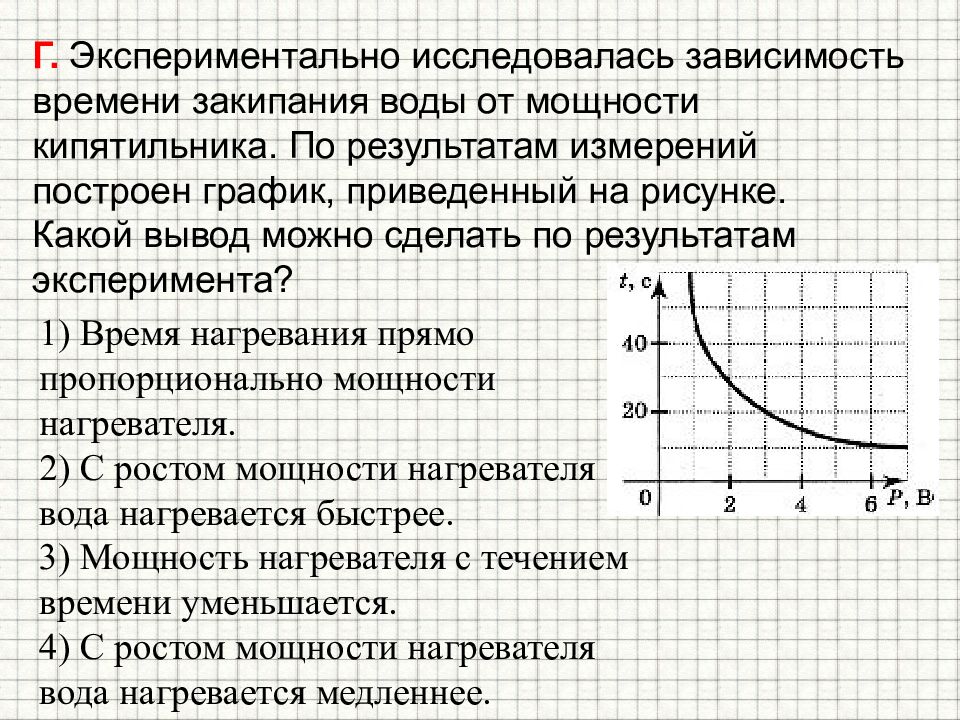
Слайд 23: Г. Экспериментально исследовалась зависимость времени закипания воды от мощности кипятильника. По результатам измерений построен график, приведенный на рисунке. Какой вывод можно сделать по результатам эксперимента?
1) Время нагревания прямо пропорционально мощности нагревателя. 2) С ростом мощности нагревателя вода нагревается быстрее. 3) Мощность нагревателя с течением времени уменьшается. 4) С ростом мощности нагревателя вода нагревается медленнее.
Слайд 24: Д. Какое количество теплоты потребуется, чтобы испарить 200 г воды, взятой при температуре кипения?
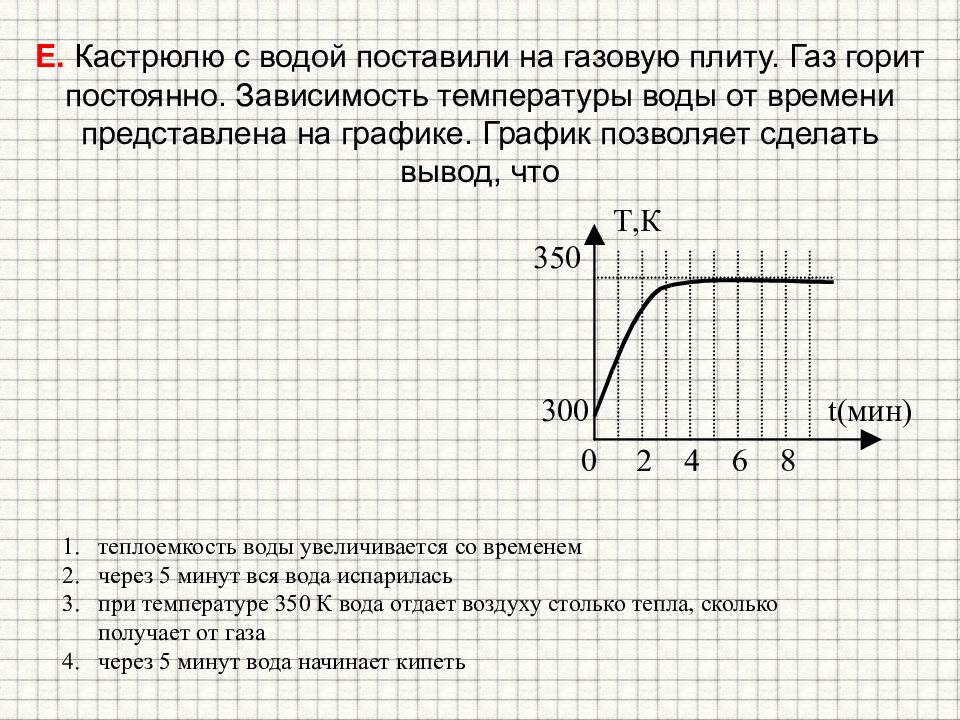
Слайд 25: Е. Кастрюлю с водой поставили на газовую плиту. Газ горит постоянно. Зависимость температуры воды от времени представлена на графике. График позволяет сделать вывод, что
теплоемкость воды увеличивается со временем через 5 минут вся вода испарилась при температуре 350 К вода отдает воздуху столько тепла, сколько получает от газа через 5 минут вода начинает кипеть
Слайд 26: Ж. Испарение жидкости происходит потому, что
разрушается кристаллическая решетка. самые быстрые частицы покидают жидкость. самые медленные частицы покидают жидкость. самые крупные частицы покидают жидкость.
Слайд 27: З. При испарении жидкость остывает. Молекулярно-кинетическая теория объясняет это тем, что чаще всего жидкость покидают молекулы, кинетическая энергия которых
равна средней кинетической энергии молекул жидкости превышает среднюю кинетическую энергию молекул жидкости меньше средней кинетической энергии молекул жидкости равна суммарной кинетической энергии молекул жидкости