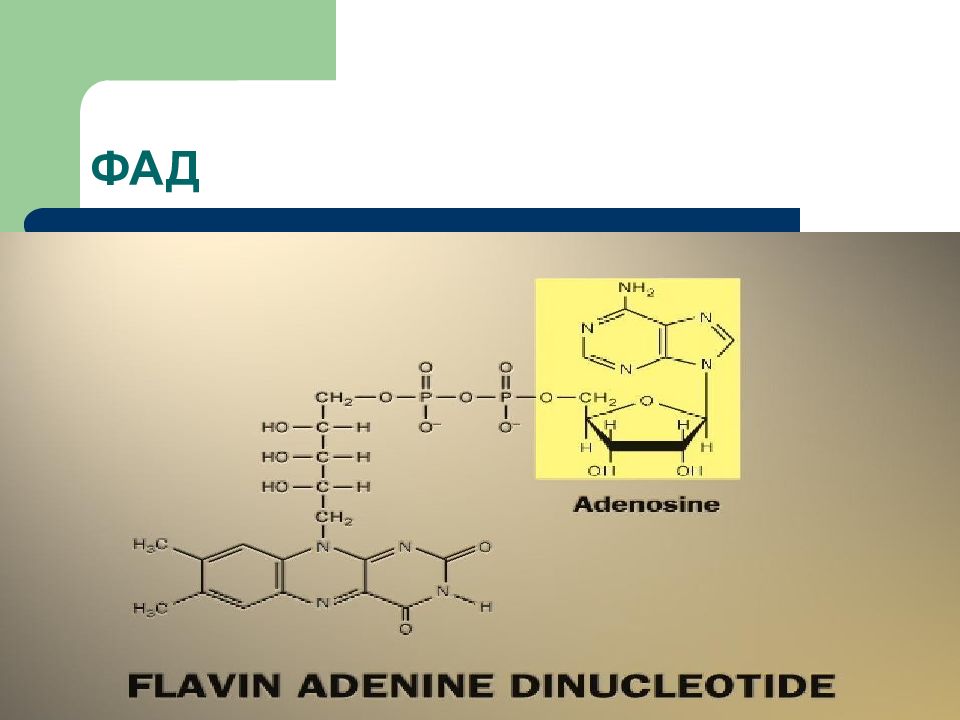
Первый слайд презентации
Лекция: Биологическое окисление. Окислительное фосфорилирование.
Слайд 2: ФИЗИОЛОГИЯ ДЫХАНИЯ
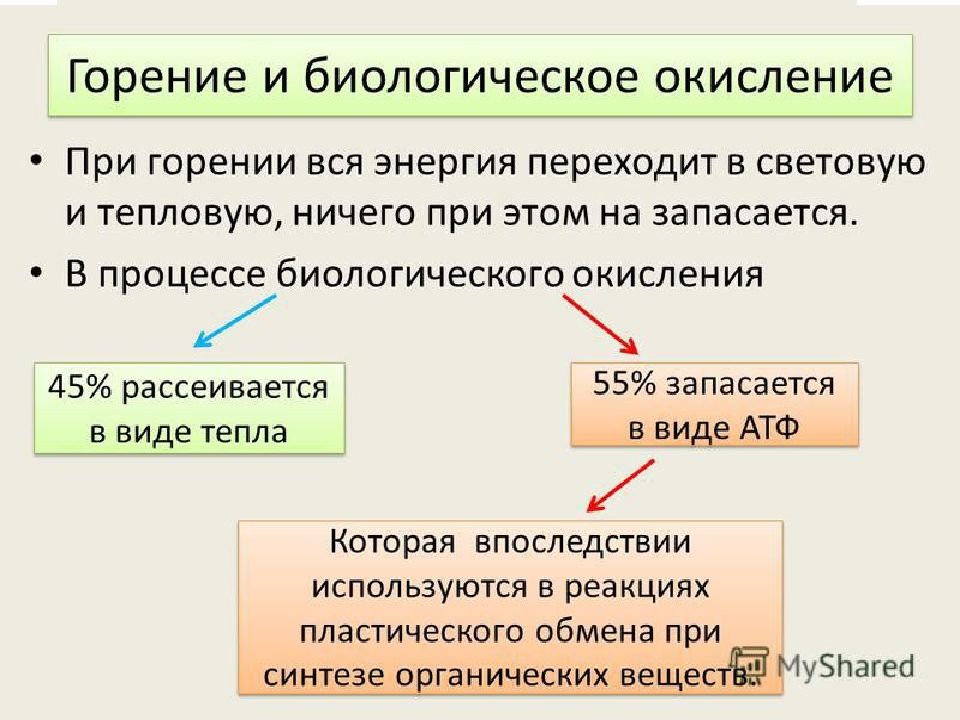
Слайд 3: Биологическое окисление
- Это совокупность окислительно-восстановительных реакций, сопровождающихся передачей протонов и электронов.
Слайд 4: ОСНОВНАЯ РОЛЬ:
Обеспечить организм энергией в доступной для использования форме (АТФ).
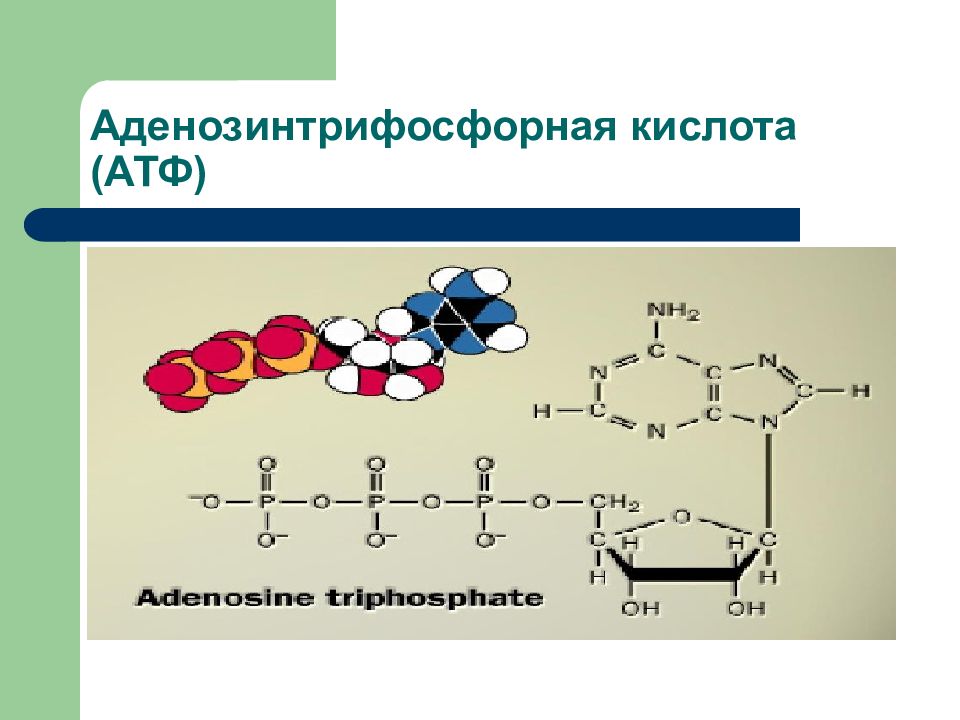
Слайд 5: Аденозинтрифосфорная кислота (АТФ)
Слайд 9: Тканевое дыхание
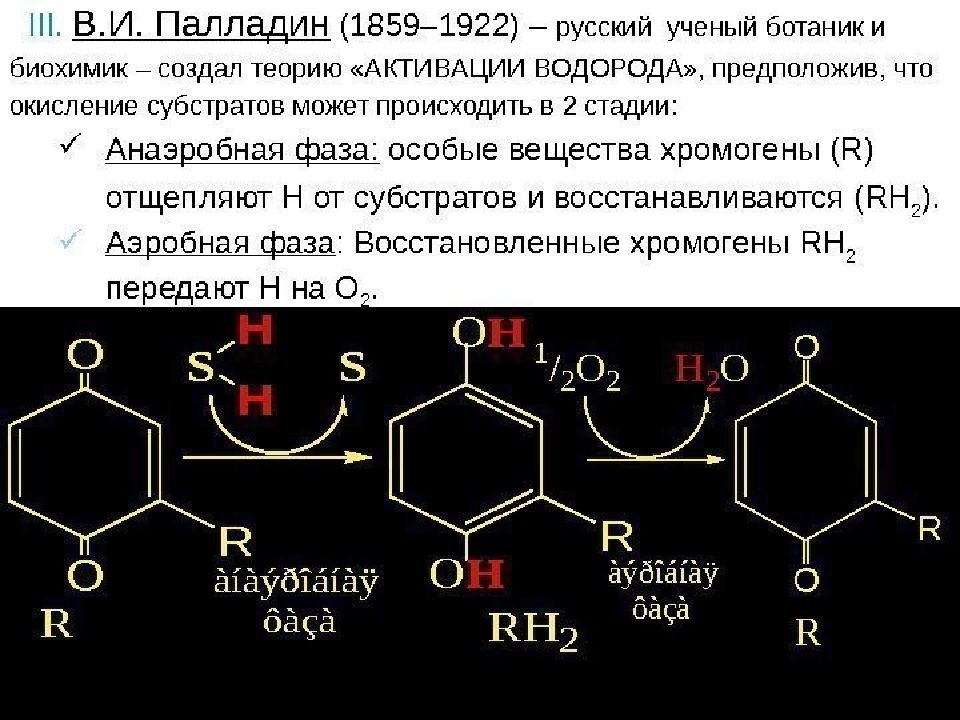
Вдыхаемый О 2 используется для синтеза Н 2 О за счет Н 2 окисляемых S : SH 2 + ½ O 2 ==> S + H 2 O
Слайд 12
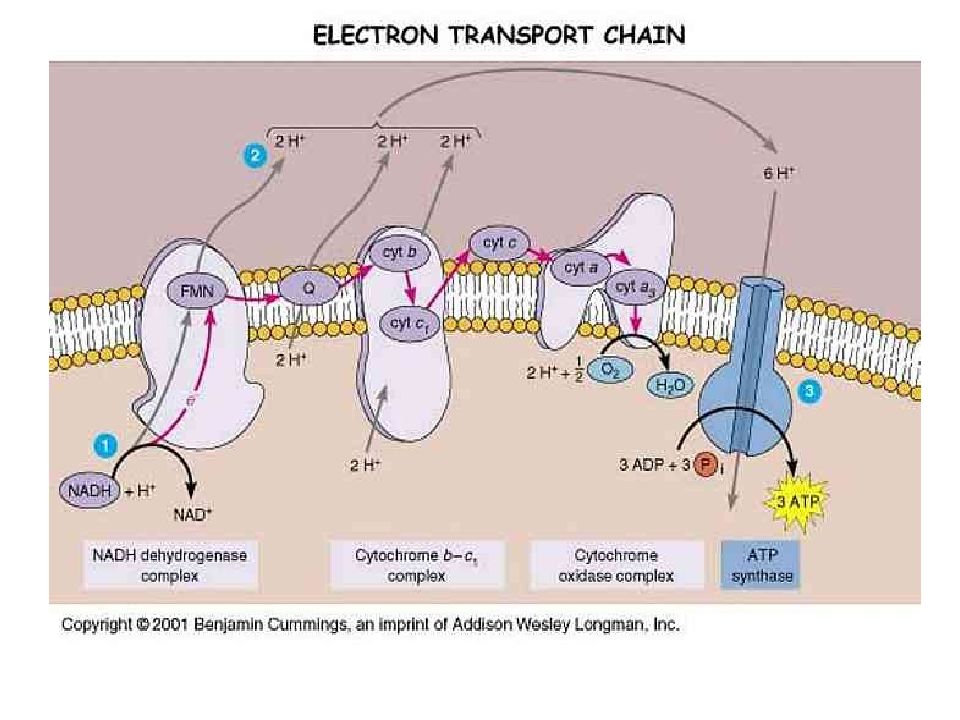
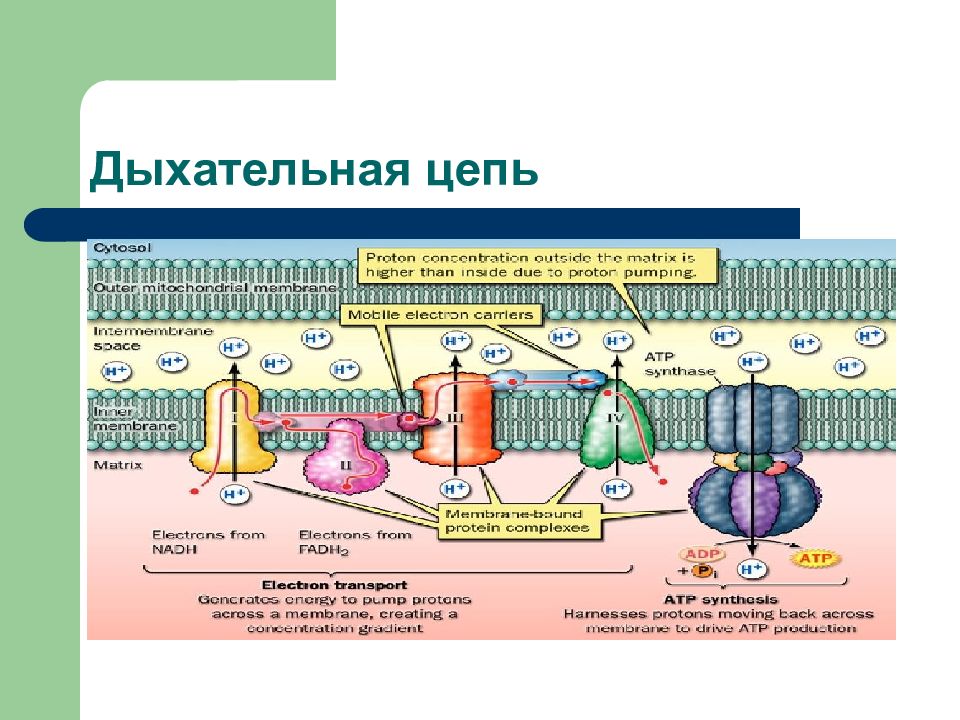
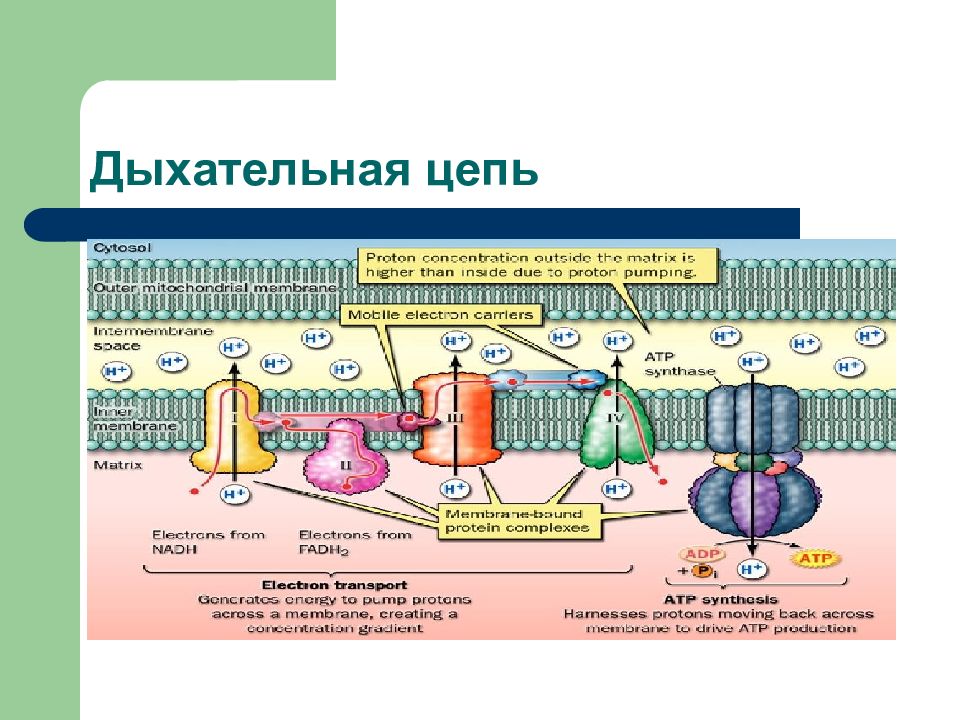
Переносчики электронов и протонов образуют цепь переноса электронов ( ЦПЭ) или дыхательную цепь ( ДЦ).
Слайд 13: ЦПЭ и МИТОХОНДРИИ
Все ферменты ЦПЭ связаны с МХ. 1 гепатоцит содержит около 1000 МХ.
Слайд 15: ФЕРМЕНТЫ НАРУЖНОЙ МЕМБРАНЫ
Моноаминооксидаза Система удлинения цепи жирных кислот Фосфолипаза А
Слайд 16: ФЕРМЕНТЫ ВНУТР.МЕМБРАНЫ
НАДН-дегидрогеназа Сукцинатдегидрогеназа Цитохромы в,с 1, с, а, а 3 Н+-АТФ-синтаза АДФ-АТФ-транслоказа
Слайд 17: ФЕРМЕНТЫ МАТРИКСА
Ферменты ЦТК (кроме сукцинатдегидрогеназы ) Ферменты бета-окисления ЖК Глутаматдегидрогеназа
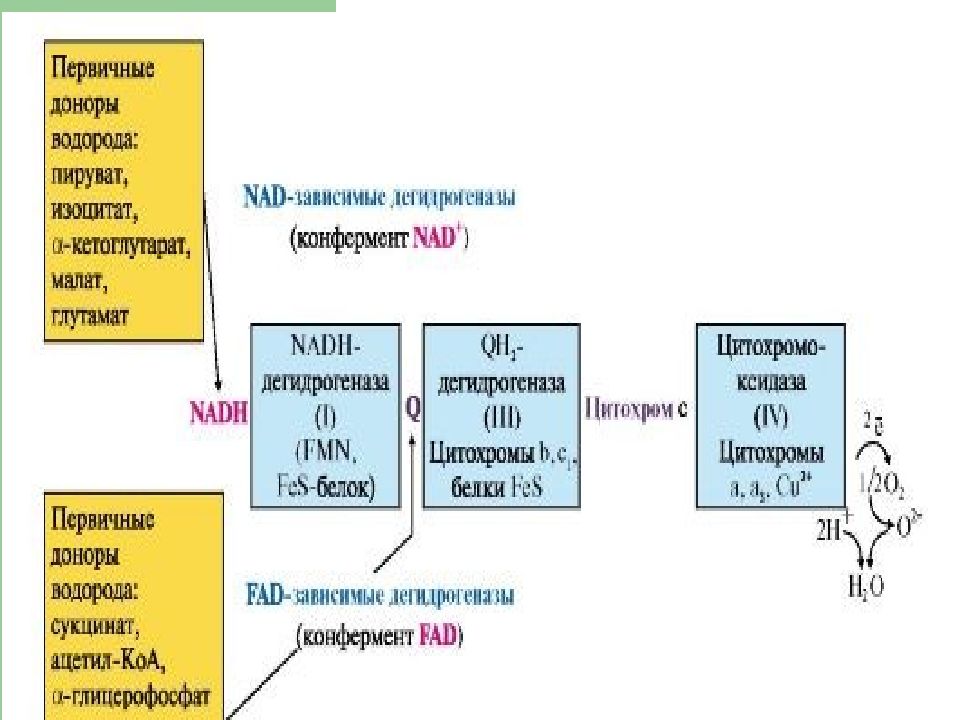
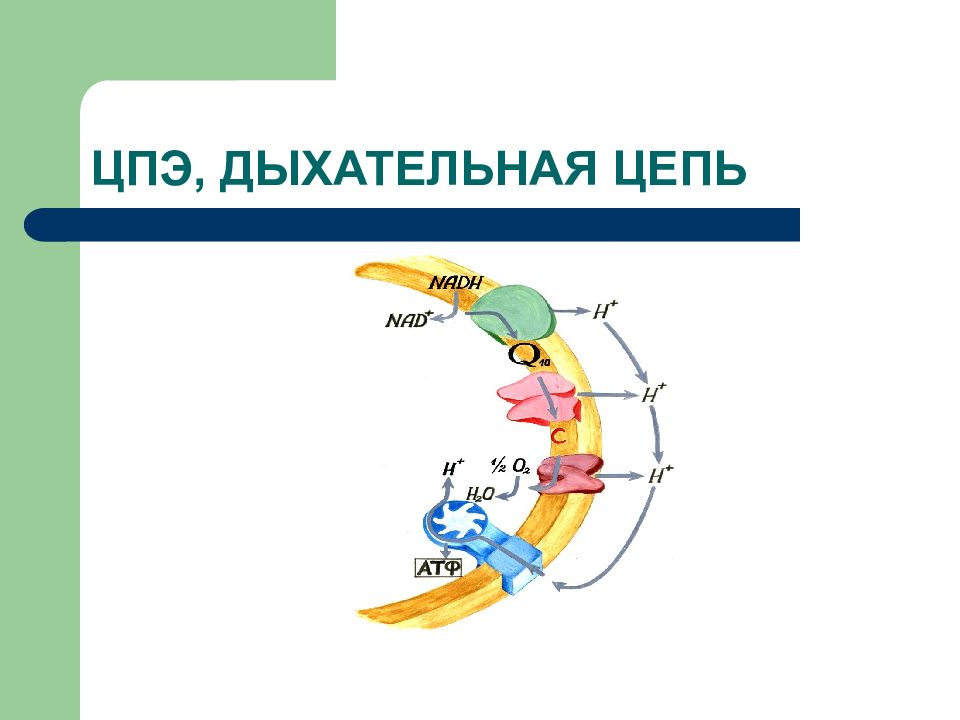
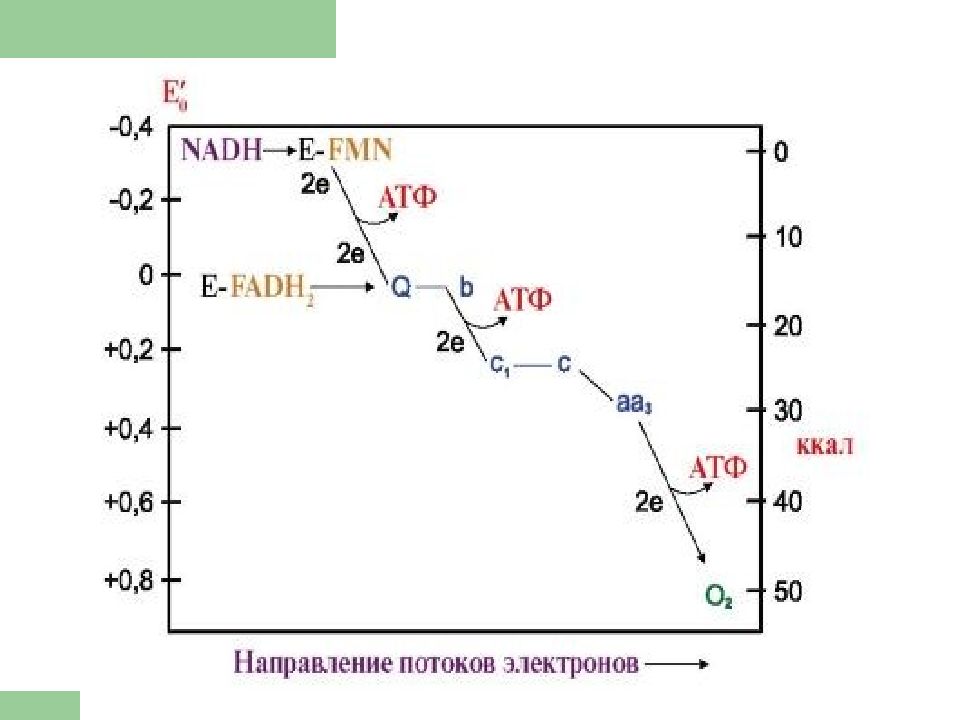
Слайд 18: ЦПЭ
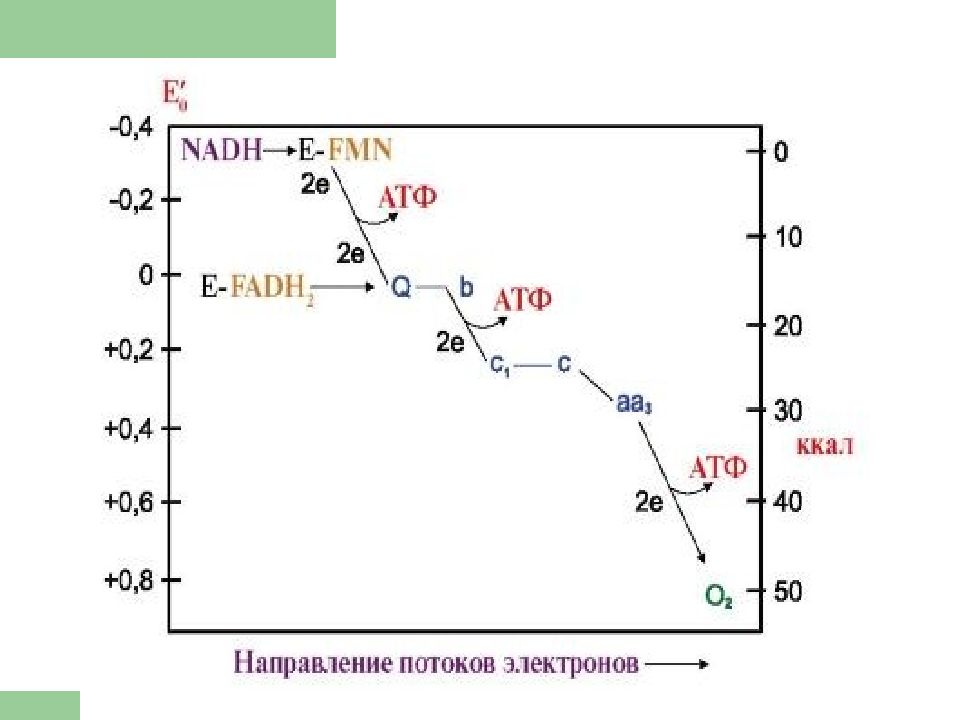
* НАД-зависимых ДЕГИДРОГЕНАЗ, ФАД-зависимых ДЕГИДРОГЕНАЗ, УБИХИНОНА, ЦИТОХРОМОВ. Последовательность расположения определяется их редокс-потенциалами.
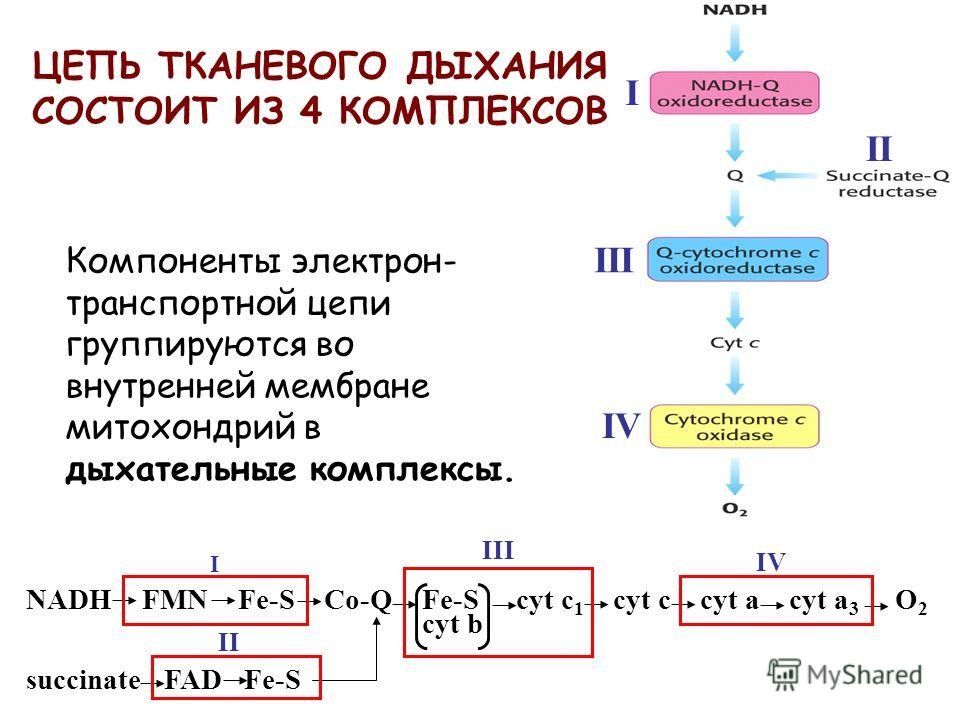
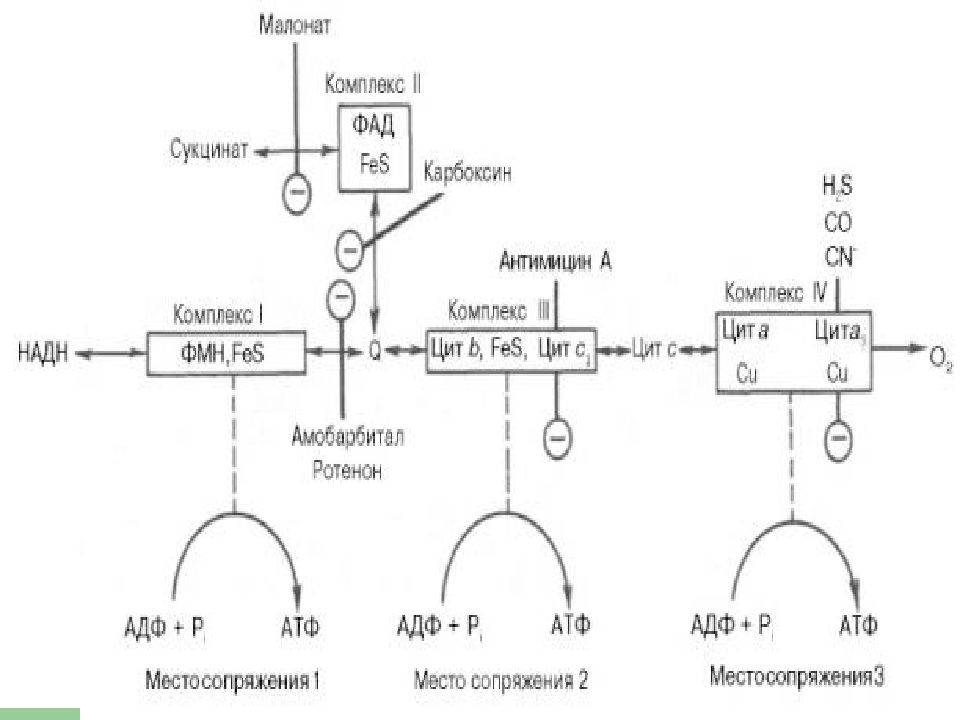
Слайд 20: Комплексы цепи переноса электронов
ЦПЭ состоит из комплексов, каждый из них осуществляет определенную стадию ЦПЭ.
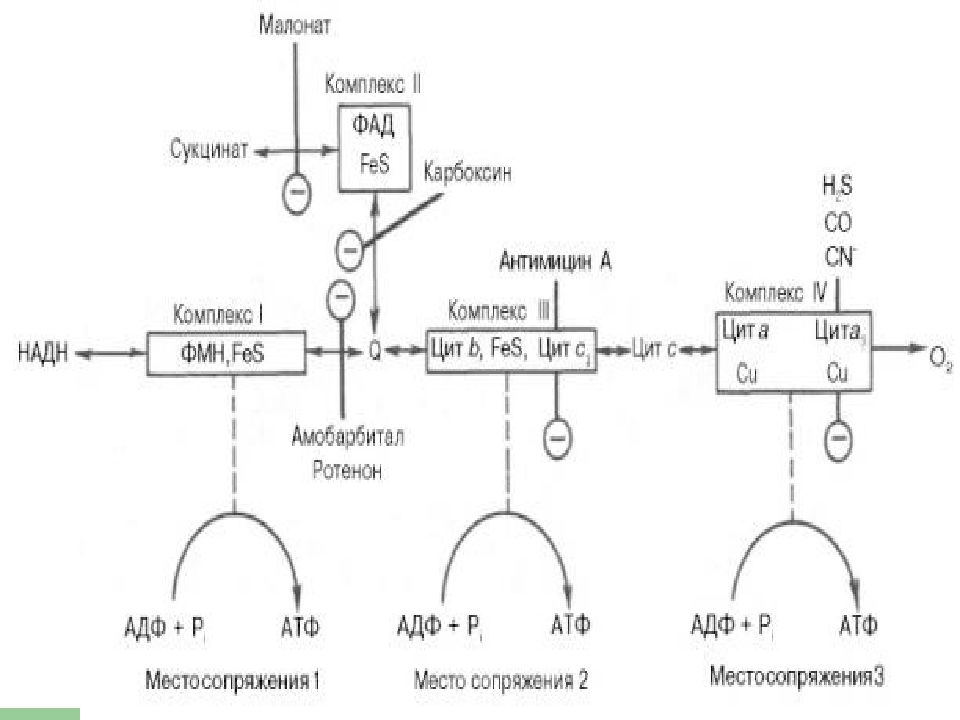
Слайд 23: Комплексы
Обозначают комплексы I, II, III и IV. I - НАДН-дегидрогеназа II - Сукцинатдегидрогеназа III - Убихинол-цитохром с-редуктаза IV - Цитохромоксидаза
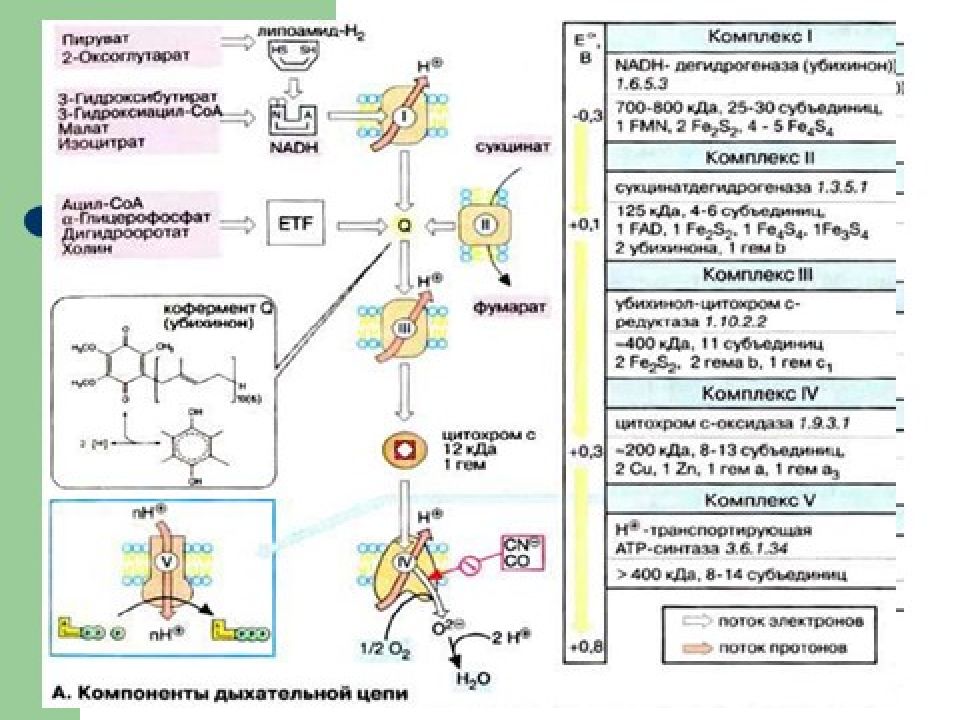
Слайд 26
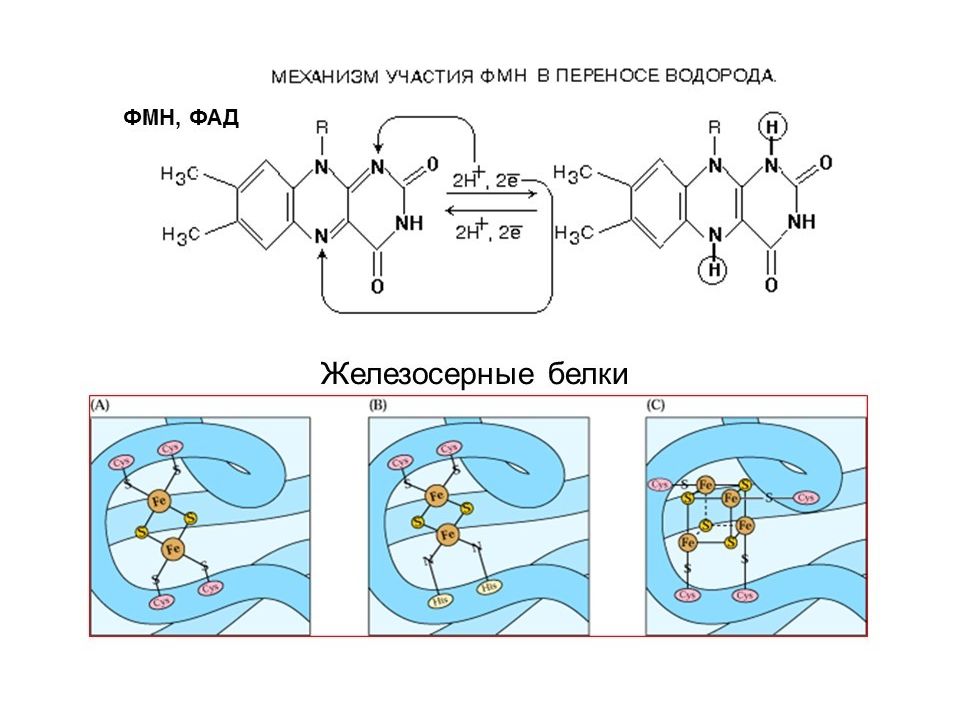
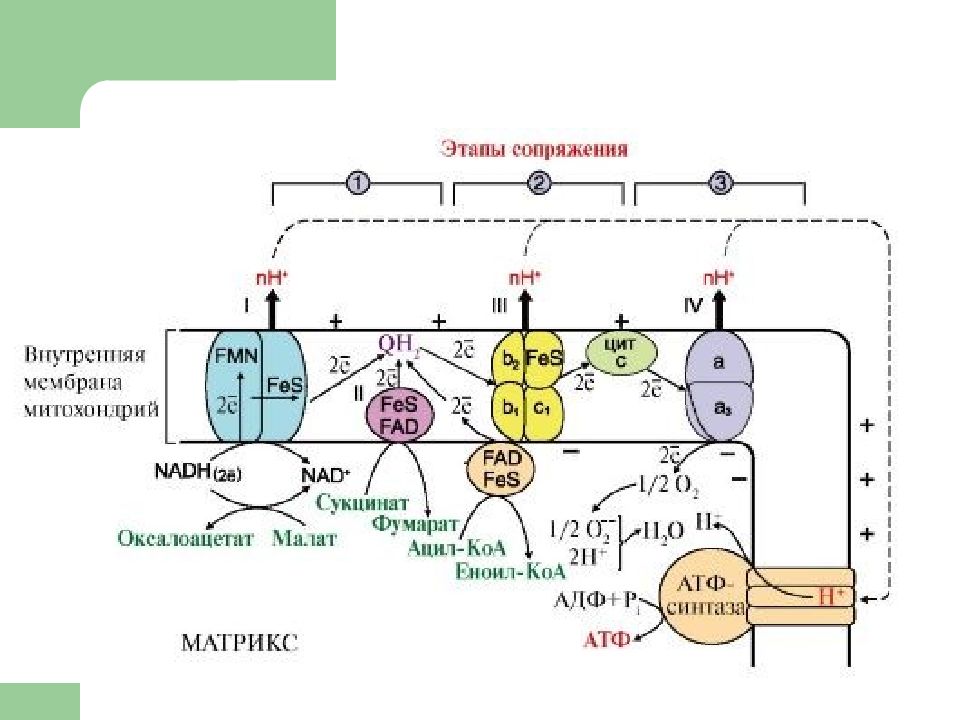
Комплексы ДЦ построены из белков и окислительно-восстановительных коферментов ( ФМН и ФАД, в комплексах I и II ), железо-серные центры (в I, II и III) и группы гема (в II, III и IV).
Слайд 28
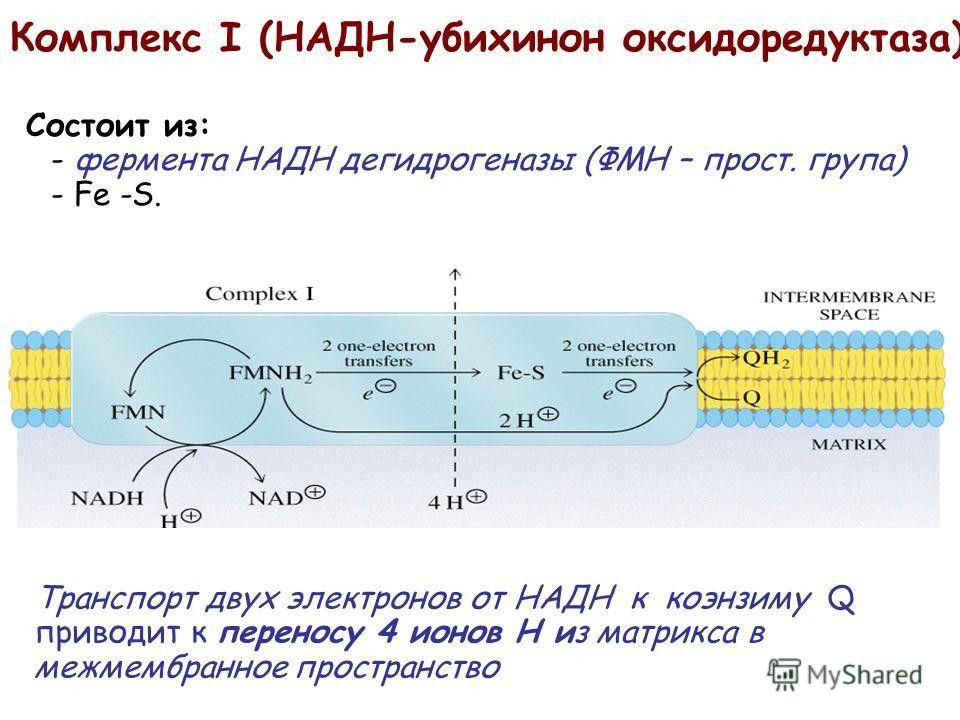
Электроны поступают в ДЦ различными путями. При окислении НАДН + Н + комплекс I переносит электроны через ФМН и Fe/S-центры на убихинон.
Слайд 29
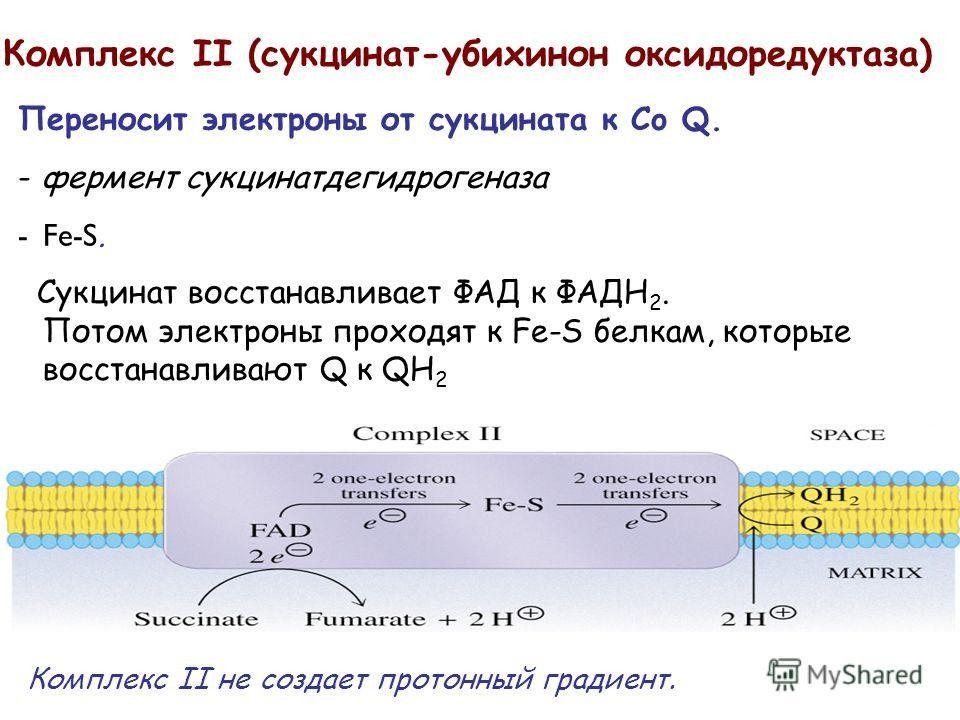
Образующиеся при окислении сукцината, ацил-КоА электроны переносятся на убихинон комплексом II через ФАДН 2. При этом окисленная форма кофермента Q восстанавливается в QH 2.
Слайд 32: Восстановленный коэнзим Q
QH 2 переносит электроны в комплекс III, который поставляет на цитохром с. Последний переносит электроны к комплексу IV, цитохромоксидазе.
Слайд 33: Комплекс I
Комплекс I катализирует окисление NADH переносчиком электронов — убихиноном (коферментом Q ).
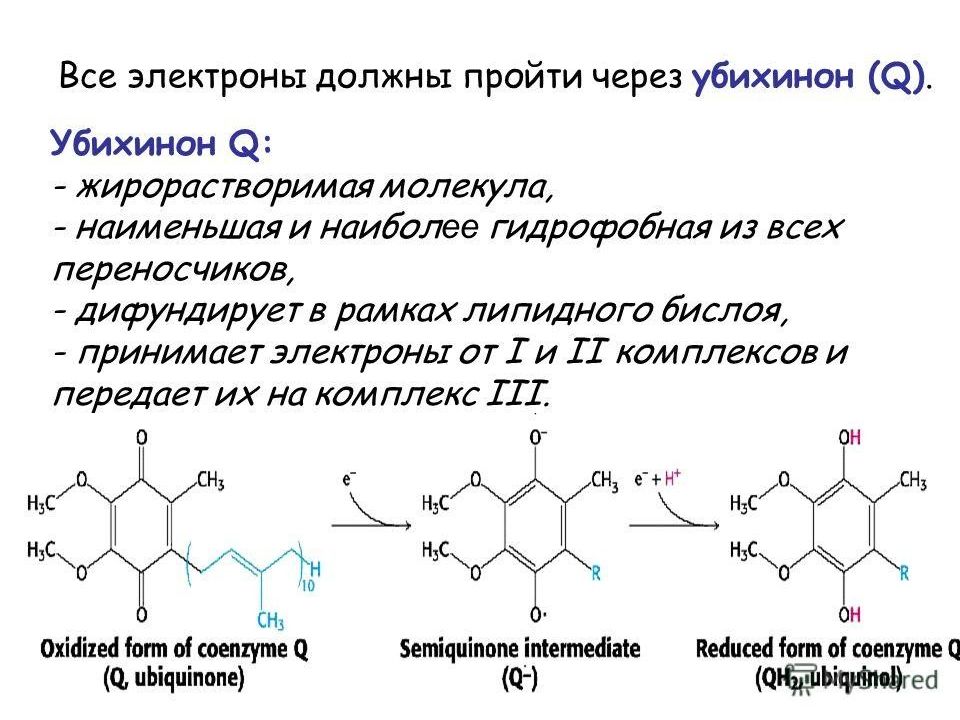
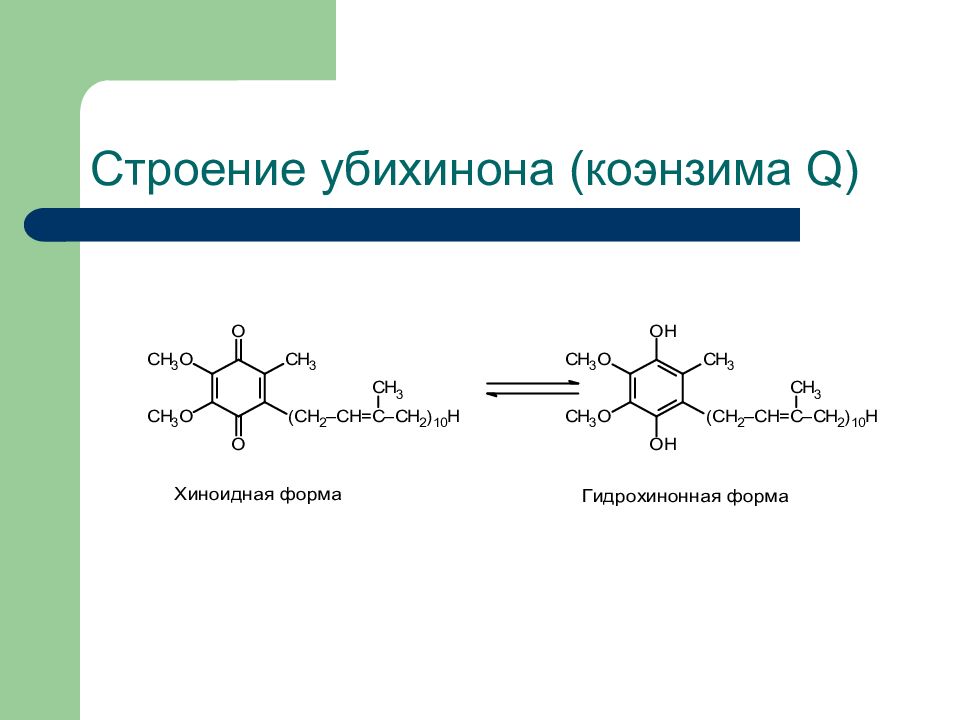
Слайд 37: Убихинон
существует в окисленной и восстановленной формах - CoQ и CoQH 2 :
Слайд 38: Восстановленный коэнзим Q
QH 2 переносит электроны в комплекс III, который поставляет на цитохром с. Последний переносит электроны к комплексу IV, цитохромоксидазе.
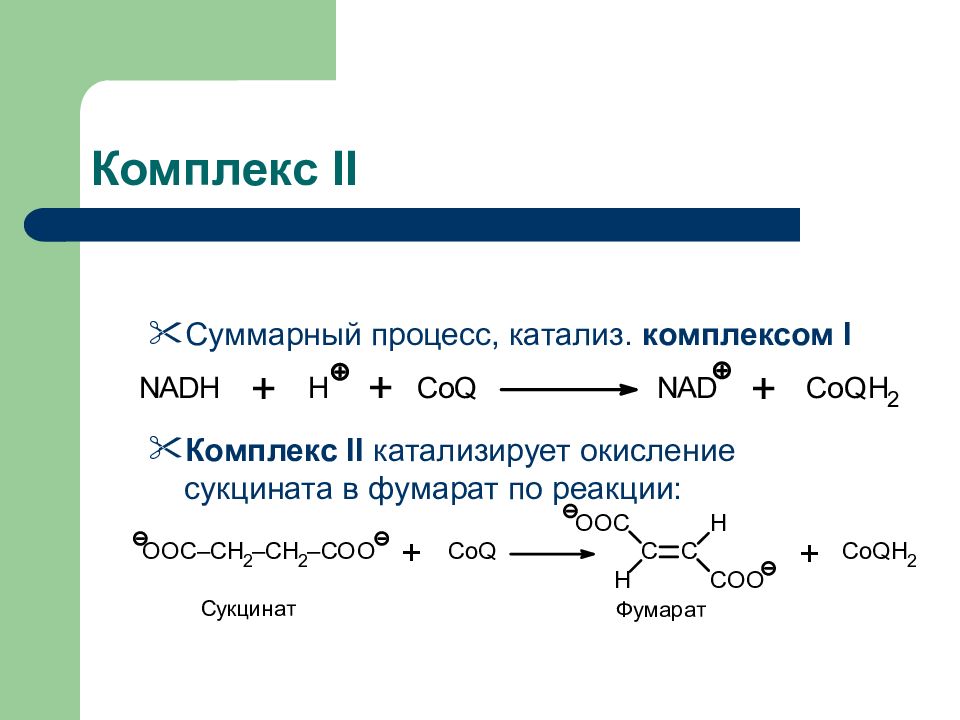
Слайд 39: Комплекс II
Суммарный процесс, катализ. комплексом I Комплекс II катализирует окисление сукцината в фумарат по реакции:
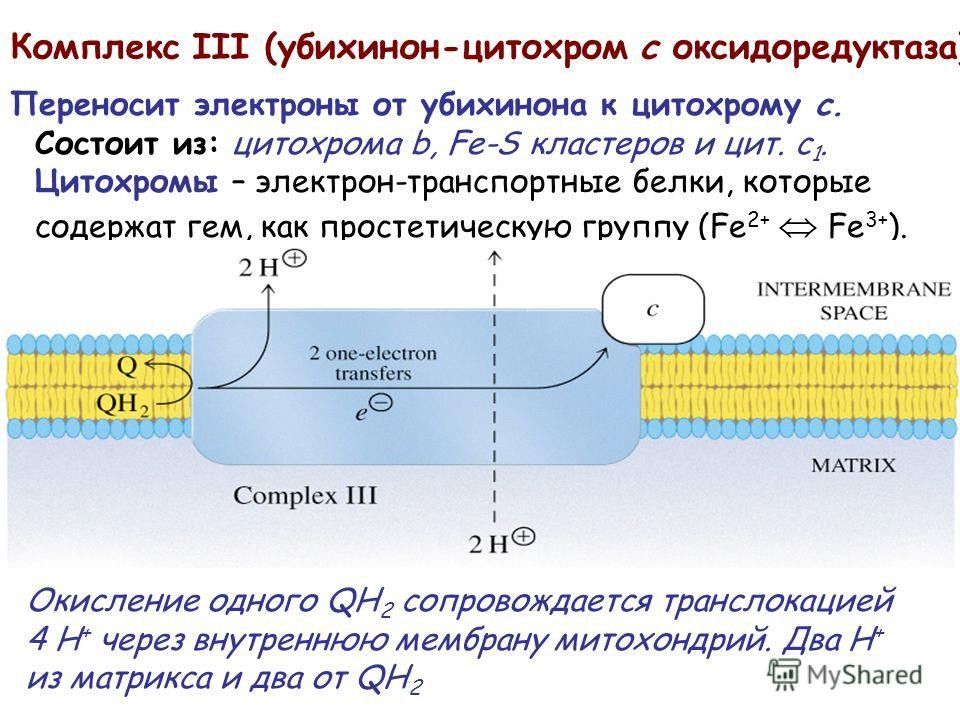
Слайд 43: Комплекс III
Комплекс III катализирует окисление Q Н 2 цитохромом с. Уравнение реакции:
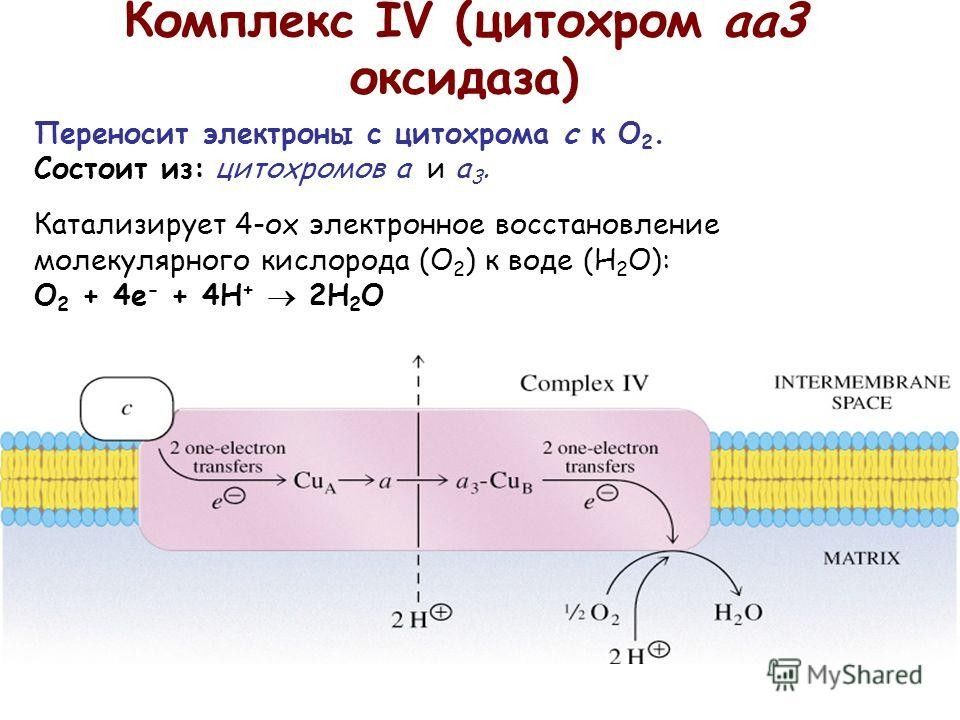
Слайд 47: Комплекс IV
Комплекс IV - цитохромоксидаза, катализирует перенос электронов от цитохрома с непосредственно на кислород по реакции:
Слайд 48
При восстановлении О 2 образуется сильный основной анион О 2-, который связывает два протона и переходит в воду.
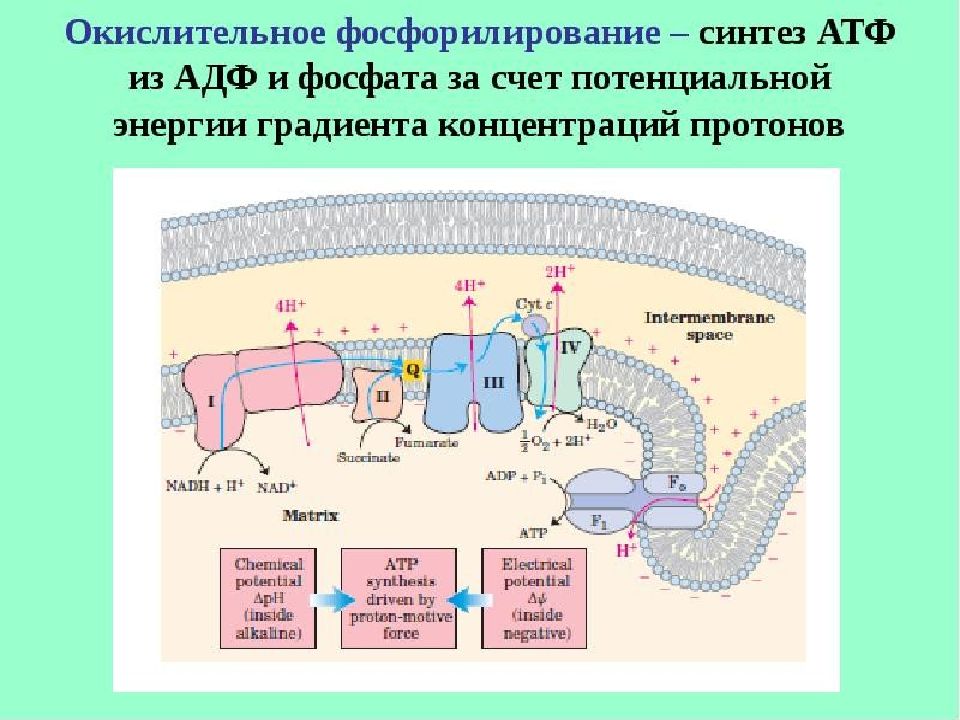
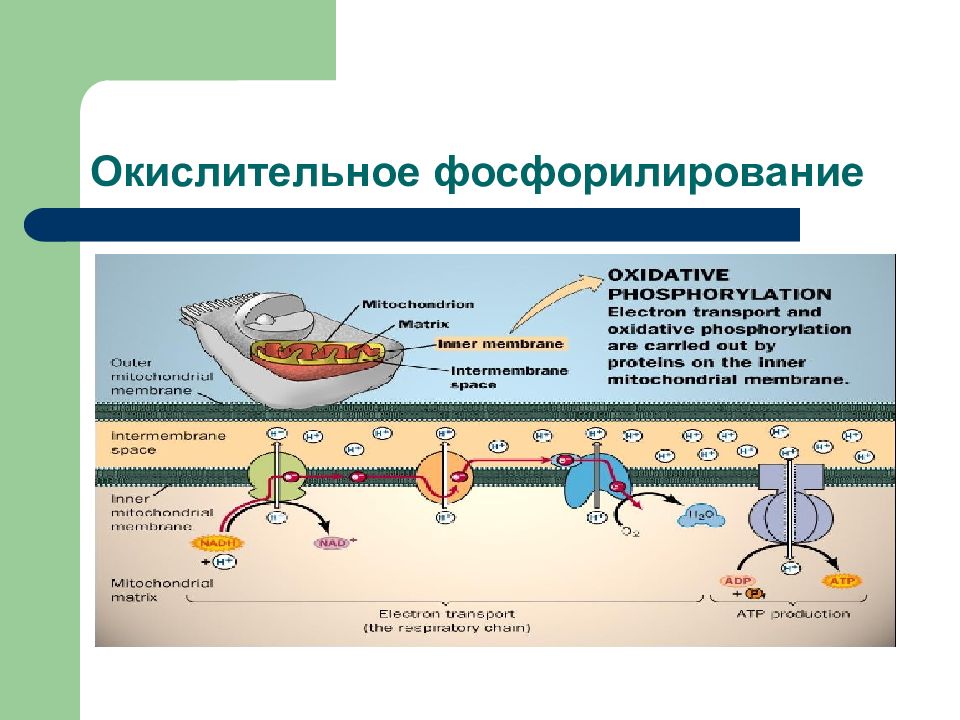
Слайд 56: Окислительное фосфорилирование
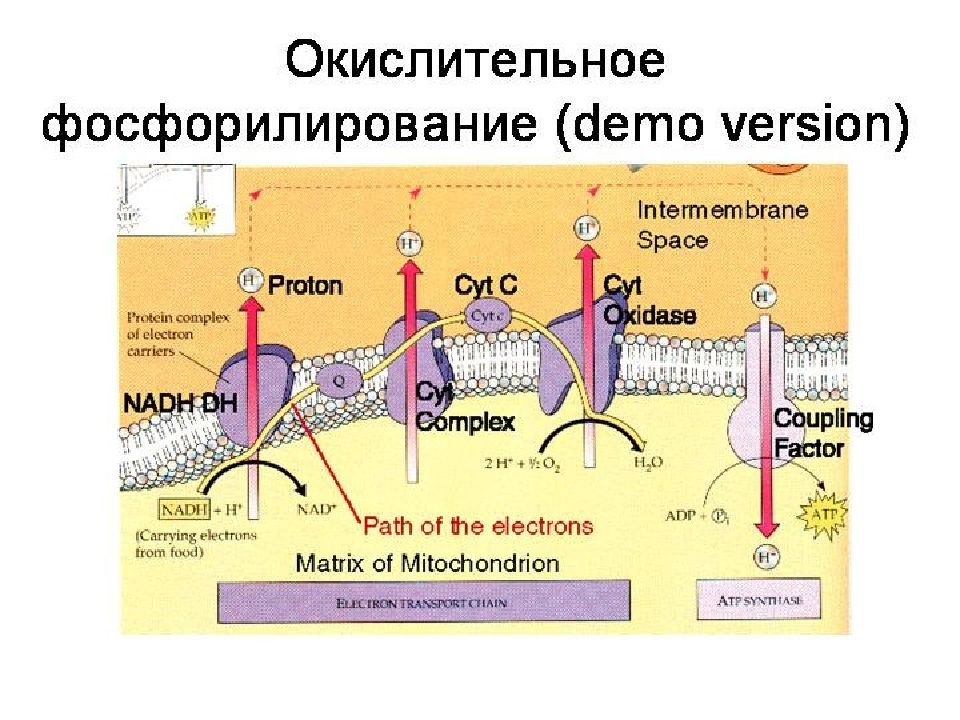
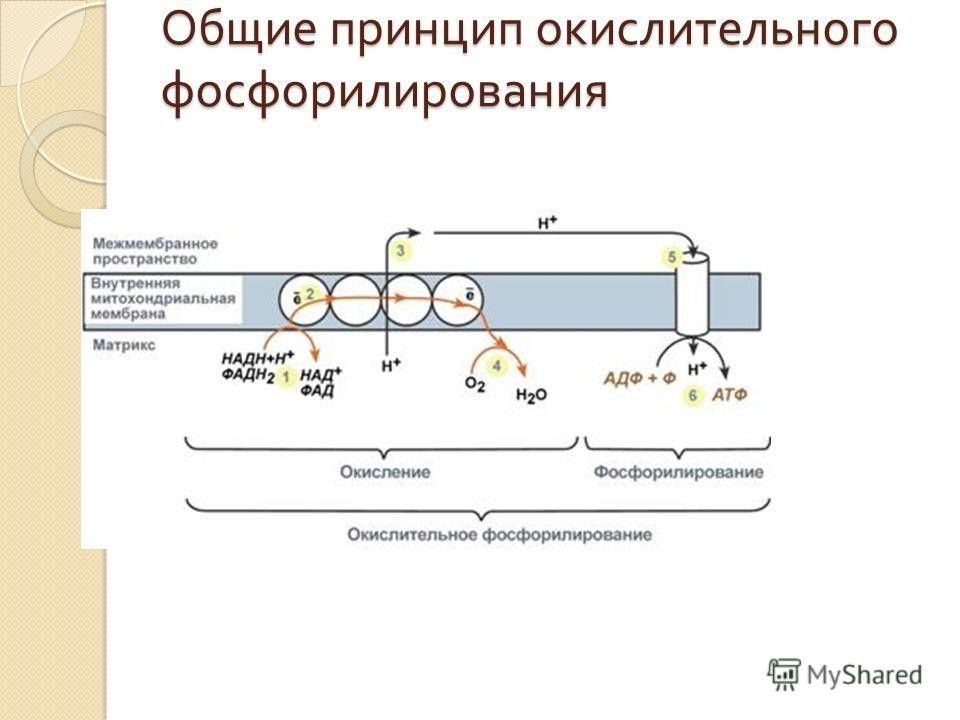
Синтез АТФ из АДФ и Н 3 РО4 за счет энергии окисления веществ, связанный с переносом электронов по ЦПЭ наз. ОКИСЛИТЕЛЬНЫМ ФОСФОРИЛИРОВАНИЕМ.
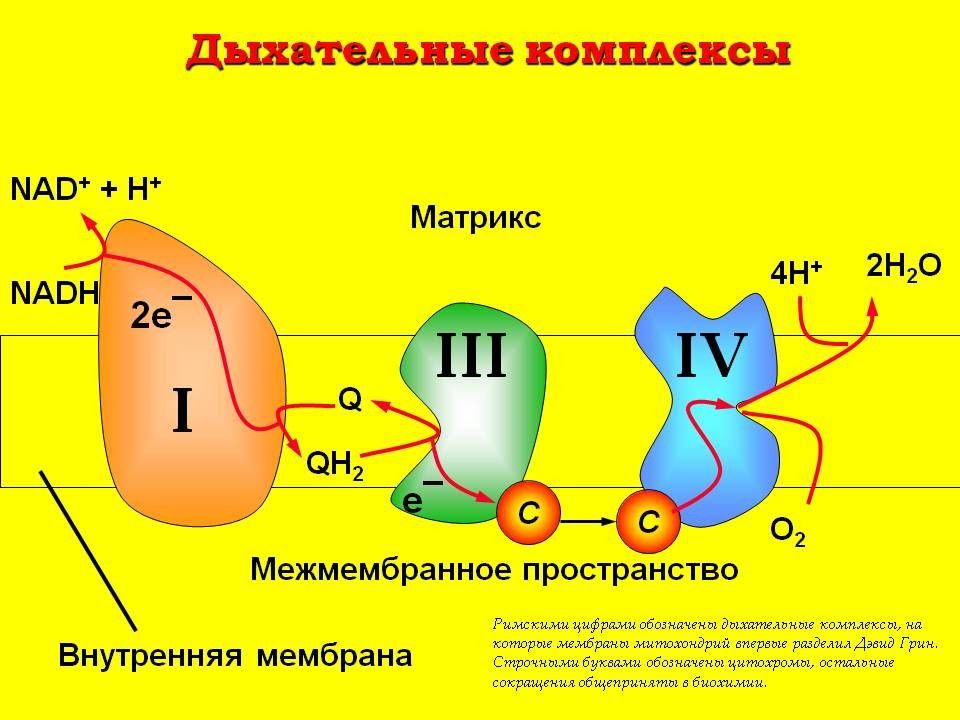
Слайд 59
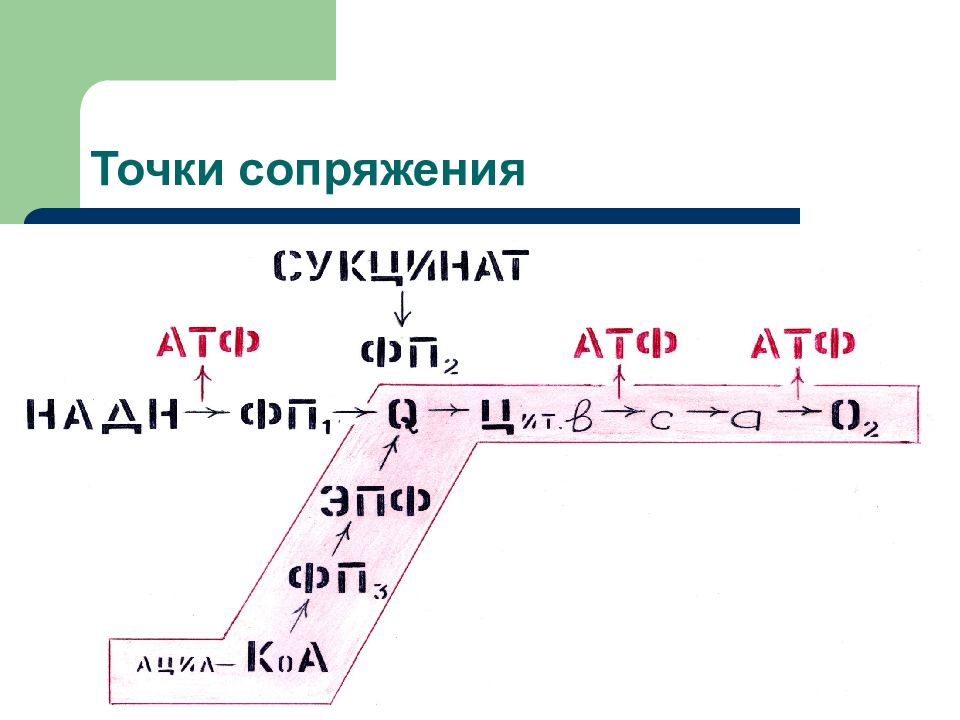
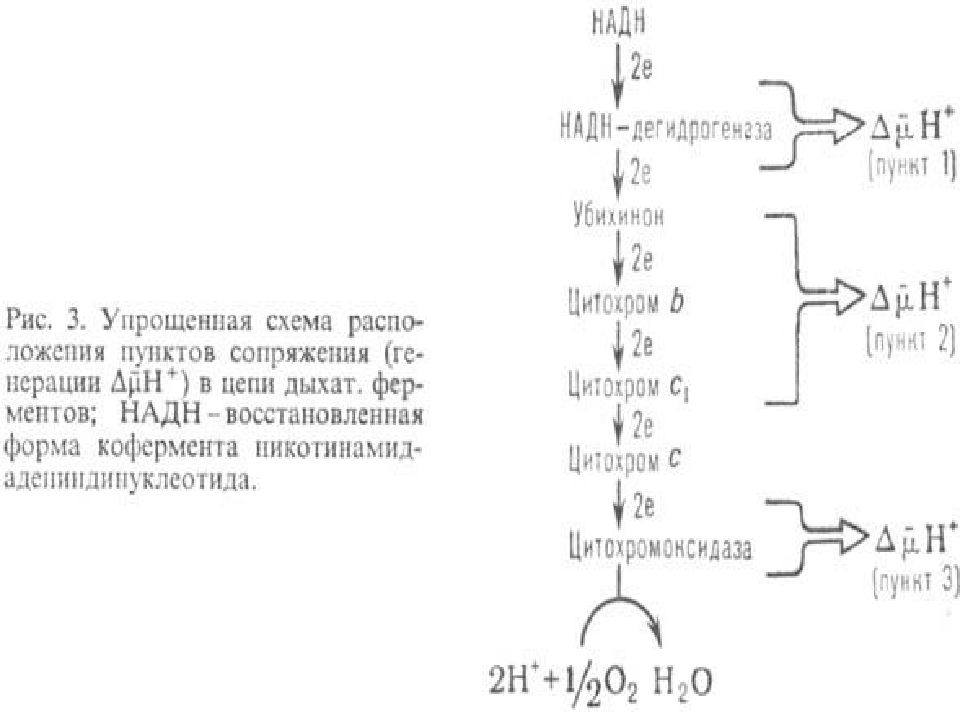
Поток электронов сопряжен с образованием комплексами I, III и IV протонного градиента.
Слайд 60
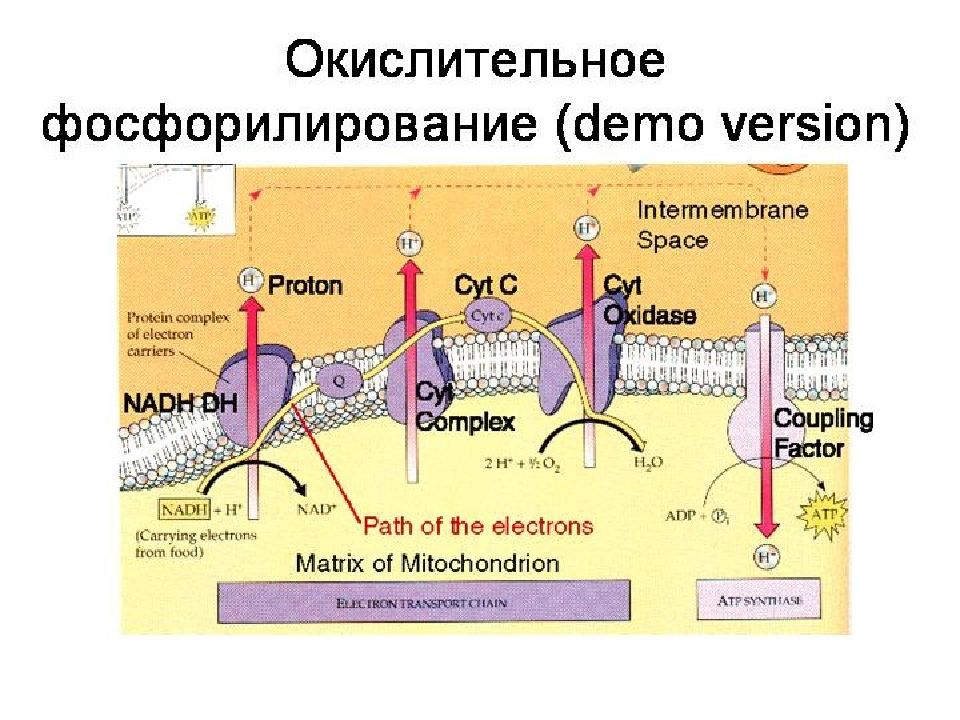
Большая часть выделяющейся энергии используется для создания градиента протонов и, наконец, для образования АТФ с помощью АТФ-синтазы.
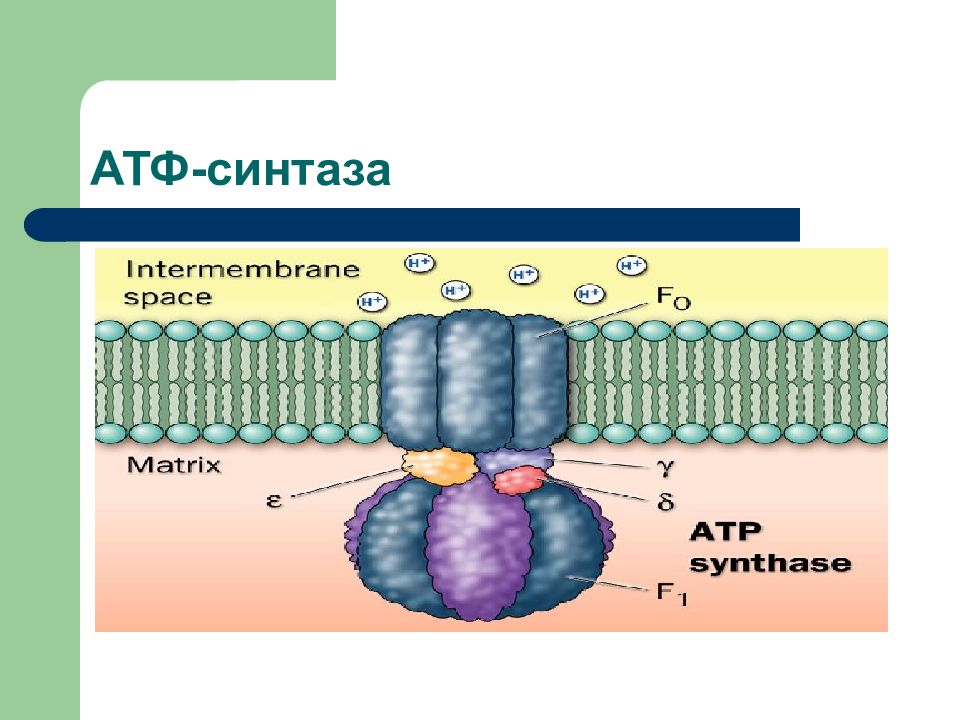
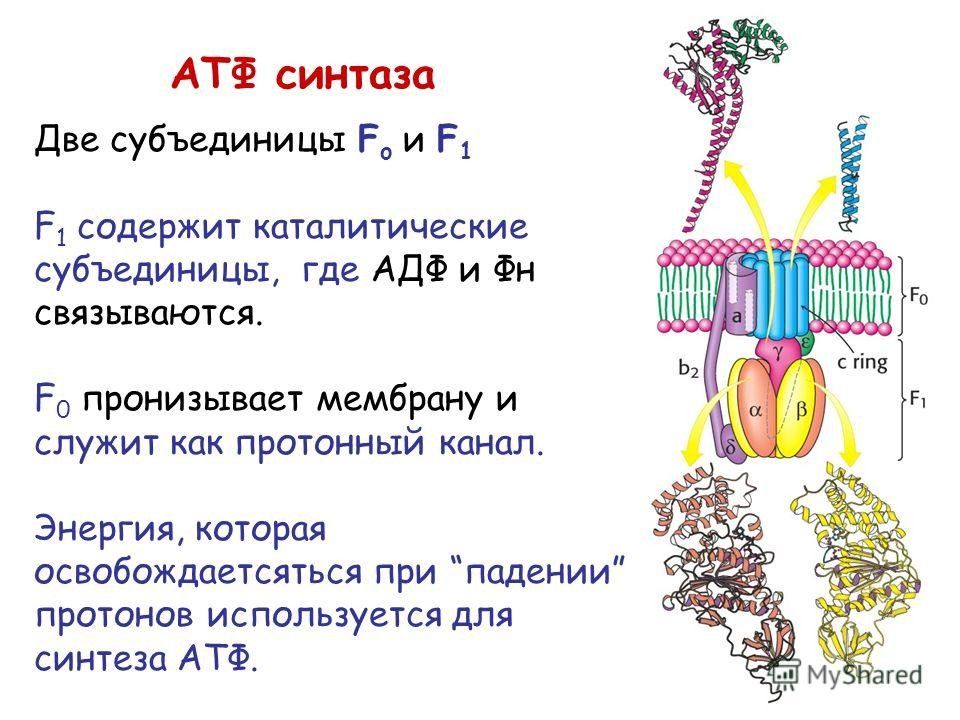
Слайд 61: АТФсинтаза
Главная функция фермента заключается в фосфорилировании A ДФ ортофосфатом с образованием АТФ.
Слайд 62: Механизм сопряжения фосфорилирования
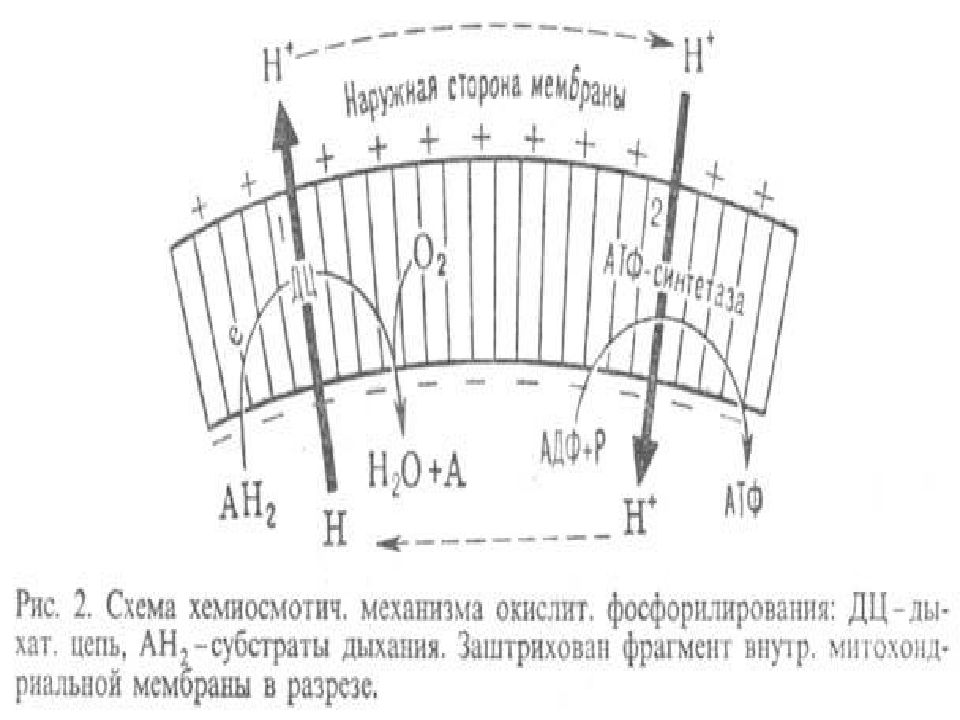
Объясняет хемиосмотическая гипотеза Митчелла.
Слайд 64: Гипотеза Митчелла
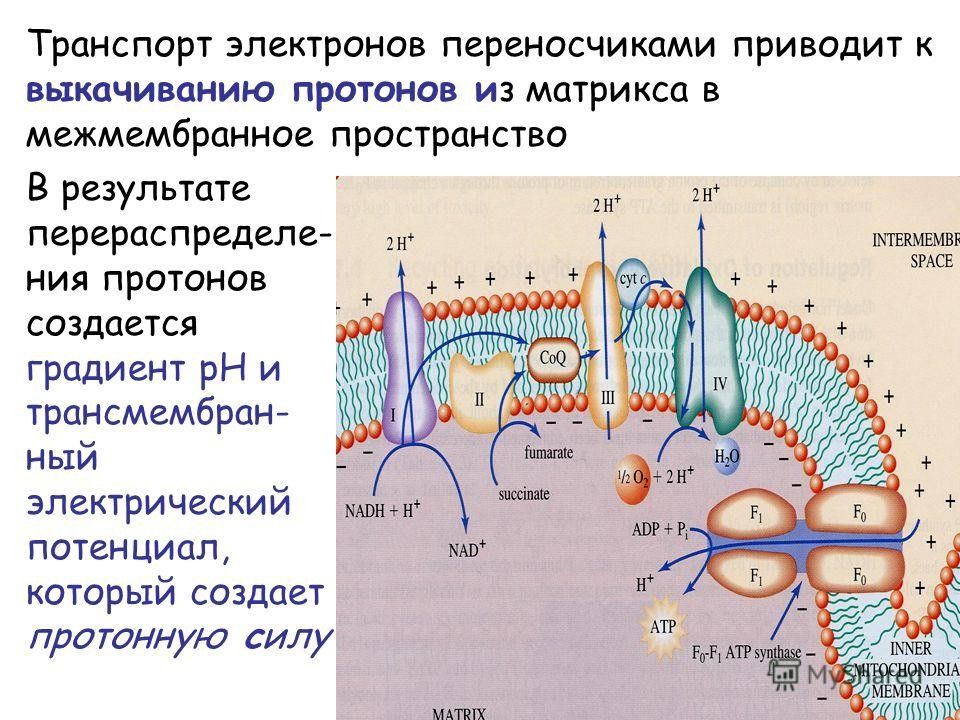
Реакции, сопровождающиеся образованием протонов, протекают на вн. МХ мембране таким образом, что протоны переносятся с внутренней стороны мембраны на внешнюю.
Слайд 67
Энергия переноса электронов и протонов вдоль ДЦ сосредотачивается в виде протонного потенциала или электрохимического градиента Н+.
Слайд 68
Диффузия протонов обратно через мембрану сопряжена с фосфорилированием, которое осуществляет АТФсинтаза.
Слайд 71
Трансмембранная разность электрических потенциалов (протонный потенциал). Трансмембранная разность концентраций ионов Н+
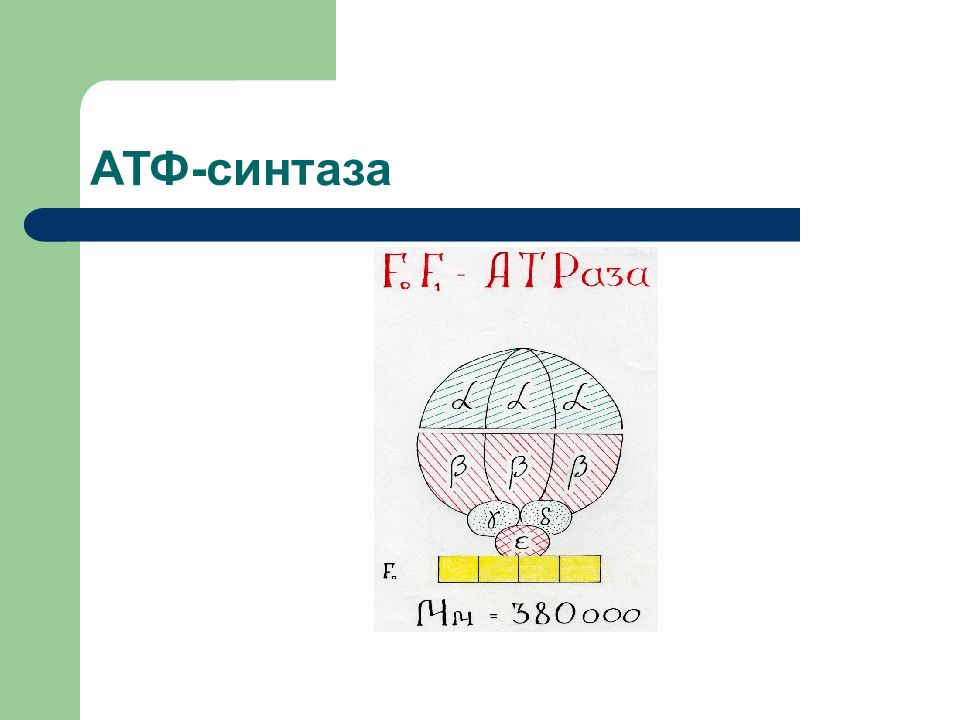
Слайд 72
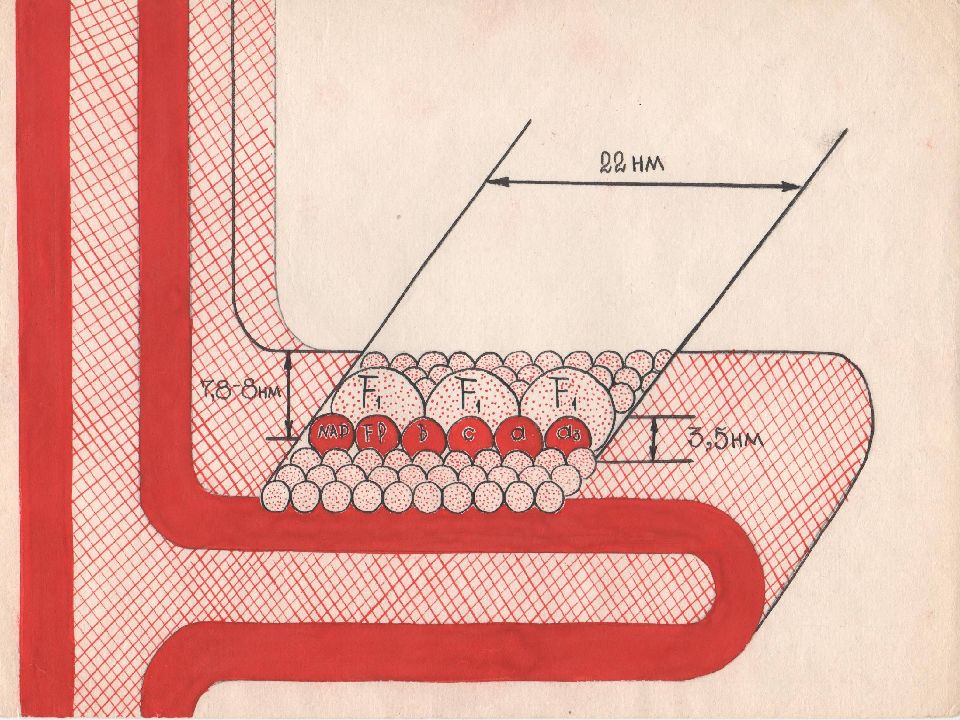
Н + - АТФ-синтаза состоит из: протонного канала (F 0 ) и каталитической субъединицы (F 1 ), образованной тремя α- и тремя β-субъединицами, между которыми расположены γ-, δ- и ε-субъединицы.
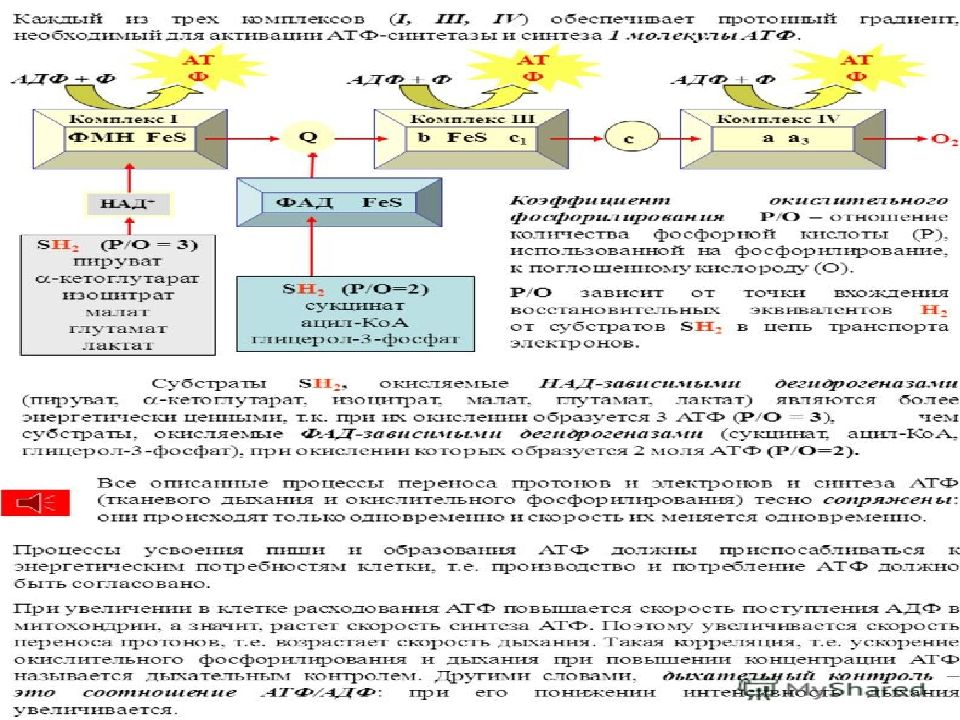
Слайд 76: Коэффициент Р/О
При окислении каждой молекулы НАДН образуется 3 молекулы АТФ ( по одной в комплексе I, III и IV ), а при окислении одной молекулы ФАДН 2 — 2 молекулы АТФ (в комплексе III и IV ).
Слайд 84
Механизм регуляции образования и потребления АТФ наз. дыхательным контролем. Скорость О.Ф. зависит от содержания АДФ.
Слайд 85
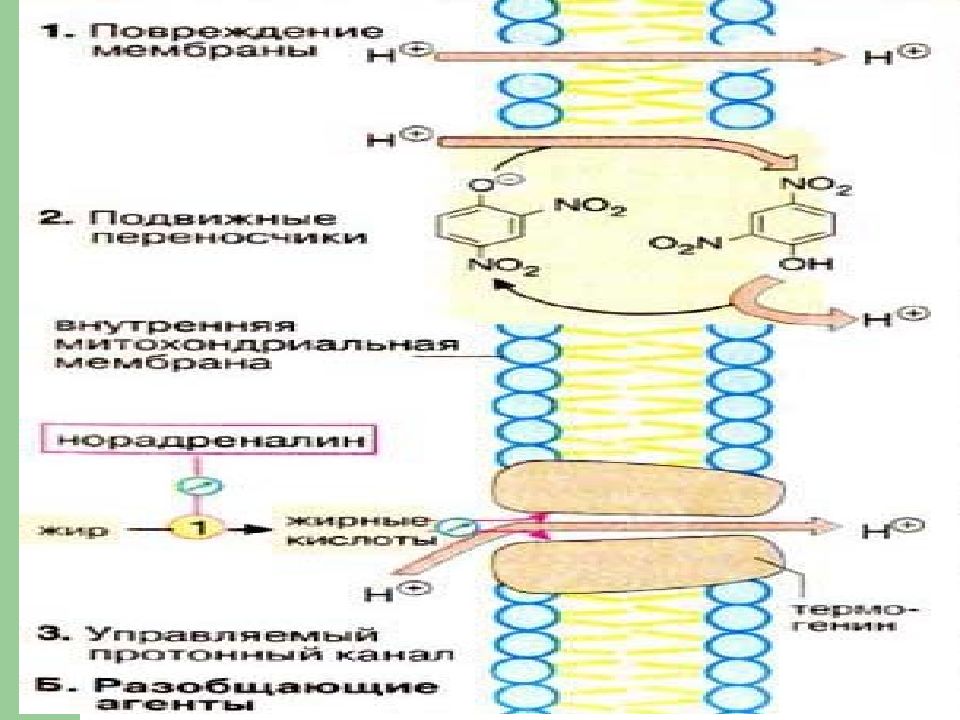
Вещества, которые функционально разделяют между собой окисление и фосфорилирование, наз. разобщающими агентами. Они содействуют переносу протонов из ММП в матрикс без участия АТФсинтазы. Разобщающие агенты
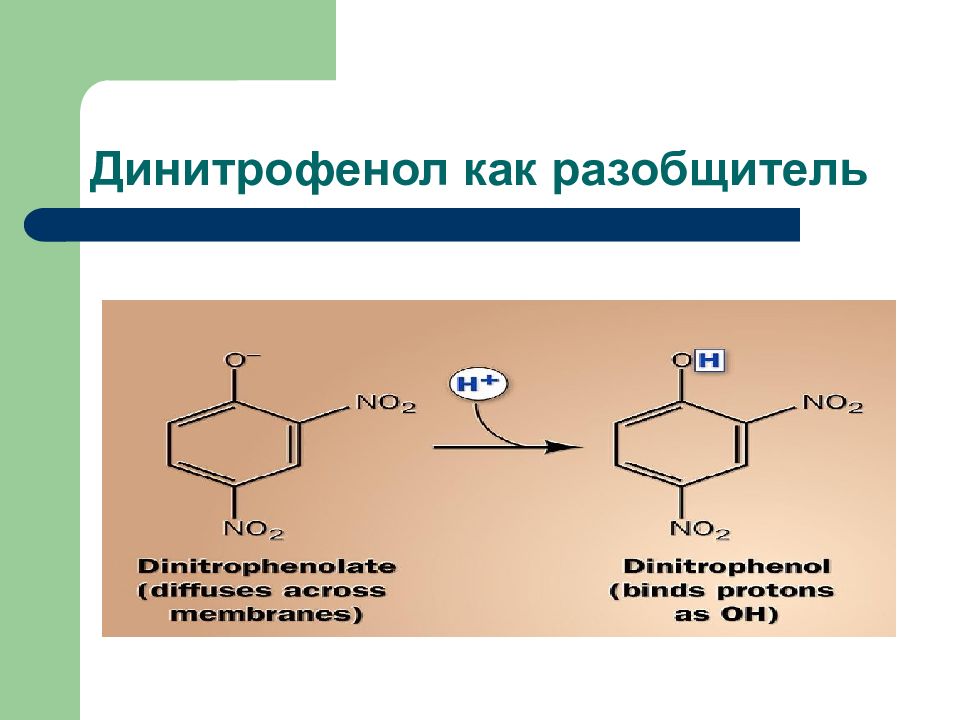
Слайд 87: Разобщение
в результате - механического повреждения внутренней мембраны; - действия протонофоров – (2,4-динитрофенол, тироксин).
Слайд 91: Гипертермия
Если создание протонного градиента подавлено, процессы окисления субстрата и переноса электронов протекают значительно быстрее, однако вместо синтеза АТФ выделяется тепло ( гипертермия ).