Первый слайд презентации: Ароматические углеводороды (арены). Гомологи бензола
Слайд 3: Цель урока:
Продолжить формирование понятий об ароматических углеводородах через: гомологический ряд и номенклатуру моноциклических аренов строение и особенности химического поведения толуола, стирола знакомство с основными способами получения толуола и его применении
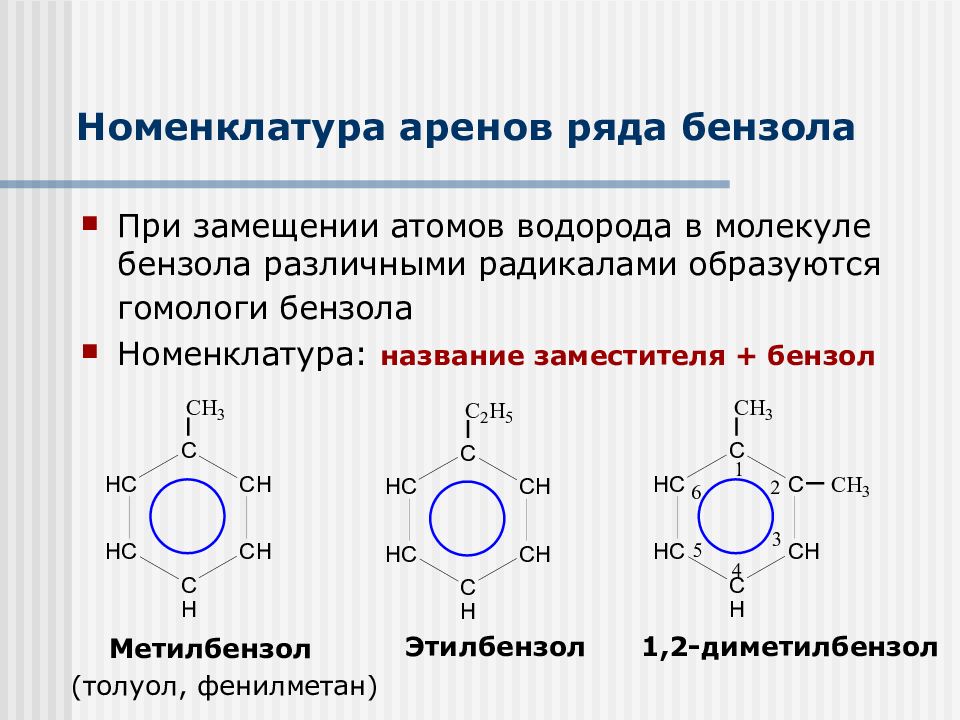
Слайд 4: Номенклатура аренов ряда бензола
При замещении атомов водорода в молекуле бензола различными радикалами образуются гомологи бензола Номенклатура: название заместителя + бензол Метилбензол (толуол, фенилметан) Этилбензол 1,2-диметилбензол
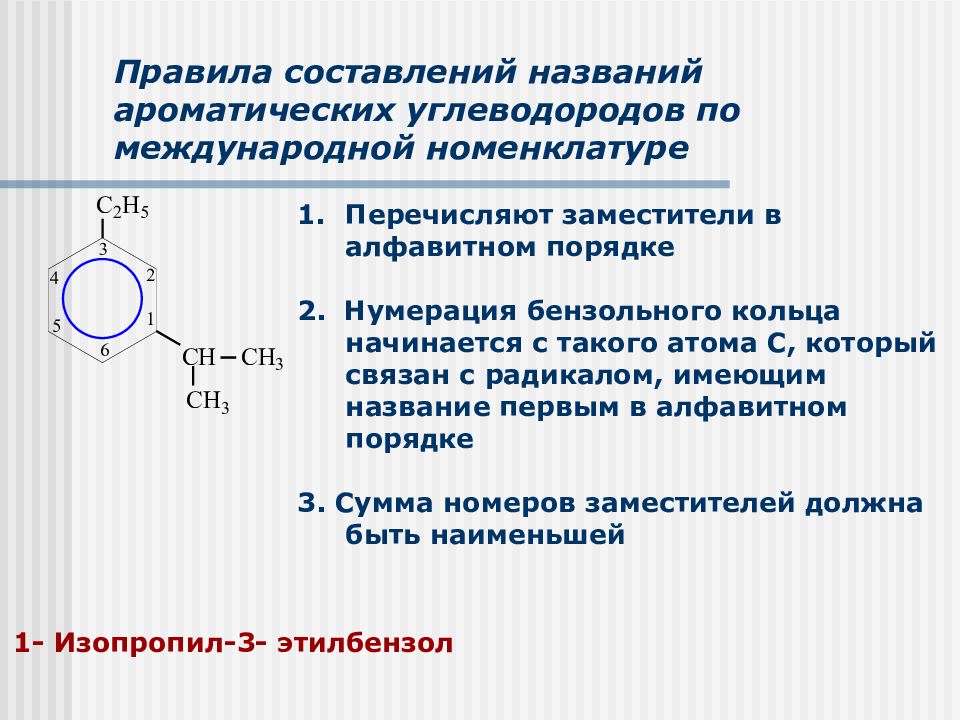
Перечисляют заместители в алфавитном порядке 2. Нумерация бензольного кольца начинается с такого атома С, который связан с радикалом, имеющим название первым в алфавитном порядке 3. Сумма номеров заместителей должна быть наименьшей 1- Изопропил-3- этилбензол
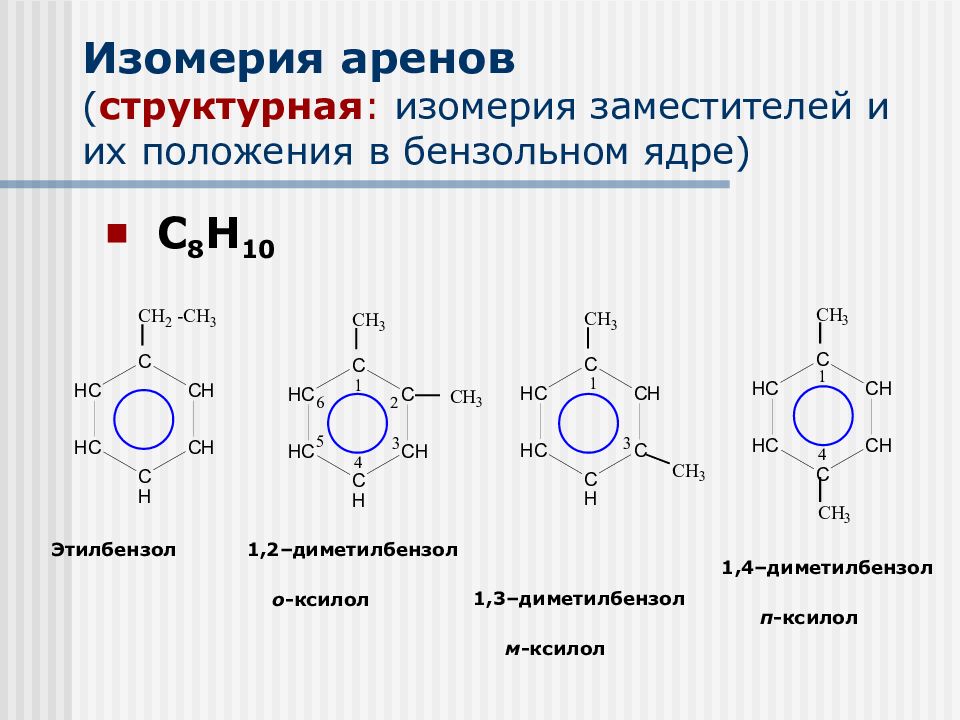
С 8 Н 10 Этилбензол 1,2–диметилбензол о -ксилол 1,3–диметилбензол м -ксилол 1,4–диметилбензол п -ксилол
Слайд 7: Физические свойства толуола
При обычных условиях-бесцветная жидкость с характерным запахом, температурой кип. 111 С, не растворим в воде ; хорошо растворяется в органических, растворителях. Толуол менее токсичен, чем бензол.
Слайд 9: Химические свойства толуола
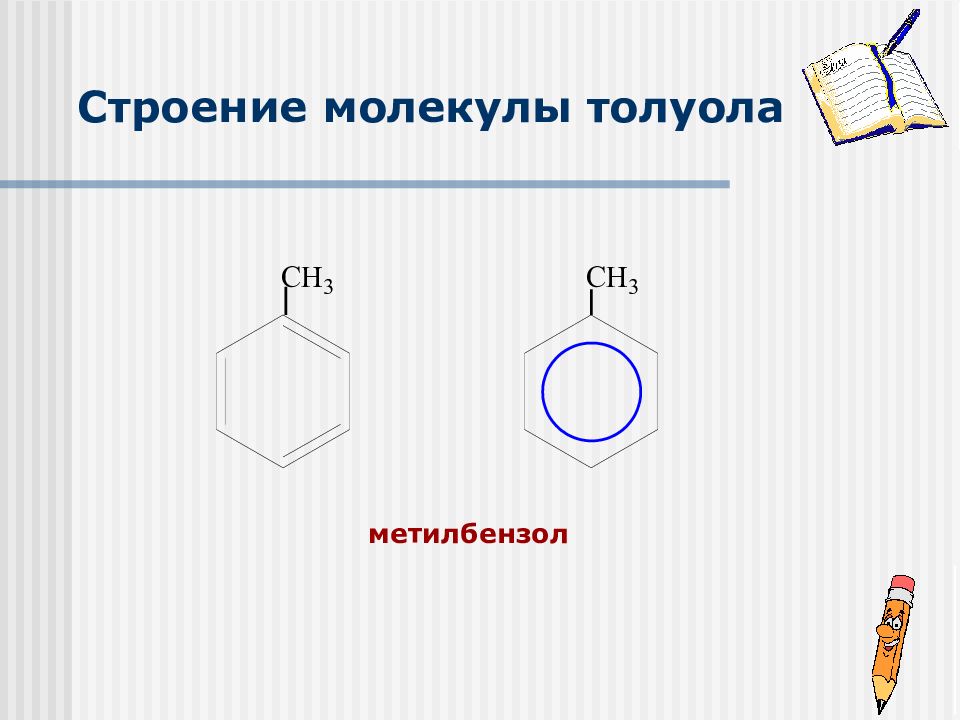
Ароматическая связь бензольного кольца и метильная группа взаимно влияют друг на друга и это влияние определяет свойства толуола.
Слайд 10: Взаимное влияние атомов в молекуле толуола
Метилбензол вступает во все реакции замещения, в которых участвует бензол, и проявляет при этом более высокую реакционную способность, реакции протекают с большей скоростью. Есть и более глубокие различия. Например, бензол не окисляется раствором KMnO 4, а толуол окисляется. ПОЧЕМУ? C H 3
Слайд 11: Правило ориентации в бензольном кольце
Заместители I рода – электронодоноры ( -OH, NH 2, -R, Hal), находясь в бензольном кольце направляют атомы илм группы атомов в орто- или параположение, так как эти заместители способны увеличивать электронную плотность в этих положениях.
Слайд 12: Правило ориентации в бензольном кольце
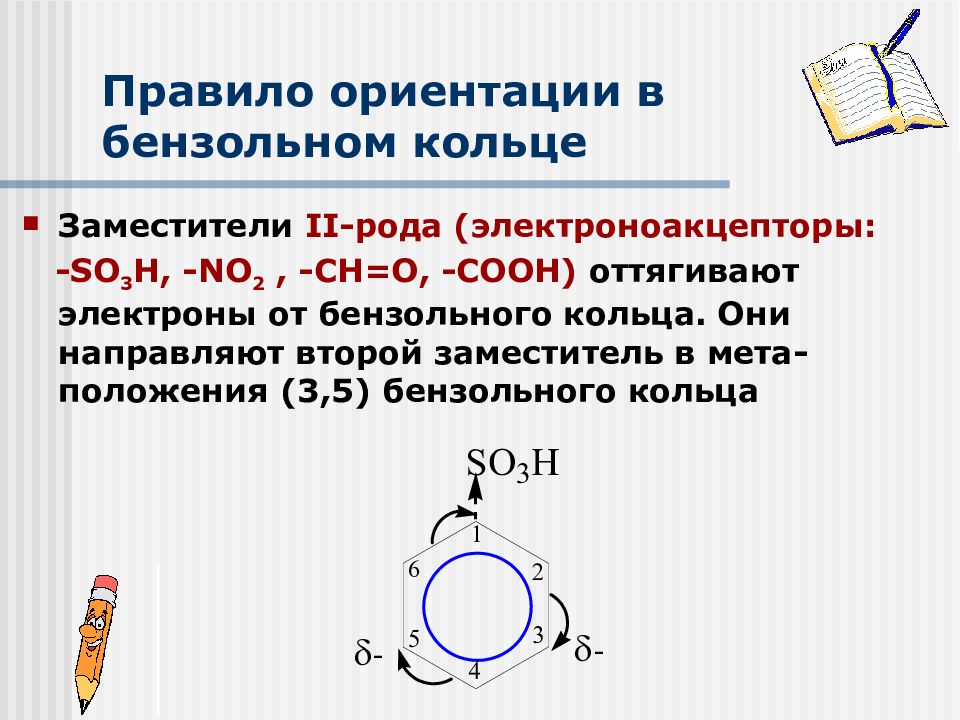
Заместители II -рода (электроноакцепторы: - S О 3 Н, -NO 2, -СН=О, -СООН) оттягивают электроны от бензольного кольца. Они направляют второй заместитель в мета-положения (3,5) бензольного кольца - -
Слайд 13: Влияние метильного радикала на бензольное кольцо
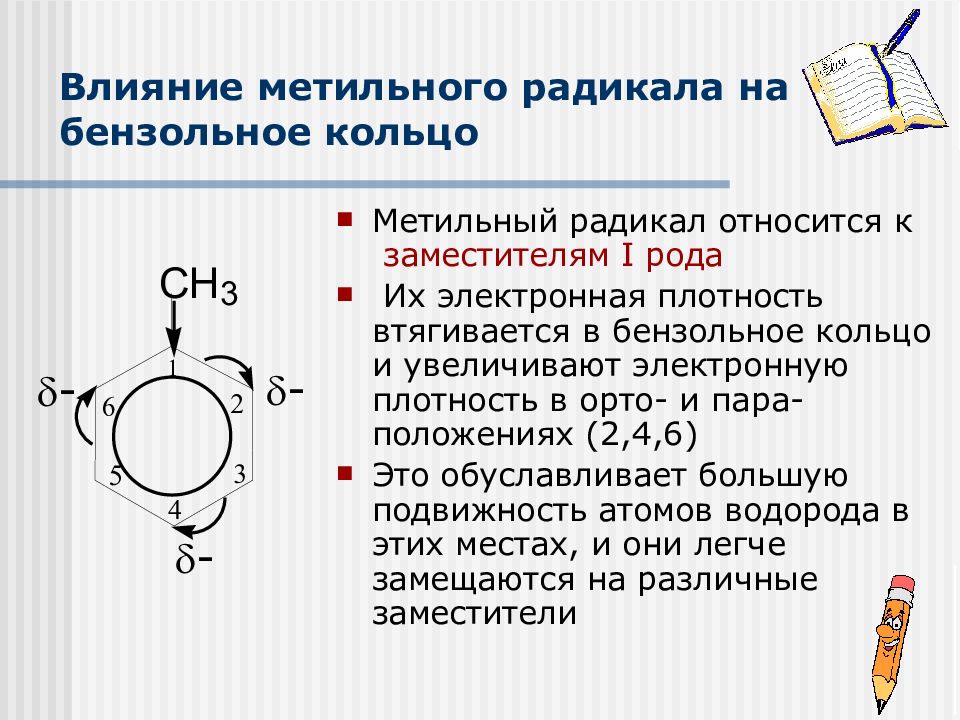
Метильный радикал относится к заместителям I рода Их электронная плотность втягивается в бензольное кольцо и увеличивают электронную плотность в орто- и пара-положениях (2,4,6) Это обуславливает большую подвижность атомов водорода в этих местах, и они легче замещаются на различные заместители - 1 3 2 4 5 6 C H 3 - -
Слайд 14: I. Реакции замещения в бензольном кольце
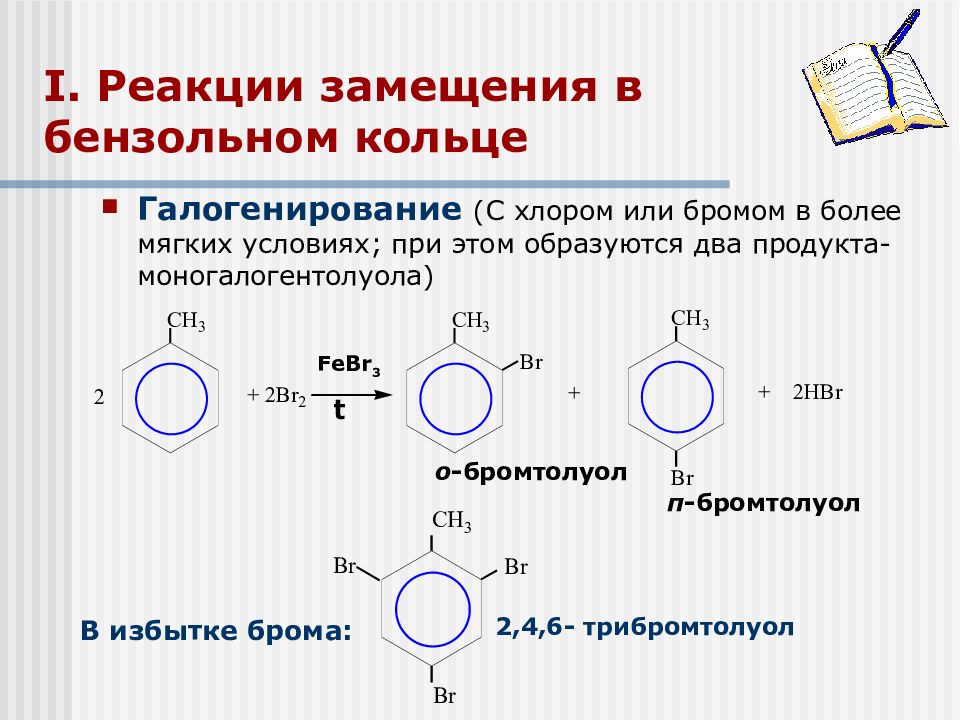
FeBr 3 t о -бромтолуол I. Реакции замещения в бензольном кольце В избытке брома: 2,4,6- трибромтолуол п -бромтолуол Галогенирование (С хлором или бромом в более мягких условиях ; при этом образуются два продукта-моногалогентолуола)
Слайд 15
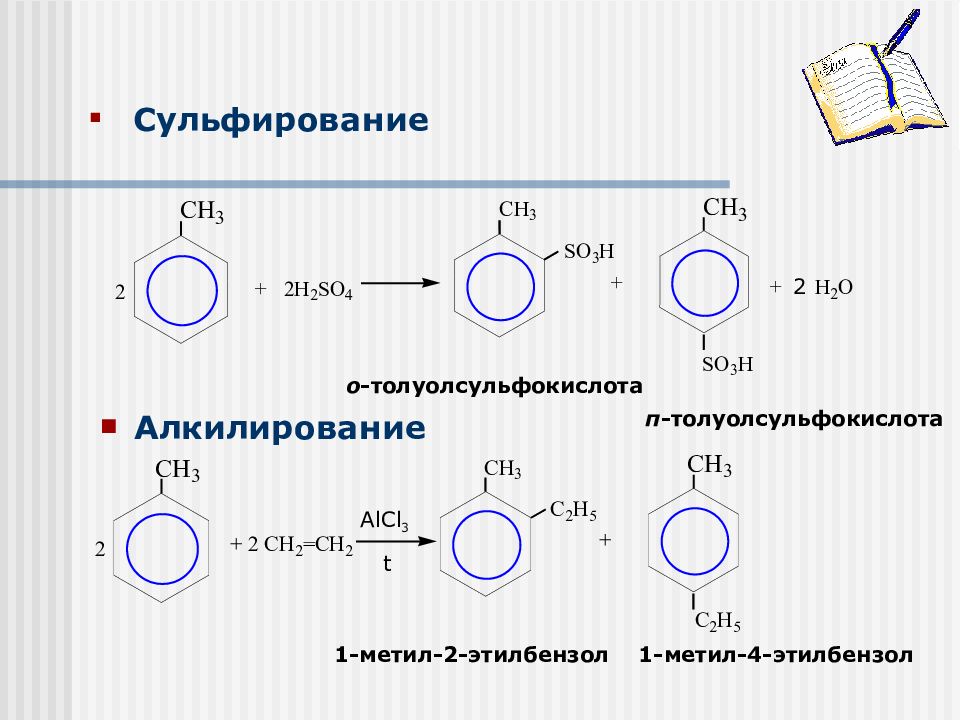
Алкилирование Сульфирование AlCl 3 t 1- метил-2-этилбензол 1- метил-4-этилбензол о -толуолсульфокислота п -толуолсульфокислота C H 3 C H 3 C H 3 S O 3 H + 2 H 2 S O 4 + 2 H 2 O 2 S O 3 H +
Слайд 17: II. Реакции замещения с участием боковой цепи
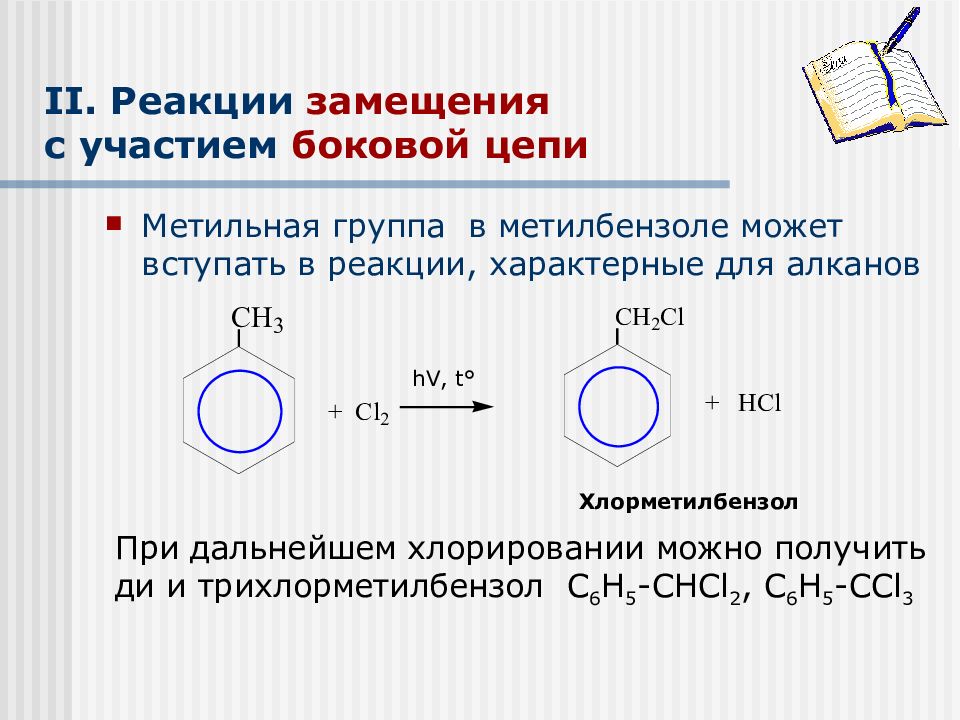
Метильная группа в метилбензоле может вступать в реакции, характерные для алканов Хлорметилбензол При дальнейшем хлорировании можно получить ди и трихлорметилбензол С 6 Н 5 -СНС l 2, С 6 Н 5 -СС l 3 h V, t°
Слайд 18: III. Реакция присоединения
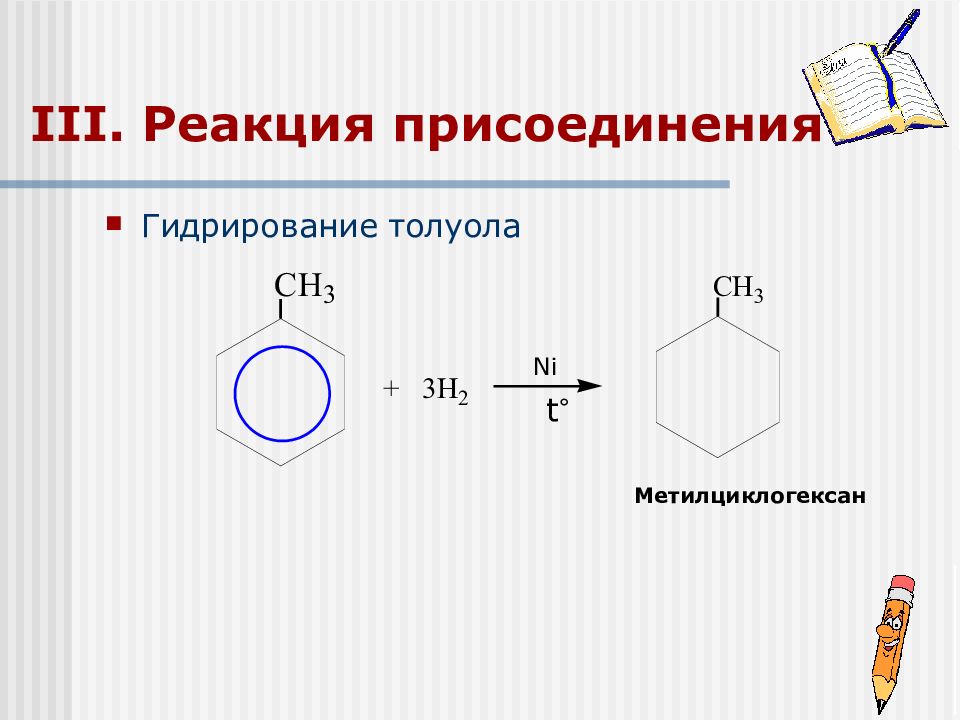
Гидрирование толуола Метилциклогексан Ni t °
Слайд 19: IV. Реакции окисления
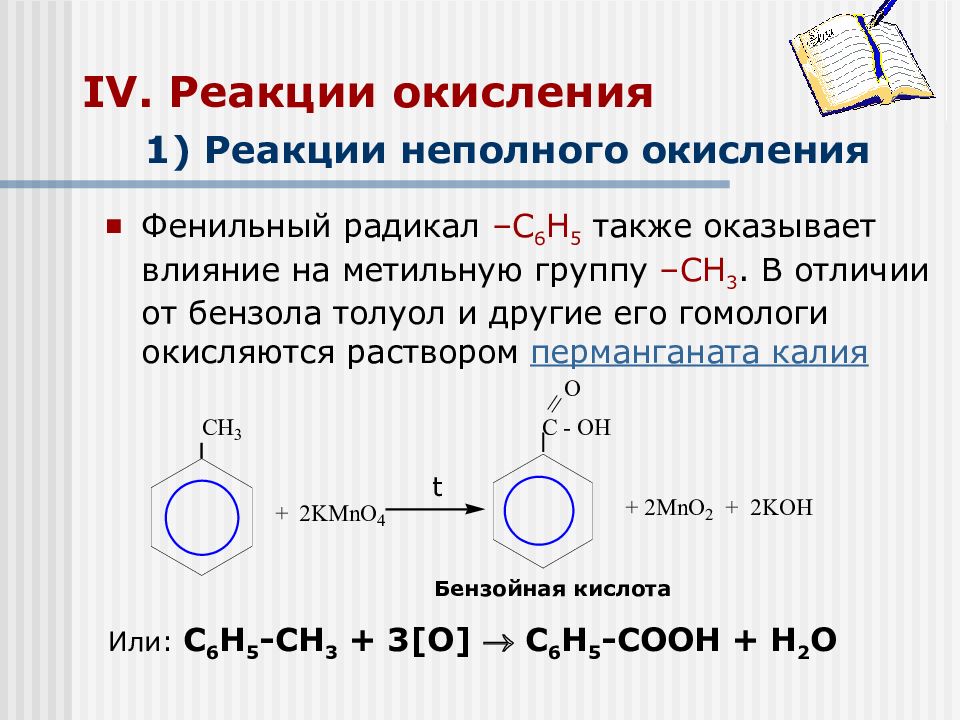
Фенильный радикал –С 6 Н 5 также оказывает влияние на метильную группу –СН 3. В отличии от бензола толуол и другие его гомологи окисляются раствором перманганата калия Или: С 6 Н 5 -СН 3 + 3 [O] С 6 Н 5 -С OOH + Н 2 O Бензойная кислота t 1) Реакции неполного окисления
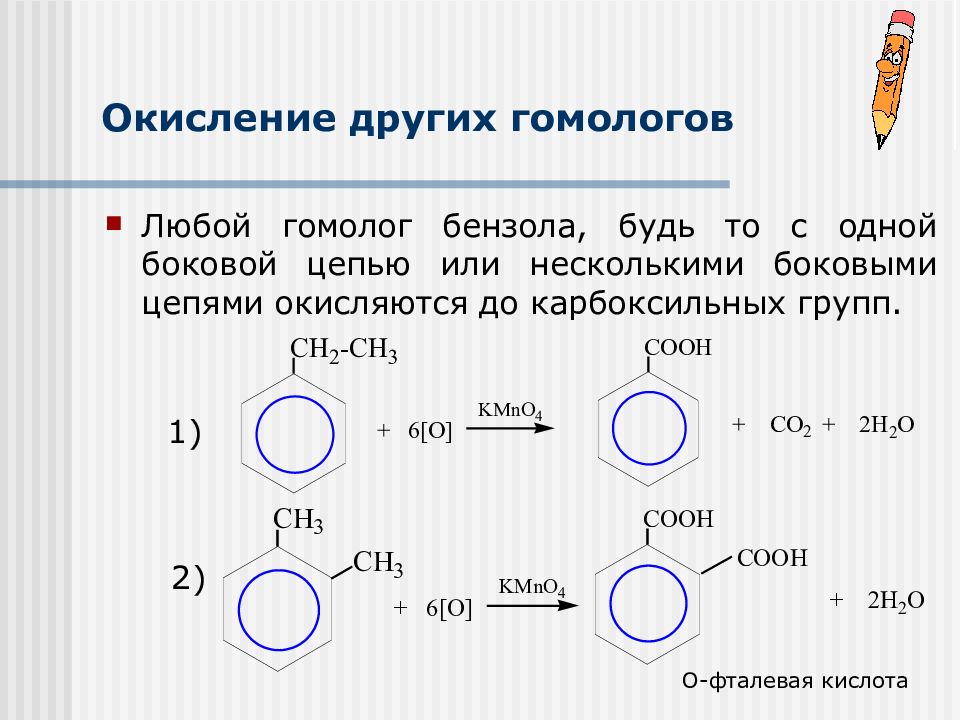
Слайд 21: Окисление других гомологов
Любой гомолог бензола, будь то с одной боковой цепью или несколькими боковыми цепями окисляются до карбоксильных групп. 1) 2) О-фталевая кислота
Слайд 22: 2) Реакции полного окисления
C 6 H 5 -CH 3 + 9O 2 7CO 2 + 4H 2 O Горение толуола в кислороде ( на воздухе горит коптящим пламенем)
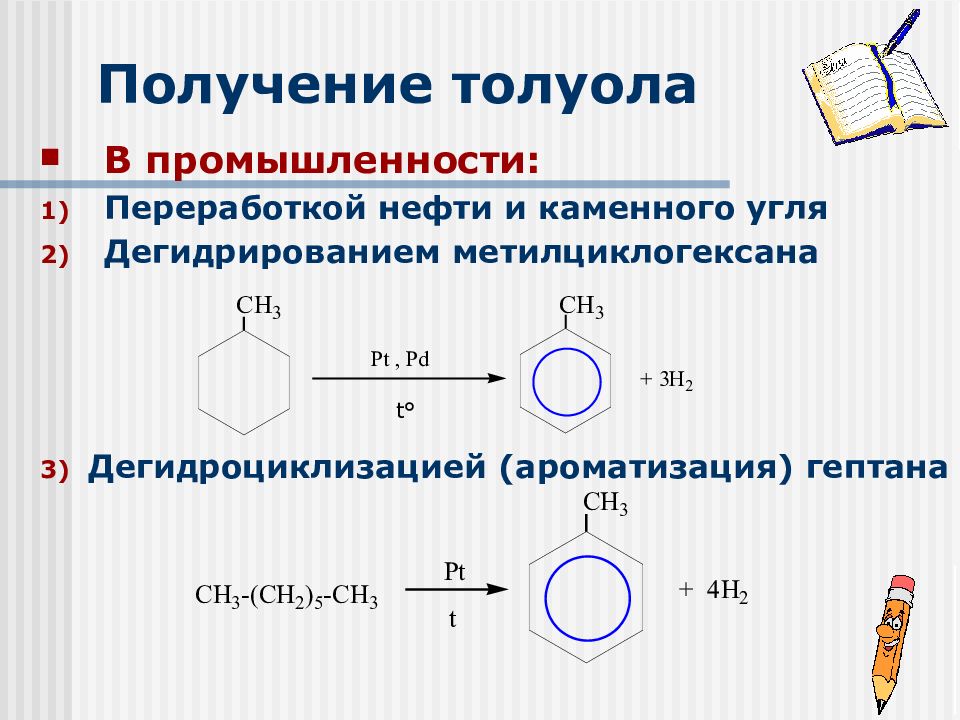
Слайд 23: Получение толуола
В промышленности: Переработкой нефти и каменного угля Дегидрированием метилциклогексана Дегидроциклизацией (ароматизация) гептана t°
Слайд 24
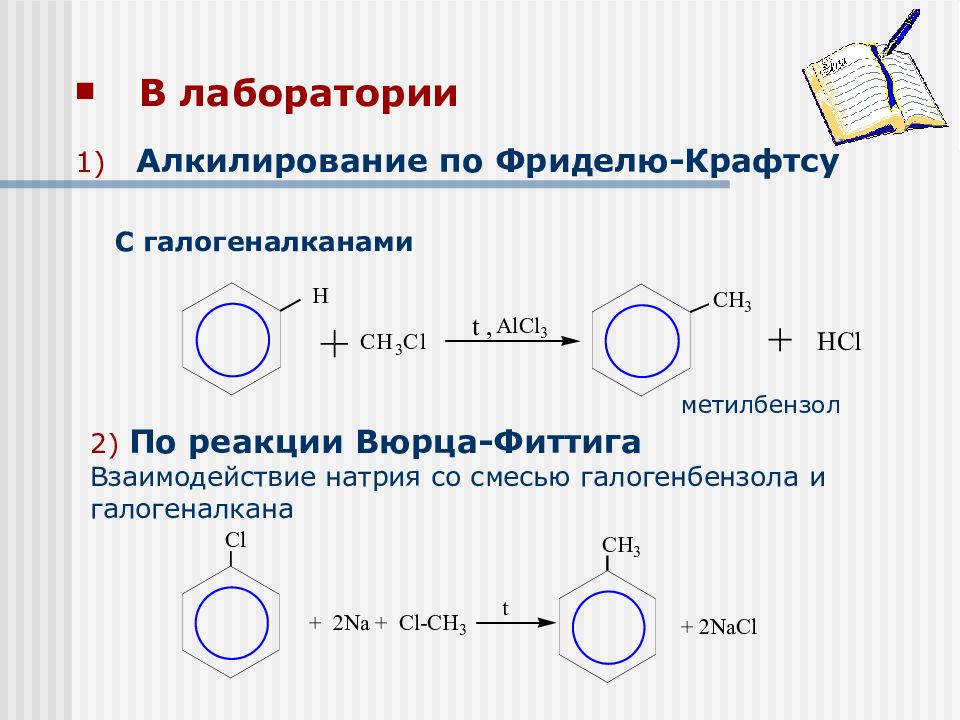
В лаборатории С галогеналканами метилбензол 2) По реакции Вюрца-Фиттига Взаимодействие натрия со смесью галогенбензола и галогеналкана Алкилирование по Фриделю-Крафтсу
Слайд 25
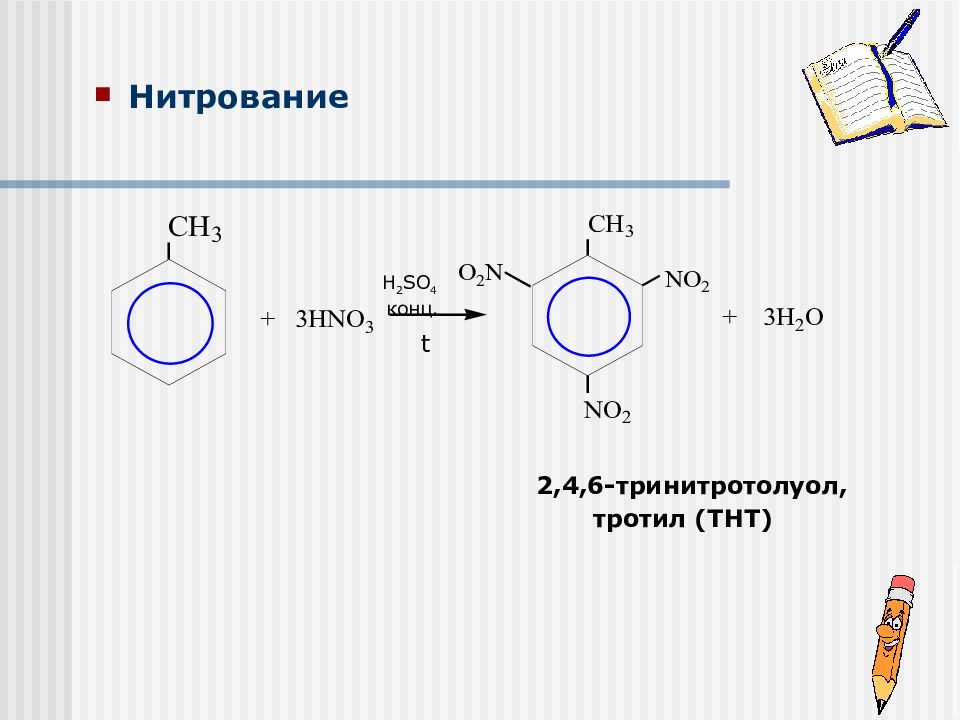
Применение толуола и его производных Толуол и его производные – важнейшее сырьё для химической промышленности В качестве растворителей Для синтеза различных красителей, лекарственных препаратов, взрывчатых веществ (тротил) В качестве добавки, улучшающее качество бензинов
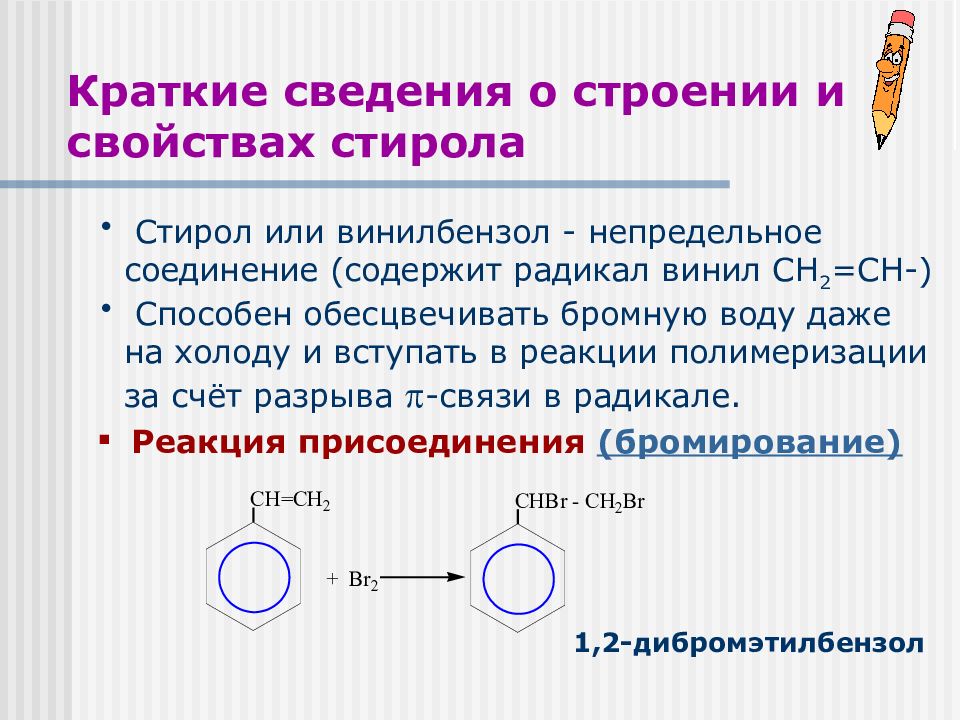
Слайд 26: Краткие сведения о строении и свойствах стирола
Стирол или винилбензол - непредельное соединение (содержит радикал винил СН 2 =СН-) Способен обесцвечивать бромную воду даже на холоду и вступать в реакции полимеризации за счёт разрыва -связи в радикале. Реакция присоединения (бромирование) 1,2-дибромэтилбензол
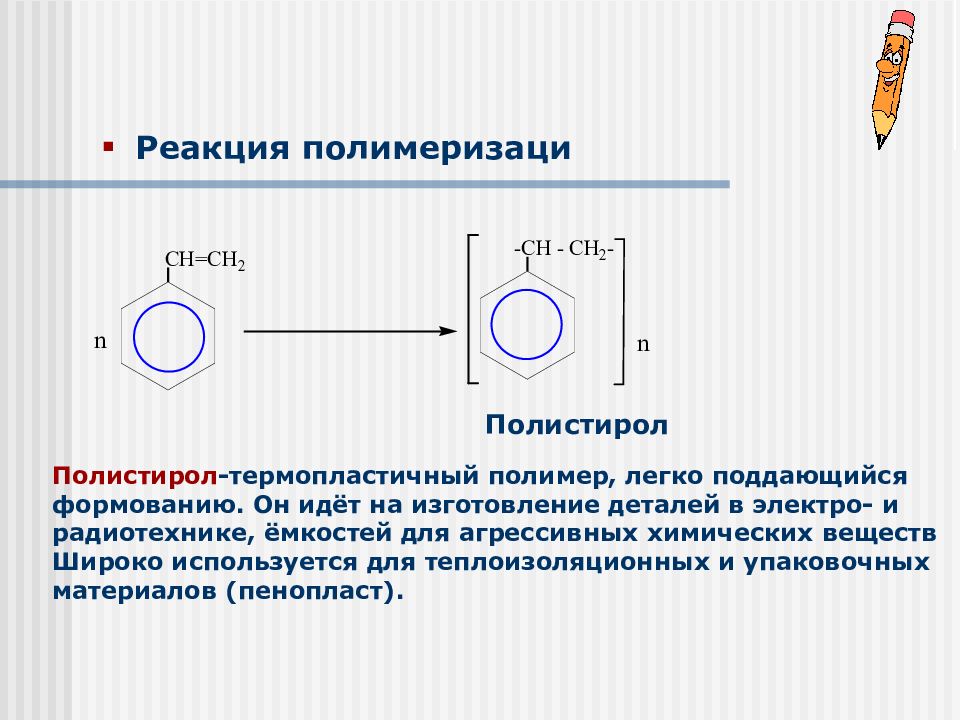
Слайд 27: Реакция полимеризаци
Полистирол Полистирол -термопластичный полимер, легко поддающийся формованию. Он идёт на изготовление деталей в электро- и радиотехнике, ёмкостей для агрессивных химических веществ Широко используется для теплоизоляционных и упаковочных материалов (пенопласт).
Слайд 28: Вопросы для самоконтроля
Приведите примеры реакций замещения с участием толуола. Объясните причины различий реакционной способности толуола по сравнению с бензолом в реакциях такого типа. Укажите, какие реагенты используются при: а) нитровании б) сульфировании в) алкилировании аренов.
Слайд 29
Приведите примеры реакций присоединения с участием толуола. Объясните, почему KMnO 4 реагирует с толуолом, но не реагирует с бензолом. Какие способы получения толуола вы знаете? Какие заместители являются ориентантами а) первого рода? б) второго рода? Приведите примеры.
Слайд 30: Упражнения и задачи для самостоятельной работы
Назовите следующие соединения: а) б) в) г) Ответы: а) 1-метил-4-пропилбензол (п-пропилтолуол) б) 1-бром-2-метилбензол (0-бромтолуол) в) 1-метил-3-нитробензол (м-нитротолуол) г) 1-метил-2-сульфобензолкислота (о-толуолсульфокислота)
Слайд 31
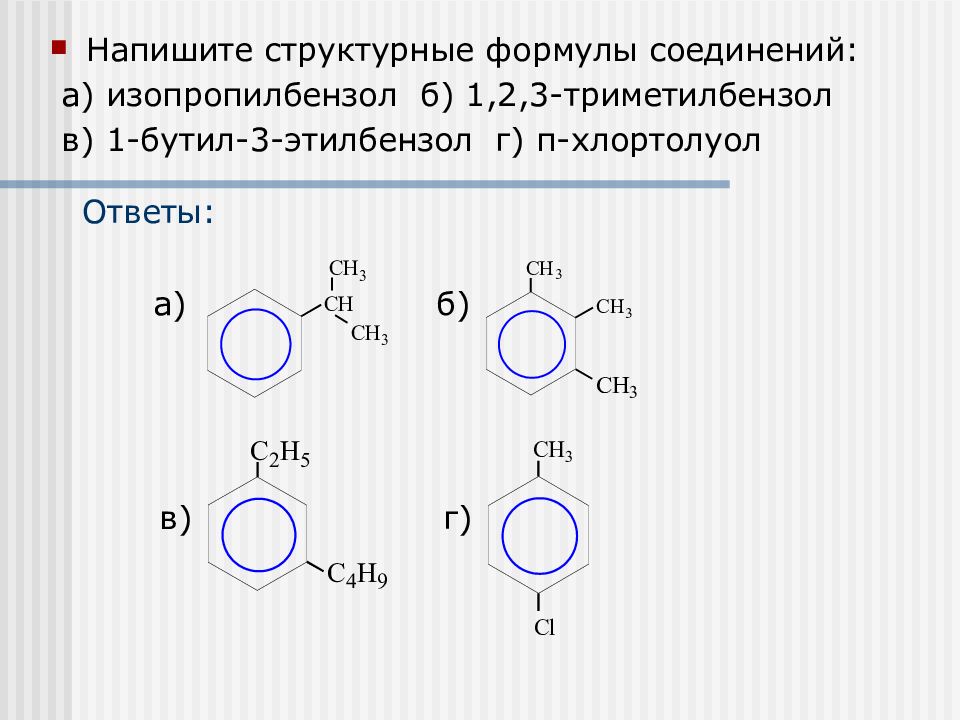
Напишите структурные формулы соединений: а) изопропилбензол б) 1,2,3-триметилбензол в) 1-бутил-3-этилбензол г) п-хлортолуол а) б) в) г) Ответы:
Слайд 32
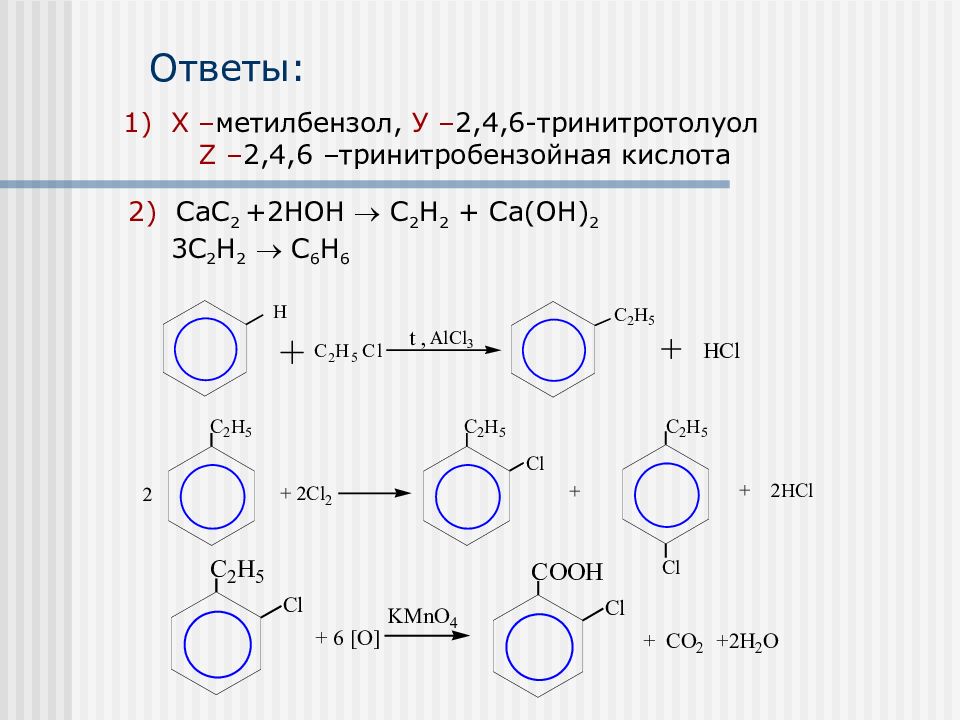
Напишите уравнения реакций следующих превращений 1) 2) Карбид кальция этин Х У Z бензол этилбензол 1-хлор-4-этилбензол п-хлорбензойная кислота
Слайд 33: 2) СаС 2 +2НОН С 2 Н 2 + Са(ОН) 2 3С 2 Н 2 С 6 Н 6
Ответы: 1) Х – метилбензол, У – 2,4,6-тринитротолуол Z – 2, 4, 6 – тринитробензойная кислота
Слайд 34
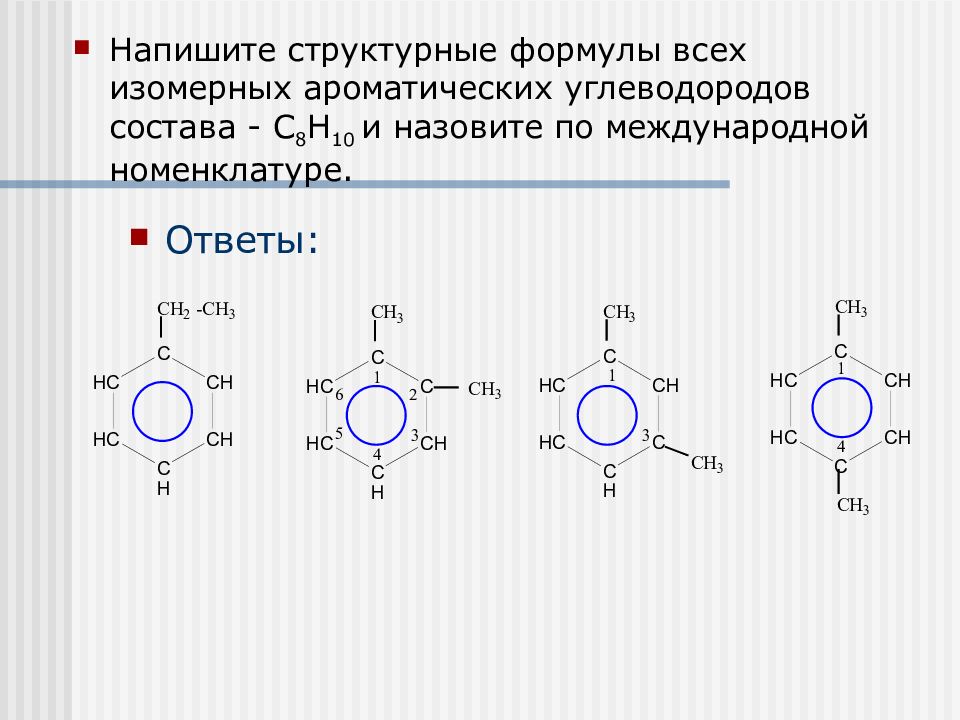
Напишите структурные формулы всех изомерных ароматических углеводородов состава - С 8 Н 10 и назовите по международной номенклатуре. Ответы:
Слайд 35: Задачи:
При сжигании 2,12 г вещества выделилось 7,04 г оксида углерода ( IV) и 1,80 г воды. Масса 1 л паров этого вещества при н.у.равна 4,73 г. Определите молекулярную формулу вещества и написать структурные формулы трёх изомеров Задача для тех, кто любит рисковать: Раствор стирола в бензоле массой 21 г на холоду и отсутствии катализаторов обесцветила 16 г брома. Какова массовая доля компонентов в исходной смеси? 1) С 8 Н 10 2) 49,52% стирола, 50,48% бензола Ответы: