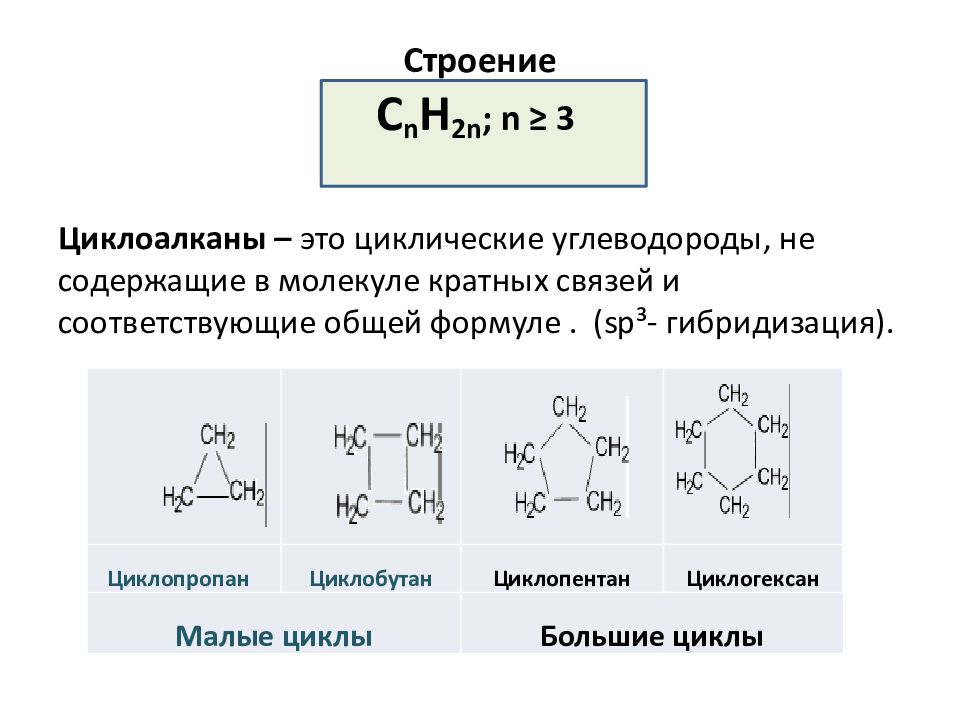
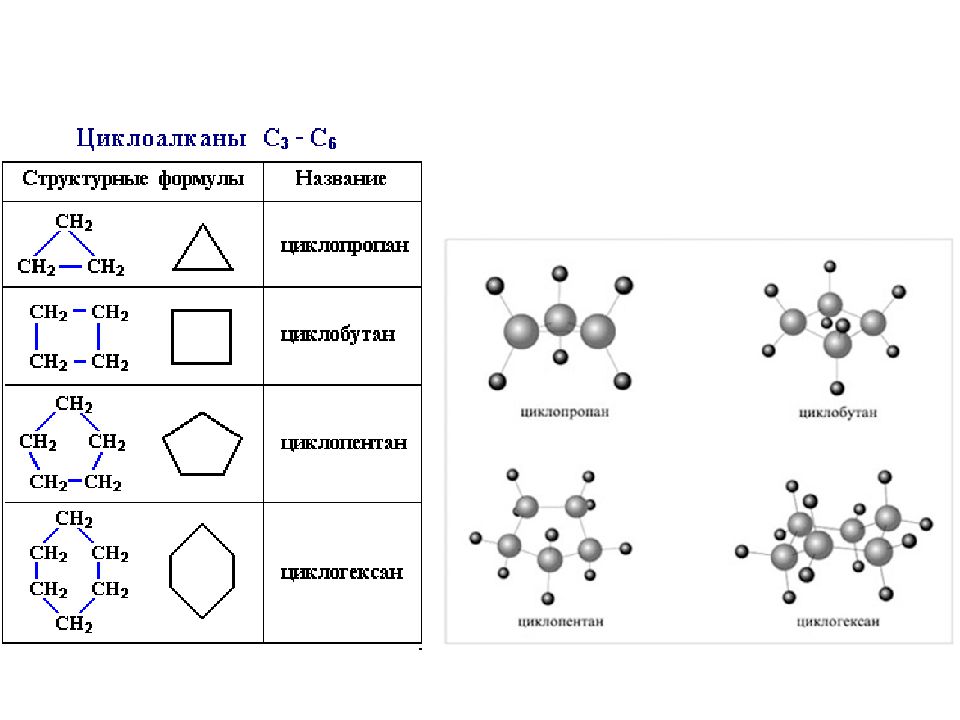
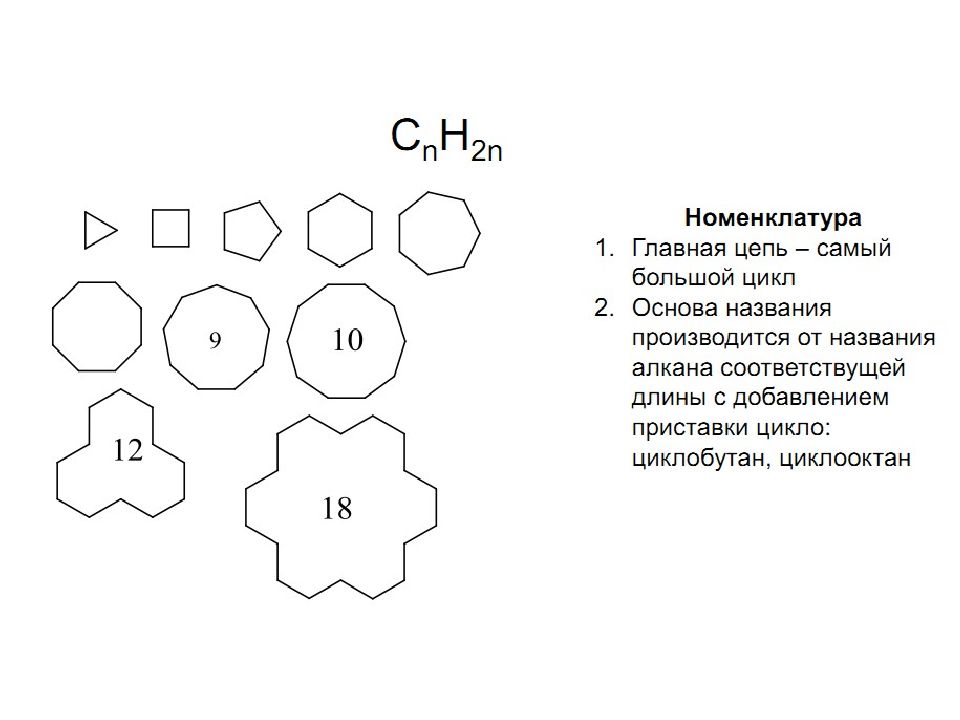
Слайд 2: Строение С n Н 2n ; n ≥ 3
Циклоалканы – это циклические углеводороды, не содержащие в молекуле кратных связей и соответствующие общей формуле. (sp³- гибридизация). Циклопропан Циклобутан Циклопентан Циклогексан Малые циклы Большие циклы
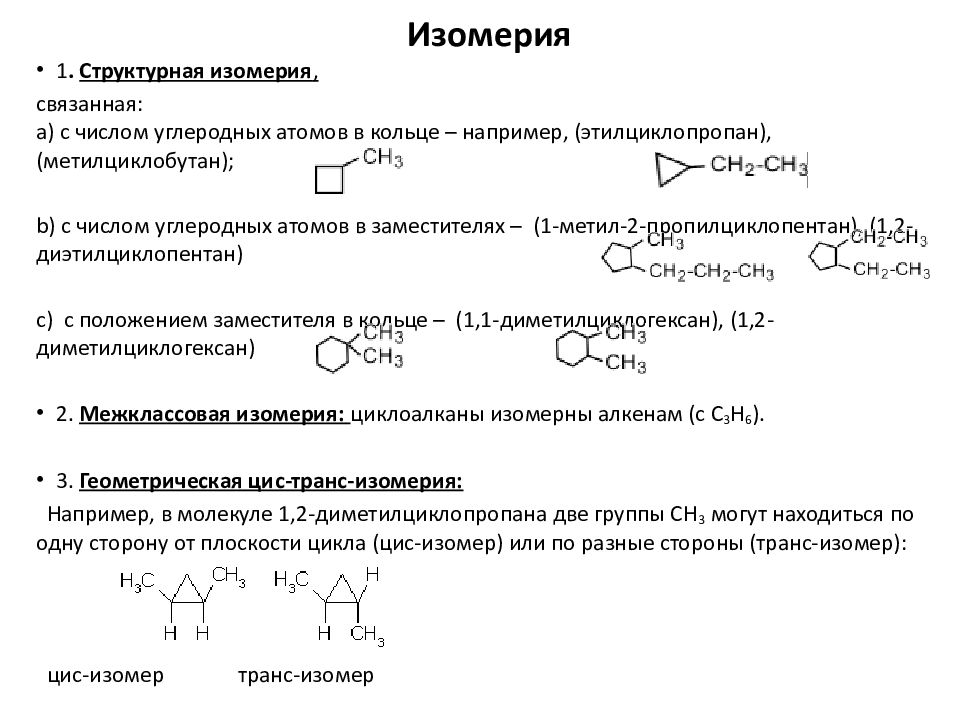
Слайд 5: Изомерия
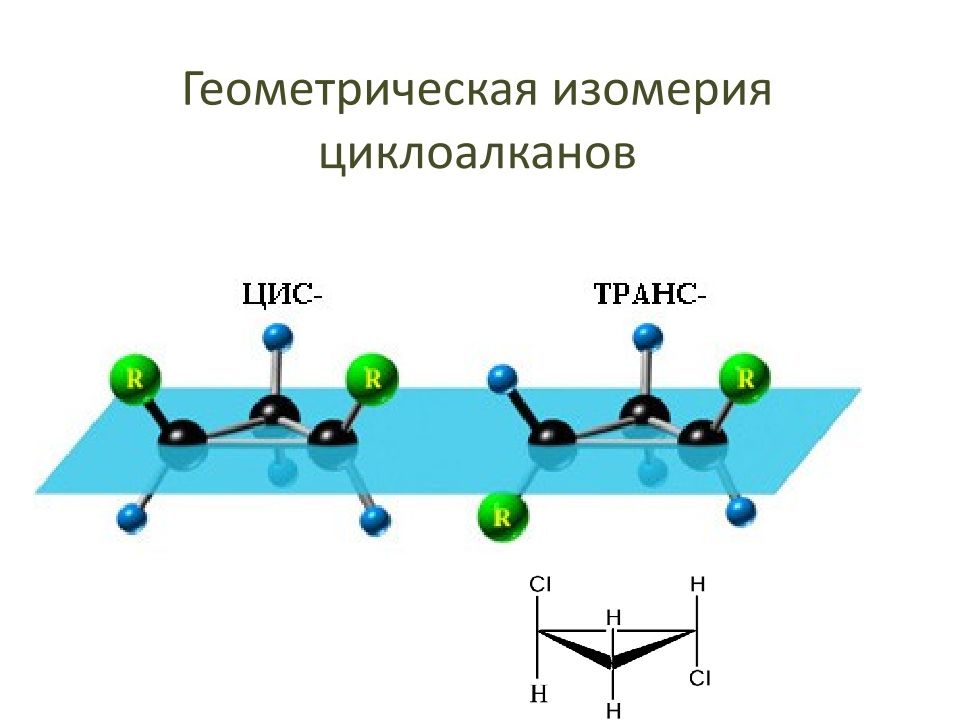
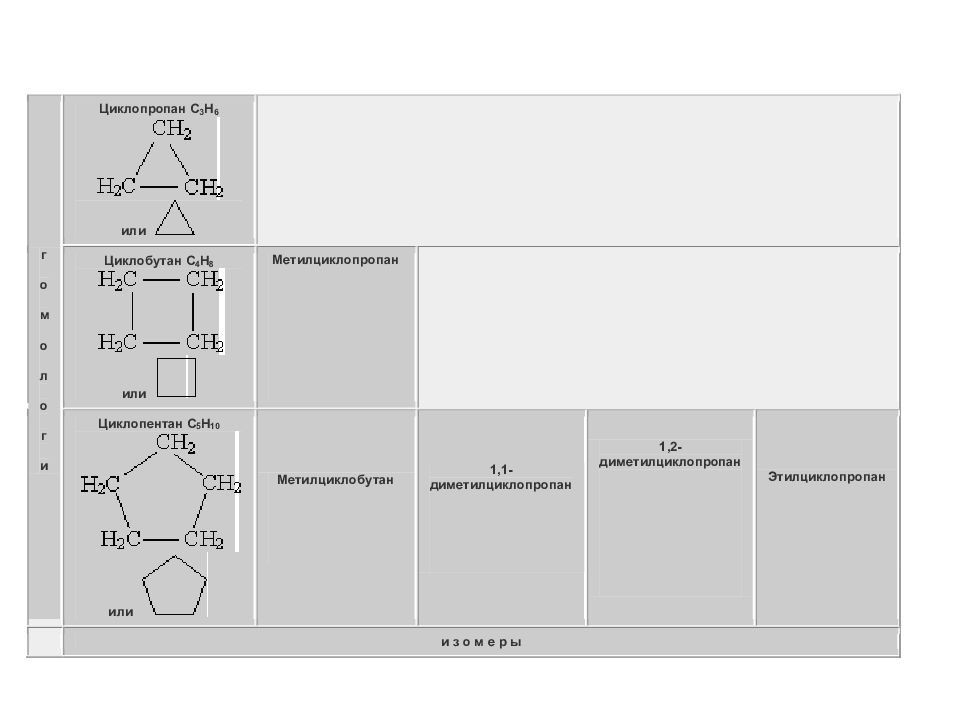
1. Структурная изомерия, связанная : a) с числом углеродных атомов в кольце – например, ( этилциклопропан ), (метилциклобутан ); b) с числом углеродных атомов в заместителях – (1-метил-2-пропилциклопентан), (1,2-диэтилциклопентан ) c) с положением заместителя в кольце – (1,1-диметилциклогексан), (1,2-диметилциклогексан) 2. Межклассовая изомерия: циклоалканы изомерны алкенам (с С 3 Н 6 ). 3. Геометрическая цис -транс-изомерия: Например, в молекуле 1,2-диметилциклопропана две группы СН 3 могут находиться по одну сторону от плоскости цикла ( цис -изомер) или по разные стороны (транс-изомер ): цис -изомер транс-изомер
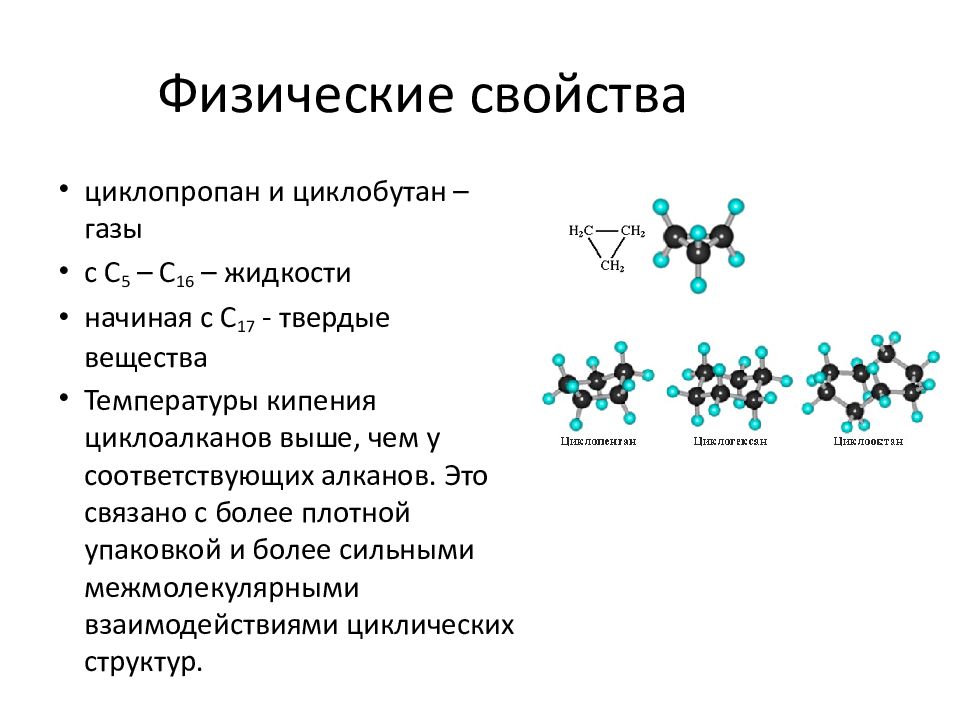
Слайд 8: Физические свойства
циклопропан и циклобутан – газы с С 5 – С 16 – жидкости начиная с С 17 - твердые вещества Температуры кипения циклоалканов выше, чем у соответствующих алканов. Это связано с более плотной упаковкой и более сильными межмолекулярными взаимодействиями циклических структур.
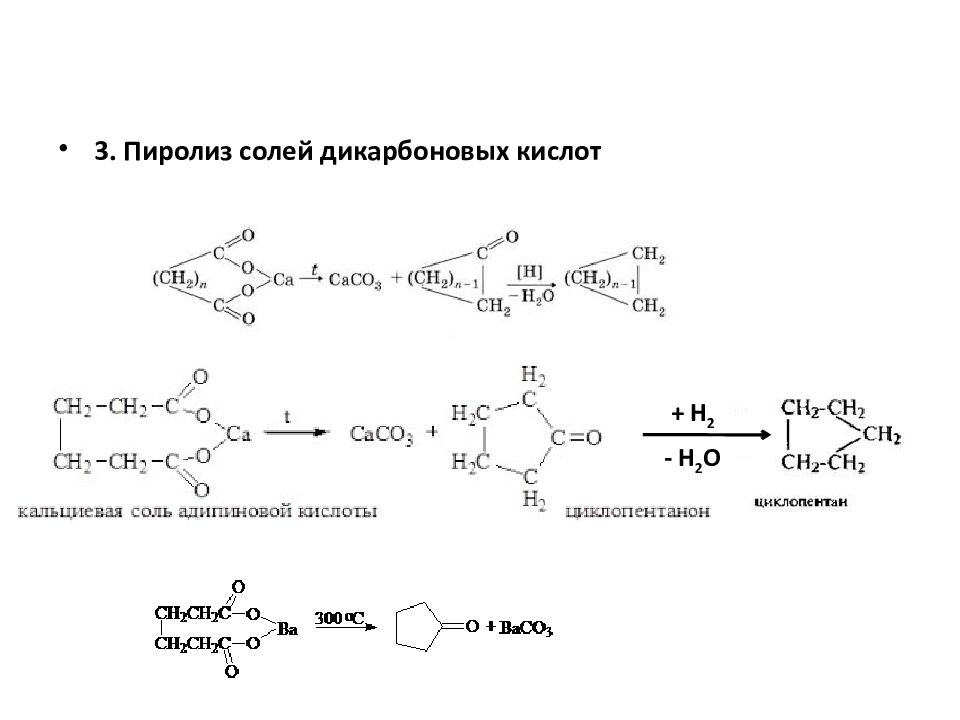
Слайд 9: Получение
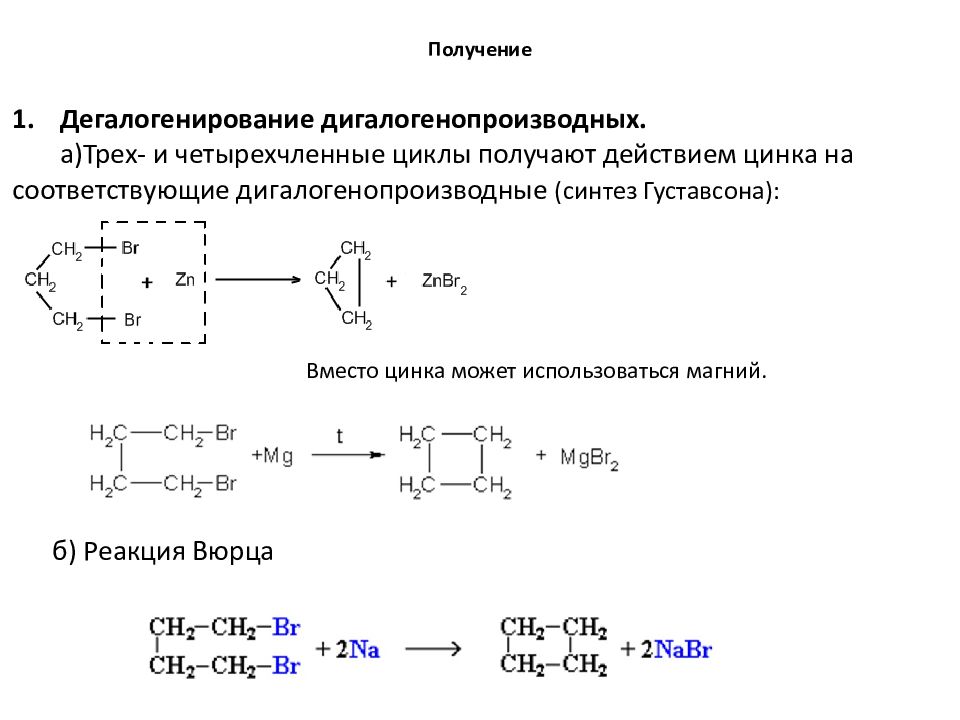
Дегалогенирование дигалогенопроизводных. а)Трех- и четырехчленные циклы получают действием цинка на соответствующие дигалогенопроизводные ( синтез Густавсона ): Вместо цинка может использоваться магний. Получение б) Реакция Вюрца
Слайд 10: Получение
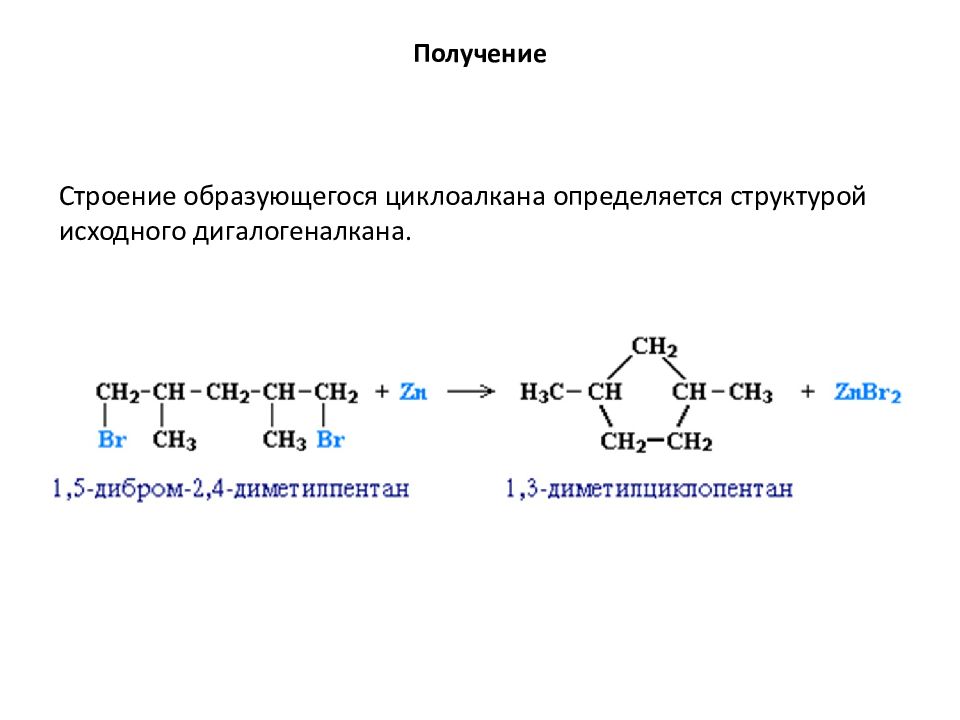
Строение образующегося циклоалкана определяется структурой исходного дигалогеналкана.
Слайд 11: Получение
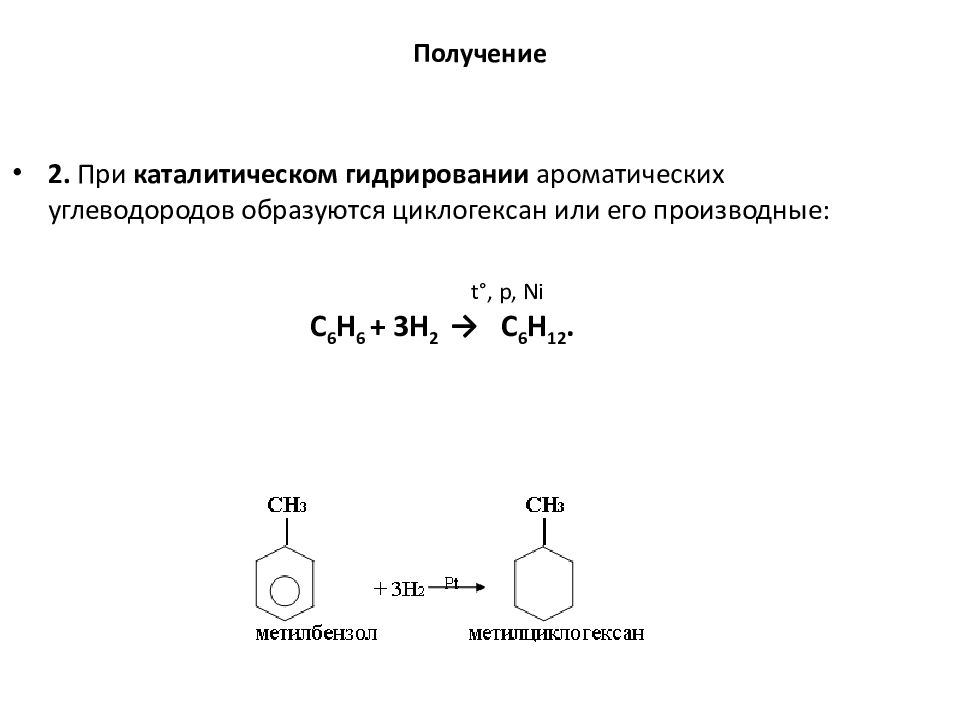
2. При каталитическом гидрировании ароматических углеводородов образуются циклогексан или его производные: t °, р, Ni C 6 H 6 + 3 H 2 → C 6 H 12.
Слайд 14: Химические свойства циклоалканов
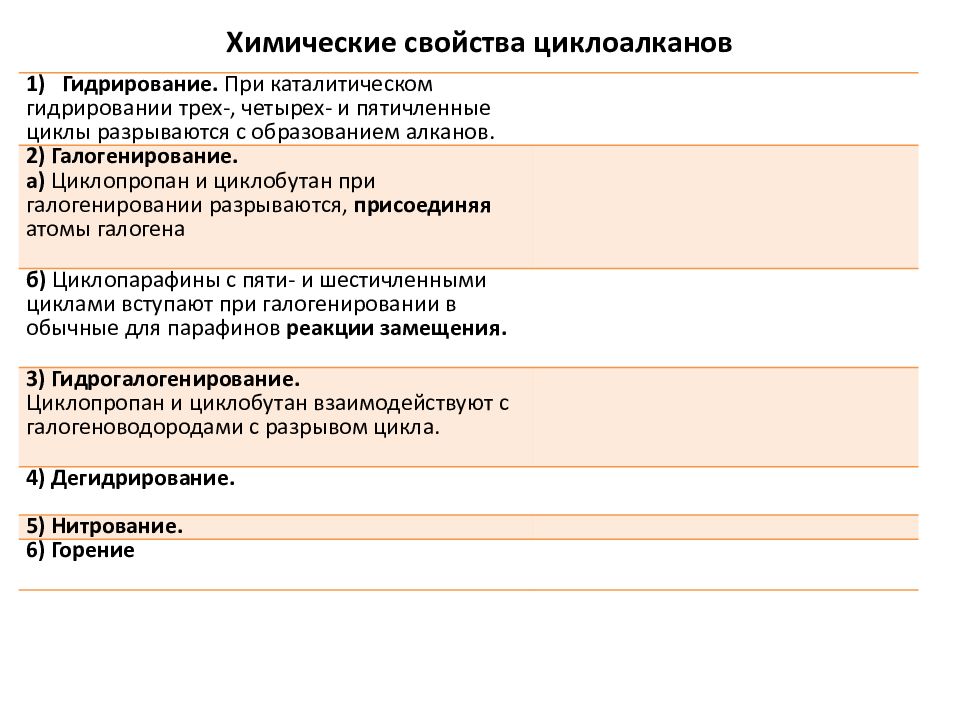
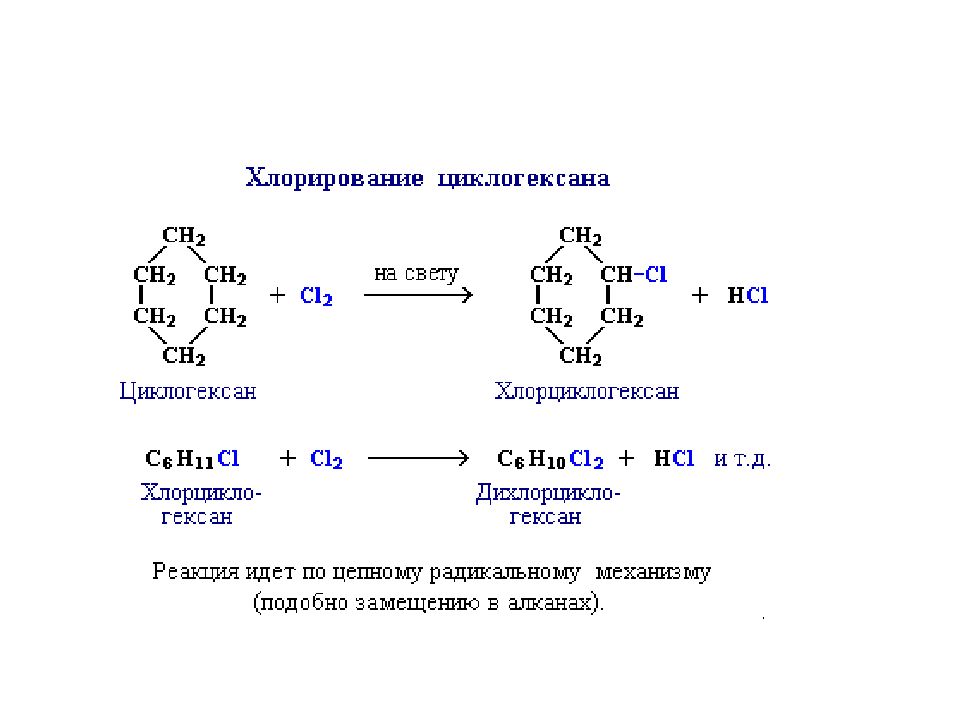
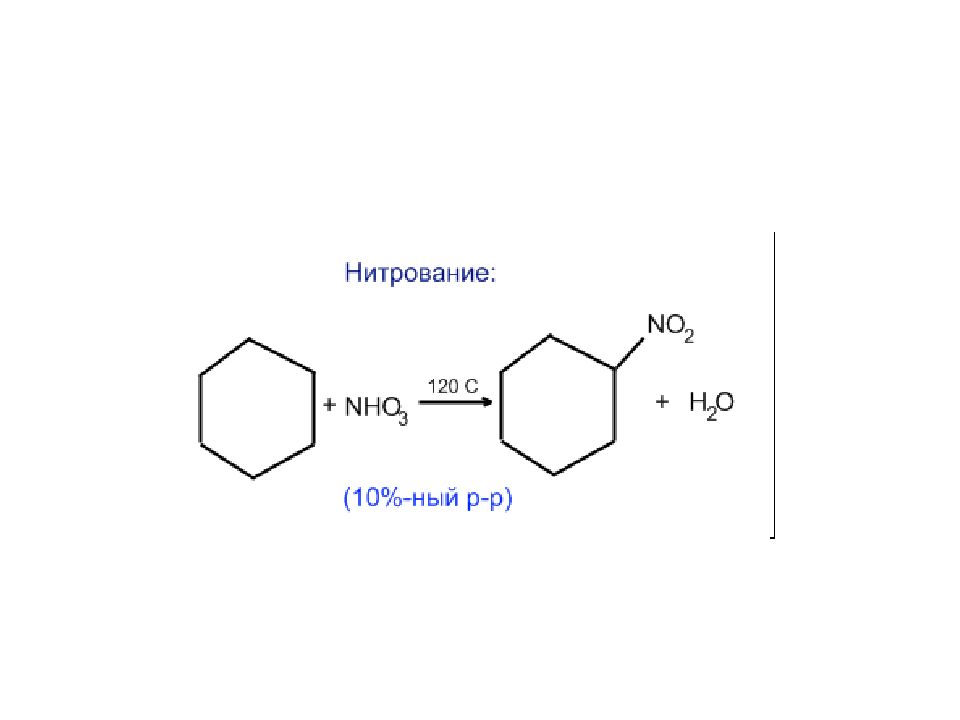
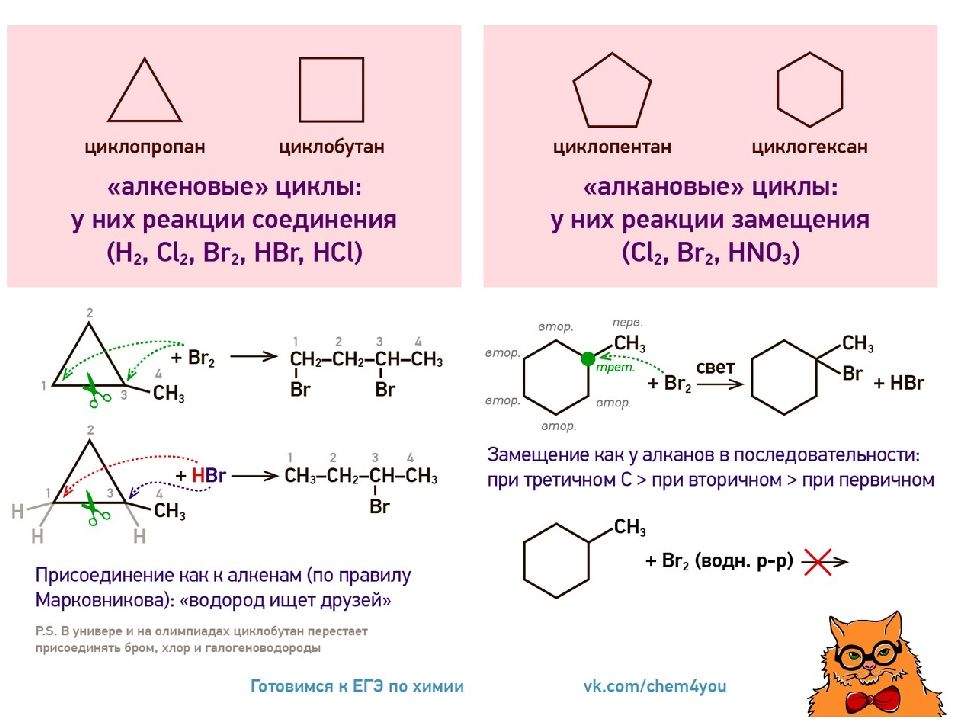
1) Гидрирование. При каталитическом гидрировании трех-, четырех- и пятичленные циклы разрываются с образованием алканов. 2) Галогенирование. а) Циклопропан и циклобутан при галогенировании разрываются, присоединяя атомы галогена б) Циклопарафины с пяти- и шестичленными циклами вступают при галогенировании в обычные для парафинов реакции замещения. 3) Гидрогалогенирование. Циклопропан и циклобутан взаимодействуют с галогеноводородами с разрывом цикла. 4) Дегидрирование. 5) Нитрование. 6) Горение
Слайд 15: Химические свойства циклоалканов
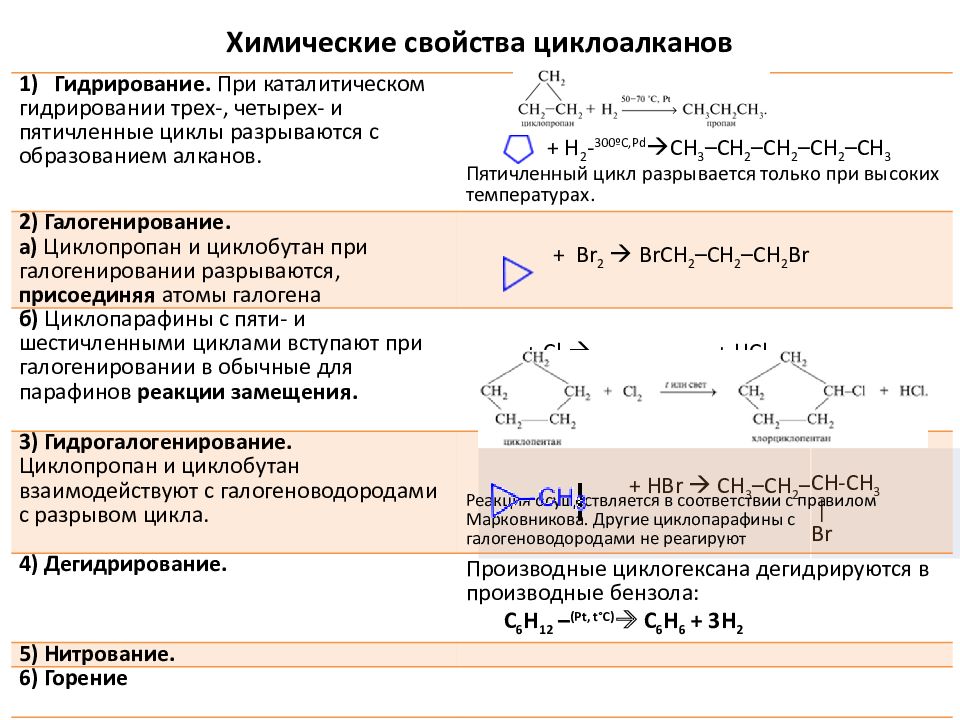
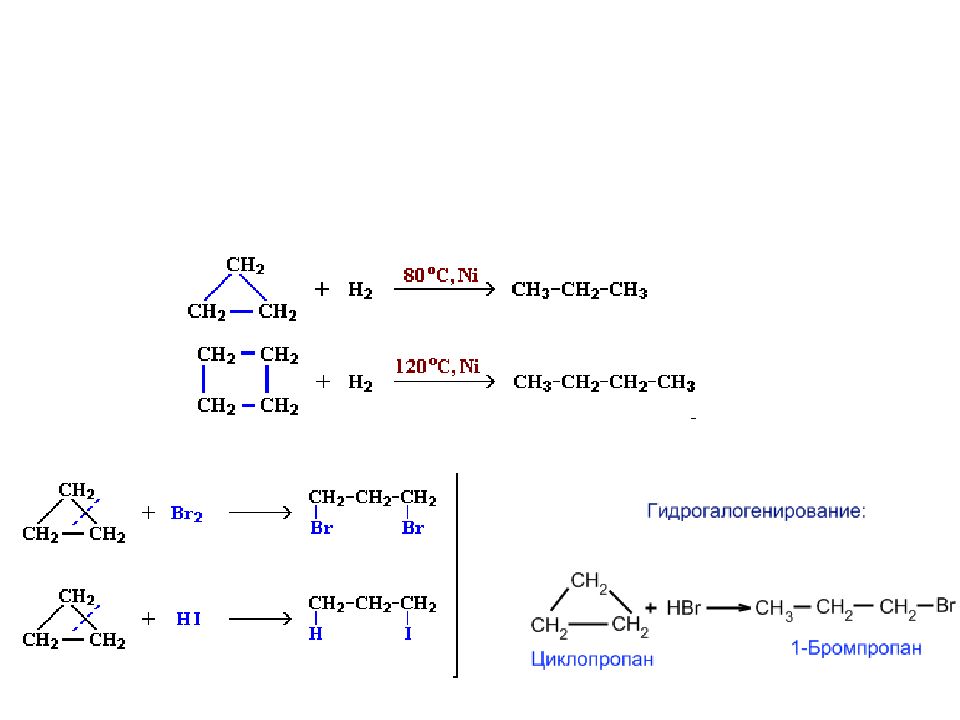
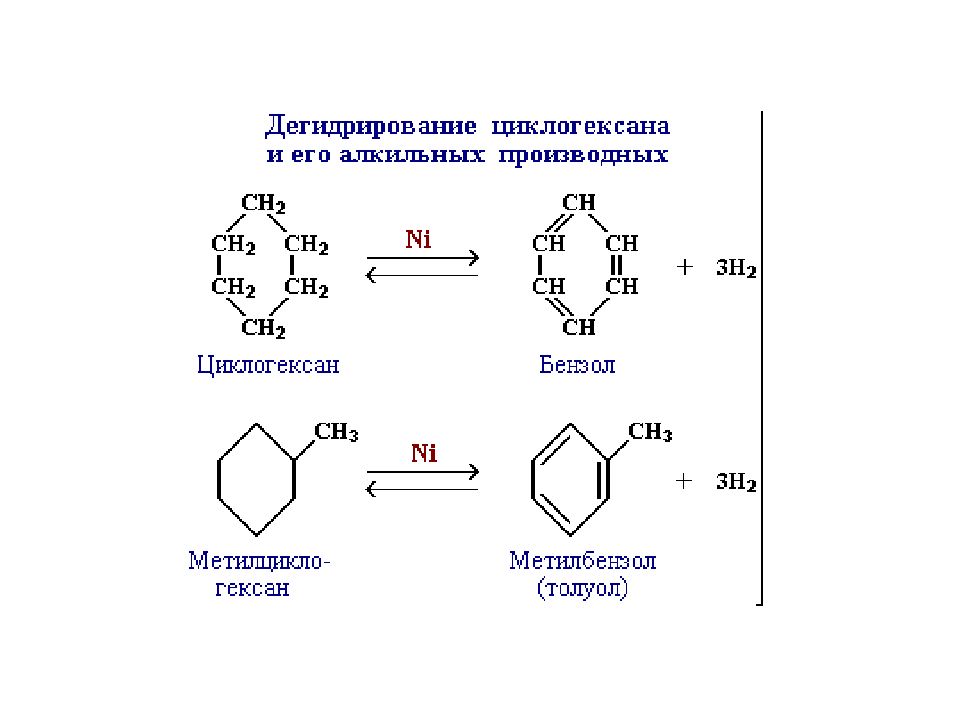
+ HBr CH 3 –CH 2 – CH-CH 3 │ Br 1) Гидрирование. При каталитическом гидрировании трех-, четырех- и пятичленные циклы разрываются с образованием алканов. + H 2 - 120ºC,Ni + H 2 - 300ºC,Pd CH 3 – CH 2 – CH 2 – CH 2 – CH 3 Пятичленный цикл разрывается только при высоких температурах. 2) Галогенирование. а) Циклопропан и циклобутан при галогенировании разрываются, присоединяя атомы галогена + Br 2 BrCH 2 –CH 2 –CH 2 Br б) Циклопарафины с пяти- и шестичленными циклами вступают при галогенировании в обычные для парафинов реакции замещения. + Cl 2 + HCl 3) Гидрогалогенирование. Циклопропан и циклобутан взаимодействуют с галогеноводородами с разрывом цикла. Реакция осуществляется в соответствии с правилом Марковникова. Другие циклопарафины с галогеноводородами не реагируют 4) Дегидрирование. Производные циклогексана дегидрируются в производные бензола: C 6 H 12 – (Pt, t°C ) C 6 H 6 + 3H 2 5) Нитрование. 6) Горение Химические свойства циклоалканов
Слайд 16: Химические свойства циклоалканов
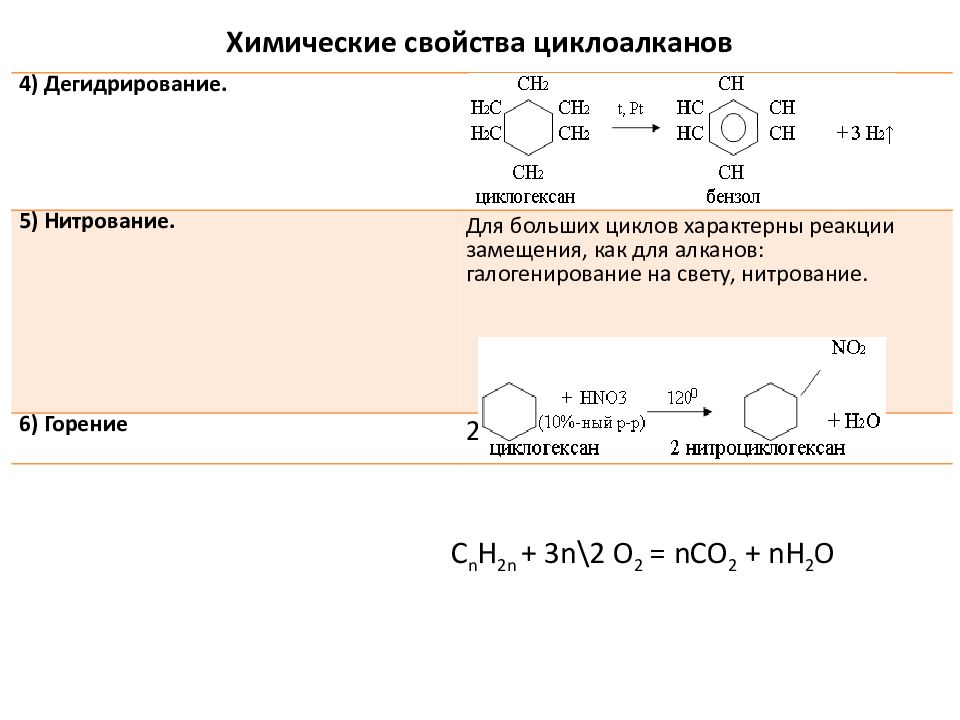
4) Дегидрирование. 5) Нитрование. Для больших циклов характерны реакции замещения, как для алканов: галогенирование на свету, нитрование. 6) Горение 2С 3 Н 6 + 9О 2 = 6СО 2 + 6Н 2 О Химические свойства циклоалканов С n H 2n + 3n\2 O 2 = nCO 2 + nH 2 O
Слайд 24: Применение, значение для человека
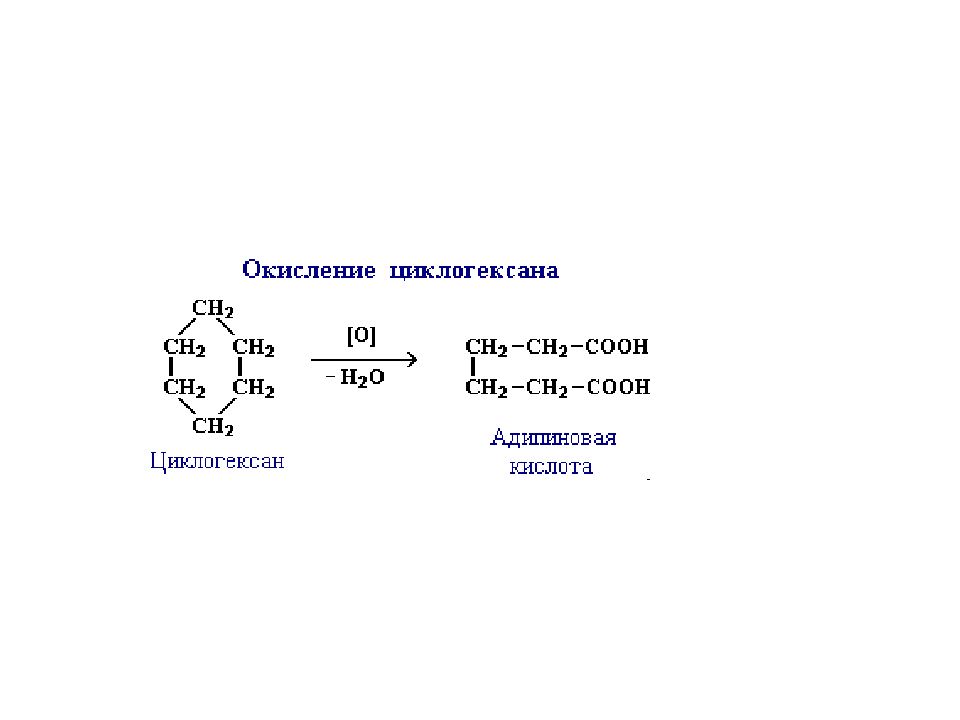
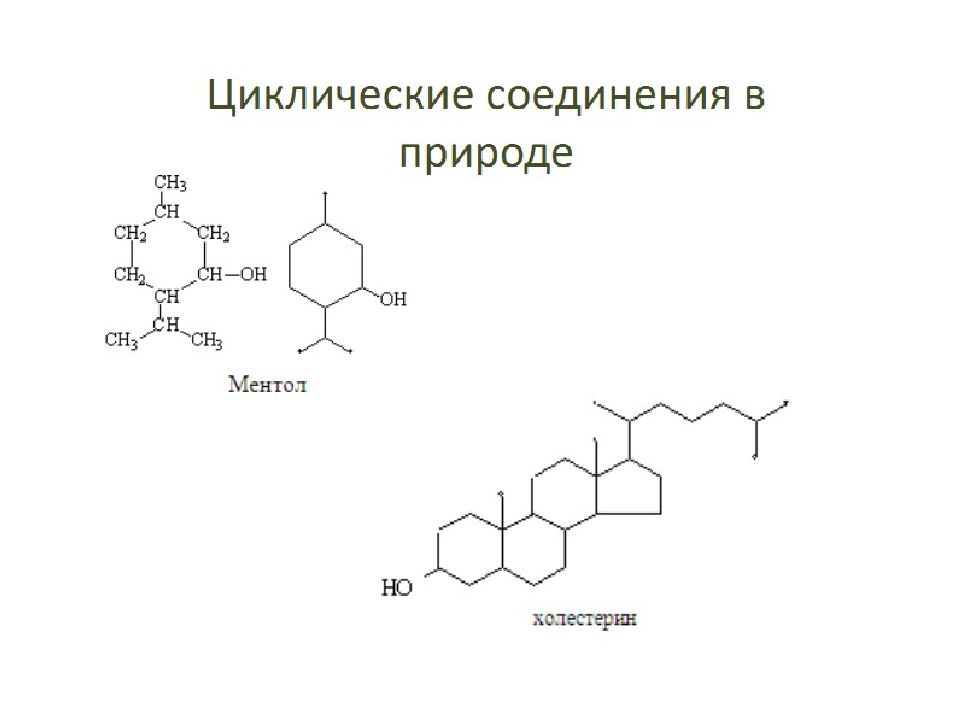
Циклоалканы широко распространены в природе, они входят в состав нефти. В нефтехимической промышленности нафтены являются источником получения ароматических углеводородов путем каталитического крекинга. Так же Смолы деревьев построены на циклоалканах, циклоалканы входят в состав восточных благовоний, мускус камфора, амбра мятные лимонные масла, и т.д. Они находят применение в разных областях народного хозяйства. Так, циклопентан используется в разных синтезах и как добавка к моторному топливу для повышения качества. Циклогексан используется для синтеза полупродуктов при производстве синтетических волокон нейлона и капрона. Они содержаться в сильнейших растительных ядах, которые опасны для человека. Так же интересно то, что холестерин родоначальник ациклических веществ, он содержит циклопентановый блок. Циклоалканы не обошли стороной витамины, например витамины группы «Д», а он в свою очередь является ключевым фактором, определяющим всасывание кальция. Циклоалканы присутствуют в незаменимых гормонах, без которых человеку не выжить, в желчных кислотах, и в половых гормонах - тестостерон, — основной мужской половой гормон, без которого невозможно размножение.
Слайд 25: Задание № 1
Напишите структурные формулы следующих циклоалканов: 1) 1,2 – диэтилциклопентан; 2) циклогептан; 3) 1-метил-2-этилциклобутан;
Слайд 26: Задание № 2
Написать уравнение циклизации следующих дигалогеналканов под действием металлического цинка: 1) 1,3- дибромпропана; 2) 1,4-дибропентана; 3) 2,4-дибромпентана.
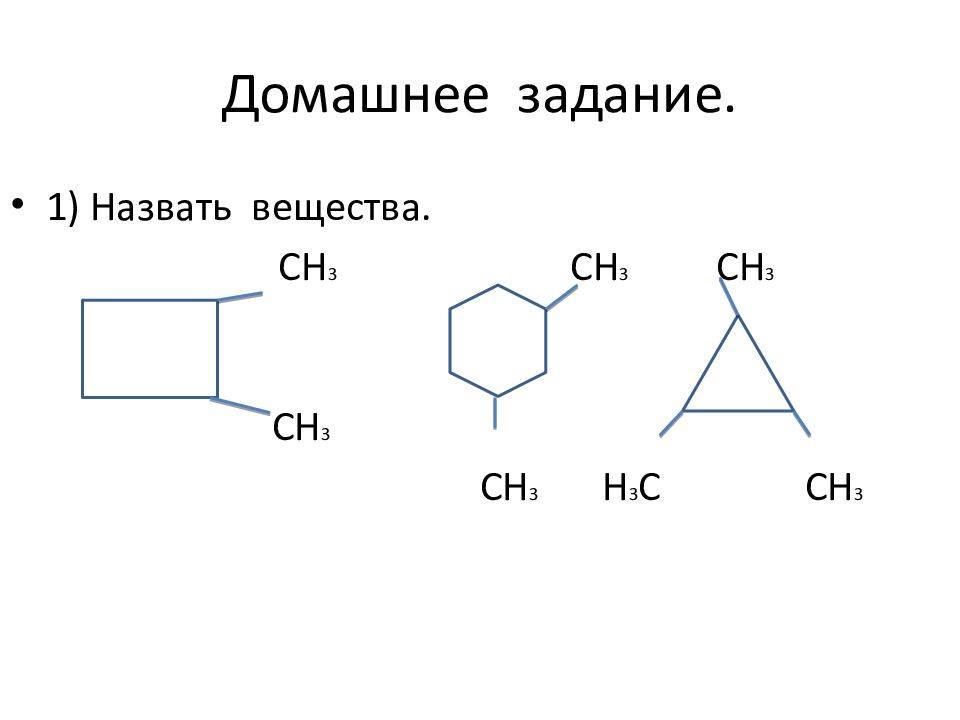
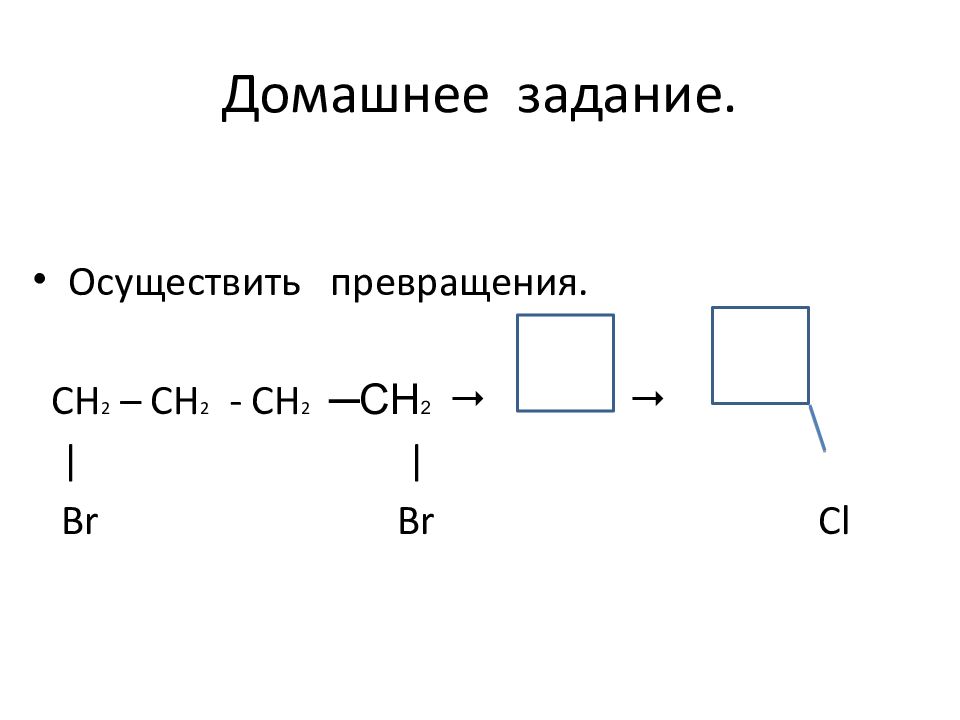
Слайд 27: Домашнее задание
1) Назвать вещества. СН 3 СН 3 СН 3 СН 3 СН 3 Н 3 С СН 3