Первый слайд презентации: 4 дәріс. Химиялық талдау әдістері. Жалпы дәрілік заттардың шынайылығын талдау. Алкандар мен алкендер негізіндегі дәрілік заттар және олардың құрамын талдау
Оқытушы Нурлыбаева А.Н. Тараз 2023 М.Х. Дулати атындағы Тараз Өңірлік университеті Химия және Химиялық технология
Слайд 2: Алкандар. ( қаныққан көмірсутектер. Парафиндер. )
Алкандар – көміртектің барлық атомдары дара ( σ -) сигма байланыспен байланысқан жалпы формуласы мынандай көмірсутектер C n H 2n+2
Слайд 3: Метанның құрылысы
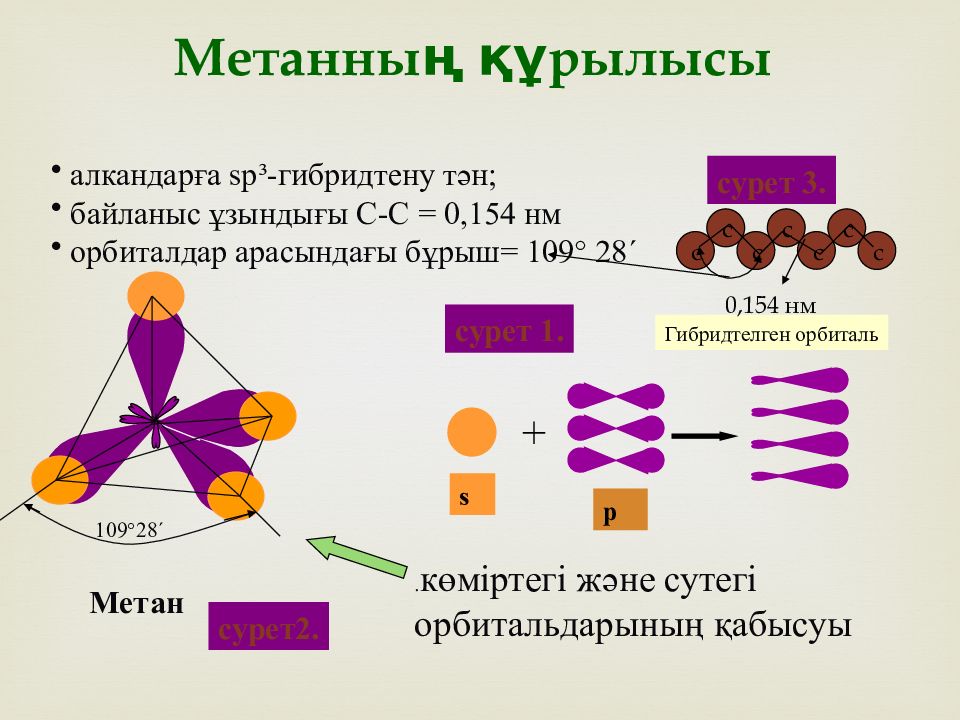
Метан алкандарға sp ³- гибридтену тән ; байланыс ұзындығы С-С = 0,154 нм орбиталдар арасындағы бұрыш= 109 ° 28 ´ . көміртегі және сутегі орбитальдарының қабысуы + 109 °28´ Метанның құрылысы s р Гибридтелген орбиталь сурет 1. сурет2. сурет 3. c c c c c c c 0,154 нм
Слайд 4: Галоген туындылар
Қаныққан көмірсутектердің галоген туындыларында бір немесе бірнеше галоген атомдары (фтор, хлор, бром немесе йод) болады. Медицинада хлороформ, йодоформ, хлоралгидрат қолданылады, бірақ этилхлорид (хлорэтан, хлорэтил) және галотан (галотан) кеңінен қолданылады (1-кесте). Галоген туындылар
Слайд 5: Хлороформ
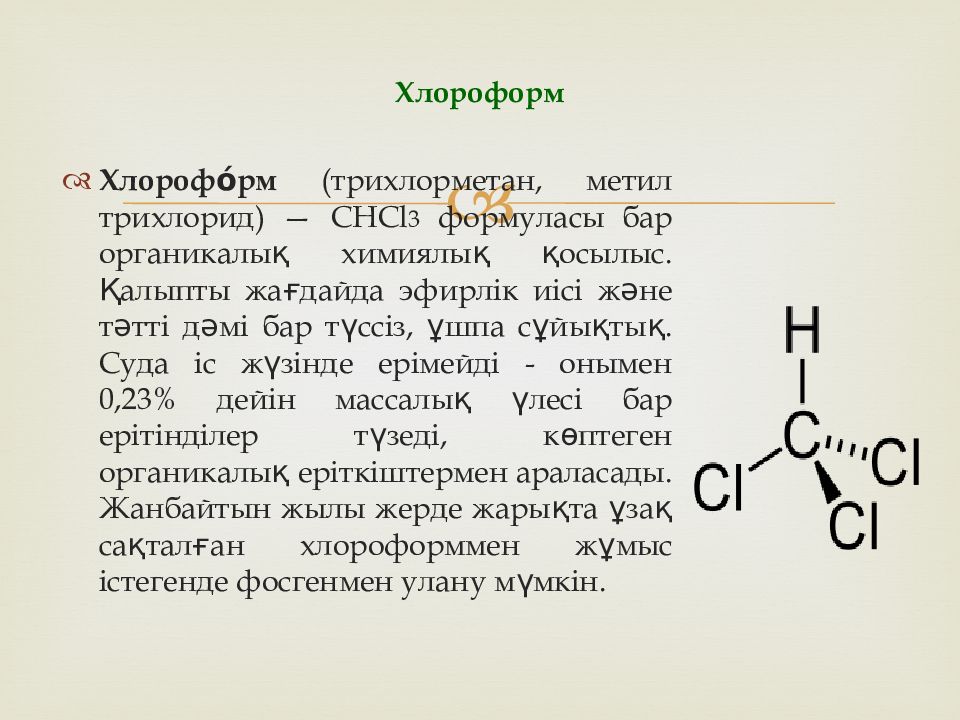
Хлорофо́рм (трихлорметан, метил трихлорид) — CHCl 3 формуласы бар органикалық химиялық қосылыс. Қалыпты жағдайда эфирлік иісі және тәтті дәмі бар түссіз, ұшпа сұйықтық. Суда іс жүзінде ерімейді - онымен 0,23% дейін массалық үлесі бар ерітінділер түзеді, көптеген органикалық еріткіштермен араласады. Жанбайтын жылы жерде жарықта ұзақ сақталған хлороформмен жұмыс істегенде фосгенмен улану мүмкін. Хлороформ
Слайд 6: Физикалық қасиеттері
Сыну көрсеткіші: 15°С кезінде 1,44858. Кристалдану температурасы: -63,55 °C Қайнау температурасы: 61,152 °C Дипольдік момент: 1,15 дебай Диэлектрлік өтімділік: 20°С кезінде 4,806 Физикалық қасиеттері
Слайд 7: Алынуы
Өнеркәсіпте хлороформ метанды немесе хлорметанды хлорлау арқылы алынады. Реакция қоспасы 400–500 °C температураға дейін қызады. Бұл жағдайда бірқатар химиялық реакциялар жүреді. Бұл қоспа ультракүлгін сәулемен жарықтандырылған кезде де болады. Процесс нәтижесі метилхлорид, дихлорометан, хлороформ және тетрахлорметаннан тұратын қоспа болып табылады. Заттарды бөлу дистилляция арқылы жүзеге асырылады. Зертханада хлороформды ацетон немесе этанол мен ағартқыш арасындағы реакция арқылы да алуға болады. Коммерциялық хлороформ құрамында тұрақтандырғыш ретінде этил спирті (1-2%) бар, ол жарықта және оттегінің қатысуымен ұзақ уақыт сақтау кезінде түзілген фосгенді байланыстырады. Бейльштейн сынағында хлороформ қолданылады, бұл реакцияда жалынның мыс иондарымен көкшіл-жасыл түске айналуы байқалады. Алынуы
Слайд 8: Қолдану процесі
19 ғасырдың аяғы мен 20 ғасырдың басында хлороформ хирургиялық операцияларда анестетик ретінде пайдаланылды. Хлороформды алғаш рет хирургиялық операцияларда анестетик ретінде ағылшын дәрігері Симпсон (1848) қолданған. Ресейде Н.И.Пирогов алғаш рет анестетик ретінде хлороформды қолданды. Алайда, бұл рөлде хлороформ кейіннен қауіпсіз заттармен ауыстырылды. Хлороформ фармацевтика өнеркәсібінде, сонымен қатар бояғыштар мен пестицидтер өндірісінде еріткіш ретінде де қолданылады. Құрамында дейтерий бар хлороформ (CDCl 3 ) ядролық магниттік резонанста (ЯМР) қолданылатын ең көп таралған еріткіш болып табылады. Қолдану процесі
Слайд 9: Тазалау процесі
бірнеше кезеңдерге бөлінеді. Алдымен хлороформды концентрлі күкірт қышқылымен шайқайды, сумен жуады, кальций хлориді немесе магний сульфатының үстінде кептіреді және тазартады. Хлороформның тазалығын сүзгі қағазынан булану арқылы тексеруге болады: хлороформнан кейін иіс болмауы керек. Көгерген, өткір, тітіркендіргіш иіс хлор, хлорсутек немесе фосген қоспаларының бар екенін көрсетеді. Тазалау процесі
Слайд 10: Денеге әсер етуі
Хлороформды ингаляциялау орталық жүйке жүйесінің жұмысына теріс әсер етеді. Құрамында 0,09% (900 ppm) хлороформ бар тыныс алу ауасы қысқа уақыт ішінде бас айналуды, шаршауды және бас ауруын тудыруы мүмкін. Хлороформның созылмалы әсері бауыр мен бүйрек ауруларын тудыруы мүмкін. Дүние жүзі тұрғындарының шамамен 10% хлороформға аллергиялық реакция бар, нәтижесінде дене температурасы көтеріледі (40°C дейін). Жиі құсу тудырады (операциядан кейінгі құсу жиілігі 75-80% жетті). Денеге әсер етуі
Слайд 11: Иодоформ
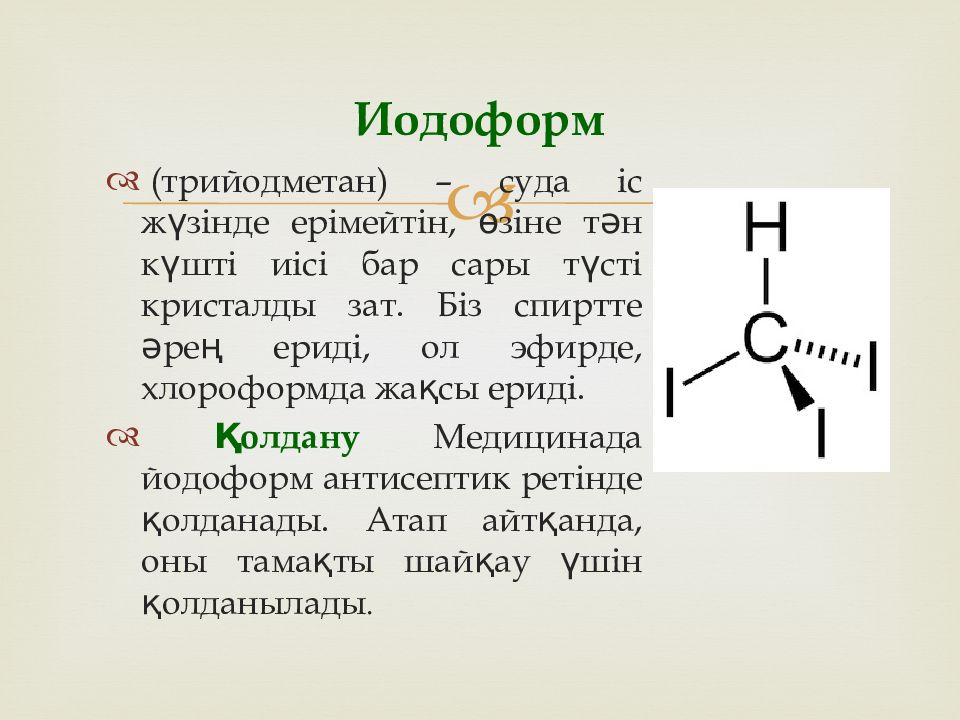
(трийодметан) – суда іс жүзінде ерімейтін, өзіне тән күшті иісі бар сары түсті кристалды зат. Біз спиртте әрең ериді, ол эфирде, хлороформда жақсы ериді. Қолдану Медицинада йодоформ антисептик ретінде қолданады. Атап айтқанда, оны тамақты шайқау үшін қолданылады. Иодоформ
Слайд 12: Физикалық қасиеттері
Химиялық формуласы CHI 3 Физикалық қасиеттері сары кристалдар Молярлық массасы 393,73 г/моль Тығыздығы 4,008 г/см³ Жылу қасиеттері ы 123°C Б алқу температурас 217°C Химиялық қасиеттері Суда ерігіштігі 0,1 г/л Физикалық қасиеттері
Слайд 13: Алынуы
Йодоформ этанолдан немесе ацетоннан йод пен сілтілердің немесе сілтілі металл карбонаттарының әсерінен алынады: 6NaHCO 3 + 4I 2 + C 2 H 5 OH → CHI 3 ↓ + HCOONa + 5NaI + 5H 2 O + 6CO 2 ↑ Йодоформды калий немесе натрий йодидін спирттік ерітіндіде электролиздеу арқылы да алуға болады. Электролиз кезінде процеске қажетті йод пен сілті түзіледі. Реакция кезінде түзілген калий (натрий) йодиді қайтадан электролизге ұшырайды, осылайша тұздың барлық йоды йодоформ түзілуіне кетеді. Алынуы
Слайд 14: Хлоралгидрат
– C 2 H 3 Cl 3 O 2, түссіз кристалдар, суда, ацетонда, этанолда және диэтил эфирінде жақсы ериді, бензолда, пиридинде және күкіртті көміртекте аз ериді. Хлоралгидрат - хлоралдың гидратация өнімі, сондықтан оның атауы. Оны алғаш рет 1832 жылы Юстус Либиг этанолды хлорлау кезінде алған. Хлоралгидрат
Слайд 15: Хлорэтан
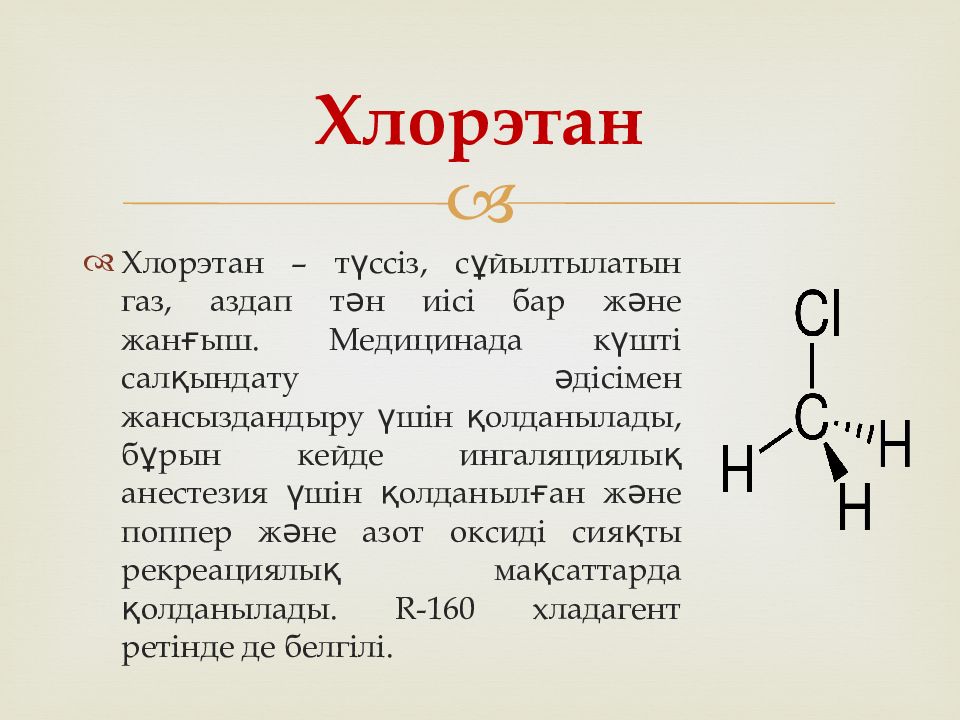
– түссіз, сұйылтылатын газ, аздап тән иісі бар және жанғыш. Медицинада күшті салқындату әдісімен жансыздандыру үшін қолданылады, бұрын кейде ингаляциялық анестезия үшін қолданылған және поппер және азот оксиді сияқты рекреациялық мақсаттарда қолданылады. R-160 хладагент ретінде де белгілі. Хлорэтан
Последний слайд презентации: 4 дәріс. Химиялық талдау әдістері. Жалпы дәрілік заттардың шынайылығын: Галатон
Түссіз, мөлдір, қозғалғыш, хлороформ иісі бар, тәтті және күйдіргіш дәмі бар ұшқыш сұйықтық. Тығыздығы - 1,865–1,870. Қайнау температурасы - 49-51 ° C. Суда аз ериді, сусыз спиртте, эфирде, хлороформда, трихлорэтиленде, майларда жақсы ериді. Мұнай /суды бөлу коэффициенті 330. Жанбайды және тұтанбайды ( оттегі және азот оксиді араласқан түтіндер жарылыстан қорғалған ). Орталық жүйке жүйесін басады және наркозды тудырады. Симпатикалық ганглийлерді блоктайды, кезбе нервтердің тонусын арттырады, миокардтың жиырылу қабілетін төмендетеді, миокардты катехоламиндерге сенсибилизациялайды. Жүйелі қан қысымын төмендетеді ; бронхтарды кеңейтеді ; сілекейдің бөлінуін тежейді ; жөтел және кекіру рефлекстерін тежейді. Галатон