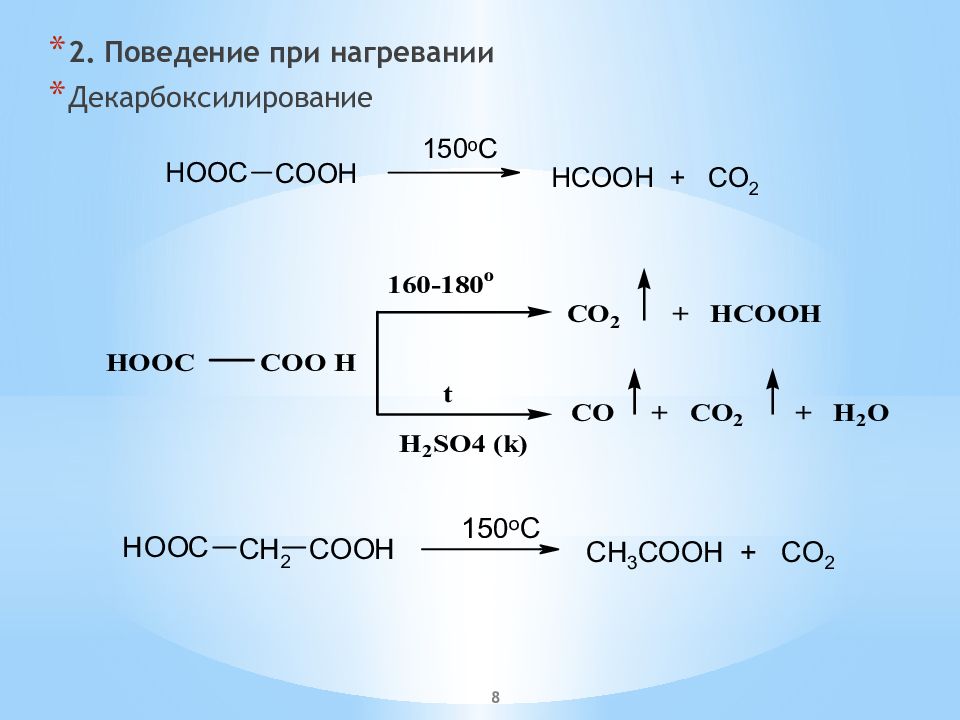
Первый слайд презентации
Дикарбоновые кислоты Ароматические кислоты Гидроксикислоты 1
Слайд 2
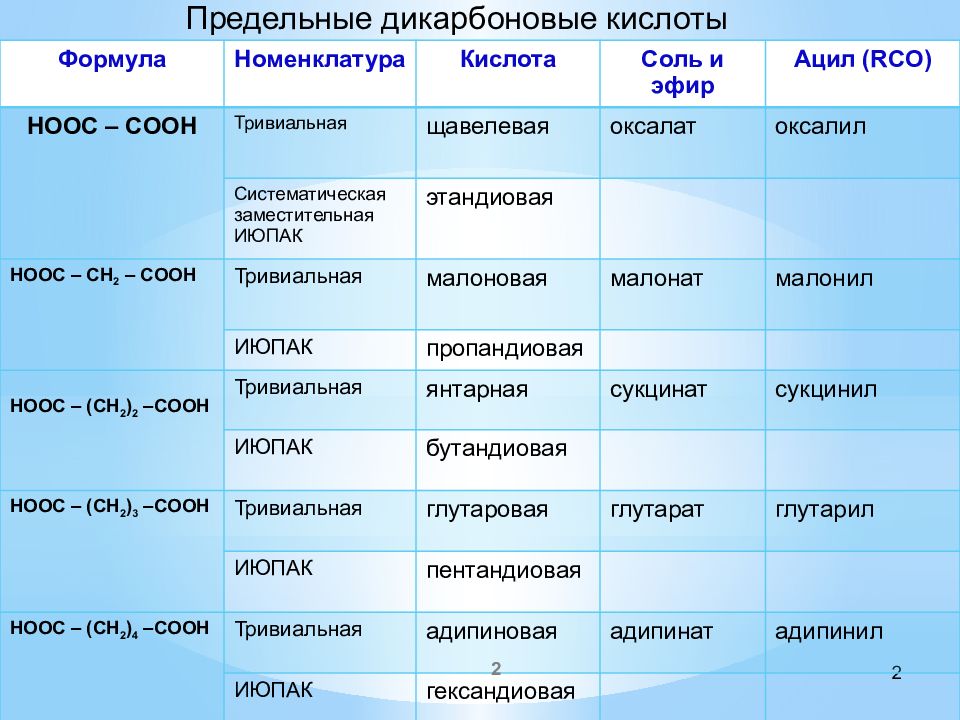
2 Формула Номенклатура Кислота Соль и эфир Ацил ( RCO) HOOC – COOH Тривиальная щавелевая оксалат оксалил Систематическая заместительная ИЮПАК этандиовая HOOC – CH 2 – COOH Тривиальная малоновая малонат малонил ИЮПАК пропандиовая HOOC – (CH 2 ) 2 –COOH Тривиальная янтарная сукцинат сукцинил ИЮПАК бутандиовая HOOC – (CH 2 ) 3 –COOH Тривиальная глутаровая глутарат глутарил ИЮПАК пентандиовая HOOC – (CH 2 ) 4 –COOH Тривиальная адипиновая адипинат адипинил ИЮПАК гександиовая 2 Предельные дикарбоновые кислоты
Слайд 3
Карбоксильная группа проявляет сильные электроноакцепторные свойства, и поэтому дикарбоновые кислоты являются более сильными кислотами, чем соответствующие монокарбоновые. Свойства дикарбоновых кислот похожи на свойства монокарбоновых кислот, за некоторыми исключениями, которые особенно проявляются для первых членов гомологического ряда. 3
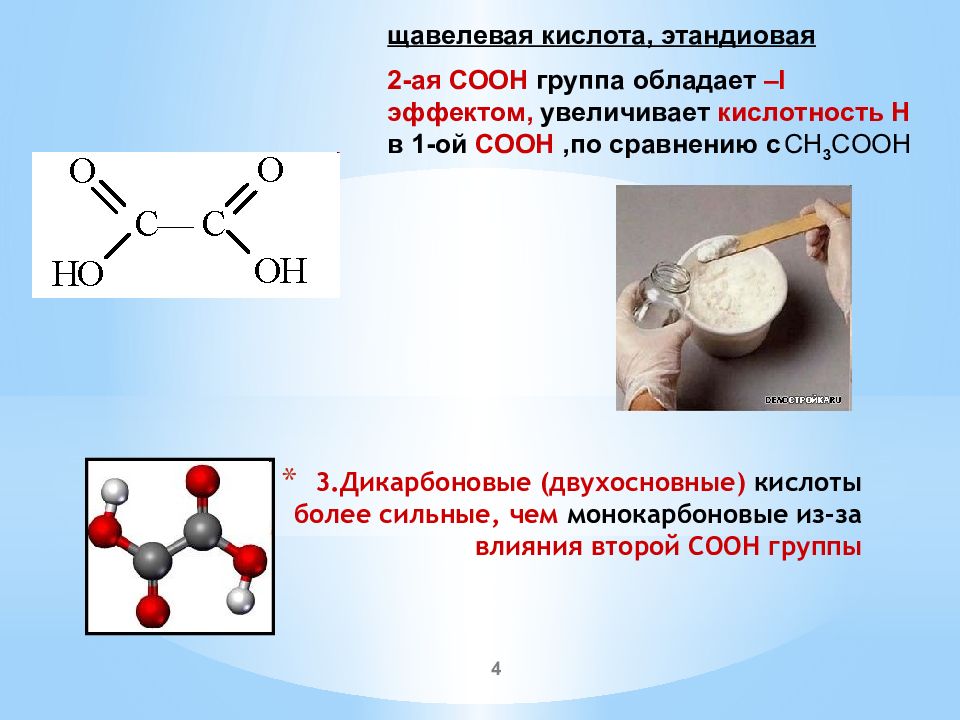
щавелевая кислота, этандиовая 2-ая СООН группа обладает – I эффектом, увеличивает кислотность Н в 1-ой СООН,по сравнению с CH 3 COOH 4
Слайд 5: Щавелевая кислота
Щавелевая кислота накапливается, когда листья стареют, в молодых листьях ее не- много Оксалатные камни в почках Щавелевая кислота и ее соли токсичны 5
Слайд 6
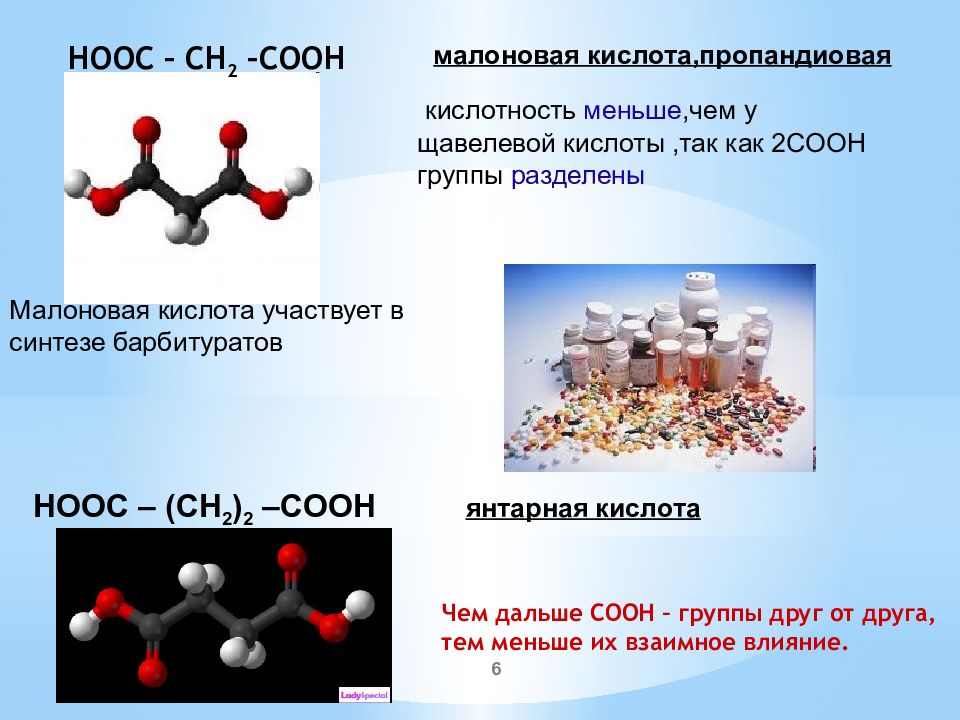
малоновая кислота,пропандиовая кислотность меньше,чем у щавелевой кислоты,так как 2СООН группы разделены Малоновая кислота участвует в синтезе барбитуратов HOOC – (CH 2 ) 2 –COOH янтарная кислота 6 Чем дальше СООН – группы друг от друга, тем меньше их взаимное влияние. HOOC – CH 2 –COOH
Слайд 7
Янтарная кислота оказывает мощное оздоровительное действие на организм Используется против старения кожи Получается в результате переработки натурального янтаря Содержится в небольших количествах- в сыре, кисломолочных продуктах и морепродуктах 7
Слайд 9
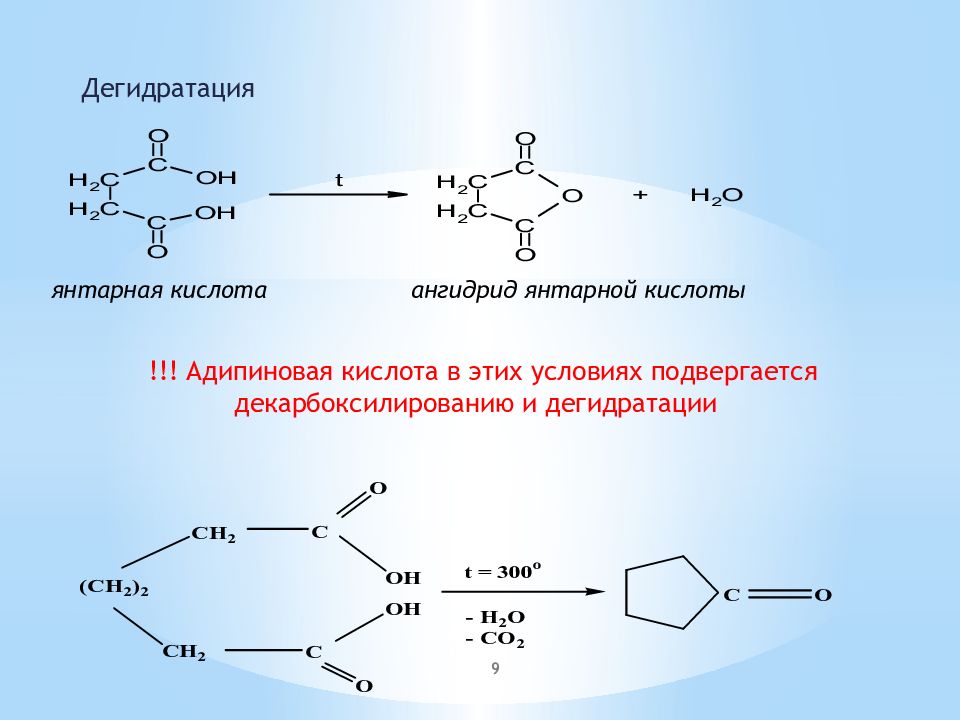
Дегидратация 9 янтарная кислота ангидрид янтарной кислоты !!! Адипиновая кислота в этих условиях подвергается декарбоксилированию и дегидратации
Слайд 11
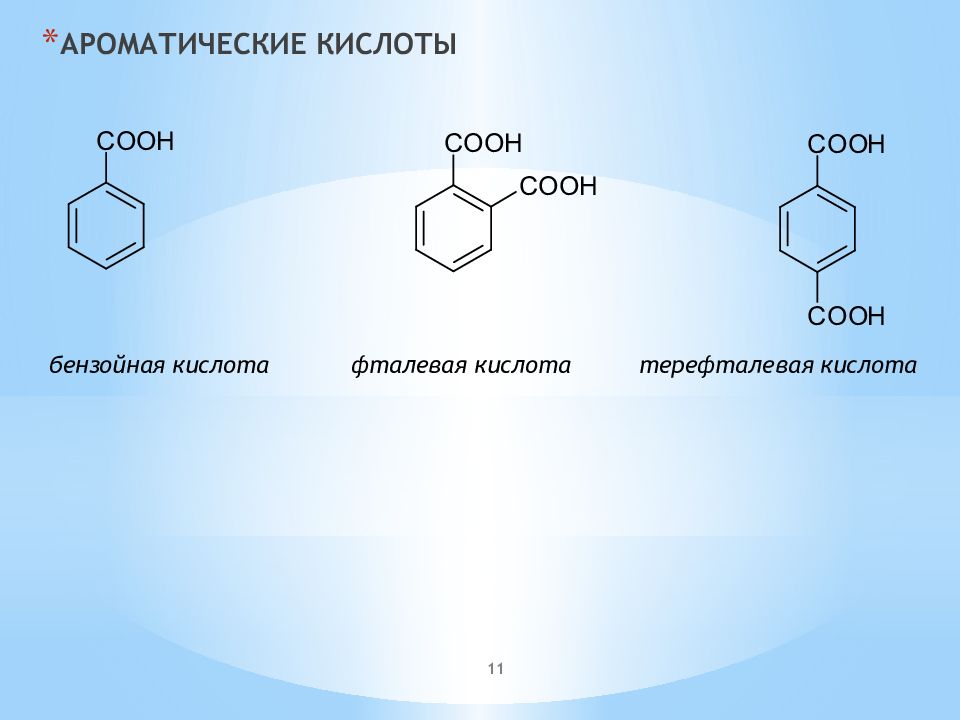
АРОМАТИЧЕСКИЕ КИСЛОТЫ бензойная кислота фталевая кислота терефталевая кислота 11
Слайд 12
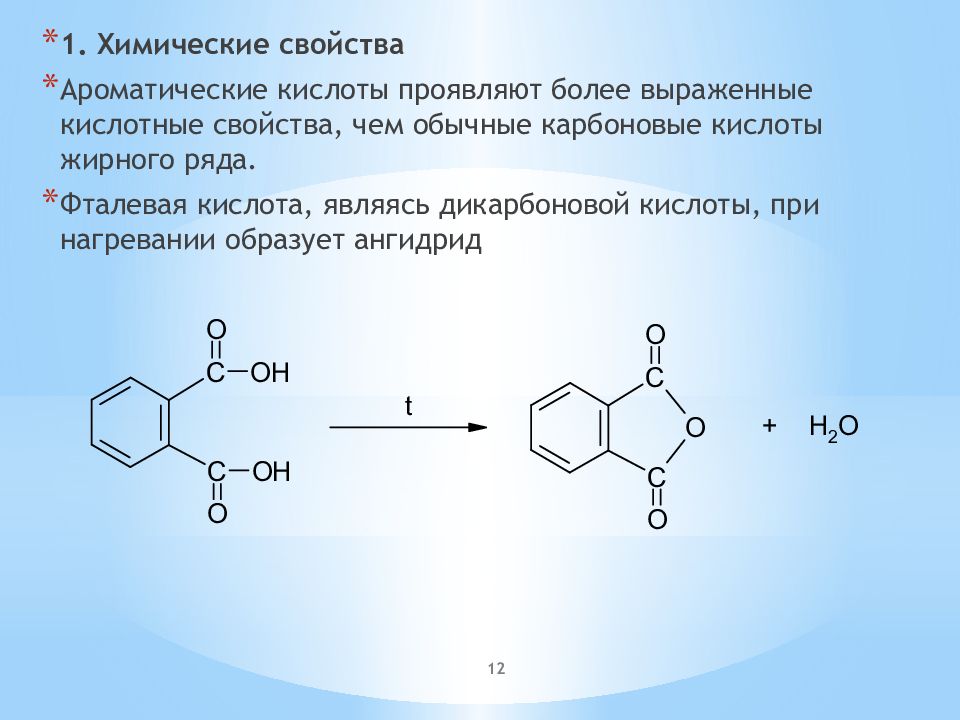
1. Химические свойства Ароматические кислоты проявляют более выраженные кислотные свойства, чем обычные карбоновые кислоты жирного ряда. Фталевая кислота, являясь дикарбоновой кислоты, при нагревании образует ангидрид 12
Слайд 13
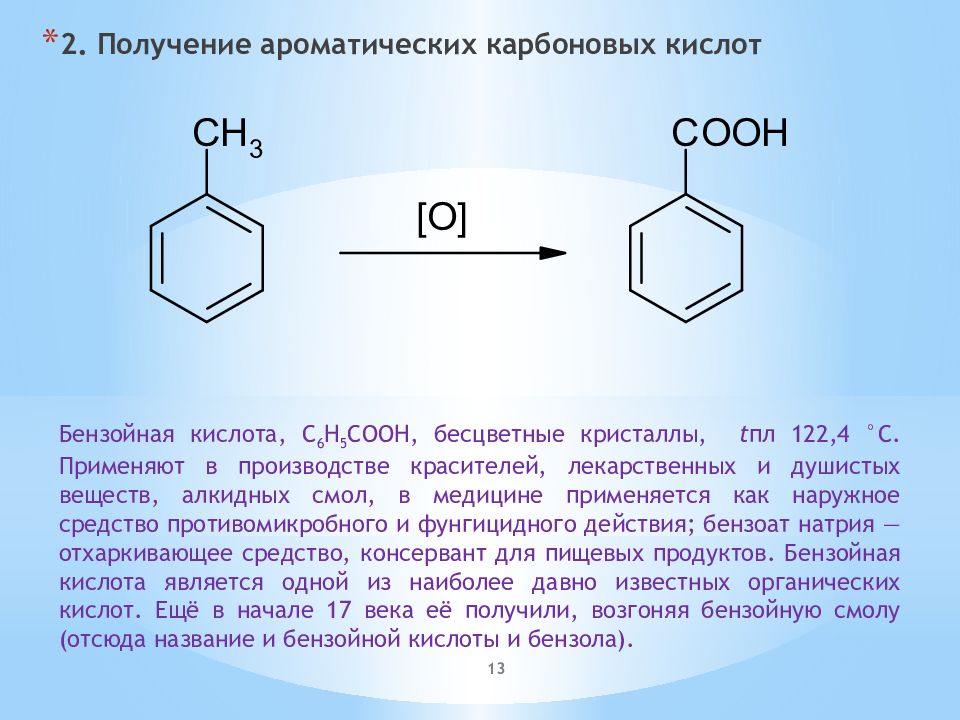
2. Получение ароматических карбоновых кислот Бензойная кислота, C 6 H 5 COOH, бесцветные кристаллы, t пл 122,4 °C. Применяют в производстве красителей, лекарственных и душистых веществ, алкидных смол, в медицине применяется как наружное средство противомикробного и фунгицидного действия; бензоат натрия — отхаркивающее средство, консервант для пищевых продуктов. Бензойная кислота является одной из наиболее давно известных органических кислот. Ещё в начале 17 века её получили, возгоняя бензойную смолу (отсюда название и бензойной кислоты и бензола). 13
Слайд 14
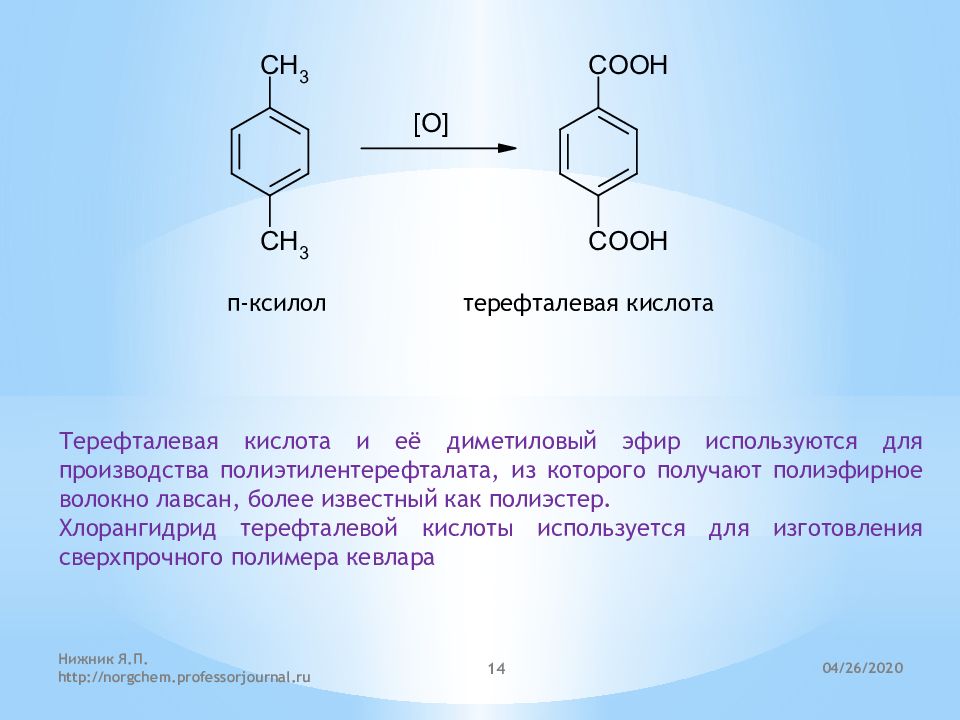
п -ксилол терефталевая кислота Терефталевая кислота и её диметиловый эфир используются для производства полиэтилентерефталата, из которого получают полиэфирное волокно лавсан, более известный как полиэстер. Хлорангидрид терефталевой кислоты используется для изготовления сверхпрочного полимера кевлара 21.04.2020 Нижник Я.П. http://norgchem.professorjournal.ru 14
Слайд 15
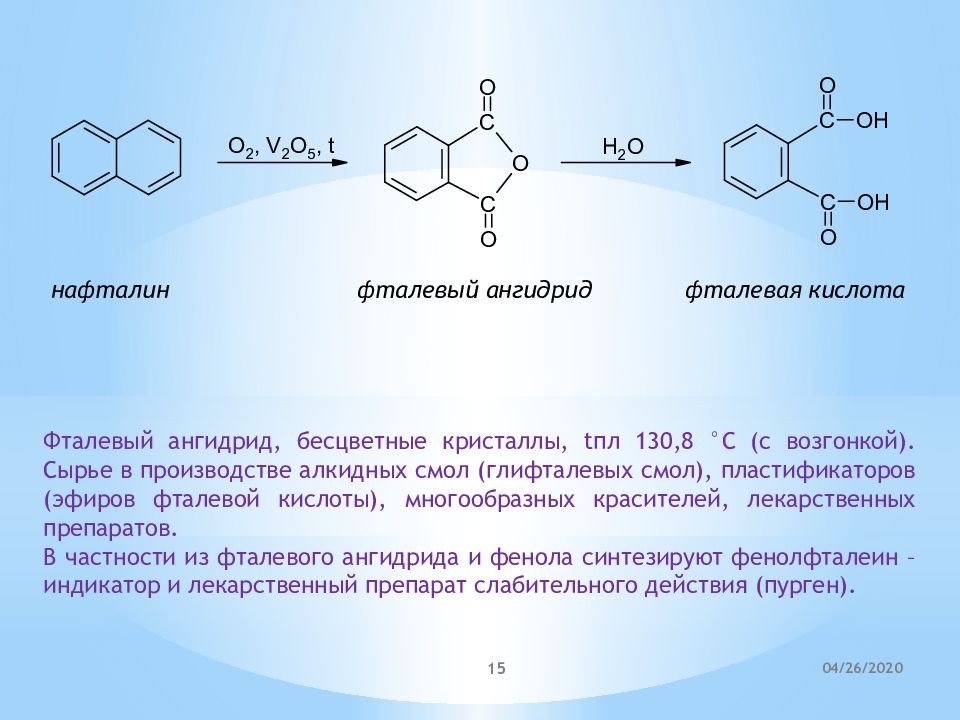
нафталин фталевый ангидрид фталевая кислота Фталевый ангидрид, бесцветные кристаллы, tпл 130,8 °С (с возгонкой). Сырье в производстве алкидных смол (глифталевых смол), пластификаторов (эфиров фталевой кислоты), многообразных красителей, лекарственных препаратов. В частности из фталевого ангидрида и фенола синтезируют фенолфталеин – индикатор и лекарственный препарат слабительного действия (пурген). 21.04.2020 15
Слайд 16
ГИДРОКСИКИСЛОТЫ (ОКСИКИСЛОТЫ) Гидроксикислоты содержат в молекуле две функциональные группы – карбоксильную (COOH) и гидроксильную ( OH ) Номенклатура Карбоксильная группа ( COOH ) по номенклатурным правилам является более старшей, чем гидроксигруппа ( OH ), поэтому карбоксильная группа определяет в названии кислоты окончание (- овая ), а гидроксигруппа – приставку 2-гидроксипропановая кислота 16
Слайд 17
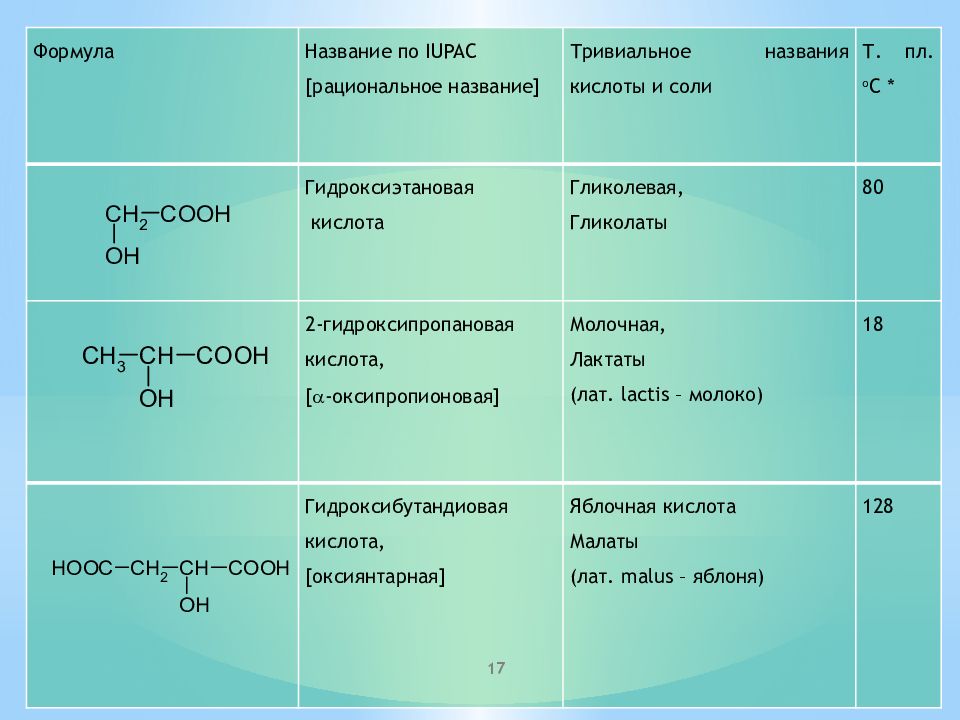
Формула Название по IUPAC [рациональное название] Тривиальное названия кислоты и соли Т. пл. o C * Гидроксиэтановая кислота Гликолевая, Гликолаты 80 2-гидроксипропановая кислота, [ a - оксипропионовая ] Молочная, Лактаты (лат. lactis – молоко) 18 Гидроксибутандиовая кислота, [ оксиянтарная ] Яблочная кислота Малаты (лат. malus – яблоня) 128 17
Слайд 18
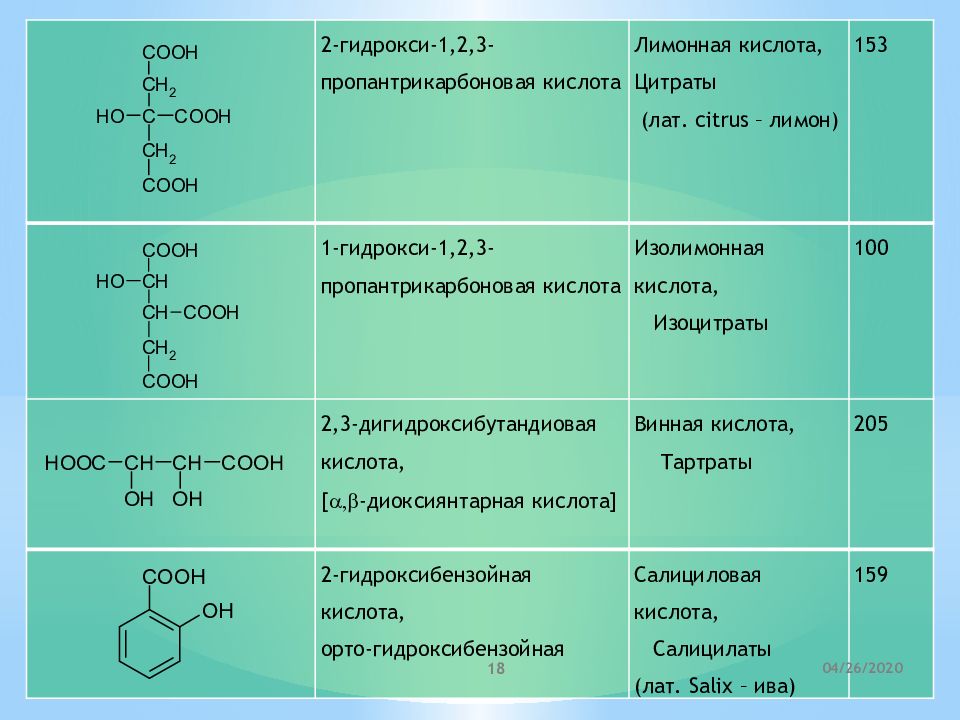
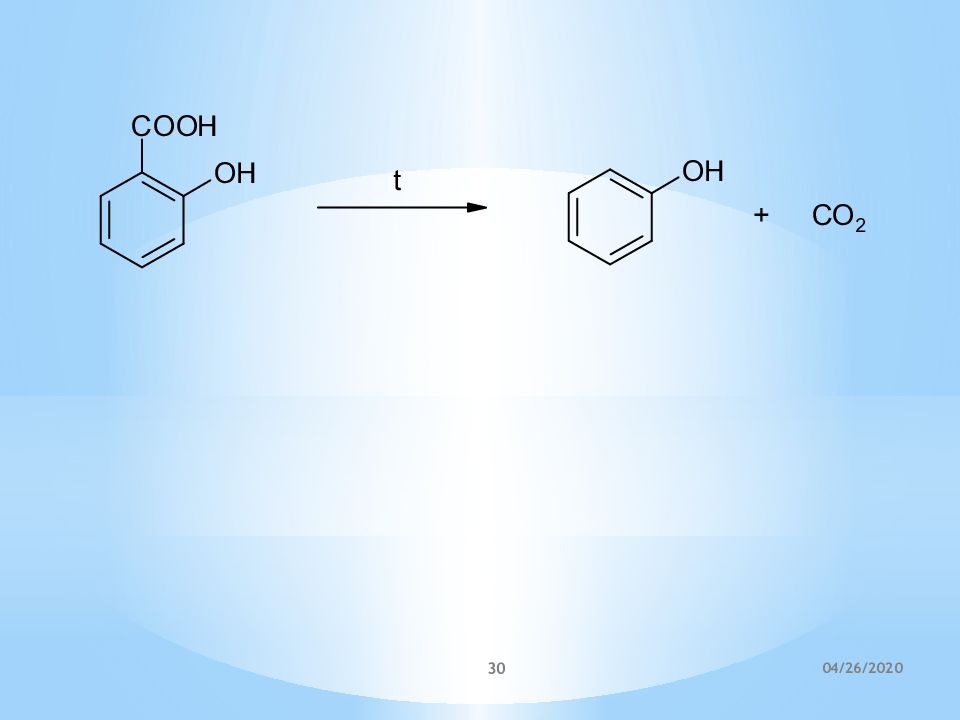
2-гидрокси-1,2,3-пропантрикарбоновая кислота Лимонная кислота, Цитраты (лат. citrus – лимон) 153 1-гидрокси-1,2,3-пропантрикарбоновая кислота Изолимонная кислота, Изоцитраты 100 2,3-дигидроксибутандиовая кислота, [ a,b - диоксиянтарная кислота ] Винная кислота, Тартраты 205 2-гидроксибензойная кислота, орто-гидроксибензойная Салициловая кислота, Салицилаты (лат. Salix – ива) 159 21.04.2020 18
Слайд 19
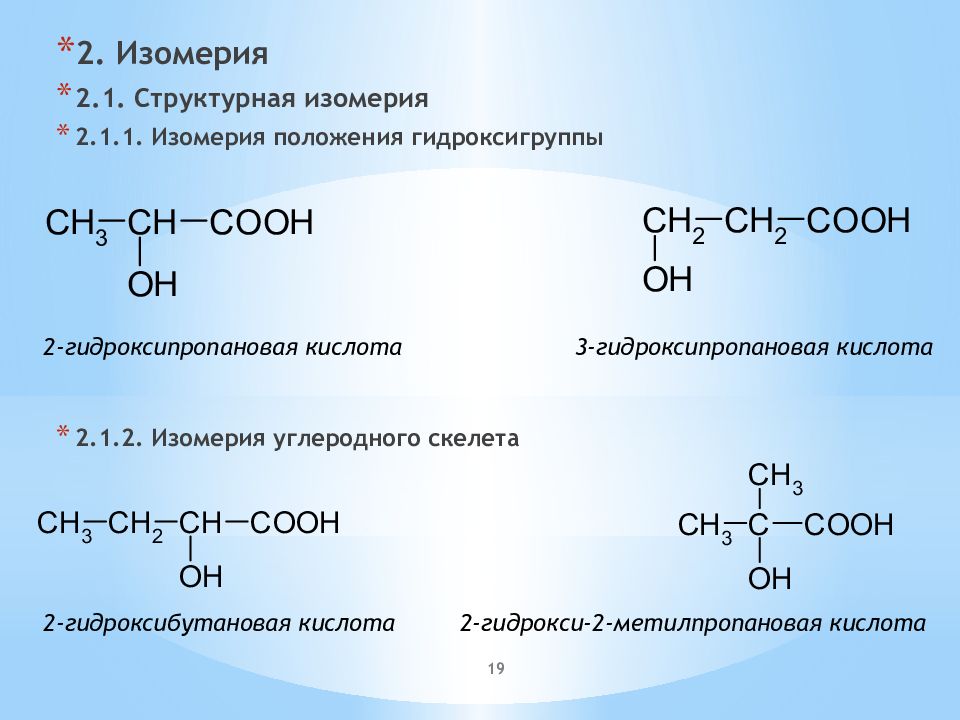
2. Изомерия 2.1. Структурная изомерия 2.1.1. Изомерия положения гидроксигруппы 2.1.2. Изомерия углеродного скелета 2-гидроксипропановая кислота 3-гидроксипропановая кислота 2-гидроксибутановая кислота 2-гидрокси-2-метилпропановая кислота 19
Слайд 20
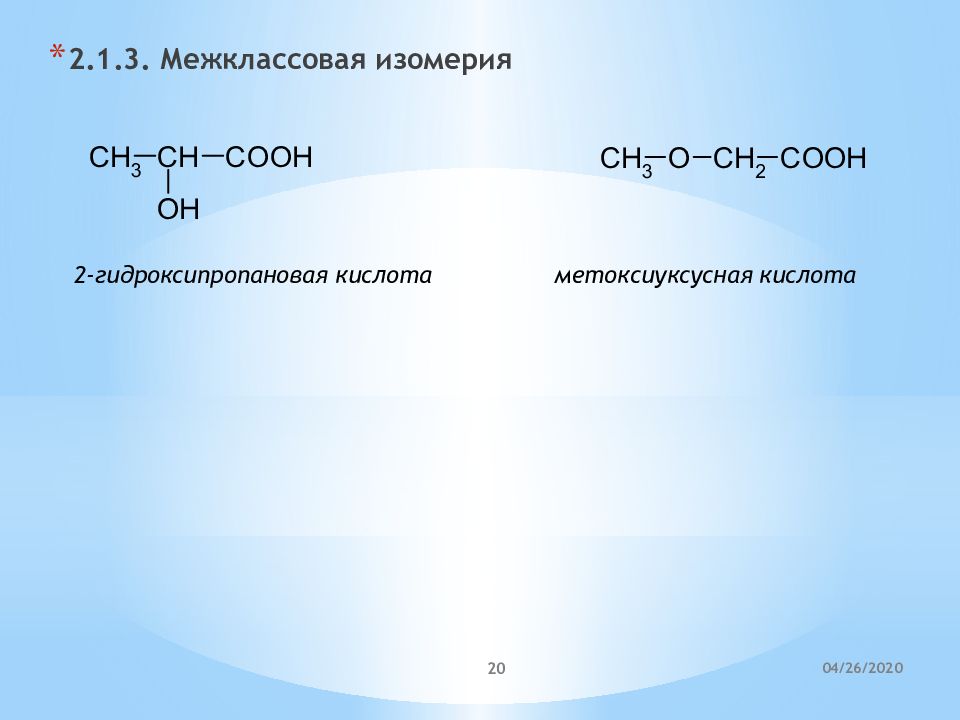
2.1.3. Межклассовая изомерия 2-гидроксипропановая кислота метоксиуксусная кислота 21.04.2020 20
Слайд 21
2.2. Пространственная изомерия Пространственная изомерия делится на оптическую изомерию ( энантиомерию ) и диастереомерию. Энантиомерия возможна в том случае, если через молекулу невозможно провести плоскость симметрии – плоскость, делящую молекулу на две абсолютно равные половины. 21.04.2020 21
Слайд 22
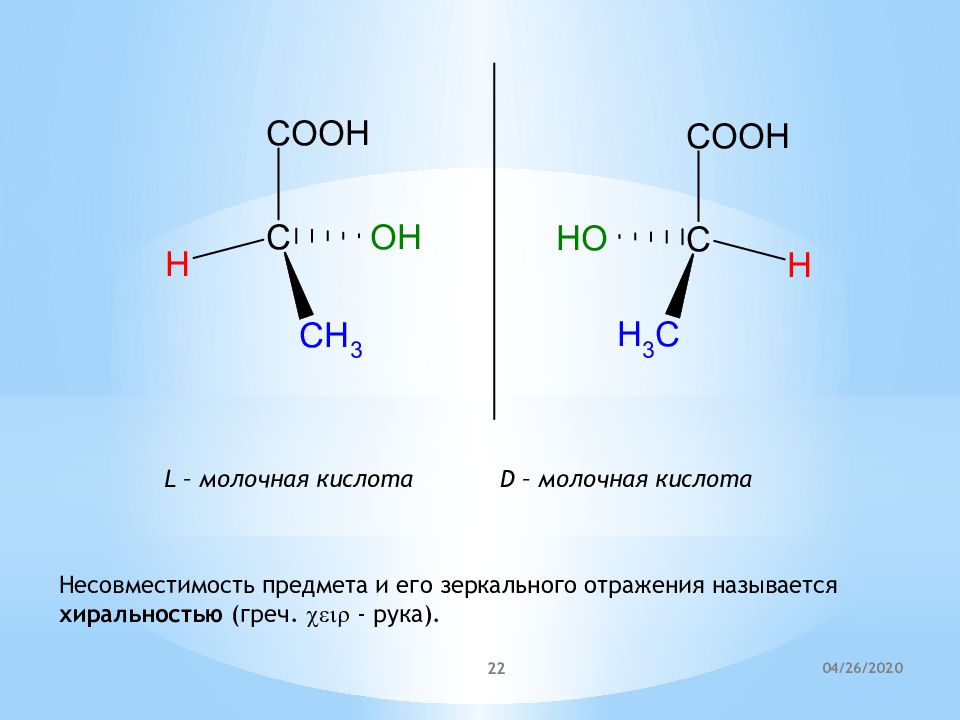
L – молочная кислота D – молочная кислота Н есовместимость предмета и его зеркального отражения называется хиральностью (греч. ceir - рука). 21.04.2020 22
Слайд 23
2. Физические и биологические свойства Гидроксикислоты являются, как правило, твёрдыми телами. Рацемическая молочная кислота может быть жидкой (т. пл. 18 о С). Запахом гидроксикислоты почти не обладают. Гидроксикислоты имеют очень большое значение в биологической химии; их можно встретить во многих очень важных метаболических путях – цикле Кребса, гликолизе, пентозофосфатном цикле, b -окислении жирных кислот, биосинтезе жирных кислот и т.д. 21.04.2020 23
Слайд 24
3. Химические свойства Гидроксикислоты являются одновременно и кислотами и спиртами, поэтому могут проявлять свойства и карбоновых кислот и спиртов. 3.1. Кислотные свойства молочная кислота лактат кальция Лактат кальция используется как модификатор в кондитерской промышленности, в медицине как кальциевый препарат, растворы используются для опрыскивания фруктов с целью их сохранения 21.04.2020 24
Слайд 25
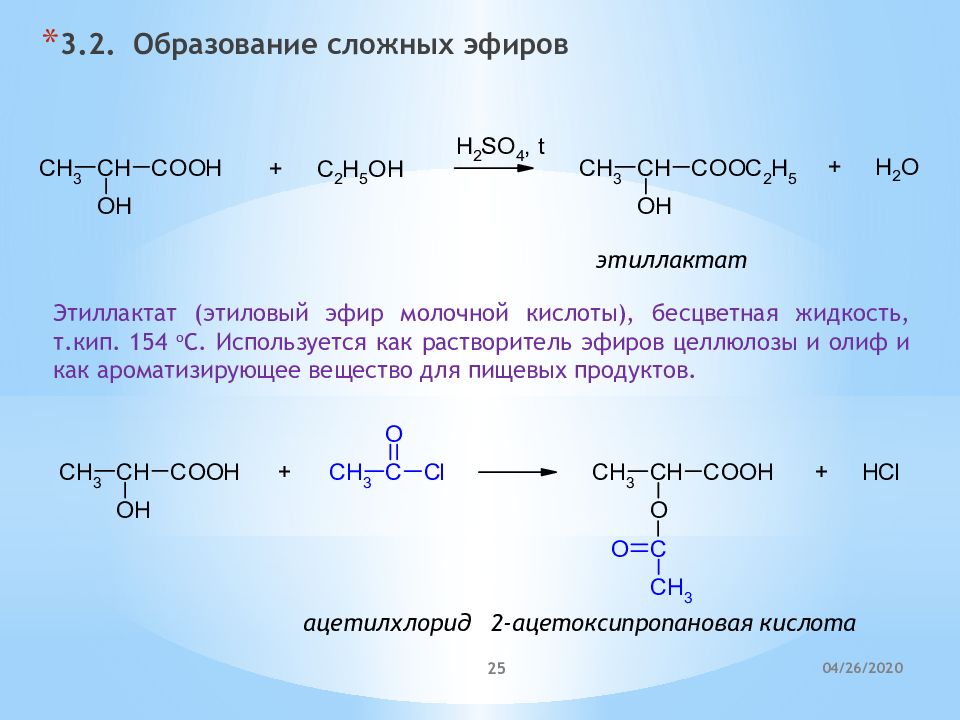
3.2. Образование сложных эфиров этиллактат Этиллактат (этиловый эфир молочной кислоты), бесцветная жидкость, т.кип. 154 o C. Используется как растворитель эфиров целлюлозы и олиф и как ароматизирующее вещество для пищевых продуктов. ацетилхлорид 2-ацетоксипропановая кислота 21.04.2020 25
Слайд 26
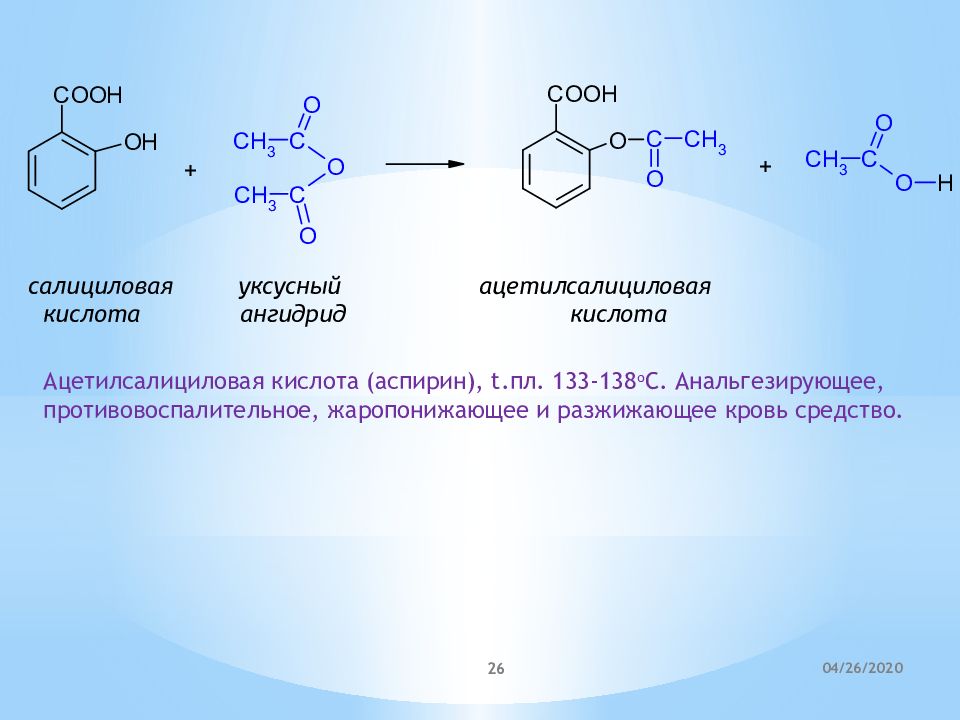
салициловая уксусный ацетилсалициловая кислота ангидрид кислота Ацетилсалициловая кислота (аспирин), t.пл. 133-138 о С. Анальгезирующее, противовоспалительное, жаропонижающее и разжижающее кровь средство. 21.04.2020 26
Слайд 27
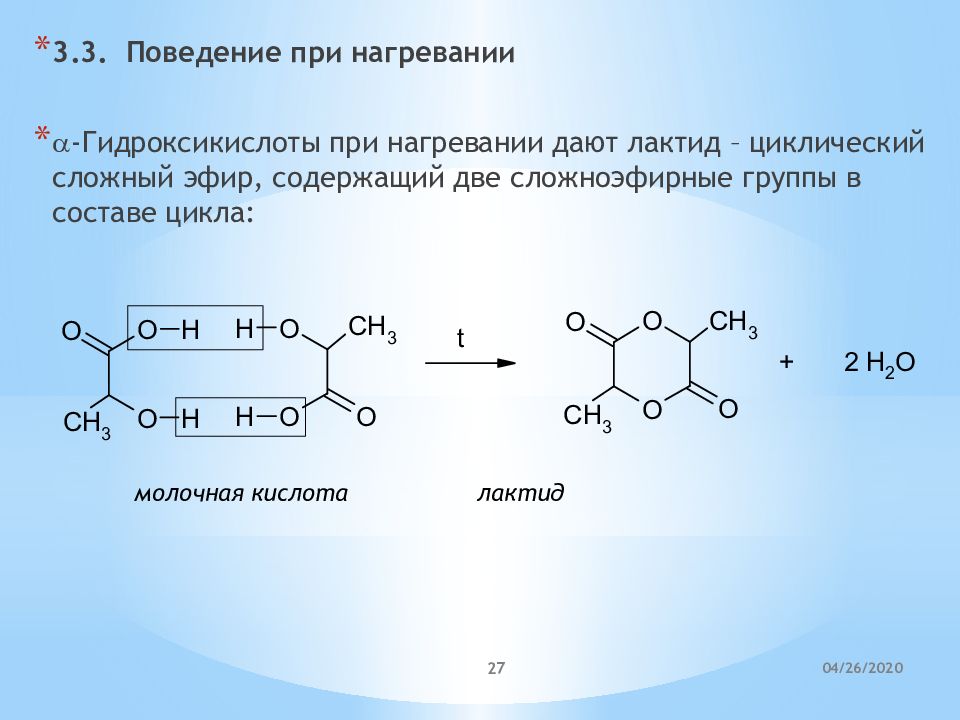
3.3. Поведение при нагревании a - Гидроксикислоты при нагревании дают лактид – циклический сложный эфир, содержащий две сложноэфирные группы в составе цикла: молочная кислота лактид 21.04.2020 27
Слайд 28
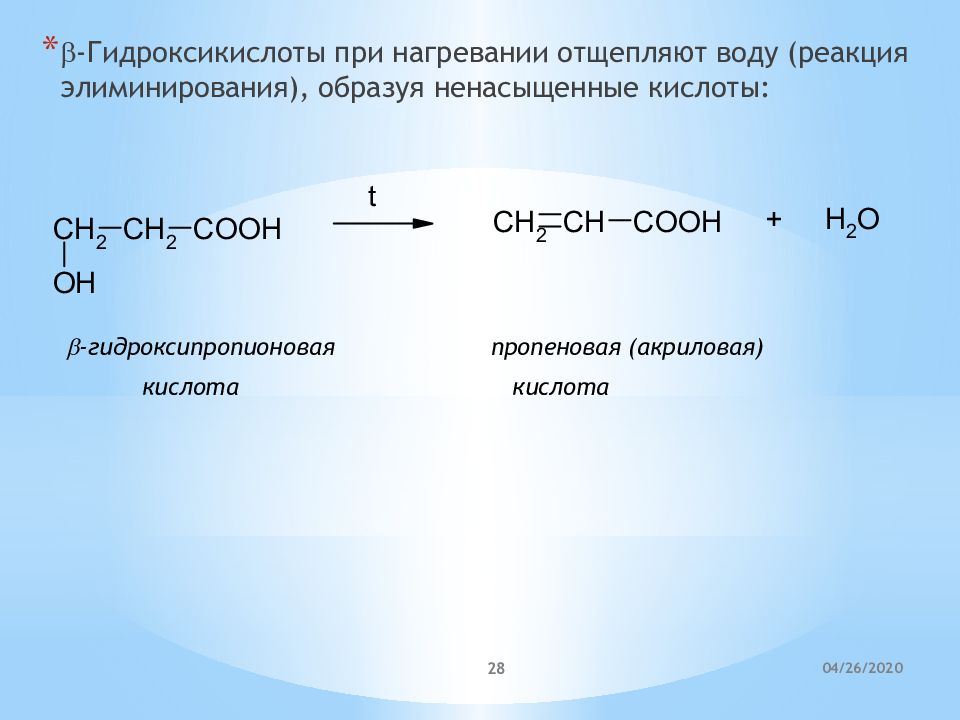
b - Гидроксикислоты при нагревании отщепляют воду (реакция элиминирования), образуя ненасыщенные кислоты: b - гидроксипропионовая пропеновая (акриловая) кислота кислота 21.04.2020 28
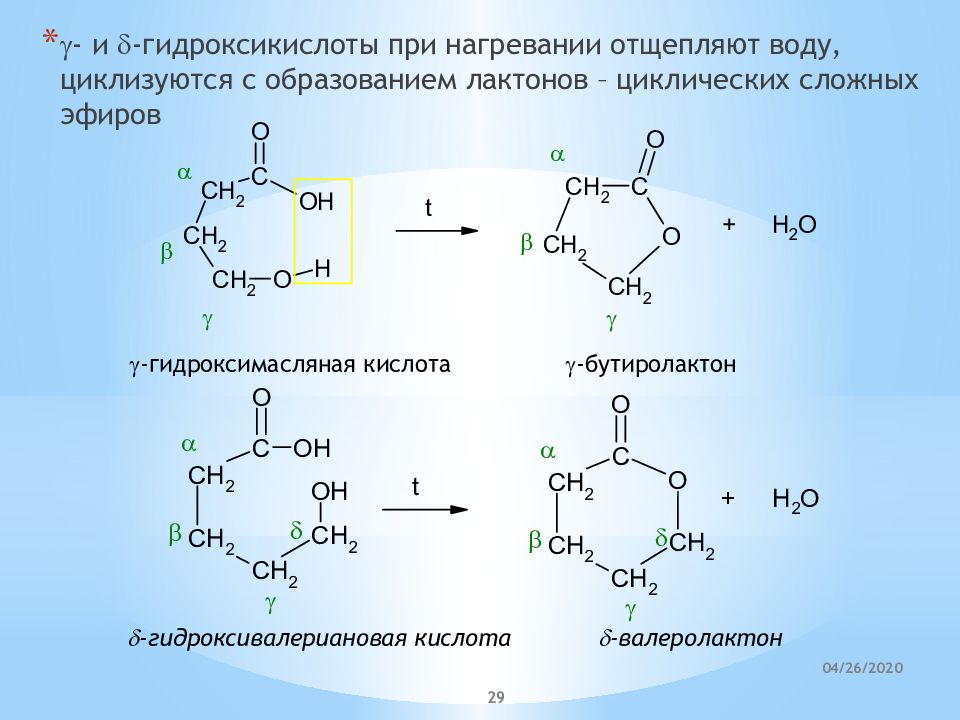
Слайд 29
g - и d - гидроксикислоты при нагревании отщепляют воду, циклизуются с образованием лактонов – циклических сложных эфиров g - гидроксимасляная кислота g - бутиролактон d - гидроксивалериановая кислота d - валеролактон 21.04.2020 29