Первый слайд презентации: Кафедра «Технология транспортного машиностроения и ремонта подвижного состава
Рауба Александр Александрович МАТЕРИАЛОВЕДЕНИЕ Краткий обзор курса
Слайд 6
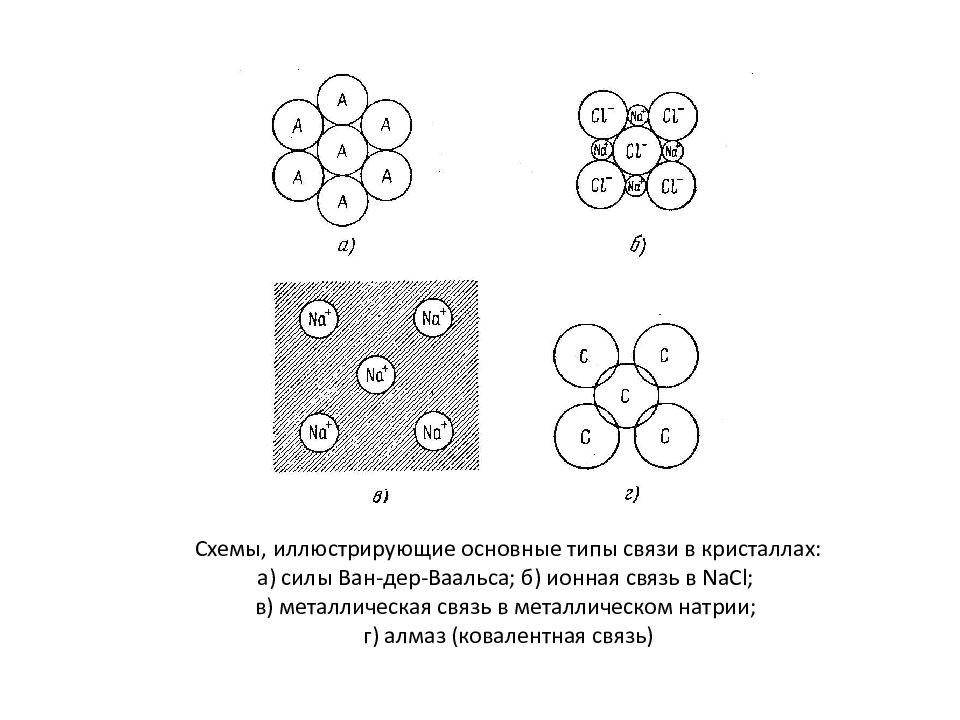
Схемы, иллюстрирующие основные типы связи в кристаллах: а) силы Ван-дер-Ваальса; б) ионная связь в NaCl ; в) металлическая связь в металлическом натрии; г) алмаз (ковалентная связь)
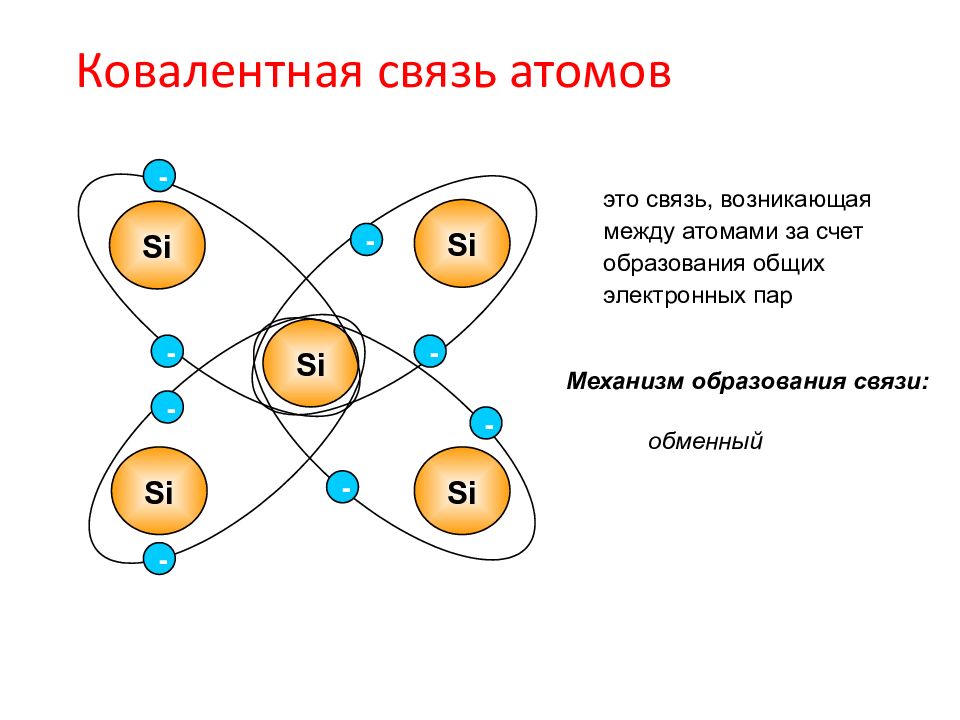
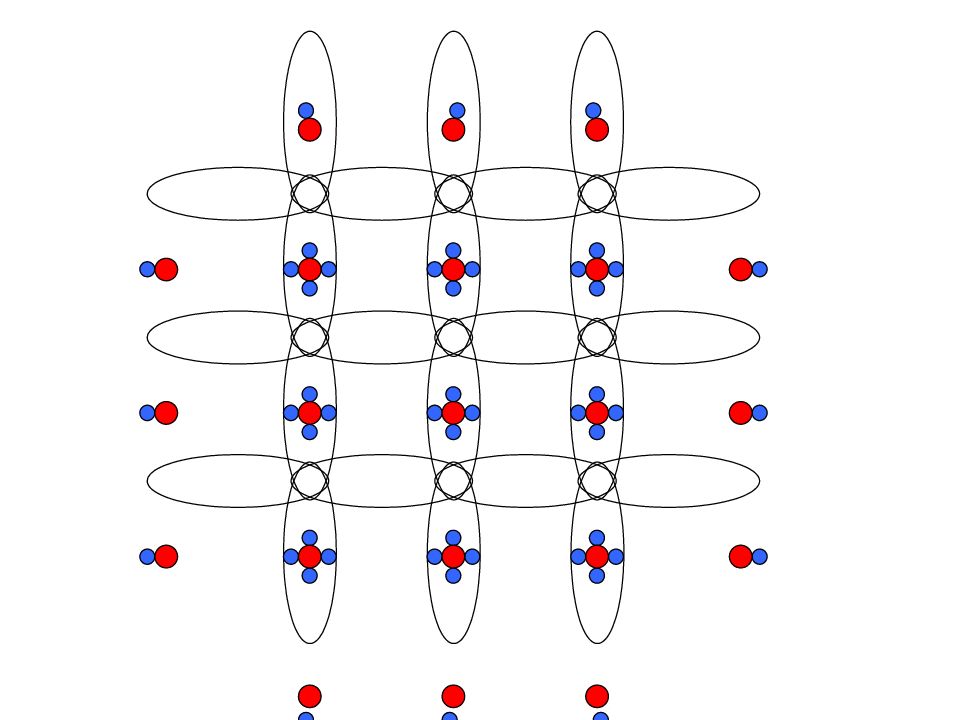
Слайд 7: Кова Ковалентная связь атомов ная связь атомов
Si Si Si Si Si - - - - - - - - это связь, возникающая между атомами за счет образования общих электронных пар Механизм образования связи: обменный
Слайд 9: Классификация веществ
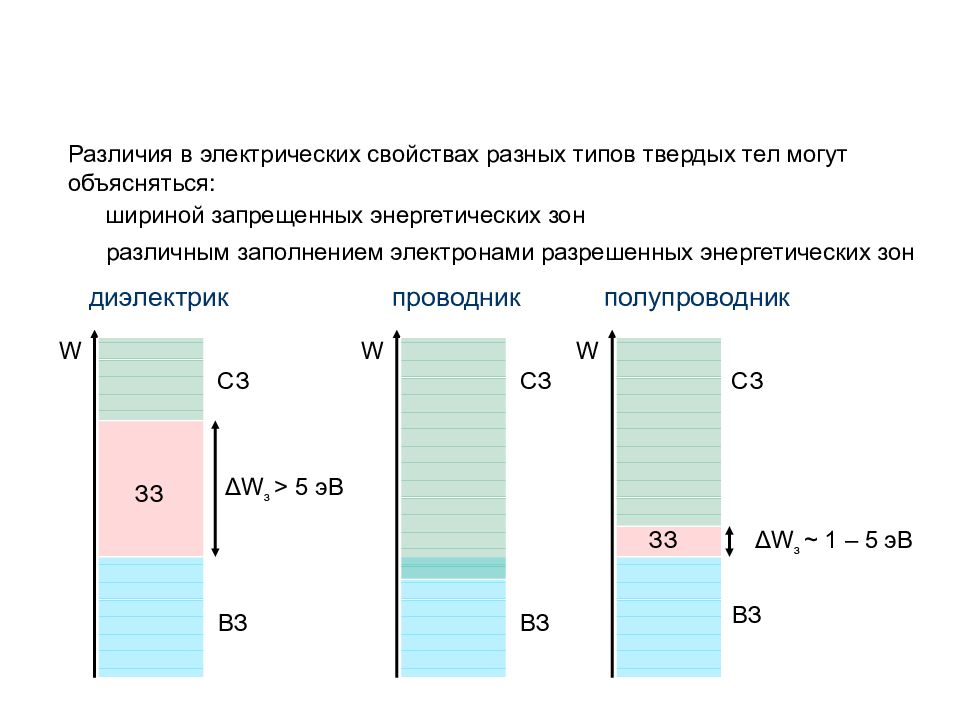
Различия в электрических свойствах разных типов твердых тел могут объясняться : шириной запрещенных энергетических зон различным заполнением электронами разрешенных энергетических зон W W W СЗ СЗ СЗ ВЗ ВЗ ВЗ ЗЗ ЗЗ диэлектрик проводник полупроводник Δ W з ~ 1 – 5 эВ Δ W з > 5 эВ
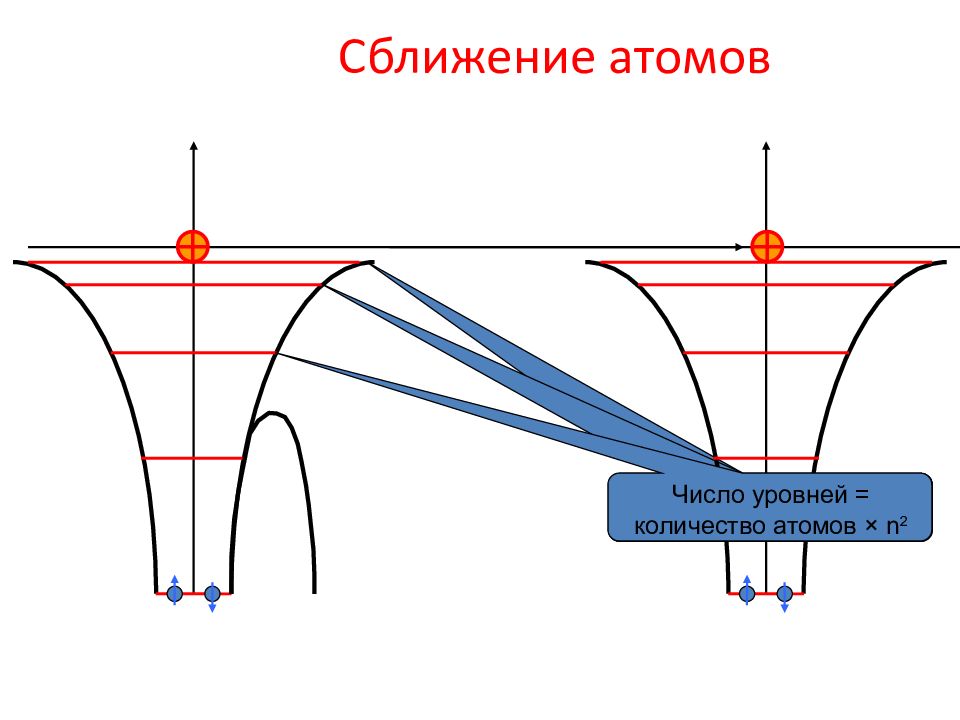
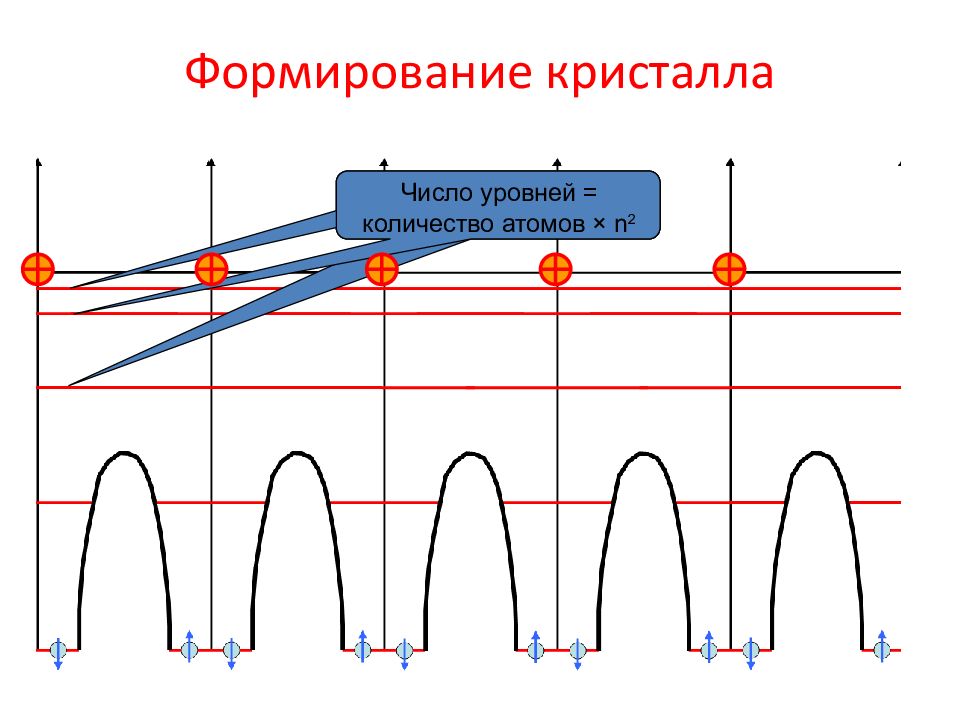
Слайд 10: Сближен Сближение атомов ие атомов
Число уровней = количество атомов × n 2
Слайд 13: Металл вне электрического поля
Обобществленные электроны образуют подобие газа, частицы которого находятся в непрерывном хаотическом движении
Слайд 16
3 ПОЛИМОРФИЗМ (АЛЛОТРОПИЯ) – способность металла в зависимости от температуры и давления изменять свое кристаллическое строение (тип кристаллической решетки –модификации: α, β, γ, δ и т.п.) ПЕРИОД кристаллической решетки - расстояние между параллельными атомными плоскостями (для металлов значение его – в пределах 0,20 – 0,70 нм
Слайд 17
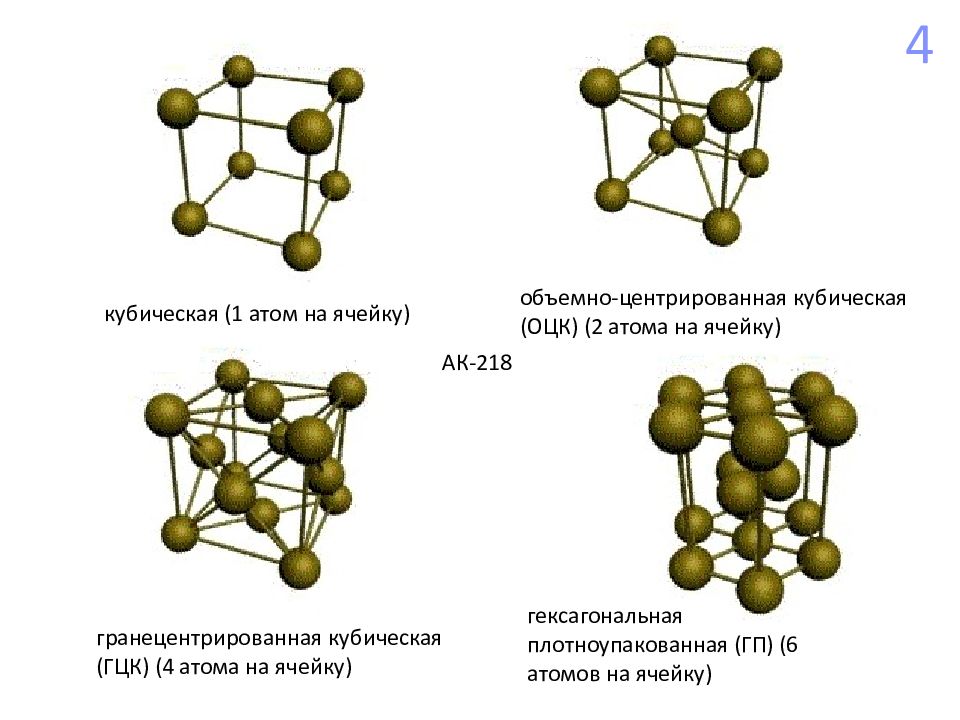
кубическая (1 атом на ячейку) объемно-центрированная кубическая (ОЦК) (2 атома на ячейку) гранецентрированная кубическая (ГЦК) (4 атома на ячейку) гексагональная плотноупакованная (ГП) (6 атомов на ячейку) АК-218 4
Слайд 18
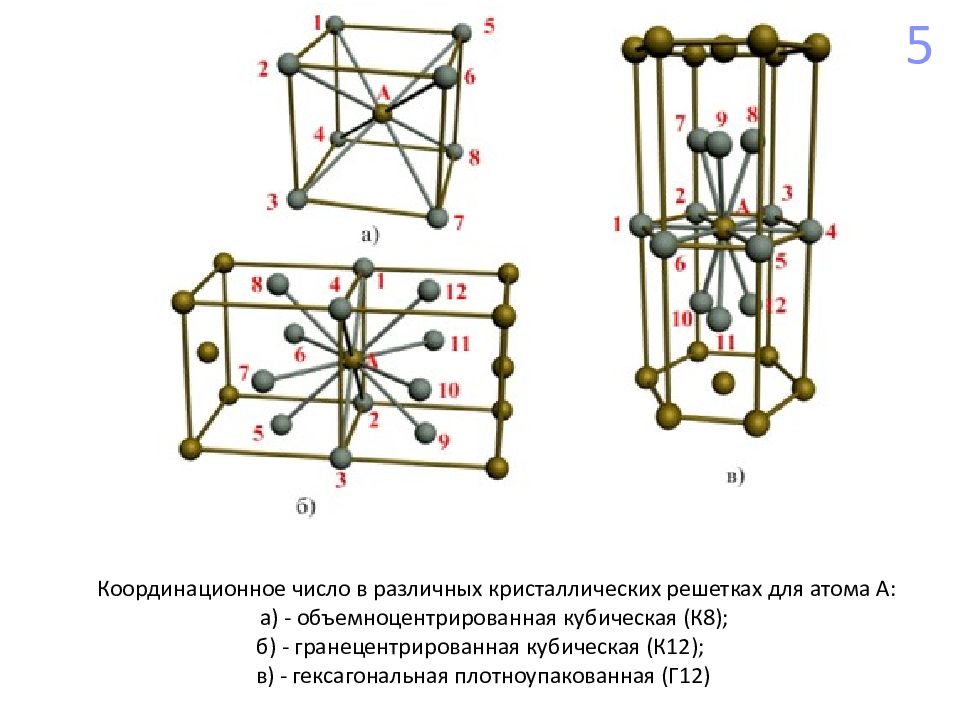
Координационное число в различных кристаллических решетках для атома А: а) - объемноцентрированная кубическая (К8); б) - гранецентрированная кубическая (К12); в) - гексагональная плотноупакованная (Г12) 5
Слайд 20
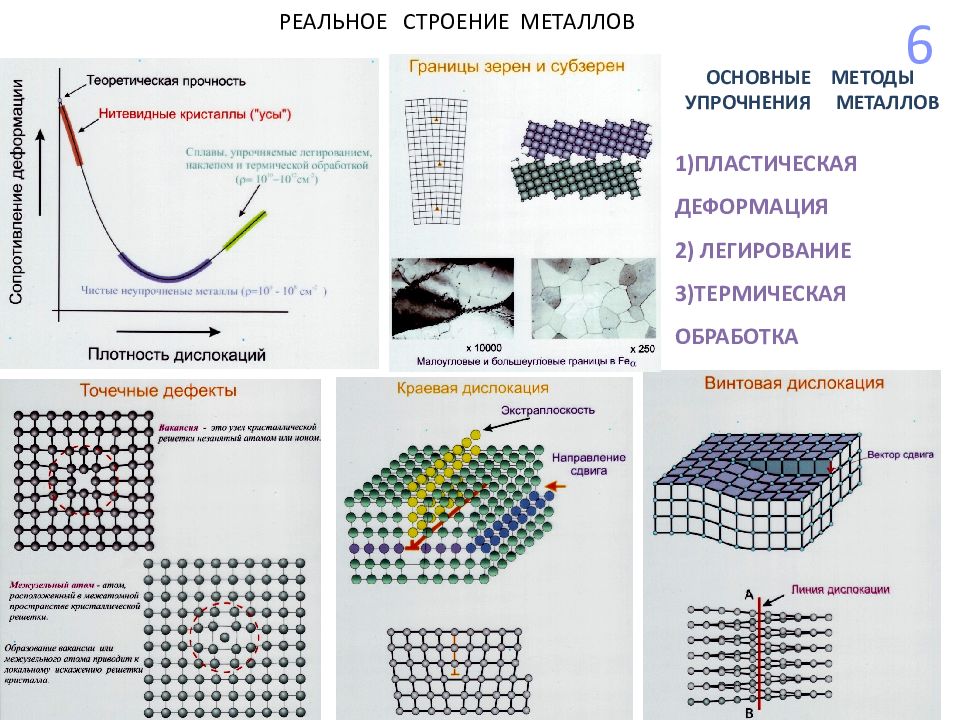
6 РЕАЛЬНОЕ СТРОЕНИЕ МЕТАЛЛОВ ОСНОВНЫЕ МЕТОДЫ УПРОЧНЕНИЯ МЕТАЛЛОВ 1)ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИЯ 2) ЛЕГИРОВАНИЕ 3)ТЕРМИЧЕСКАЯ ОБРАБОТКА
Слайд 21
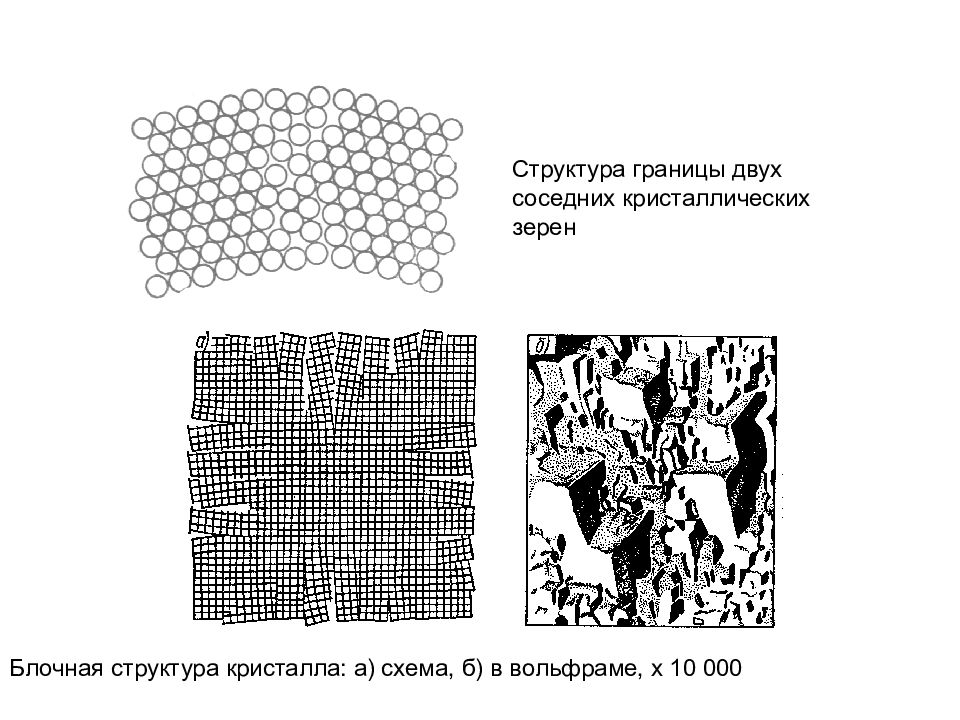
Блочная структура кристалла: а) схема, б) в вольфраме, х 10 000 Структура границы двух соседних кристаллических зерен
Слайд 23
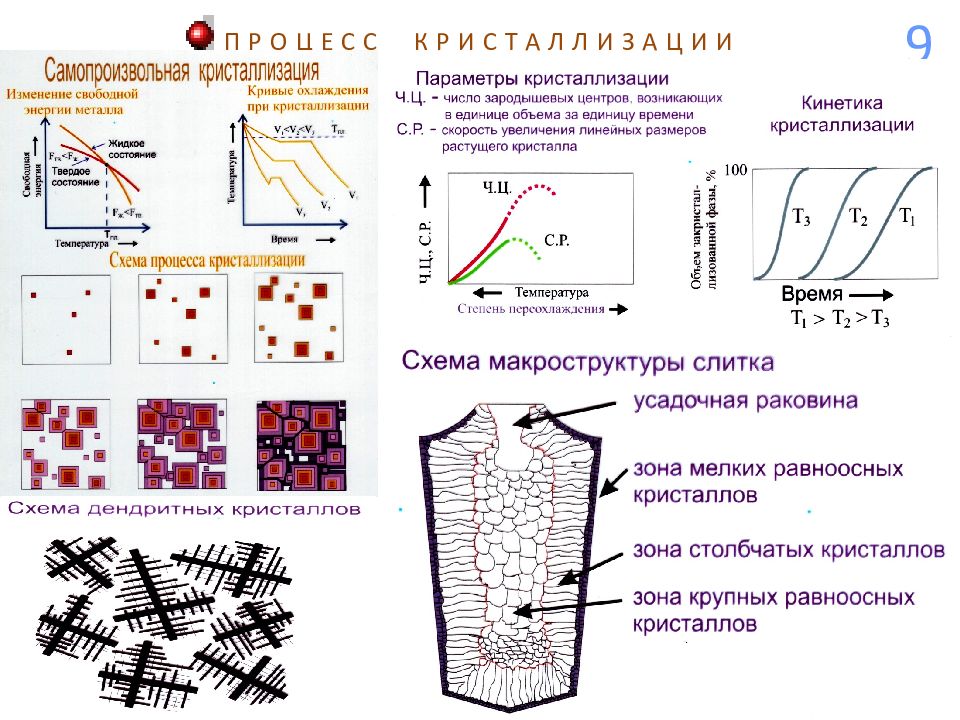
Схема строения дендрита: 1–3 – оси первого, второго и третьего порядка Схема строения дендрита: 1–3 – оси первого, второго и третьего порядка Макроструктура стального слитка
Слайд 24
10 ОСНОВНЫЕ ПОНЯТИЯ О СПЛАВАХ СПЛАВЫ – ТВЕРДЫЕ РАСТВОРЫ (ВСЕГДА ОДНОФАЗНЫ, МЯГКИЕ И ПЛАСТИЧНЫЕ ) СПЛАВЫ – СМЕСИ (МЕХАНИЧЕСКИЕ ) ВСЕГДА МНОГОФАЗНЫ ФАЗА – однородная часть системы, с поверхностью раздела, при переходе через которую структура и свойства вещества изменяется скачком. Структура (строение ) - характеристика сплава по таким параметрам как количество, размер, форма, распределение, взаимное расположение отдельных фаз и структурных составляющих. СТРУКТУРНАЯ СОСТАВЛЯЮЩАЯ – это однородная часть строения, образовавшаяся в результате первичной или вторичной кристаллизации сплава. Она может состоять из одной или нескольких фаз.
Слайд 25
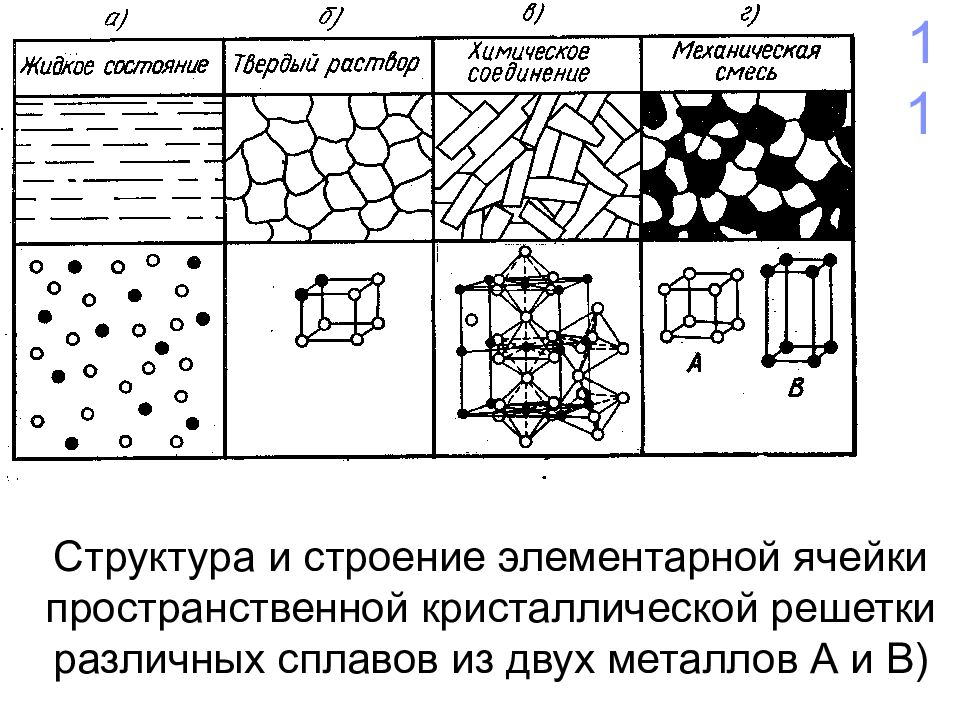
Структура и строение элементарной ячейки пространственной кристаллической решетки различных сплавов из двух металлов А и В) 11
Слайд 26
ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ТВЕРДЫМ РАСТВОРОМ называется сплав, в котором атомы растворенных компонентов находятся в кристаллической решетке компонента растворителя. МЕХАНИЧЕСКАЯ СМЕСЬ (сплав-смесь) компонентов образуется тогда, когда они не образуют твердых растворов и химических соединений и кристаллы каждого компонента будут сохранять свои состав и свойства. Сплав - смесь, получающийся из жидкого раствора в результате первичной кристаллизации, называется эвтектикой. Она образуется при строго определенных температуре ( соотвенственно эвтектической линии) и концентрации компонентов сплава (координаты эвтектической точки ), которые называются эвтектическими. Сплав-смесь, кристаллизующаяся из твердого раствора строго определенной концентрации и при строго определенной температуре (вторичная кристаллизация), называется эвтектоидом. Сплав – Химическое соединение – это фаза, состав которой выражается химической формулой А n В m
Слайд 27
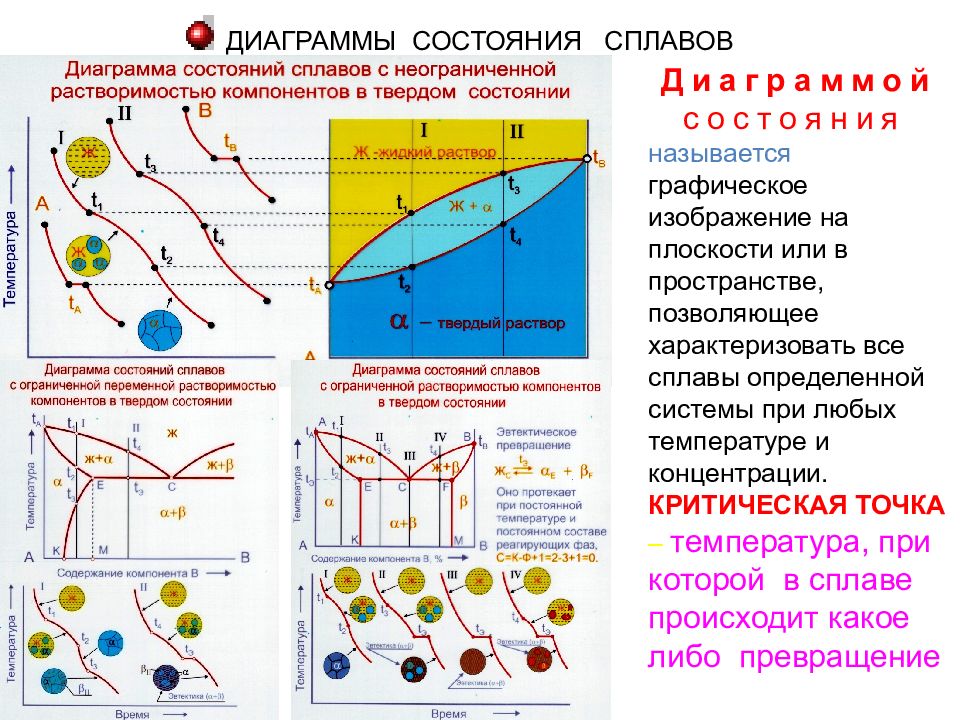
ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ Диаграммой состояния называется графическое изображение на плоскости или в пространстве, позволяющее характеризовать все сплавы определенной системы при любых температуре и концентрации. КРИТИЧЕСКАЯ ТОЧКА – температура, при которой в сплаве происходит какое либо превращение
Слайд 28
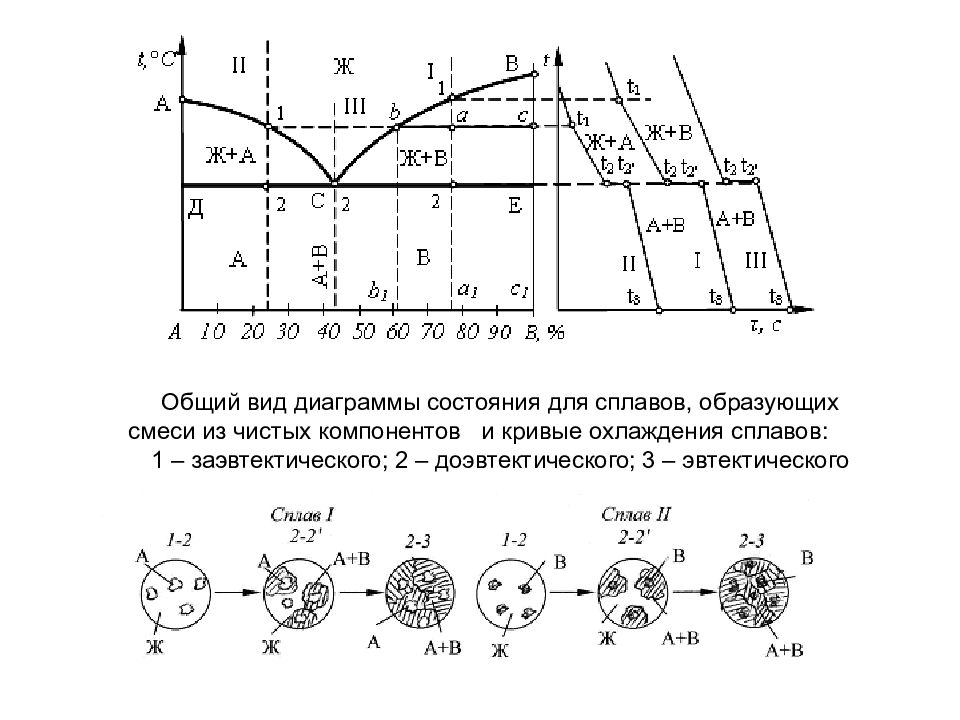
Общий вид диаграммы состояния для сплавов, образующих смеси из чистых компонентов и кривые охлаждения сплавов: 1 – заэвтектического; 2 – доэвтектического; 3 – эвтектического
Слайд 29
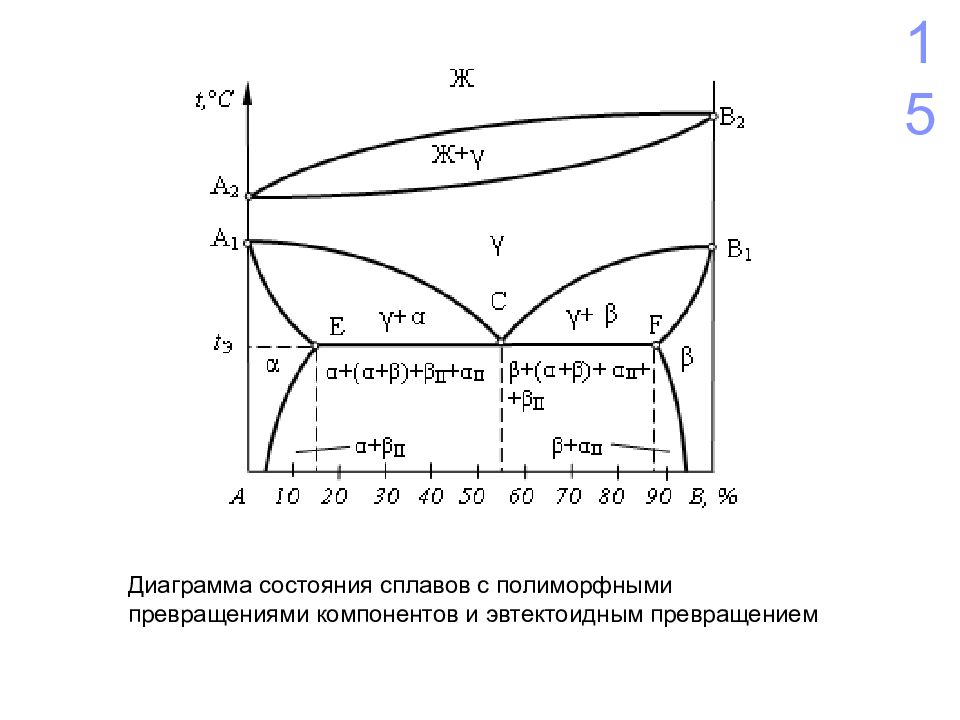
Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением 15
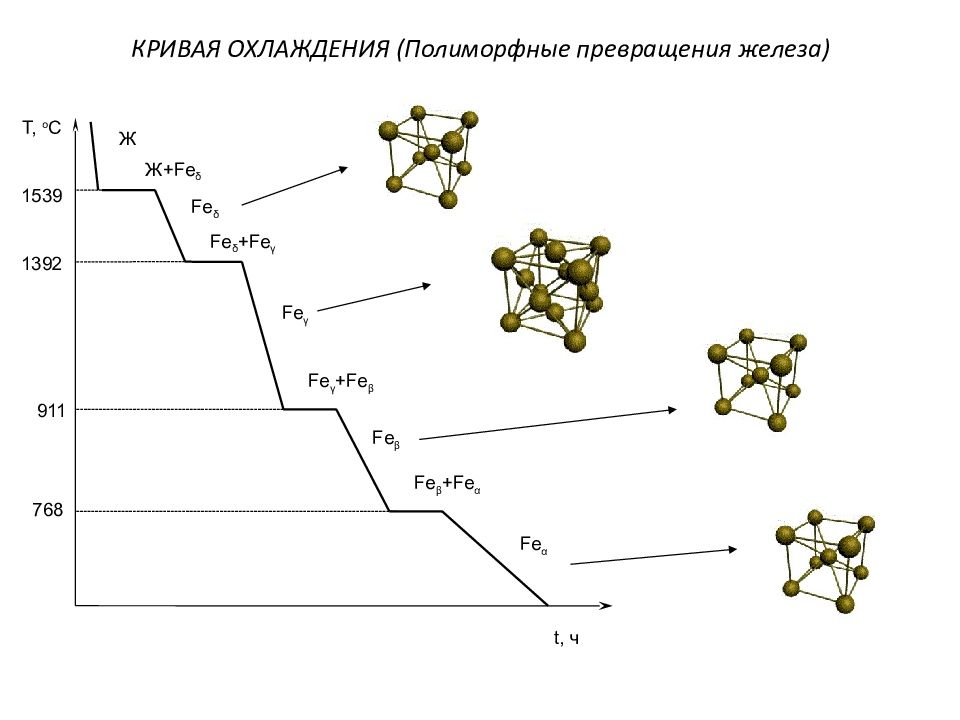
Слайд 30: КРИВАЯ ОХЛАЖДЕНИЯ (Полиморфные превращения железа)
Т, о С 1539 1392 911 768 Ж Ж+ Fe δ Fe δ +Fe γ Fe γ +Fe β Fe β +Fe α Fe δ Fe γ Fe β Fe α t, ч
Слайд 31
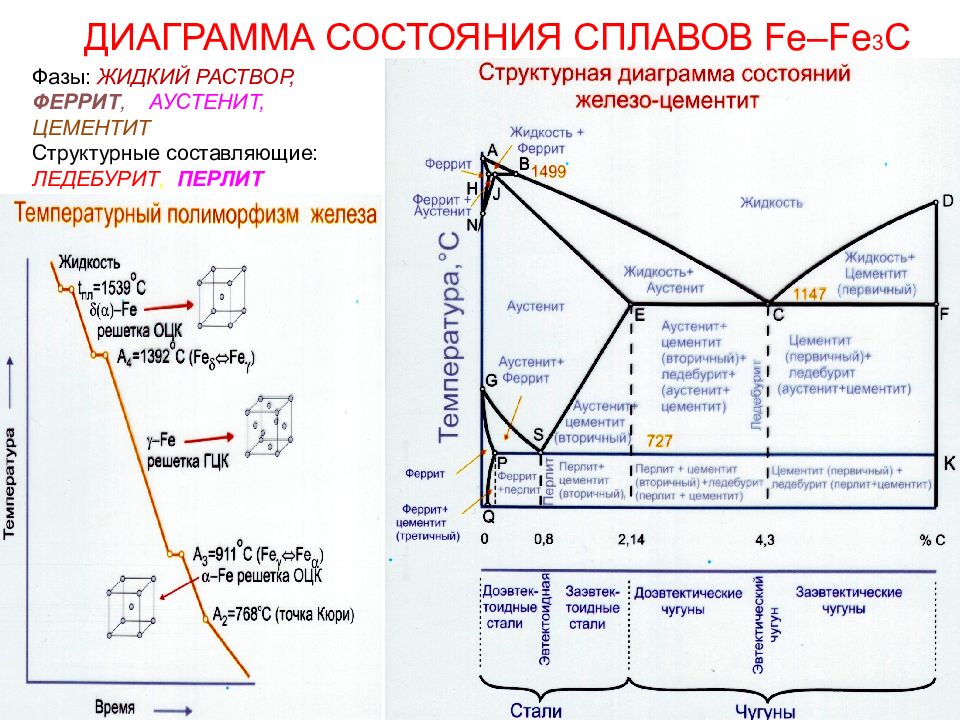
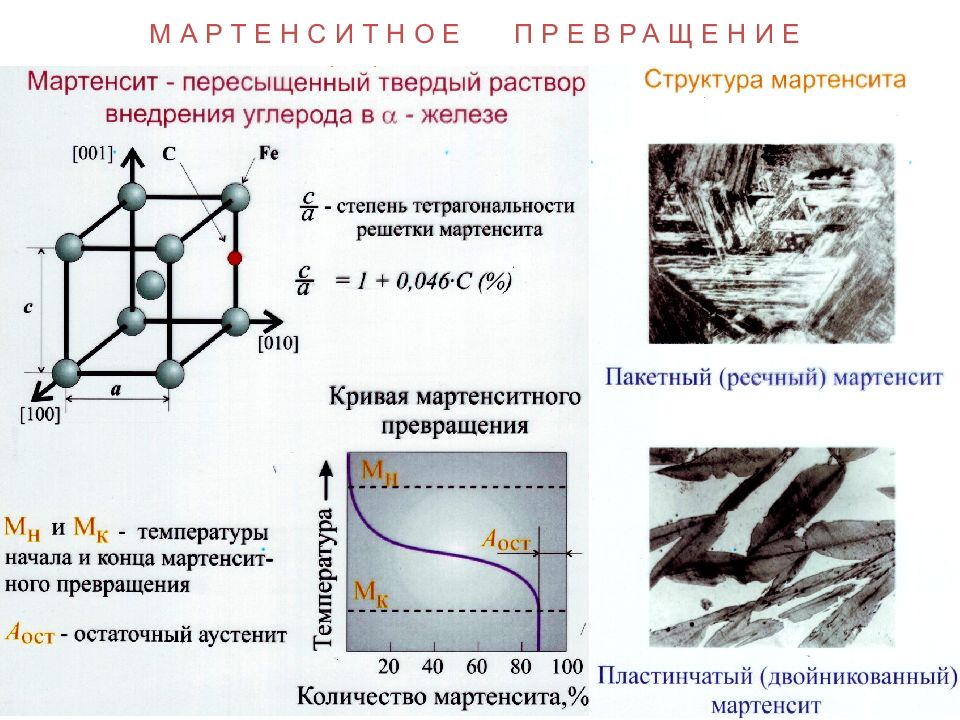
ДИАГРАММА СОСТОЯНИЯ СПЛАВОВ Fe–Fe 3 C Фазы: ЖИДКИЙ РАСТВОР, ФЕРРИТ, АУСТЕНИТ, ЦЕМЕНТИТ Структурные составляющие: ЛЕДЕБУРИТ, ПЕРЛИТ
Слайд 32: ПЛОСКОЕ СЕЧЕНИЕ ЗЕРЕН ФЕРРИТА
Слайд 36
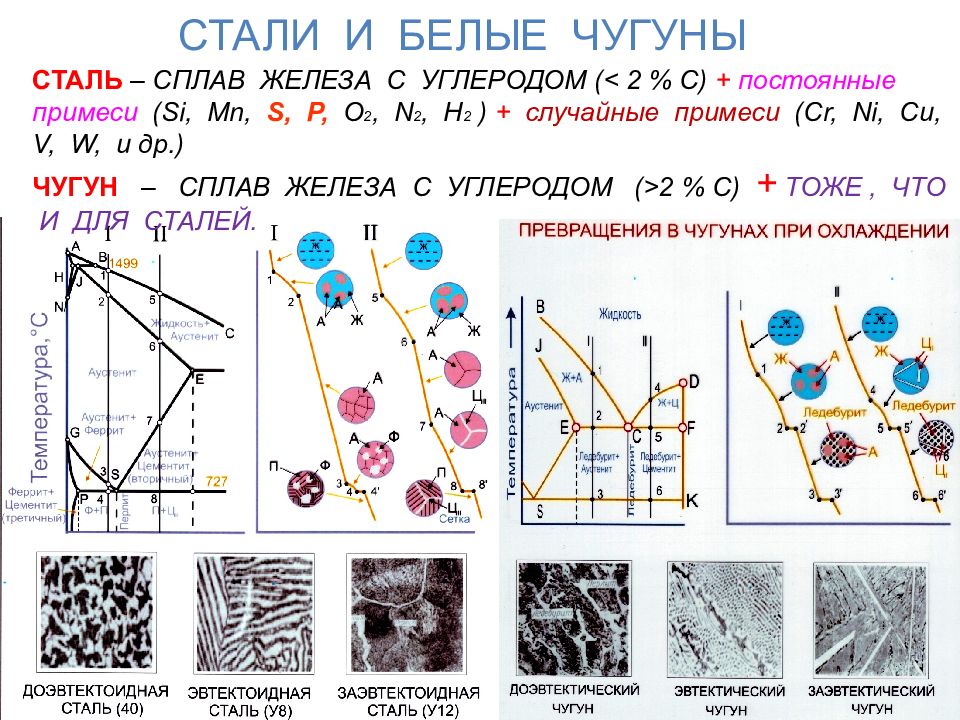
СТАЛИ И БЕЛЫЕ ЧУГУНЫ СТАЛЬ – СПЛАВ ЖЕЛЕЗА С УГЛЕРОДОМ (< 2 % С) + постоянные примеси ( Si, Mn, S, P, O 2, N 2, H 2 ) + случайные примеси ( Cr, Ni, Cu, V, W, и др.) ЧУГУН – СПЛАВ ЖЕЛЕЗА С УГЛЕРОДОМ (>2 % С) + ТОЖЕ, ЧТО И ДЛЯ СТАЛЕЙ.
Слайд 38
ПРИНЦИПЫ ОБОЗНАЧЕНИЕ МАРОК УГЛЕРОДИСТЫХ СТАЛЕЙ Углеродистые конструкционные стали обыкновенного качества (ГОСТ 380-94 ): Ст0, Ст1кп, Ст3сп, Ст3Гпс, Ст6пс. Буквы « Ст » - «Сталь», ЦИФРЫ – условный номер марки, буква «Г» – марганец при его содержании 0,80 % и более, буквы « кп », « пс », « сп » – степень раскисления стали: « кп » – кипящая, « пс » – полуспокойная, « сп » – спокойная. Углеродистые качественные конструкционные стали (ГОСТ 1050-88): горячекатаные (кованные - 08, 08 кп, 10, 15пс, …, 40 и др.-); 20Л, 25Л – литейные ; А12, АС40 – автоматные. ЦИФРЫ – содержание углерода в сотых долях процента. Углеродистые инструментальные стали : (У7, У8, У10, У12) - качественные ; У10А, У12А – высококачественные Буквы: «У» - обозначение углеродистых инструментальных; «А» - высококачественные с пониженным содержанием вредных примесей S и P ; ЦИФРЫ - содержание углерода в десятых долях процента. Например, У11–углеродистая инструментальная качественная со средним содержанием углерода - 11/10 % или 1,1 %
Слайд 39
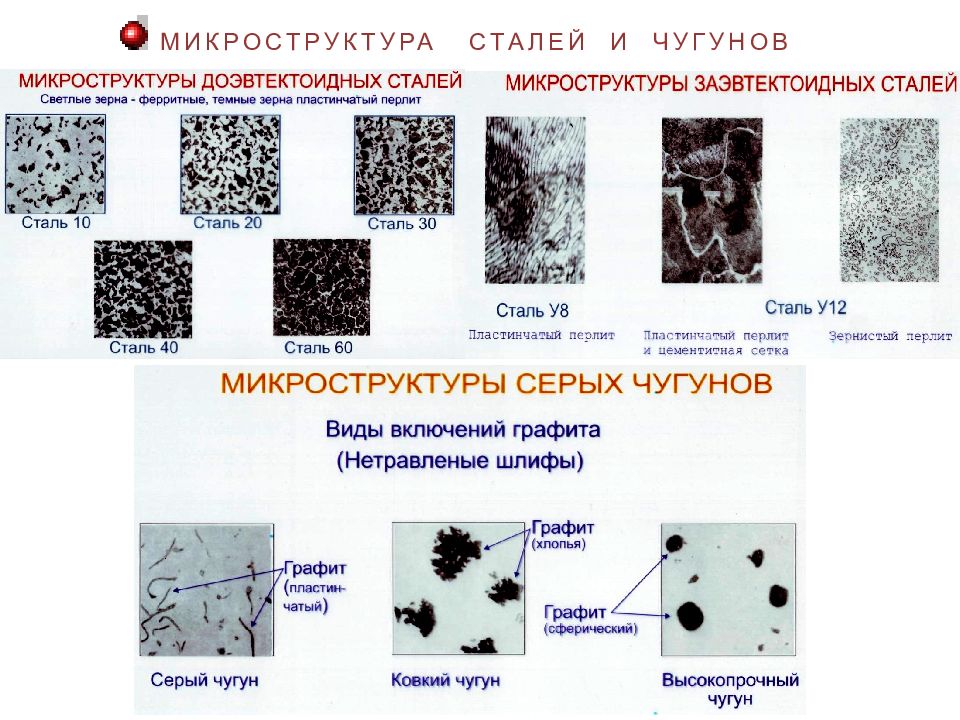
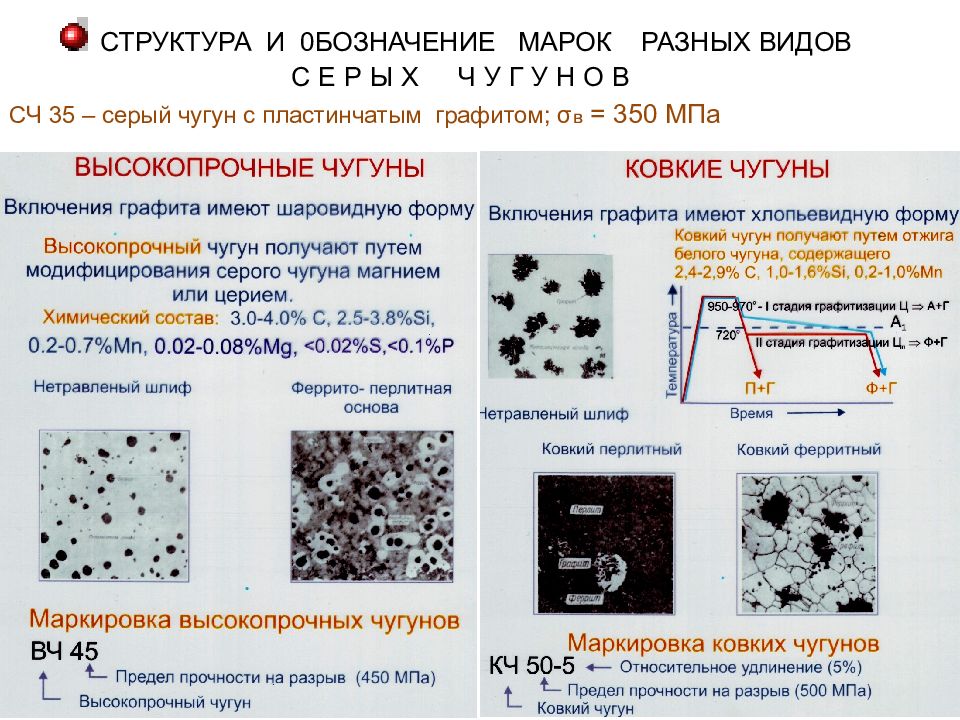
СТРУКТУРА И 0БОЗНАЧЕНИЕ МАРОК РАЗНЫХ ВИДОВ СЕРЫХ ЧУГУНОВ СЧ 35 – серый чугун с пластинчатым графитом; σ в = 350 МПа
Слайд 41
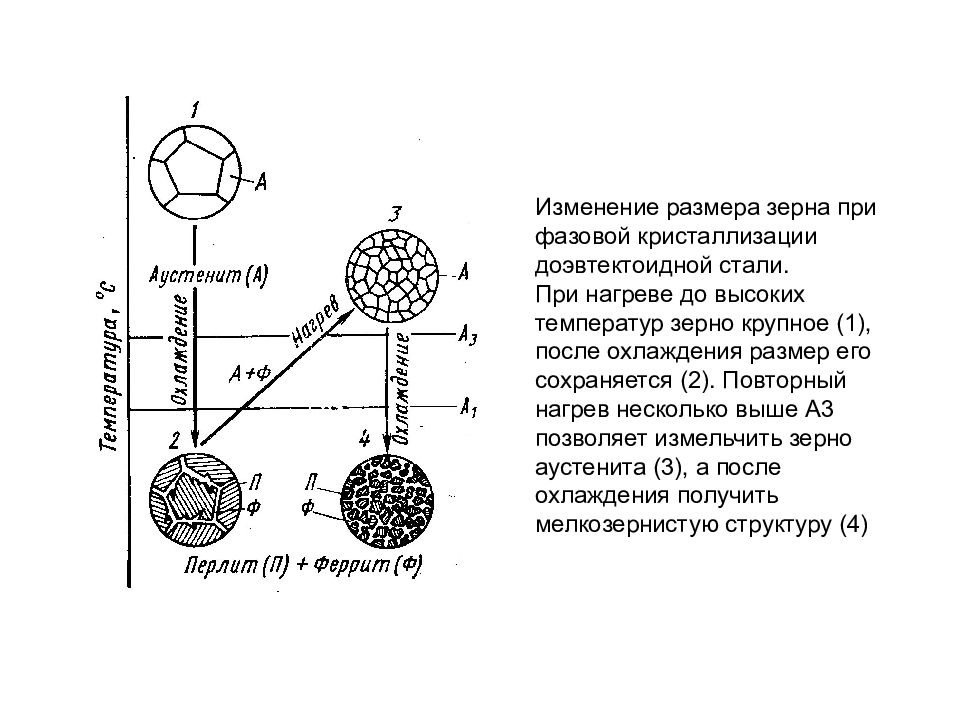
Изменение размера зерна при фазовой кристаллизации доэвтектоидной стали. При нагреве до высоких температур зерно крупное (1), после охлаждения размер его сохраняется (2). Повторный нагрев несколько выше А3 позволяет измельчить зерно аустенита (3), а после охлаждения получить мелкозернистую структуру (4)
Слайд 42: Схема роста зерна аустенита в наследственно мелкозернистой и крупнозернистой эвтектоидной стали
Слайд 45
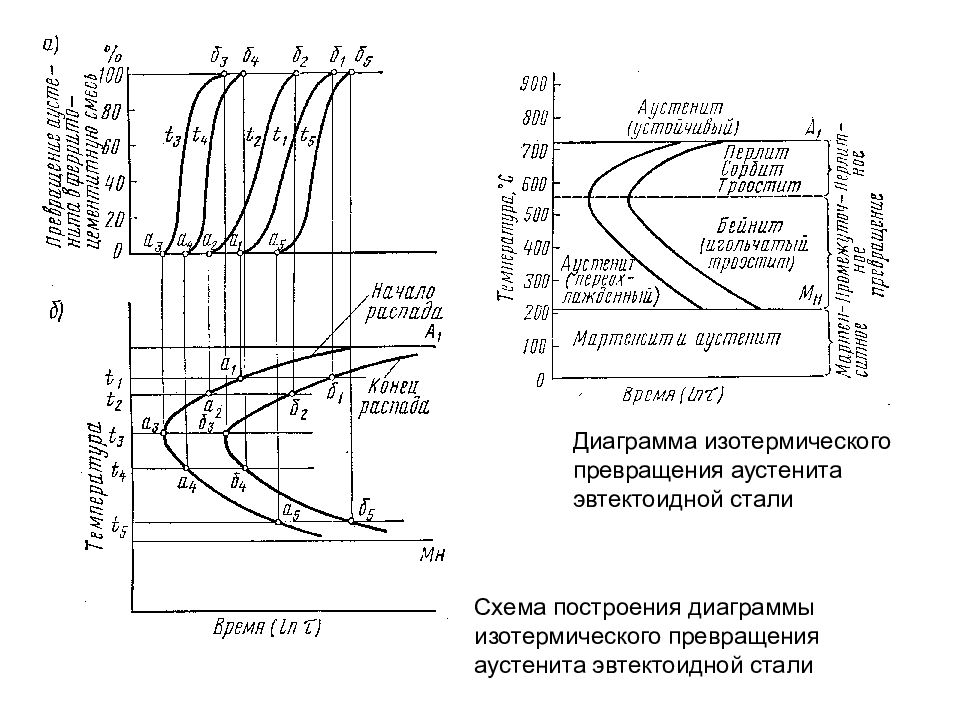
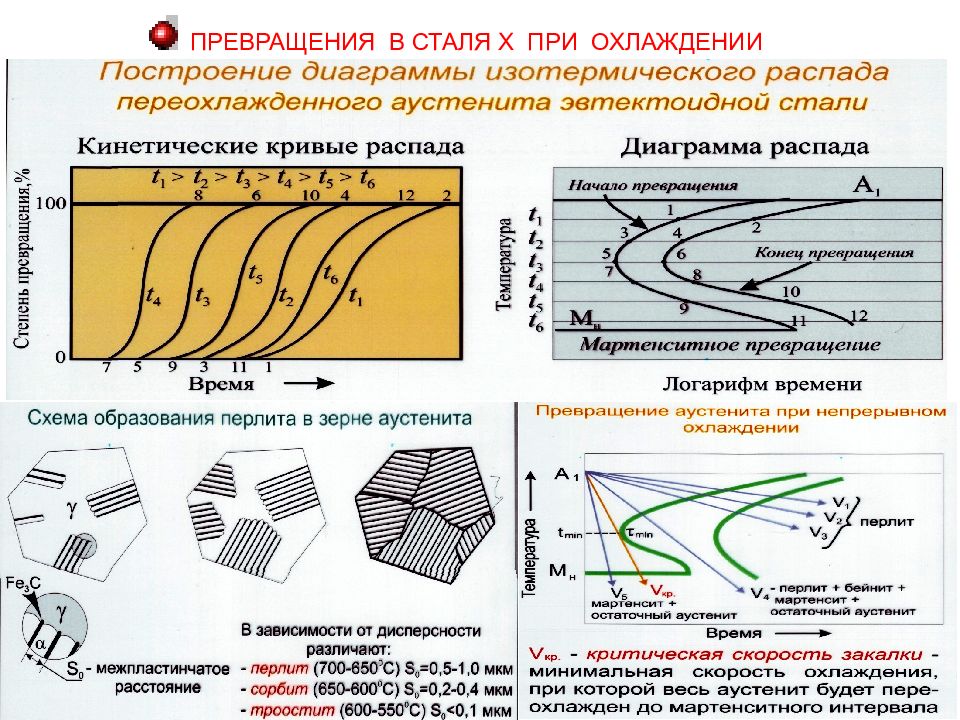
Схема построения диаграммы изотермического превращения аустенита эвтектоидной стали Диаграмма изотермического превращения аустенита эвтектоидной стали
Слайд 47
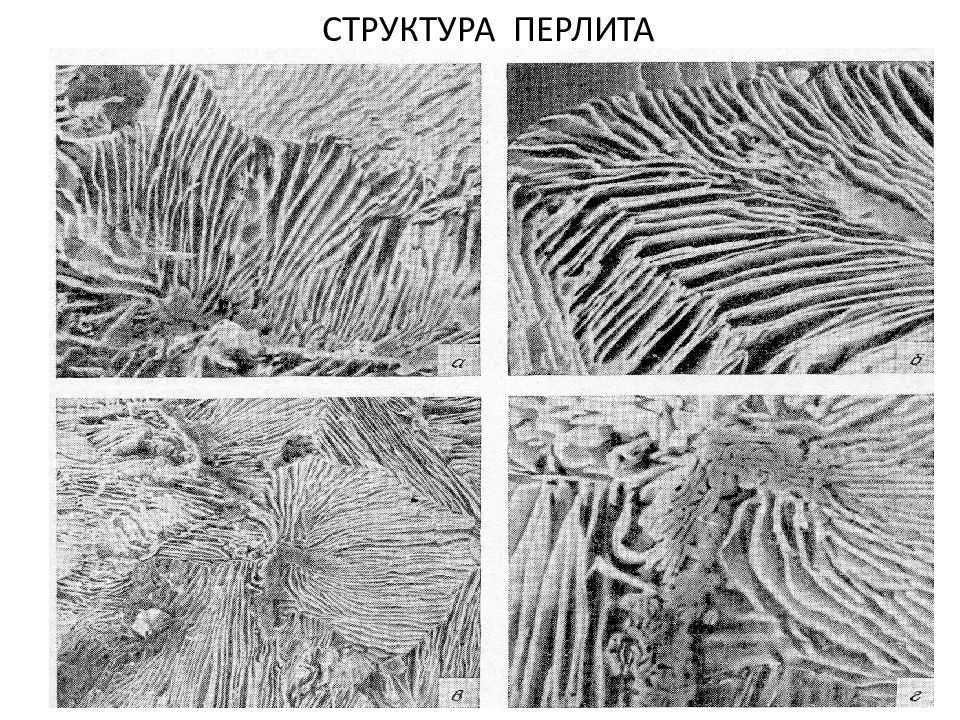
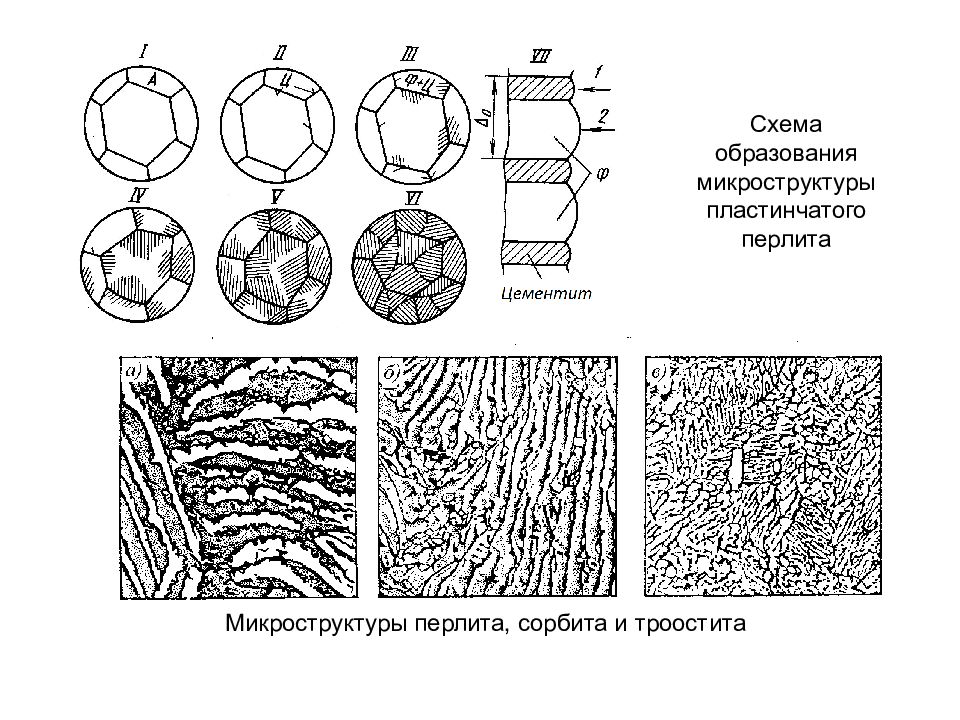
Схема образования микроструктуры пластинчатого перлита Микроструктуры перлита, сорбита и троостита
Слайд 50
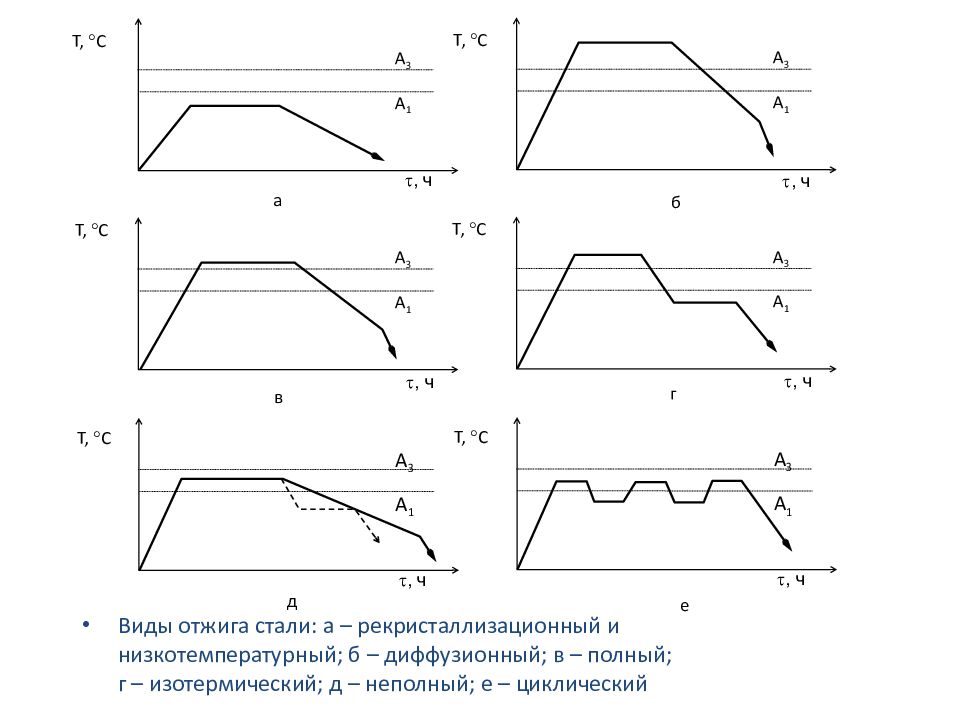
Виды отжига стали: а – рекристаллизационный и низкотемпературный; б – диффузионный; в – полный; г – изотермический; д – неполный; е – циклический А 3 А 1 Т, С , ч а А 3 А 1 Т, С б А 3 А 1 А 3 А 1 А 3 А 1 д А 3 А 1 е , ч , ч Т, С Т, С Т, С Т, С в г , ч , ч , ч
Слайд 51
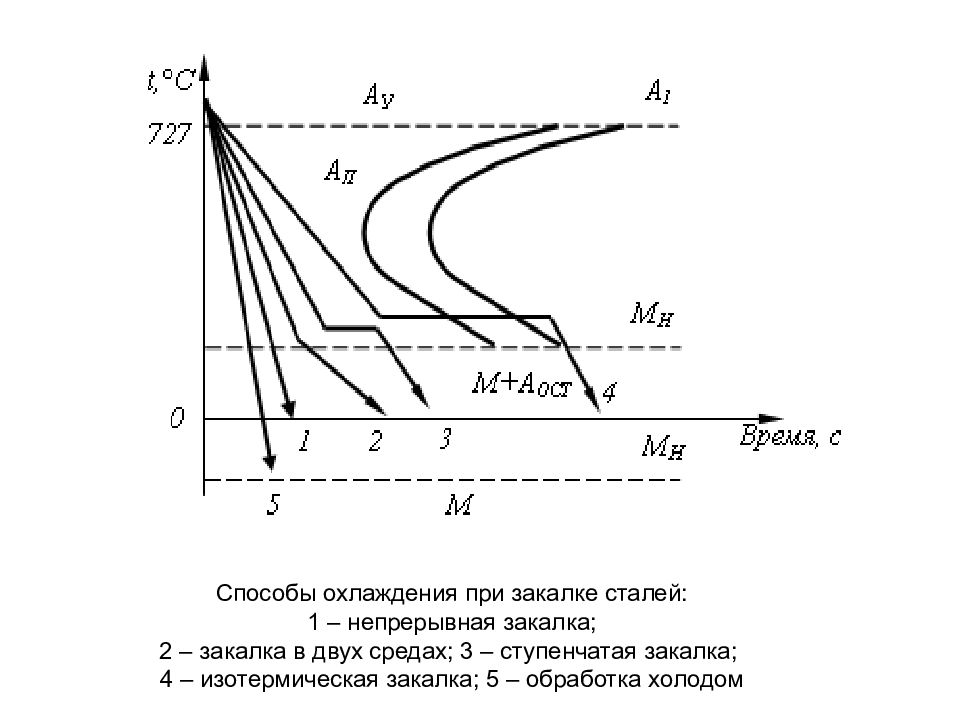
Способы охлаждения при закалке сталей: 1 – непрерывная закалка; 2 – закалка в двух средах; 3 – ступенчатая закалка; 4 – изотермическая закалка; 5 – обработка холодом
Слайд 54
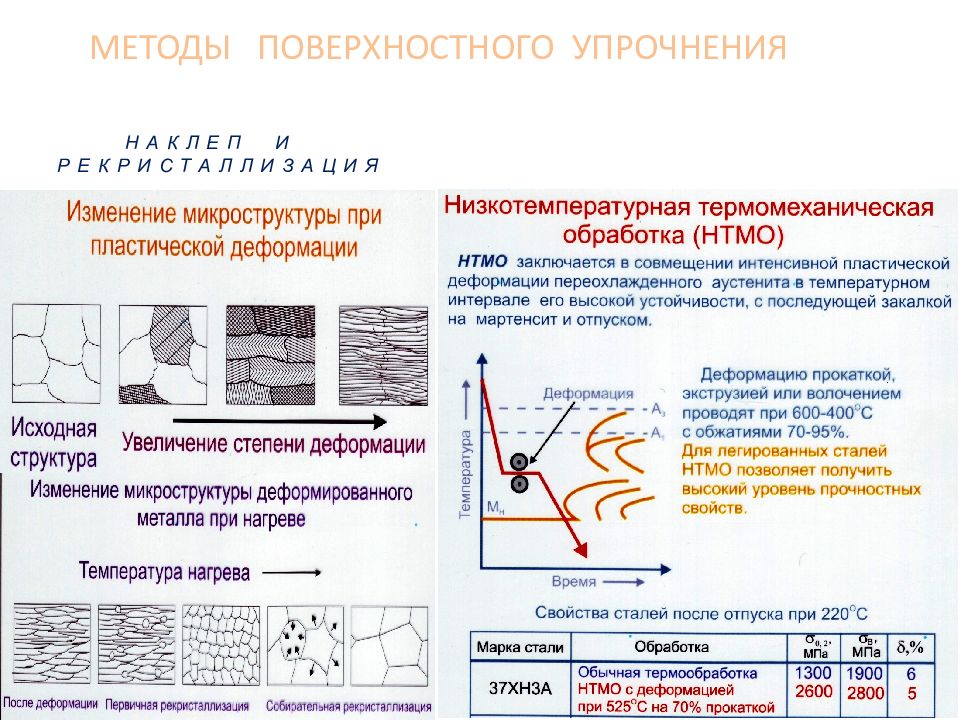
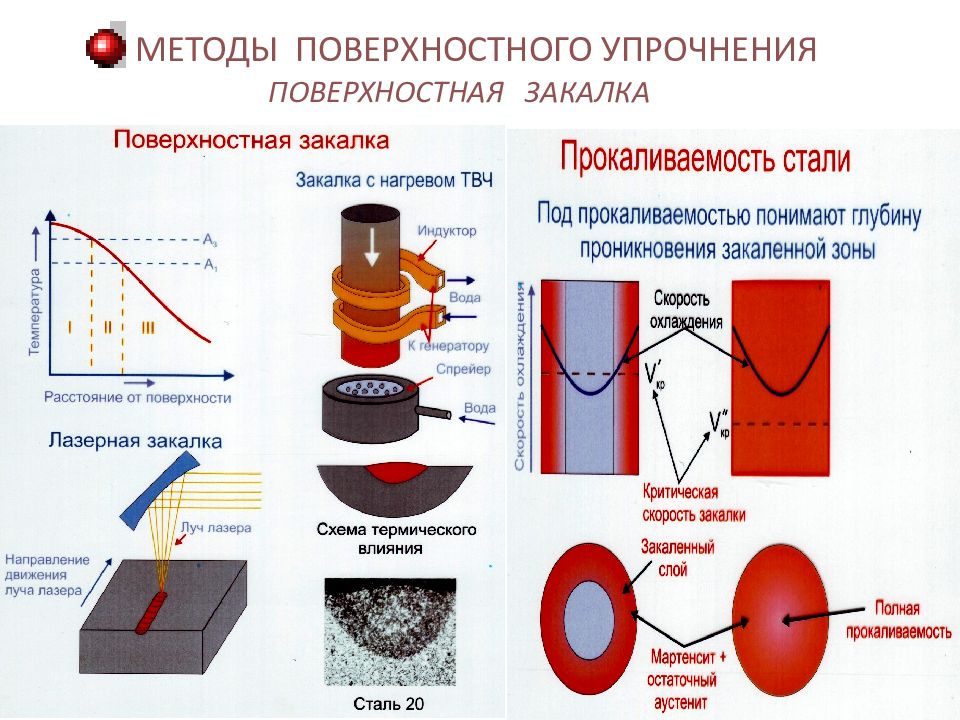
ХТО – называют поверхностное насыщение стали каким-либо химическим элементом (углеродом, азотом, бором и т. п.) путем его диффузии из внешней среды. Изделие помещают, в среду богатую элементом (КАРБЮРИЗАТОР), и нагревают. Происходят следующие процессы: диссоциация – распад молекул карбюризатора и образование атомов диффундирующего элемента; адсорбция – поглощение атомов элемента поверхностью детали; диффузия – проникновение атомов элемента от поверхности вглубь металла (в поверхностные слои детали). МЕТОДЫ ПОВЕРХНОСТНОГО УПРОЧНЕНИЯ ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА
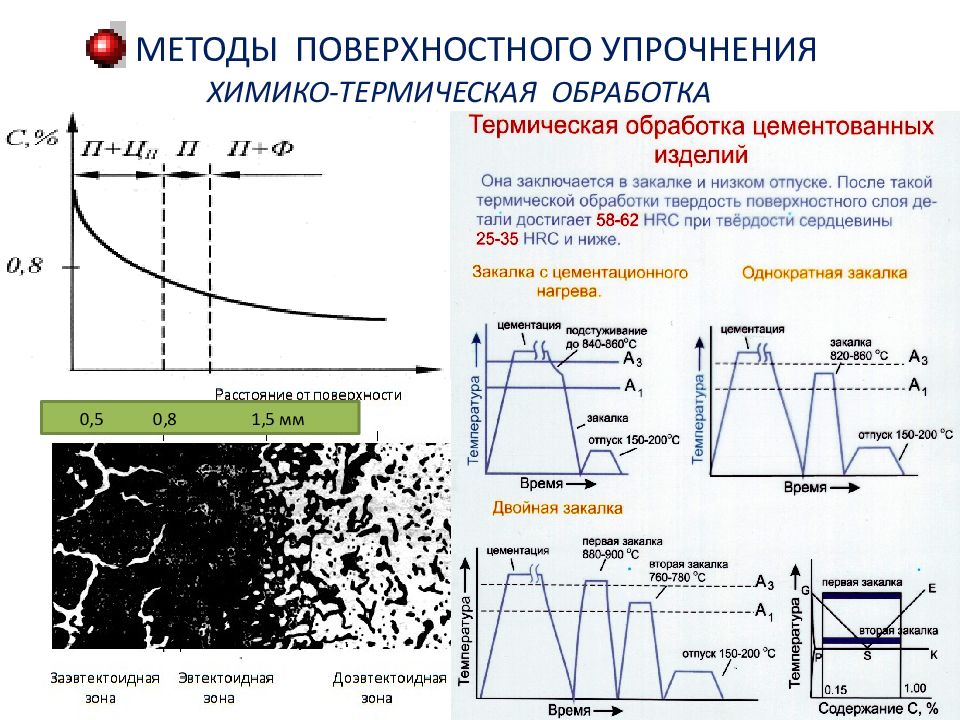
Слайд 55: МЕТОДЫ ПОВЕРХНОСТНОГО УПРОЧНЕНИЯ ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА
0,5 0,8 1,5 мм
Слайд 57
Каждый легирующий элемент обозначается буквой: А – азот, Б – ниобий, В – вольфрам, Г – марганец, Д – медь, Е – селен, К –кобальт, Н – никель, М – молибден, П – фосфор, Р – бор, С – кремний, Т – титан, Ф – ванадий, Х – хром, Ц – цирконий, Ч – редкоземельные элементы, Ю – алюминий. 12Х2НВФА, 14Г2, 10ХСНД, 18Г2С, 15, 20Х, 15ХФ, 20Х2Н4А, 20ХГНР, 40ХН2МА, 35, 70С2ХАБ ШХ15, А12, А40Г, 20Х12ВНМФ, 40Х15Н7Г7Ф2МС, У12, У10А, ХВСГ
Слайд 58: Алюминий и его сплавы
Температура плавления, °С 660 Плотность, кг/м 3 2700 Физические и механические свойства алюминия: Состояние листа Толщина листа, мм σв, МПа, не менее δ, %, не менее Отожженный Нагартованный Горячекатаный 1–10 4–10 5–10,5 60 130 70 28 5 15
Слайд 59
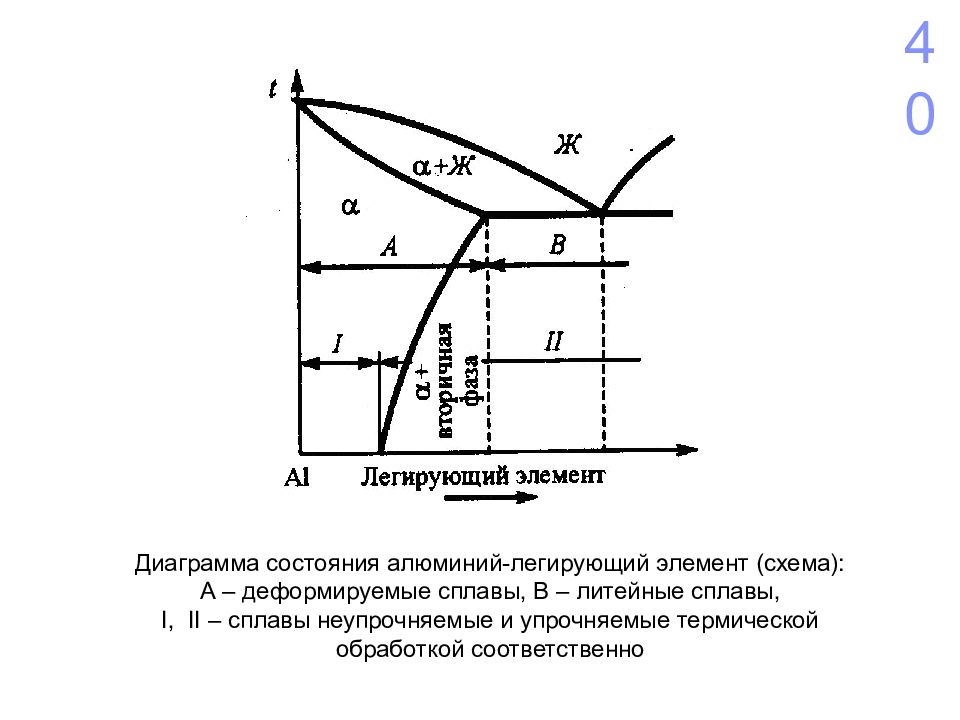
Диаграмма состояния алюминий-легирующий элемент (схема): А – деформируемые сплавы, В – литейные сплавы, I, II – сплавы неупрочняемые и упрочняемые термической обработкой соответственно 40
Слайд 60: Медь и ее сплавы
Физические и механические свойства меди : Температура плавления, ºС 1083 Плотность, кг/м 3 8940 Предел прочности, МПа 200–250 Относительное удлинение, % 40–50 41
Слайд 61
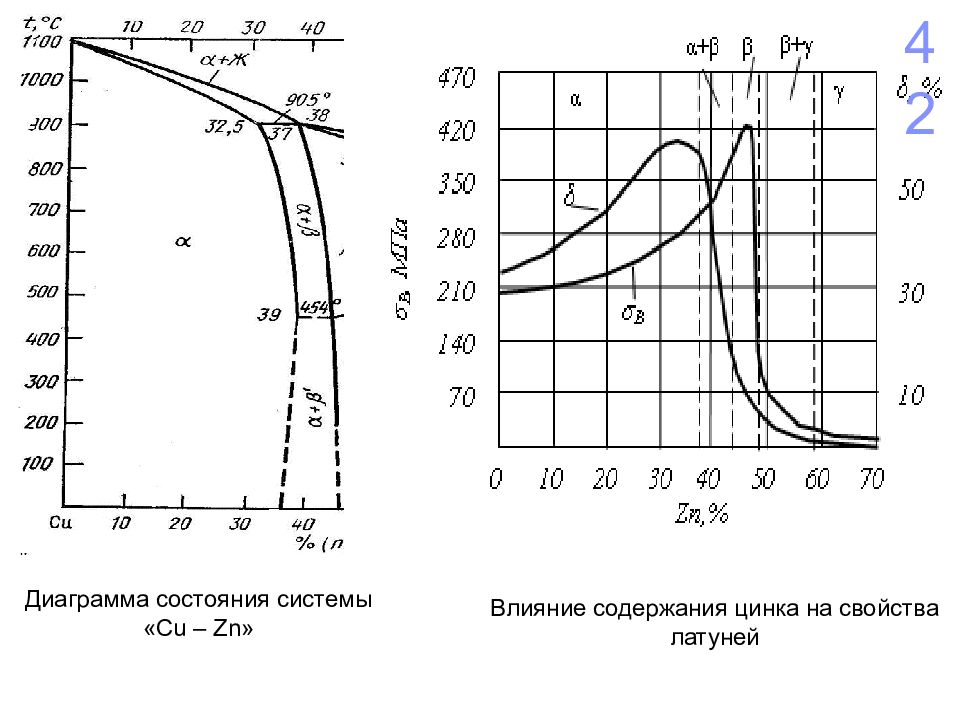
Диаграмма состояния системы « Cu – Zn » Влияние содержания цинка на свойства латуней 42
Слайд 62
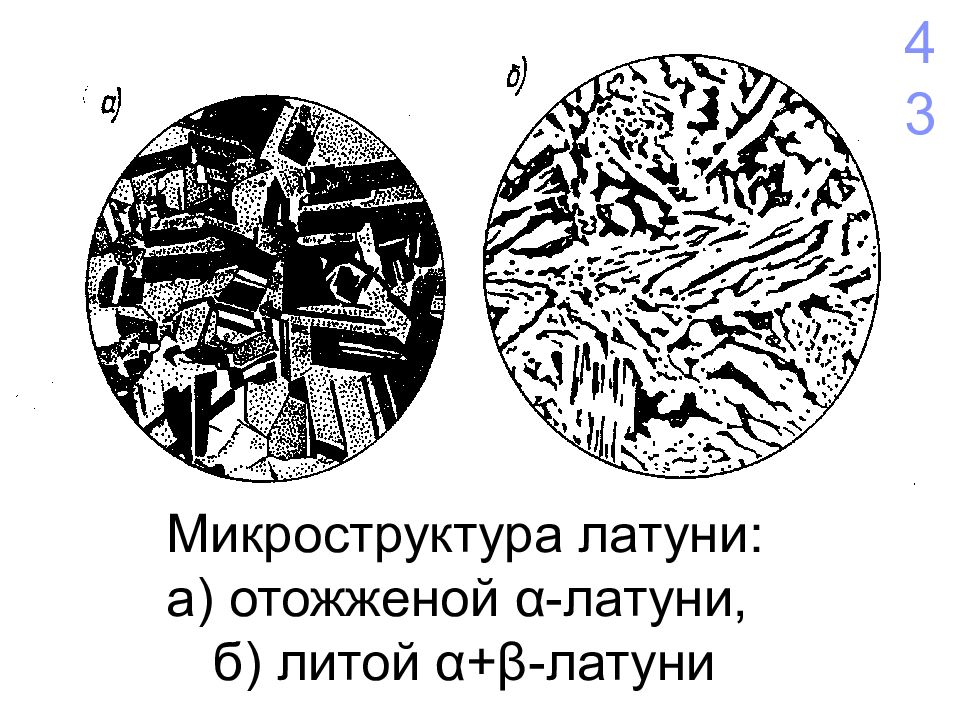
Микроструктура латуни: а) отожженой α -латуни, б) литой α + β -латуни 43
Слайд 64
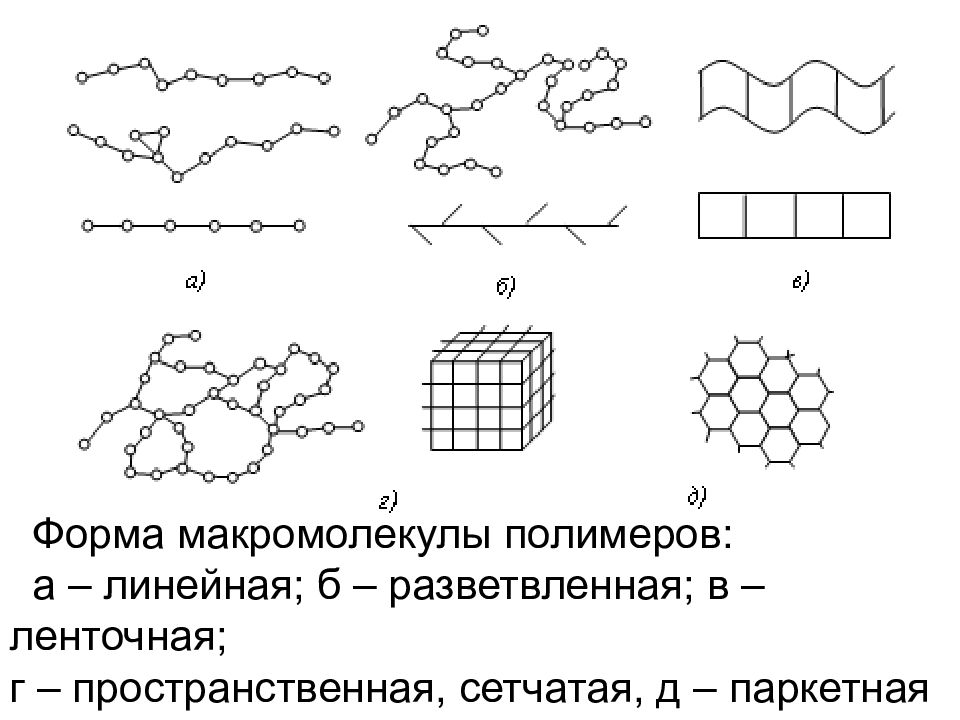
Форма макромолекулы полимеров: а – линейная; б – разветвленная; в – ленточная; г – пространственная, сетчатая, д – паркетная
Слайд 65
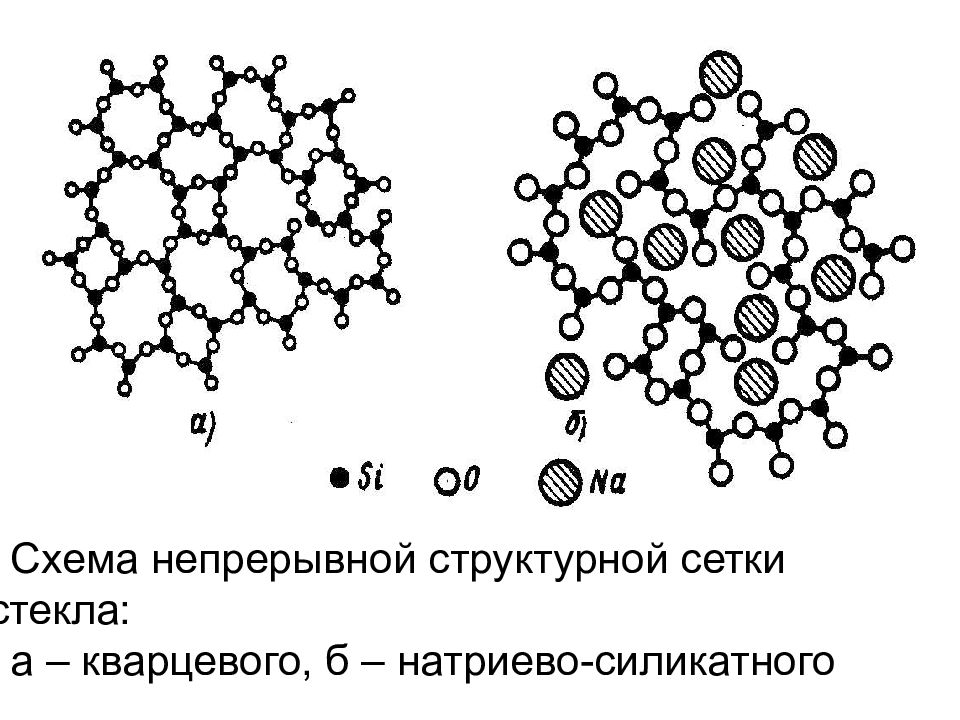
Схема непрерывной структурной сетки стекла: а – кварцевого, б – натриево-силикатного
Слайд 66
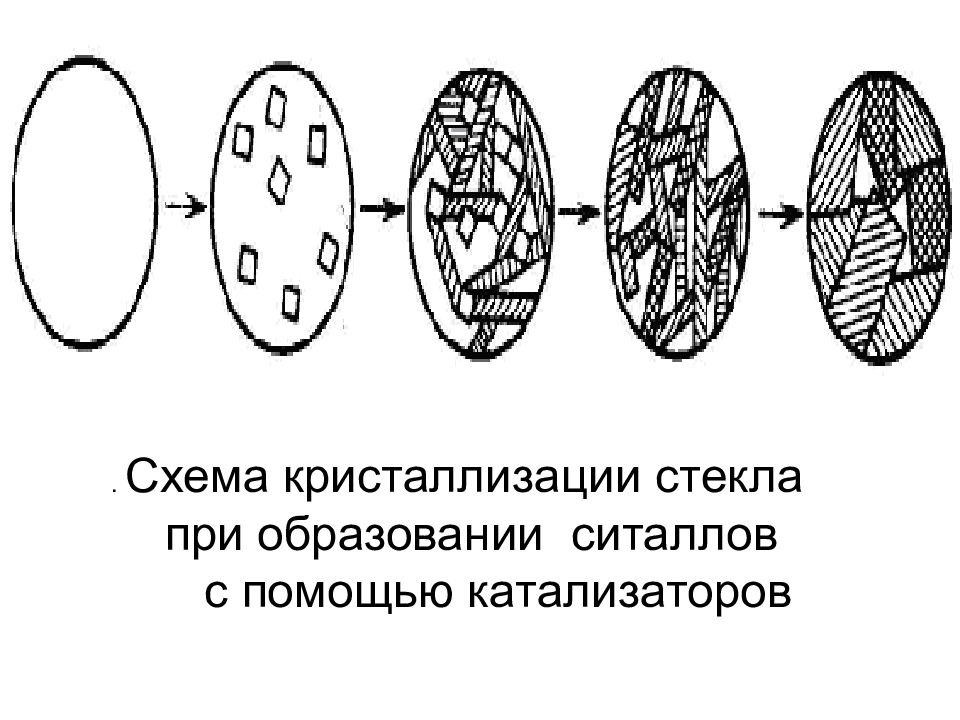
. Схема кристаллизации стекла при образовании ситаллов с помощью катализаторов
Слайд 67
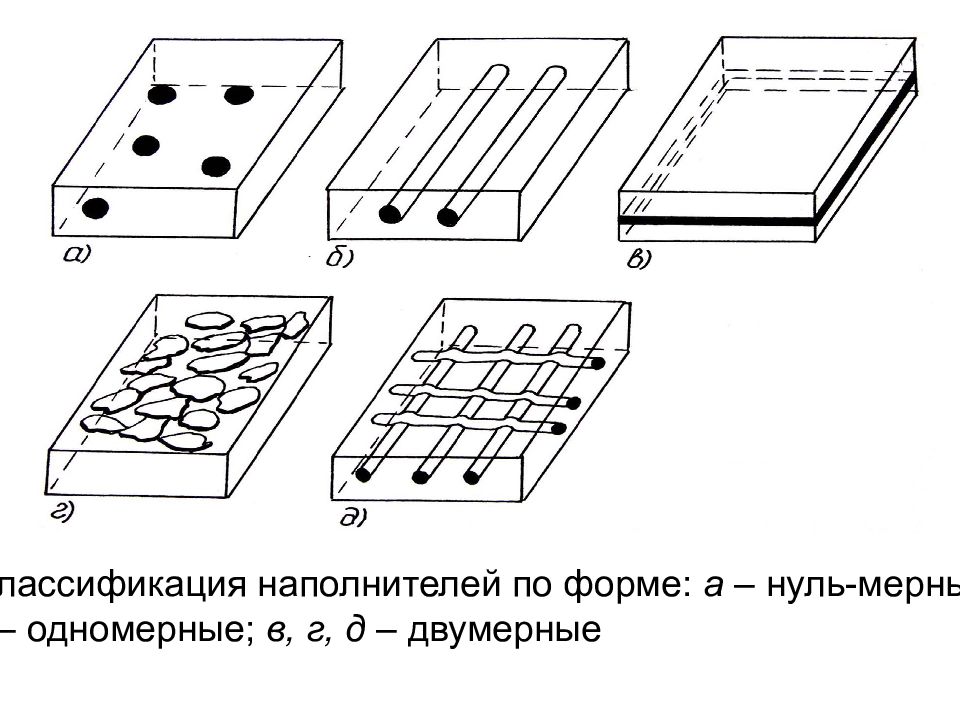
. Схема строения композиционных материалов: а – дисперсноупрочненные; б - волокнистые; в - слоистые