Первый слайд презентации: Основы Атомно-эмиссионного спектрального анализа. Происхождение атомных спектров
Основан на термическом возбуждении свободных атомов или ионов и регистрации спектра испускания в у. ф. и видимой части спектра. Каждая спектральная линия соответствует переходу между отдельными стационарным энергетическим состоянием атомов. Δ Е = Е в – Е о = hυ
Слайд 3: Интенсивность спектральных линий
Описывается законом распределения Больцмана. Y = A· N (1 - x ) · L -Е ⁄ КТ где: Y – интенсивность, А – коэффициент пропорциональности (зависит от вероятности спонтанного перехода), N – число возбужденных атомов, х – степень ионизации, L – число 2,7 или основание натурального логарифма ln, Е – энергия возбуждения, К – константа Больцмана, Т – температурный источник возбуждения в К 0.
Слайд 4: Интенсивность спектральных линий
интенсивность зависит: 1. от числа возбужденных атомов 2. от энергии возбуждения
Слайд 5: Резонансные линии
Резонансные линии – самые интенсивные линии, связанные с нижним энергетическим состоянием атомов. 1. часто находятся в трудно доступной области спектра (далекий у. ф.) 2. при большой концентрации может наблюдаться высокое почернение фотопластинки, превышающее область нормального почернения эмульсии.
Слайд 6: Последние линии
Последние линии – интенсивные линии, расположенные в доступной для исследования области спектра. При уменьшении концентрации вещества они исчезают последние. Такие линии часто используются для обнаружения предельно малых концентраций. В качестве последних линий могут быть использованы резонансные линии или другие интенсивные линии доступные для исследования.
Слайд 7: Происхождение атомных спектров
Легче всего возбуждаются электроны, которые находятся далеко от ядра, (линии появляются в видимом диапазоне). Если электроны находятся ближе к ядру, то линии появляются в рентгеновской области. Промежуточные электроны в у.ф. области.
Слайд 8: Происхождение атомных спектров
L = n - 1 0 1 2 3 обозначение s p d f формы Число электронов 2 6 10 14
Слайд 9: Связь спектров элементов с периодической системой Д.И. Менделеева
Потенциал возбуждения ионизации находится в периодической зависимости от величины заряда атомных ядер (порядковый номер). Для элементов одного периода разность энергий между уровнями растет с увеличением заряда ядра, следовательно, потенциал возбуждения последних линий увеличивается, а длина волны уменьшается. 1. Все металлы легко возбуждаются. Поэтому последние линии имеют высокую длину волны. Цветные металлы имеют простой спектр, черные – сложный.
Слайд 10
2. Все инертные газы трудновозбудимы. 3. Элементы 1 группы имеют один внешний электрон на S уровне слабо связанный с ядром, следовательно, потенциал возбуждения или ионизации низкий. потенциал возбуждения от лития к цезию связь будет уменьшаться.
Слайд 11
4. Элементы 2 группы имеют нижний терм или уровень S и потенциал возбуждения больше чем для щелочных металлов. Элементы побочных групп имеют внешние электроны на d уровни, лантаноиды и актиноиды на f уровне, следовательно потенциал возбуждения последних линий, которые находятся в у.ф. и видимой области.
Слайд 12
Элементы находятся в конце каждого периода и имеют высокий потенциал возбуждения, поэтому последние линии имеют низкую длину волны и находятся в далекой у. ф. области. Поэтому для анализа используются другие доступные интенсивные линии. Для элементов находящихся в одной группе расстояние между уровнями уменьшается при переходе к тяжелым металлам, т.к. ослабляются связи электронов с ядром, следовательно, потенциал возбуждения последних линий увеличивается, а длина волны уменьшается.
Слайд 13: Источники излучения и атомизации в АЭСА
Функции источников Перевод пробы из жидкого или твердого состояния в газообразное. Термическая диссоциация ( атомизация ). Возбуждение атомов.
Слайд 14
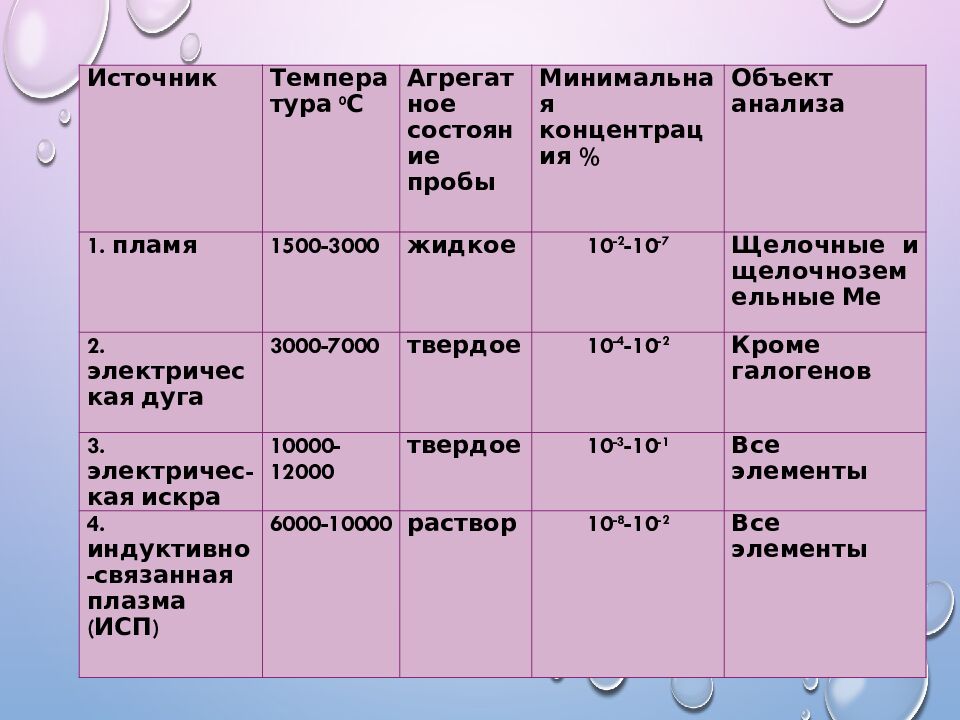
Источник Температура 0 С Агрегатное состояние пробы Минимальная концентрация % Объект анализа 1. пламя 1500-3000 жидкое 10 -2 -10 -7 Щелочные и щелочноземельные Ме 2. электрическая дуга 3000-7000 твердое 10 -4 -10 -2 Кроме галогенов 3. электричес -кая искра 10000-12000 твердое 10 -3 -10 -1 Все элементы 4. индуктивно-связанная плазма (ИСП) 6000-10000 раствор 10 -8 -10 -2 Все элементы
Слайд 16
От температуры источника зависит химическое состояние анализируемого вещества и интенсивность излучения, т.е. 1.Полнота атомизации пробы 2.Доля возбужденных частиц.
Слайд 17: Пламя
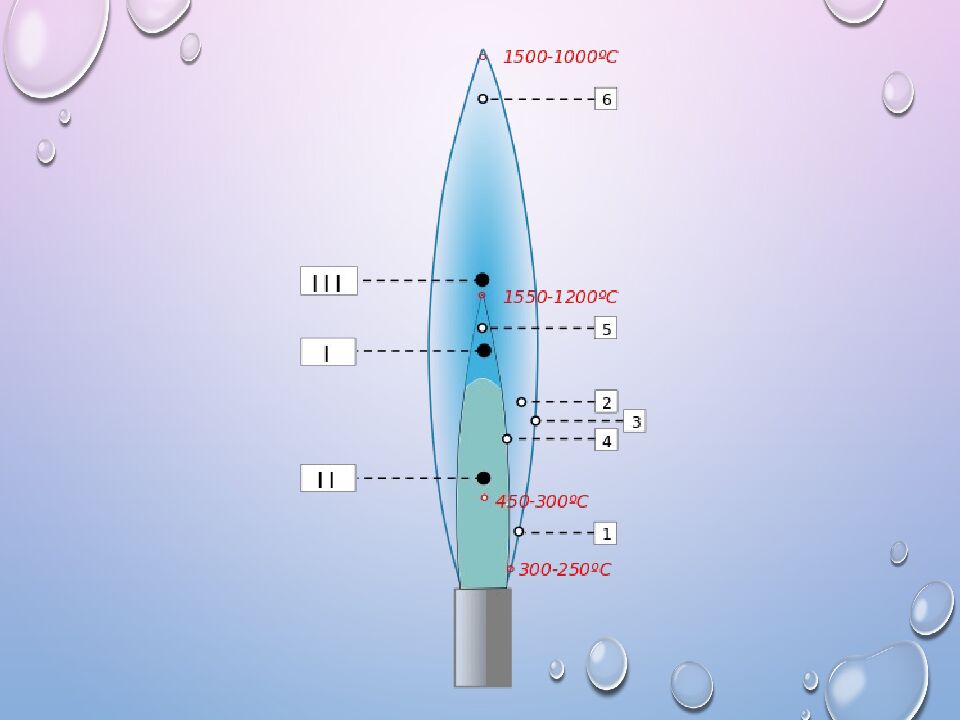
– самый низкий температурный источник (открыт Кирхгофом и Бунзеном). 1. В восстановительной зоне наблюдается термическая диссоциация ( атомизация ) и неполное сгорание горючей смеси ( горючий газ + окислитель входит в пламя). 2. Внутренний конус отделяет зону 1 от зоны 3. Внутренний конус и восстановительная зона содержит много возбужденных молекул и свободных радикалов излучение накладывается на эмиссионные линии атомов. в анализе зона 1 не используется. 3. В окислительной зоне наблюдается полное сгорание горючей смеси. Зона III интенсивно излучает в ик области и мало излучает в уф и видимой области Т.о. для анализа используется зона III в у.ф. области и видимой области.
Слайд 19: Характеристика пламени
Горючий газ Горючий окислитель Температура Объекты анализа Природный газ (пропан + бутан) Воздух 1800 0 С Щелочные металлы Ацетилен С 2 Н 2 Воздух 2200 0 С Щелочные и щелочноземельные Ме Водород Н 2 О 2 2800 0 С Тяжелые Ме, щелочные и щелочноземельные Ме Ацетилен О 2 3100 0 С Тоже самое и Ag, C и, М n Ацетилен N 2 О 3200 0 С То же самое и Pb, Cr, Cd, Fe, Sn.
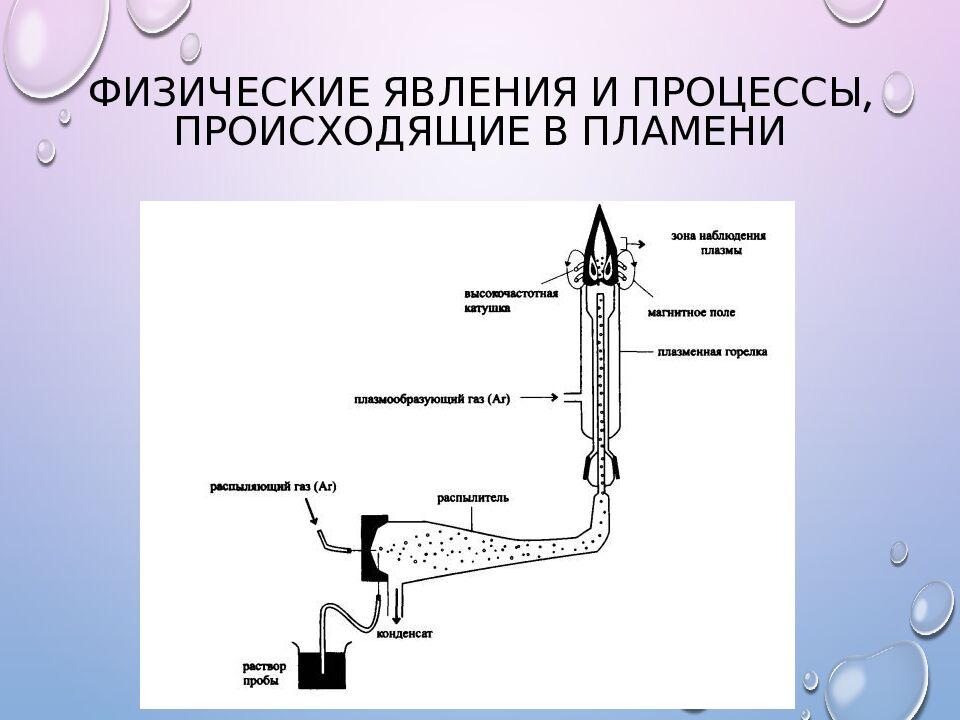
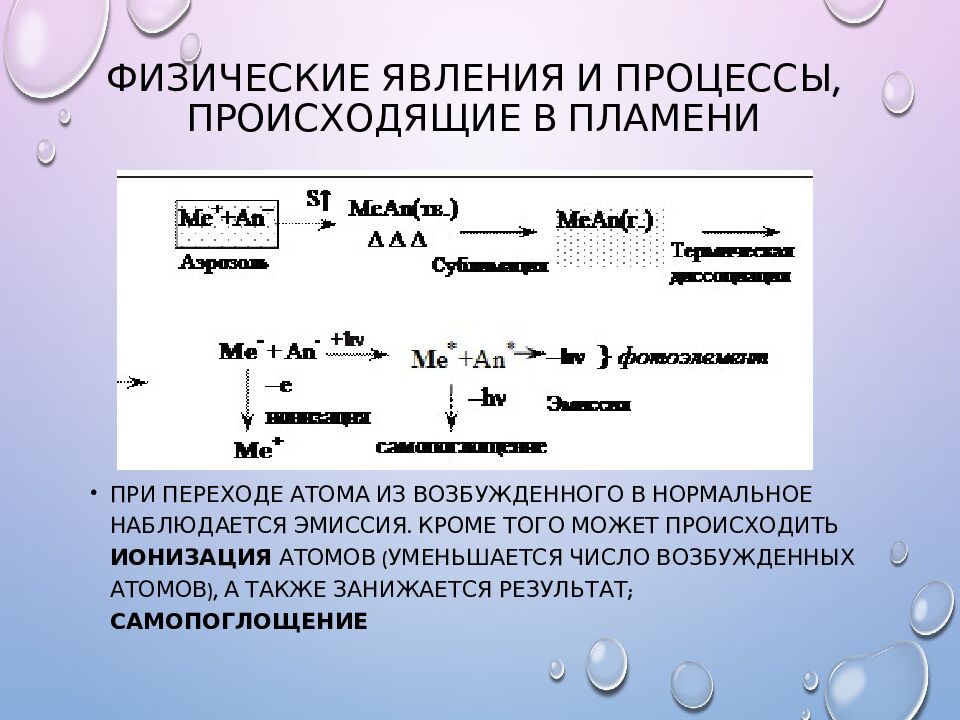
Слайд 21: Физические явления и процессы, происходящие в пламени
При переходе атома из возбужденного в нормальное наблюдается эмиссия. Кроме того может происходить ионизация атомов (уменьшается число возбужденных атомов), а также занижается результат; самопоглощение
Слайд 22
Достоинство пламени. 1. Высокая стабильность пламени, обеспечивает хорошую воспроизводимость результатов. 2.Выбор состава горючей смеси, следовательно, температура позволяет оптимизировать условия атомизации и устранить физико-химические помехи (ионизация и самопоглощение). Недостатки. 1. Большой расход материала (непродолжительное пребывание частиц к источнику ). 2.Не экономический источник. 3. Высокая неоднородность анализируемой пробы (множество молекул, атомов и ионов с разной кинетической энергией или температурой), следовательно, обуславливает процессы самопоглощения и самообращения – возбуждение частицы не излучают, а передают свою энергию не возбужденным атомам.
Слайд 23
Теоретические пути повышения интенсивности. 1. Увеличение температуры пламени (замена горючей смеси). 2. Увеличение продолжительности пребывания атомов в зоне III ( окислительная зона, скорость истечения газа). 3. Снижение затрат энергии на атомизацию пробы (уменьшение размеров капель аэрозоля).
Слайд 27: Электрическая дуга
Работа всех электрических источников света (искра, дуга) основана на газовом разряде – прохождение тока через воздух или другой газ. В обычных условиях газ не проводит электрический ток (изолятор). Если подключить 2 электрода к внешнему источнику тока и в воздушном промежутке создать заряженные частицы, то воздух начинает проводить ток.
Слайд 29
По виду образования заряженных частиц разряд делится на 2 группы : 1. Самостоятельный – при повышении напряжения заряженные частицы в воздухе приобретают высокую кинетическую энергию и передают ее молекулам газа или электродам. Поэтому возрастает количество заряженных частиц в воздушном промежутке за счет ионизации атомов и молекул и эмиссия частиц электродов. При самостоятельном газовом разряде между электродами образуется плазма – это газ, имеющий высокую t и состоящую из заряженных и нейтральных частиц. 2. Не самостоятельный разряд возникает при освещении электродов в у. ф. и рентгеновском излучении.
Последний слайд презентации: Основы Атомно-эмиссионного спектрального анализа. Происхождение атомных спектров
Электрическая дуга создает продолжительный разряд при высокой силе тока (5-7 Ампер) и не высоким напряжением (50-80 Вольт). Разряд пропускают между двумя электродами, которые изготавливают из анализируемого образца. Способы введения пробы в зону электрического разряда: Анализируемый металл сам служит электродом Растворы вводят с помощью распылителей. Порошкообразные пробы помещают в специальные углубления в электродах