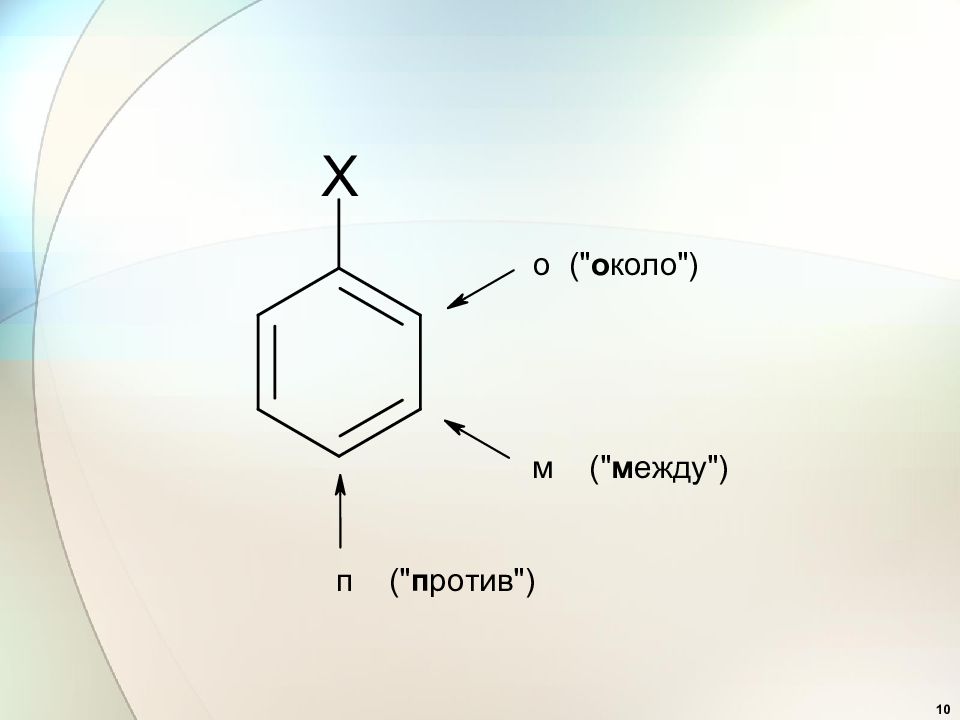
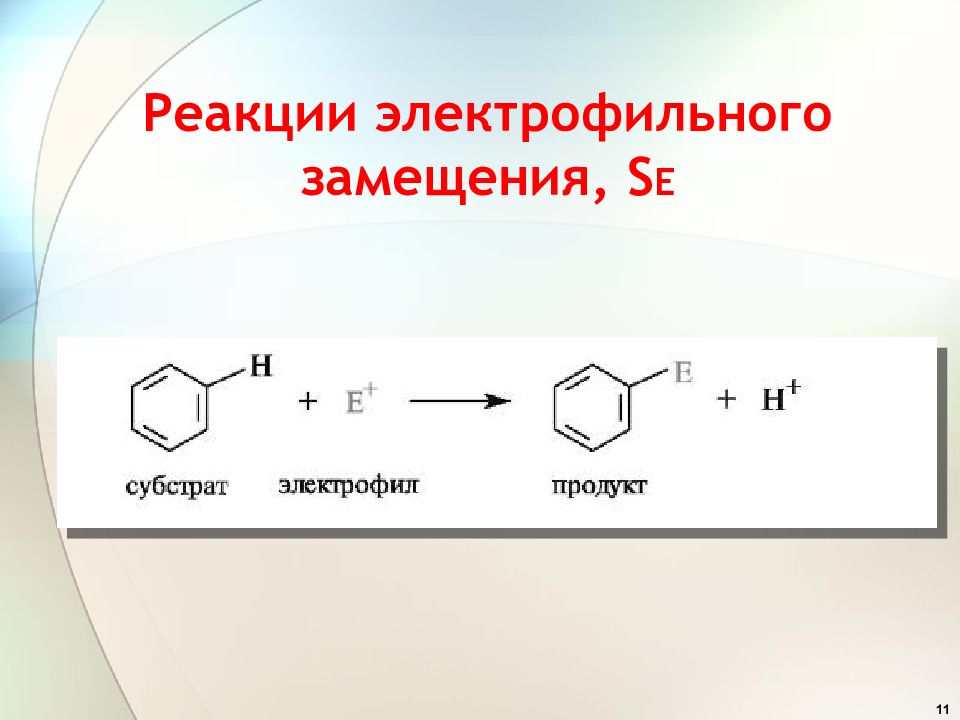
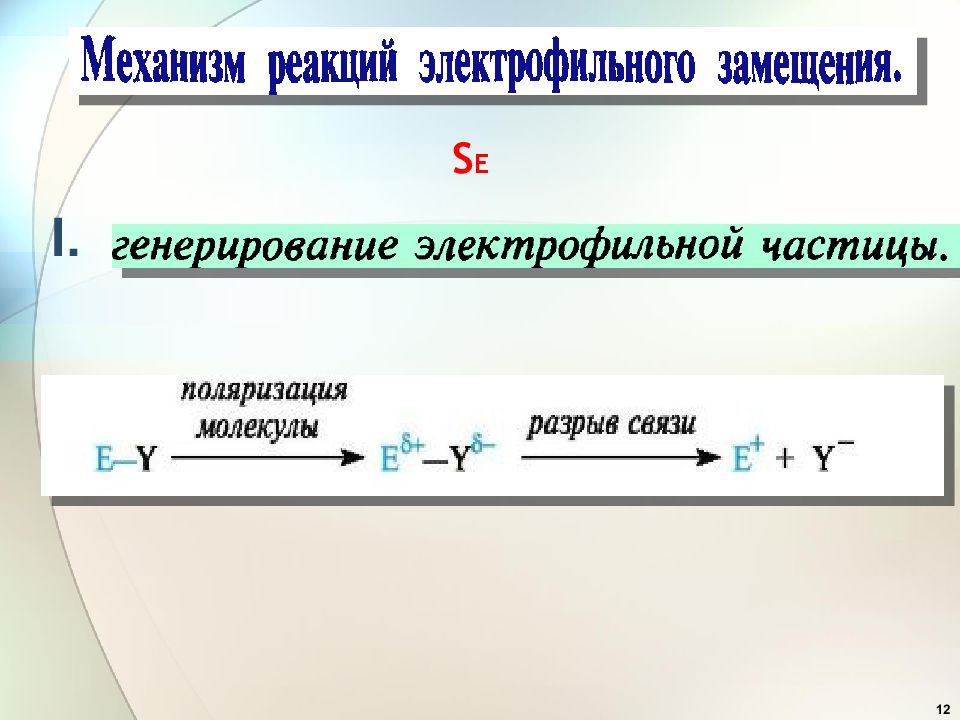
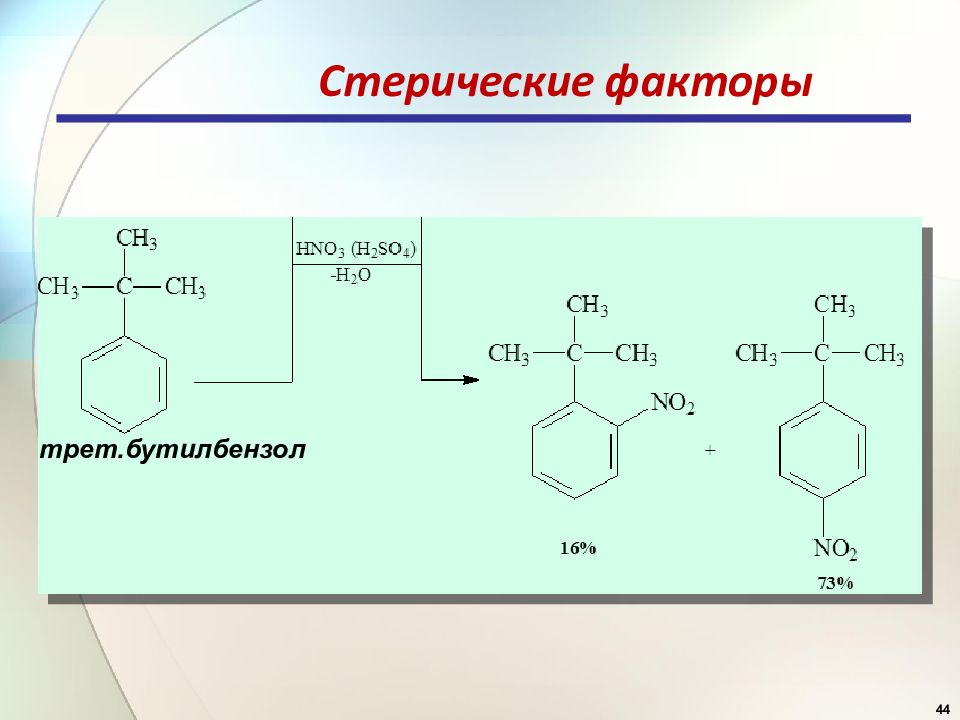
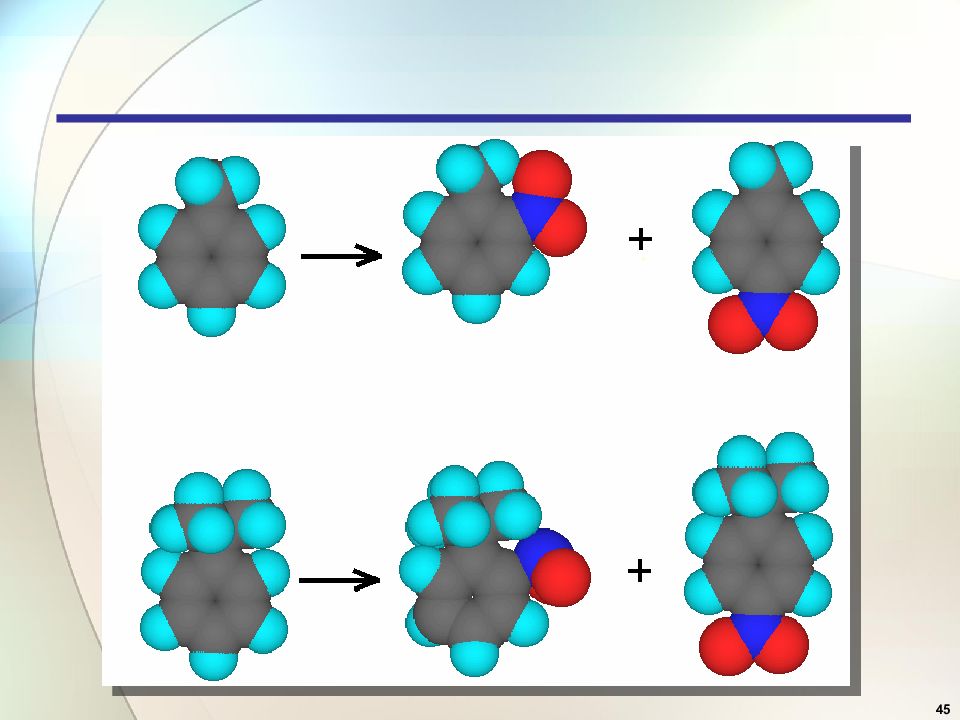
Первый слайд презентации: 6. Электрофильное замещение в ароматических соединениях, S E
1
2 ОСОБЕННОСТИ СТРОЕНИЯ и РЕАКЦИОННОЙ СПОСОБНОСТИ АРЕНОВ ( Ar ).
Слайд 3
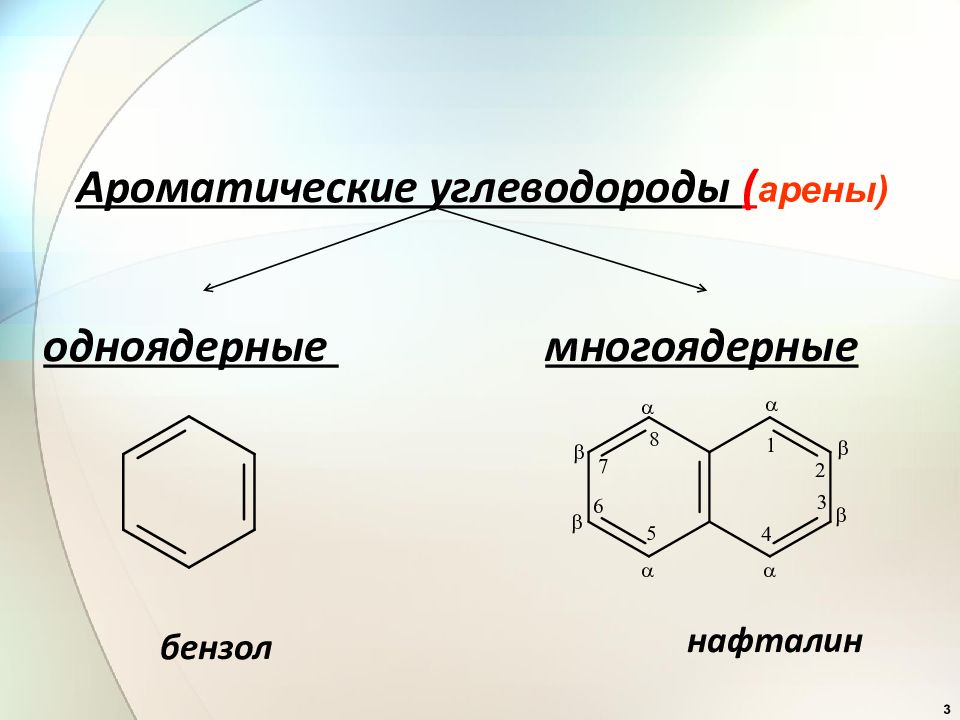
3 Ароматические углеводороды ( арены) одноядерные многоядерные бензол нафталин
Слайд 4
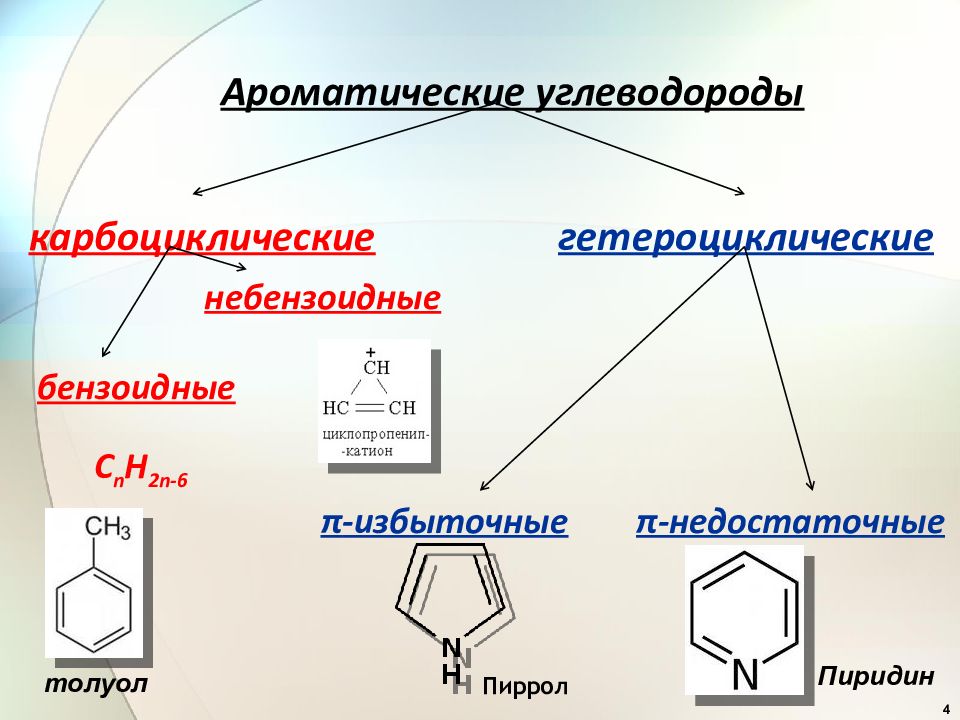
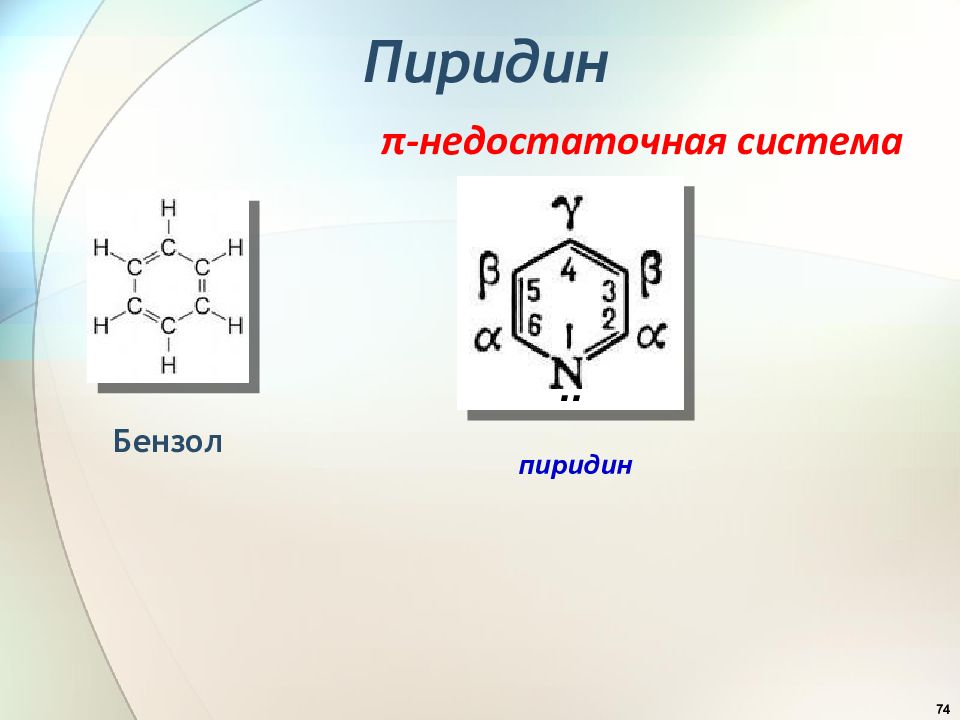
4 Ароматические углеводороды карбоциклические гетероциклические небензоидные бензоидные С n H 2 n -6 π -избыточные π -недостаточные толуол Пиррол Пиридин
Слайд 5: Арены
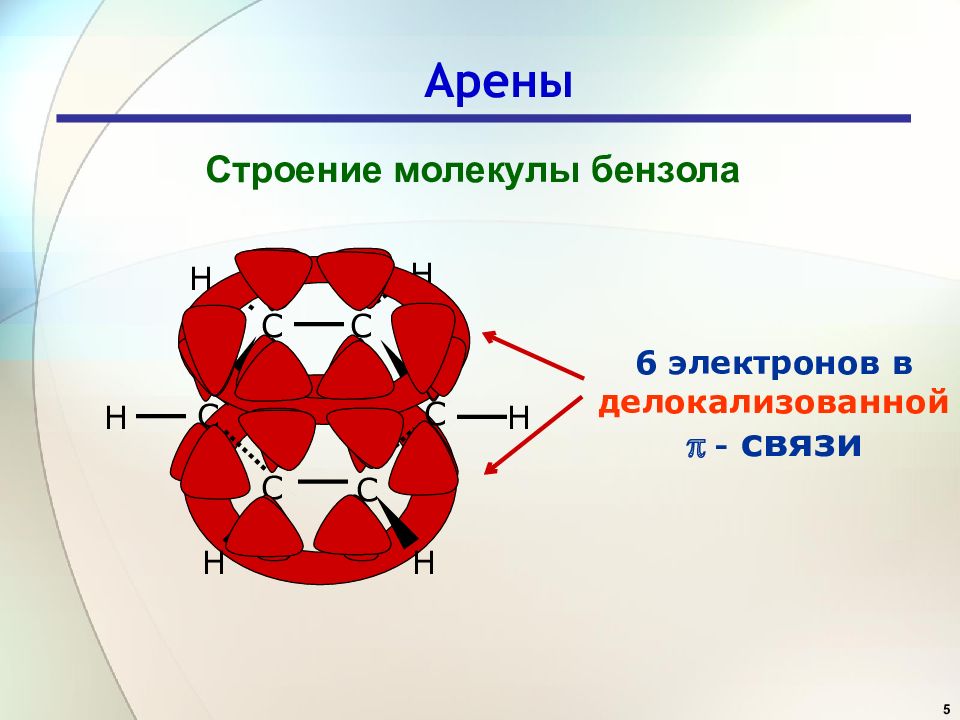
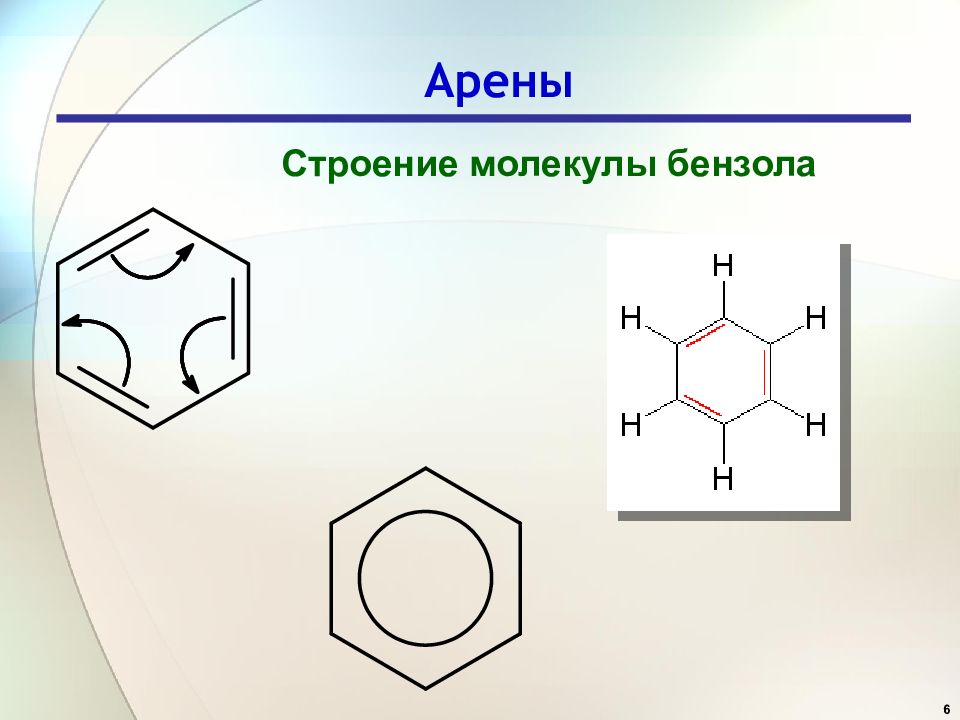
5 Арены Строение молекулы бензола C C C C C C H H H H H H 6 электронов в делокализованной - связи
Слайд 14
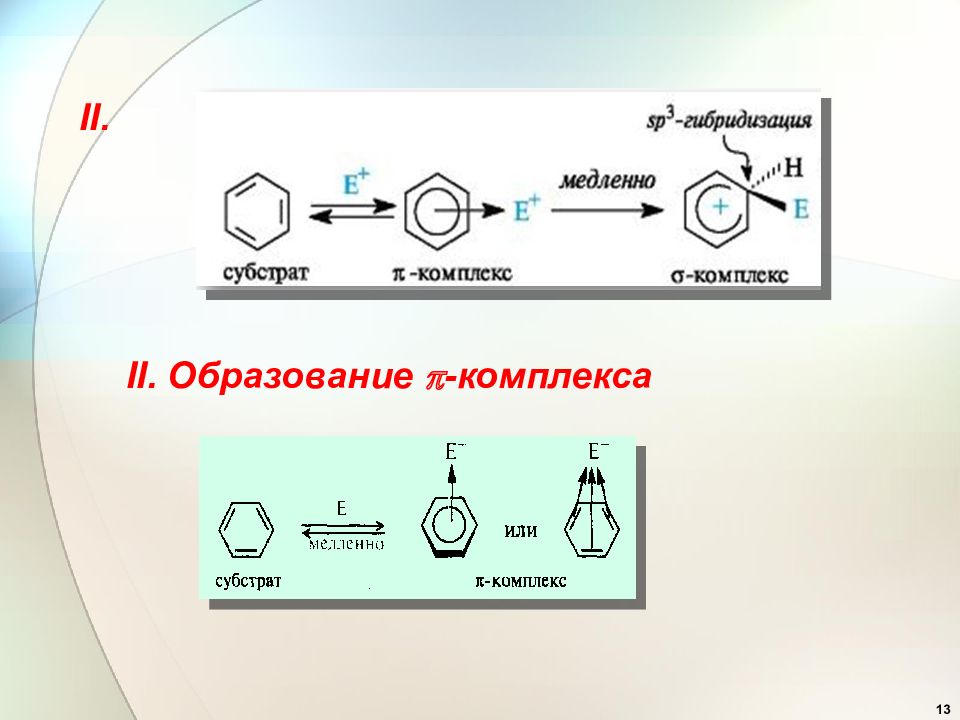
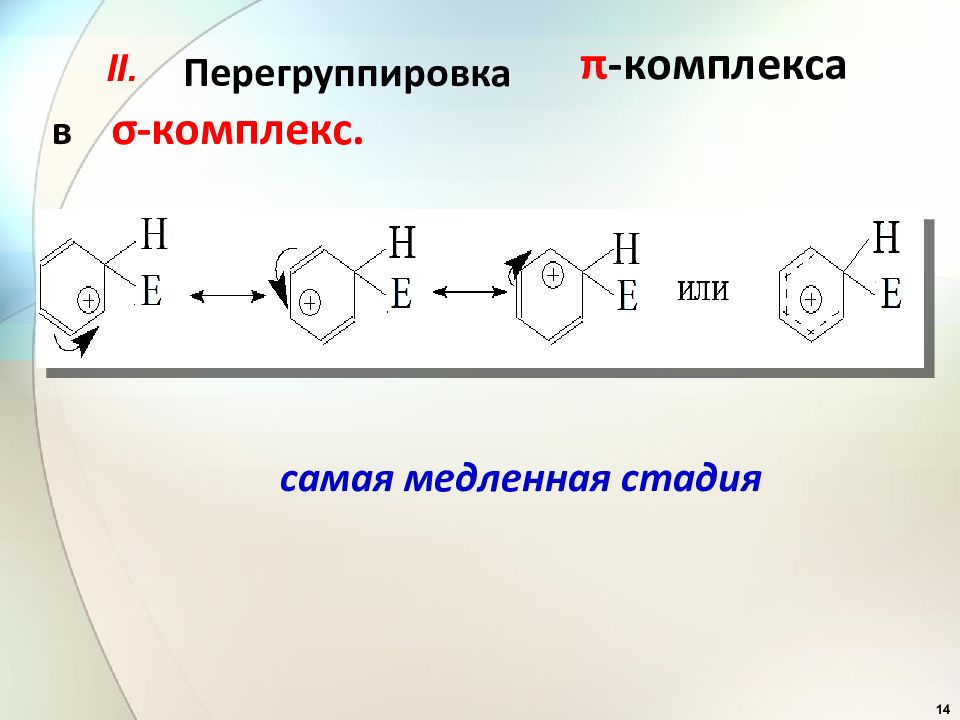
14 самая медленная стадия Перегруппировка в σ -комплекс. π -комплекса II.
Слайд 18
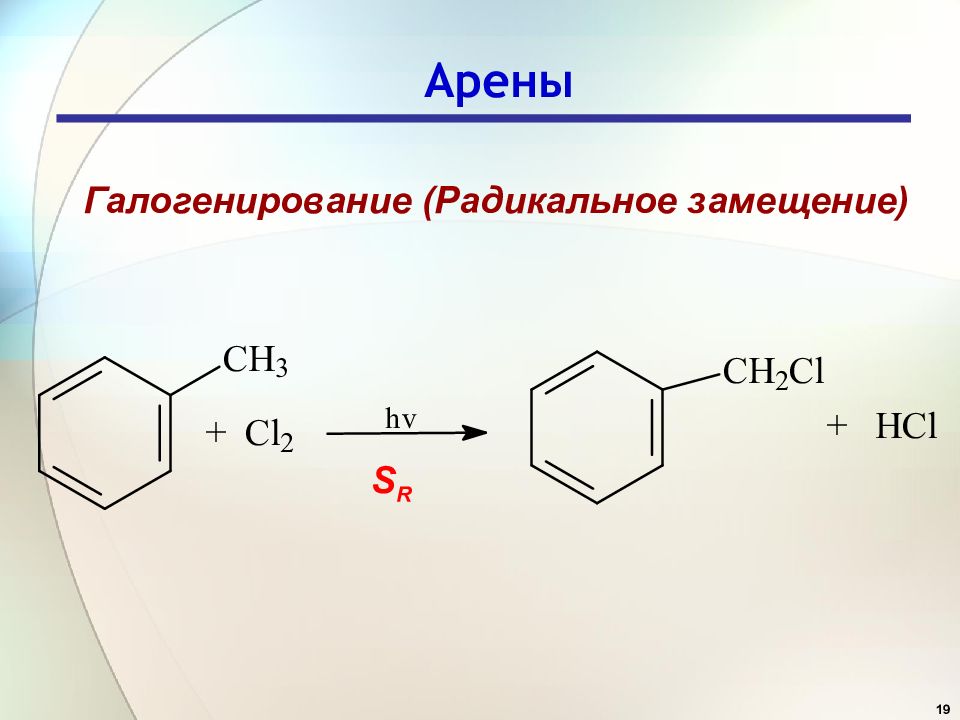
18 Для хлорирования в лабораторных условиях используют смесь HOCl с кислотой (хлор газ!): Хлорноватистая кислота
Слайд 22
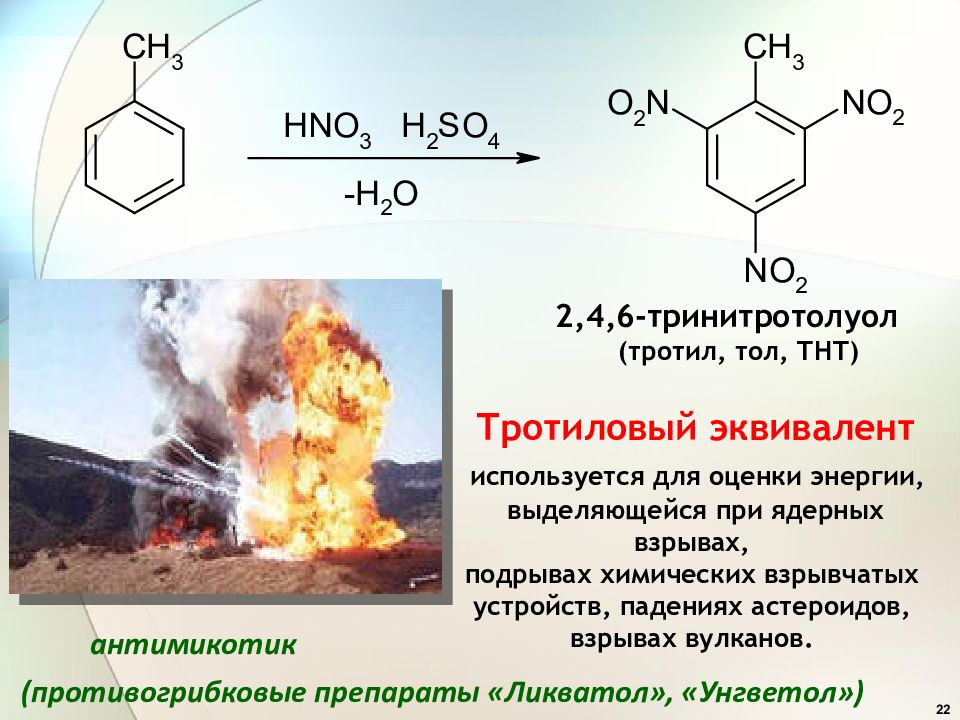
22 Тротиловый эквивалент используется для оценки энергии, выделяющейся при ядерных взрывах, подрывах химических взрывчатых устройств, падениях астероидов, взрывах вулканов. 2,4,6-тринитротолуол (тротил, тол, ТНТ) антимикотик (противогрибковые препараты « Ликватол », « Унгветол »)
Слайд 23
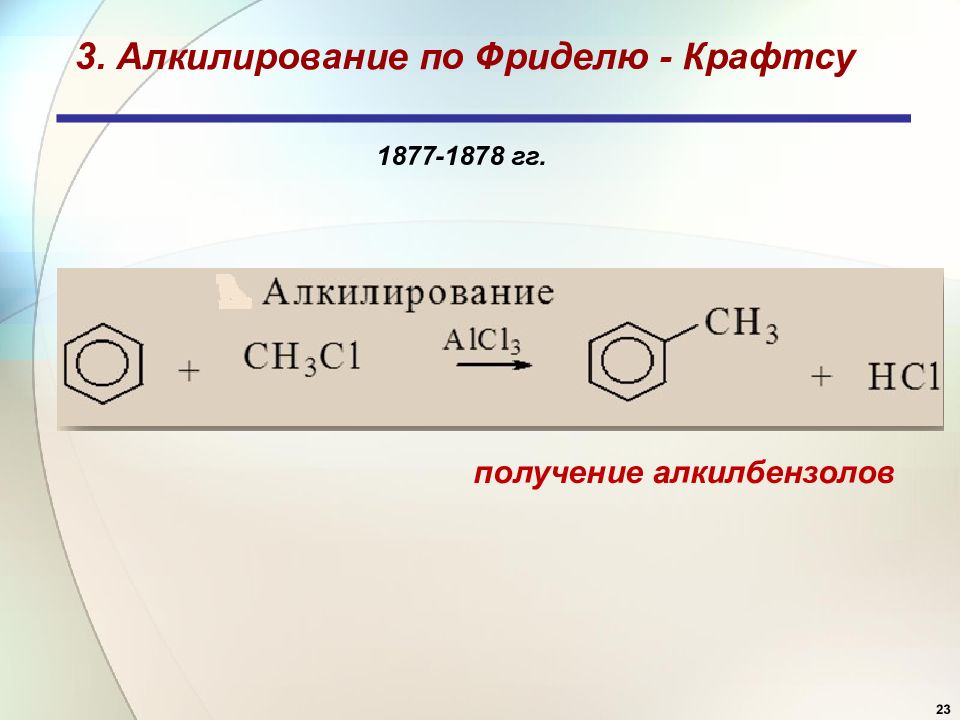
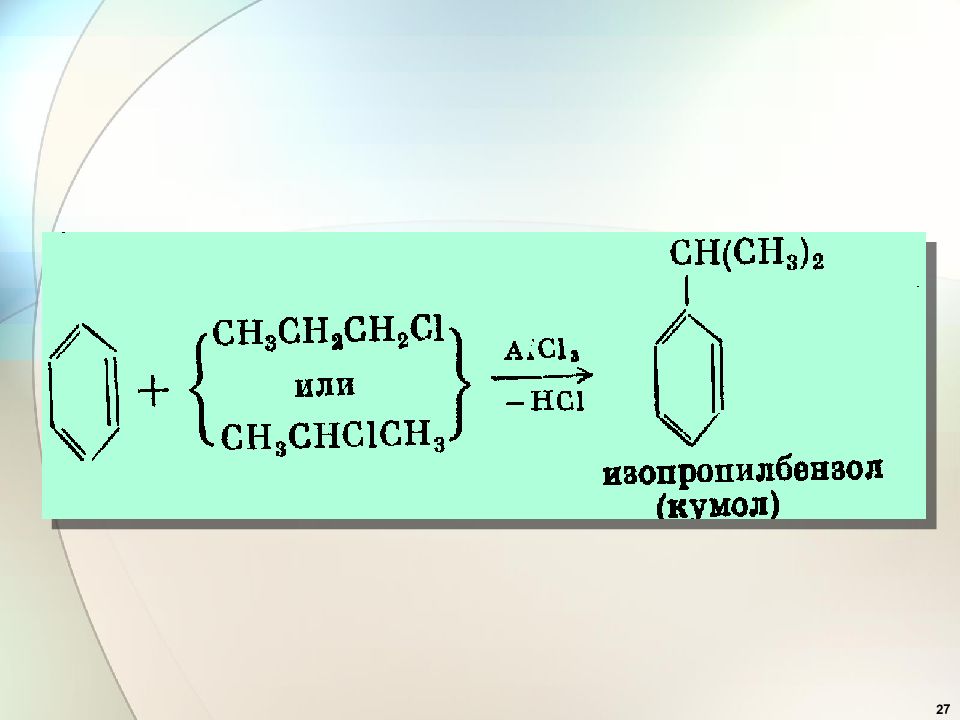
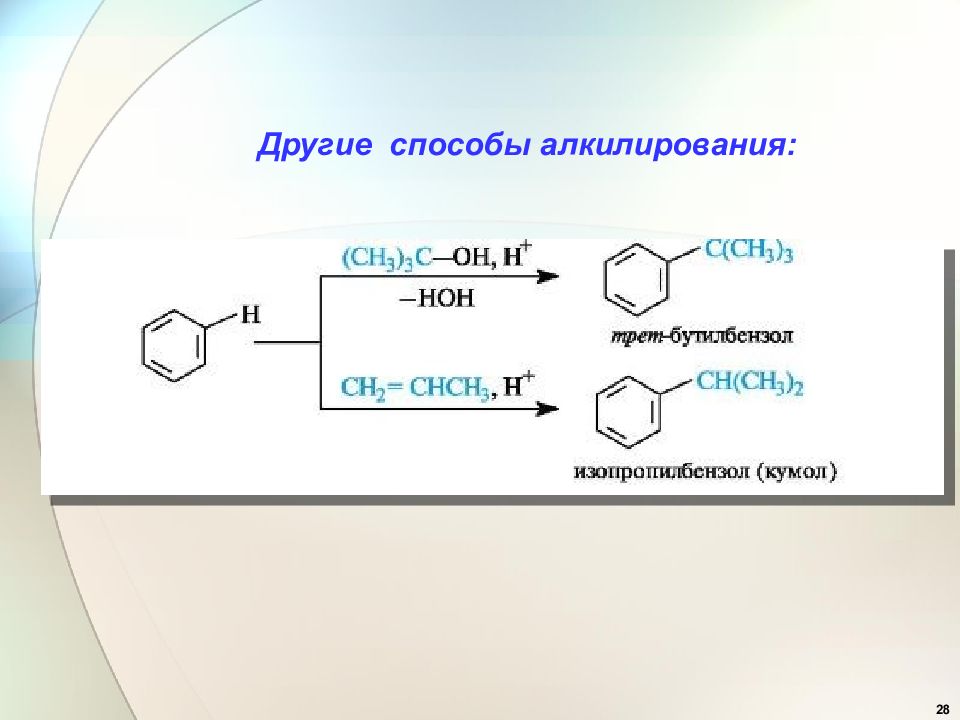
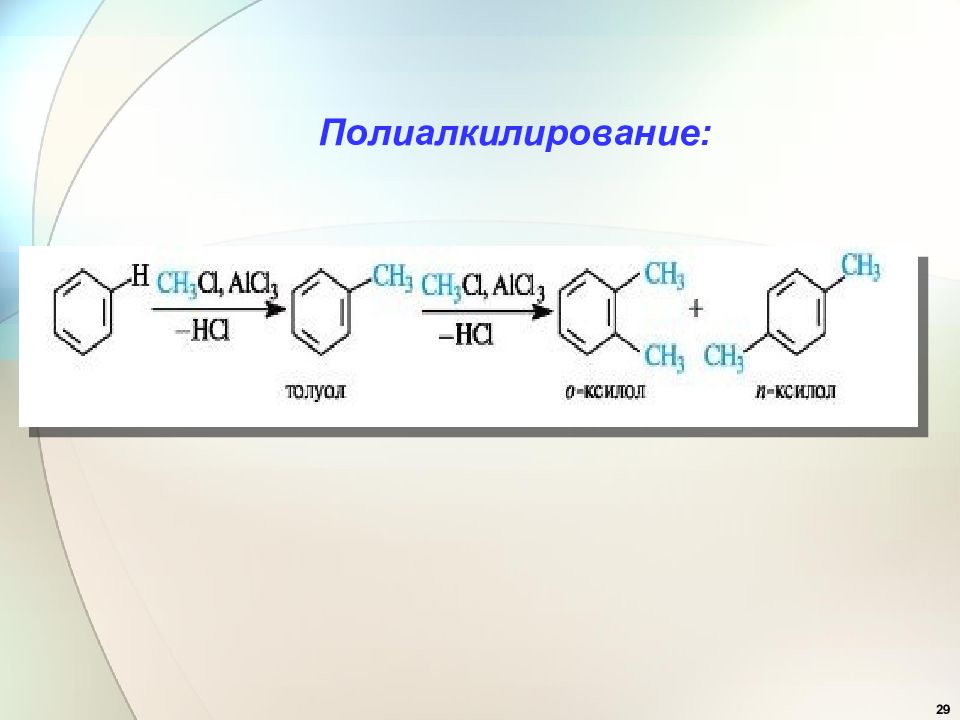
23 3. Алкилирование по Фриделю - Крафтсу 1877-1878 гг. получение алкилбензолов
Слайд 24: Реакция Фриделя — Крафтса
24 Реакция Фриделя — Крафтса Крафтс (Crafts) Джеймс Мейсон (8.3.1839 — 20.6.1917, США) Фридель ( Friedel ) Шарль (12.3.1832 — 20.4.1899, Франция) Страница из блокнота Фриделя
Слайд 26
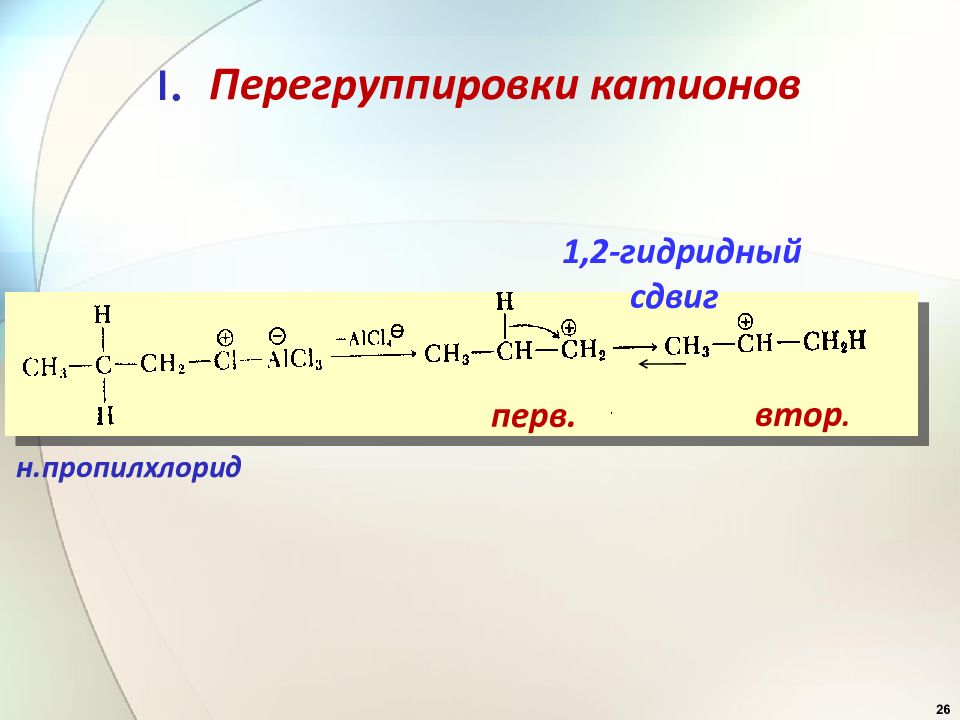
26 Перегруппировки катионов н.пропилхлорид I. перв. втор. 1,2-гидридный сдвиг
Слайд 30
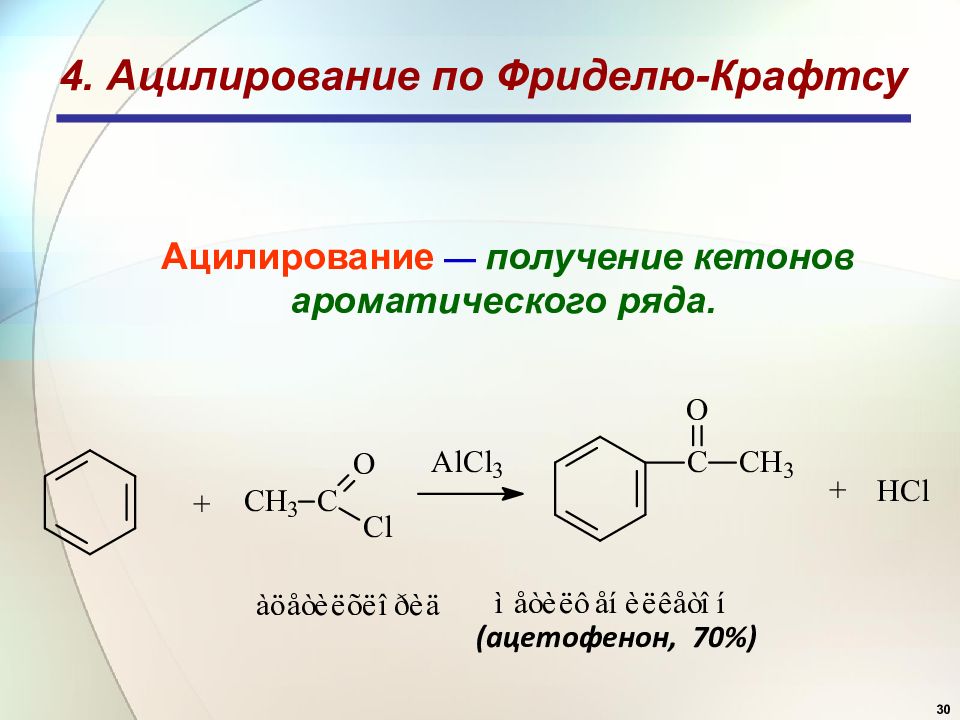
30 4. Ацилирование по Фриделю-Крафтсу Ацилирование — получение кетонов ароматического ряда. ( ацетофенон, 70%)
Слайд 31: Ацилирование
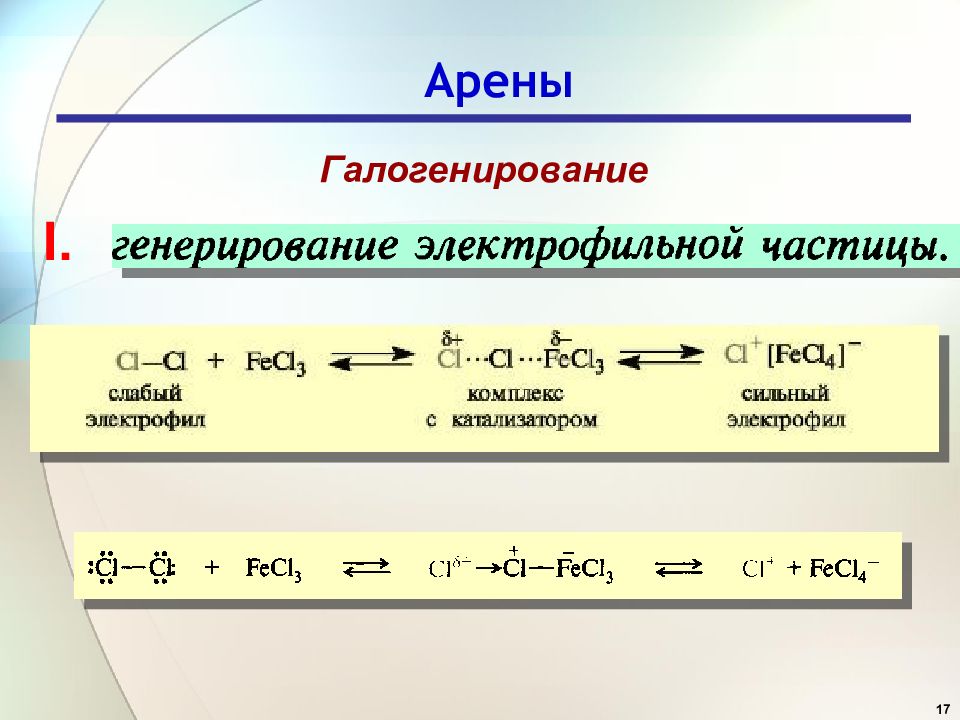
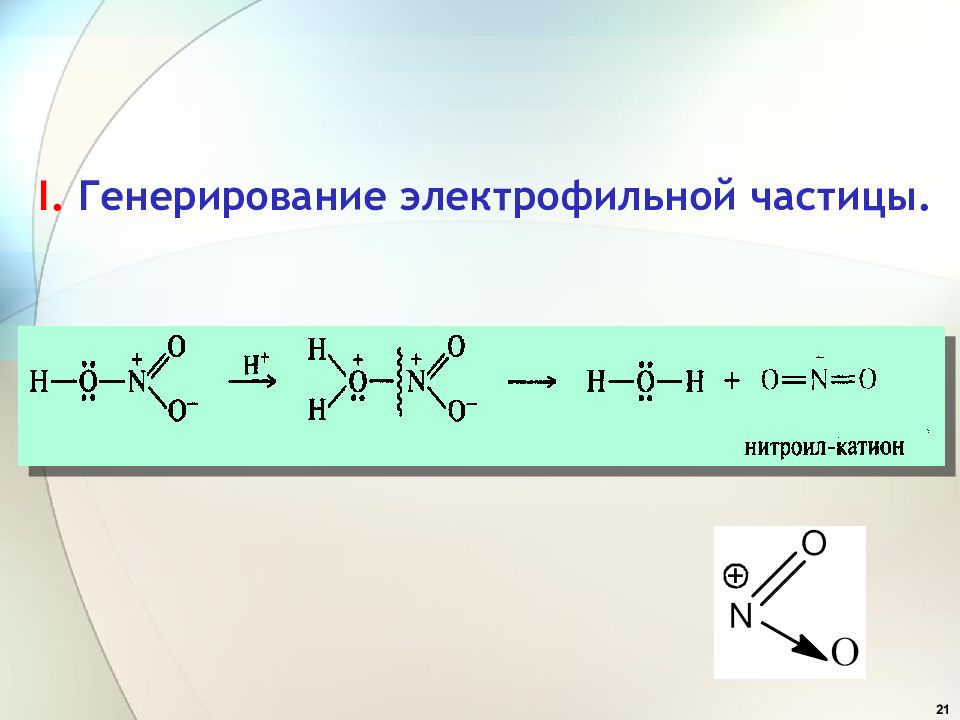
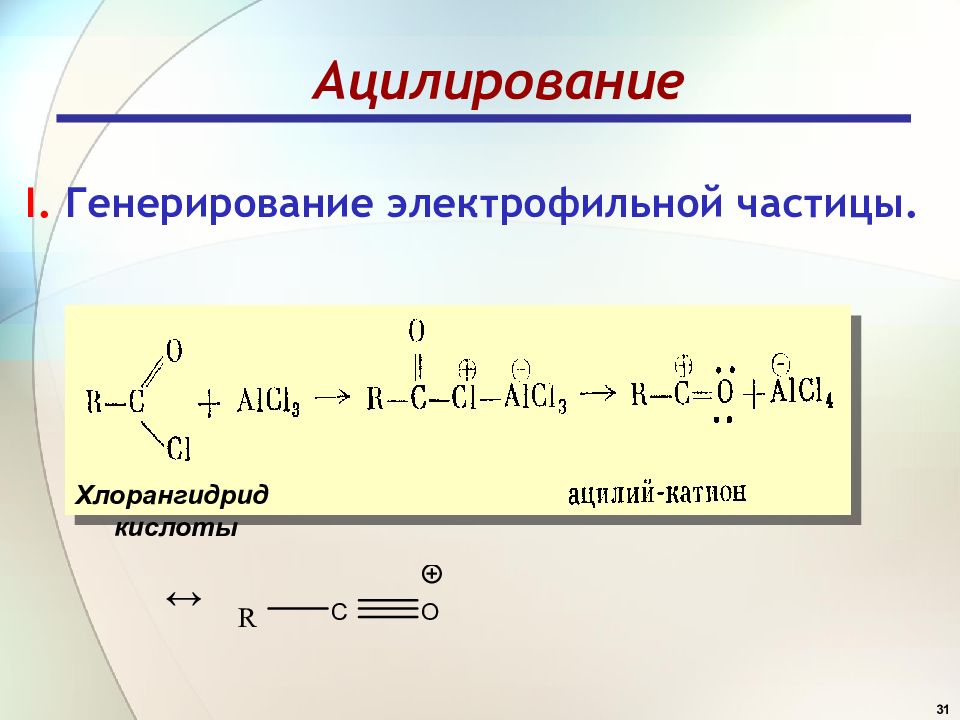
31 Ацилирование ↔ I. Генерирование электрофильной частицы. Хлорангидрид кислоты
Слайд 36
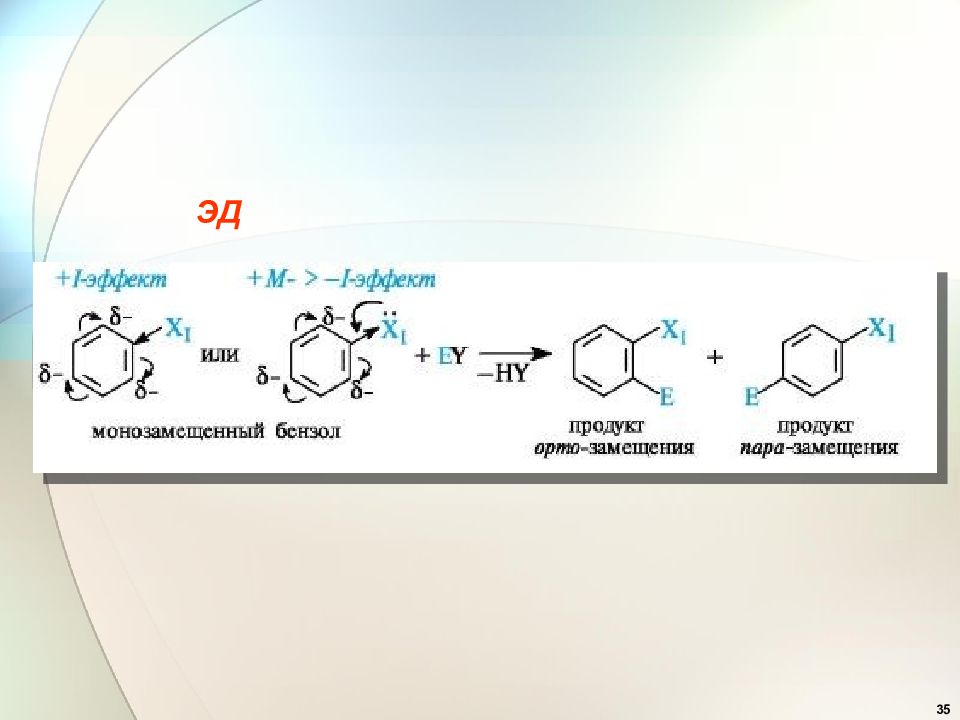
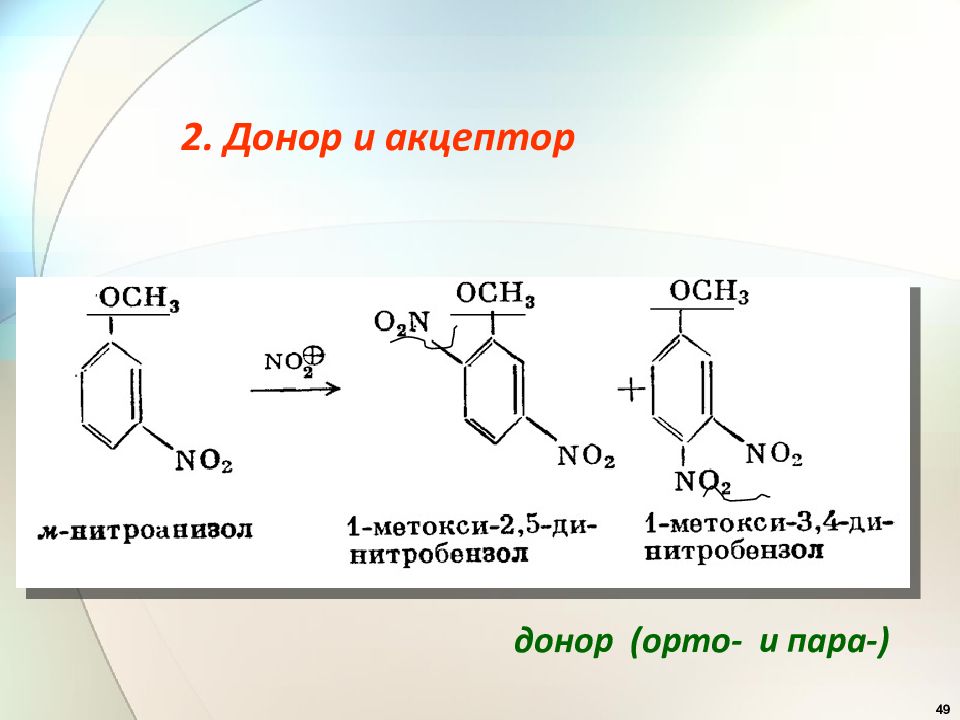
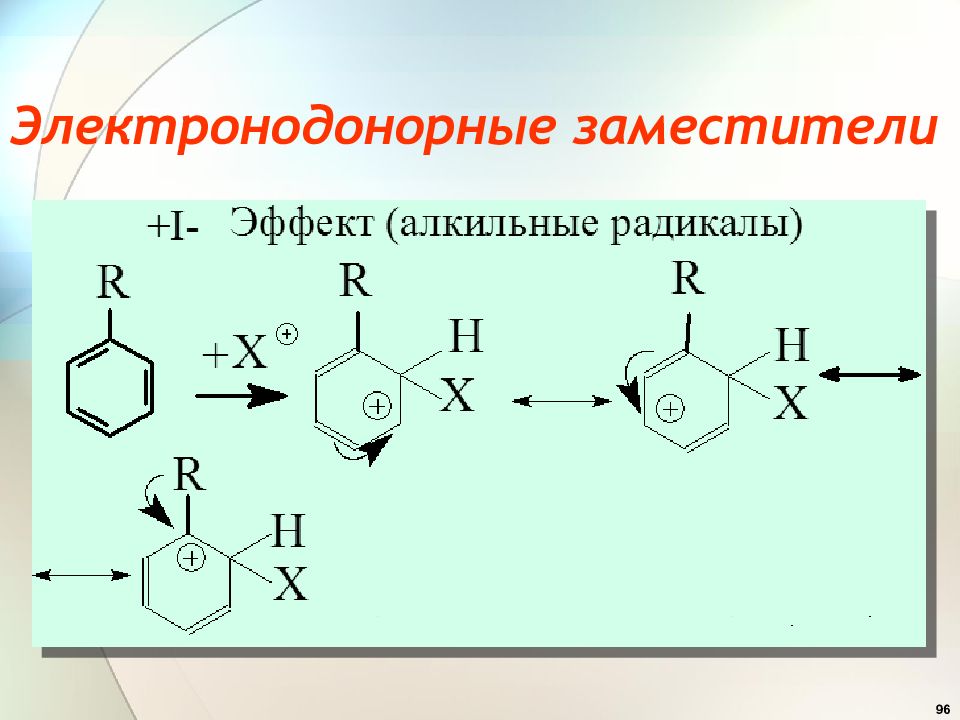
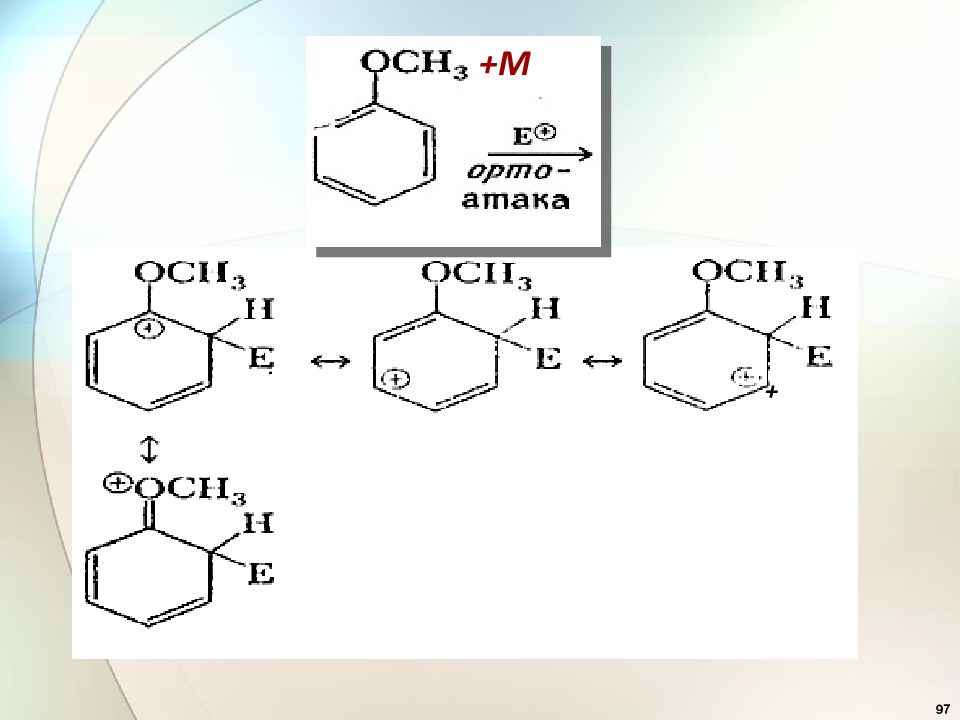
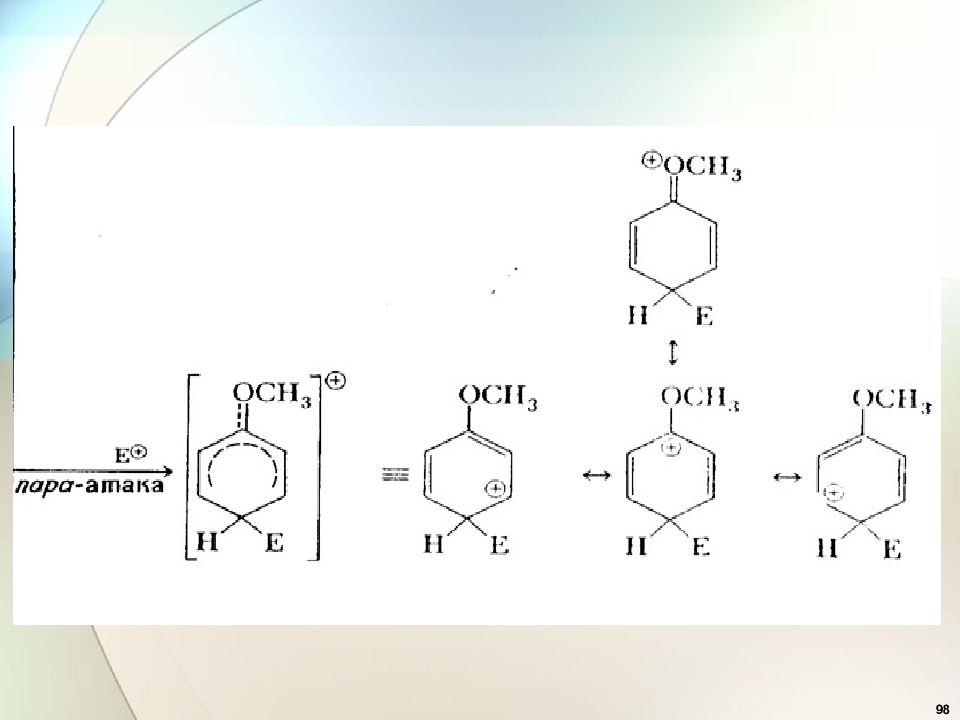
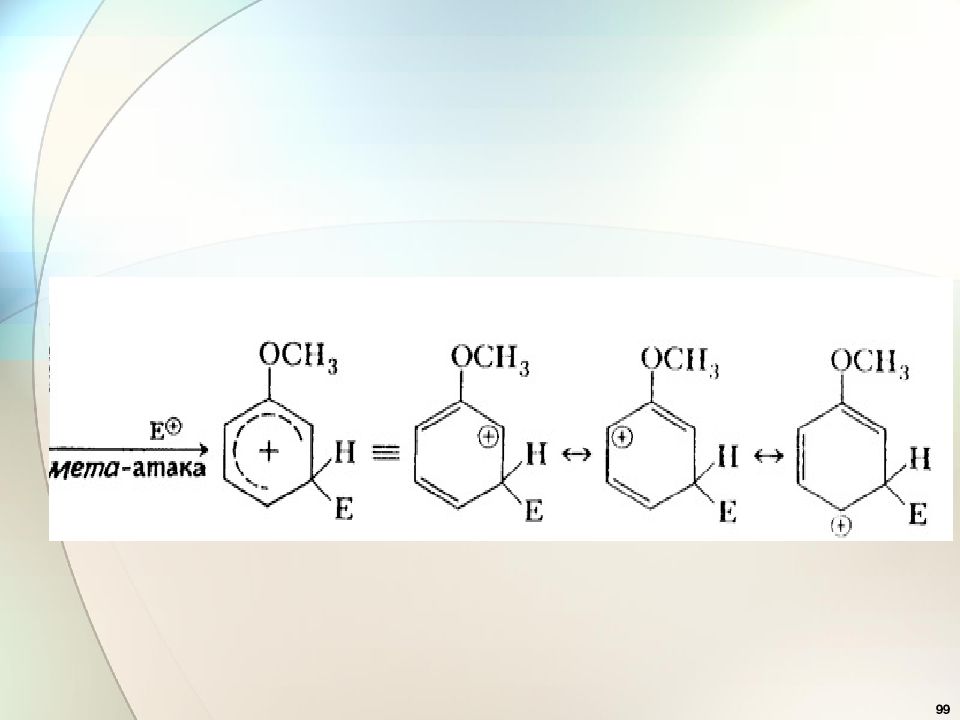
36 Эффекты заместителей при электрофильном замещении Заместители ( ориентанты ) первого рода (доноры) : — ОН, — OR, — OCOR, — SH, - SR, — NH 2, — NHR, -NR 2, -NHCOCH 3, -Alk, – C 6 H 5, Они активируют бензольное кольцо и ориентируют новый заместитель в орто - и пара-положения ( орто - и пара- ориентанты ). .
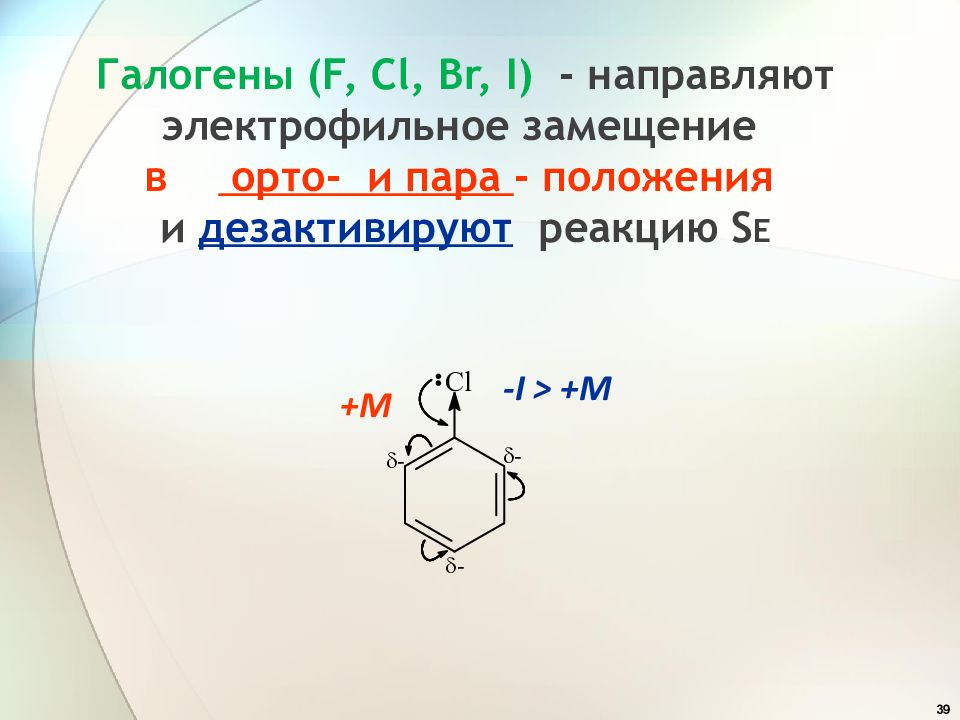
Слайд 39: Галогены ( F, Cl, Br, I ) - н аправляют электрофильное замещение в орто - и пара - положения и дезактивируют реакцию S E
39 Галогены ( F, Cl, Br, I ) - н аправляют электрофильное замещение в орто - и пара - положения и дезактивируют реакцию S E +М - I > +M
Слайд 41
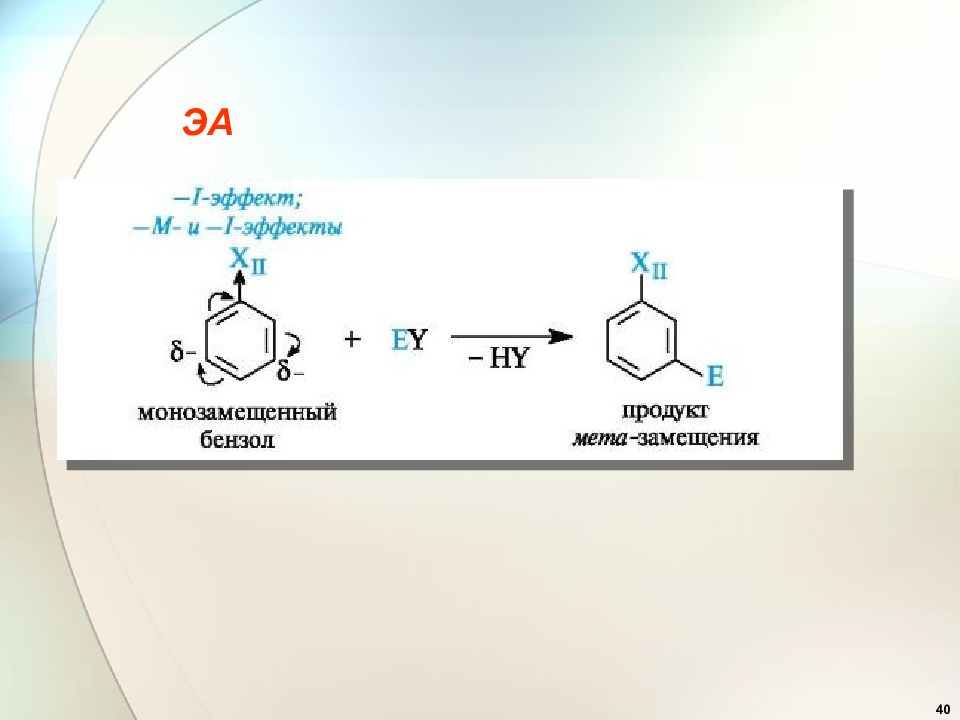
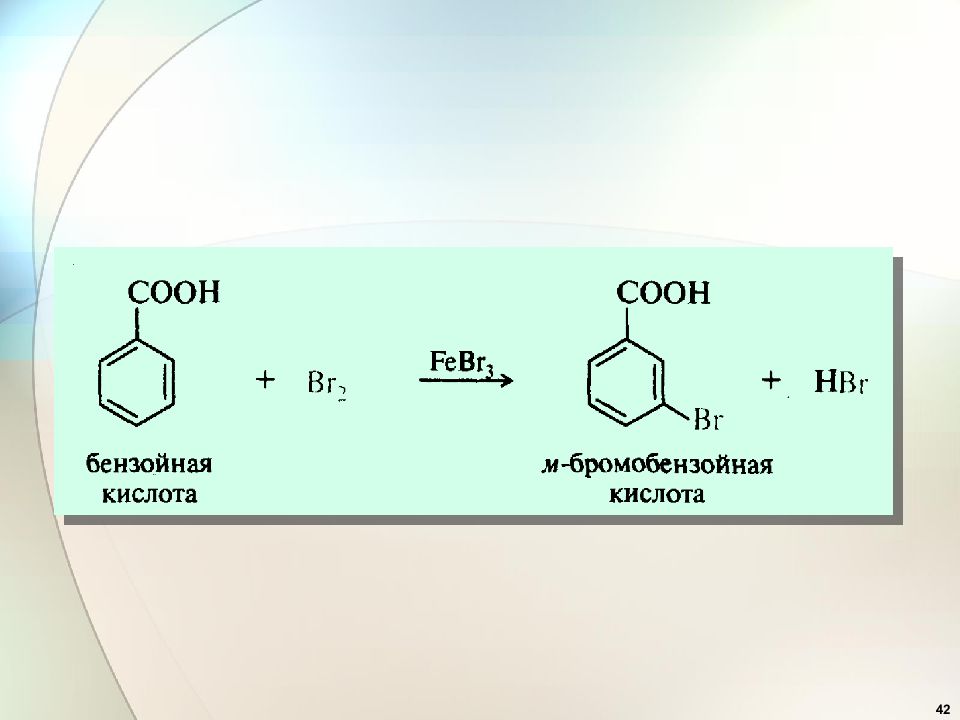
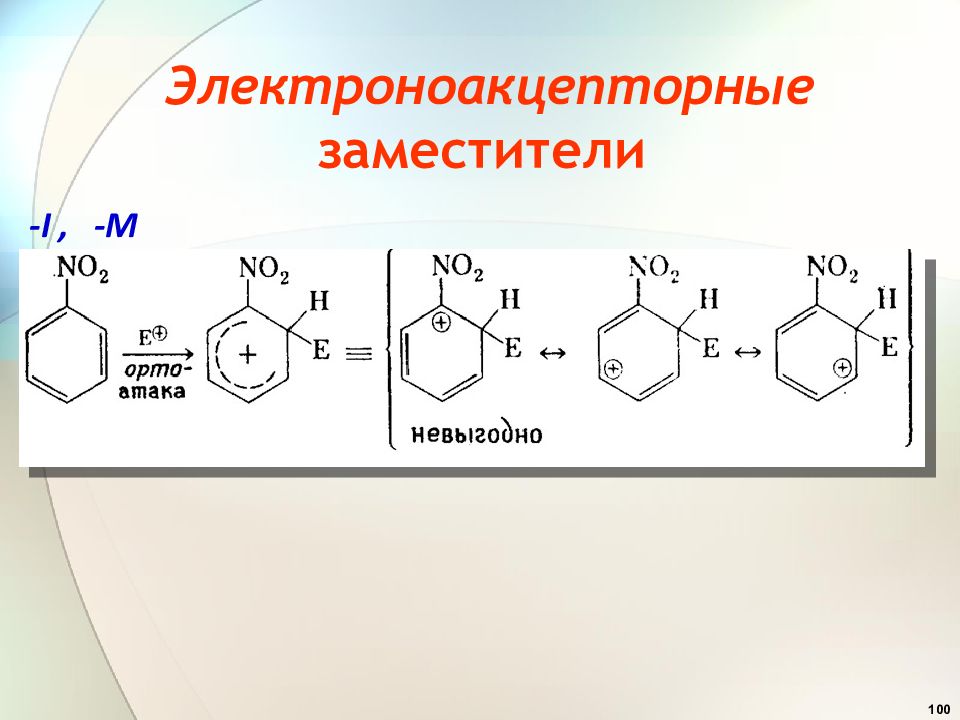
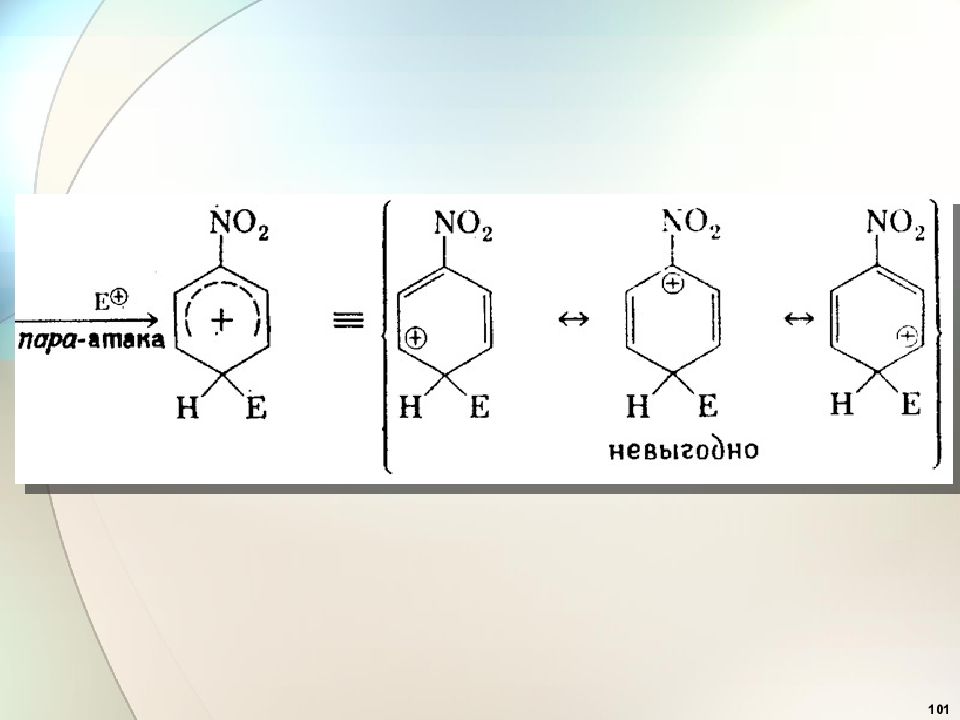
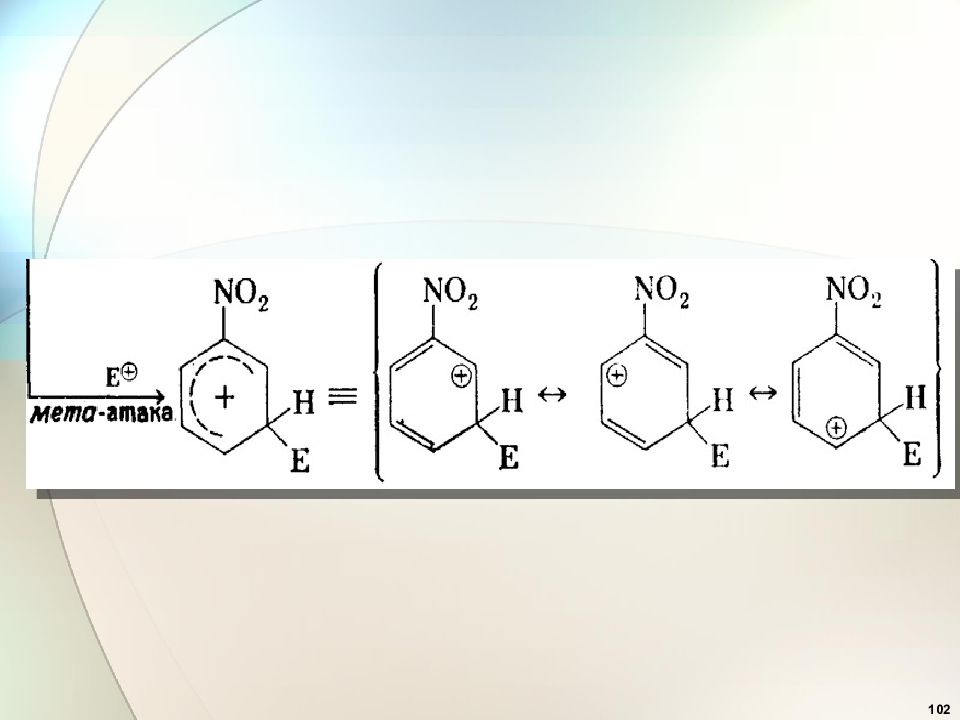
41 Эффекты заместителей при электрофильном замещении 2. Заместители ( ориентанты ) второго рода (акцепторы) : — CN, —СООН, — SO 3 H, —СНО, — COR, — COOR, — NO 2 дезактивируют бензольное кольцо и вновь входящий заместитель ориентируют в мета-положение ( мета- ориентанты ).
Слайд 43: Арены
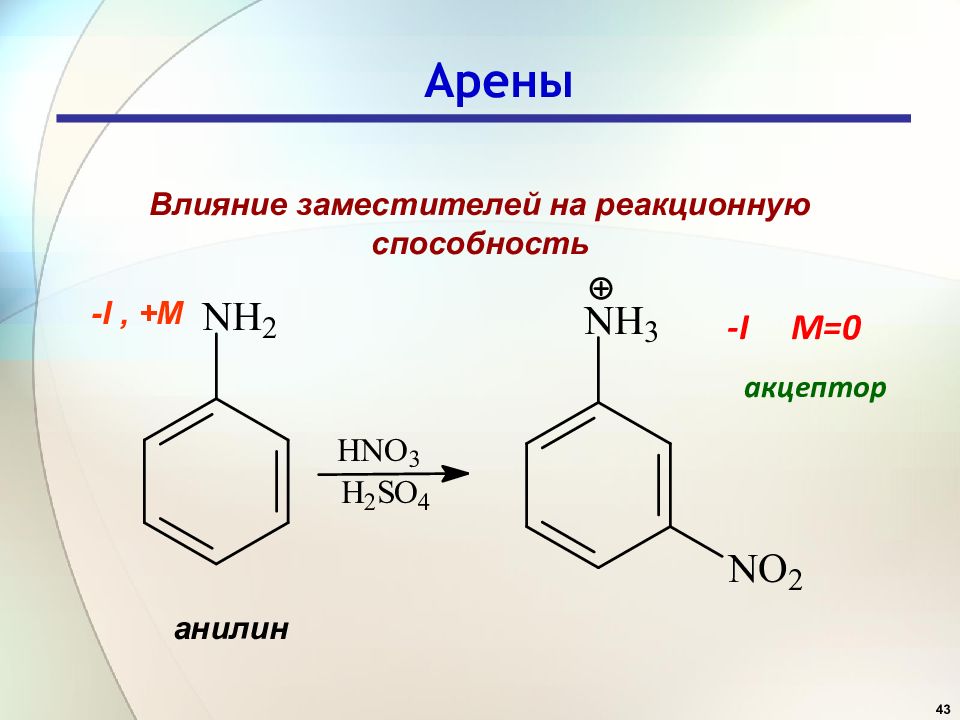
43 Арены Влияние заместителей на реакционную способность -I M=0 акцептор анилин -I, +M
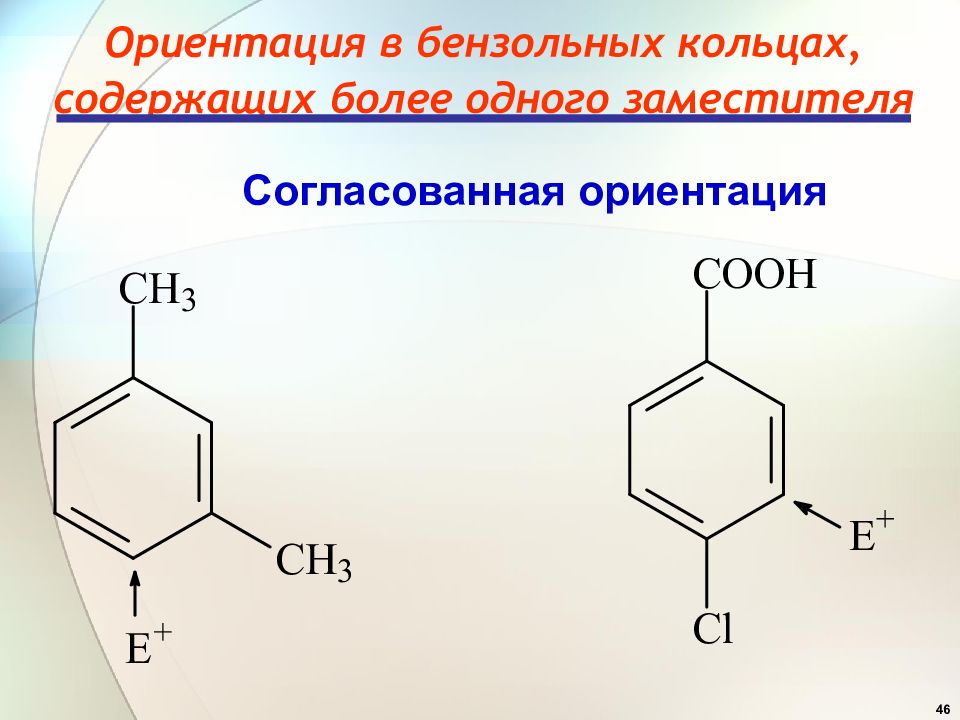
Слайд 46: Ориентация в бензольных кольцах, содержащих более одного заместителя
46 Ориентация в бензольных кольцах, содержащих более одного заместителя Согласованная ориентация
Слайд 48
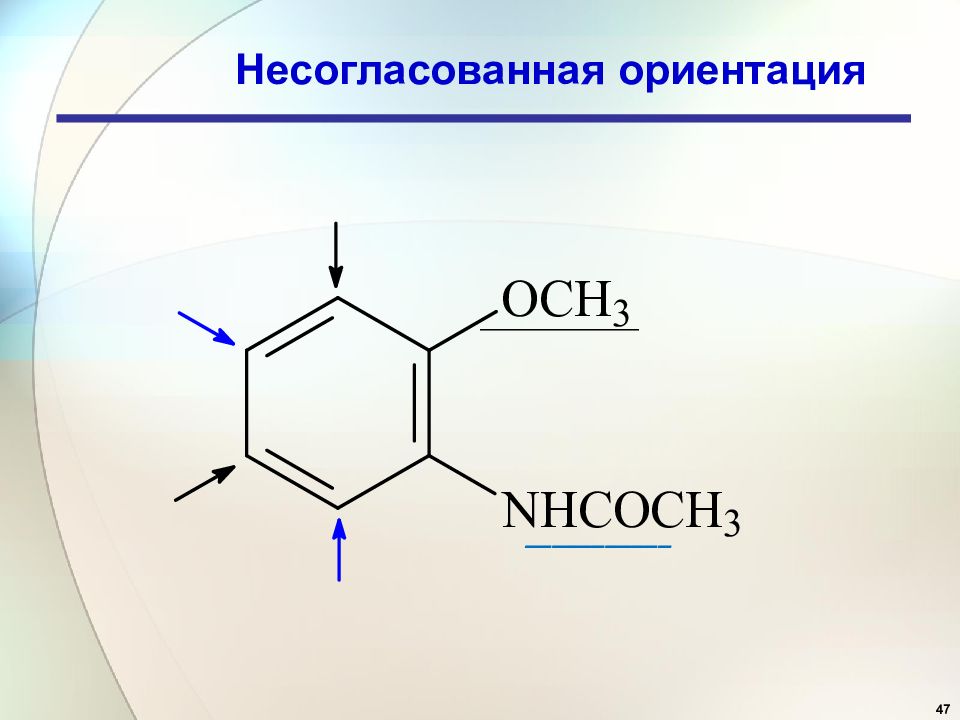
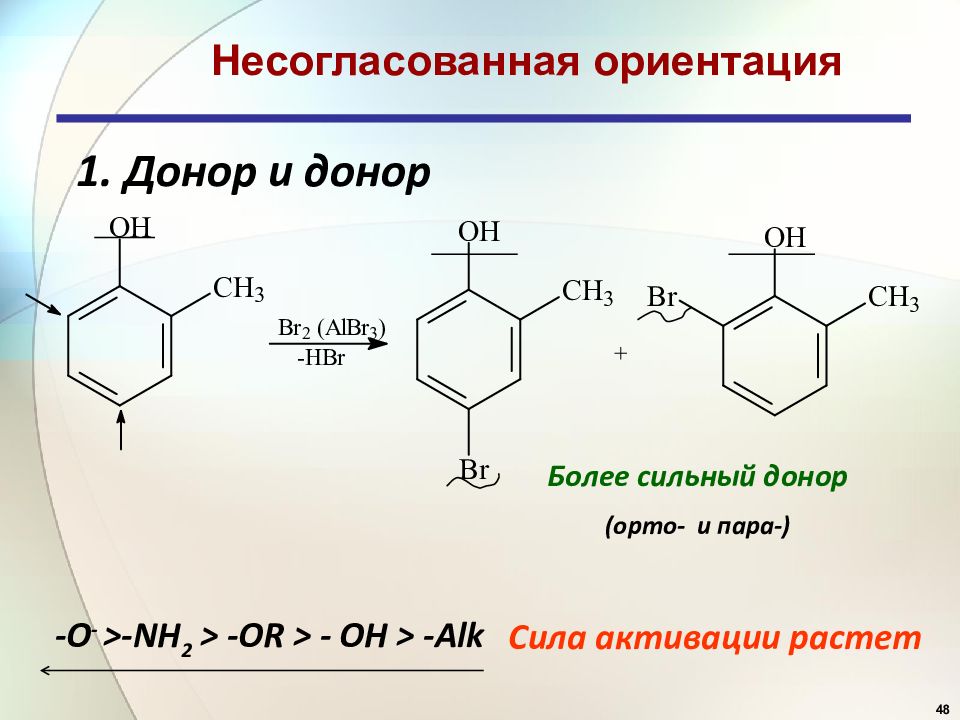
48 1. Донор и донор Несогласованная ориентация Более сильный донор ( орто - и пара-) - O - >- NH 2 > - OR > - OH > - Alk Сила активации растет
Слайд 50
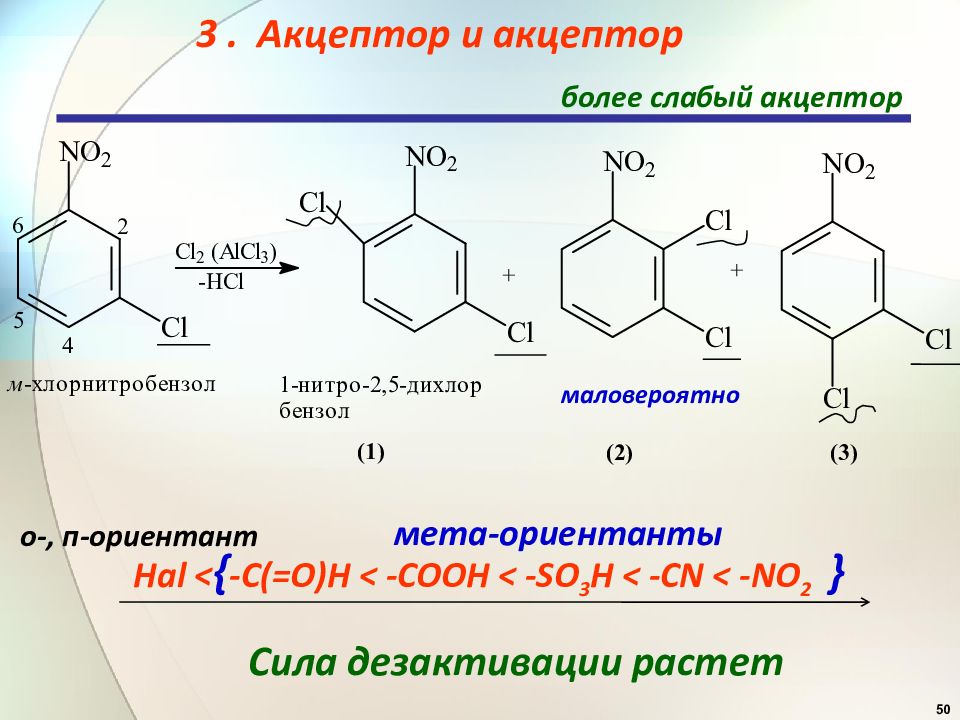
50 3. Акцептор и акцептор более слабый акцептор маловероятно Hal < { -C (=O)H < -COOH < -SO 3 H < -CN < - NO 2 } Сила дезактивации растет мета- ориентанты о-, п- ориентант
Слайд 53: Многоядерные ароматические соединения
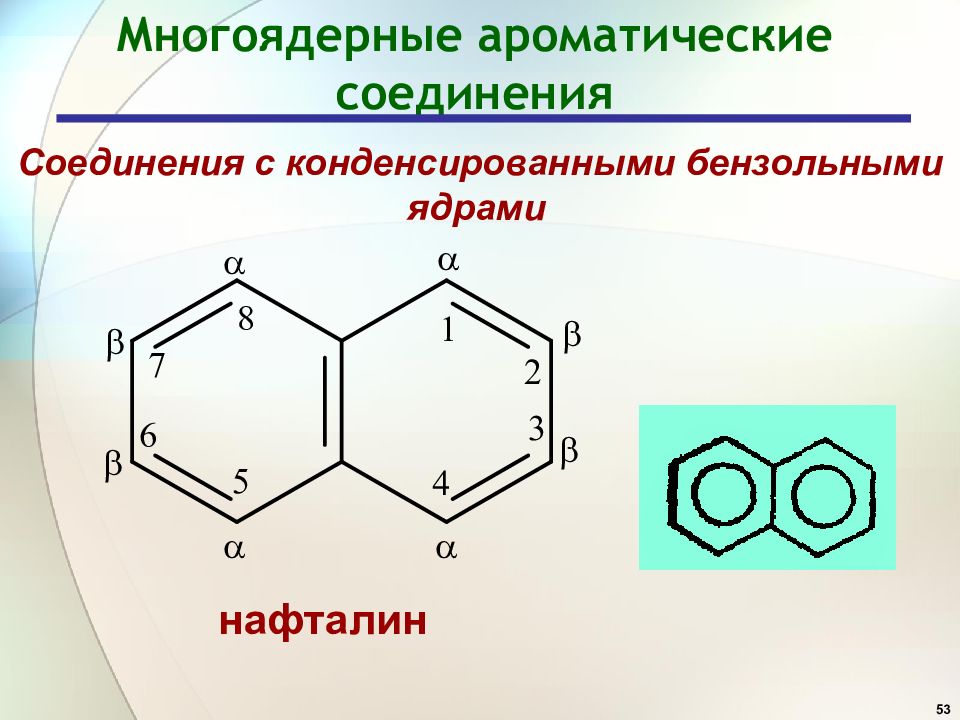
53 Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами нафталин
Слайд 54
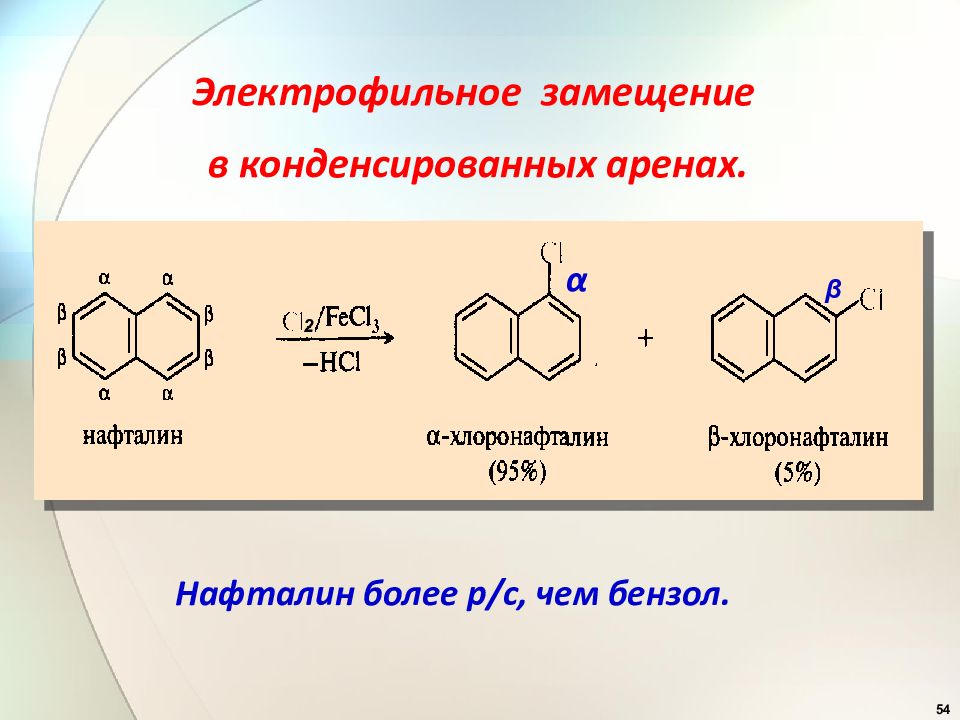
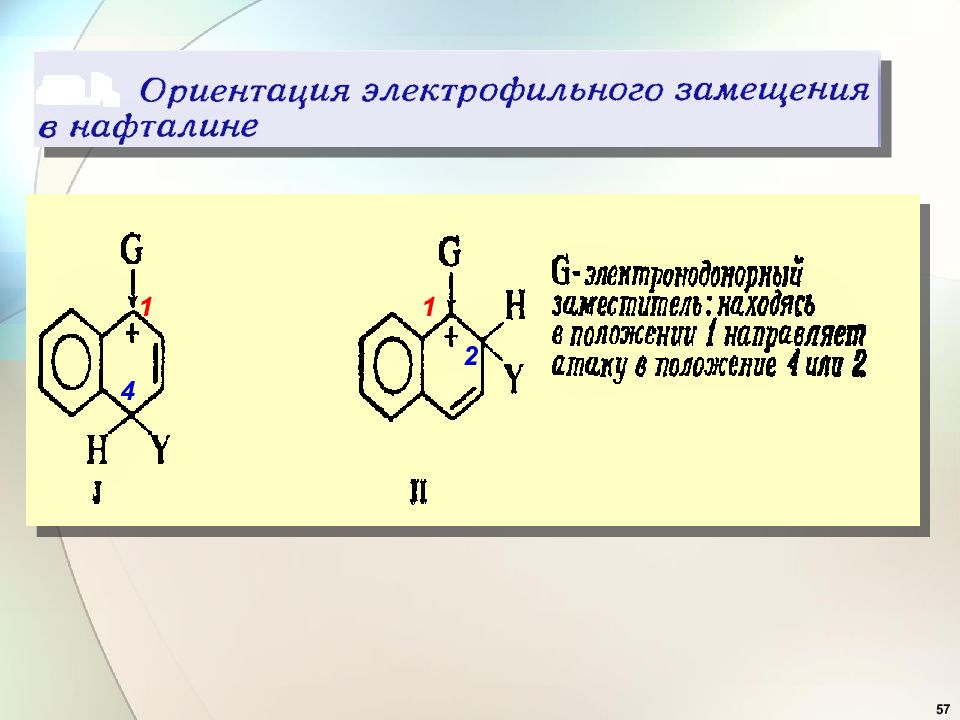
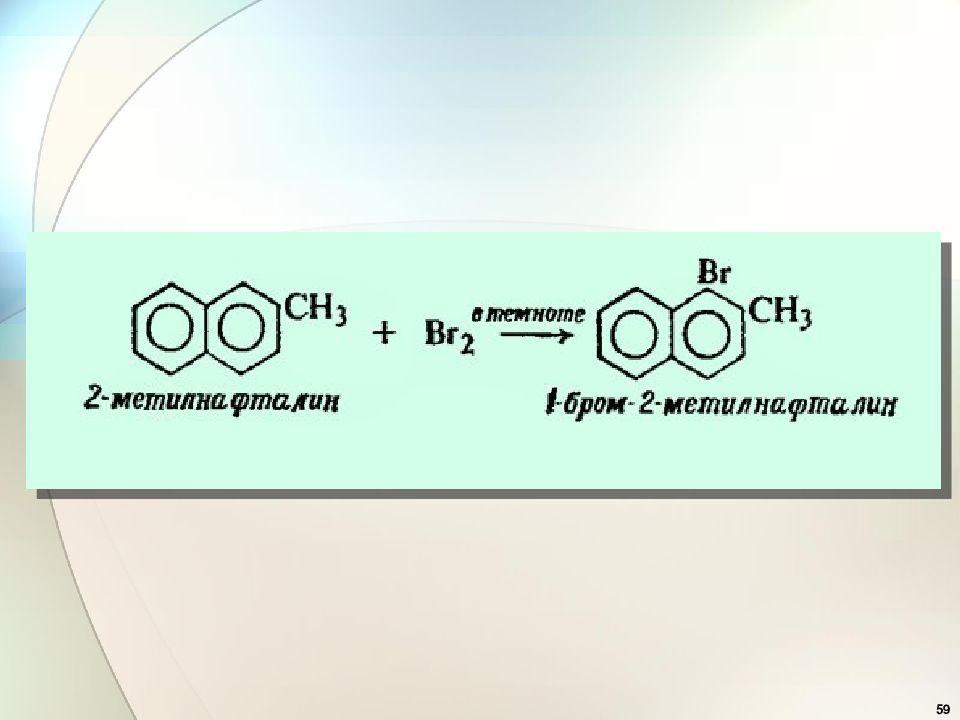
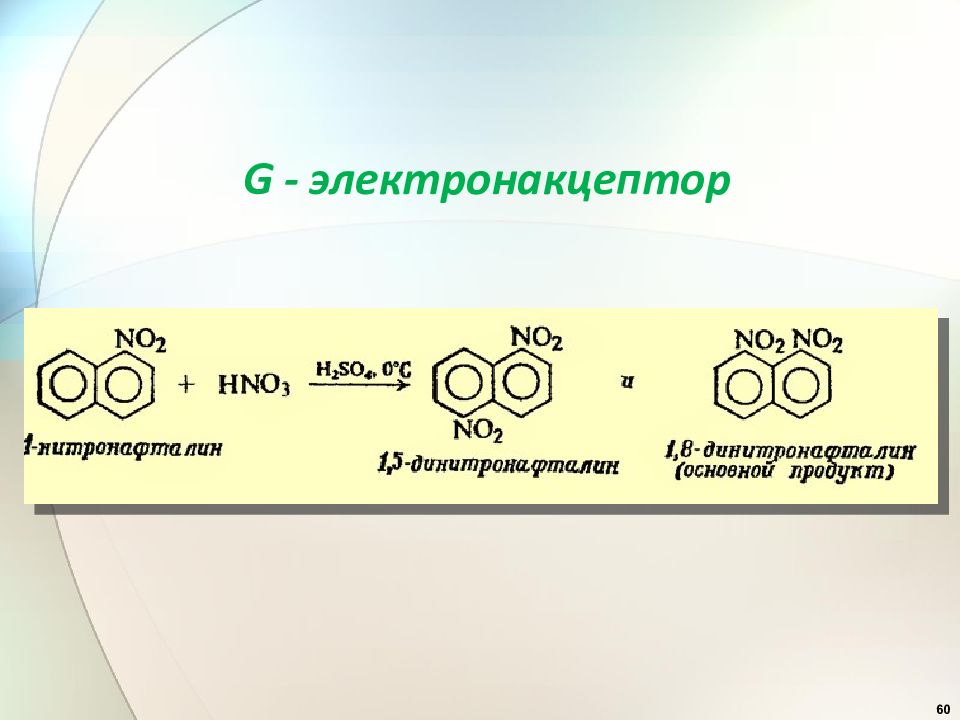
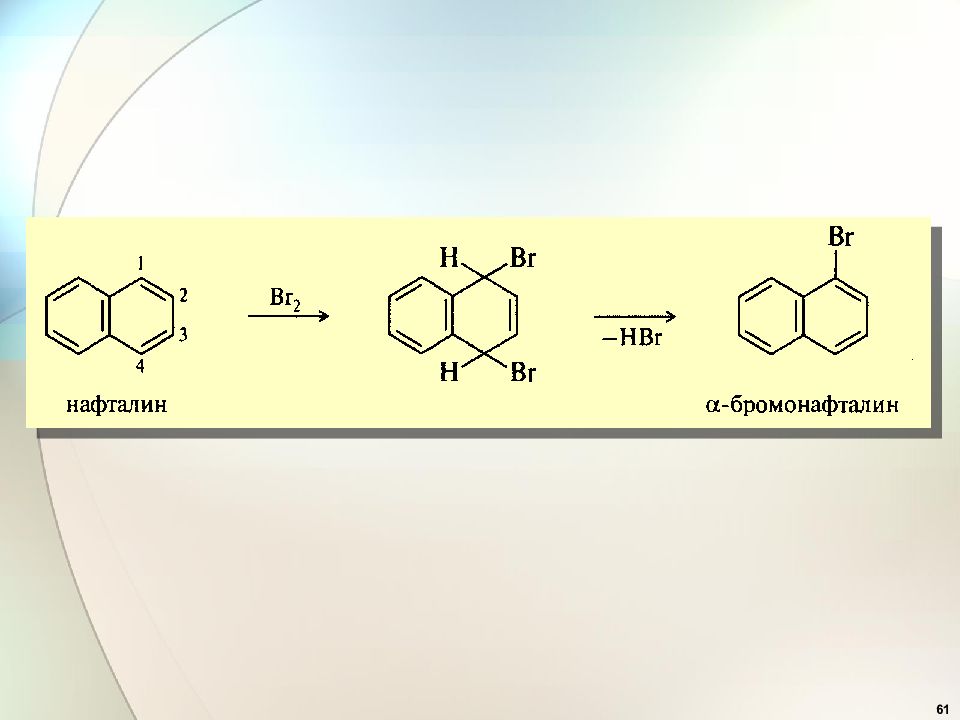
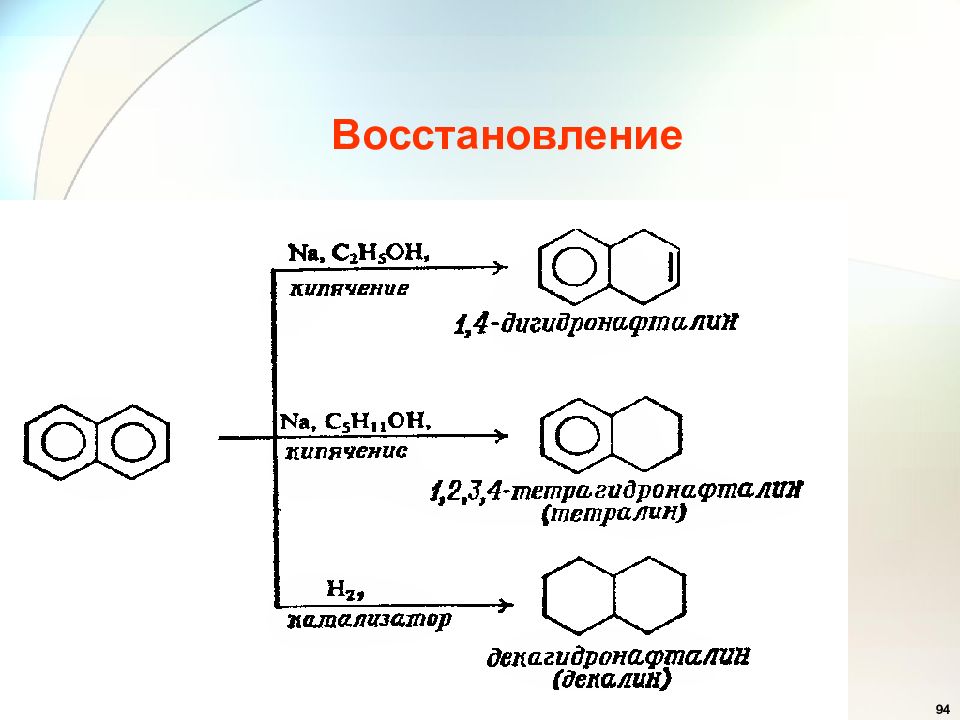
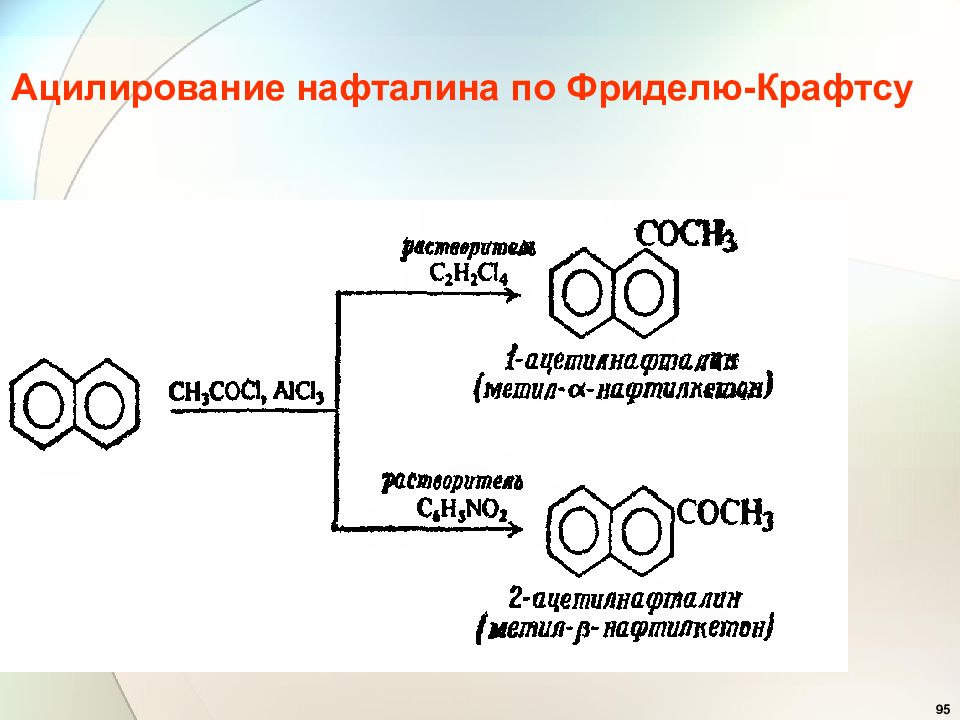
54 Электрофильное замещение в конденсированных аренах. Нафталин более р/с, чем бензол. α β 2
Слайд 55
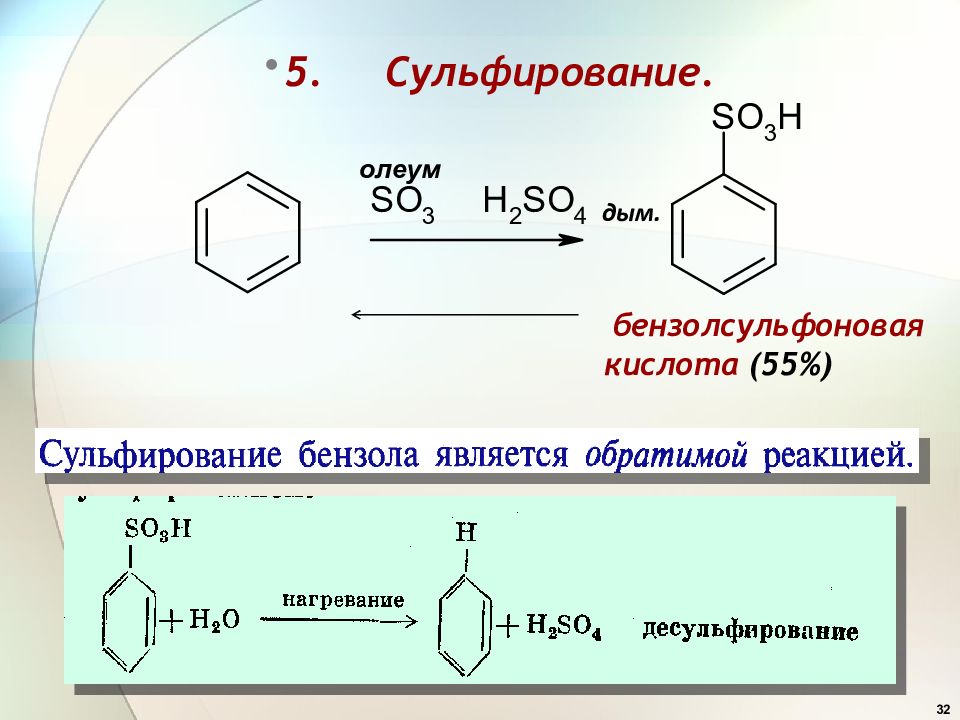
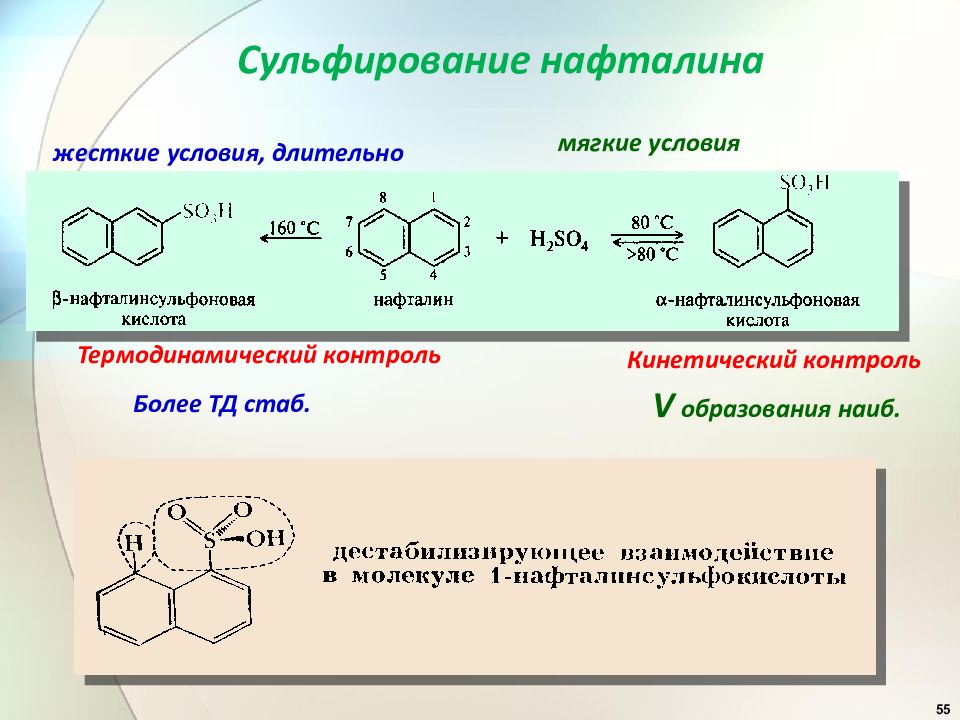
55 Кинетический контроль Термодинамический контроль мягкие условия жесткие условия, длительно V образования наиб. Более ТД стаб. Сульфирование нафталина
Слайд 66
66 28.02.2014 66 Физические и биологические свойства аренов. Бензпирен – мощный канцероген !
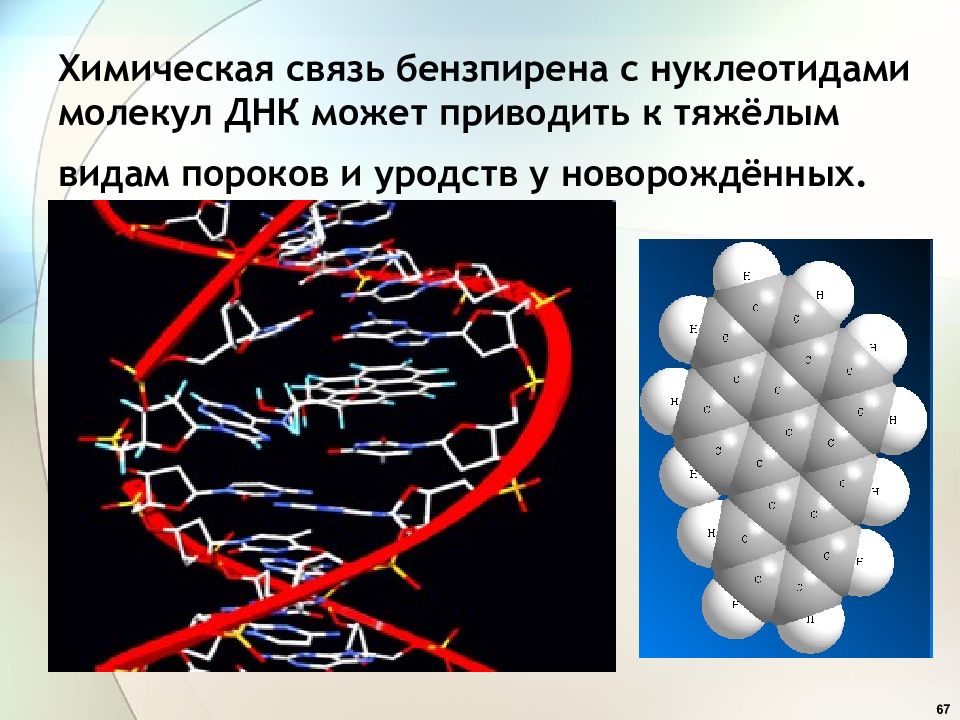
Слайд 67: Химическая связь бензпирена с нуклеотидами молекул ДНК может приводить к тяжёлым видам пороков и уродств у новорождённых
67 Химическая связь бензпирена с нуклеотидами молекул ДНК может приводить к тяжёлым видам пороков и уродств у новорождённых.
Слайд 68
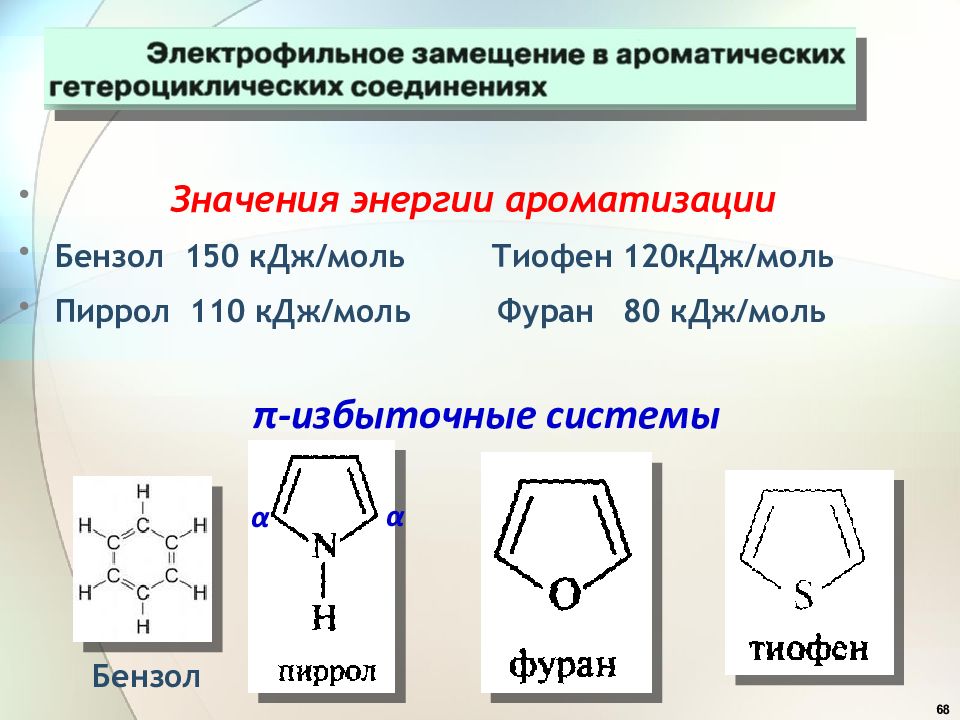
68 Значения энергии ароматизации Бензол 150 кДж/моль Тиофен 120кДж/моль Пиррол 110 кДж/моль Фуран 80 кДж/моль π-избыточные системы Бензол α α
Слайд 69
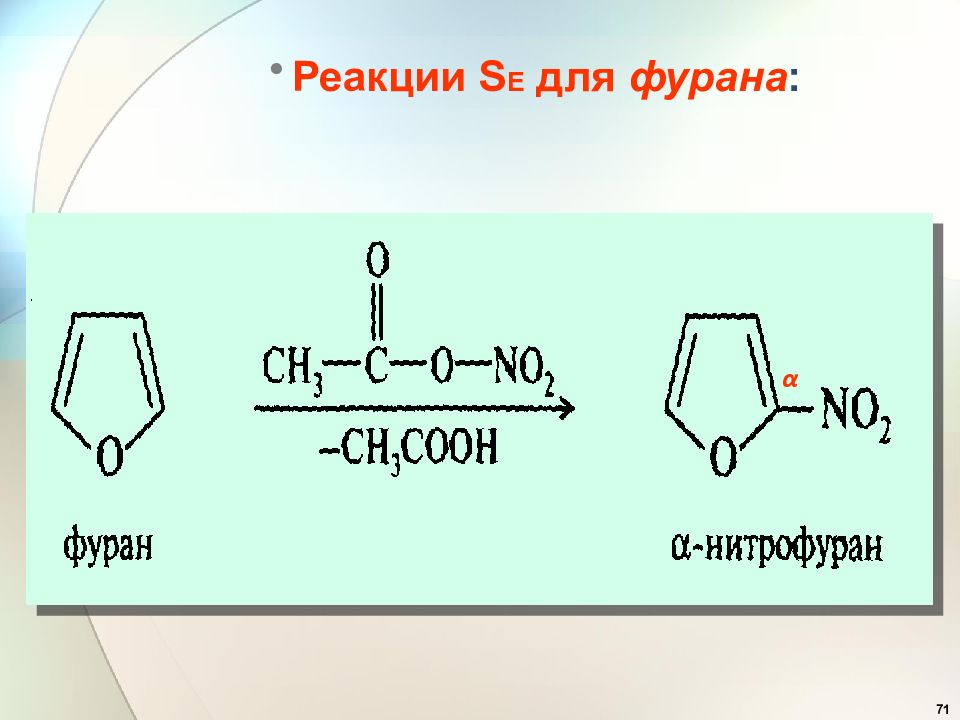
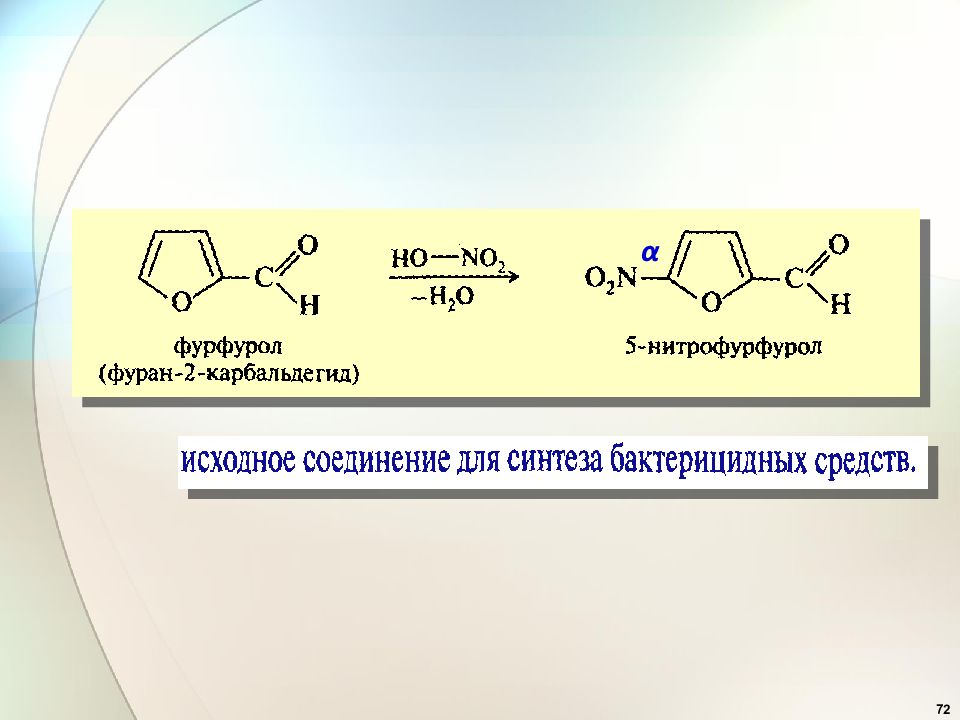
69 Ацидофобность – нестабильность в сильнокислой среде пиррольных и фурановых ядер.
Слайд 70
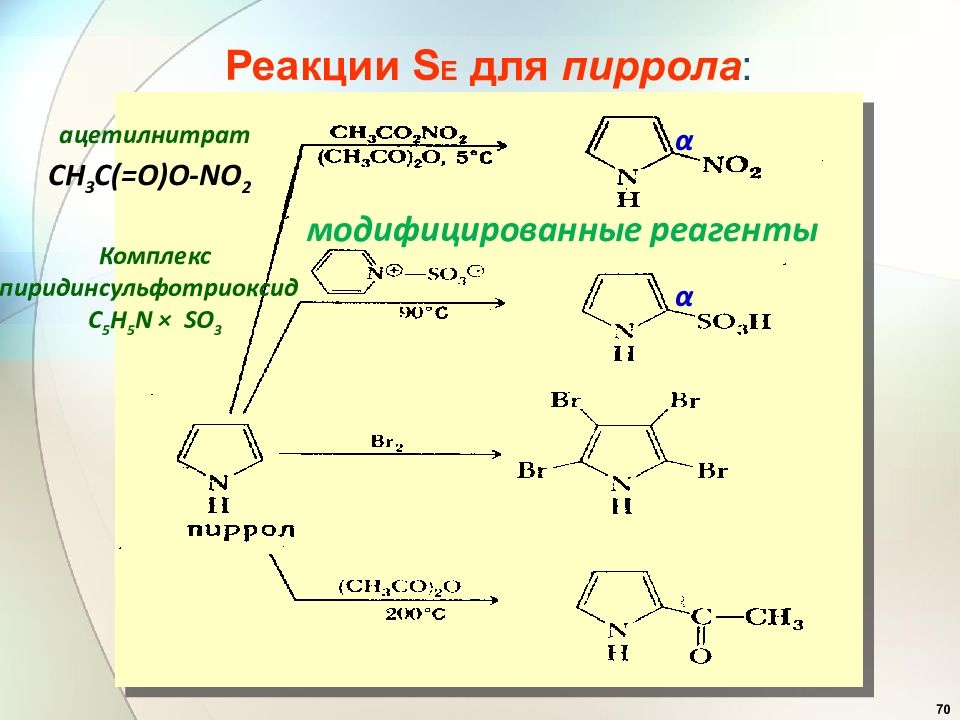
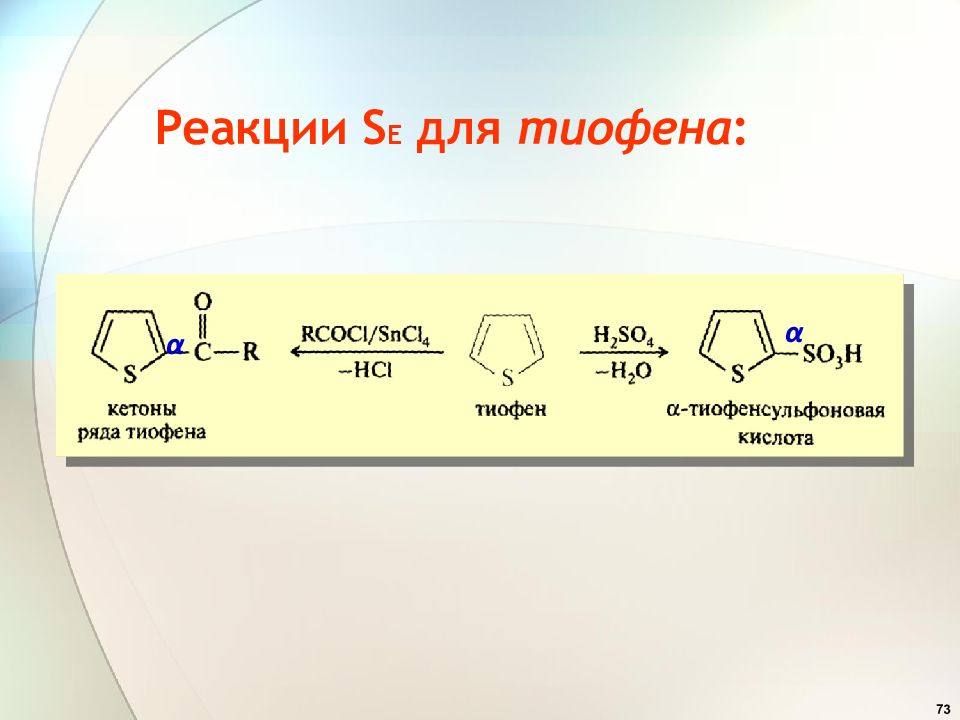
70 Реакции S E для пиррола : модифицированные реагенты α ацетилнитрат CH 3 C(=O)O-NO 2 α Комплекс пиридинсульфотриоксид C 5 H 5 N × SO 3
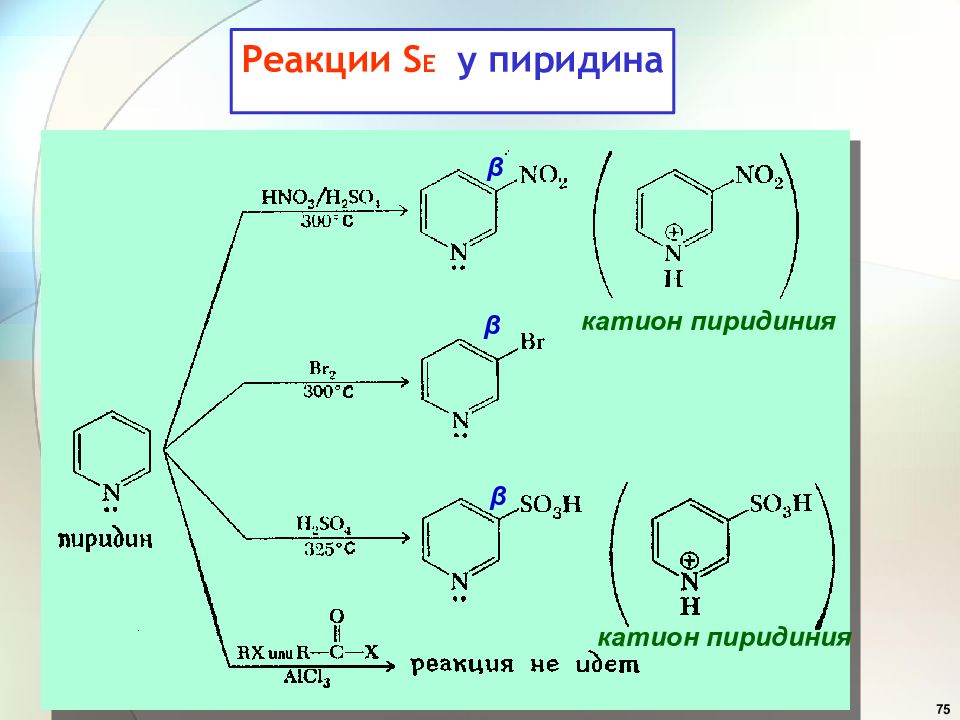
Слайд 77: Реакции нуклеофильного замещения, S N у пиридина
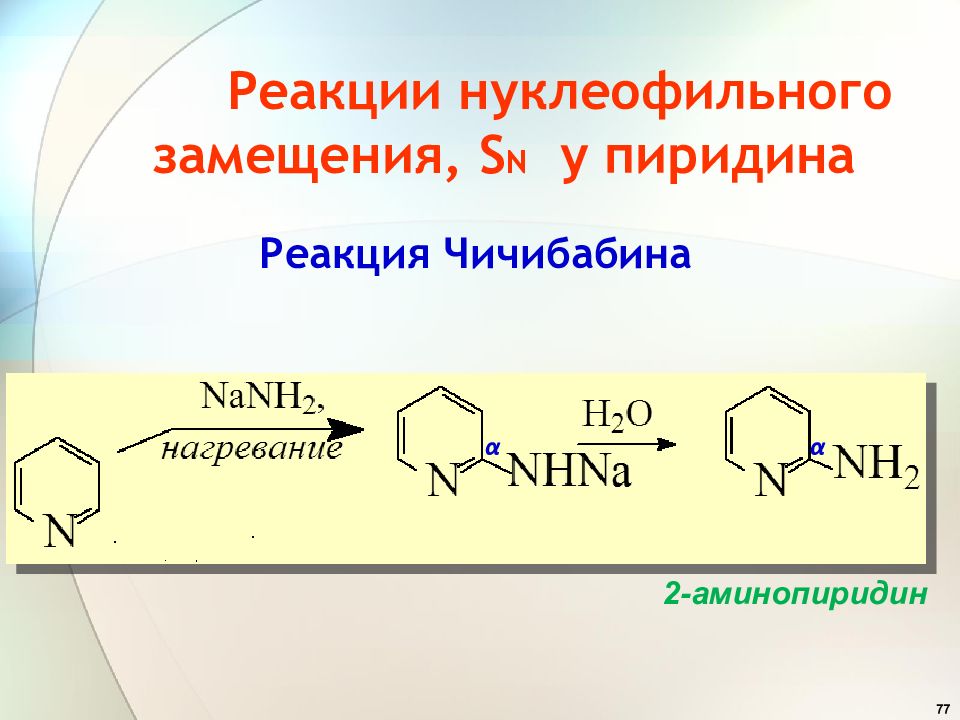
77 Реакции нуклеофильного замещения, S N у пиридина Реакция Чичибабина α α 2-аминопиридин
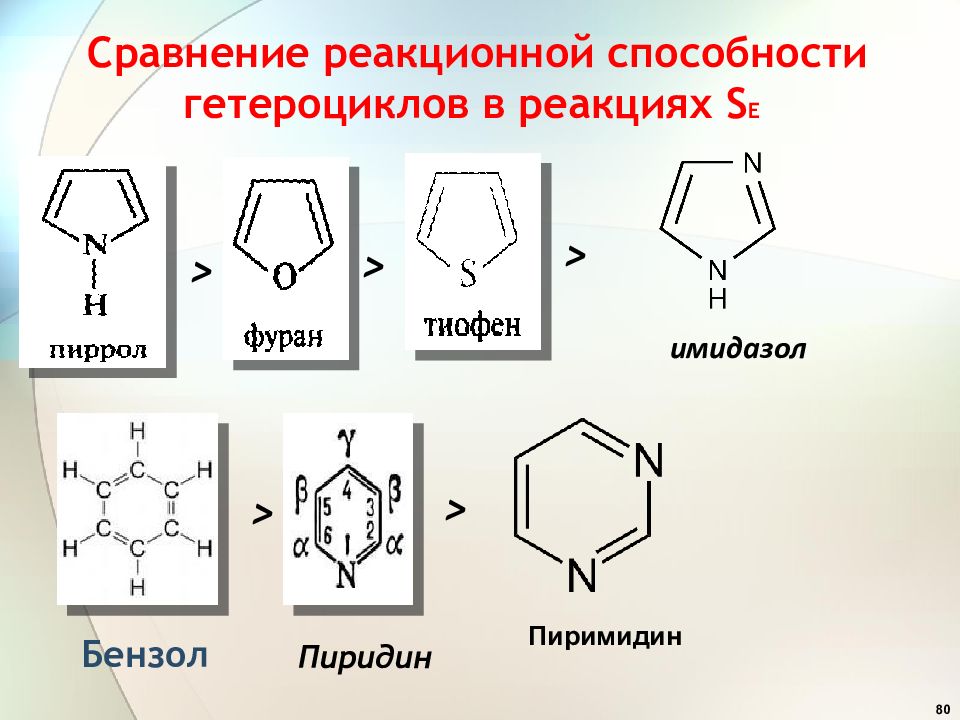
Слайд 80: Сравнение реакционной способности гетероциклов в реакциях S E
80 Бензол Пиридин Пиримидин > > > > > имидазол
Слайд 83: Арены
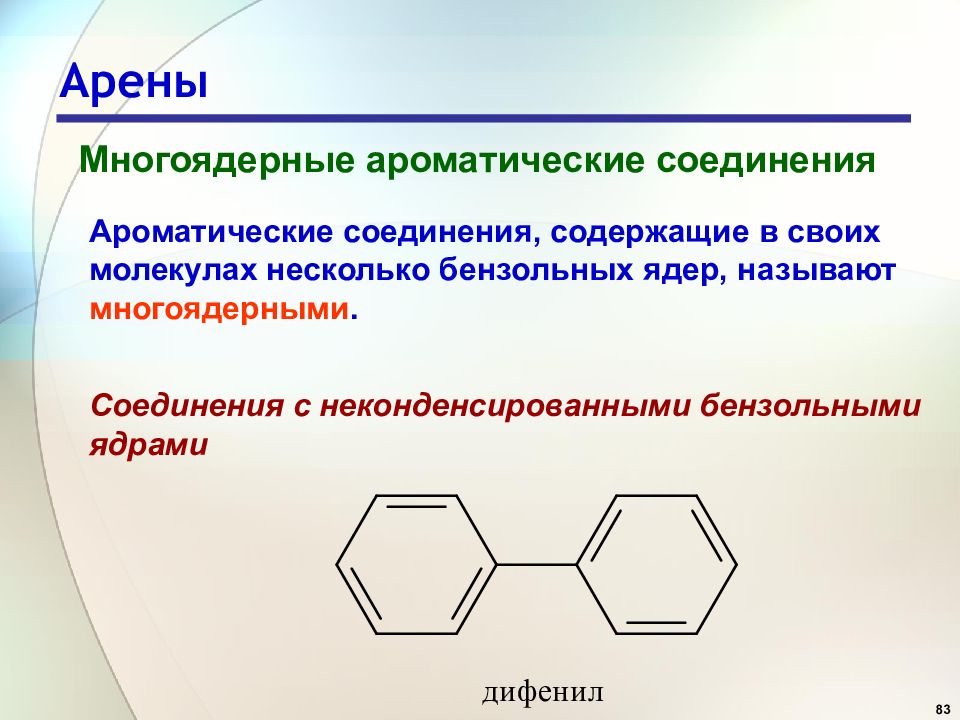
83 Арены Многоядерные ароматические соединения Ароматические соединения, содержащие в своих молекулах несколько бензольных ядер, называют многоядерными. Соединения с неконденсированными бензольными ядрами
Слайд 84: Арены
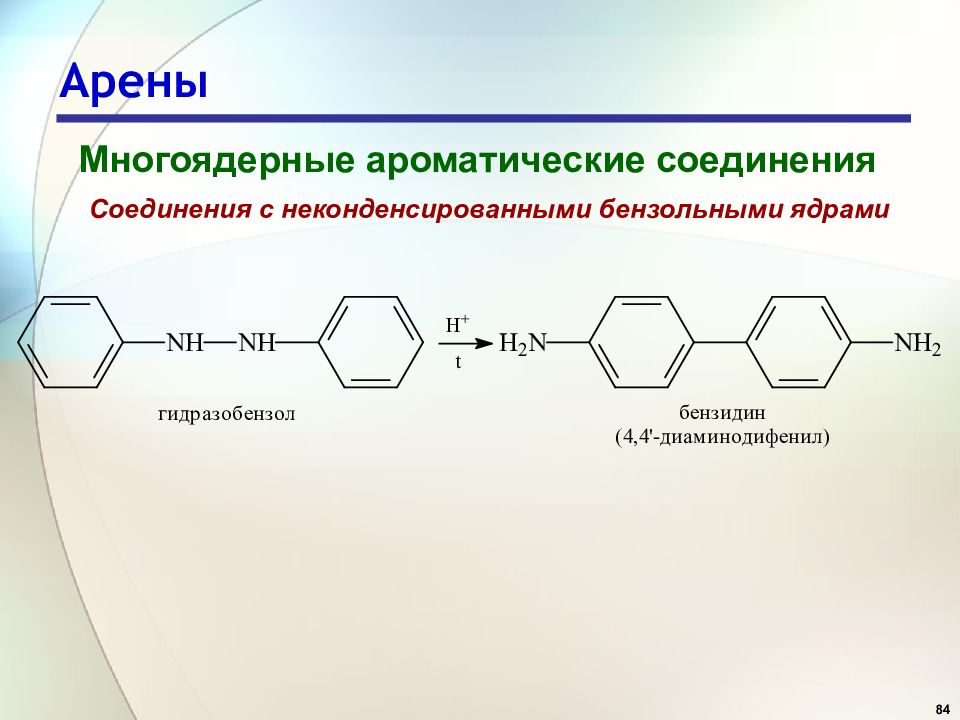
84 Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами
Слайд 85: Арены
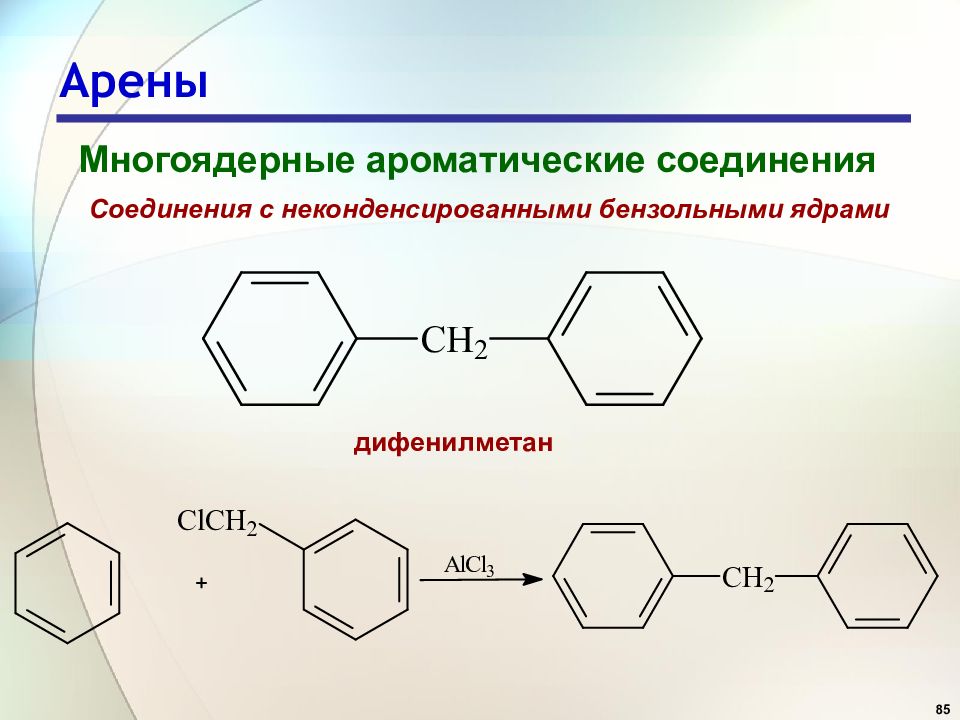
85 Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами дифенилметан
Слайд 86: Арены
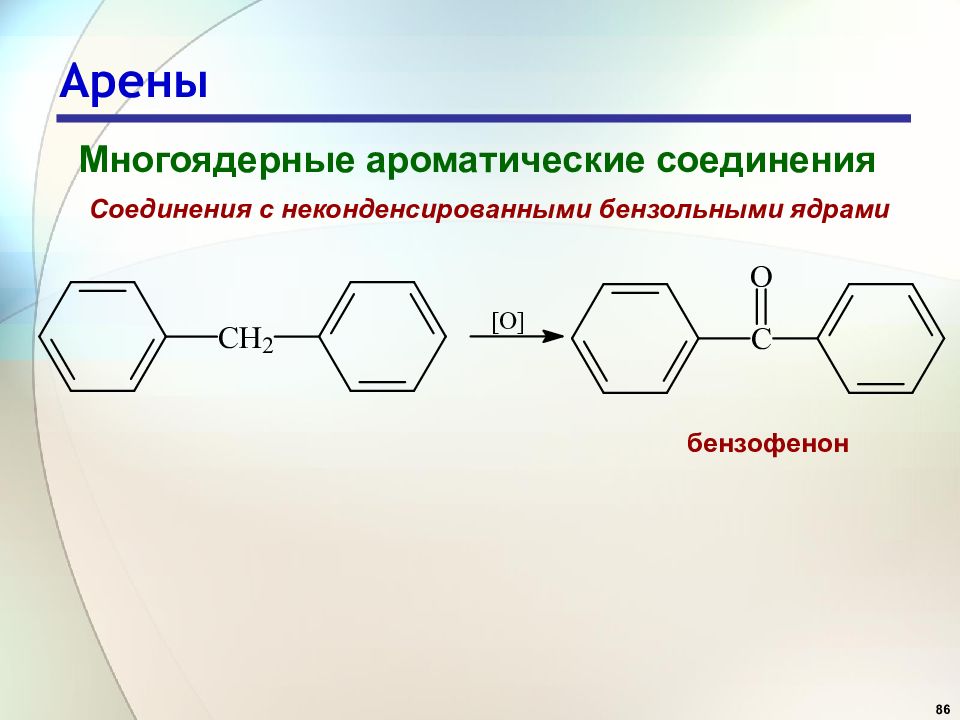
86 Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами бензофенон
Слайд 87: Арены
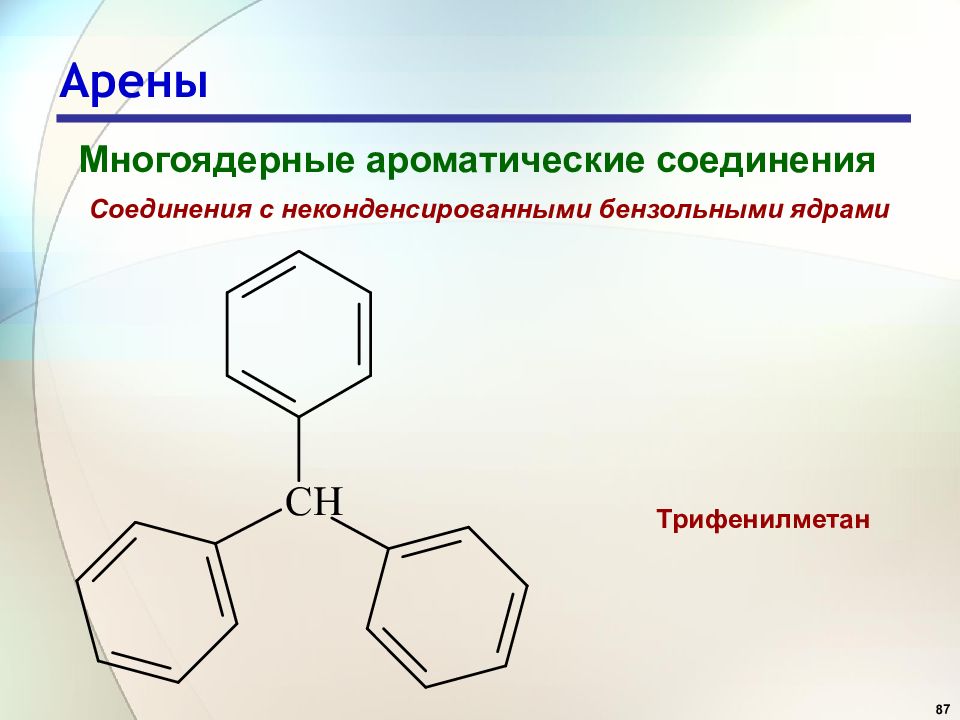
87 Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами Трифенилметан
Слайд 89: Арены
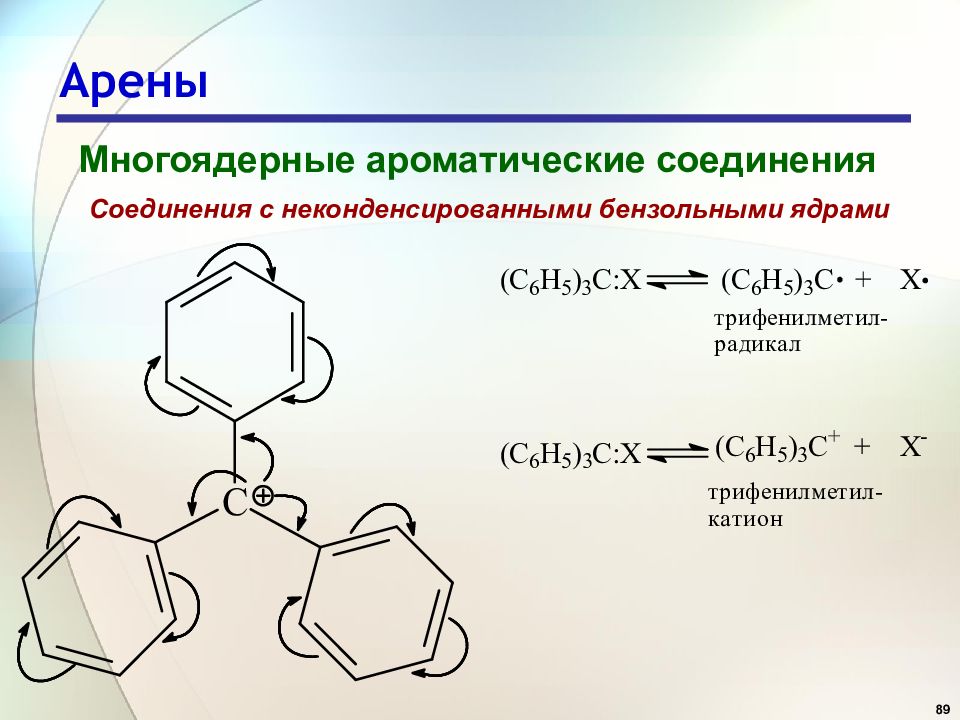
89 Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами
Слайд 90: Арены
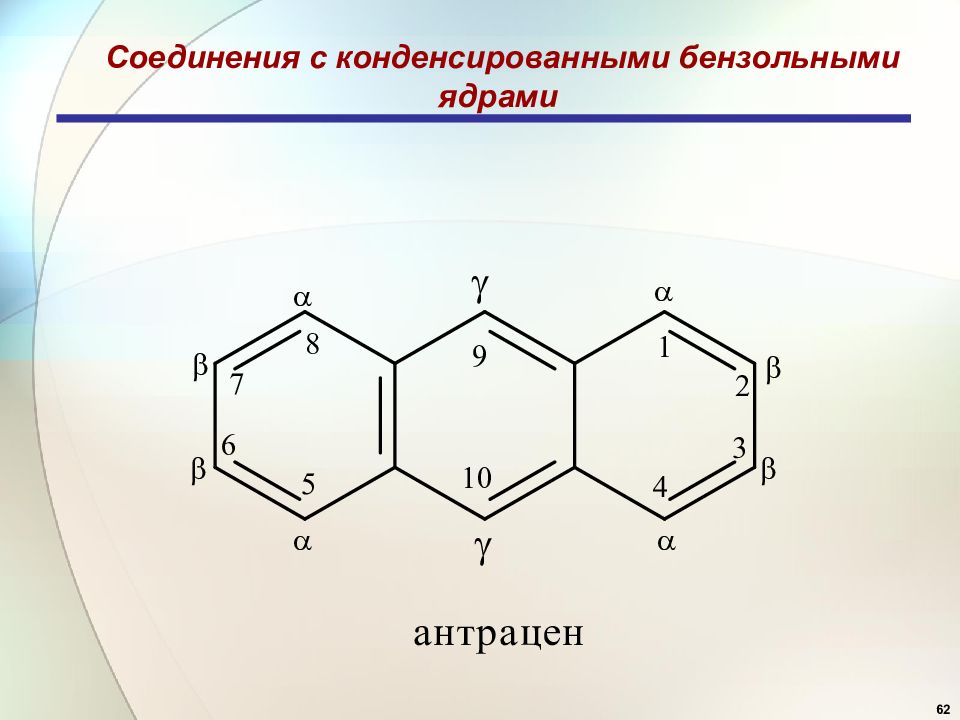
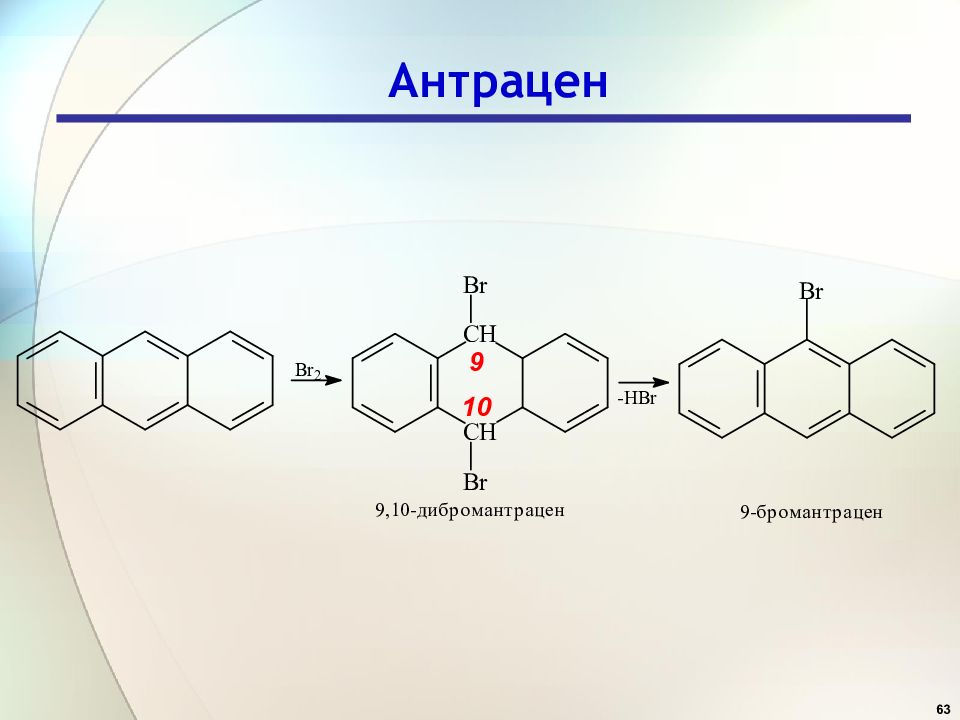
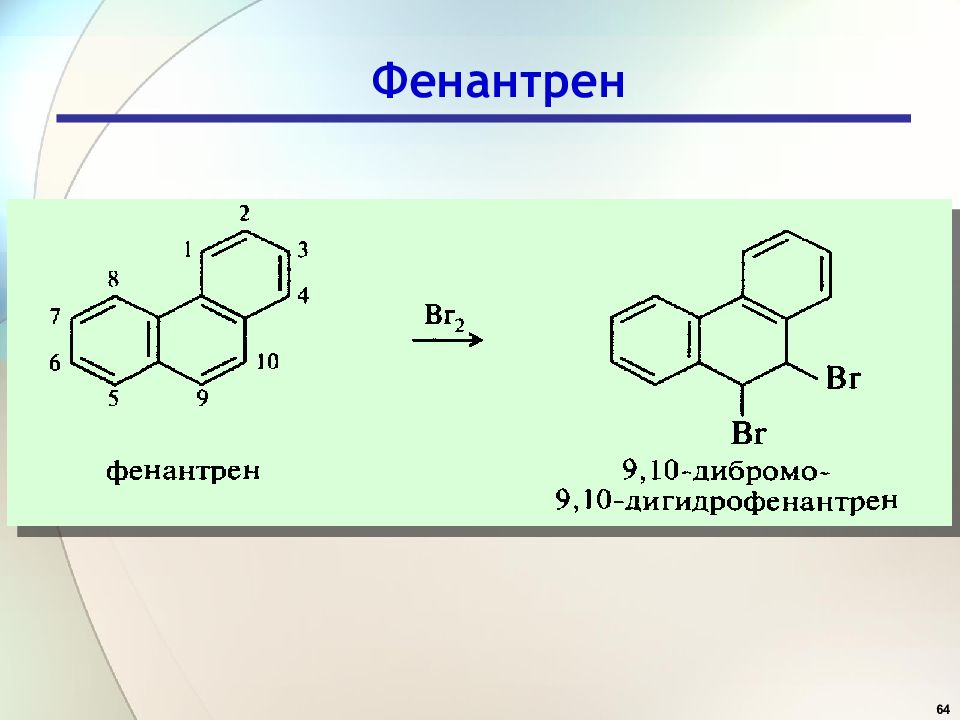
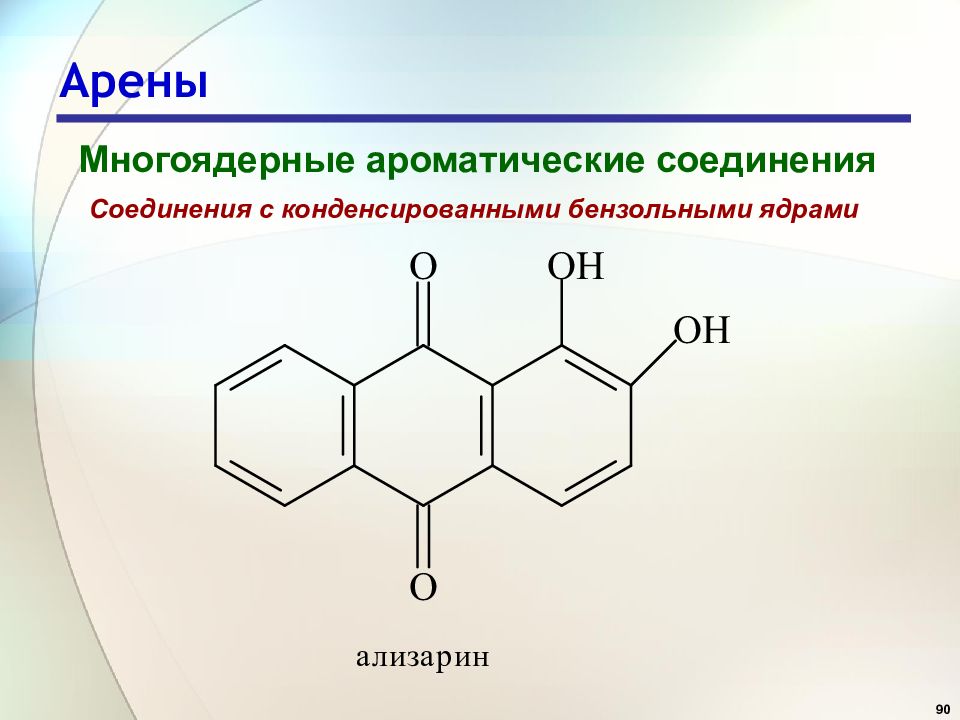
90 Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами
Слайд 91: Арены
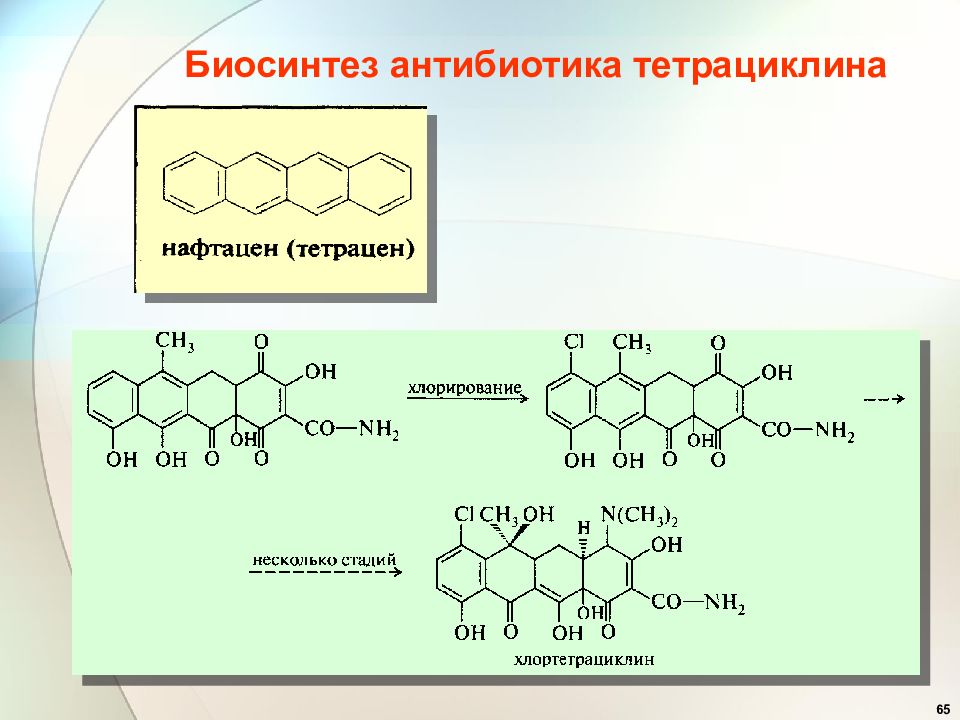
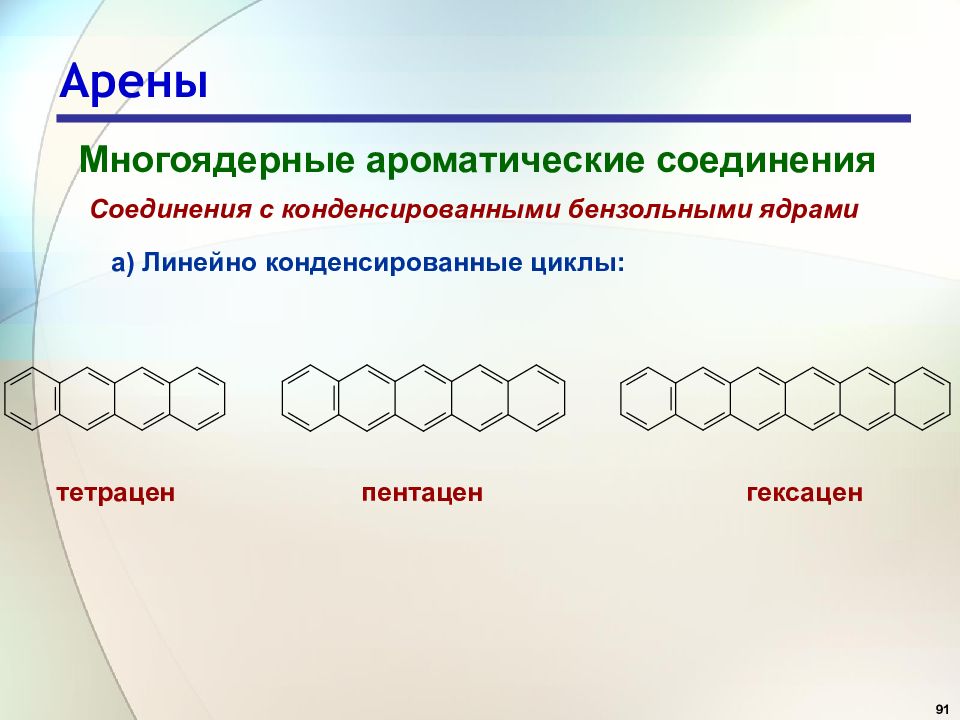
91 Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами а) Линейно конденсированные циклы: тетрацен пентацен гексацен
Слайд 92: Арены
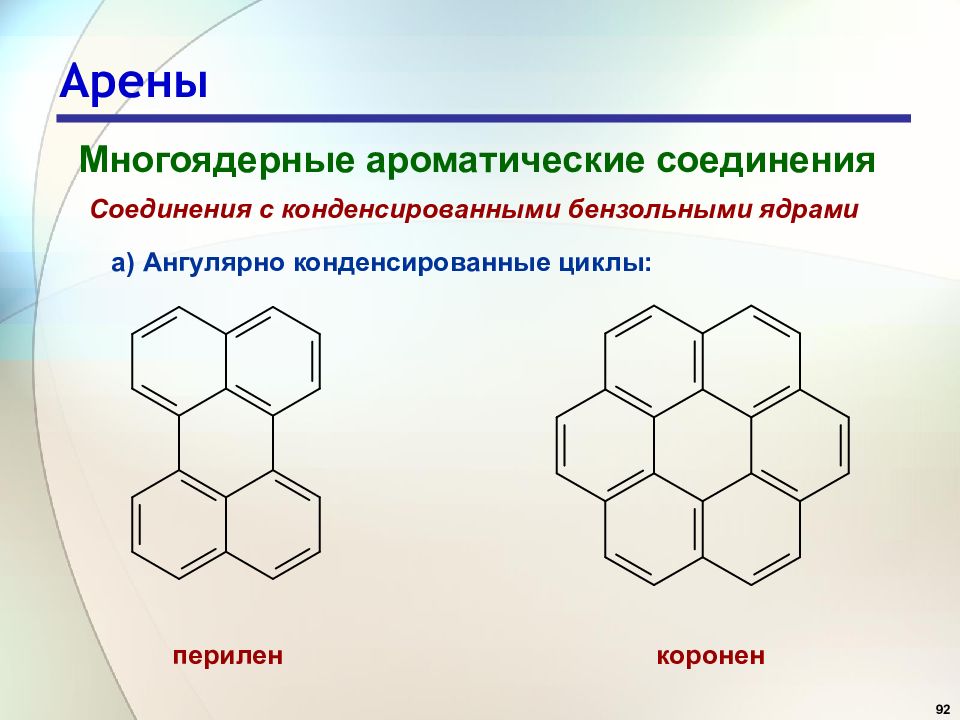
92 Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами а) Ангулярно конденсированные циклы: перилен коронен
Слайд 93: Арены
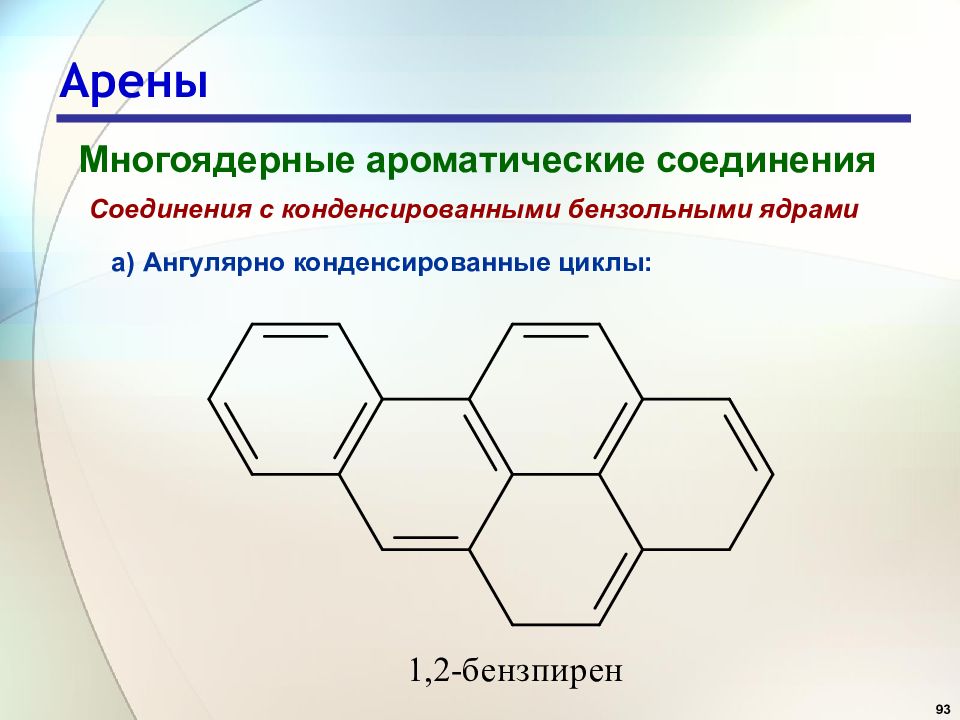
93 Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами а) Ангулярно конденсированные циклы: