Первый слайд презентации: 9 ЛЦ ФХ Хромановые и фенилхромановые соединения
Токоферола ацетат (витамин Е) Рутин (витамин Р)
Слайд 2: Токоферола ацетат ( Tocopheroli acetas )
Витамин E (токоферол) — жирорастворимый витамин, являющийся важным антиоксидантом. В природе существует в восьми различных формах ( α-токоферол, γ-токоферол и δ-токоферол ), отличающихся биологической активностью и исполняемыми в теле функциями.
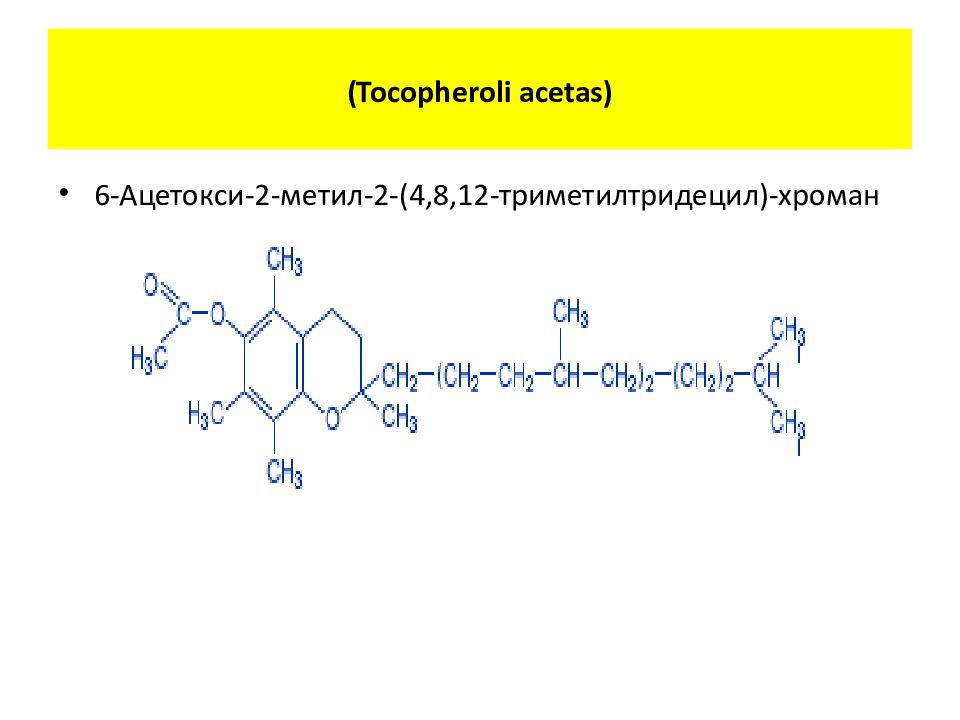
Слайд 3: ( Tocopheroli acetas )
6-Ацетокси-2-метил-2-(4,8,12-триметилтридецил)- хроман
Слайд 4: Токоферола ацетат
Светло-желтая прозрачная вязкая маслянистая жидкость со слабым запахом. На свету окисляется и темнеет. Практически нерастворим в воде, растворим в 95 % спирте, очень легко в эфире, хлороформе и растительных маслах. В основе молекулы токоферола лежит ядро хромана ( бензодигидропирана ). Применяется в виде сложного эфира (ацетата), который более устойчив. Токоферол имеет характерное поглощение в УФ области спектра с максимумом при 285 нм в абсолютном спирте.
Слайд 5: токоферол
В основе молекулы токоферола лежит ядро хромана ( бензодигидропирана ). Применяется в виде сложного эфира (ацетата), который более устойчив. Токоферол имеет характерное поглощение в УФ области спектра с максимумом при 285 нм в абсолютном спирте.
Слайд 6: Токоферола ацетат
Токоферола ацетат является синтетическим продуктом витамина Е. Под названием " Витамин Е " известен ряд соединений ( токоферолов ), близких по химической природе и биологическому действию.
Слайд 7: Витамин Е
Витамин Е и его аналоги представляют собой производные хромана, состоящий из кольца бензола и у-дегидропирана. В основе химического строения токоферолов лежит спирт протокол (в ядре хромана водород у С6 замещен на-ОН-группу, а в положении С2 - на метильную группу и боковой изопреноидную цепь-С16Н33) - 2-метил-2-(4 ', 8', 12'-триметил-тридецил)-6-хроманол. Токоферолы отличаются друг от друга количеством и расположением метильных групп в бензольном кольце и обозначаются буквами греческого алфавита - а, ß, у, ô. Наиболее активен а-токоферол, который содержит 3 метильные группы в 5, 7 и 8 положениях хроманового ядра. Характерно, что уменьшение количества метильных групп в ядре, а также замена или укорочение боковой цепи сопровождаются снижением биологической активности токоферолов.
Слайд 8: Восстановительные свойства
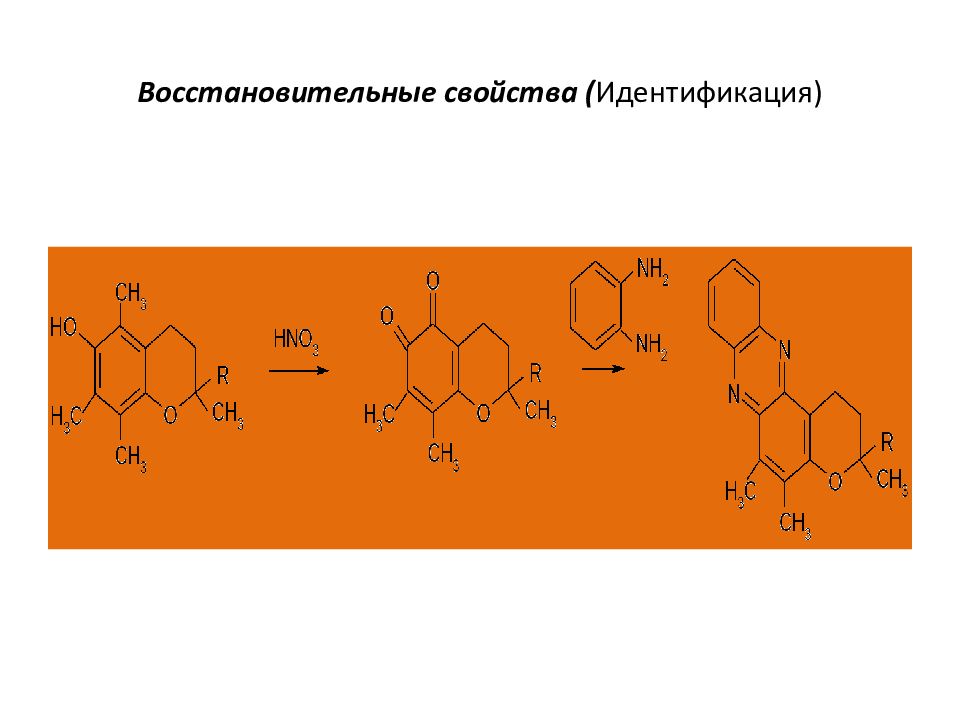
Восстановительные свойства. Для идентификации токоферолов широко используют реакции окисления, обусловленные присутствием в их молекулах фенольного гидроксила и сопровождающиеся образованием окрашенных веществ. Химическая структура продуктов окисления и их окраска зависят от характера окислителя. Так, например, при нагревании до 80°С с концентрированной азотной кислотой происходит образование окрашенного в красно-оранжевый цвет о-токоферилхинона, который при конденсации с о-фенилендиамином дает флюоресцирующий азиновый краситель красно-оранжевого цвета:
Слайд 10: Восстановительные свойства ( Идентификация)
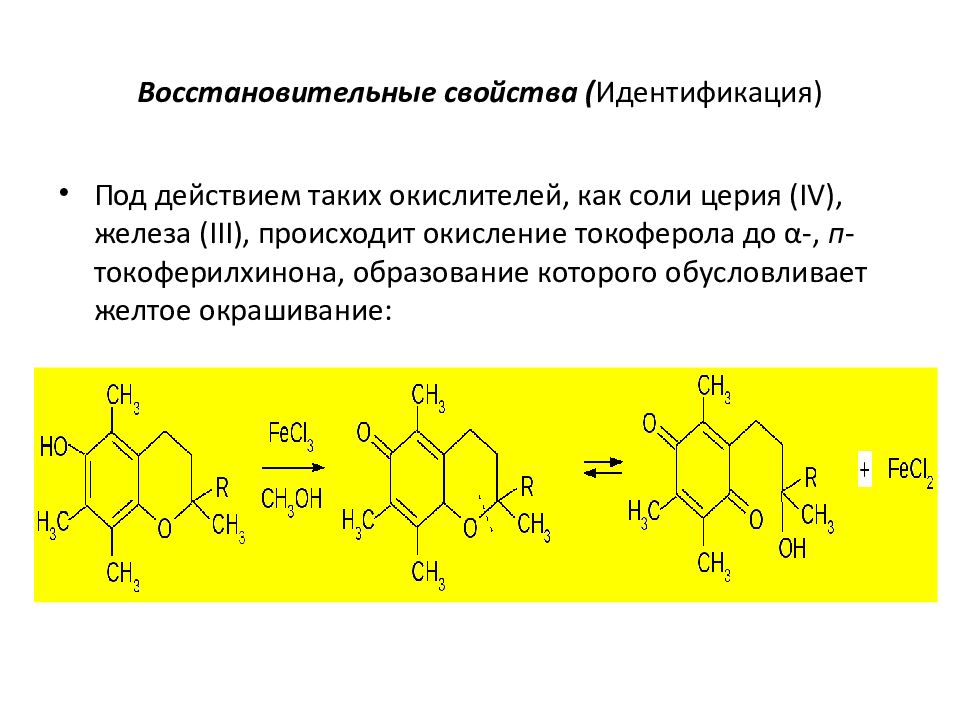
Под действием таких окислителей, как соли церия (IV), железа (III), происходит окисление токоферола до α-, п -токоферилхинона, образование которого обусловливает желтое окрашивание:
Слайд 11: Идентификация
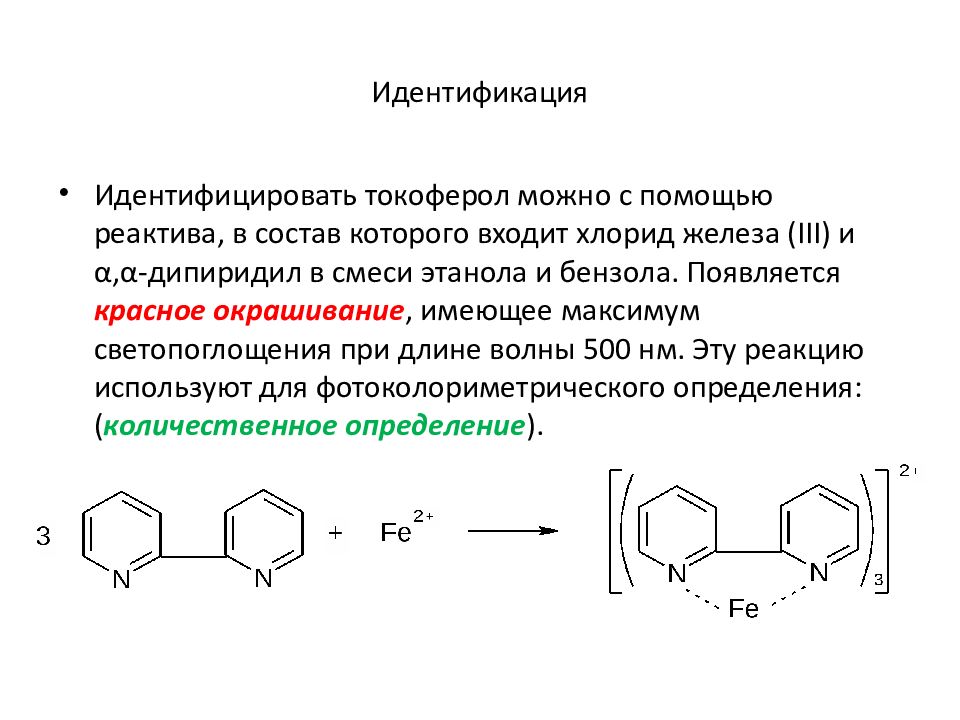
Идентифицировать токоферол можно с помощью реактива, в состав которого входит хлорид железа (III) и α, α-дипиридил в смеси этанола и бензола. Появляется красное окрашивание, имеющее максимум светопоглощения при длине волны 500 нм. Эту реакцию используют для фотоколориметрического определения: ( количественное определение ).
Слайд 12: Идентификация
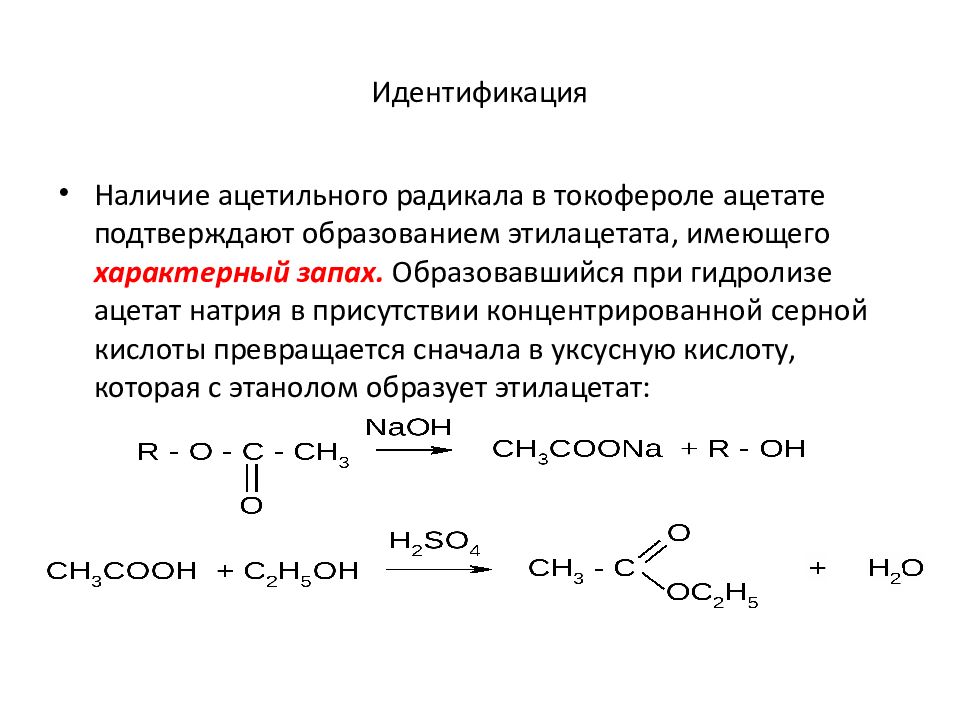
Наличие ацетильного радикала в токофероле ацетате подтверждают образованием этилацетата, имеющего характерный запах. Образовавшийся при гидролизе ацетат натрия в присутствии концентрированной серной кислоты превращается сначала в уксусную кислоту, которая с этанолом образует этилацетат:
Слайд 13: Количественное определение
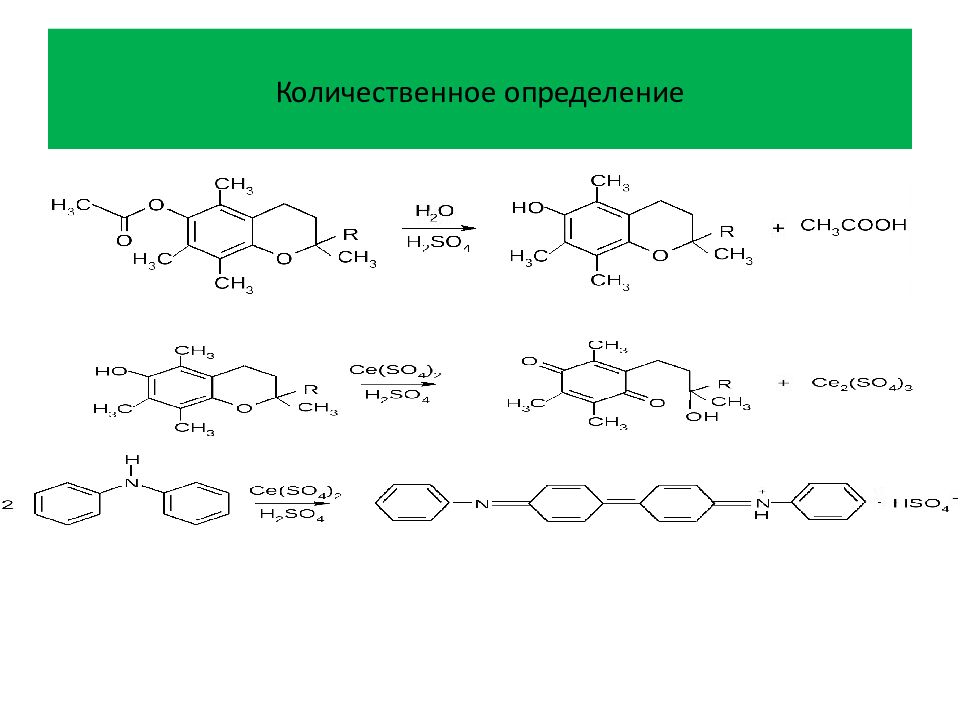
В основе фотоколориметрического анализа токоферолов широко используют реакции окисления, которые лежат и в основе цериметрического метода. Определение основано на кислотном гидролизе (кипячением с обратным холодильником в присутствии серной кислоты). Затем выделившийся токоферол титруют сульфатом церия (IV) (индикатор дифениламин) до появления сине-фиолетового окрашивания:
Слайд 14: Количественное определение
Цериметрия. Около 0,12 г препарата (точная навеска) растворяют в 10 мл абсолютного спирта, добавляют 10 мл раствора серной кислоты в абсолютном спирте и кипятят в течение 2 часов на водяной бане в колбе с обратным холодильником. После охлаждения до комнатной температуры смесь переносят в мерную колбу емкостью 50 мл и доводят объем раствора до метки абсолютным спиртом. К 20 мл этого раствора добавляют 20 мл абсолютного спирта, 10 мл воды и 2 капли раствора дифениламина и титруют при постоянном перемешивании 0,01 моль/л раствором сульфата церия со скоростью 25 капель в 10 секунд, защищая титруемый раствор от действия прямого солнечного света, до появления сине-фиолетового окрашивания, устойчивого в течение 10 секунд. Параллельно проводят контрольный опыт. 1 мл 0,01 моль/л раствора сульфата церия соответствует 0,002364 г С 31 Н 52 О 3, которого в препарате должно быть не менее 95,0 %.
Слайд 16: Функции
защищает клеточные структуры от разрушения свободными радикалами (действует как антиоксидант); участвует в биосинтезе гема ; препятствует тромбообразованию ; участвует в синтезе гормонов; поддерживает иммунитет; обладает антиканцерогенным эффектом; обеспечивает нормальное функционирование мускулатуры.
Слайд 17: (МЕ)
Количество витамина E обычно измеряется в международных единицах (МЕ). 1 МЕ = 0,67 мг a- токоферола = 1 мг a- токоферола ацетата 1,49 МЕ = 1 мг a- токоферола = 1,49 мг a- токоферола ацетата. Для обозначения профилактических доз витамина также используется термин «эквиваленты токоферола» или ЭТ ( TE) 1 мг = TE1 мг a- токоферола 0,5 мг = TE1 мг b- токоферола 0,1 мг = TE1 мг g- токоферола 0,3 мг = TE1 мг a- токотриенола
Слайд 18: Источники
Растительные масла: подсолнечное, хлопковое, кукурузное; семечки яблок, орехи (миндаль, арахис), турнепс, зеленые листовые овощи, злаковые, бобовые, яичный желток, печень, молоко, овсянка, соя, пшеница и ее проростки. Травы, богатые витамином Е: одуванчик, люцерна, льняное семя, крапива, овес, лист малины, плоды шиповника.
Слайд 19: Фенилхромановые соединения
К данной группе лекарственных веществ относятся флавоноиды (витамины группы Р – рутозид (рутин), кверцетин и дигидрокверцетин.
Слайд 20: Фенилхромановые соединения-флавоноиды (витамины группы Р): рутозид (рутин), троксерутин ( троксевазин )
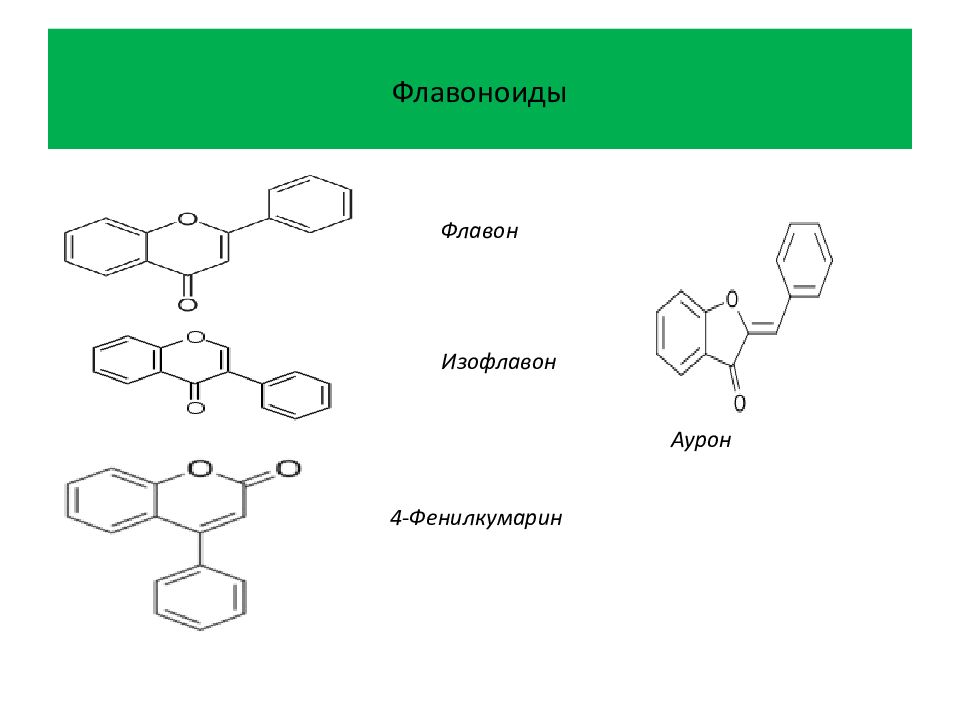
Флавоноиды — это крупнейший класс растительных полифенолов. С химической точки зрения, флавоноиды представляют собой гидроксипроизводные флавона (собственно флавоноиды ), 2,3-дигидрофлавона ( флаваноны ) изофлавона ( изофлавоноиды ), 4-фенилкумарина ( неофлавоноиды ), а также флавоны с восстановленной карбонильной группой ( флаванолы ) [1]. Зачастую к флавоноидам относят и другие соединения С 6 -С 3 -С 6 ряда, в которых имеются два бензольных ядра, соединенных друг с другом трехуглеродным фрагментом — халконы, дигидрохалконы и ауроны [2] :
Слайд 22: флавоноиды
Среди флавоноидов есть как водорастворимые, так и липофильные соединения, окрашенные преимущественно в жёлтый, оранжевый и красный цвета. Некоторые классы флавоноидов — антоцианины и ауроны — являются растительными пигментами, обуславливающими окраску цветов и плодов растений.
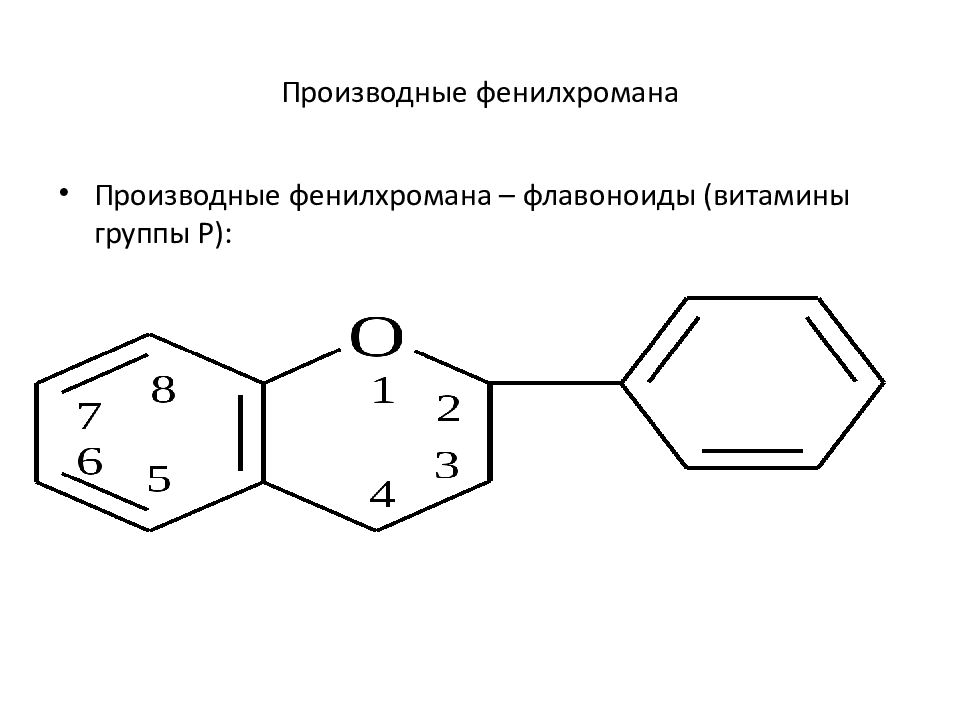
Слайд 23: Производные фенилхромана
Производные фенилхромана – флавоноиды (витамины группы Р):
Слайд 24: Rutozidum (Rutină)
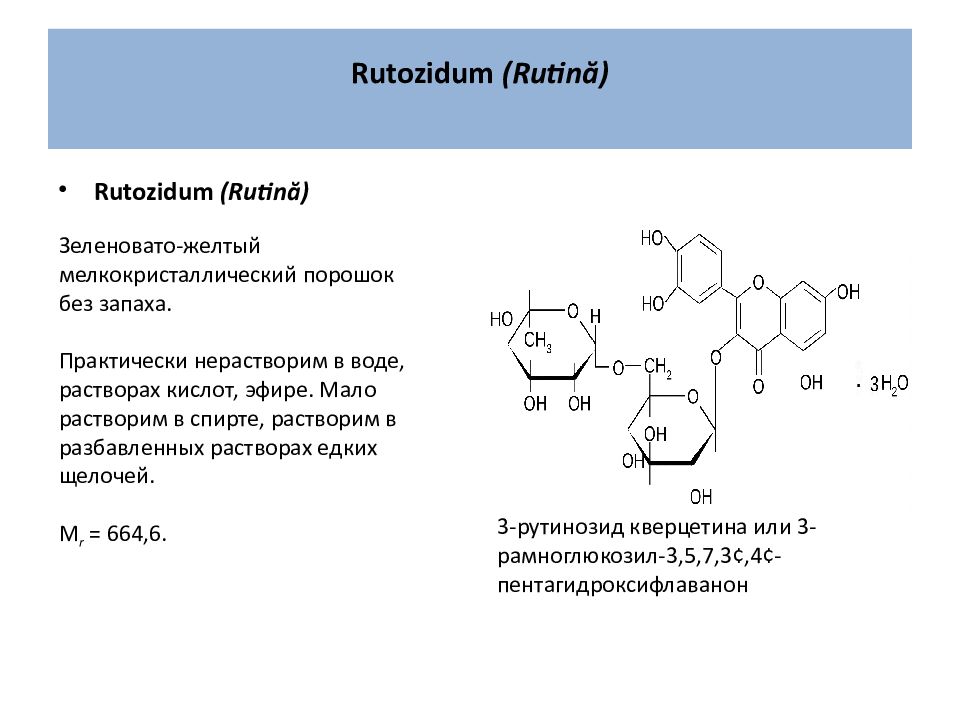
Rutozidum (Rutină) 3-рутинозид кверцетина или 3-рамноглюкозил-3,5,7,3¢,4¢-пентагидроксифлаванон Зеленовато-желтый мелкокристаллический порошок без запаха. Практически нерастворим в воде, растворах кислот, эфире. Мало растворим в спирте, растворим в разбавленных растворах едких щелочей. М r = 664,6.
Слайд 25
По химическому строению рутозид является гликозидом. Сахарная часть (дисахарид рутиноза ) включает D -глюкозу и L - рамнозу. Гликози́ды — органические соединения, молекулы которых состоят из двух частей: углеводного ( пиранозидного или фуранозидного ) остатка и неуглеводного фрагмента (т. н. агликона ). В качестве гликозидов в более общем смысле могут рассматриваться и углеводы, состоящие из двух или более моносахаридных остатков. Преимущественно кристаллические, реже аморфные вещества, хорошо растворимые в воде и спирте. Гликозиды представляют собой обширную группу органических веществ, встречающихся в растительном (реже в животном) мире и/или получаемых синтетическим путём. При кислотном, щелочном, ферментативном гидролизе они расщепляются на два или несколько компонентов — агликон и углевод (или несколько углеводов). Многие из гликозидов токсичны или обладают сильным физиологическим действием, например гликозиды наперстянки, строфанта и другие.
Слайд 26: Гидролитическое разложение
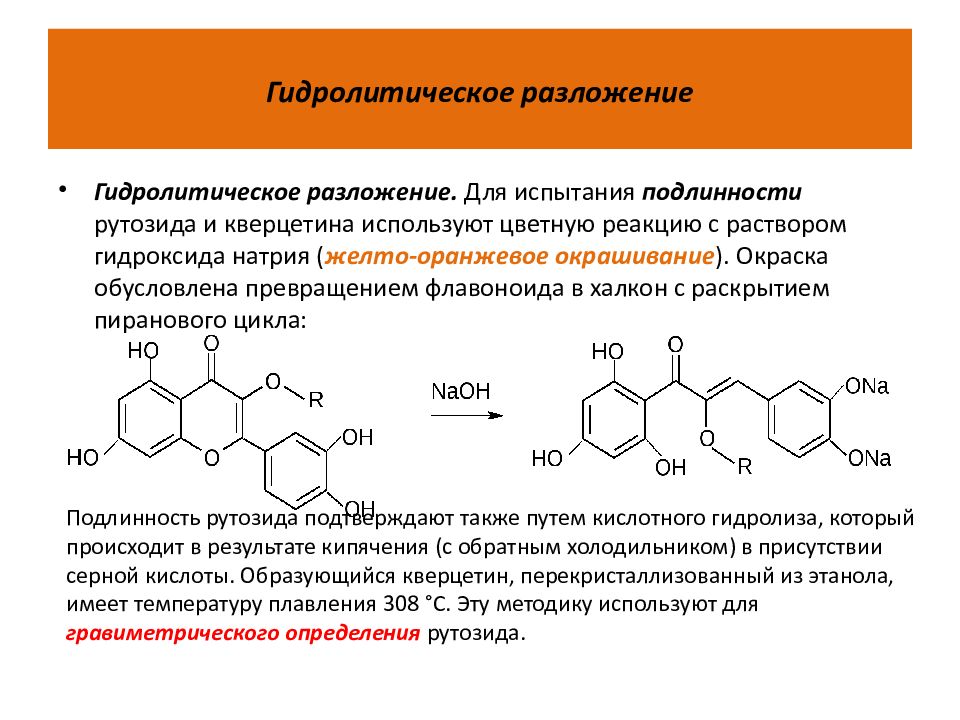
Гидролитическое разложение. Для испытания подлинности рутозида и кверцетина используют цветную реакцию с раствором гидроксида натрия ( желто-оранжевое окрашивание ). Окраска обусловлена превращением флавоноида в халкон с раскрытием пиранового цикла: Подлинность рутозида подтверждают также путем кислотного гидролиза, который происходит в результате кипячения (с обратным холодильником) в присутствии серной кислоты. Образующийся кверцетин, перекристаллизованный из этанола, имеет температуру плавления 308 °С. Эту методику используют для гравиметрического определения рутозида.
Слайд 27: Специфическая реакция подлинности
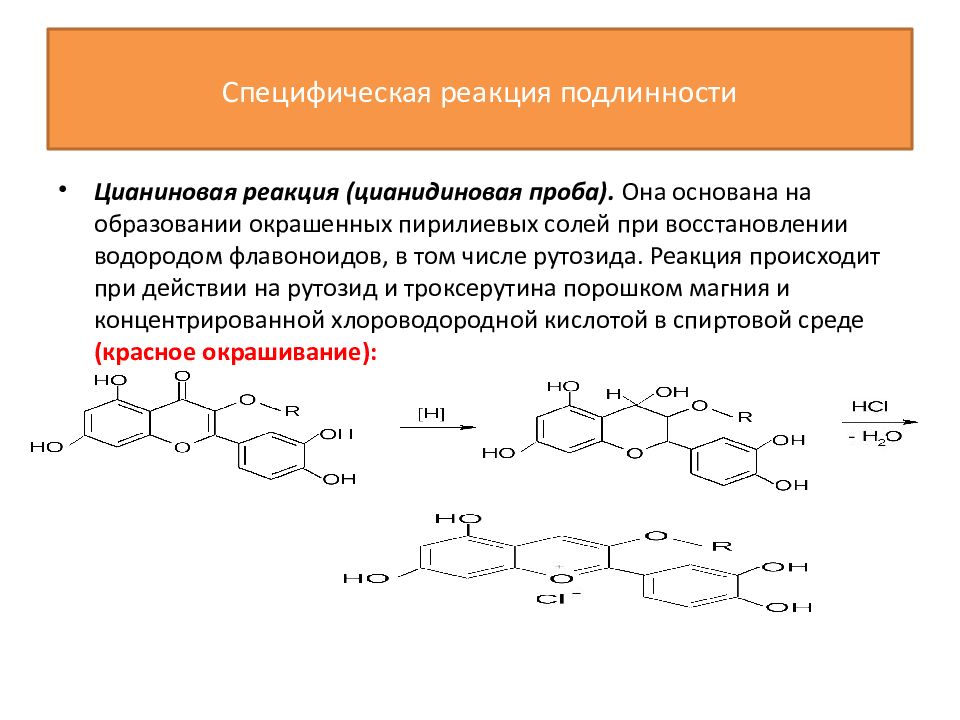
Цианиновая реакция ( цианидиновая проба). Она основана на образовании окрашенных пирилиевых солей при восстановлении водородом флавоноидов, в том числе рутозида. Реакция происходит при действии на рутозид и троксерутина порошком магния и концентрированной хлороводородной кислотой в спиртовой среде (красное окрашивание):
Последний слайд презентации: 9 ЛЦ ФХ Хромановые и фенилхромановые соединения: Количественное определение
За счет ароматичности системы и наличия сопряженных двойных связей в сочетании с карбонильной группой для рутозида характерно поглощение в УФ области спектра. Измеряют оптическую плотность спиртовог раствора ЛВ при определенной длине волны.