Слайд 2
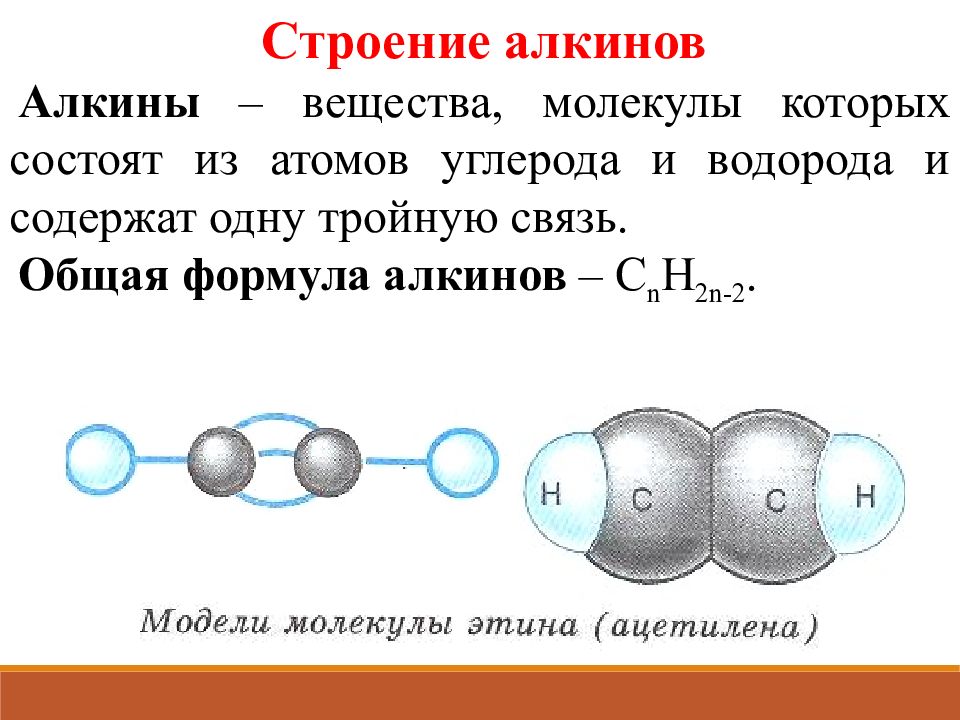
Строение алкинов Алкины – вещества, молекулы которых состоят из атомов углерода и водорода и содержат одну тройную связь. Общая формула алкинов – C n H 2n-2.
C n H 2n –2 n = 2 n = 3 n = 4 H-C ≡ C-H эт ин (ацетилен) H-C ≡ C- С H 3 проп ин HC ≡ C- С H 2 - С H 3 H 3 C-C ≡ С - С H 3 бут ин-1 бут ин-2
Слайд 4
Изомерия алкинов C 5 H 8 СН С СН 2 СН 2 СН 3 СН 3 С С СН 2 СН 3 СН С СН СН 3 СН 3 пентин-1 пентин-2 3- метилбутин-1 Структурная изомерия: 1.Изомерия положения тройной связи 2. Изомерия углеродного скелета 3. Межклассовая изомерия (с алкадиен ами ) СН 2 =СН– СН 2 –СН=СН 2 СН 2 = С = СН–СН 2 –СН 3 СН 2 = СН–СН = СН–СН 3 пентадиен-1,2 пентадиен-1,3 пентадиен-1,4
Слайд 5
Строение алкинов H-C ≡ C-H Вид связи Н-С – ковалентная полярная Вид связи С ≡ С – ковалентная неполярная C ≡ C σ –св. π –св. Всего в молекуле ацетилена: σ -связей – π -связей – 3 2
Слайд 6
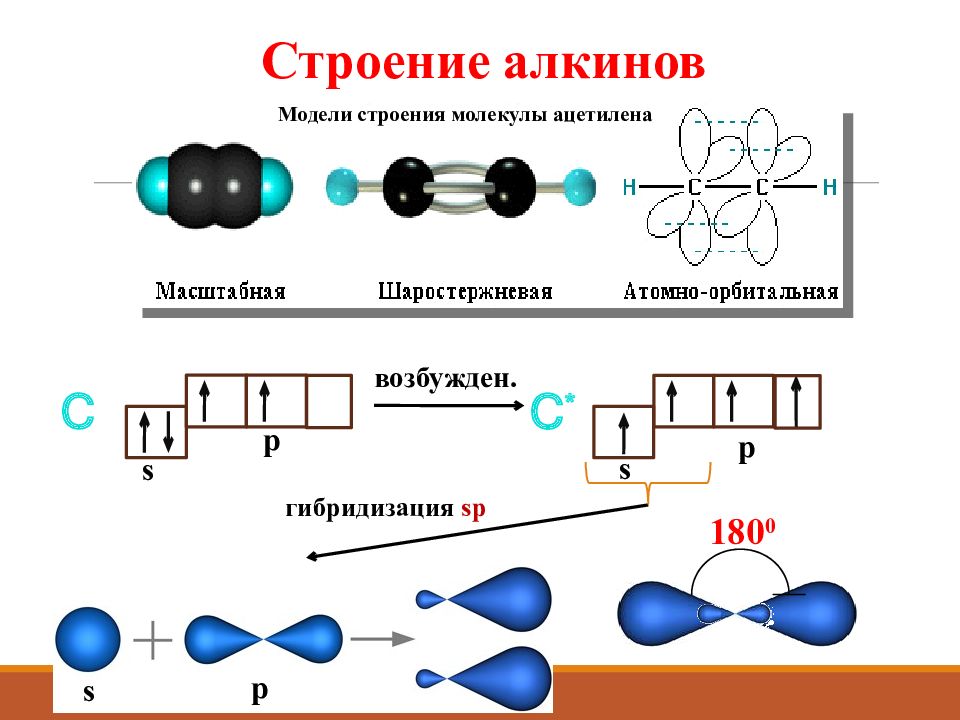
Строение алкинов Модели строения молекулы ацетилена s p возбужден. C C * s p гибридизация sp s p 180 0
Слайд 7
Строение алкинов Вид гибридизации – sp Валентный угол – 180 0 Длина связи С ≡ С 0,12 нм Строение молекулы линейное
Слайд 8
При обычных условиях: от С 2 Н 2 до С 4 Н 6 – газы с С 5 Н 8 – жидкости с С 16 Н 30 – твердые тела Алкины имеют специфический запах. Они лучше растворяются в воде, чем алканы и алкены. Физические свойства алкинов
Слайд 9
Физические свойства Название Формула Температура кипения Ацетилен (этин) С H CH - 83,8 Пропин С H 3 – С CH -23,3 Бутин – 1 С H 3 – CH 2 – С CH +8,5 Бутин – 2 С H 3 – C С – CH 3 +27,0 Температуры кипения и плавления алкинов закономерно повышаются при увеличении молекулярной массы соединений.
Слайд 10
Получение алкинов 1.Термический крекинг метана: 2.Карбидный способ: 3.Способ дегидрогалогенирования: H 3 C – C Н – С H 2 Cl Cl H-C ≡ C- С H 3 + 2 KOH (спирт) + 2K С l +2H 2 O
Слайд 11: Закончи фразу»:
Алкины – это непредельные углеводороды… Общая формула алкинов… Изомерия алкинов начинается с.. Молекула ацетилена имеет ……строение Агрегатное состояние алкинов- ….. Алкины получают путем…..
Слайд 13
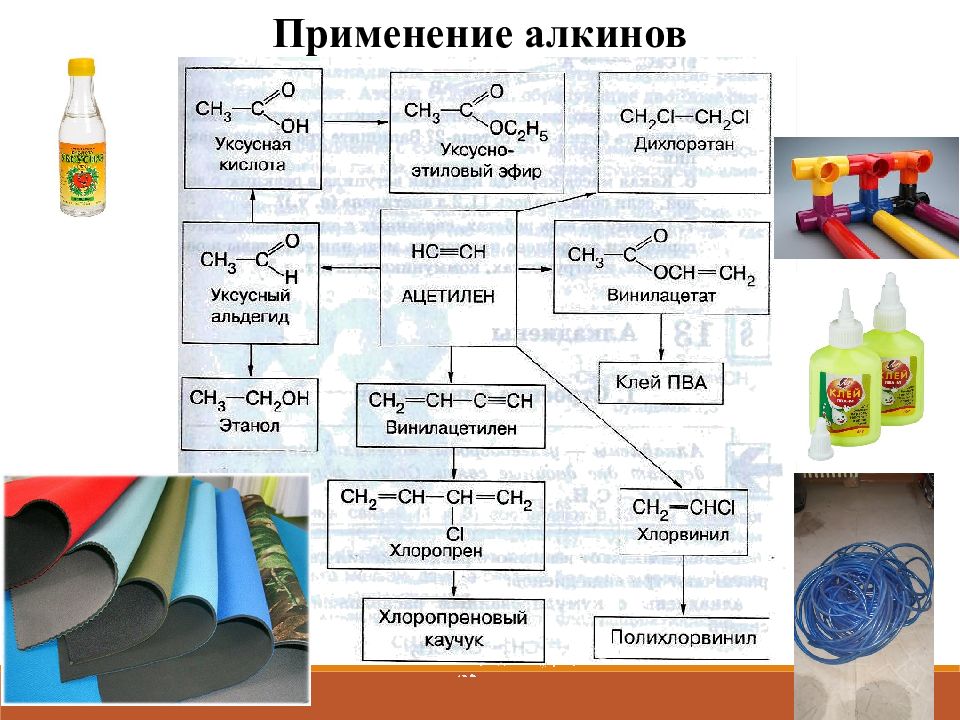
1) С H CH + 2H 2 CH 3 – CH 3 2) С H CH + 2 Br 2 CHBr 2 – CHBr 2 O 3) С H CH + H 2 O HgSO 4 CH 3 –C реакция Кучерова H 4) 3С H CH C ; 4 5 0 0 Бензол С H C – CH 3 + HBr С H 2 = CBr – CH 3 Химические свойства 1. Гидрирование 2. Галогенирование 3. Гидратация 4. Полимеризация 5. Гидрогалогенирование
Слайд 14: Реакция полимеризации
1. Димеризация под действием водного раствора CuCl и NH 4 Cl : Н C CH + Н C CH Н 2 C = CH C CH (винилацетилен) 2. Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского ): С, 500 С 3Н C CH С 6 H 6 (бензол)
Слайд 15: Реакции замещения
При взаимодействии ацетилена (или R C C H ) с аммиачными растворами оксида серебра выпадают осадки нерастворимых ацетиленидов: HC CH + 2[ Ag ( NH 3 ) 2 ] OH AgC CAg + 4 NH 3 + 2 H 2 O Качественная реакция на концевую тройную связь
Слайд 17: Горение ацетилена
При сгорании (полном окислении) ацетилена выделяется большое количества тепла: HC CH + 2О 2 2СО 2 + Н 2 О + Q Ацетилен горит на воздухе светящимся и коптящим пламенем!!!
Слайд 19
Контрольные вопросы 1.Вставьте в текст соответствующие слова и символы из скобок. Алкинами называются…(ациклические, циклические) углеводороды, содержащие в молекуле одну… (двойную, тройную) углерод – углеродную связь и имеющие общую формулу…( C n H 2n+2, C n H 2n, C n H 2n - 2 ). Первым представителем этого гомологического ряда является…(этин, этен, этан). Атомы углерода, связанные кратной связью, находятся в состоянии…( sp -, sp 2 -, sp 3 -) гибридизации. Угол между осями гибридных орбиталей равен…(90 0,109 0 28 ',120 0,180 0 ). Каждый из таких атомов углерода образует с соседними атомами…(одну, две, три, четыре) σ -связи и… (одну, две, три, четыре) π -связь. Длина углерод – углеродной связи в ацетилене… (больше, меньше), чем в этане, и равна … (0,154 нм, 0,120 нм, 0,134 нм).
Слайд 20
2. Укажите формулу алкина: а) C 3 H 4, б) C 4 H 8, в) C 5 H 12, г) C 6 H 6. 3. Как называется углеводород CH 3 – CH – C C - CH 3 CH 3 а) 2-этилпентин–3 б) 4-метилпентин–2 в) 3-метилгексин–4 г) 4-метилгексин–4 4. Укажите формулу 4,4-диметилпентина-2: CH 3 а) CH C – CH – CH – CH 3 б) CH C – C – CH 2 – CH 3 CH 3 CH 3 CH 3 CH 3 С H 3 в) CH 3 – C C – C – CH 3 г) CH C – CH 2 – C – CH 3 CH 3 С H 3
Слайд 21
5. Для пентина-2 выберите формулы: 1) гомологов; 2) изомеров. а) CH 3 – C C – CH 3 б) CH C – CH – CH 3 CH 3 в) CH C – CH 2 – CH 2 – CH 3 г) CH 3 – C C – CH 2 – CH 2 – CH 3 6. Как называется углеводород CH 3 – CH– CH – C C – CH –CH 3 С H 3 CH 3 C 2 H 5 а) 2-этил-5,6-диметилгептин-3 б) 2,4-диметил-6-этилгептин-2 в) 1,4,5-триметил-1-этилгексин-2 г) 2,3,6-триметилоктин-4 7. У алкинов отсутствует изомерия: а) углеродного скелета б) геометрическая, в) положение кратной связи, г) верного ответа нет.
Последний слайд презентации: Алкины
8. Ацетилен представляет собой: а) газ, б) жидкость, в) твердое вещество. 9. Реакцией Кучерова называется: а) гидратация ацетилена, б) тримеризация ацетилена, в) галогенирование ацетилена, в) гидрогалогенирование ацетилена. 10. Бензол получается из ацетилена по реакции: а) димеризации, б) тримеризации, в) окисления, г) гидратации.