Первый слайд презентации: Анализ особо чистых веществ
Слайд 2: Маркировка
Квалификации, установленные для реактивов: "чистый" (Ч) применяются в самых разнообразных лабораторных работах как учебного, так и производственного характера "чистый для анализа" ( ЧДА) – предназначены для аналитических работ, выполняемых с большой точностью, могут быть использованы в научно-исследовательских работах "химически чистый" (ХЧ) – предназначены для ответственных научных исследований, они используются также в аналитических лабораториях в качестве веществ, по которым устанавливаются титры рабочих растворов "особо чистый" ( ОСЧ), п репараты самой высокой очистки предназначены лишь для специальных целей
Слайд 3: Особо чистые вещества
такие вещества, содержание лимитируемых примесей в которых находится на уровне от 10 -6 до 10 -7 % ( по массе), а сумма остальных примесей 10 -3 - 10 -4 % ( по массе ). ЧИСТОЕ ВЕЩЕСТВО (идеально чистое вещество), простое или сложное вещество, обладающее только одному ему присущим комплексом постоянных свойств, которые обусловлены определенным набором атомов и молекул.
Слайд 4: Комплекс свойств чистого вещества
Х имическая чистота (отсутствие посторонних атомов) Изотопическая чистота – отсутствие в чистом веществе примесей его изотопов, продукты распада которых могут менять желательные свойства Ф изическое совершенство (отсутствие структурных дефектов) Кристаллохимическая чистота - отсутствие в чистом веществе полиморфных фаз
Слайд 5: Идеально чистое вещество
Это понятие имеет абстрактный характер, как, например, абсолютный нуль температуры или идеальный газ, и получить идеально чистое вещество также невозможно. О граничения кинетического характера: скорость очистки веществ от примеси прямо пропорциональна концентрации и падает по мере ее уменьшения. Ограничения термодинамического характера: процесс загрязнения вещества, т.е. разупорядочения системы, протекает самопроизвольно: получить абсолютно чистое вещество невозможно.
Чистоту оценивают по содержанию в веществе посторонних примесей: в относительно чистом фосфиде галлия, с суммарной концентрацией примеси 10 -5 % ( по массе) масс-спектральным методом анализа было обнаружено 72 примеси.
Слайд 7: Единицы измерения
В отечественной практике концентрации примеси в чистом веществе выражают в атомных процентах и процентах по массе. В зарубежной практике часто применяют, более мелкие единицы: 0/00 – промилле, ppm – часть на миллион или грамм на тонну; ppb – часть на биллон (миллиард) или милиграмм на тонну; очень редко ppT – часть на триллион.
Слайд 8: Классификация веществ особой чистоты
Вещества особой чистоты делятся на три класса : Класс А делится на подклассы А1 (содержание основного вещества 99,9%) и А2 (99,99% основного вещества). Цифра после буквы А характеризует число девяток после запятой. Класс В различают подклассы В3, В4, В5 и В6. Ультрачистые вещества образуют класс С, делящийся на подклассы С7-С10.
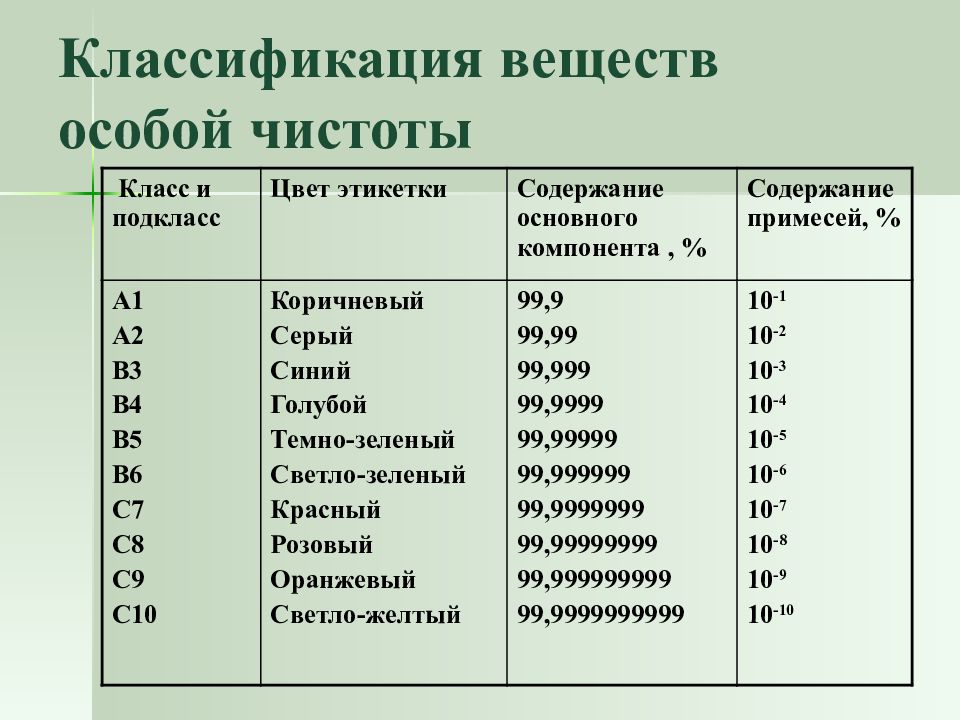
Слайд 9: Классификация веществ особой чистоты
Класс и подкласс Цвет этикетки Содержание основного компонента, % Содержание примесей, % А1 А2 B3 B4 B5 B6 C7 C8 C9 C10 Коричневый Серый Синий Голубой Темно-зеленый Светло-зеленый Красный Розовый Оранжевый Светло-желтый 99,9 99,99 99,999 99,9999 99,99999 99,999999 99,9999999 99,99999999 99,999999999 99,9999999999 10 -1 10 -2 10 -3 10 -4 10 -5 10 -6 10 -7 10 -8 10 -9 10 -10
Слайд 10: Маркировка особо чистых веществ
В маркировку особо чистых веществ помимо наименования марки «ОСЧ» входят две цифры. Первая обозначает количество лимитируемых примесей, вторая – показатель отрицательной степени их суммы, выраженной в процентах по массе. Например, для особо чистого SiO 2 нормируется десять примесей ( Аl, В, Fe, Са, Mg, Na, Р, Ti, Sn, Рb ), причем общее содержание их не превышает 1·10 -5 %. Для такого препарата устанавливается индекс "ОСЧ-10-5 ".
Слайд 11: Применение особо чистых веществ:
В производстве полупроводниковых материалов и приборов в ядерной технике в радио- и квантовой электронике как индивидуальные вещества
Слайд 12: Требования, которые необходимо соблюдать в работе:
Специально оборудованные помещения с тщательно профильтрованным воздухом. Недопустимы пылящие полы, стены и потолки. Полное отсутствие металлических предметов. Использование посуды из пластмасс особых типов (посуда и аппараты должны быть химически стойкие, не подвергаться выщелачиванию), из кварца и фторопласта.
Слайд 13: Требования, которые необходимо соблюдать в работе:
Для проведения работы в условиях, исключающих влияние воздуха, а также попадания в реакционную смесь пыли, рекомендуется применять герметизованную кварцевую аппаратуру. Вещества высокой чистоты следует брать пинцетом, кончики которого защищены пластмассой.
Слайд 14: Требования, которые необходимо соблюдать в работе:
Применение дистиллированной воды (даже дважды пли трижды перегнанной) недопустимо — можно применять лишь воду, прошедшую дополнительную очистку с помощью ионитов. Использование лавсановой спецодежды (не дающей ворсинок), особые туфли и резиновые перчатки.
Слайд 17
Пластиковые банки с герметично закрывающейся крышкой пинцет с пластиковыми концами Пинцет с тефлоновым покрытием
Слайд 18: М етоды очистки, используемые в современном производстве реактивов
Перекристаллизация Химическое осаждение Транспортные реакции Дистилляция и ректификация Экстракция Зонная плавка Ионный обмен и адсорбция
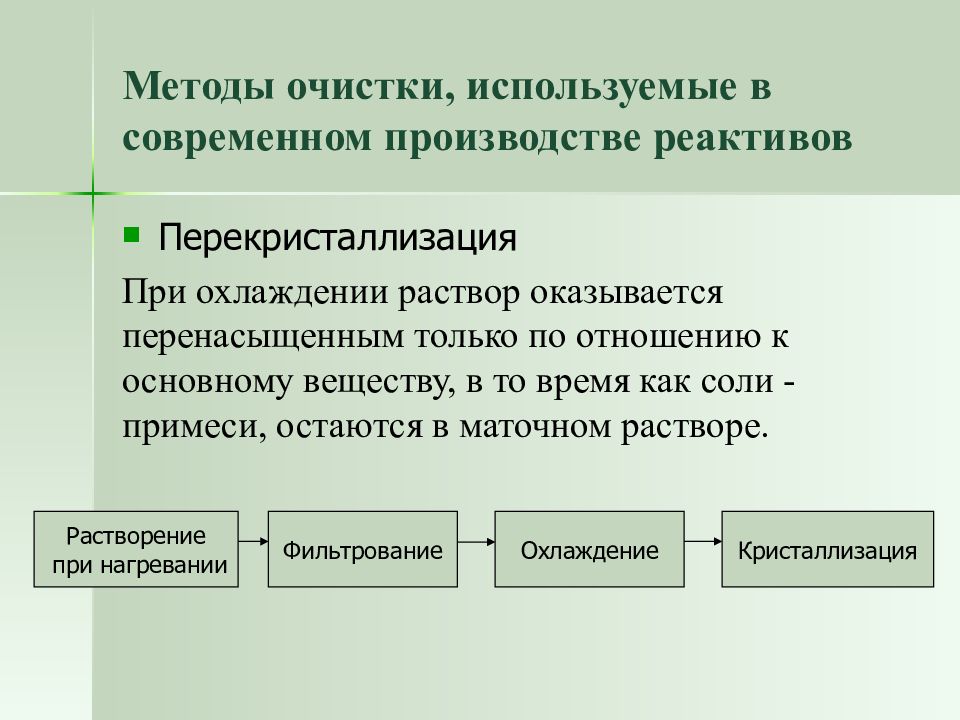
Слайд 19: Методы очистки, используемые в современном производстве реактивов
Перекристаллизация При охлаждении раствор оказывается перенасыщенным только по отношению к основному веществу, в то время как соли - примеси, остаются в маточном растворе. Растворение при нагревании Фильтрование Охлаждение Кристаллизация
Слайд 20: Методы очистки, используемые в современном производстве реактивов
Химическое осаждение Одним из простейших методов разделения веществ, в частности очистки реактивов, является перевод примеси (или основного вещества) в осадок. Это может быть достигнуто, если при действии подходящего реагента удаляемый компонент смеси образует малорастворимое соединение, например, выделение примеси Fe 3+ в NH 4 Cl при действии NH 4 OH: Fe 3+ + 3NH 4 OH = Fe (OH) 3 + 3NH 4 +
Слайд 21: Методы очистки, используемые в современном производстве реактивов
Транспортные реакции Этот метод широко используется при получении особо чистых веществ для полупроводниковой техники и радиоэлектроники. Принцип его в том, что очищаемое твердое или жидкое вещество А, взаимодействует по обратимой реакции с газообразным веществом В, образует газообразный продукт С, переносимый (транспортируемый) в другую часть системы, где вследствие изменения условий происходит его разложение с выделением чистого вещества А: Aтв,жидк + Bгаз = Cгаз Ni + 4CO= Ni (CO) 4
Слайд 22: Методы очистки, используемые в современном производстве реактивов
Дистилляция и ректификация Метод основан на том, что при испарении смеси жидкостей, пар получается обычно иного состава - происходит его обогащение легкокипящими компонентами смеси. Поэтому из многих смесей можно удалить легко кипящие примеси или, наоборот, перегнать основное вещество, оставив трудно кипящие примеси в перегонном аппарате.
Слайд 23: Методы очистки, используемые в современном производстве реактивов
Экстракция Метод основан на извлечении одного из компонентов раствора с помощью несмешивающегося с раствором органического растворителя. Экстрагируемый компонент распределяется между раствором и слоем органического растворителя в отношении, зависящем от коэффициента распределения: K = Cорг.р -ль/ Cраств
Слайд 24: Методы очистки, используемые в современном производстве реактивов
Зонная плавка Этот метод очистки основан на различии растворимости примеси в твердом веществе и в расплаве. Образец твердого вещества (например, стержень из металла, подлежащего очистке) медленно передвигают через узкую зону нагревания, при этом происходит постепенное расплавление отдельных участков образца, находящихся в данный момент в зоне нагревания. Примеси, содержащиеся в образце, накапливаются в жидкой фазе, вместе с ней передвигаются вдоль образца и по окончании плавки оказываются в конце образца. Как правило, зонную плавку повторяют многократно.
Последний слайд презентации: Анализ особо чистых веществ: Методы очистки, используемые в современном производстве реактивов
Ионный обмен и адсорбция Разделение проводят с помощью ионообменных смол, представляющих высокомолекулярные соединения с реакционноспособными H + или OH - -группами (катиониты или аниониты). При пропускании раствора электролита через такую смолу происходит обмен ионов металла или кислотного остатка, соответственно на H + или OH -