Кафедра иммунологии
Практическое занятие № 11
Слайд 3: Фронтальный опрос
Какие звенья иммунной системы изучаются в клинической практике? Какие методы иммунного анализа вам известны? Как происходила эволюция методов иммунного анализа? Каковы основные принципы оценки иммунограммы? Каковы возрастные особенности иммунологических показателей? Дайте определение понятию «иммунодефицитные состояния». Какие механизмы лежат в основе развития аутоиммунной патологии? Какие виды гиперчувствительности Вам известны?
К одному и тому же эпитопу антигена может образоваться целый спектр антител, отличающихся по структуре, степени специфичности и прочности связывания с эпитопом. Это же относится как к белковым, так и к полисахаридным антигенам.
Слайд 5: Эволюция методов иммунного анализа- поликлональные и моноклональные антитела
При введении антигена вырабатывается большое семейство антител, направленных к разным его эпитопам и различающихся также внутри группы антител, направленных к одному и тому же эпитопу. В крови иммунизированных животных появляется богатый и уникальный по составу спектр антител, который и обеспечивает их абсолютную специфичность в распознавании данного антигена.
Слайд 6: Поликлональные антитела –многокомпонентные смеси антител
Поликлональные антитела широко используются для нейтрализации бактериальных токсинов (дифтерийного, столбнячного), змеиных ядов (кобры, гадюки), вирусов, попавших в кровь (особенно эффективно для вируса кори), и для идентификации индивидуальных белков (и других антигенов), находящихся в клетке или в тканевых экстрактах. Однако иногда требуются не многокомпонентные смеси антител, возникающие в крови в ответ на введение антигена, а антитела, направленные лишь к одной детерминанте антигена.
Слайд 8: Жорж Кёлер и Сезар Мильштейн. Нобелевская премия за создание моноклональных антител
Идея состояла в том, чтобы взять линию миеломных клеток, которые потеряли способность синтезировать свои собственные антитела и слить такую клетку с нормальным В –лимфоцитом, синтезирующим антитела, с тем, чтобы после слияния отобрать образовавшиеся гибридные клетки, синтезирующие нужное антитело.
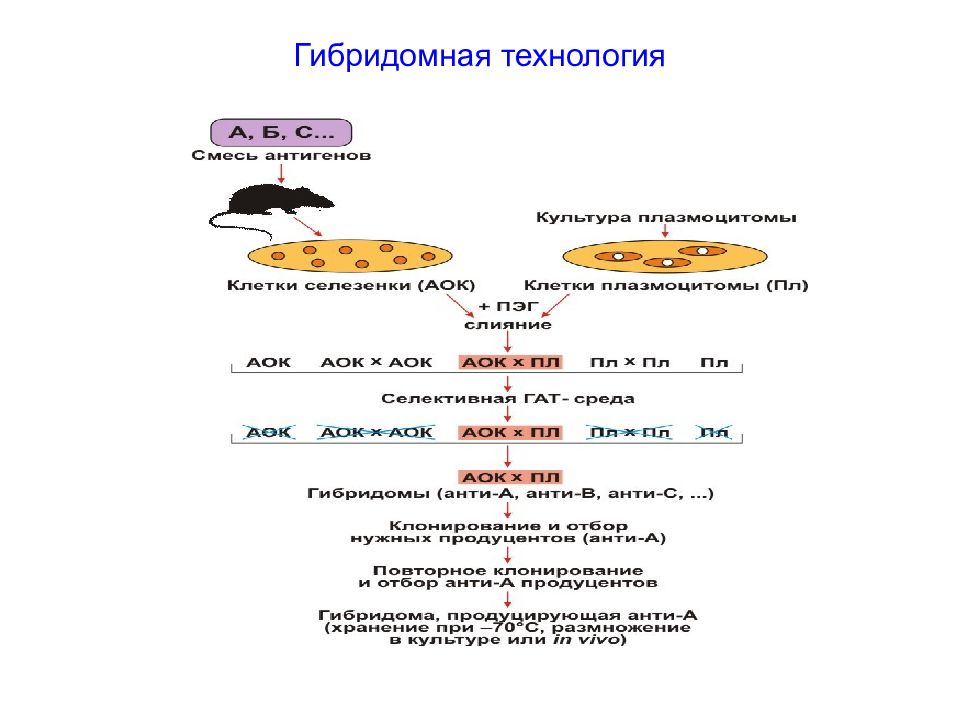
Слайд 9: Гибридомная технология
Соматический гибрид нормальной антителообразующей и опухолевой клеток ( гибридóма ) дает потомство, обладающее бессмертием опухолевой клетки и способностью к синтезу антител, унаследованному от клетки нормальной. Гибридомы продуцируют огромное количество моноклональных антител, обладающих уникальной специфичностью.
Слайд 10: 1975 год: впервые получены моноклональные антитела (МАТ) с помощью гибридомной технологии (Нобелевская премия 1984 года)
Моноклональные антитела — это иммуноглобулины, синтезируемые одним клоном клеток. Моноклональное антитело связывается только с одной антигенной детерминантой на молекуле антигена. Гибридомная технология - слияние с помощью полиэтиленгликоля лимфоцитов сёлезенки предварительно иммунизированных организмов определенным антигеном с раковыми клетками, способными к бесконечному делению. Отбирают клоны клеток, синтезирующие необходимые антитела. Гибридомы - бессмертные клоны клеток, синтезирующие моноклональные антитела.
Слайд 11: Биотехнология создания моноклональных антител
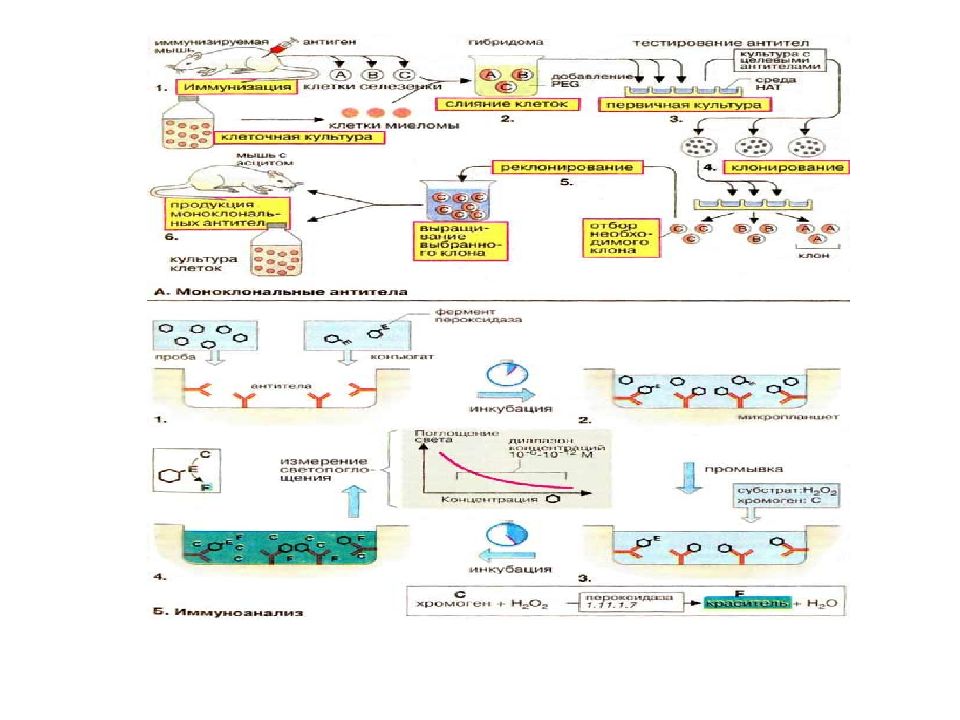
Животное иммунизируют, в ответ на введение антигена в организме мыши активизируются продуцирующие антитела потомки В-лимфоцитов. Эти клетки могут жить только в организме хозяина, при переводе на искусственную питательную среду они гибнут. Если слить иммунную клетку с опухолевой, образуются гибридные клетки, способные неограниченно долго жить в искусственных средах. Одновременно они сохраняют способность синтезировать антитела.
Слайд 14: Гуманизированные антитела
Мышиные лимфоциты синтезировали мышиные иммуноглобулины, введение таких моноклональных антител человеку вызывало иммунную реакцию отторжения. В 1988 году Грег Винтер разработал специальную методику гуманизации моноклональных антител - замена в составе моноклональных антител белков мыши белковыми компонентами человека - химерные (гуманизированные) антитела.
Слайд 17: Применение моноклональных антител
1. Диагностические методы определения молекул (иммунный анализ). 2.Терапия с использованием моноклональных антител (антицитокиновая терапия; анти - IgE –терапия и др.).
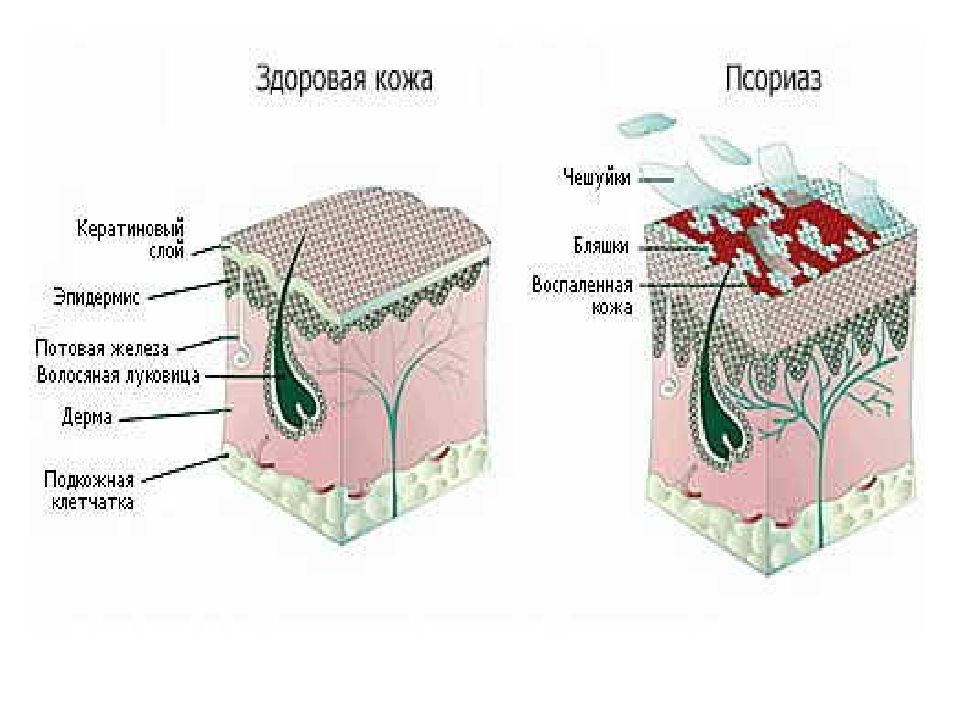
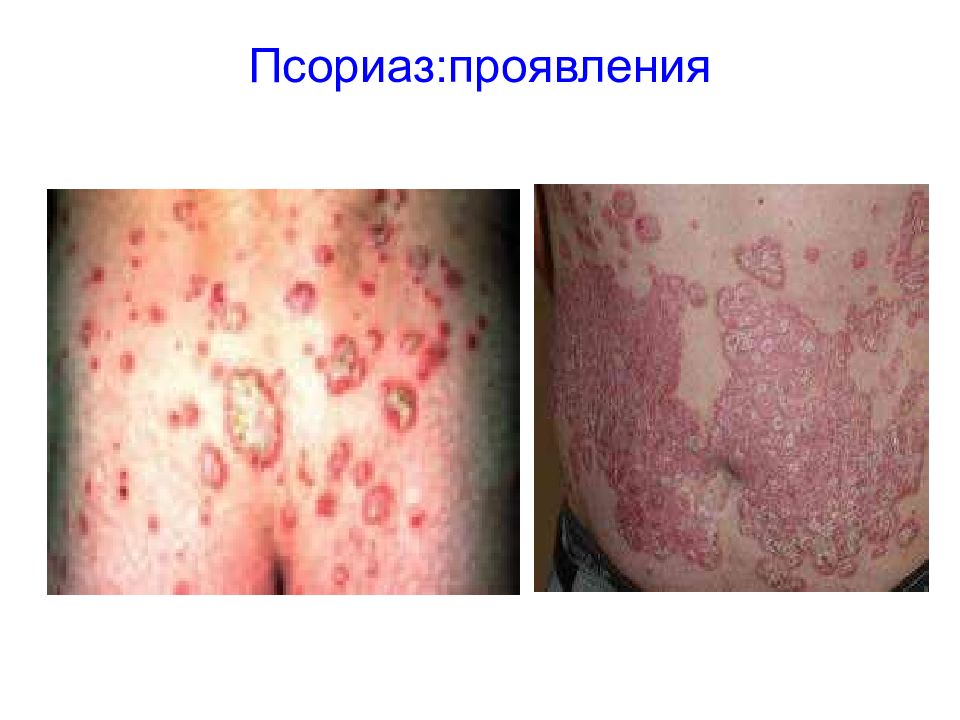
Слайд 19: Псориаз
Возможными кандидатами на аутоантигены при псориазе являются кератин 13, гетерогенный ядерный нуклеопротеин-1. Однако, точно аутоантигены при псориазе не установлены.Считается, что это –аутоантигены кожи.
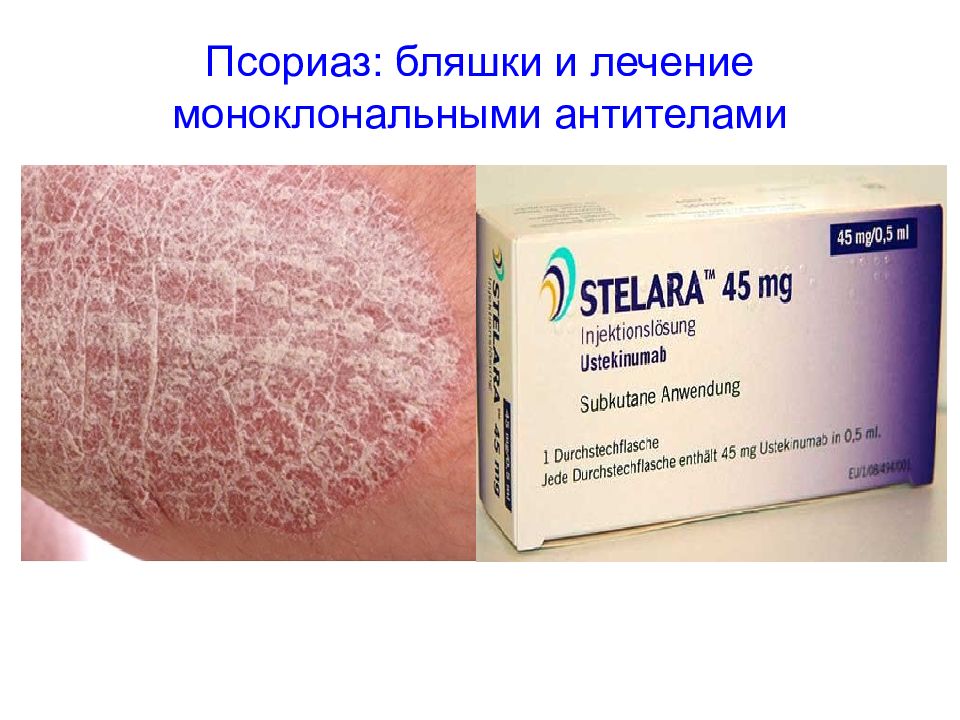
Слайд 24: Терапия моноклональными антителами при псориазе:
Активно используются для лечения псориаза, следующие препараты мононоклональных антител: инфликсимаб (препарат Ремикейд), блокада TNF-альфа; адалимумаб (препарат Хумира), блокада TNF-альфа; устекинумаб (препарат Стелара), блокада действия IL-23 и IL-12, блокада активации Т-клеток.
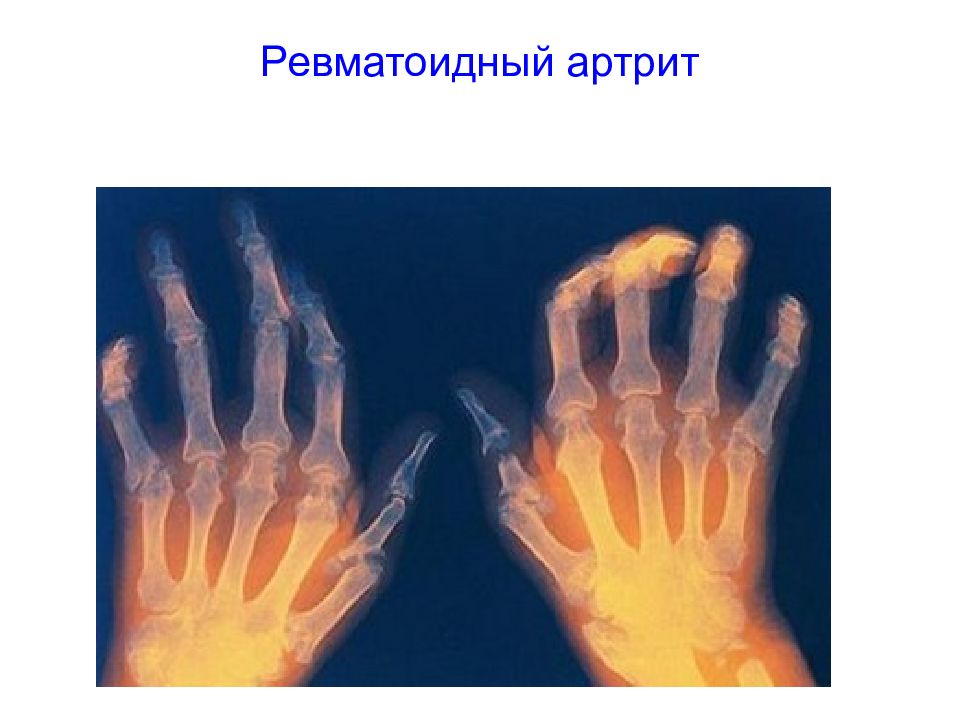
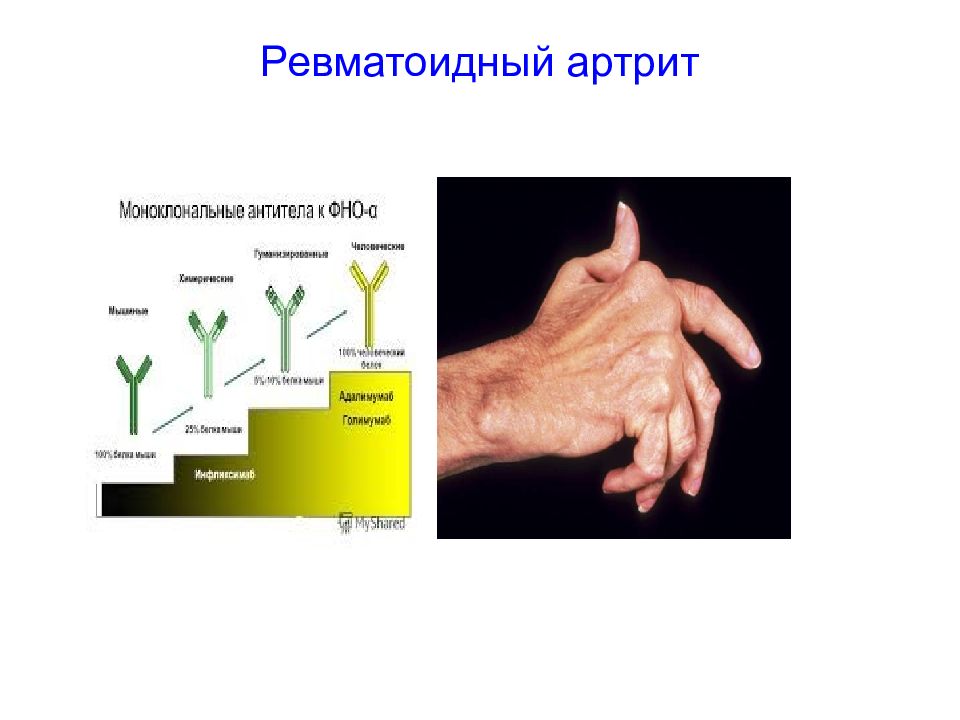
Слайд 25: Ревматоидный артрит
Иммунное воспаление в суставах приводит к появлению на суставных поверхностях костей эрозий, что в дальнейшем становится причиной развития выраженных суставных деформаций. Возможные этиологическаие факторы: Вирус Эпштейна-Барр, стрептококки группы В. (антигенная мимикрия: компоненты микробных и вирусных тел имеют сродство к тканях суставов, способны длительное время накапливаться в них и вызывать развитие воспаления).
Слайд 28
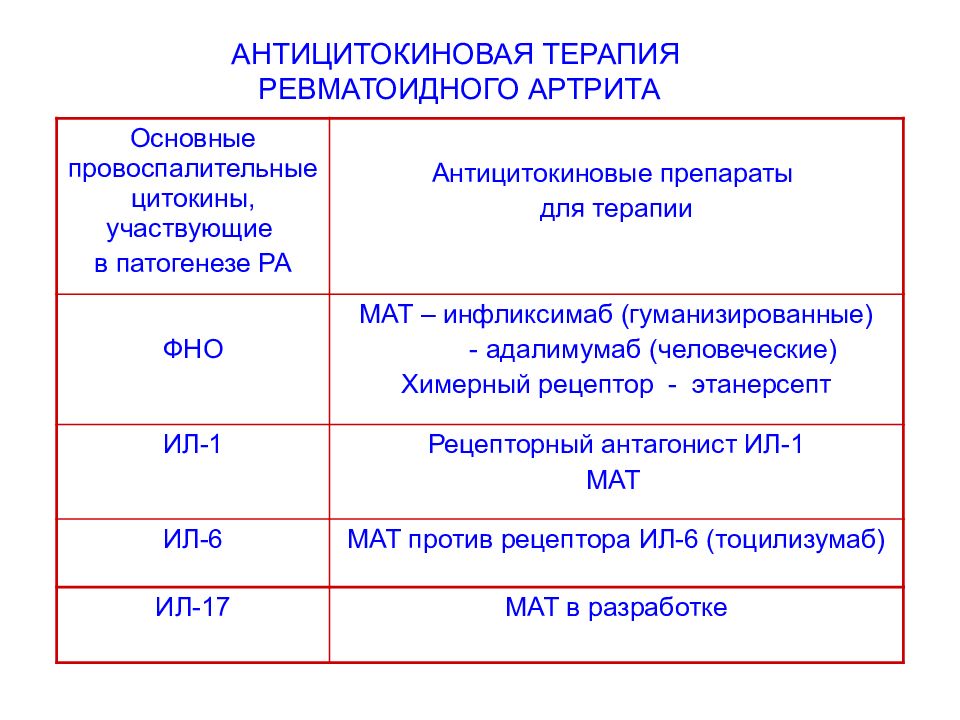
Основные провоспалительные цитокины, участвующие в патогенезе РА Антицитокиновые препараты для терапии ФНО МАТ – инфликсимаб ( гуманизированные ) - адалимумаб (человеческие) Химерный рецептор - этанерсепт ИЛ-1 Рецепторный антагонист ИЛ-1 МАТ ИЛ-6 МАТ против рецептора ИЛ-6 ( тоцилизумаб ) ИЛ-17 МАТ в разработке АНТИЦИТОКИНОВАЯ ТЕРАПИЯ РЕВМАТОИДНОГО АРТРИТА
Слайд 29: Лечение болезни Крона: ведолизумаб
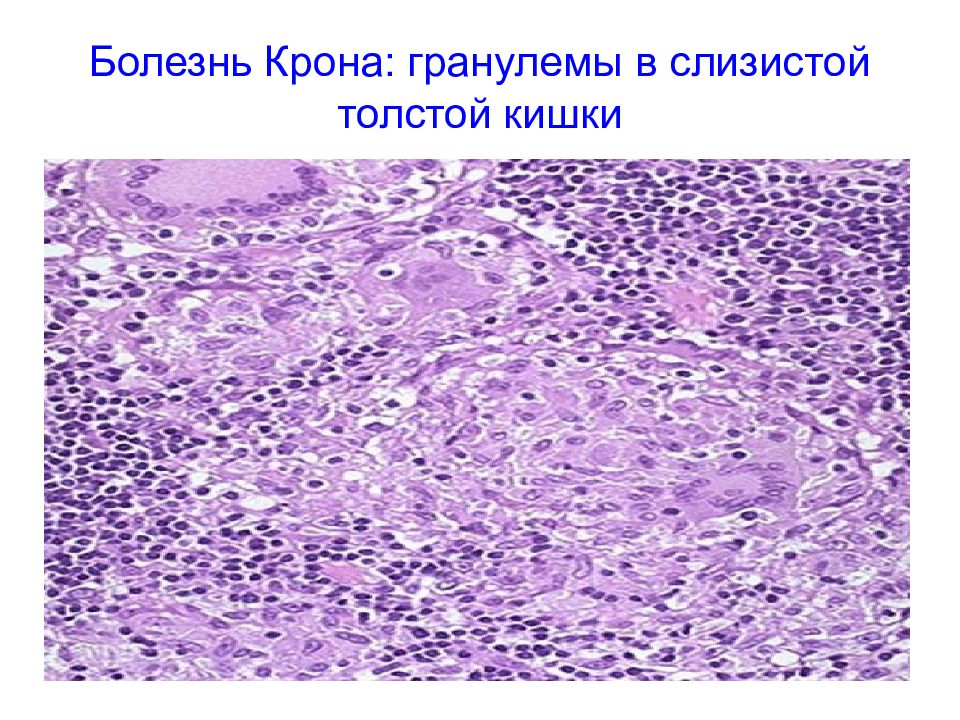
Болезнь Крона - хроническое рецидивирующее воспалительное заболевание ЖКТ с поражением слизистой оболочки и подслизистого слоя и образованием гранулем. Механизм патогенеза –ГЗТ. Современная терапия: Ведолизумаб - - гуманизированное моноклональное антитело, связывающееся с интегрин-альфа4-бета7 - белком клеточной мембраны, ответственным за миграцию иммунных клеток - лейкоцитов в слизистую оболочку кишечника, и тем самым блокирующее чрезмерную воспалительную реакцию в этой области.
Слайд 31: Волшебные пули»: моноклональные антитела в онкологии
Механизм действия антител можно рассмотреть на примере алемтузумаба (Кэмпаса) — препарата для терапии хронического лимфолейкоза. Вариабельный регион алемтузумаба соединяется с антигеном CD52 на поверхности лимфоцитов, а константный регион — с Fc-рецепторами на поверхности цитотоксических клеток, которые уничтожают мишень (антителозависимая клеточно-опосредованная цитотоксичность). Кэмпас активирует систему комплемента, что приводит к образованию комплекса, разрушающего мембрану злокачественной клетки (комплемент-зависимая цитотоксичность). Именно эти два механизма, а также индукция апоптоза считаются основными в действии данных антител.
Слайд 32: Лечение лихорадки Эбола
Джеймс Петтит из Института по изучению инфекционных заболеваний Армии США с коллегами смешал три типа моноклональных антител: 13F6, 13C6, 6D8. Коктейль был назван MB-003. Препарат в 100 процентах случаев излечивал зараженных вирусом Эбола приматов, если средство применяли в течение часа после инфицирования. 43 процента макак-резусов выздоровели, получив MB-003 спустя 104 часа с момента заражения. Джин Олингер, соавтор исследования, сообщил, что результаты позволяют определить MB-003 как средство лечения лихорадки Эбола. Антитела, входящие в состав коктейля, уничтожают как вирус, так и зараженные клетки. Побочных эффектов выявлено не было. Препарат будет востребован в странах Африки, где часто случаются вспышки лихорадки Эбола.
Слайд 33: Иммунный анализ –использование моноклональных антител
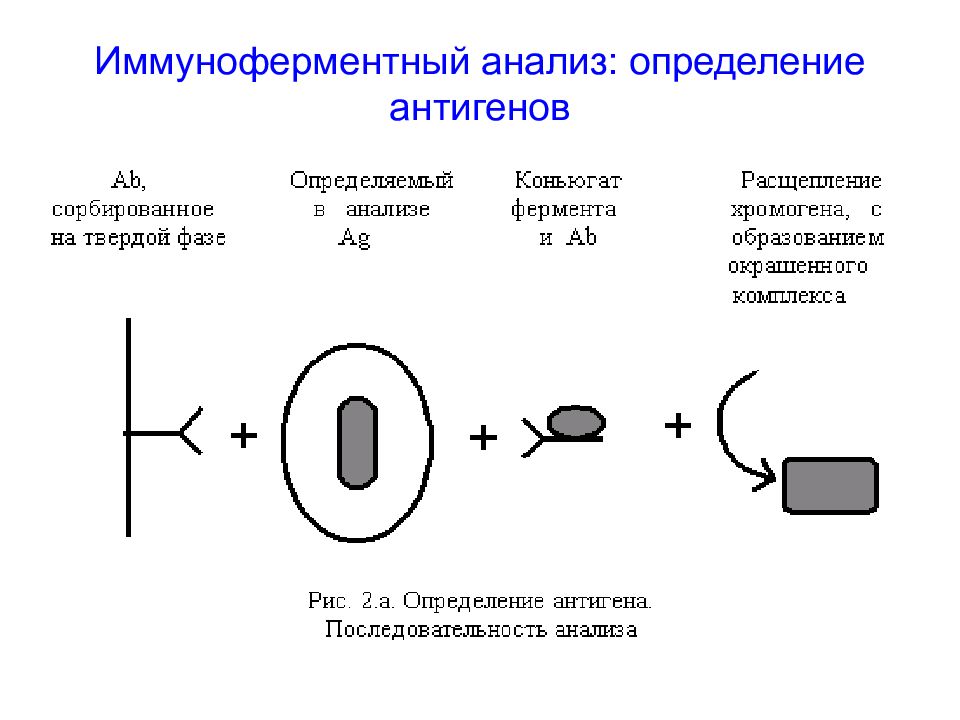
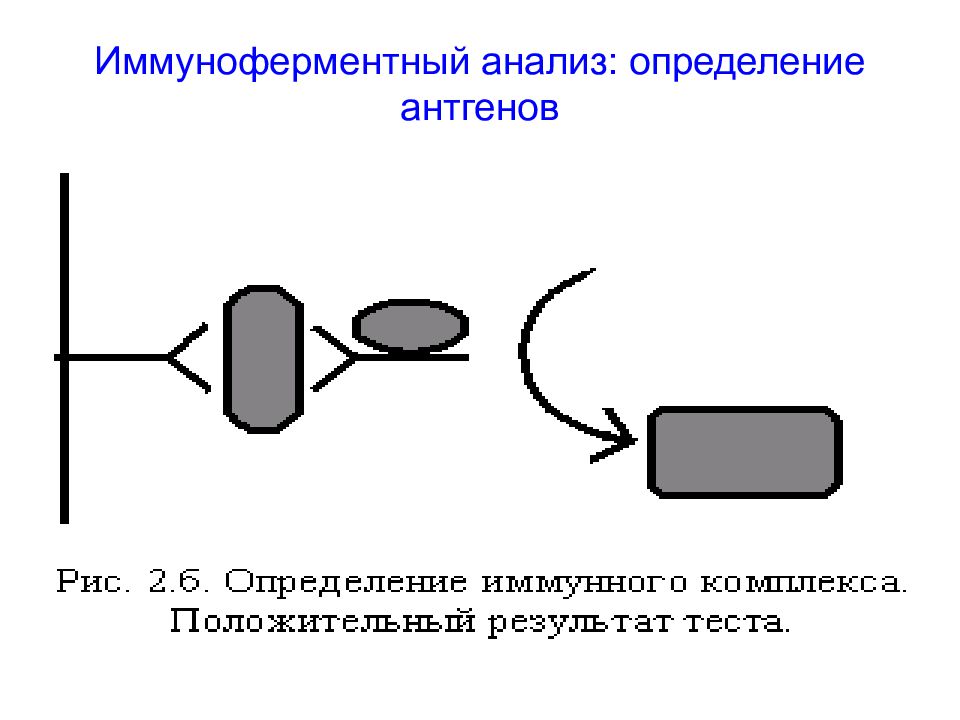
Для выполнения иммунного анализа используются моноклональные антитела, созданные к определенным антигенам. После образования иммунного комплекса с помощью большого разнообразия методов производится визуализация комплекса АГ-АТ с последующим определением количества искомого вещества (антигенов или антител).
Слайд 35: Исследование иммунной системы: иммунограмма и иммунный статус
Иммунограмма – карта первичного обследования иммунного статуса, отражающая основные показатели тестов оценки иммунной системы человека. Иммунный статус –комплекс количественных и функциональных показателей, отражающих конкретное состояние иммунной системы человека в данный момент времени, определяемое с помощью стандартизированных и разрешенных методов.
Слайд 36: Исследование иммунной системы: иммунодиагностика
Задачи: проведение лабораторных и клинических исследований, результаты которых позволяют выявить конкретные нарушения в иммунной системе.
Слайд 37: Исследование иммунной системы: двухуровневый подход
Для оценки состояния иммунной системы используют тесты двух уровней. Тесты первого уровня - ориентировочные, легкодоступные, выполняются в лечебных учреждениях общего профиля, не требуют дорогостоящего оборудования и реактивов. Тесты второго уровня – более углубленное исследование состояния иммунной системы в специализированных иммунологических лабораториях. Требующие дорогостоящей аппататуры, реактивов,
Слайд 38: Исследование иммунной системы: тесты первого уровня
Выявляют «грубые дефекты» клеточного и гуморального звена врожденного и адаптивного иммунитета: 1. Определение абсолютного и относительного числа лейкоцитов и лимфоцитов крови (клинический анализ крови) 2.Определение абсолютного и относительного числа: Т лимфоцитов ( CD 3+) ; В лимфоцитов ( CD 19 +) ; NK (натуральных киллеров) ( CD 16 / CD 5 6 +).
Слайд 39: Исследование иммунной системы: тесты первого уровня
3. Оценка субпопуляций Т лимфоцитов: CD 4 + -Т-хелперы; CD 8 + Т цитотоксический; отношение CD 4 +/ CD 8 + - иммунорегуляторный индекс. 4.Определение концентраций сывороточных иммуноглобулинов классов M ; G ; A. 5.Оценка фагоцитарной активности моноцитов и нейтрофилов. 6. Оценка бактерицидной активности фагоцитов (выработка кислородных радикалов). 7. Оценка активности комплемента.
Слайд 40: Исследование иммунной системы: тесты второго уровня
В зависимости от задач, стоящих перед лечащим врачом, тесты второго уровня могут варьировать. Цель выполнения тестов второго уровня- выявить причины иммунологических нарушений, выявленных с помощью тестов первого уровня.
Слайд 41: Исследование иммунной системы: тесты второго уровня
Определение числа Т хелперов 1,2,17 типов. Определение числа Т регуляторных лимфоцитов (естественных T reg и индуцированных – Th3). Определение числа γδ Т–лимфоцитов 4. В онкогематологии : определение фенотипа клеток на разных стадиях иммунопоэза (для уточнения стадии развития малигнизации). 5. Определение маркеров активации клеток: CD25 ; CD 69; CD 71; HLA-DR.
Слайд 42: Исследование иммунной системы: тесты второго уровня
7. Оценка пролиферативного ответа Т и В-лимфоцитов на митогены(поликлональные активаторы) или на конкретные антигены. 8. Изучение апоптоза в культуре лимфоцитов. 9. Определение цитокинов. 10. Различные этапы фагоцитоза и рецепторный аппарат фагоцитов. 11. Содержание различных компонентов системы комплемента.
Слайд 43: Исследование иммунной системы: тесты второго уровня
12. Активность киллеров (натуральных киллеров и цитотоксических Т лимфоцитов) с определением гназимов / перфоринов и осуществлением апоптоза через Fas/Fas L. 13. Оценка пролиферативного ответа Т и В-лимфоцитов на митогены (поликлональные активаторы) или на конкретные антигены. 14. Классы и подклассы иммуноглобулинов. 15. Определение цитокинов в различных биологических жидкостях.
Слайд 44: 3 вида патологических состояний по результатам оценки иммунного статуса
Без существенных изменений иммунного статуса. 2. С недостаточностью иммунного ответа( иммунодефицитные состояния). 3.С повышенной активацией иммунного ответа (аутоиммунные заболевания, аллергия, воспаление).
Слайд 45: 2. Патологические состояния по результатам оценки иммунного статуса: иммунодефицитные состояния
Основные термины и понятия: Первичная иммунологическая недостаточность (ПИН)- наследственно - обусловленные дефекты иммунной системы. Вторичная иммунологическая недостаточность (ВИН) –нарушения иммунной системы как у детей, так и у взрослых, не связанные с генетическими дефектами в иммунной системе.
Слайд 46: 3. Патологические состояния по результатам оценки иммунного статуса: состояния с повышенной активацией иммунного ответа (аутоиммунные заболевания, аллергия, воспаление)
Аутоиммунные заболевания – заболевания, в основе патогенеза которых лежит иммунный ответ, направленный против антигенов клеток и межклеточного вещества собственного организма. Аутоантигены – антигены собственного организма, не стимулирующие запуск иммунного ответа в норме.
Слайд 47: Патогенетический подход к оценке иммунной системы (1990 г. Ковальчук Л.В. И Чередеев А.Н.)
Лабораторная оценка ключевых этапов иммунного ответа, позволяющая установить уровень дефекта в иммунной системе. Изучают стадии иммунного ответа: Распознавание; Активация; Пролиферация; Дифференцировка; Эффекторные механизмы.
Слайд 48: 1. Оценка процессов распознавания
In vitro взаимодействие лимфоцитов с макрофагами, предварительно обработанными антигеном. Определение экспрессии молекул MHC II класса(презентация антигена). Выявление специфических CD 4+ и / или CD 8+ лимфоцитов. Смешаная культура лимфоцитов.
Слайд 49: 2. Оценка активации лимфоцитов
Экспрессия маркеров активации клеток: CD25 ; CD 69; CD 71; HLA-DR. Определение внутриклеточных сигнальных молекул, ядерных факторов транскрипции, активность ферментов и др. Уровни провоспалительных цитокинов в сыворотке крови и в биологических жидкостях.
Слайд 50: 3. Оценка эффекторных функций лимфоцитов
Тесты клеточной цитотоксичности. Образование иммуноглобулинов в культуре В лимфоцитов. Синтез цитокинов и ответ на них in vitro.
Слайд 51: Этиологический принцип оценки иммунного статуса
Выбор наиболее информативных тестов для оценки иммунного статуса в соответствии с этиологией заболевания Например: при вирусной этиологии следует изучать: Систему интерферонов. Активность цитотоксических клеток. Определение цитокинов ( TNF- α, IL-12 и др.)
Слайд 52: Этиологический принцип оценки иммунного статуса
При бактериальной природе заболевания следует изучать: Фагоцитарную и оксидативную активность фагоцитов. В-лимфоциты. Уровни иммуноглобулинов. Активность системы комплемента.
Слайд 53: Иммунограмма
Набор тестов, позволяющий в целом оценить состояние основных звеньев иммунитета : Фагоцитарное звено Т- клеточный ответ Гуморальный ответ
Слайд 54: Методы оценки иммунограммы
Все иммунологические методы, адаптированные к клинической практике, подразделяются на : Скрининговые – позволяют установить те или иные нарушения функционировании иммунной системы. Уточняющие – позволяют объяснить механизмы таких нарушений.
Слайд 55: Методы оценки иммунограммы: система фагоцитов (нейтрофилов)
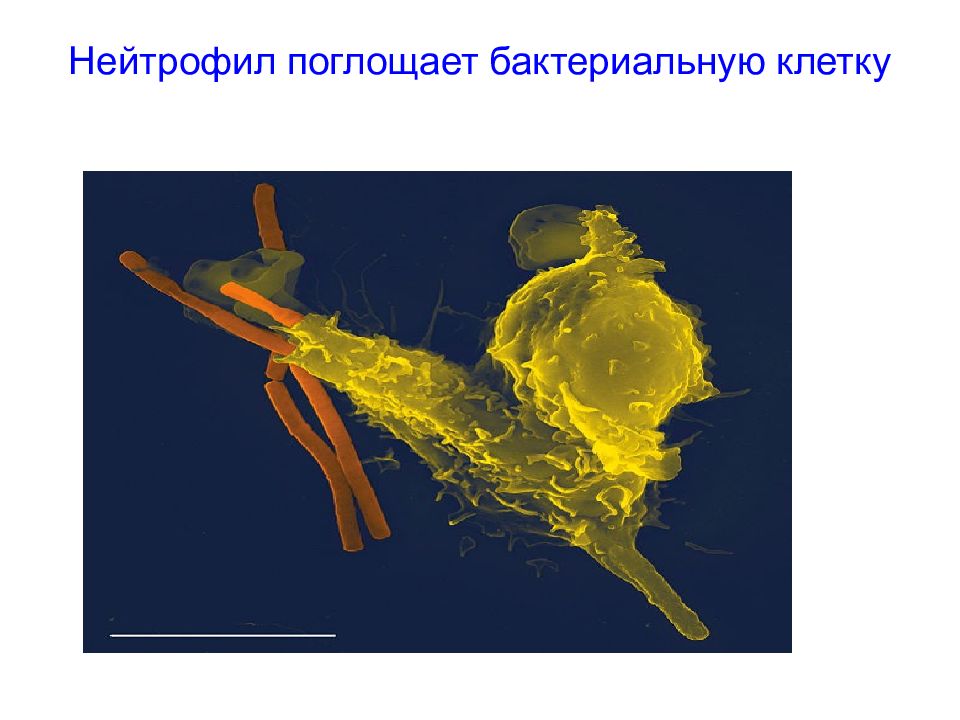
СКРИНИНГОВЫЕ МЕТОДЫ Оценка абсолютного числа нейтрофилов Исследование интенсивности фагоцитоза (Фагоцитарное число – % фагоцитирующих клеток, Фагоцитарный индекс – среднее число частиц, поглощенных одной клеткой). Бактерицидность (по НСТ - тесту или с помощью метода хемилюминесценции).
Слайд 57: Система нейтрофилов
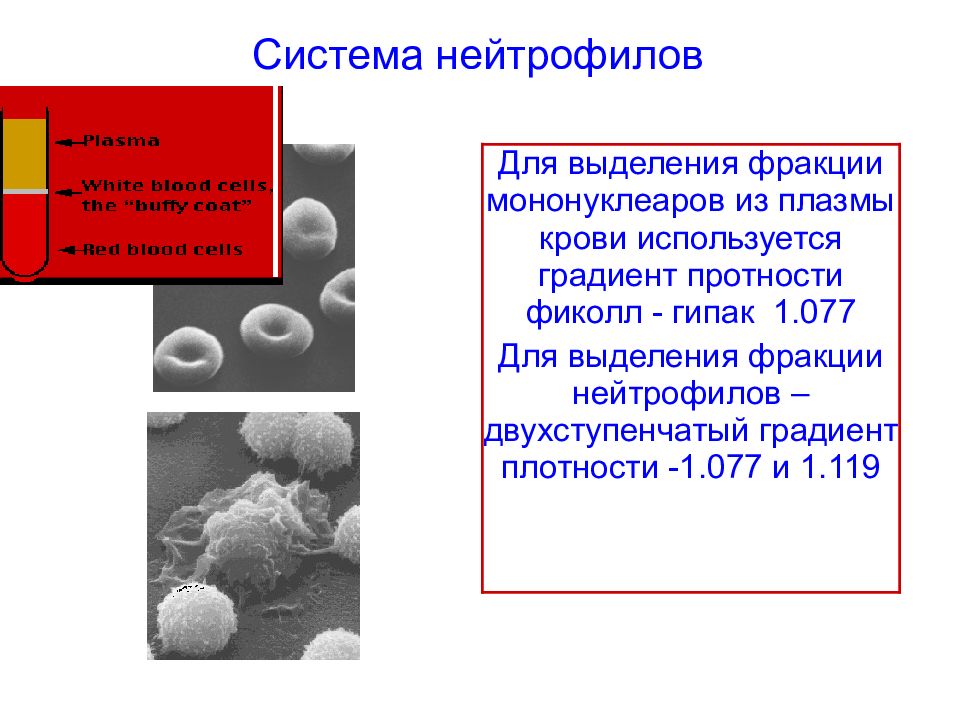
Для выделения фракции мононуклеаров из плазмы крови используется градиент протности фиколл - гипак 1.077 Для выделения фракции нейтрофилов –двухступенчатый градиент плотности -1.077 и 1.119
Слайд 58: Система нейтрофилов
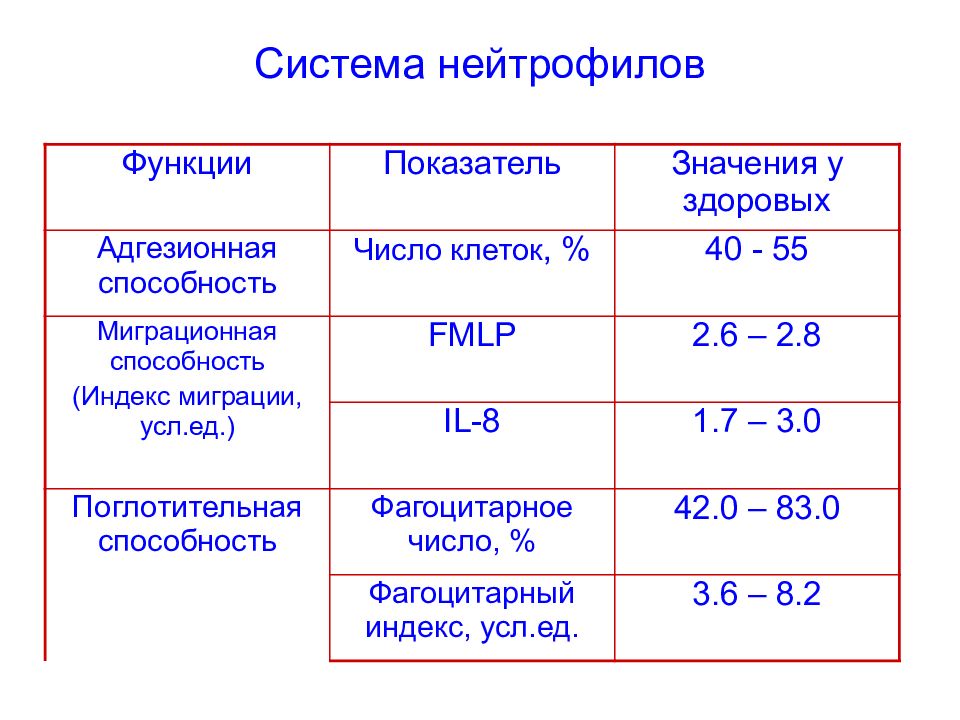
Функции Показатель Значения у здоровых Адгезионная способность Число клеток, % 40 - 55 Миграционная способность (Индекс миграции, усл.ед.) FMLP 2.6 – 2.8 IL-8 1.7 – 3.0 Поглотительная способность Фагоцитарное число, % 42.0 – 83.0 Фагоцитарный индекс, усл.ед. 3.6 – 8.2
Слайд 59: Система нейтрофилов
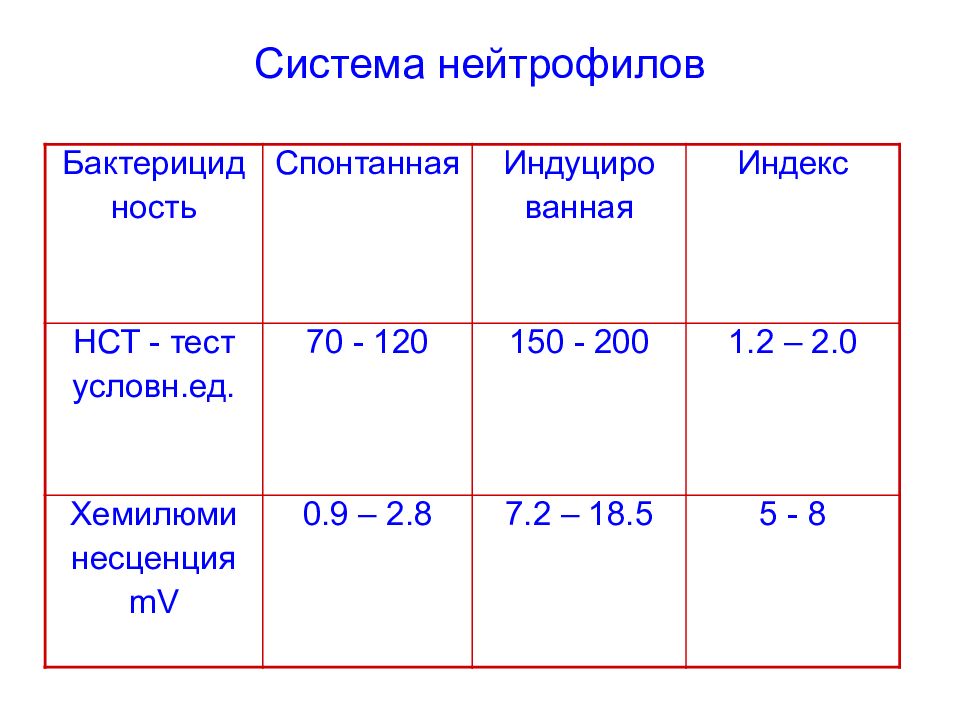
Бактерицид ность Спонтанная Индуциро ванная Индекс НСТ - тест условн.ед. 70 - 120 150 - 200 1.2 – 2.0 Хемилюми несценция mV 0.9 – 2.8 7.2 – 18.5 5 - 8
Слайд 60: Методы оценки иммунограммы: система фагоцитов (нейтрофилов)
УТОЧНЯЮЩИЕ МЕТОДЫ Оценка интенсивности хемотаксиса (направленной миграции клеток) Исследование адгезионной способности нейтрофилов к пластику, либо исследование интенсивности экспрессии адгезионных молекул на поверхности клетки ( CD11/CD18).
Слайд 61: Методы оценки иммунограммы: система Т- лимфоцитов
СКРИНИНГОВЫЕ МЕТОДЫ Определение общего числа лимфоцитов Определение процентного и абсолютного числа зрелых Т-лимфоцитов ( CD3 + клеток) и двух основных популяций – CD4 +(хелперов) и CD8 + (цитотоксических) клеток. Исследование ответа Т-лимфоцитов в реакции бласттрансформации (РБТЛ) –то есть оценка способности Т клеток к делению (клональной экспансии).
Слайд 62: Методы оценки иммунограммы: система Т- лимфоцитов
УТОЧНЯЮЩИЕ МЕТОДЫ Определение маркеров активации Т-лимфоцитов – экспрессии CD25 (рецептор к интерлейкину 2) и молекул HLA II класса на поверхностной мембране т лимфоцитов. Исследование продукции цитокинов. Изучение пролиферативного ответа Т ллимфоцитов в реакции бласттрансформации на специфические антигены.
Слайд 63: Методы оценки иммунограммы: система В- лимфоцитов
СКРИНИНГОВЫЕ МЕТОДЫ Определение процентного и абсолютного числа В-лимфоцитов ( CD 19+ клеток). Определение уровней «неспецифических» иммуноглобулинов классов А, M, G, E в сыворотке крови. Определение циркулирующих иммунных комплексов. Исследование пролиферативной активности В - лимфоцитов в РБТЛ на В - клеточные митогены.
Слайд 64: Методы оценки иммунограммы: система В- лимфоцитов
УТОЧНЯЮЩИЕ МЕТОДЫ Определение «специфических» (т.е. выработанных на конкретный антиген) иммуноглобулинов классов А, M, G, E в сыворотке крови. Определение продукции цитокинов Определение секреторного иммуноглобулина класса А ( s IgA).
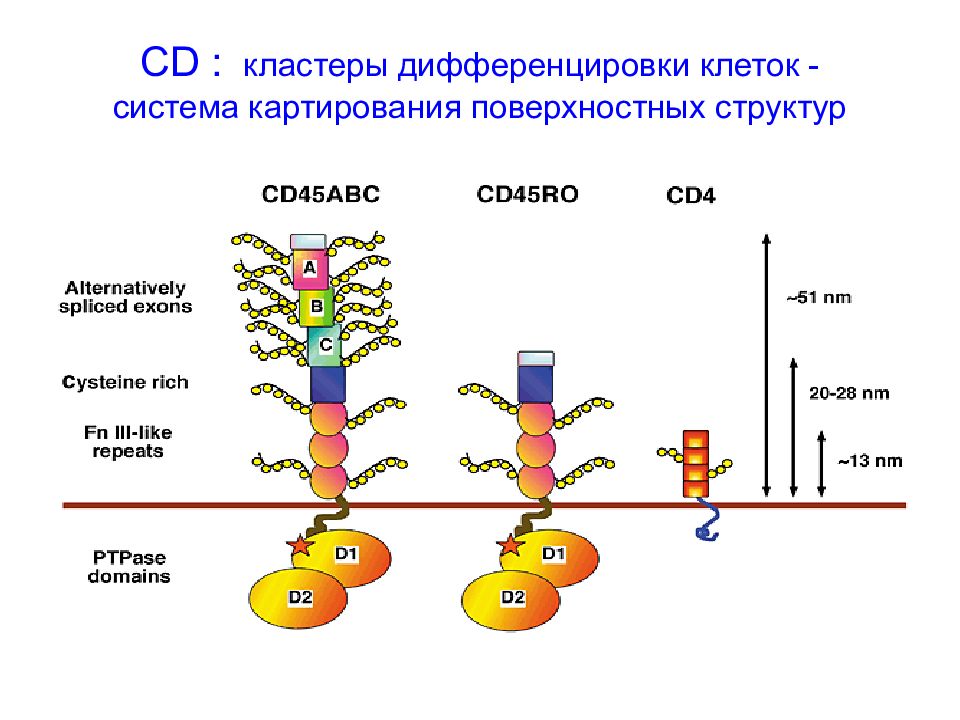
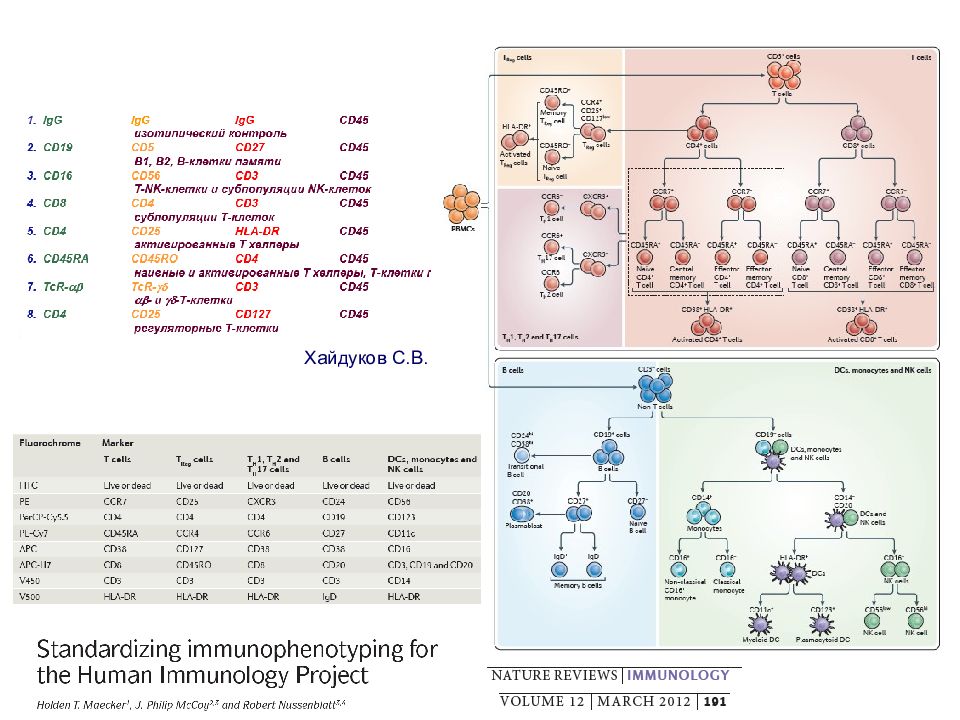
Слайд 65: CD : кластеры дифференцировки клеток - система картирования поверхностных структур
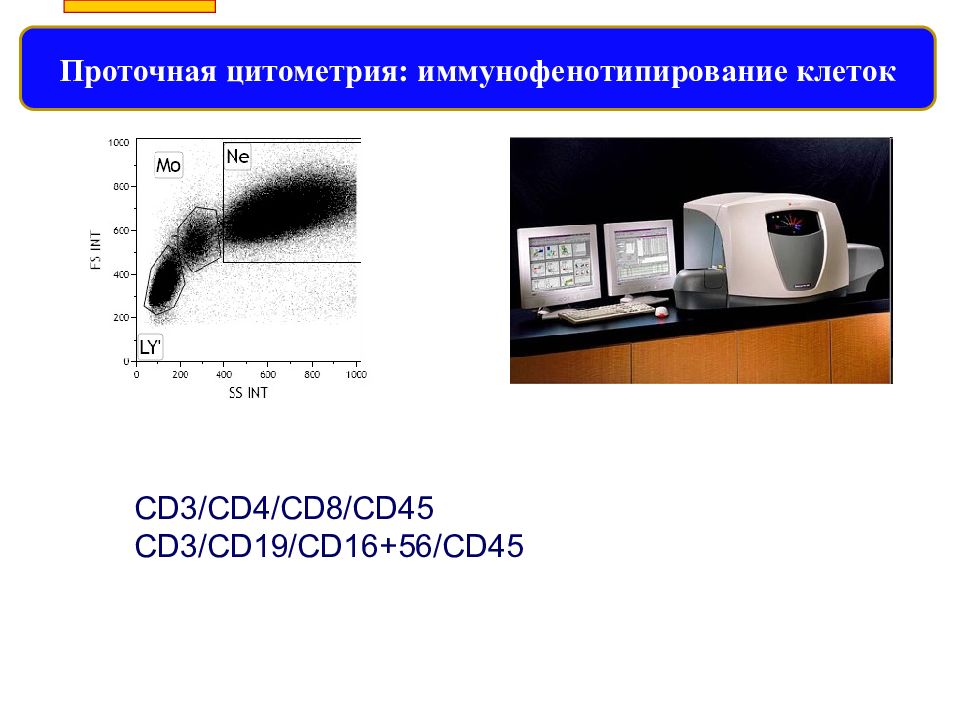
Слайд 66
Проточная цитометрия : иммунофенотипирование клеток CD 3/ CD 4/ CD 8/ CD 45 CD 3/ CD 19/ CD 16+56/ CD 45
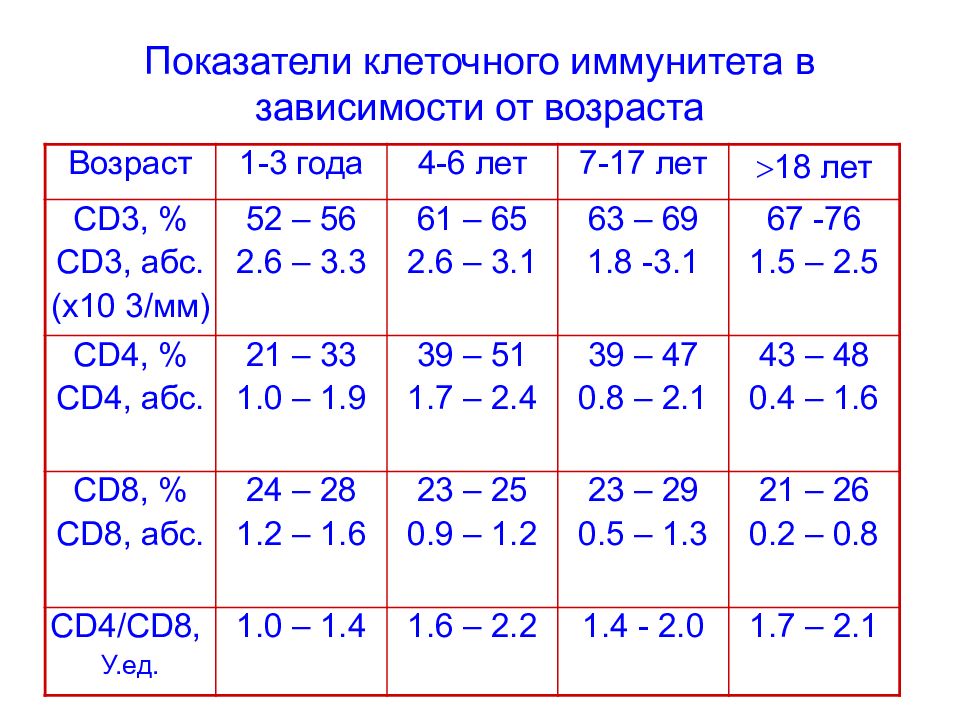
Слайд 68: Показатели клеточного иммунитета в зависимости от возраста
Возраст 1-3 года 4-6 лет 7-17 лет 18 лет CD3, % CD3, абс. (х10 3/мм) 52 – 56 2.6 – 3.3 61 – 65 2.6 – 3.1 63 – 69 1.8 -3.1 67 -76 1.5 – 2.5 CD 4, % CD 4, абс. 21 – 33 1.0 – 1.9 39 – 51 1.7 – 2.4 39 – 47 0.8 – 2.1 43 – 48 0.4 – 1.6 CD 8, % CD 8, абс. 24 – 28 1.2 – 1.6 23 – 25 0.9 – 1.2 23 – 29 0.5 – 1.3 21 – 26 0.2 – 0.8 CD 4/ CD 8, У.ед. 1.0 – 1.4 1.6 – 2.2 1.4 - 2.0 1.7 – 2.1
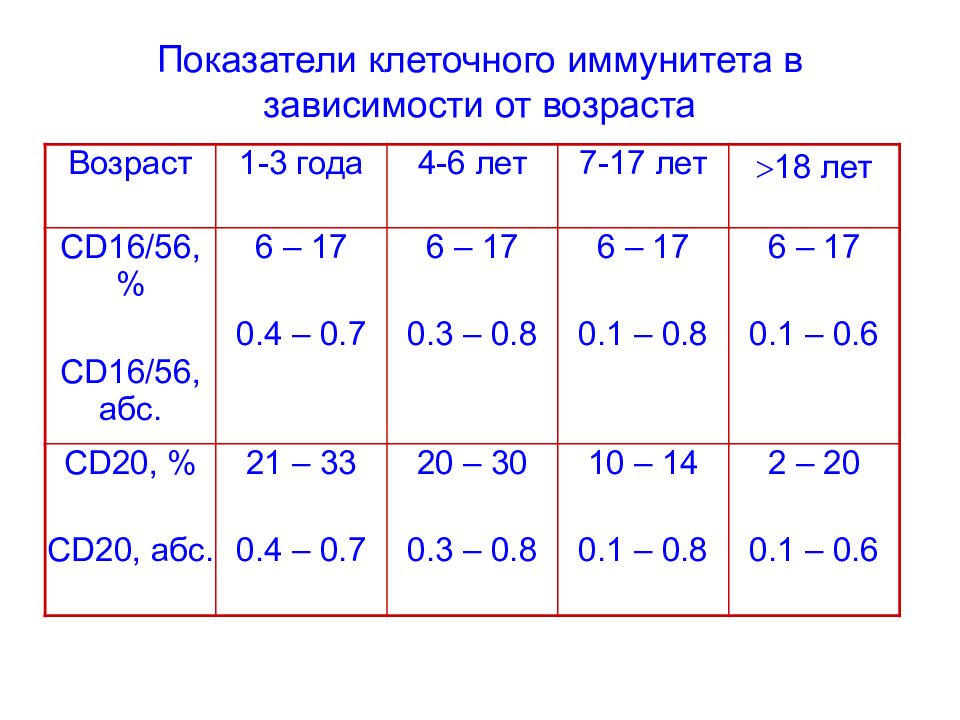
Слайд 69: Показатели клеточного иммунитета в зависимости от возраста
Возраст 1-3 года 4-6 лет 7-17 лет 18 лет CD 16 / 56, % CD 16 / 56, абс. 6 – 17 0.4 – 0.7 6 – 17 0.3 – 0.8 6 – 17 0.1 – 0.8 6 – 17 0.1 – 0.6 CD 20, % CD 20, абс. 21 – 33 0.4 – 0.7 20 – 30 0.3 – 0.8 10 – 14 0.1 – 0.8 2 – 20 0.1 – 0.6
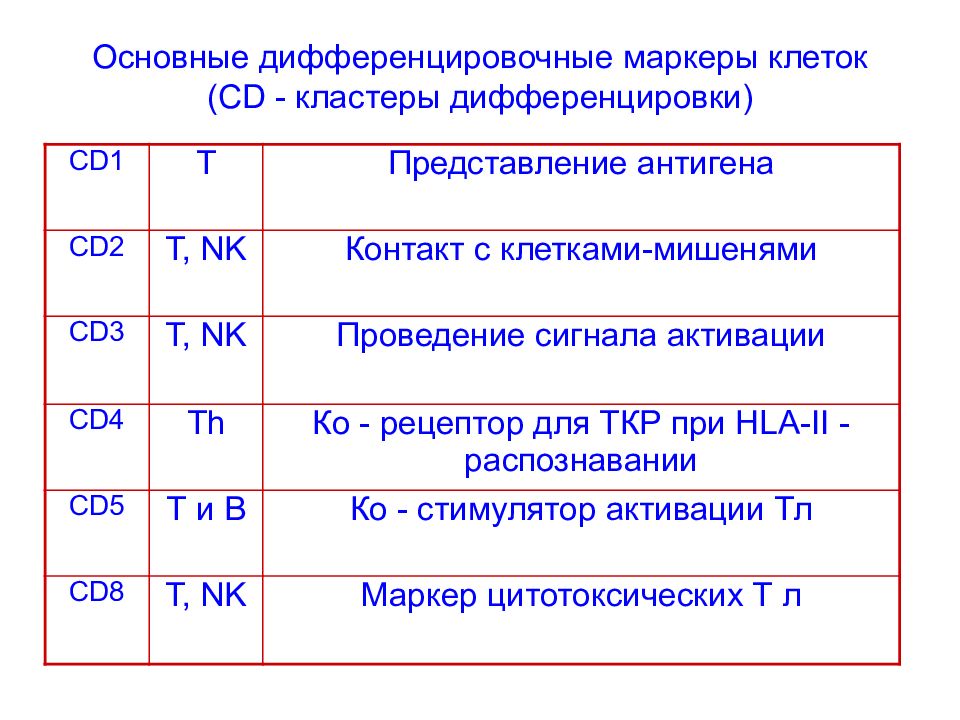
Слайд 70: Основные дифференцировочные маркеры клеток ( CD - кластеры дифференцировки)
CD 1 Т Представление антигена CD 2 T, NK Контакт с клетками-мишенями CD 3 T, NK Проведение сигнала активации CD 4 Th Ко - рецептор для ТКР при HLA-II -распознавании CD 5 Т и В Ко - стимулятор активации Тл CD 8 T, NK Маркер цитотоксических Т л
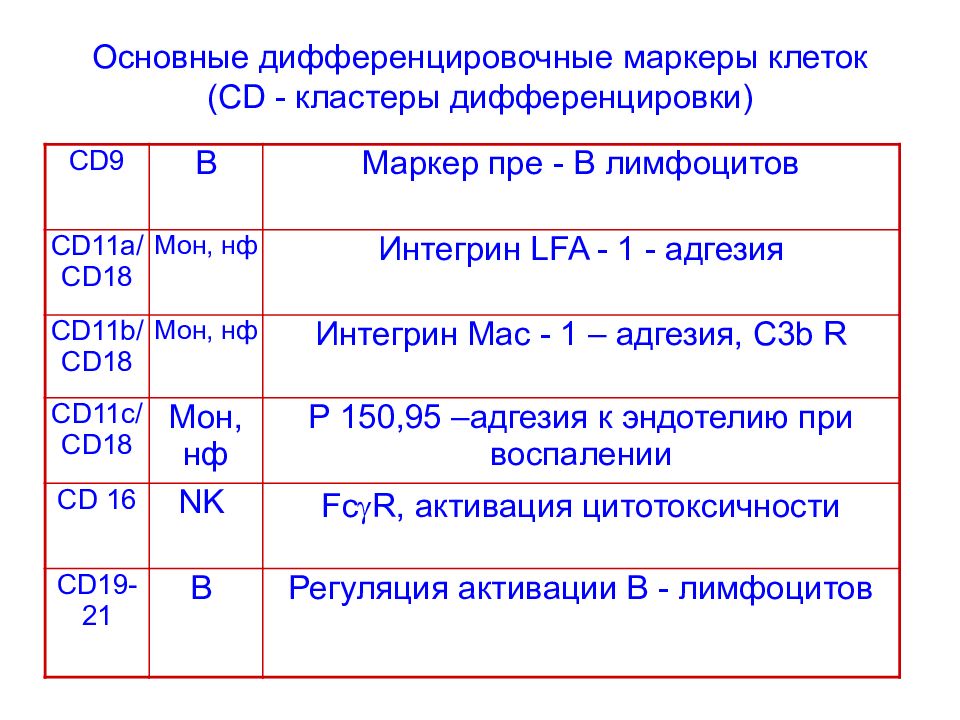
Слайд 71: Основные дифференцировочные маркеры клеток ( CD - кластеры дифференцировки)
CD 9 B Маркер пре - В лимфоцитов CD 11а/ CD 18 Мон, нф Интегрин LFA - 1 - адгезия CD 11 b / CD 18 Мон, нф Интегрин Mac - 1 – адгезия, C3b R CD 11 c / CD 18 Мон, нф Р 150,95 –адгезия к эндотелию при воспалении CD 16 NK Fc R, активация цитотоксичности CD 19-21 В Регуляция активации В - лимфоцитов
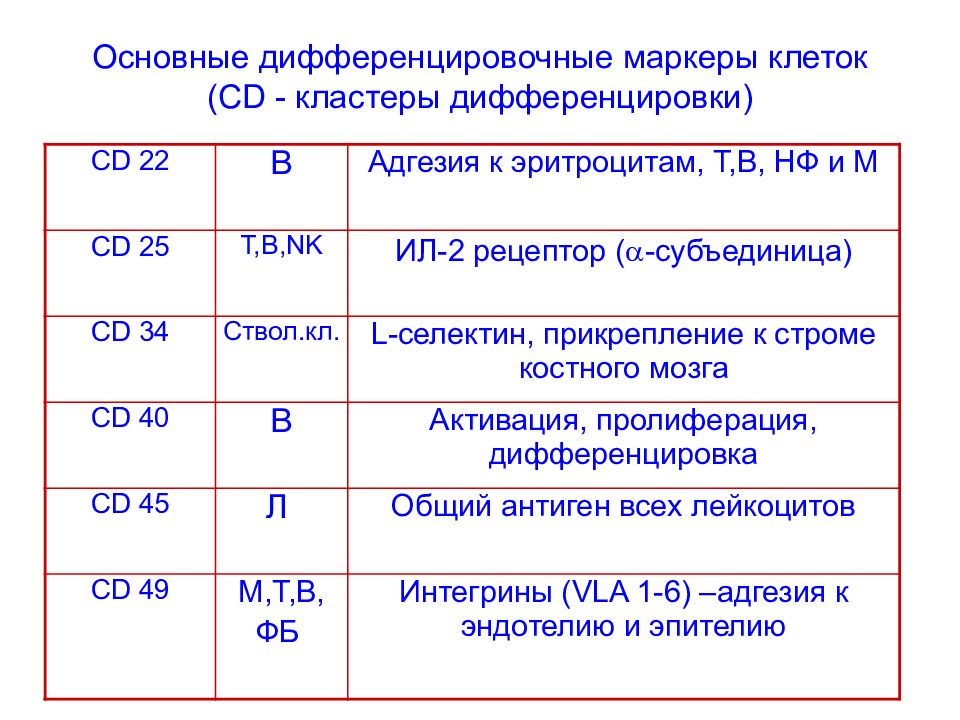
Слайд 72: Основные дифференцировочные маркеры клеток ( CD - кластеры дифференцировки)
CD 22 B Адгезия к эритроцитам, Т,В, НФ и М CD 25 Т,В, NK ИЛ-2 рецептор ( -субъединица) CD 34 Ствол.кл. L- селектин, прикрепление к строме костного мозга CD 40 В Активация, пролиферация, дифференцировка CD 45 Л Общий антиген всех лейкоцитов CD 49 М,Т,В, ФБ Интегрины ( VLA 1-6) – адгезия к эндотелию и эпителию
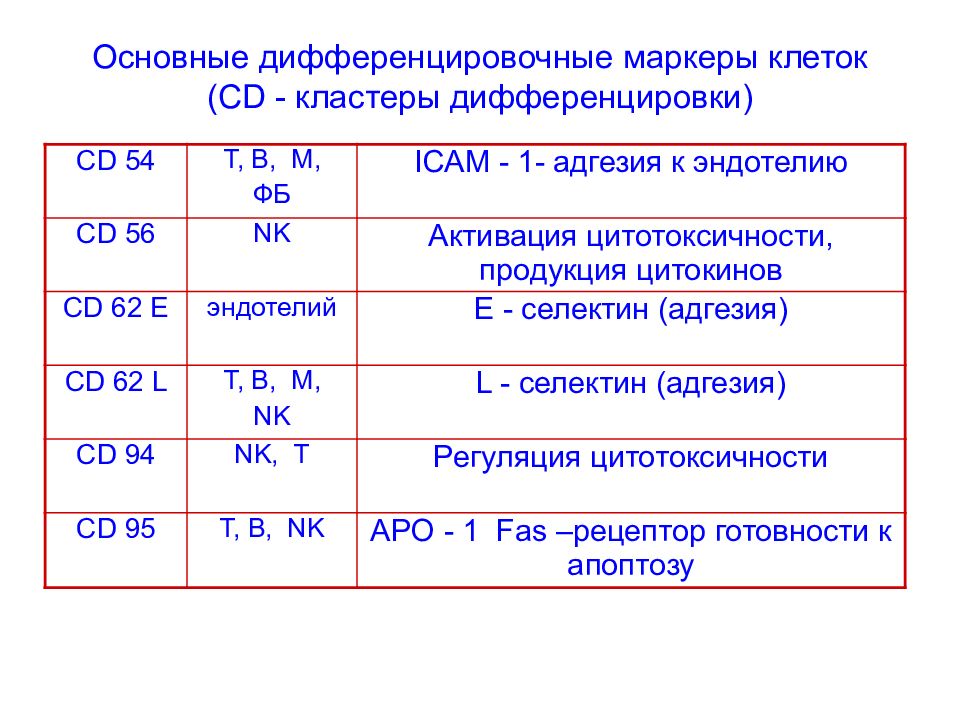
Слайд 73: Основные дифференцировочные маркеры клеток ( CD - кластеры дифференцировки)
CD 54 Т, В, М, ФБ ICAM - 1 - адгезия к эндотелию CD 56 NK Активация цитотоксичности, продукция цитокинов CD 62 Е эндотелий Е - селектин (адгезия) CD 62 L Т, В, М, NK L - селектин (адгезия) CD 94 NK, Т Регуляция цитотоксичности CD 95 Т, В, NK APO - 1 Fas –рецептор готовности к апоптозу
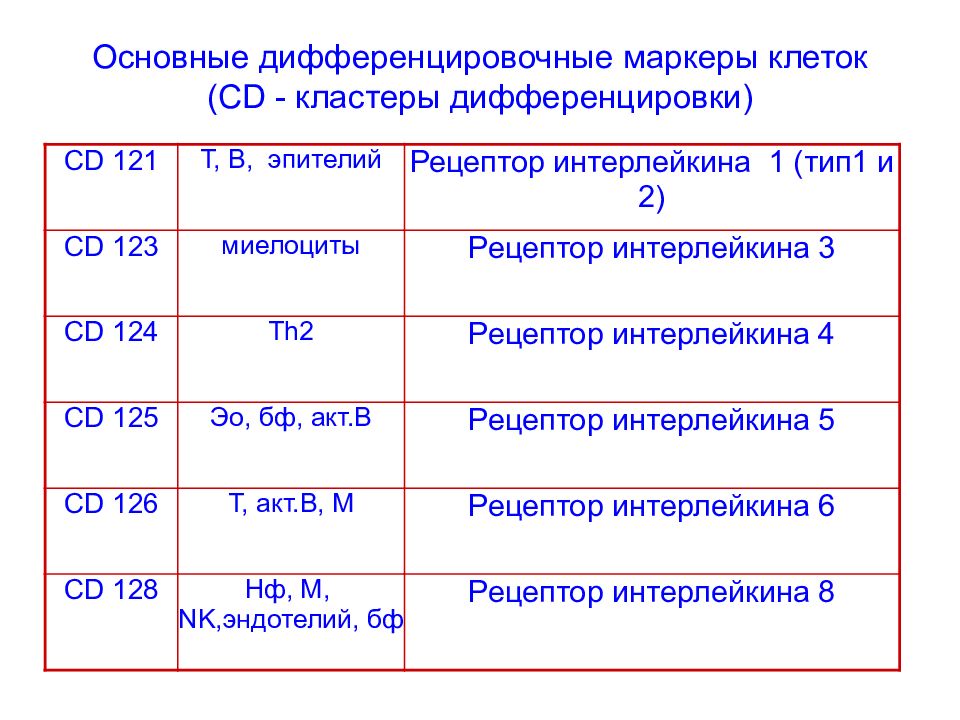
Слайд 74: Основные дифференцировочные маркеры клеток ( CD - кластеры дифференцировки)
CD 121 Т, В, эпителий Рецептор интерлейкина 1 (тип1 и 2) CD 123 миелоциты Рецептор интерлейкина 3 CD 124 Th2 Рецептор интерлейкина 4 CD 125 Эо, бф, акт.В Рецептор интерлейкина 5 CD 126 Т, акт.В, М Рецептор интерлейкина 6 CD 128 Нф, М, NK,эндотелий, бф Рецептор интерлейкина 8
Слайд 75: Скрининг - Т- клеточного звена иммунитета
Т- клеточный иммунодефицит характеризуется: CD3+, CD 4 +, CD4 + /CD8 +, CD25 + Активация иммунной системы характеризуется : CD25 +, HLA II Переключение ответа с Th 1 на Th 2: CD 19+ (косвенно). Аутоиммунный компонент: CD4 + /CD8 + (за счет миграции CD8 + в орган-мишень), CD 16 / 56+
Слайд 76: Методы оценки гуморального звена иммунитета
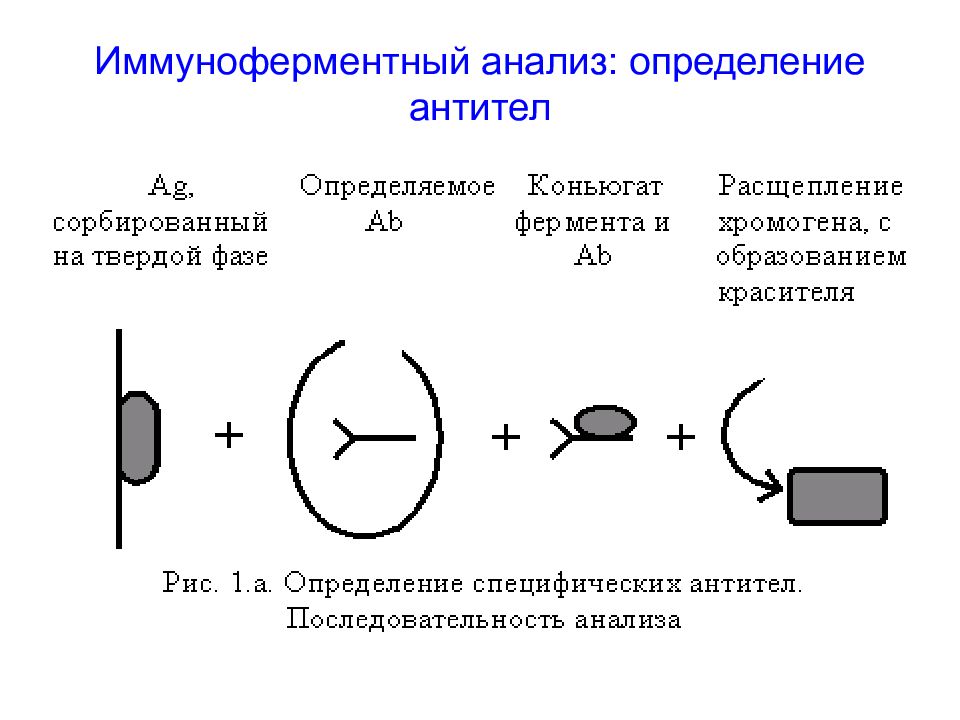
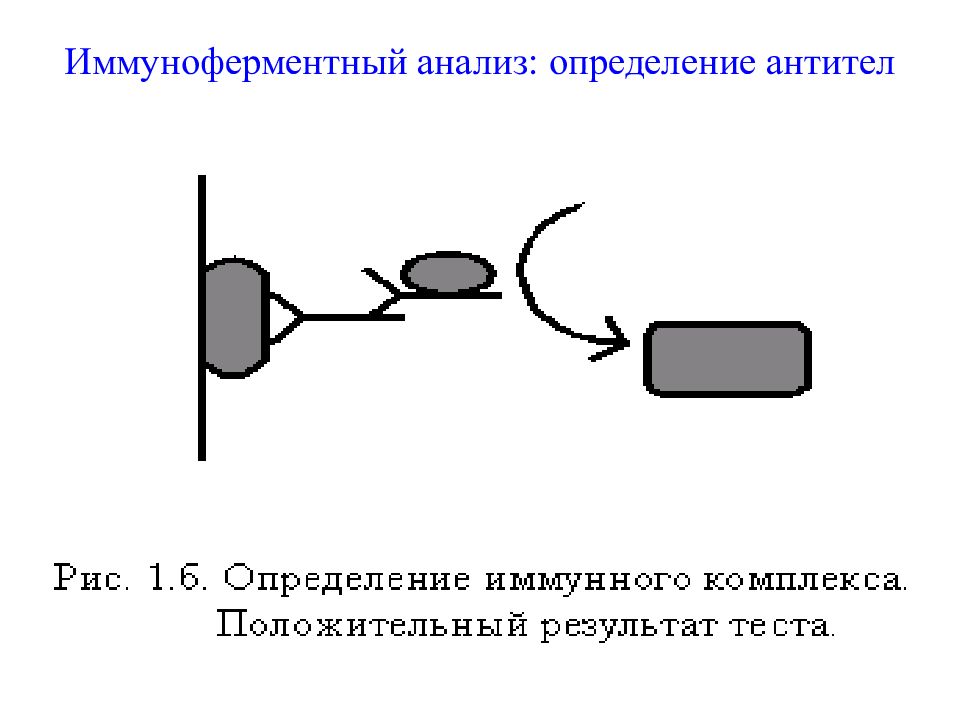
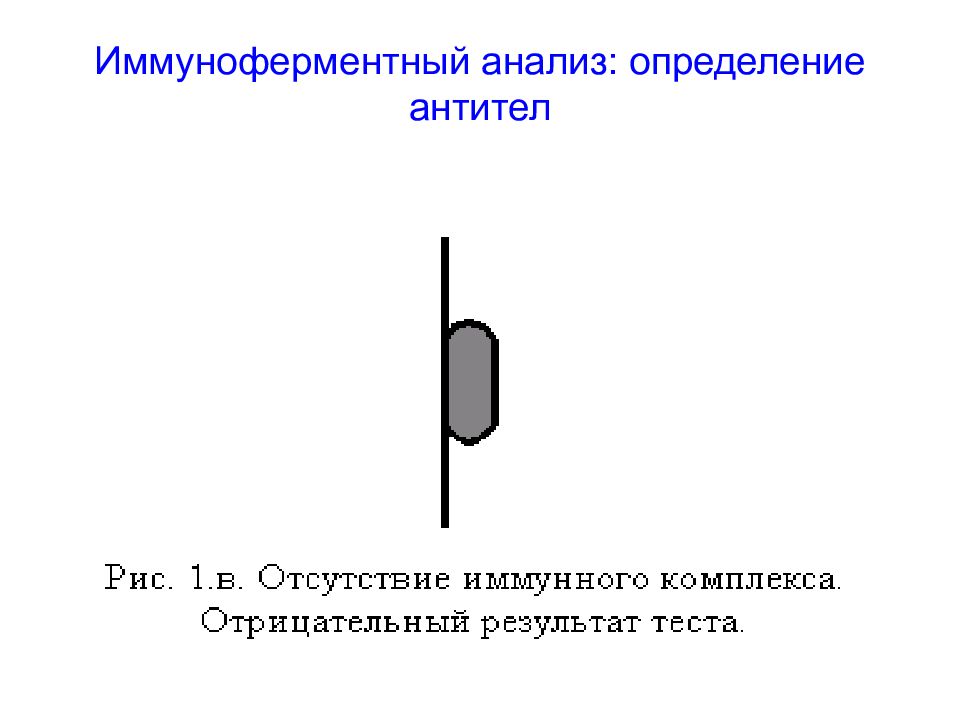
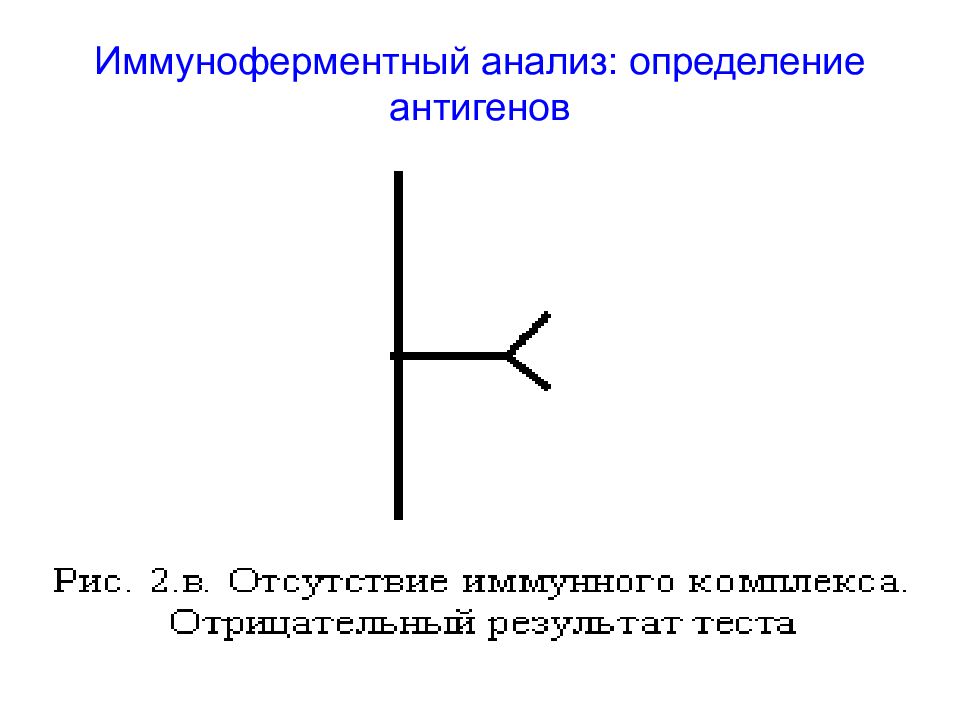
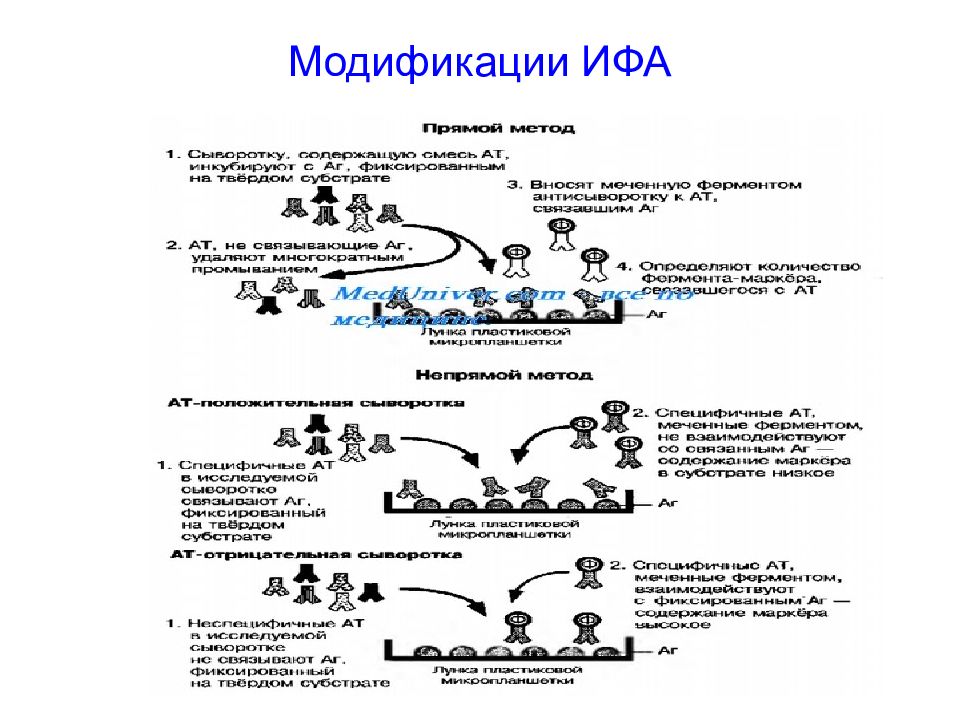
Метод иммуноферментного анализа (ИФА) основан на реакции антиген-антитело и используется для регистрации либо антигенов, либо антител – в зависимости от задач. Для регистрации комплексов АГ-АТ используются флуоресцентные методы, хемилюминесцентные, электрохимические и др.
Слайд 77: Полистироловый 96 - луночный планшет для иммуноферментного анализа (твердая фаза)
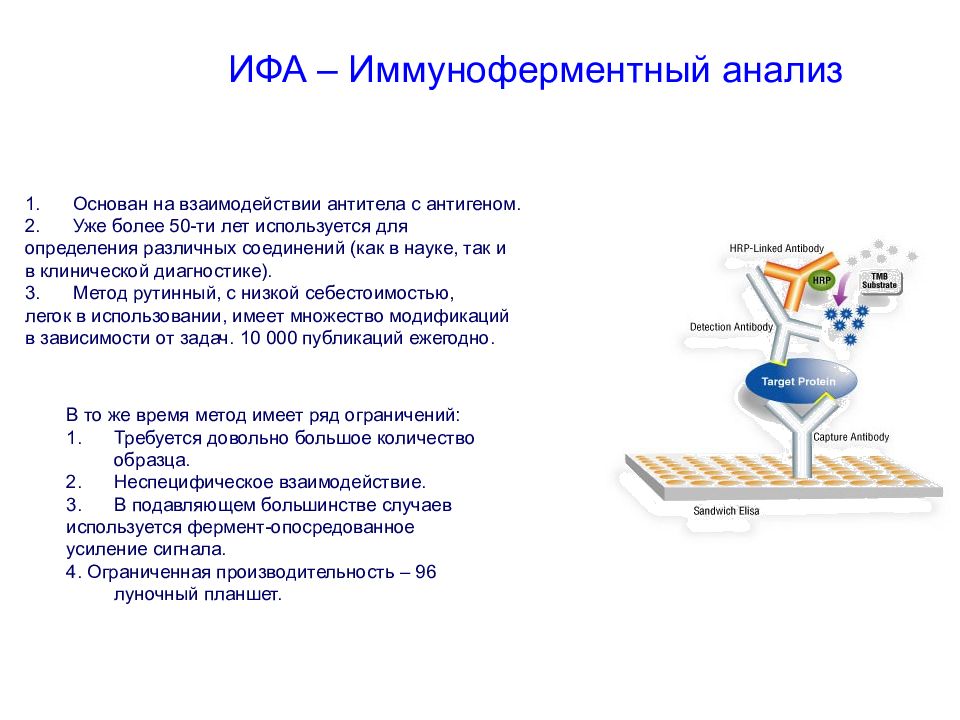
Слайд 85: ИФА – Иммуноферментный анализ
Основан на взаимодействии антитела с антигеном. Уже более 50-ти лет используется для определения различных соединений (как в науке, так и в клинической диагностике). Метод рутинный, с низкой себестоимостью, легок в использовании, имеет множество модификаций в зависимости от задач. 10 000 публикаций ежегодно. В то же время метод имеет ряд ограничений: Требуется довольно большое количество образца. Неспецифическое взаимодействие. В подавляющем большинстве случаев используется фермент-опосредованное усиление сигнала. 4. Ограниченная производительность – 96 луночный планшет.
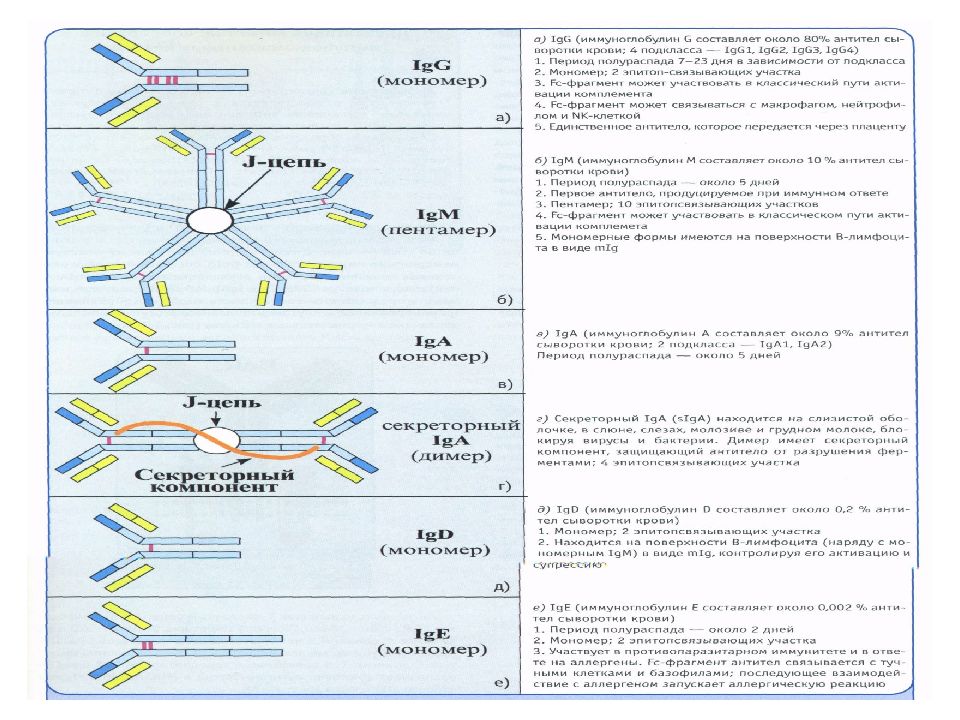
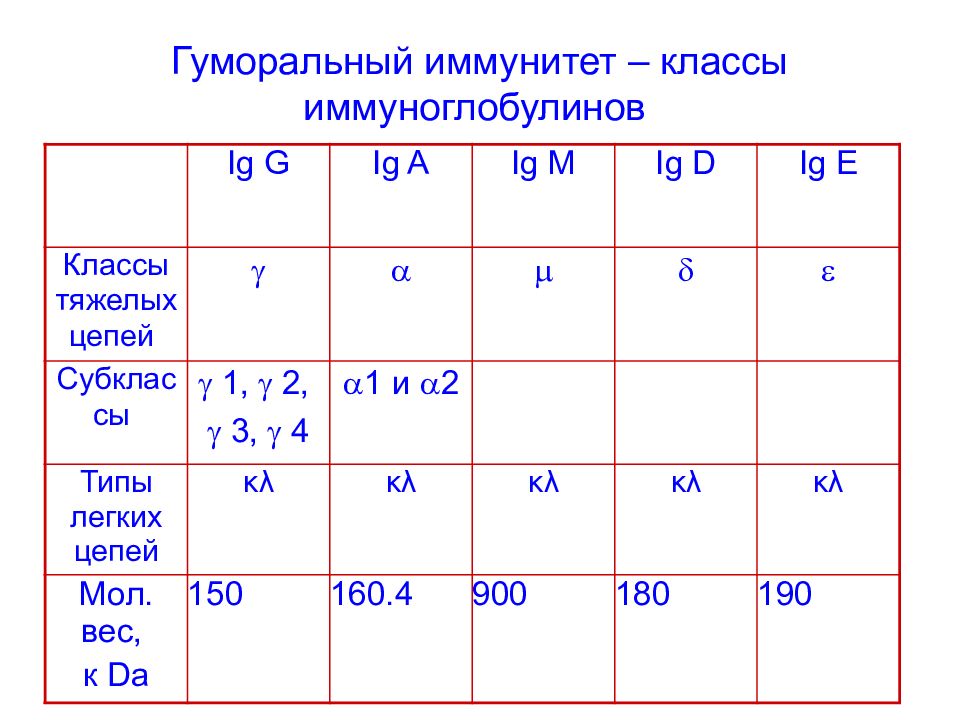
Слайд 87: Гуморальный иммунитет – классы иммуноглобулинов
Ig G Ig A Ig M Ig D Ig E Классы тяжелых цепей Субклас сы 1, 2, 3, 4 1 и 2 Типы легких цепей κλ κλ κλ κλ κλ Мол. вес, к Da 150 160.4 900 180 190
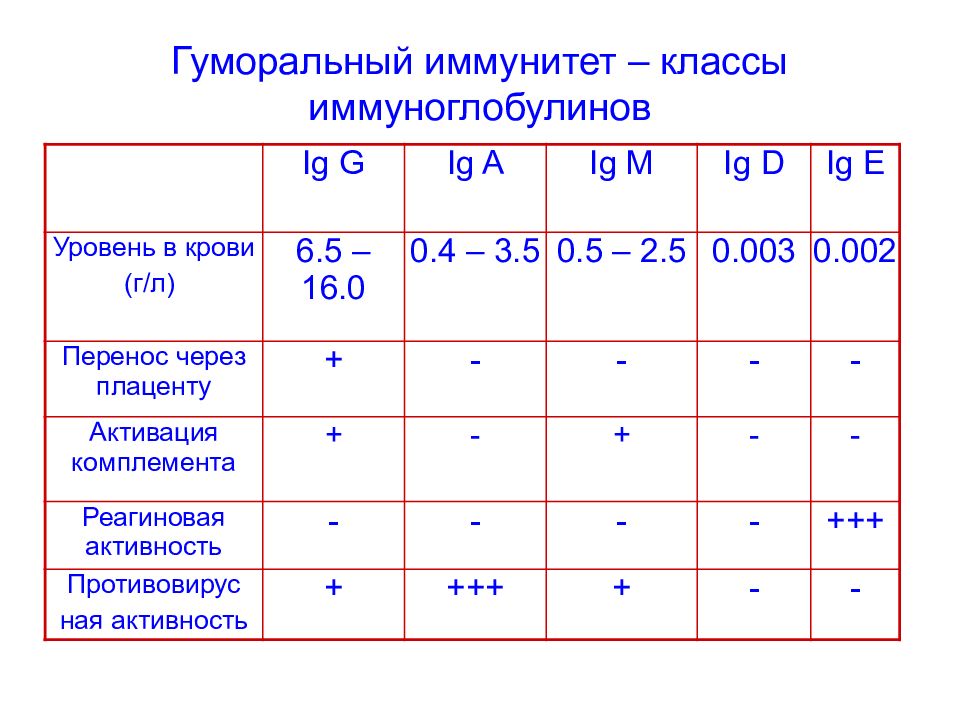
Слайд 88: Гуморальный иммунитет – классы иммуноглобулинов
Ig G Ig A Ig M Ig D Ig E Уровень в крови (г/л) 6.5 – 16.0 0.4 – 3.5 0.5 – 2.5 0.003 0.002 Перенос через плаценту + - - - - Активация комплемента + - + - - Реагиновая активность - - - - +++ Противовирус ная активность + +++ + - -
Слайд 89: Субклассы иммуноглобулина G
АнтиВИЧ, анти HBs, против вируса гепатита С - антитела - IgG1/IgG3. Против гриппа, парагриппа, вируса Эпштейн-Барр- IgG1/IgG3. После курса вакцинации к HBs -антигену – IgG 4 –антитела.
Слайд 90: Субклассы иммуноглобулина G
На Т- зависимые белковые антигены вырабатываются IgG1/IgG3 субклассы (вирусные белки) На Т- независимые полисахаридные антигены – IgG2 (бактерии) При длительной стимуляции белковыми антигенами могут вырабатываться IgG 4 антитела
Слайд 91: Субклассы иммуноглобулина G
При паразитарных заболеваниях: Митогенная стимуляция продуктами жизнедеятельности гельминтов В-лимфоцитов (поликлональная активация) –истощение, иммуносупрессия Спектр антител –различен в зависимости от жизненного цикла паразита.
Слайд 92: Субклассы иммуноглобулина G
При паразитарных заболеваниях: Токсоплазмозы – IgG 3 и IgG 4; Эхинококкозы – IgG 4; Аскаридозы - IgG 4; При токсокарозах – IgG 1 и IgG 2.
Слайд 93: Субклассы иммуноглобулина G
Антитела к бактериям при туберкулезе - IgG1 При сифилисе - IgG1/IgG3 К H.Pylori – все 4 подкласса IgG
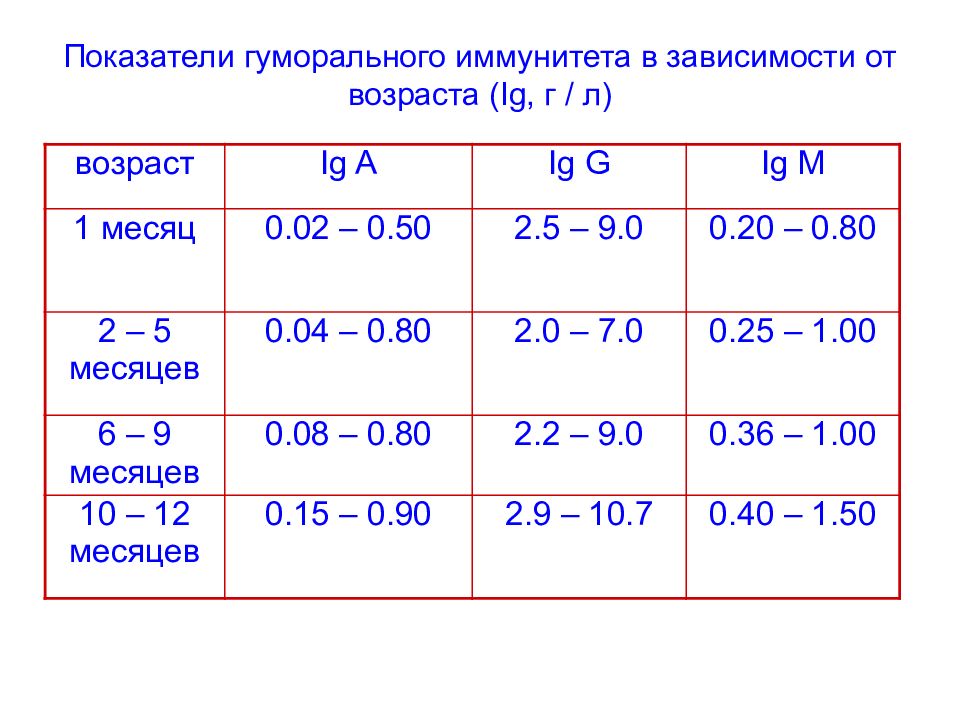
Слайд 94: Показатели гуморального иммунитета в зависимости от возраста (Ig, г / л)
возраст Ig A Ig G Ig M 1 месяц 0.02 – 0.50 2.5 – 9.0 0.20 – 0.80 2 – 5 месяцев 0.04 – 0.80 2.0 – 7.0 0.25 – 1.00 6 – 9 месяцев 0.08 – 0.80 2.2 – 9.0 0.36 – 1.00 10 – 12 месяцев 0.15 – 0.90 2.9 – 10.7 0.40 – 1.50
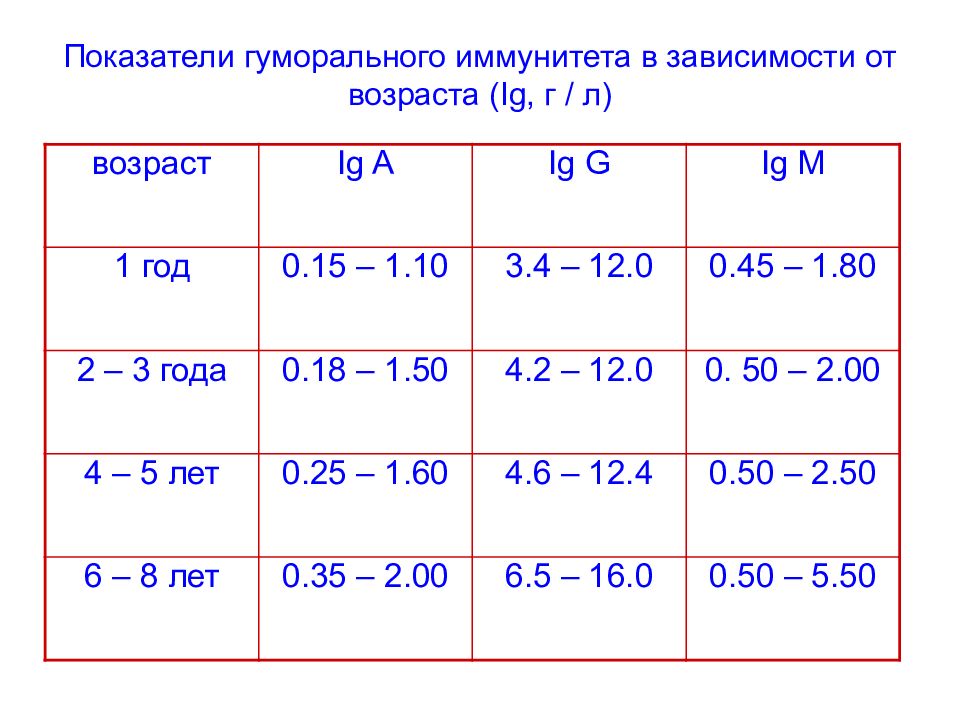
Слайд 95: Показатели гуморального иммунитета в зависимости от возраста (Ig, г / л)
возраст Ig A Ig G Ig M 1 год 0.15 – 1.10 3.4 – 12.0 0.45 – 1.80 2 – 3 года 0.18 – 1.50 4.2 – 12.0 0. 50 – 2.00 4 – 5 лет 0.25 – 1.60 4.6 – 12.4 0.50 – 2.50 6 – 8 лет 0.35 – 2.00 6.5 – 16.0 0.50 – 5.50
Слайд 96: Показатели гуморального иммунитета в зависимости от возраста ( Ig, г / л)
Возраст Ig A Ig G Ig M 9 – 12 лет 0.45 – 2.50 6.5 – 16.0 0. 5 – 2.5 > 12 лет 0.45 – 3.50 6.5 – 16.0 0. 5 – 2.5
Слайд 97: Определение иммунных комплексов
Иммунные комплексы это комплексы антигенов с антителами. Удержание иммунных комплексов в растворимом состоянии обеспечивается действием классического пути активации комплемента.
Слайд 98: Уровни иммунных комплексов у здоровых лиц
Возраст 3 – 5 лет 6 – 8 лет 9 – 11 лет старше 12 лет ЦИК, % 59 - 112 48 - 96 49 - 100 51 - 120
Слайд 99: Иммунные комплексы
Белки комплемента снижают число антигеннных эпитопов (т.е. валентность антигена), с которыми могут связаться антитела. Это приводит к уменьшению размера комплексов и делает их растворимыми. Такие содержащие компоненты комплемента иммунные комплексы легко связываются с C 3 b -рецепторами на поверхности эритроцитов.
Слайд 100: Иммунные комплексы
Иммунные комплексы, связанные с эритроцитами, реже оказывают повреждающее действие, эффективно элиминируются макрофагами в селезенке и печени. При недостаточности системы комплемента клиренс из организма иммунных комплексов нарушается.
Слайд 101: Иммунные комплексы
Иммунные комплексы, не связанные с эритроцитами, активно поглощаются печенью, затем высвобождаются вновь и откладываются в таких тканях, как кожа, почки, мышцы, вызывая в них воспалительные реакции.
Слайд 102: Иммунные комплексы
Крупные иммунные комплексы хорошо фиксируют комплемент и быстро связываются с эритроцитами, вследствие чего они, как правило, уже в течение нескольких минут извлекаются из кровотока. Мелкие иммунные комплексы образуются при избытке антигена в условиях активного воспалительного процесса.
Слайд 103: Иммунные комплексы
Они остаются циркулировать в крови более длительный период времени. При определенных условиях, зависящих от особенности кровотока в органе-мишени, классов иммуноглобулинов, формирующих иммунные комплексы, электрических зарядов антител и антигенов и ряда других - могут откладываться в различных органах и тканях.
Слайд 104: Иммунные комплексы
Откладываться ИК могут, например, в почечных клубочках, в легочной ткани, вызывая воспалительные реакции. Длительное отложение иммунных комплексов на эндотелии приводит к развитию «болезней иммунных комплексов»-с активацией системы комплемента, нейтрофилов, разрушением собственных тканей.
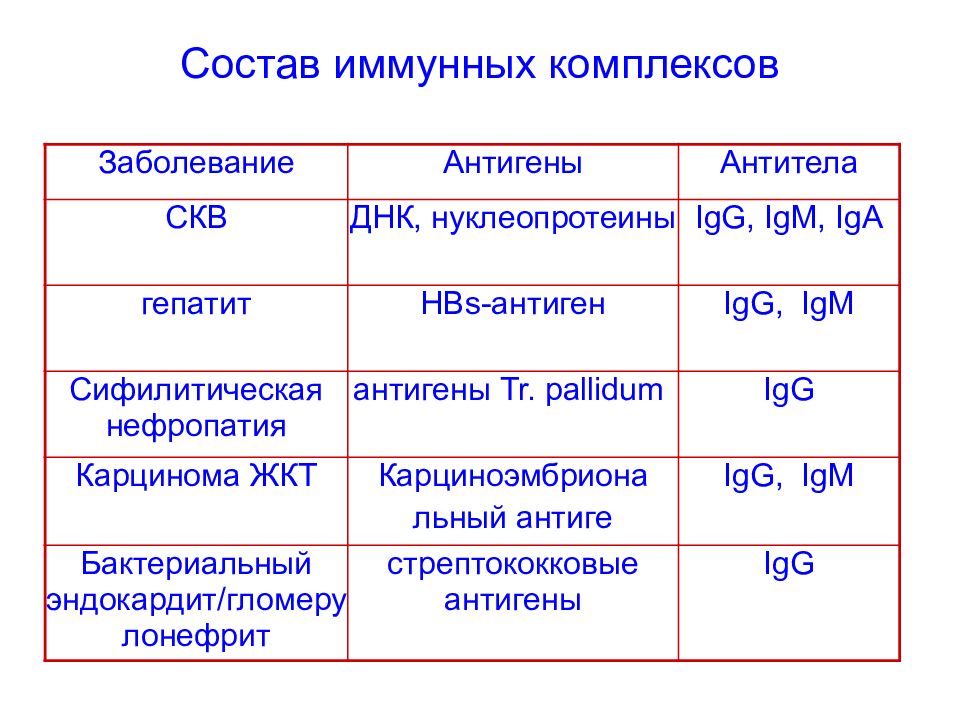
Слайд 105: Состав иммунных комплексов
Заболевание Антигены Антитела СКВ ДНК, нуклеопротеины IgG, IgM, IgA гепатит HBs -антиген IgG, IgM Сифилитическая нефропатия антигены Tr. pallidum IgG Карцинома ЖКТ Карциноэмбриона льный антиге IgG, IgM Бактериальный эндокардит/гломерулонефрит стрептококковые антигены IgG
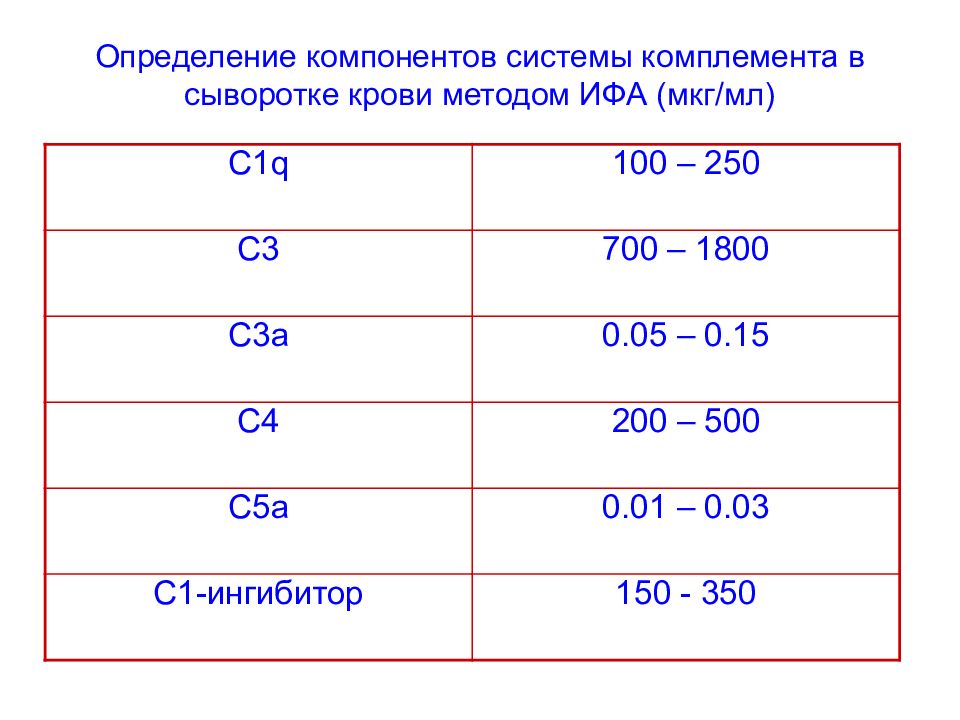
Слайд 106: Определение компонентов системы комплемента в сыворотке крови методом ИФА (мкг/мл)
C1q 100 – 250 C3 700 – 1800 C3a 0.05 – 0.15 C4 200 – 500 C5a 0.01 – 0.03 C1 -ингибитор 150 - 350
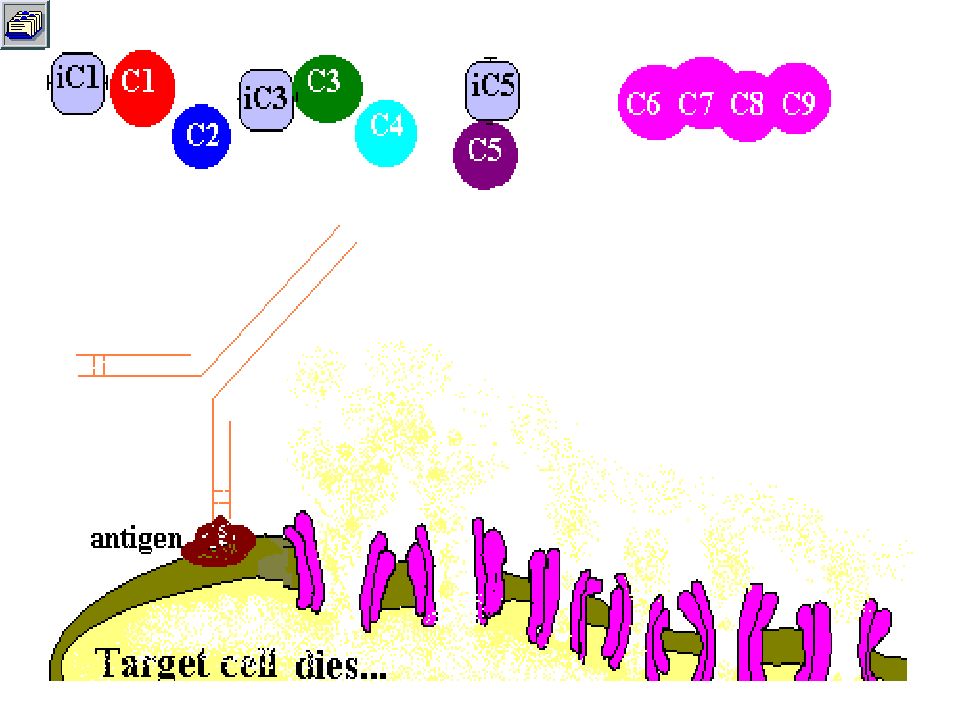
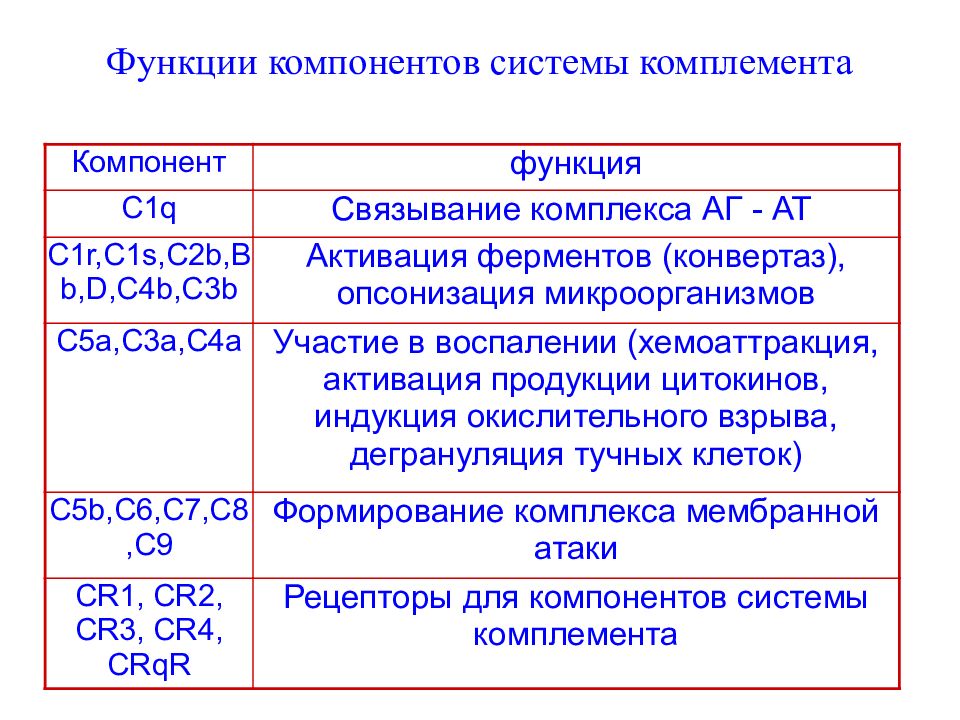
Слайд 108: Функции компонентов системы комплемента
Компонент функция C1q Связывание комплекса АГ - АТ C1r,C1s,C2b,Bb,D,C4b,C3b Активация ферментов (конвертаз), опсонизация микроорганизмов C5a,C3a,C4a Участие в воспалении (хемоаттракция, активация продукции цитокинов, индукция окислительного взрыва, дегрануляция тучных клеток) C5b,C6,C7,C8,C9 Формирование комплекса мембранной атаки CR1, CR 2, CR 3, CR 4, CRqR Рецепторы для компонентов системы комплемента
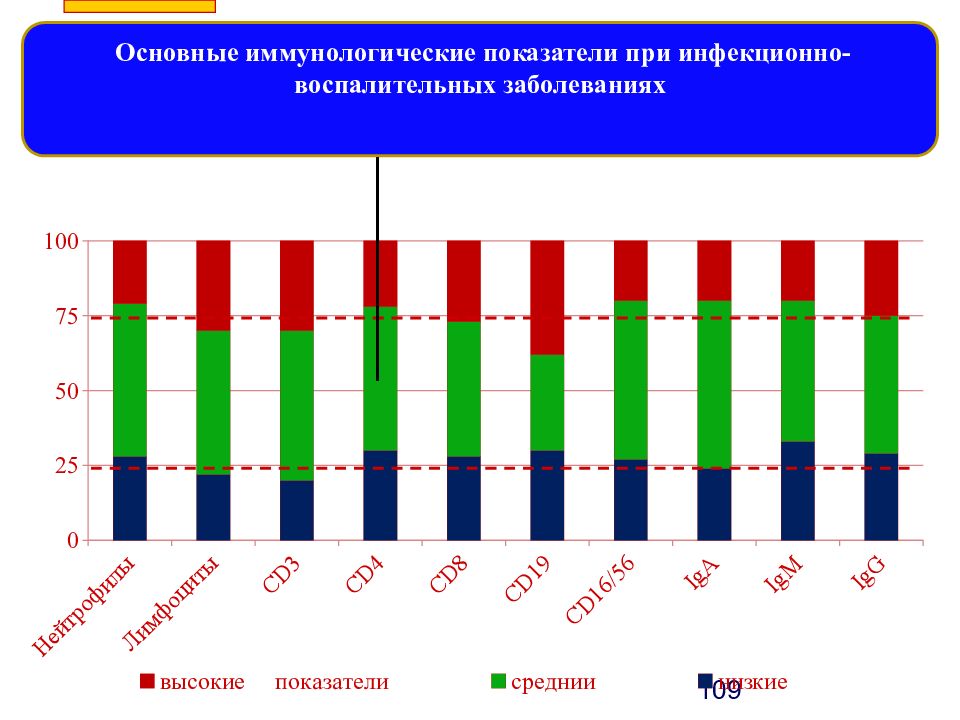
Слайд 109
Основные иммунологические показатели при инфекционно-воспалительных заболеваниях 109
Слайд 110: Биологический материал для определения концентрации цитокинов ( мультиплексный анализ)
Периферическая кровь сыворотка крови плазма крови (ЭДТА) Биологические жидкости цереброспинальная жидкость секреты смывы моча и т.д. Экстракты тканей
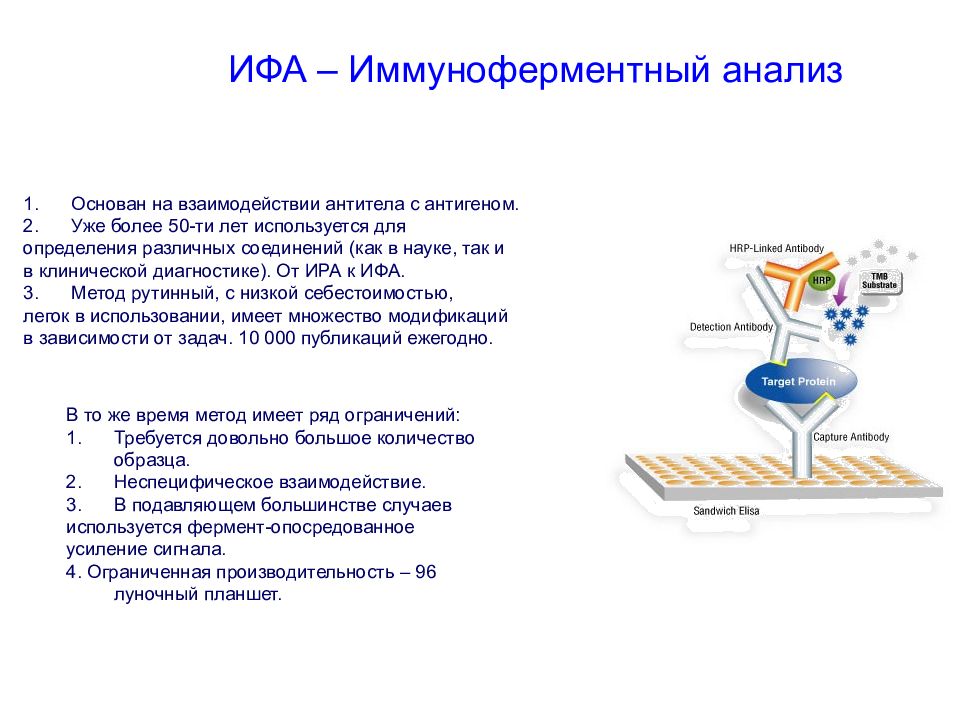
Слайд 111: ИФА – Иммуноферментный анализ
Основан на взаимодействии антитела с антигеном. Уже более 50-ти лет используется для определения различных соединений (как в науке, так и в клинической диагностике). От ИРА к ИФА. Метод рутинный, с низкой себестоимостью, легок в использовании, имеет множество модификаций в зависимости от задач. 10 000 публикаций ежегодно. В то же время метод имеет ряд ограничений: Требуется довольно большое количество образца. Неспецифическое взаимодействие. В подавляющем большинстве случаев используется фермент-опосредованное усиление сигнала. 4. Ограниченная производительность – 96 луночный планшет.
Слайд 112
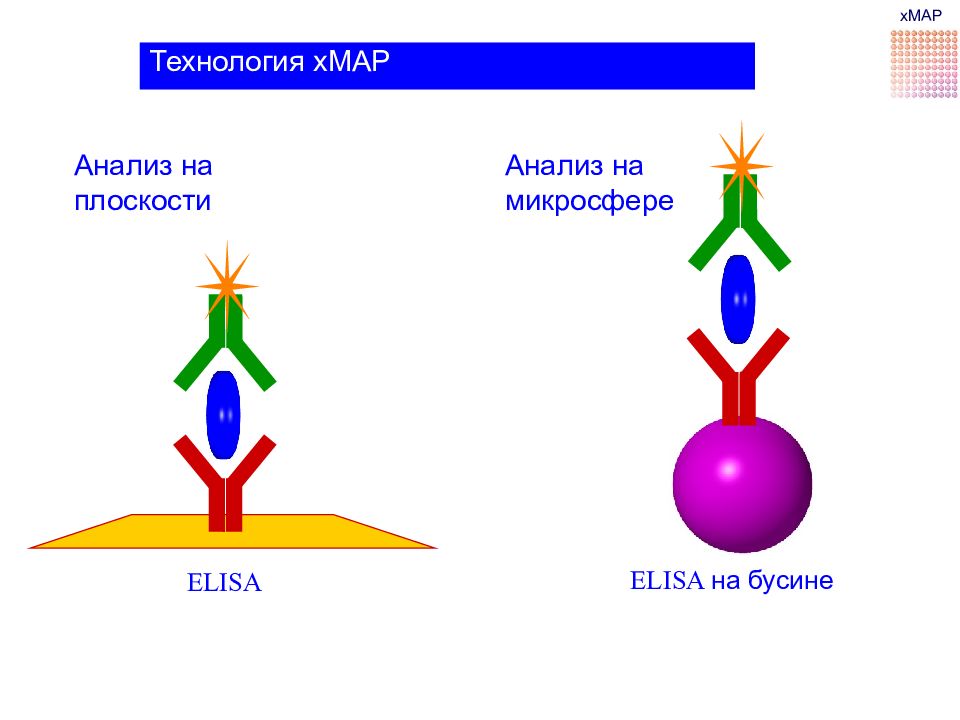
Анализ на микросфере ELISA ELISA на бусине Технология xMAP xMAP Анализ на плоскости
Слайд 113
Конъюгация антител с микросферами Первичные антитела к интересующим нас белковым аналитам пришиваются к микросферам различных типов
Слайд 114
Добавление образца к смеси микросфер Инкубация Отмывка Связывание молекул образца
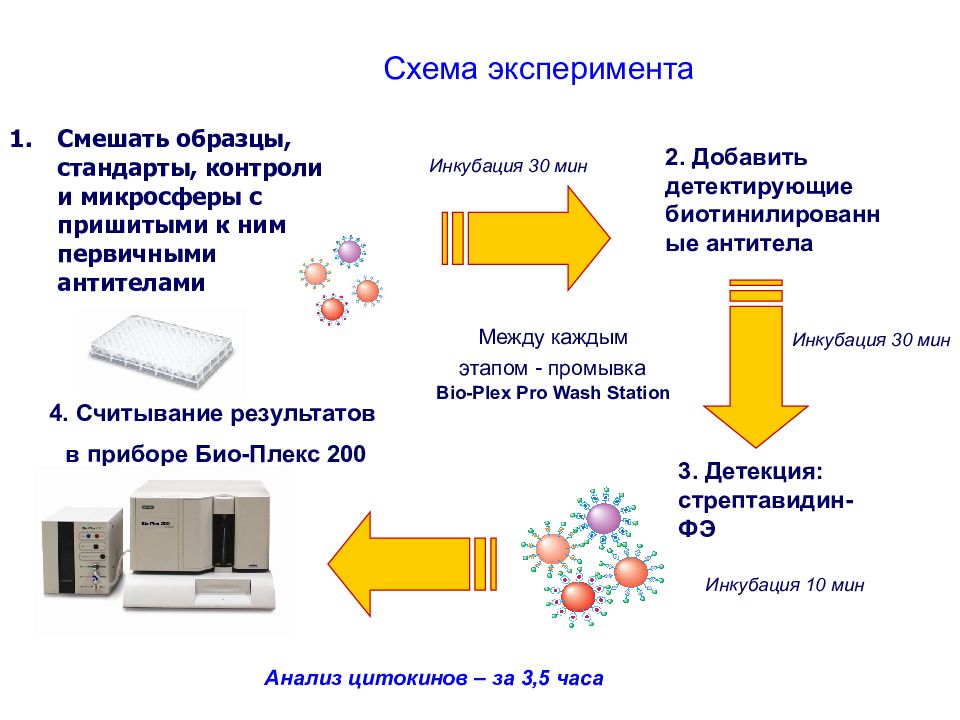
Слайд 115: Схема эксперимента
Смешать образцы, стандарты, контроли и микросферы с пришитыми к ним первичными антителами 3. Детекция: стрептавидин-ФЭ Инкубация 30 мин 2. Добавить детектирующие биотинилированные антитела Инкубация 10 мин 4. Считывание результатов в приборе Био-Плекс 200 Анализ цитокинов – за 3,5 часа Между каждым этапом - промывка Bio-Plex Pro Wash Station Инкубация 30 мин
Слайд 116: Преимущества хМАР
Стратегия : Увеличение числа лабораторий, которые могут позволить себе х MAP посредством продаж более доступной системы Фокусирование на пользователях, работающих с ELISA ( ИФА), предлагая им действительно недорогое решение их задач
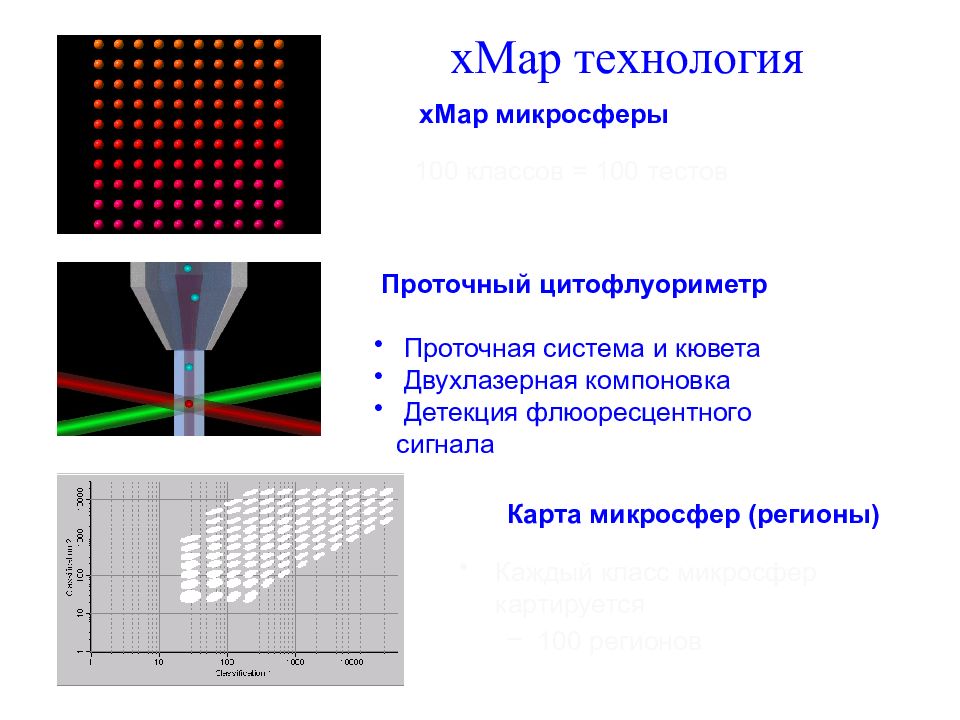
Слайд 117: xMap технология
100 классов = 100 тестов xMap технология xMap микросферы Проточный цитофлуориметр Проточная система и кювета Двухлазерная компоновка Детекция флюоресцентного сигнала Карта микросфер ( регионы ) Каждый класс микросфер картируется 100 регионов
Слайд 118: Приборы для х-МАР технологии
Luminex-100 Luminex-200 MAGPIX Luminex FLEXMAP 3D
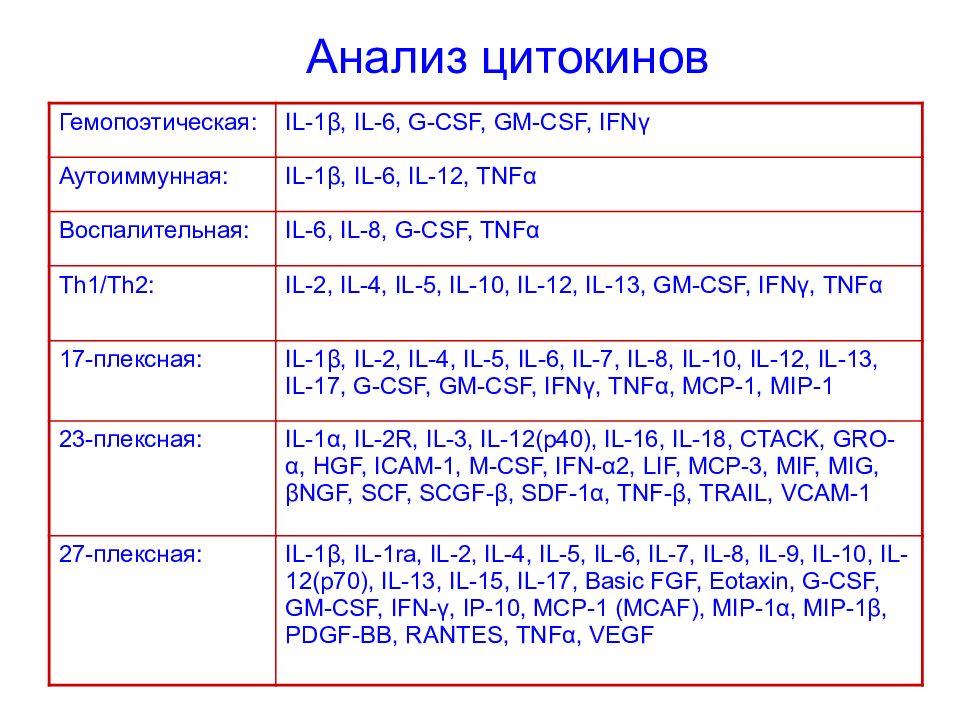
Слайд 119: Анализ цитокинов
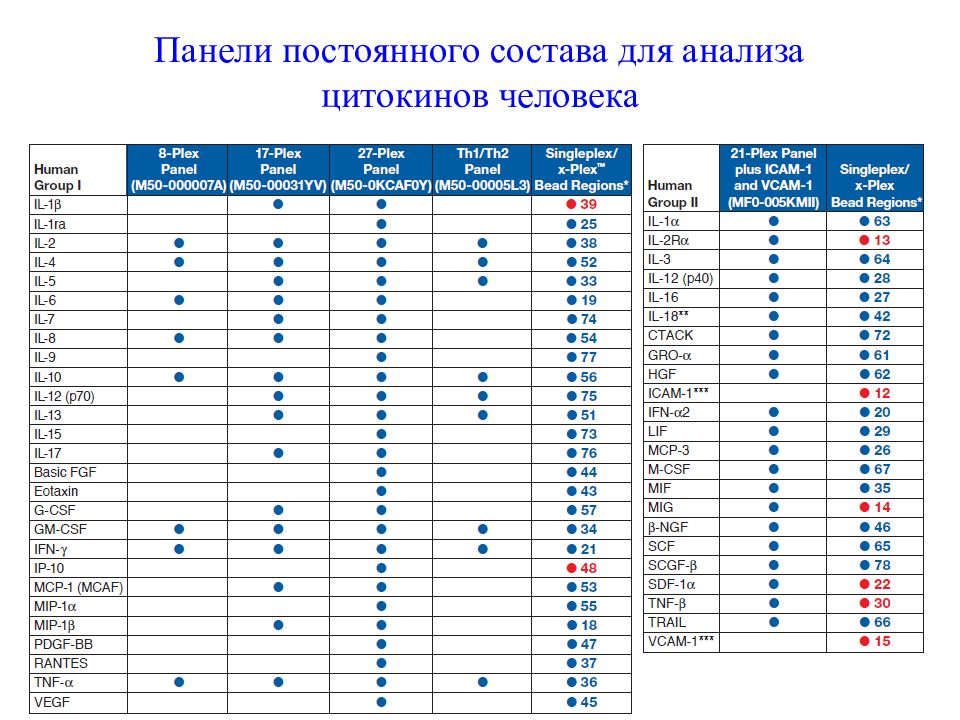
Гемопоэтическая : IL-1 β, IL-6, G-CSF, GM-CSF, IFN γ Аутоиммунная : IL-1 β, IL-6, IL-12, TNF α Воспалительная : IL-6, IL-8, G-CSF, TNF α Th1/Th2: IL-2, IL-4, IL-5, IL-10, IL-12, IL-13, GM-CSF, IFN γ, TNF α 17-плексная : IL-1 β, IL-2, IL-4, IL-5, IL-6, IL-7, IL-8, IL-10, IL-12, IL-13, IL-17, G-CSF, GM-CSF, IFN γ, TNF α, MCP-1, MIP-1 23-плексная : IL-1 α, IL-2R, IL-3, IL-12(p40), IL-16, IL-18, CTACK, GRO- α, HGF, ICAM-1, M-CSF, IFN- α 2, LIF, MCP-3, MIF, MIG, β NGF, SCF, SCGF- β, SDF-1 α, TNF- β, TRAIL, VCAM-1 27-плексная : IL-1 β, IL-1ra, IL-2, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-12(p70), IL-13, IL-15, IL-17, Basic FGF, Eotaxin, G-CSF, GM-CSF, IFN- γ, IP-10, MCP-1 (MCAF), MIP-1 α, MIP-1 β, PDGF-BB, RANTES, TNF α, VEGF
Слайд 120
Скрининг на широкий спектр биомаркеров Цитокины и факторы роста (126 показателей ) Белки сигнальной трансдукции (50 показателей ) Специализированные панели на патологические состояния Острая фаза (9 показателей ) Онкопанель (16 показателей) Ангиогенез (9 показателей ) Диабет (26 показателей ) Изотипирование АТ (7 показателей ) Прецизионная цитокиновая панель Pro (10 показателей )
Слайд 123: Аллергодиагностика (в том числе в стоматологии)
Определение общего и специфических иммуноглобулинов класса Е: Определение специфических IgE к разнообразным аллергенам (пищевым, пыльцевым, бытовым, грибковым и др.). Определение иммуноглобулинов класса Е к лекарственным препаратам. Определение иммуноглобулинов класса Е к зубопротезным материалам.
Слайд 124: Иммуноглобулины класса Е
1 МЕ/мл = 2.4 нг (1968 г., ВОЗ) Определяется у плода с 11 недель развития, через плаценту не проникает. Эффекторные функции: Индукция выделения биогенных аминов из тучных клеток, базофилов. Индукция цитотоксичности эозинофилов, моноцитов /макрофагов.
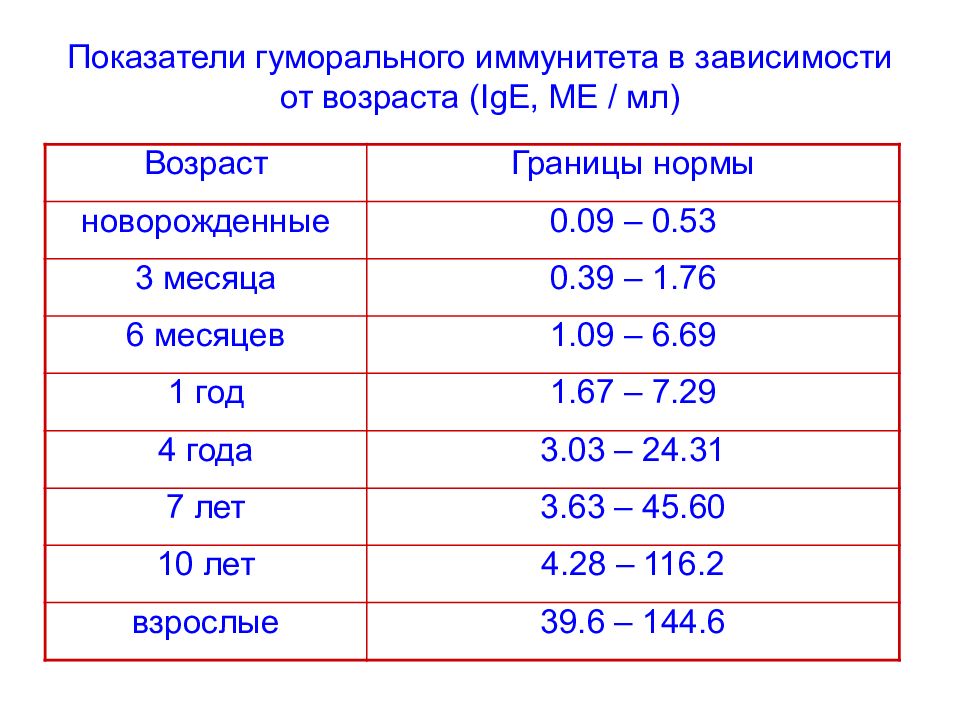
Слайд 125: Показатели гуморального иммунитета в зависимости от возраста (Ig Е, МЕ / мл)
Возраст Границы нормы новорожденные 0.09 – 0.53 3 месяца 0.39 – 1.76 6 месяцев 1.09 – 6.69 1 год 1.67 – 7.29 4 года 3.03 – 24.31 7 лет 3.63 – 45.60 10 лет 4.28 – 116.2 взрослые 39.6 – 144.6
Слайд 126: Иммуноглобулины класса Е
Повышенные уровни IgE в сыворотке крови определяются при: Атопии Гельминтозах Изолированном дефиците Ig А Гипоплазии тимуса (синдромы Ди-Джорджи и Вискотт-Олдриджа) Хроническом гранулематозе у детей
Слайд 127: Диагностика: специфические Ig E
Ведущим в интерпретации данных аллергообследования является характеристика клинических проявлений и данных анамнеза. Отсутствие повышенных уровней специфических Ig E в крови может быть неинформативным: при атопическом рините –местный синтез. Возможность синтеза IgG4 аллерген специфических антител. Доступность лабораторного аллергообследования не должна преувеличивать его диагностическую роль.
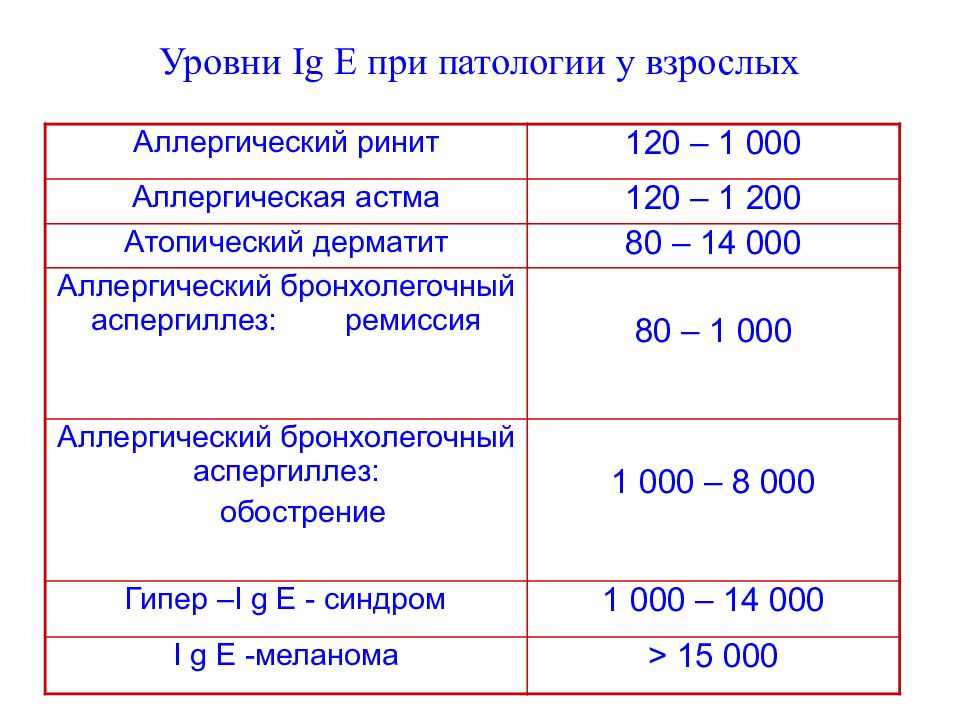
Слайд 128: Уровни Ig E при патологии у взрослых
Аллергический ринит 120 – 1 000 Аллергическая астма 120 – 1 200 Атопический дерматит 80 – 14 000 Аллергический бронхолегочный аспергиллез: ремиссия 80 – 1 000 Аллергический бронхолегочный аспергиллез: обострение 1 000 – 8 000 Гипер – I g E - синдром 1 000 – 14 000 I g E -меланома > 15 000
Слайд 129: Аллергия или псевдоаллергия?
Если повышен уровень триптазы тучных клеток – может быть как истинная аллергия, так и псевдоаллергия (вопрос-почему?) Если повышен уровень ECP –эозинофильного катионного белка -аллергия истинная (вопрос-почему?)
Слайд 130: Псевдоаллергия-определение
Псевдоаллергия (греч. pseudēs ложный) - патологический процесс, по клиническим проявлениям похожий на аллергию, но не имеющий иммунологической стадии развития. Конечные стадии истинной аллергии совпадают с псевдоаллергией : патохимическая стадия - освобождение (и образование de novo ) медиаторов; патофизиологическая стадия - реализация клинических симптомов.
Слайд 131: Неиммунный механизм дегрануляции тучных клеток – факторы (не IgE ), приводящие к дестабилизации мембраны тучной клетки и к ее дегрануляции
Слайд 132: Метод CAST – с ellular antigen stimulation test
Технология CAST (тест антигенной стимуляции клеток) основана на определении маркеров активации базофилов под действием аллергенов in vitro либо методом проточной цитометрии (базофилы, экспрессирующие CD63), либо на определении сульфидолейкотриенов (LTC4, LTD4, LTE4), секретируемых базофилами. Его также называют провокационным тестом in vitro.
Слайд 133: Применение метода CAST
Для диагностики и подтверждения IgE-зависимой аллергии и псевдоаллергических реакций, особенно лекарственной непереносимости, в случаях противоречивых или отрицательных результатов кожных тестов и анализа IgE; Для диагностики аллергии к ядам насекомых, Для принятия решения о проведении специфической иммунотерапии (СИТ) аллергенами насекомых; Для контроля СИТ (уровень лейкотриенов снижается после успешного лечения).
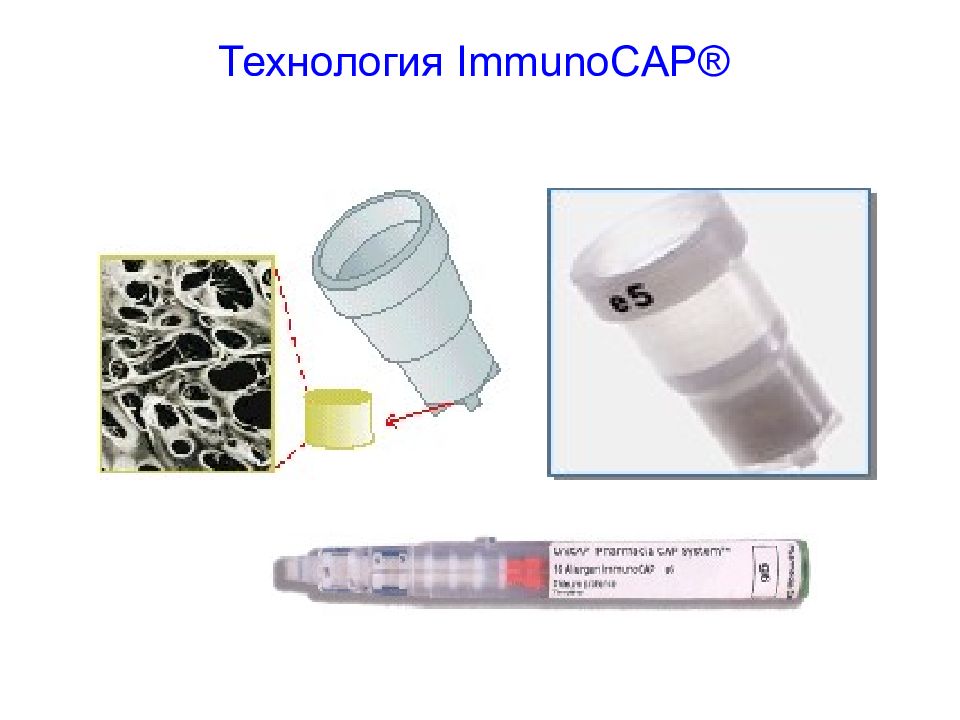
Слайд 134: ImmunoCAP® - «золотой стандарт» аллергодиагностики in vitro
В аллергодиагностике оборудование и реагенты к нему играют основную роль для получения качественных результатов. Для этих целей используется технология ImmunoCAP® (оборудование и аллергены) фирмы "Phadia«(Швеция), являющейся мировым лидером в данной области.
Слайд 136: ImmunoCAP® : иммунофлюоресцентный метод
Связывающая способность : в технологии ImmunoCAP® твёрдой фазой является трёхмерная активированная целлюлозная губка, которая связывается с антителами по всему объёму. Другие технологии, такие как активированные лунки планшета, активированные шарики и активированные бумажные диски для связывания используют поверхность, чем обусловлена их значительно меньшая связывающая способность.
Слайд 138: ImmunoCAP® : параметры метода
Специфичность - не отмечено взаимодействия с другими иммуноглобулинами человека в физиологических концентрациях. Чувствительность - в настоящее время пациент считается сенсибилизированным к аллергену, если концентрация антител к этому аллергену превышает 0,35 кЕ/л. Нижний предел детекции прибора составляет гораздо более малые значения, например: перхоть кошки (e1) - 0,06 КЕ/л., молоко коровы (f2) - 0,05 кЕ/л., яичный белок (f1) - 0,08 кЕ/л., берёза бородавчатая (t3) - менее 0,01 КЕ/л.
Слайд 139: Триптаза тучных клеток
Тест ImmunoCAP ® Tриптаза измеряет общий уровень альфа- и бета- триптазы в сыворотке или плазме. Бета-триптаза, хранящаяся внутри гранул, высвобождается только при активации тучных клеток. Временное повышение уровня триптазы служит клиническим маркером, подтверждающим тяжелые реакции, такие как анафилаксия.
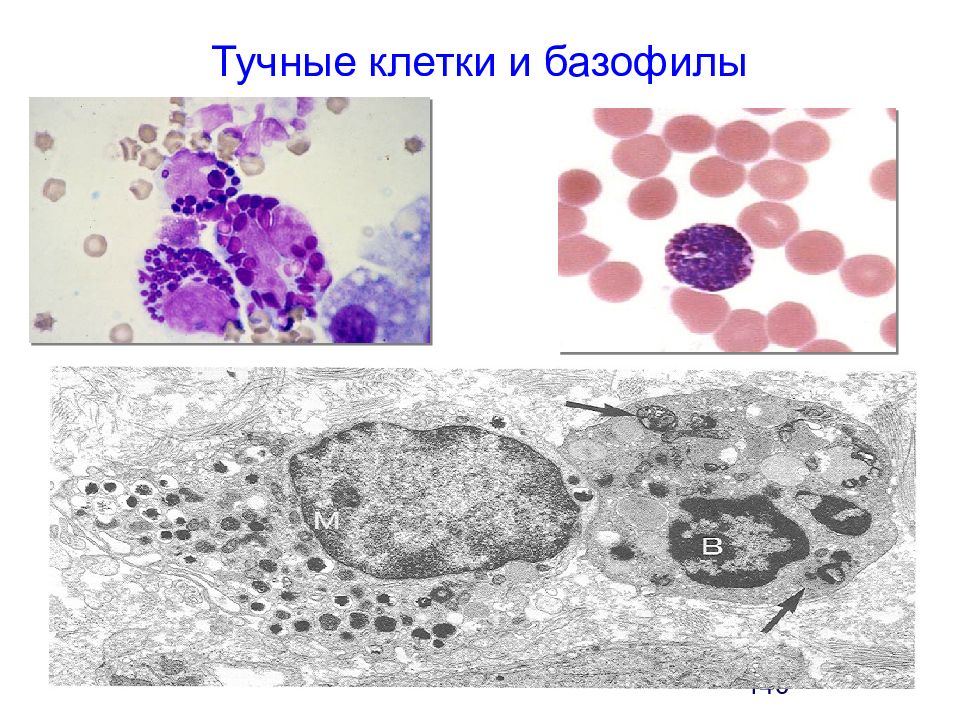
Слайд 141: Триптаза
Тучные клетки содержат почти в 300 раз больше триптазы (12 пикограмм на 1 тучную клетку), чем базофил (0.046 пикограмм на 1 базофил). Существует 5 видов изоферментов триптазы - альфа; бета; гамма; дельта; эпсилон. В тучной клетке человека содержится преимущественно альфа субтип. Референтные значения для триптазы в сыворотке крови ≤ 11.4 µ g / L.
Слайд 142: Триптаза тучных клеток
Триптаза – маркер рецидива острой миелоидной лейкемии : больше 10 мкг/л группа риска больше 20 мкг/л системный мастоцитоз больше 200 мкг/л гематологические неоплазмы (уровень нормы - 2.96±1.75 мкг/л)
Слайд 143: Эозинофильный катионный белок (ЕСР)
ЕСР - маркер выраженности аллергического воспаления в шоковом органе (при полинозах, при аллергической бронхиальной астме). У больных полинозом с хорошим клиническим эффектом СИТ(специфической иммунотерапии) отмечается торможение сезонного прироста содержания ЕСР в назальных секретах.
Слайд 144: Методы диагностики аллергии in vivo
Кожные пробы Аппликационные пробы Сублингвальные пробы и т.д. Провокационные пробы (используются редко).
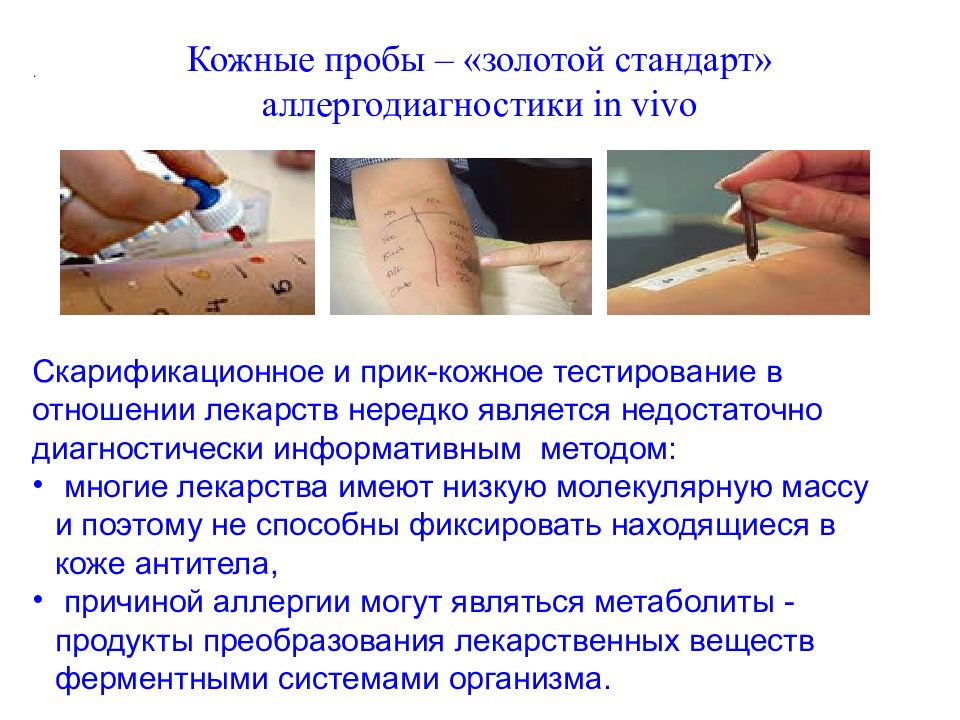
Слайд 145: Кожные пробы – «золотой стандарт» аллергодиагностики in vivo
. Скарификационное и прик-кожное тестирование в отношении лекарств нередко является недостаточно диагностически информативным методом: многие лекарства имеют низкую молекулярную массу и поэтому не способны фиксировать находящиеся в коже антитела, причиной аллергии могут являться метаболиты - продукты преобразования лекарственных веществ ферментными системами организма.
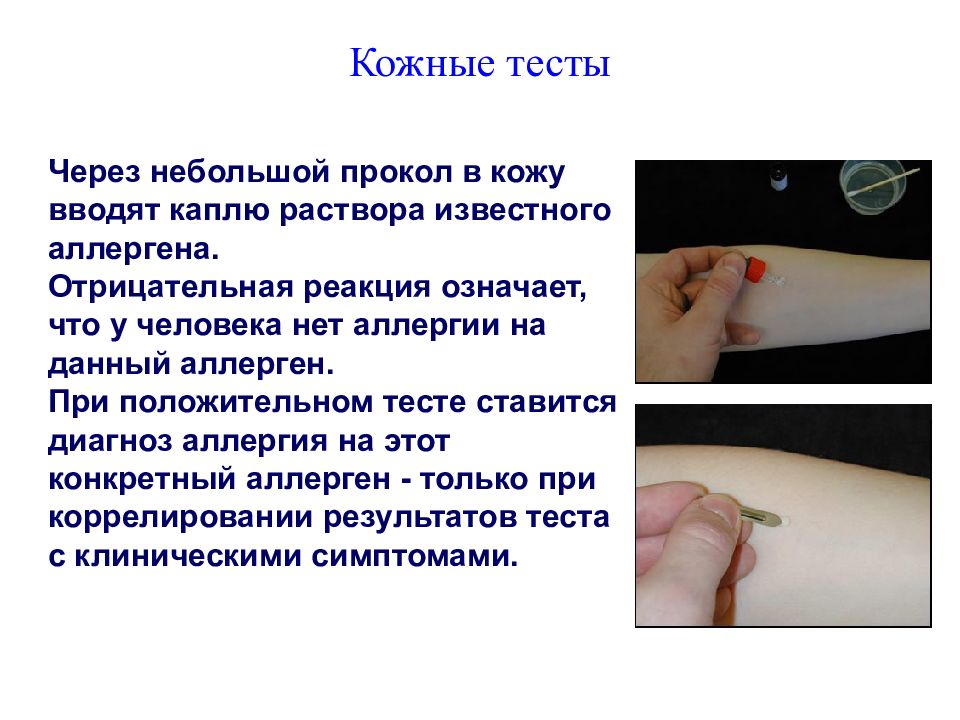
Слайд 146: Кожные тесты
Через небольшой прокол в кожу вводят каплю раствора известного аллергена. Отрицательная реакция означает, что у человека нет аллергии на данный аллерген. При положительном тесте ставится диагноз аллергия на этот конкретный аллерген - только при коррелировании результатов теста с клиническими симптомами.
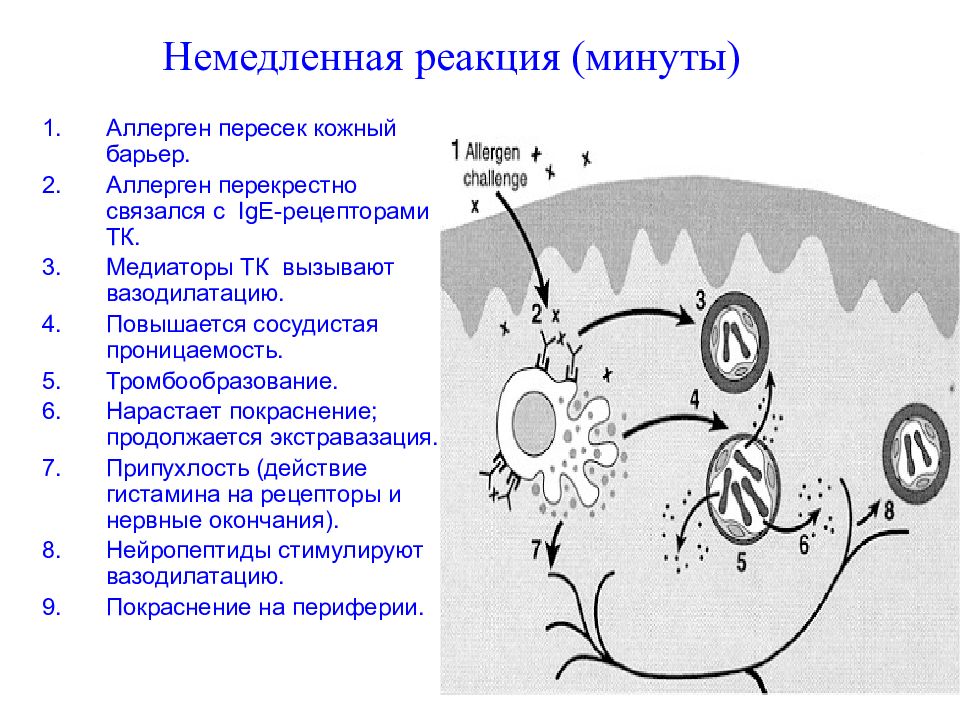
Слайд 147: Немедленная реакция (минуты)
147 Немедленная реакция (минуты) A ллерген пересек кожный барьер. Аллерген перекрестно связался с IgE -рецепторами ТК. Медиаторы ТК вызывают вазодилатацию. Повышается сосудистая проницаемость. Тромбообразование. Нарастает покраснение; продолжается экстравазация. Припухлость (действие гистамина на рецепторы и нервные окончания). Нейропептиды стимулируют вазодилатацию. Покраснение на периферии.
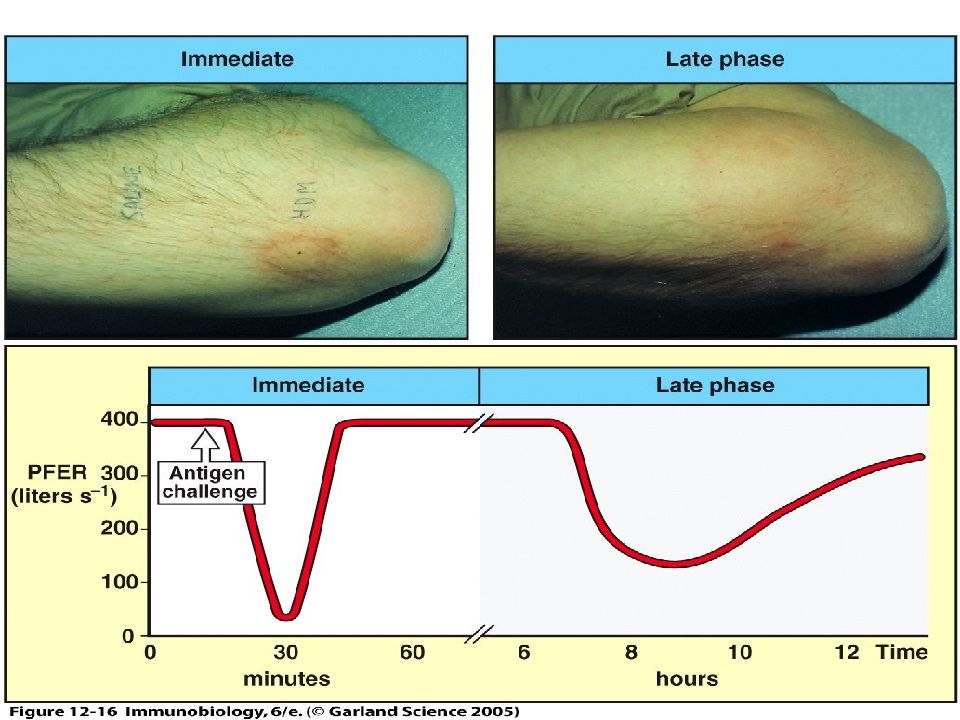
Слайд 148: Поздний ответ
148 Поздний ответ 1.Тучные клетки и 2. Th2 продуцируют цитокины 3. Воспаление и привлечение новых клеток воспаления из периферических кровеносных сосудов продолжается…
Слайд 149: Кожные тесты
Несмотря на большой прогресс в диагностике аллергических состояний, аллергологи часто сталкиваются с проблемой необходимости подтверждения неясных результатов кожных тестов. Некоторые виды аллергии (на лекарственные средства, пищевые добавки) очень плохо выявляются кожными тестами или серологически –определением в крови аллерген - специфичных иммуноглобулинов (IgE), для них в настоящее время достоверны только дорогостоящие и опасные провокационные тесты.
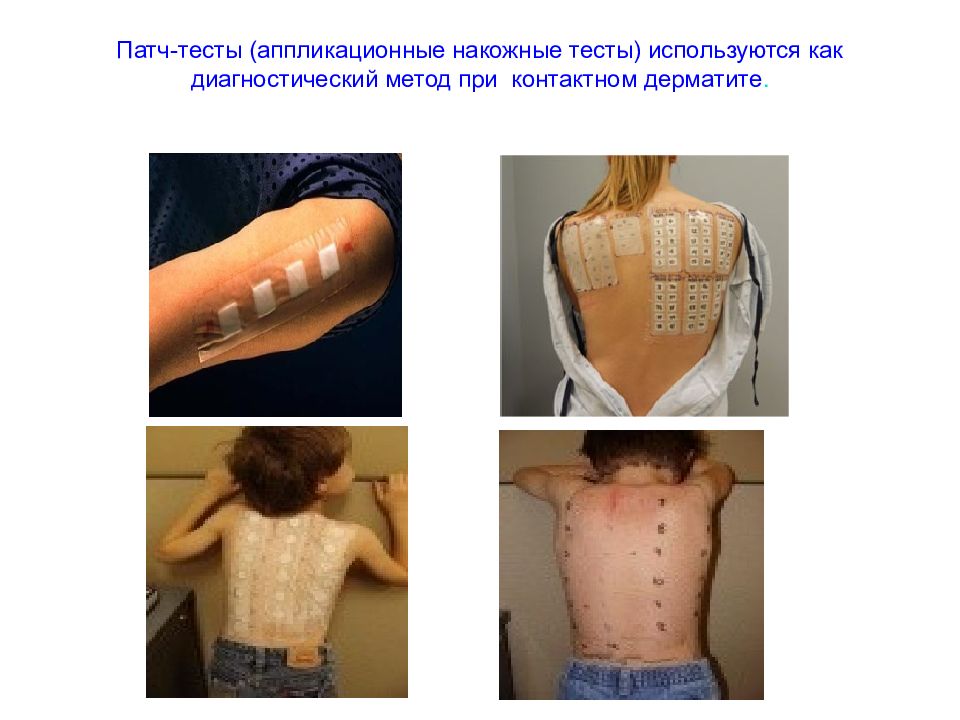
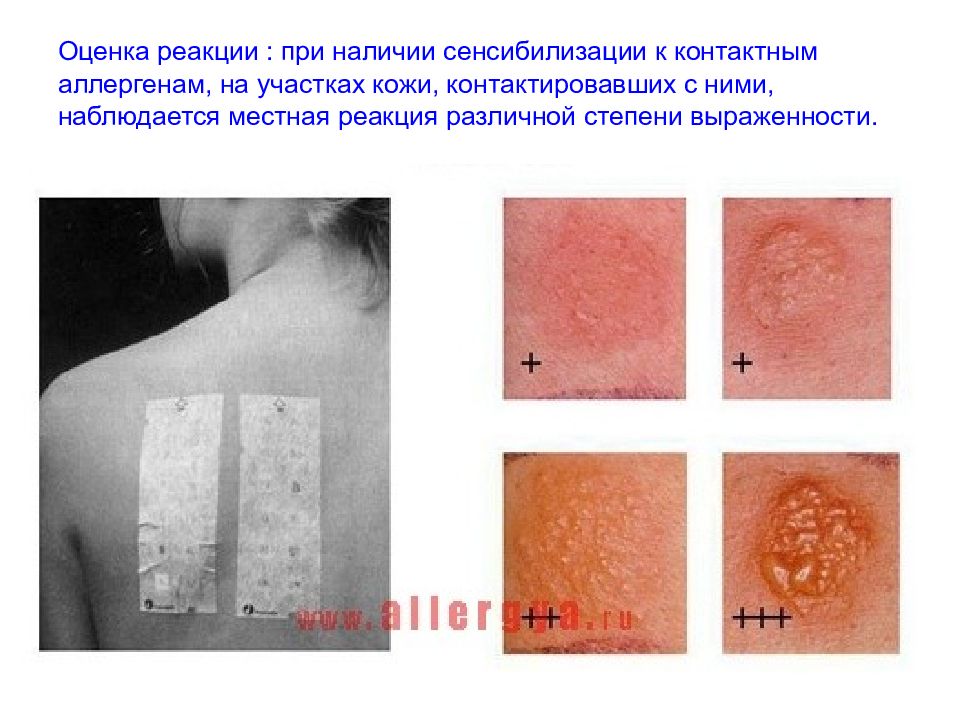
Слайд 151: Патч-тесты (аппликационные накожные тесты) используются как диагностический метод при контактном дерматите
Слайд 152: Оценка реакции : при наличии сенсибилизации к контактным аллергенам, на участках кожи, контактировавших с ними, наблюдается местная реакция различной степени выраженности
Слайд 153: Направление на иммунологическое исследование
В направлении должны быть указаны возраст, пол пациента, так как эти параметры могут определять особенности иммунограммы в норме. В спецанамнез должны быть включены: Используемая медикаментозная терапия в последние 6 месяцев. Наличие химио- и радио –терапии. Профессиональные вредности. Пребывание в зоне, загрязненной радионуклеидами. Результаты предыдущих иммунологических обследований (для оценки динамики).
Слайд 154: Основные принципы оценки иммунограммы
Комплексность оценки: иммунограмма – набор тестов, позволяющих оценить различные звенья иммунной системы. Сравнительная характеристика изменений показателей всех звеньев иммунной системы.
Слайд 155: Основные принципы оценки иммунограммы
3. Оценка наиболее выраженный сдвигов иммунологических параметров: сопоставление полученных показателей у больного с величиной нормальных значений, полученных при обследовании здоровых лиц (обязательно использовать «возрастные» нормы).
Слайд 156: Основные принципы оценки иммунограммы
4. Изучение иммунологических показателей в динамике заболевания и в сопоставлении с данными других исследований (микробиологических, вирусологических). 5. Ведущим в анализе иммунограммы является характеристика клинических симптомов (анализировать иммунограмму должны совместно - лечащий врач и врач клинической лабораторной диагностики).
Слайд 157: Основные принципы оценки иммунограммы
6. Постановку диагноза «иммунодефицитное состояние» и назначение адекватной иммунотерапии после проведения иммунологического обследования проводит только лечащий врач, а не врач –лаборант, который может лишь фиксировать изменения в отдельных звеньях иммунной системы.
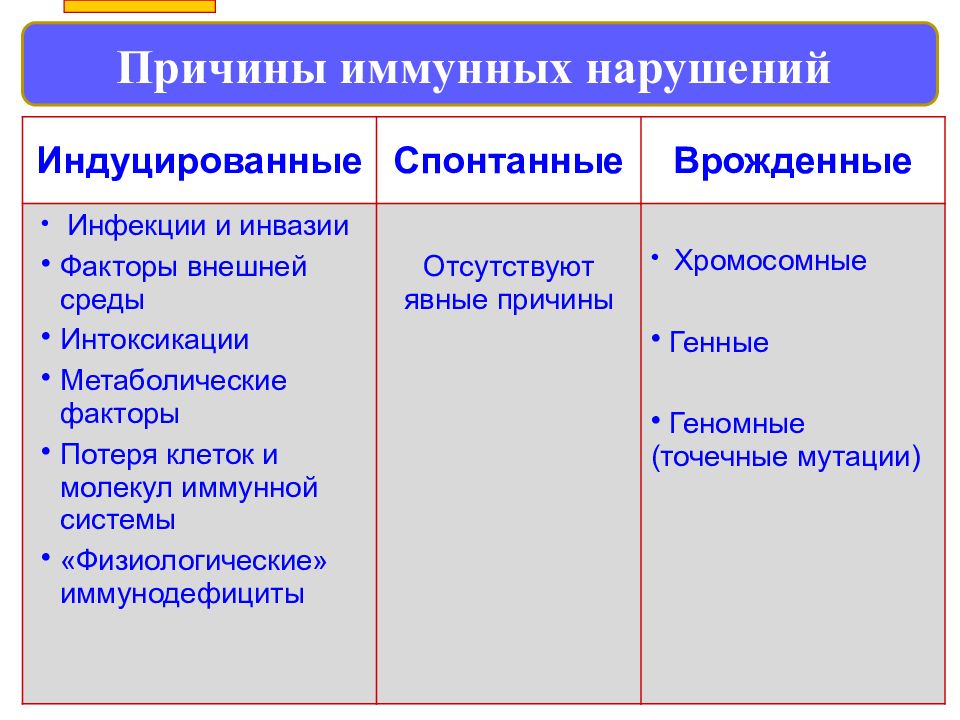
Слайд 158
Причины иммунных нарушений 158 Индуцированные Спонтанные Врожденные Инфекции и инвазии Факторы внешней среды Интоксикации Метаболические факторы Потеря клеток и молекул иммунной системы «Физиологические» иммунодефициты Отсутствуют явные причины Хромосомные Генные Геномные (точечные мутации)
Слайд 159: Основные виды патологии иммунной системы
Количественная или функциональная недостаточность того или иного звена иммунитета (иммунодефицитные состояния). Нарушения в распознавании антигена иммунной системой (аутоиммунные заболевания). Гиперреактивный или измененный тип иммунного ответа (аллергические заболевания).
Слайд 160: Вопросы
Какие звенья иммунной системы изучаются в клинической практике? Какие методы иммунного анализа вам известны? Как происходила эволюция методов иммунного анализа? Каковы основные принципы оценки иммунограммы ? Каковы возрастные особенности иммунологических показателей? Дайте определение понятию « иммунодефицитные состояния». Какие механизмы лежат в основе развития аутоиммунной патологии? Какие виды гиперчувствительности Вам известны? Какие виды аллергических заболеваний вам известны? Перечислите основные клетки-эффекторы аллергических реакций.
Слайд 161: Тестовые вопросы
В лабораторной диагностике в зависимости от детализации анализа отклонений тесты иммунного анализа подразделяются на: тесты I уровня тесты I I уровня тесты I I I уровня тесты IV уровня тесты уровня Объектом иммунологических исследований могут служить: кровь слюна мокрота спинномозговая жидкость жидкость бронхоальвеолярного лаважа
Слайд 162: Тестовые вопросы
К современным методам иммунного анализа не относятся: Иммуноферментный анализ Иммунофлюоресцентный анализ Иммунофенотипирование Хемилюминесцентный анализ Методы розеткообразования Моноклональные антитела получают: При иммунизации лабораторных животных разными антигенами Путем слияния нормальных продуцирующих антитела В-лимфоцитов с опухолевой линией клеток и образованием гибридом Путем замораживания плазматических клеток С помощью фракционирования клеток С помощью центрифугирования клеток на градиенте плотности (р=1.0770)
Слайд 163: Тестовые вопросы
В каком возрасте начинают проявляться врожденные иммунодефицитные состояния гуморального звена? В возрасте 2 недель В возрасте 1 месяц В возрасте 2 месяца В 3-месячном возрасте В возрасте от 4 месяцев Какие из перечисленных причин иммунодефицитных состояний не относятся к первичным: Нарушение активности или отсутствие фермента Отсутствие какой-либо популяции клеток иммунной системы При дефектах генов, кодирующих молекулы адгезии Иммунодефицитные состояния, вызванные вирусами Иммунодефицитные состояния, вызванные иммунодепрессантами
Слайд 164: Тестовые вопросы
К основным причинам вторичной иммунологической недостаточности не относится: Белковое голодание Нефротический синдром ( гипопротеинемия ) Применение иммунодепрессантов Дефекты генов, кодирующих адгезионные молекулы Хрониостресс Какой тип гиперчувствительности лежит в основе развития заболеваний: Атопический дерматит Аллергический ринит Атопическая бронхиальная астма Аллергический конъюктивит Атопическая крапивница
Последний слайд презентации: Государственное бюджетное образовательное учреждение высшего профессионального: Тестовые вопросы
Какие заболевания не относятся к «аллергическим»? Атопический дерматит Аллергический ринит Атопическая бронхиальная астма Аллергический конъюктивит Неиммунологическая крапивница В развитии каких аутоиммунных заболеваний преимущественное участие не принимают механизмы гиперчувствительности I I типа? Аутоиммунная гемолитическая анемия Болезнь Грейвса Миастения гравис Идиопатическая тромбоцитопеническая пурпура Системная красная волчанка