Первый слайд презентации: Контроль качества лабораторных исследований
Слайд 2
Контроль качества лабораторных исследований – это система мер по оценке и контролю качества выполнения лабораторного анализа на всех этапах его осуществления.
Слайд 3
Задачами контроля качества клинических лабораторных исследований являются: обеспечение качества лабораторных исследований; обеспечение преемственности результата; оценка надежности используемых лабораторных методов; оценка надежности результатов исследования.
Слайд 4
Приказ МЗ СССР №380 от 23.04.75 г. «О состоянии и перспективах развития клинико-диагностической службы в стране». Приказ МЗ РФ №45 от 07.02.2000 г. «О системе мер по повышению качества клинических лабораторных исследований в учреждениях здравоохранения Российской Федерации».
Слайд 5: ВИДЫ КОНТРОЛЯ КАЧЕСТВА:
внешний осуществляется Федеральной системой внешней оценки качества (ФСВОК) внутрилабораторный осуществляется на уровне КДЛ
Слайд 6
Основная терминология Аналитическая серия – совокупность измерений лабораторного показателя, выполненных единовременно в одних и тех же условиях без перенастройки и калибровки аналитической системы.
Слайд 7
Контрольный материал - материал, предназначенный для осуществления контроля качества лабораторных исследований и приближающийся по наиболее существенным свойствам к исследуемому материалу.
Слайд 8
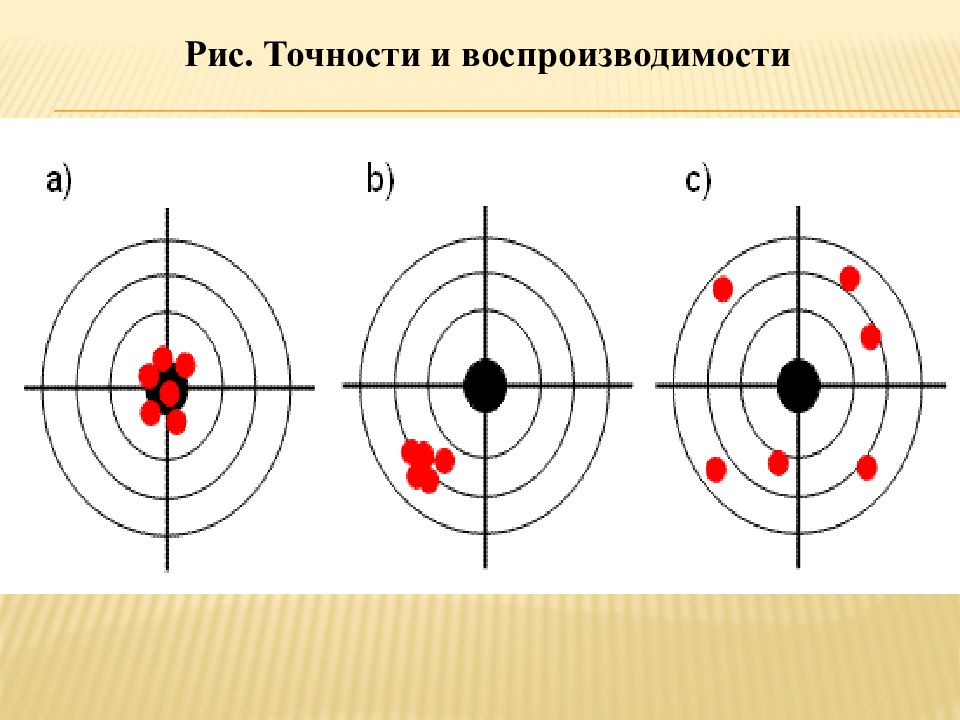
Правильность измерений – качество измерений, отражающее близость к нулю систематических погрешностей. Точность измерений – качество измерений, отражающее близость результатов к истинному значению измеряемой величины. Воспроизводимость измерений – качество измерений, отражающее близость друг к другу результатов измерений, выполняемых в различных условиях.
Слайд 10
Различают внутрисерийную и межсерийную воспроизводимость. Сходимость измерений ( внутрисерийная воспроизводимость ) – качество измерений, отражающее близость друг к другу результатов измерений, выполняемых в одинаковых условиях. Межсерийная воспроизводимость – качество измерений, отражающее близость друг к другу результатов измерений, выполняемых в разных условиях.
Слайд 11
Погрешность измерения - отклонение результата измерения от истинного значения измеряемой величины. Систематическая погрешность измерения - составляющая погрешности измерения, остающаяся постоянной или закономерно изменяющаяся при повторных измерениях одной и той же величины. Случайная погрешность измерения - составляющая погрешности измерения, изменяющаяся случайным образом при повторных измерениях одной и той же величины.
Качество выполнения в КДЛ исследований во многом определяется: особенностями используемого метода; тщательностью его исполнения; квалификацией сотрудников; техническим совершенством используемой аппаратуры; качеством и чистотой реактивов; точностью мерной посуды.
Преаналитический Аналитический Постаналитический
Слайд 14: Внелабораторные ошибки
Канцелярские Ошибки Ошибочный больной Ошибочный образец Ошибочная заявка Прочие Ошибки при взятии пробы Ошибочный антикоагулянт Ошибка положения тела Гемолиз Задержка отделения сыворотки Прочие
Слайд 15: ФАКТОРЫ ПРЕАНАЛИТИЧЕСКОГО ЭТАПА, ВЛИЯЮЩИЕ НА РЕЗУЛЬТАТ ИССЛЕДОВАНИЯ
Идентификация пациента и образца биоматериала. Биологические факторы: учитываемые: пол, возраст, физиологическое состояние; биологические ритмы, влияние среды обитания. регулируемые: диета, положение тела, курение, употребление алкоголя или наркотиков. Ятрогенные факторы: диагностические процедуры; оперативное вмешательство; лечебные процедуры; прием лекарственных препаратов.
Слайд 16
Свойства анализируемого компонента: стабильность в крови при различных температурах; метаболизм in vitro, включающий чувствительность к свету. Условия взятия, хранения и транспортировки биоматериала: время взятия, срок сбора; подготовка участка тела для взятия материала; процедура взятия материала; посуда; воздействие факторов среды; процедура пробоподготовки.
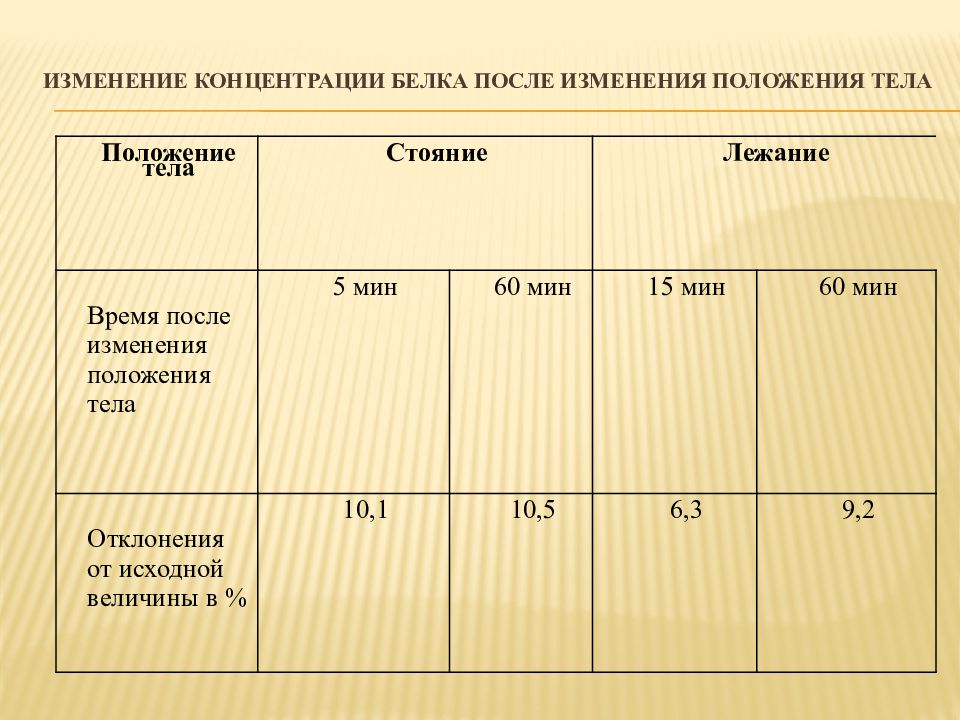
Слайд 17: Изменение концентрации белка после изменения положения тела
Положение тела Стояние Лежание Время после изменения положения тела 5 мин 60 мин 15 мин 60 мин Отклонения от исходной величины в % 10,1 10,5 6,3 9,2
Слайд 18: Требования ко времени выполнения некоторых преаналитических этапов биохимических исследований
Наименование биологической жидкости и этапа анализа Время от момента получения биологической жидкости, или предыдущего этапа Взятие капиллярной или венозной крови С 7 до 9 ч утра, зарегистриро вать в направлении на анализ точное время взятия крови Анализ компонентов из свежей капиллярной и венозной крови Проведение исследования в течение 2-3 мин Перемешивание крови с антикоагулянтами для получения плазмы Не позднее, чем через 2 мин после наложения жгута
Слайд 19
Получение сыворотки и плазмы: Центрифугирование в стеклянных пробирках Не позднее, чем через 1 ч после взятия Центрифугирование для получения плазмы Немедленно после взятия Центрифугирование для получения сыворотки в одноразовых коммерческих пробирках Через 30-60 мин после взятия Отделение сыворотки от сгустка или клеток крови Сразу же после центрифугиро вания Сыворотка, плазма, если нельзя выполнить анализ в течение 3 ч Биологическую жидкость помещают в холодильник на 24 ч (если нет особых указаний) Моча Порция доставляется немедленно после окончания сбора мочи с указанием объема и времени, за которое она собрана, а также кон серванта. Спинно-мозговая жидкость Доставка в лабораторию в течение 1 ч после взятия без охлаждения. Доставка в течение 3 ч после взятия в чашке со льдом.
Слайд 20: СТАНДАРТИЗАЦИЯ ПРЕАНАЛИТИЧЕСКОГО ЭТАПА:
время взятия с 7 до 9 ч утра; взятие крови натощак, т.е. последний прием пищи 12-14 ч назад; исключить физическую активность и психоэмоциональные нагрузки за 3 дня до исследования; исключить прием алкоголя; исключить прием лекарств за 3 дня до исследования; за 15 мин до взятия обследуемый находится в состоянии покоя; время наложения жгута не превышает 1 мин; пальцы руки не сжимать не разжимать; не похлопывать ладонью по месту взятия; соблюдать определенные места для взятия крови, соблюдать методику взятия; первые 5-6 капель крови собрать на стерильный марлевый тампон.
Слайд 21: МЕРЫ ПРЕДОТВРАЩАЮЩИЕ ГЕМОЛИЗ:
соразмерное сдавление вен при наложении жгута; взятие крови из вен острыми иглами с коротким срезом, с большим диаметром; кровь вытекает в пробирку самотеком; исключить: сильное нагревание или переохлаждение, механическую тряску, затягивание сроков обработки пробы; исключить недостаточно полное центрифугирование; транспортировать только в закрытом виде.
Слайд 22: аналитические ошибки
грубые случайные систематические Грубая ошибка – это одиночное значение исследуемого компонента, выходящее за пределы установленной для данного компонента области (за допустимые пределы погрешности).
Слайд 23
Случайная ошибка – одиночное значение, не выходящее за пределы установленной для данного исследуемого компонента области, но стремящееся к выходу за эти пределы. Систематическими ошибками - называют погрешности, одинаковые по знаку, происходящие от определенных причин, влияющих на результаты либо в сторону увеличения, либо в сторону уменьшения его.
Слайд 24: Виды систематических ошибок:
Ошибки методические. Ошибки оперативные. Ошибки индивидуальные. Ошибки, зависящие от применяемых приборов и реактивов.
Слайд 25
Контрольными материалами называют однородные материалы, результаты исследования которых, используются для оценки погрешности выполняемого аналитического измерения. Контрольный материал не может быть использован в качестве калибровочного!
Слайд 26
Контрольные материалы: промышленного производства: аттестованные не аттестованные приготовленные в лаборатории (слитые сыворотки, плазма, моча).
Слайд 27
Контрольные материалы: универсальные (содержащие большое число анализируемых компонентов) специальные (для контроля качества отдельных определений или групп показателей).
Слайд 28: Требованиям к Контрольным материалам :
стабильность при хранении; минимальные межфлаконные вариации; гомогенность ; простота в использовании; та же матрица, что и материал для исследования; концентрация вещества в контрольном материале должна охватывать область нормальных и патологических значений.
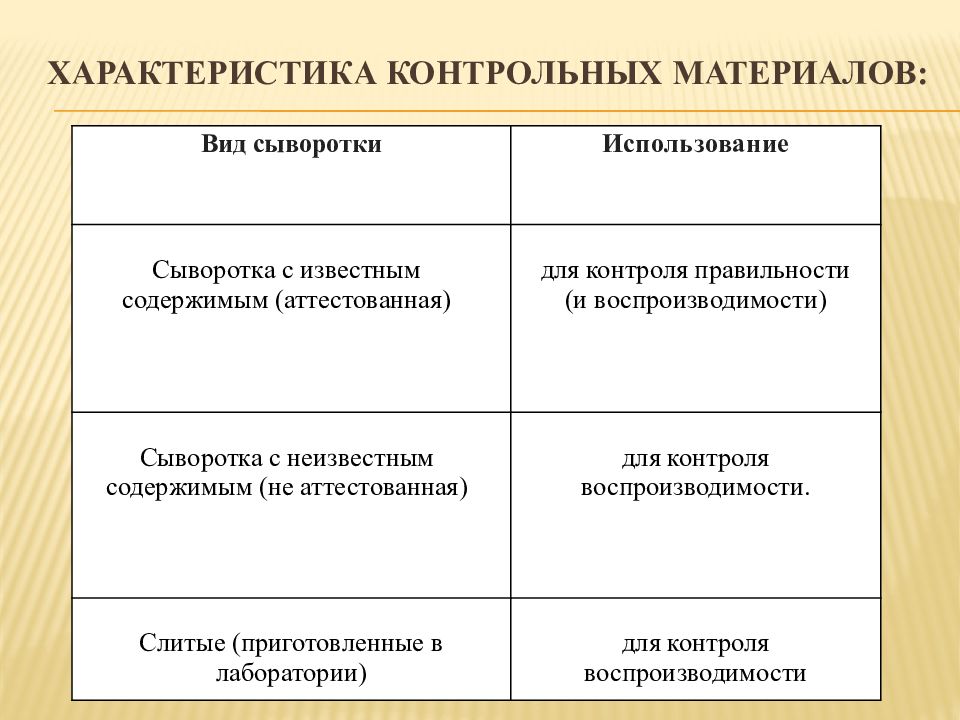
Слайд 29: Характеристика контрольных материалов:
Вид сыворотки Использование Сыворотка с известным содержимым (аттестованная) для контроля правильности (и воспроизводимости ) Сыворотка с неизвестным содержимым (не аттестованная) для контроля воспроизводимости. Слитые (приготовленные в лаборатории) для контроля воспроизводимости
Слайд 30: Внутрилабораторный контроль качества состоит из трех последовательных стадий:
оценка сходимости результатов измерения; оценка воспроизводимости и правильности результатов измерений, построение контрольных карт; проведение оперативного (текущего) контроля качества результатов лабораторных исследований в каждой аналитической серии.
Слайд 31: Порядок проведения внутрилабораторного контроля качества
Стадия I : оценка сходимости результатов измерения. рассчитывается С V BC по 10-ти измерениям и сравнивается с С V 10 (из приказа №45) : С V BC ≤ 0,5 · С V 10
Слайд 32: Стадия II : оценка воспроизводимости и правильности результатов измерений, построение контрольной карты
Предварительная оценка воспроизводимости (С V 10 ) и правильности (В 10 ). С V 10(М C ) ≤ С V 10 (ПДЗ) В 10 ≤ В 10 (ПДЗ) Окончательная оценка воспроизводимости (С V 20 ) и правильности (В 20 ). С V 20(М C ) ≤ С V 20 (ПДЗ) В 20 ≤ В 20 (ПДЗ)
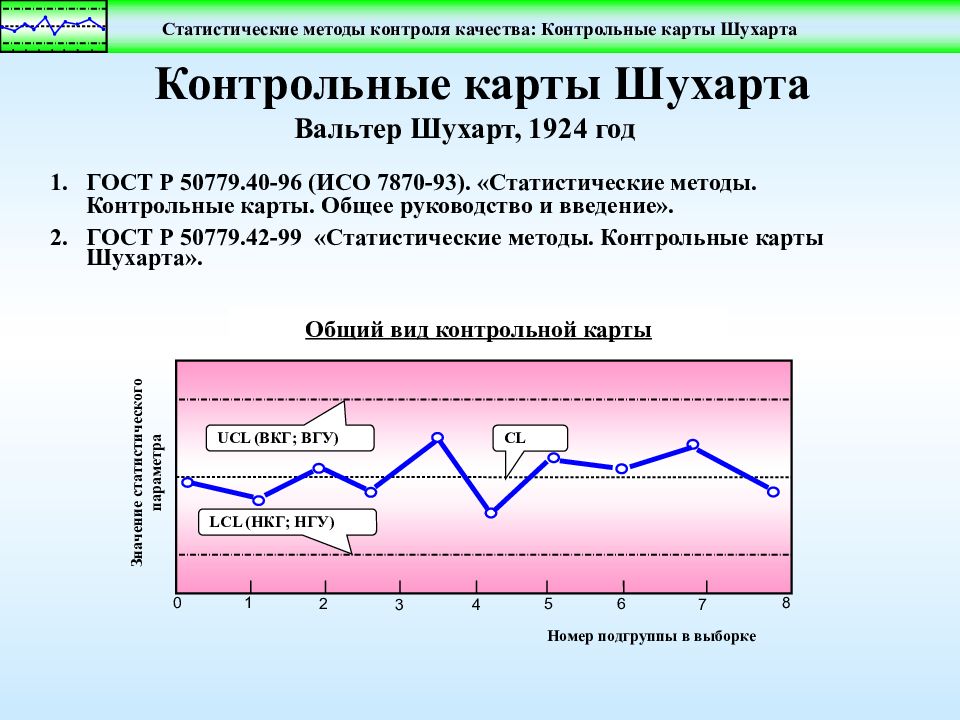
Слайд 33: Построение контрольной карты Шухарта или Леви-Дженнингс
Рассчитывают: среднюю арифметическую величину Х ср среднее квадратическое отклонение S контрольные пределы: Х ср ± 1 S, Х ср ± 2 S, Х ср ± 3 S.
Слайд 34: Контрольная карта – это график сопоставления измеряемых величин с временем исследования
Дата проведения (номер серии) 1 2 3 4 5 6 7 8 Результат анализа Хср Хср + S Хср + 2S Хср + 3S Хср - S Хср - 2S Хср - 3S
Слайд 36
1 Дата X X – Xср. ( X – Xср.)² 01.06. 98 2 4 02.06. 102 2 4 03.06. 100 0 0 04.06. 100 0 0 05.06. 95 5 25 06.06. 105 5 25 07.06. 101 1 1 08.06. 99 1 1 09.06. 97 3 9 10.06. 100 0 0 11.06. 103 3 9 12.06. 99 1 1 13.06. 102 2 4 14.06. 100 0 0 15.06. 98 2 4 16.06. 104 4 16 17.06. 101 1 1 18.06. 97 3 9 19.06. 99 1 20.06. Итого 100 2000 0 0 114 X 1 +X 2 +Xn 20 00 X ср. = = n 2 0 X ср. = 100 ммоль /л ∑( X – Xср.)² = 114
Слайд 37: Расчет среднеквадратического отклонения
∑( X – Xср.)² 114 S = √ n – 1 = √ 1 9 = 2,5
Слайд 39: CV в % для некоторых тестов
Перечень биохимических исследований КВ % (CV 20 ) Калий, кальций, магний, натрий 2 Альбумин, общий белок, хлорид – ионы 3 Аммиак, глюкоза, железо, креатинин, медь, общие липиды, фосфор неорг. 5 Адреналин, АлАТ, АсАТ, иммуноглобулины, КФК, ЛДГ, мочевая кислота, мочевина, триглицериды, ЩФ, холестерин 7 Белковые фракции, глюкозо-6-фосфатдегидрогеназ 8 L- амилаза, билирубин, ГГТП 10
Слайд 40: Установление контрольных пределов
X ср. + 1S = 10 0 + 2,5•1 = 102,5 X ср. – 1 S = 10 0 – 2,5•1 = 97,5 X ср. + 2 S = 100 + 2,5•2 = 105 X ср. – 2 S = 10 0 – 2,5• 2 = 95 X ср. + 3 S = 10 0 + 2,5•3 = 107,5 X ср. – 3 S = 10 0 – 2,5•3 = 92,5
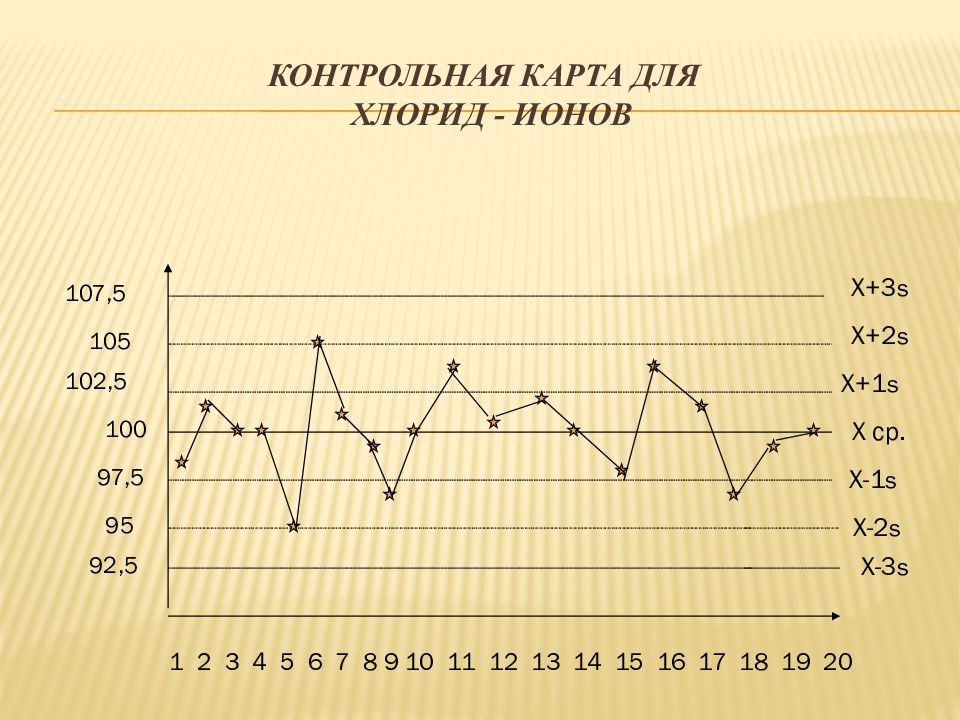
Слайд 41: Контрольная карта для хлорид - и онов
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 X ср. X+1 s X+2 s X+3 s X-2 s X-1 s X-3 s 100 102,5 105 107,5 97,5 95 92,5
Слайд 42: Контрольные правила Westgard
1 2s - если одно контрольное измерение оказалось за пределами ( Xср. + 2S), тогда проводится проверка нижеследующих контрольных признаков : 1 3s - одно контрольное измерение выходит за пределы ( Xср. + 3S); 2 2s - два последних контрольных измерения превышают предел ( Xср.+ 2S) или лежат ниже ( Xср. - 2S) ;
Слайд 43
R 4s - два контрольных измерения одной аналитической серии находятся по разные стороны от коридора ( Xср. + 2S ) ; 4 1s - четыре последних контрольных измерения превышают предел ( Xср.+ 1S) или лежат ниже ( Xср. - 1 S) ; 10х - десять последних контрольных измерений лежат по одну сторону от Хср.
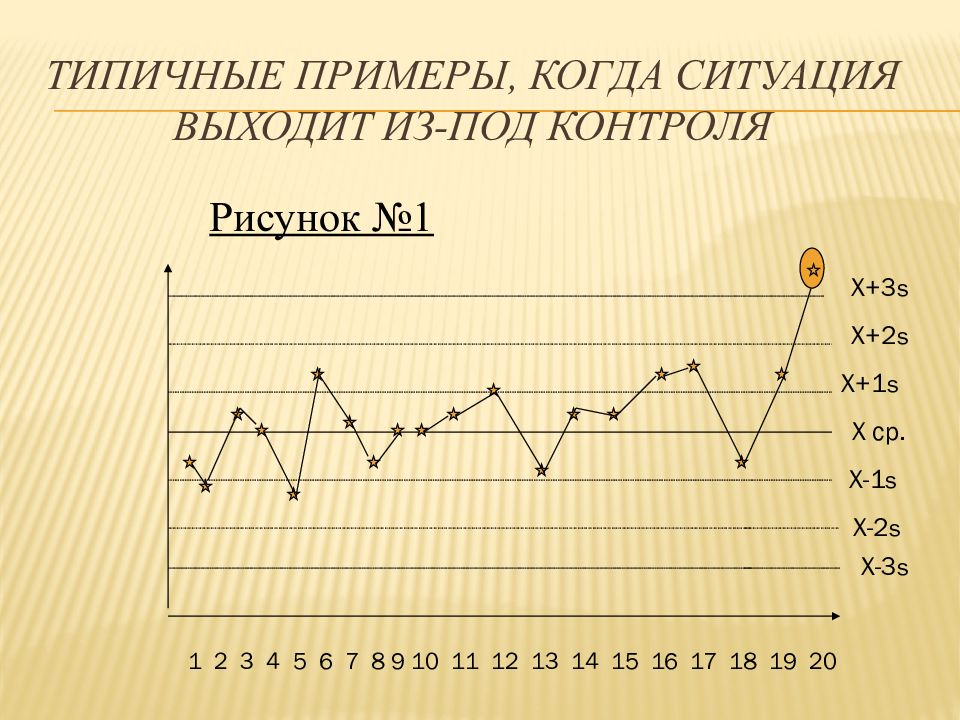
Слайд 44: Типичные примеры, когда ситуация выходит из-под контроля
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 X ср. X+1 s X+2 s X+3 s X-2 s X-1 s X-3 s Рисунок №1
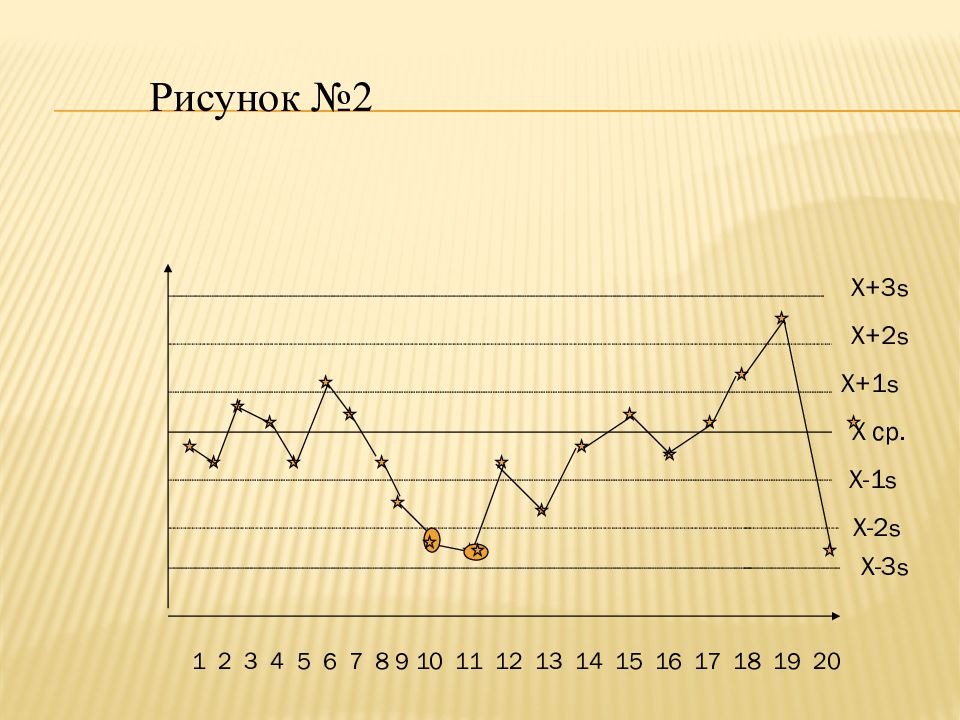
Слайд 45
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 X ср. X+1 s X+2 s X+3 s X-2 s X-1 s X-3 s Рисунок №2
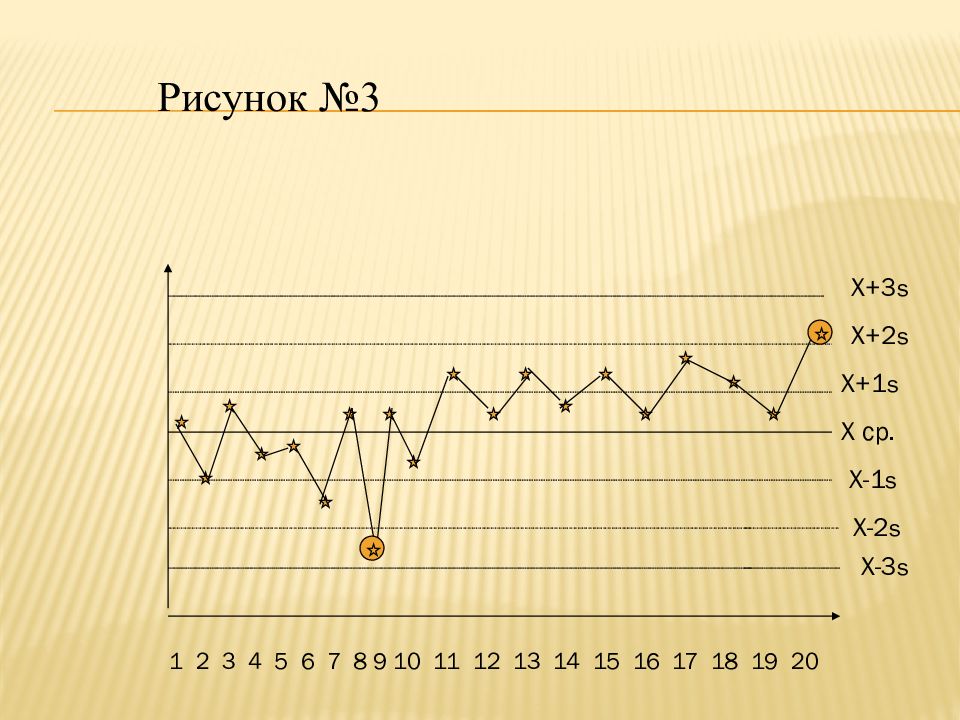
Слайд 46
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 X ср. X+1 s X+2 s X+3 s X-2 s X-1 s X-3 s Рисунок №3
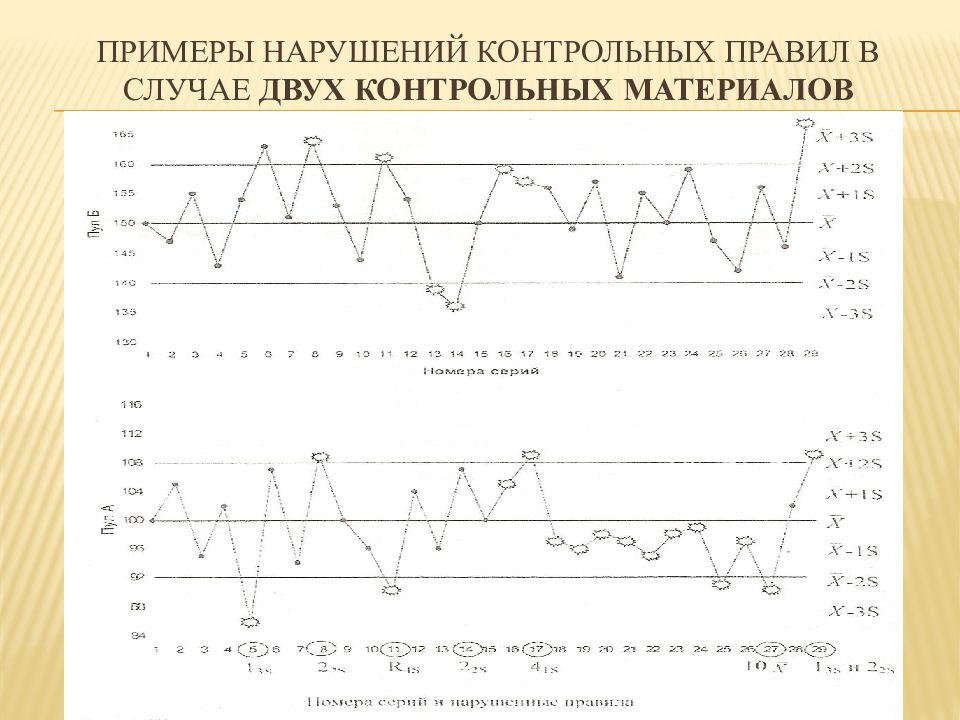
Слайд 47: Примеры нарушений контрольных правил в случае двух контрольных материалов
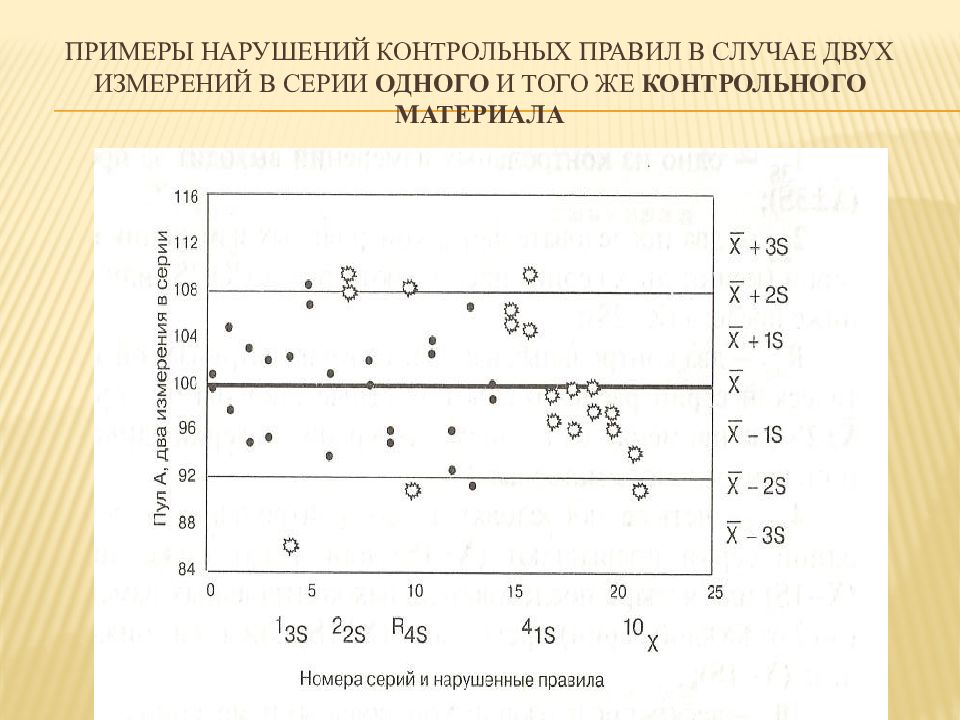
Слайд 48: Примеры нарушений контрольных правил в случае двух измерений в серии одного и того же контрольного материала
Слайд 49
Обнаружение контрольных признаков 1 3s и R 4s свидетельствует о наличие случайных ошибок. 1 3s - о грубой ошибке. Наличие контрольных признаков 2 2S, 4 1S, 10 X – о систематических ошибках.
Слайд 50: КАЛИБРОВКА
– это соотнесение показаний прибора с концентрацией определяемого вещества. Для проведения калибровки используются калибраторы (или стандартные растворы) - материалы, в которых с предельно допустимой точностью установлена концентрация определяемого соединения.
Слайд 51: построениЕ калибровочнОГО графикА
используют четыре различных концентрации (калибровочных точек) в диапазоне низких, нормальных и высоких концентраций определяемого аналита ; для каждой концентрации согласно методике определения проводят три параллельных исследования, в которых определяют оптическую плотность D ; если результаты получаются разными, то усреднять их не следует.
Слайд 52
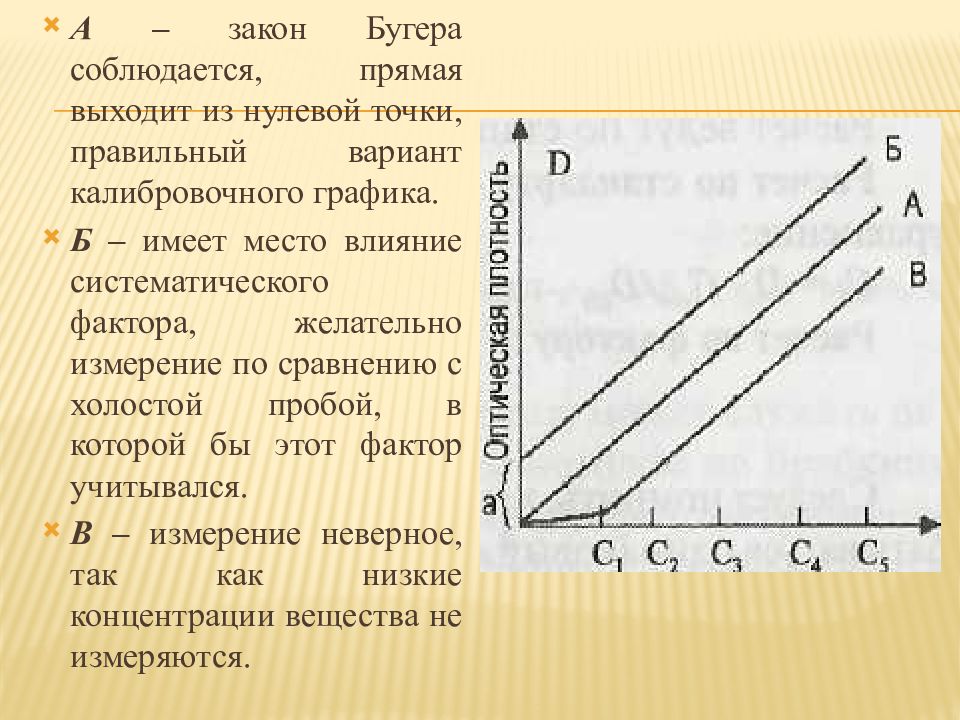
А – закон Бугера соблюдается, прямая выходит из нулевой точки, правильный вариант калибровочного графика. Б – имеет место влияние систематического фактора, желательно измерение по сравнению с холостой пробой, в которой бы этот фактор учитывался. В – измерение неверное, так как низкие концентрации вещества не измеряются.
Последний слайд презентации: Контроль качества лабораторных исследований: Оценка калибровочной кривой:
определяется минимальная концентрация, которую достоверно можно отличить от близлежащих величин по кривой; определяется зона линейности (отрезок кривой, на которой четко прослеживается пропорциональность возрастания оптической плотности с увеличением концентрации); определяется выход на плато (установление концентрации, начиная с которой увеличение ее не приводит к возрастанию оптической плотности); определяется рабочая зона - участок кривой от минимально определяемой концентрации до выхода на плато.