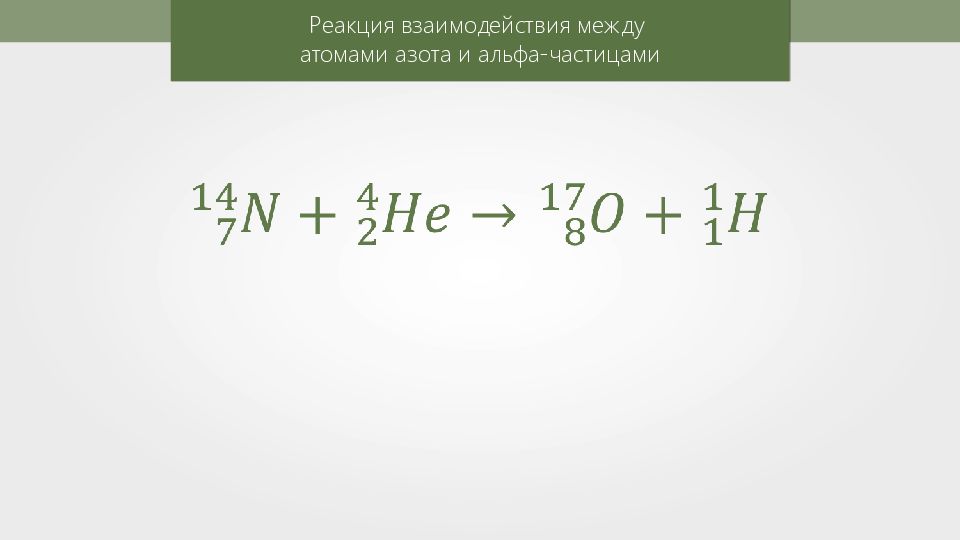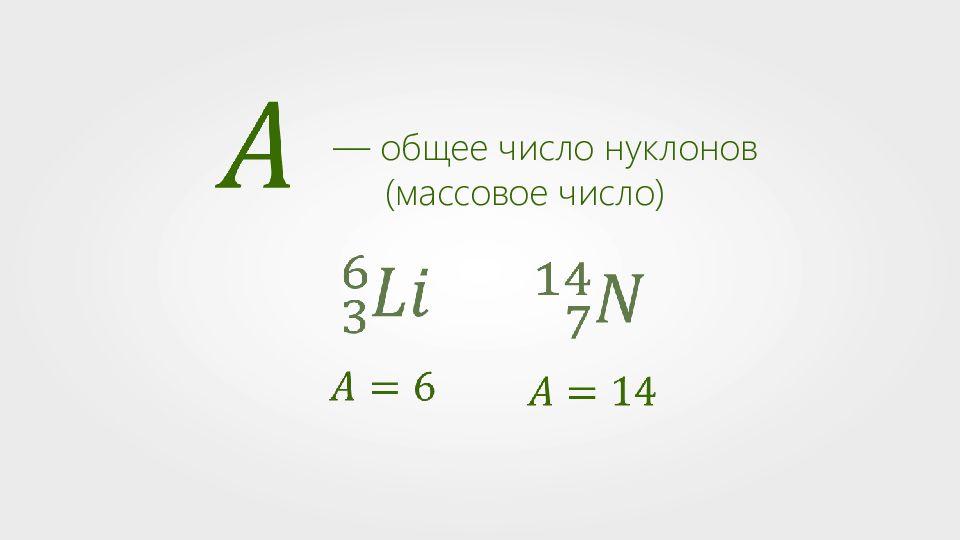Слайд 2
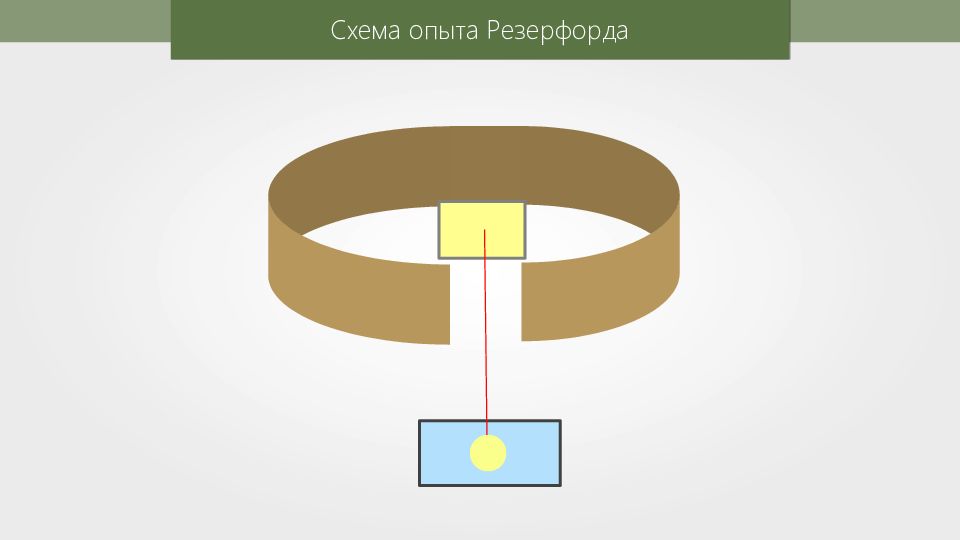
Эрнест Резерфорд 1871–1937 гг. В 1913 г. предположил, что одна из частиц, входящих в состав каждого атома, есть не что иное, как ядро атома водорода.
Слайд 3
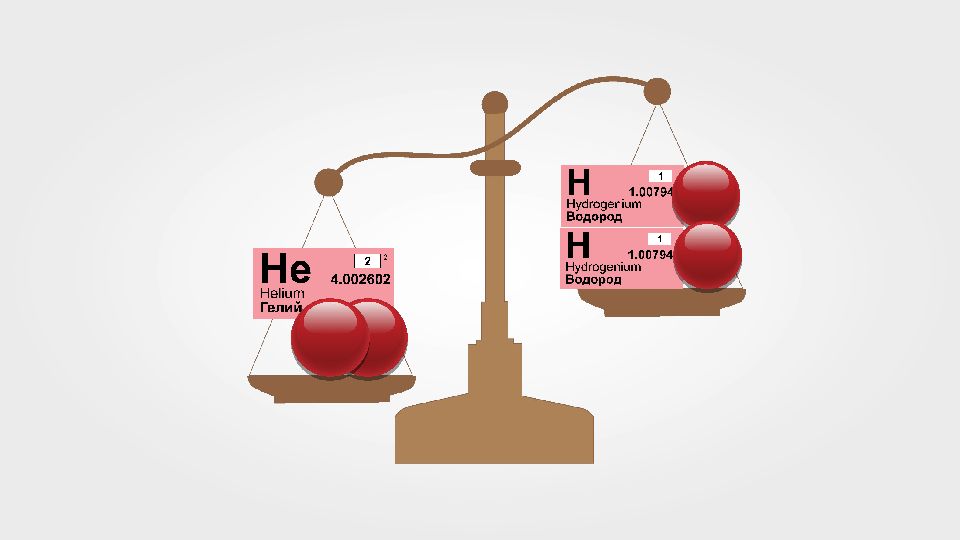
Масса ядра любого химического элемента отличается от массы ядра водорода в целое число раз. Атом водорода
Слайд 5
Эрнест Резерфорд 1871–1937 гг. Атом водорода, то есть частица, которая, входит в состав атома, Резерфорд назвал протоном. В переводе с греческого слово «протон» означает «первый».
Слайд 7
Обозначение протона Величина заряда протона по модулю равна величине заряда электрона.
Слайд 12
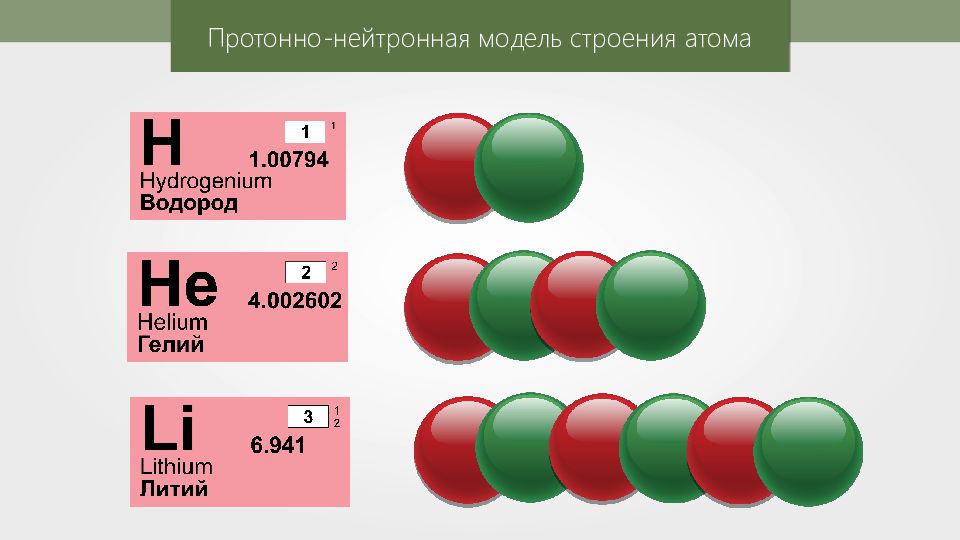
Эрнест Резерфорд 1871–1937 гг. Предположил, что существует нейтральная частица, то есть частица, у которой нет заряда. Эта частица входит в состав ядра. Она получила название нейтрон.
Слайд 19
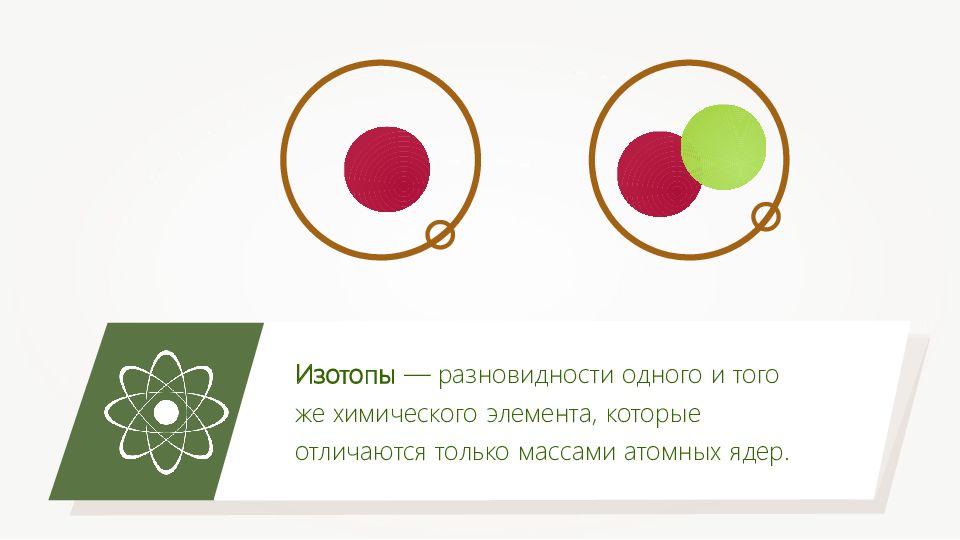
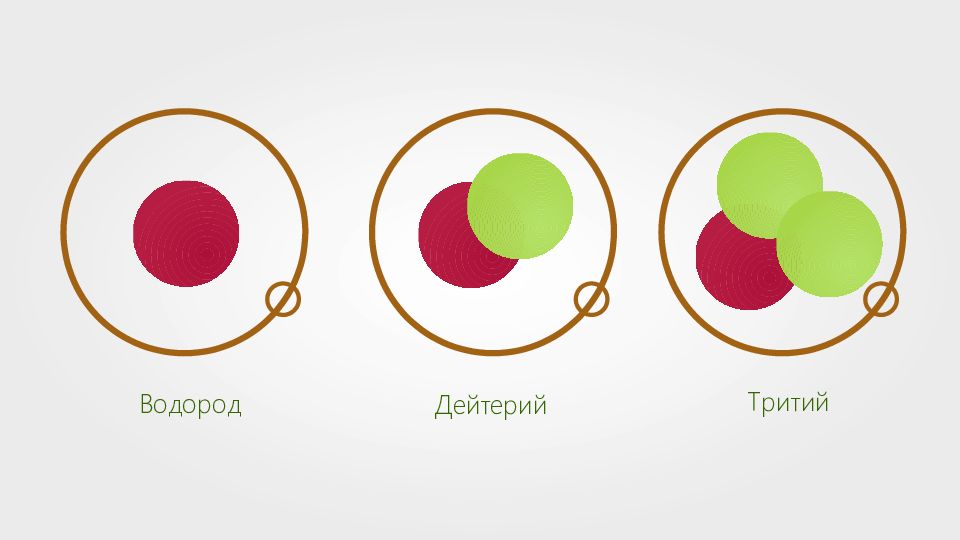
Изотопы — разновидности одного и того же химического элемента, которые отличаются только массами атомных ядер.