Первый слайд презентации: Знаки химических элементов. Относительная атомная масса
скисание молока, испарение воды, образование ржавчины, горение древесины, гашение соды уксусом, горение свечи, таянье льда, кипение воды, подгорание пищи на сковороде, испарение жидкой ртути, замерзание воды, почернение серебряных изделий, образование тумана,
Слайд 3
физические химические испарение воды скисание молока таянье льда образование ржавчины кипение воды горение древесины образование тумана гашение соды уксусом испарение жидкой ртути горение свечи замерзание воды подгорание пищи на сковороде почернение серебряных изделий
Слайд 4
Другого ничего в природе нет Ни здесь, ни там, в космических глубинах: Все – от песчинок малых до планет – Из элементов состоит единых. «Читая Менделеева» С. Щипачев
Слайд 5
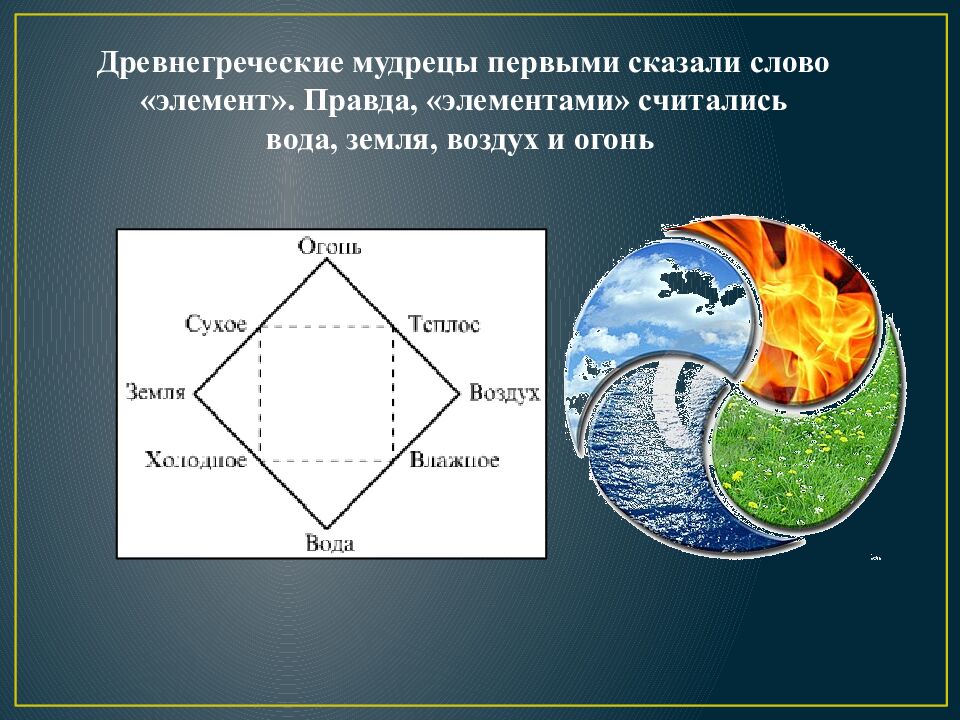
Древнегреческие мудрецы первыми сказали слово «элемент». Правда, «элементами» считались вода, земля, воздух и огонь
Слайд 6
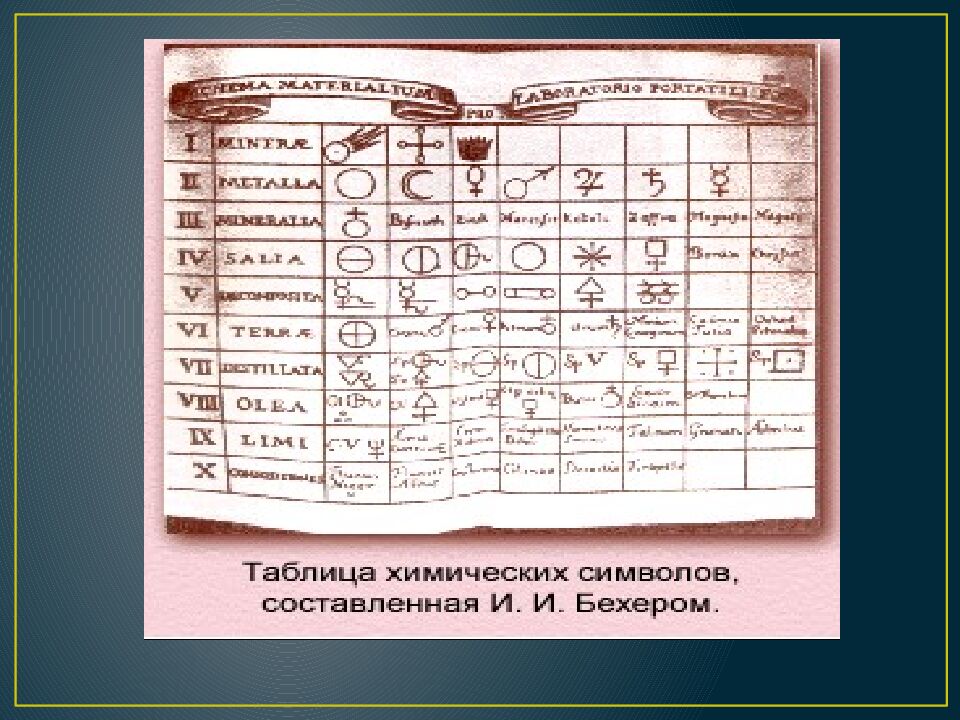
В средние века ученые знали уже десять химических элементов – семь металлов ( золото, серебро, медь, железо, олово, свинец, и ртуть ) и три неметалла ( серу, углерод, и сурьму ). Обозначение химических элементов алхимиками СЕРЕБРО СВИНЕЦ ОЛОВО ЗОЛОТО РТУТЬ МЕДЬ
Слайд 7: В древности и средние века были известны только 7 металлов
Золото Ртуть Медь Железо Серебро Олово Свинец
Золото называлось Солнцем, а обозначалось кружком с точкой: Медь – Венерой, символом этого металла служило «венерино зеркальце»: А железо – Марсом; как и полагается богу войны, обозначение этого металла включало щит и копье:
Слайд 10: Алхимики считали, что элементы связаны со звёздами и планетами
Золото - Солнце Серебро - Луна Медь - Венера Железо - Марс
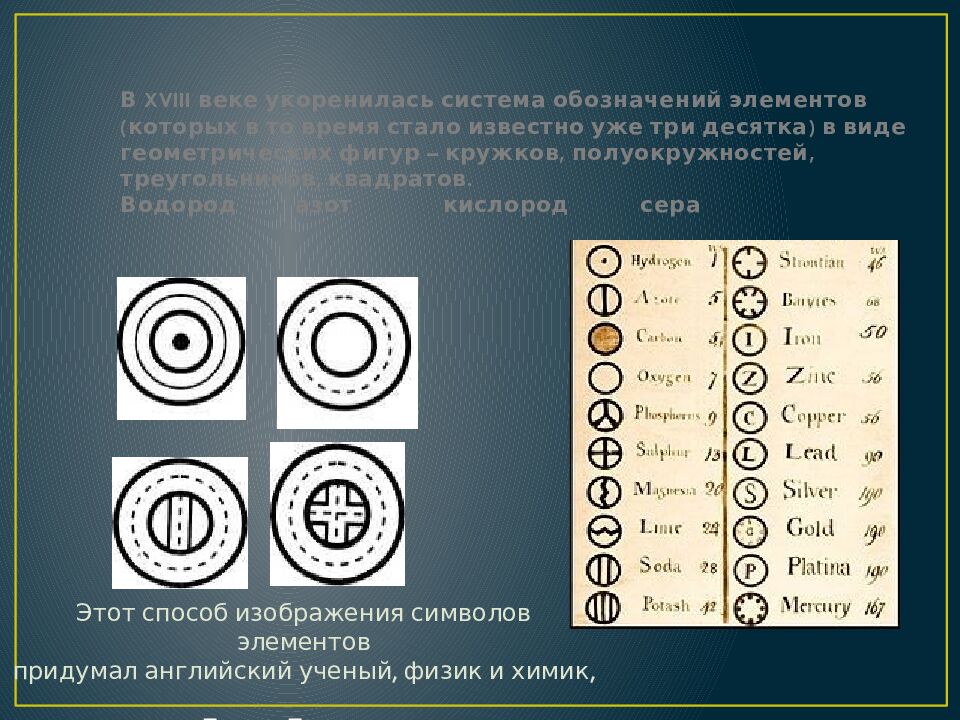
Слайд 12: В XVIII веке укоренилась система обозначений элементов (которых в то время стало известно уже три десятка) в виде геометрических фигур – кружков, полуокружностей, треугольников, квадратов. Водород азот кислород сера
Этот способ изображения символов элементов придумал английский ученый, физик и химик, Джон Дальтон.
Слайд 14: В 1814 году шведский химик Йенс Якоб Берцелиус предложил обозначать химические элементы первой буквой латинского названия элемента
Углерод – Carboneum – C Золото – Aurum – Au Водород – Hydrogenium – H Ртуть - Hidrargirum - Hg Символ Русское название Произношение Ag Серебро Аргентум C Углерод Це P Фосфор Пэ F Фтор Фтор Cl Хлор Хлор Zn Цинк Цинк
Слайд 16
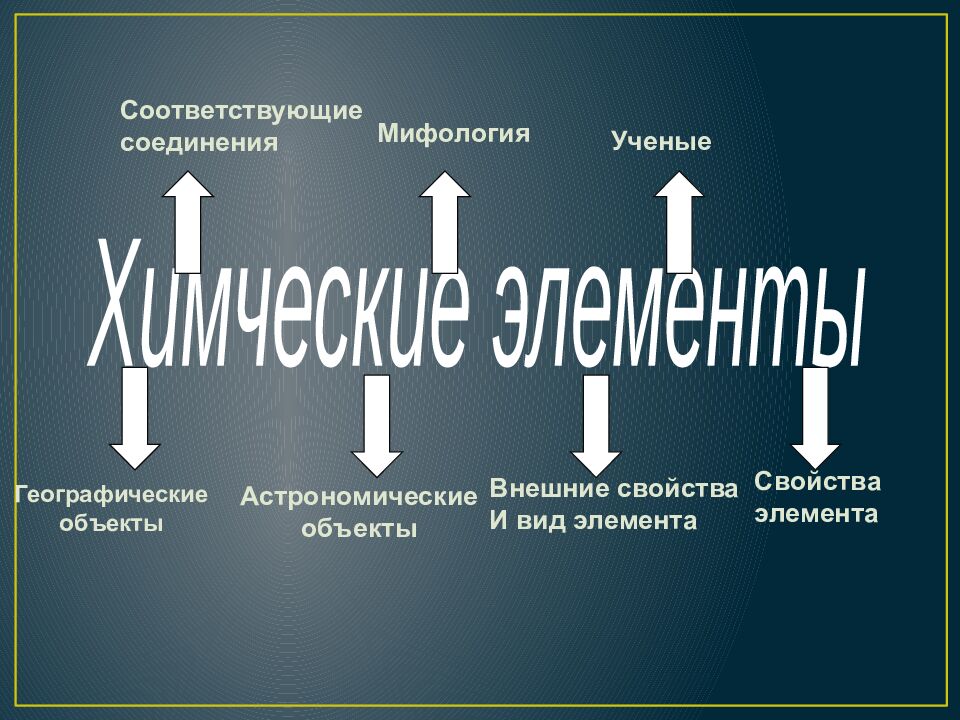
Географические объекты Астрономические объекты Внешние свойства И вид элемента Свойства элемента Соответствующие соединения Мифология Ученые Химческие элементы
Слайд 17
Географические объекты Германий ( от лат.- Germnia) Полоний ( в честь Польши ) Галлий ( от лат. Gallia- Франция ) Рутений (от. Ruthenia - Россия)
Слайд 18
Астрономические объекты Селен ( от греч. Selene- луна ) Нептуний (в честь планеты Нептун ) Гелий ( от греч. Helios- Солнце) Плутоний ( в честь планеты Плутон)
Слайд 19
Внешние свойства и вид элемента Литий ( от греч. Lithos – камень) Барий ( от греч. Barys – тяжелый)
Слайд 20
свойства элемента Серебро ( лат. название от argentum – светлый, белый) Железо ( лат. название от греко-латинского Fars -быть твердым) Водород ( лат. название от греч. Hydry genes- порождающий воду)
Слайд 21
Соответствующие соединения Азот ( лат. название от греч. Hitron genes- образующий селитру) Алюминий ( лат. alumen- квасцы)
Слайд 22
Мифология Ванадий ( в честь Vanadis - скандинавская богиня красоты ) Кобальт ( от нем. Kobold- гром )
Слайд 23
Менделевий ( Md ) № 101 – в честь Д.И. Менделеева Ученые Кюрий ( в честь французских химиков Пьера (1859-1906 ) и Марии (1867-1934)
Слайд 24: Элементы, названные в честь городов
Гафний ( Hf ) № 72 – в честь Копенгагена Берклий ( Bk ) № 97 – в честь города в США
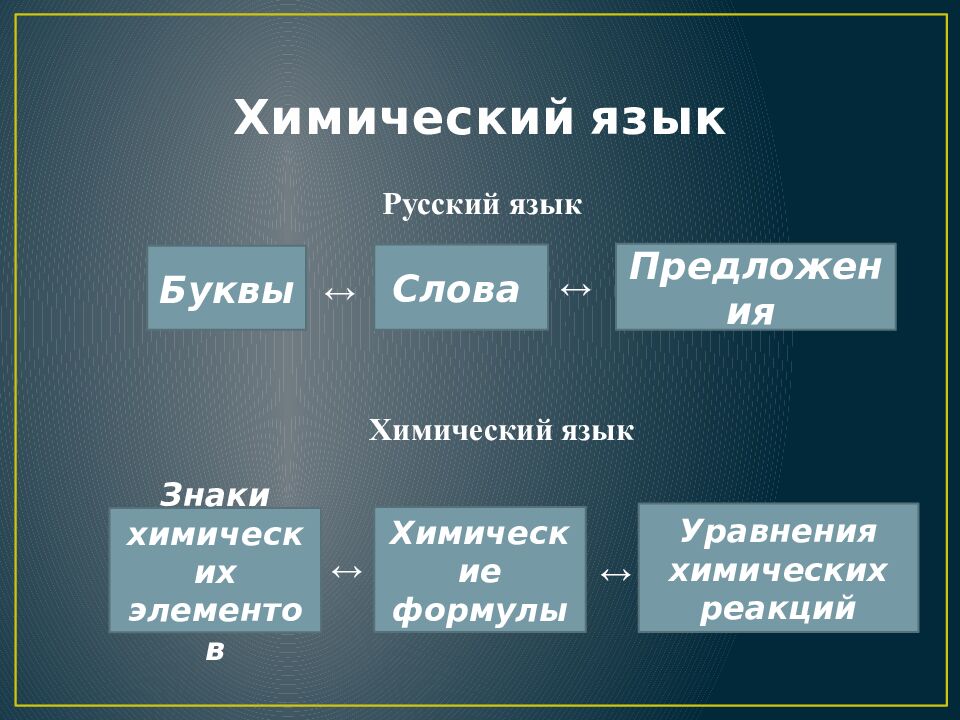
Слайд 25: Химический язык
Русский язык Буквы Слова Предложения Знаки химических элементов Химические формулы Уравнения химических реакций Химический язык ↔ ↔ ↔ ↔
Слайд 26
Авторы славянской письменности Кирилл и Мефодий Отец химической письменности Й. Я. Берцелиус
Слайд 27
Знаки химических элементов неметаллы металлы Кислород – О Железо - Fe Водород - H Натрий - Na Сера - S Кальций - Ca Фосфор - P Медь - Cu Азот - N Магний - Mg Кремний - Si Калий - K
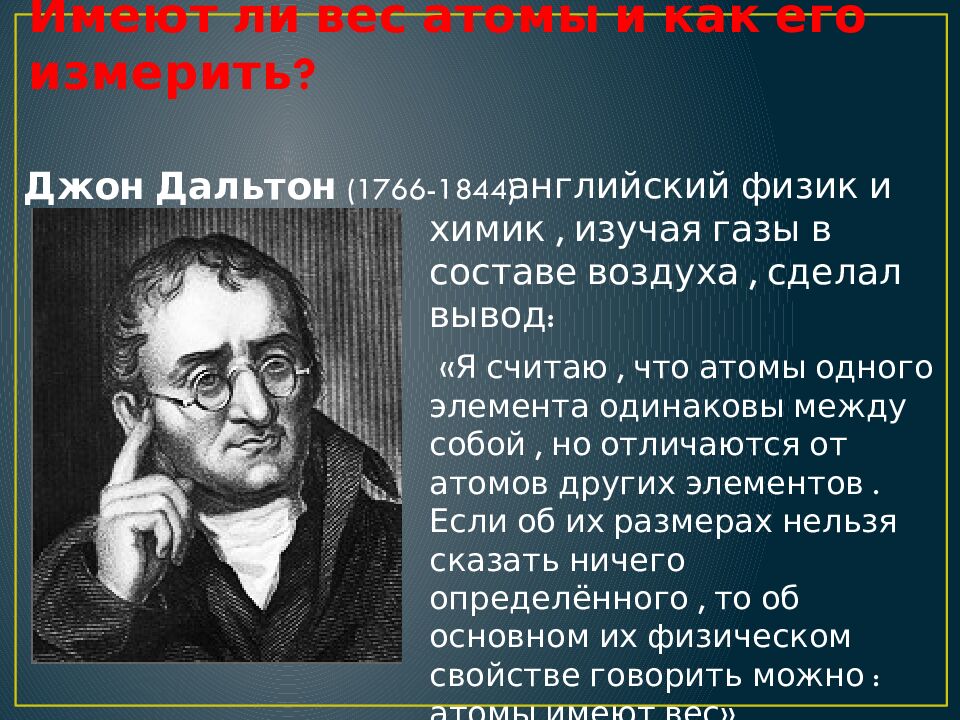
Слайд 28: Имеют ли вес атомы и как его измерить?
Джон Дальтон (1766-1844) английский физик и химик, изучая газы в составе воздуха, сделал вывод: «Я считаю, что атомы одного элемента одинаковы между собой, но отличаются от атомов других элементов. Если об их размерах нельзя сказать ничего определённого, то об основном их физическом свойстве говорить можно : атомы имеют вес».
Слайд 29: Массы атомов ничтожно малы
Масса самого лёгкого атома водорода 0,000 000 000 000 000 000 000 001 674 г или 1,674 * 10 -24 г Масса самого тяжёлого атома урана 0,000 000 000 000 000 000 000 395 г или 3,95 * 10 -22 г Пользоваться такими величинами неудобно!
Слайд 30: Эталон для сравнения атомных масс
Учёные пытались сопоставить во сколько раз массы атомов одних элементов тяжелее других. Джон Дальтон сравнивал атомные массы химических элементов с массой самого лёгкого атома водорода и в 1803 году составил первую таблицу относительных атомных масс элементов по водороду. Шведский химик Йёнс Якоб Берцелиус в 1818 году предложил для сравнения массу атома кислорода. В 1961 году эталоном измерения или атомной единицей массы принята 1/12 часть массы атома углерода. Эталон для сравнения атомных масс н о 1 / 12 C
Слайд 31: Атомная единица массы
m(1 а.е.м.)= 0,00000000000000000000000000166 кг= 1,66 × 10 -27 кг m a (H)=1 а.е.м. m a (He)=4 а.е.м.
Слайд 32: Относительная атомная масса -А r
А r показывает во сколько раз масса атома элемента больше 1/12 части массы атома углерода или а.е.м. А r англ. « relative » - относительный величина безразмерная
Слайд 34: Значения относительных атомных масс некоторых химических элементов
водород 1 1,00797 кислород углерод 15,9994 12,01115 8 6 А r (Н) =1 А r (С) =12 А r (О) =16
Слайд 35: Дробное значение А r
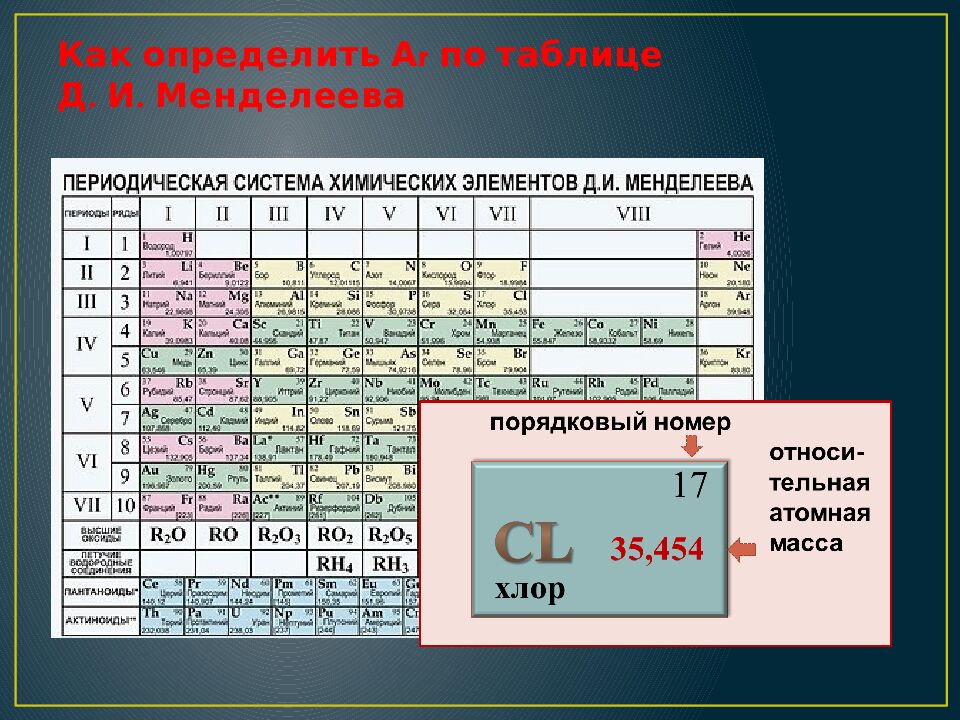
хлор 17 35,454 В расчётах используют значения относительных атомных масс, округлённые до целых чисел, но в случае с хлором для более точных вычислений пользуются дробной величиной А r (С l )=35,5
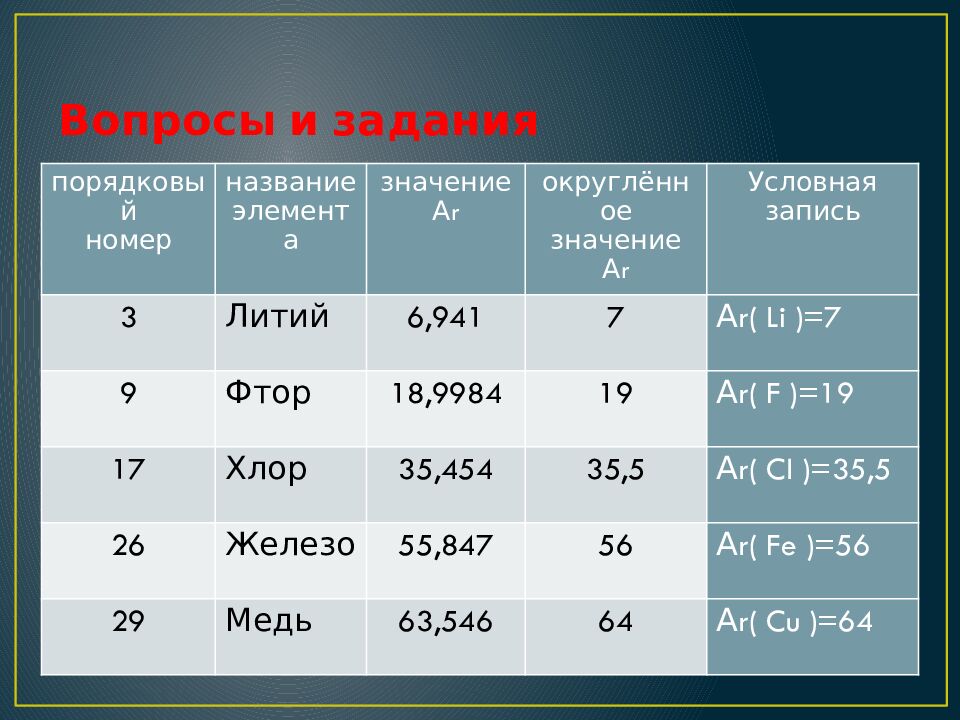
Последний слайд презентации: Знаки химических элементов. Относительная атомная масса: Вопросы и задания
Что означают записи: m a (Al)=27 a.e. м. m a (S)=32 a.e. м. А r(Al)=26,9815≈27 Ar (S)=32,064≈32 Напишите округлённые значения относительных атомных масс элементов № 3, 9, 17, 26, 29 Определите во сколько раз масса атома железа больше а) массы атома водорода б) массы атома кислорода в) 1/12 массы атома углерода порядковый номер название элемента значение А r округлённое значение А r Условная запись 3 Литий 6,941 7 А r( Li )=7 9 Фтор 18,9984 19 А r( F )=19 17 Хлор 35,454 35,5 А r( Cl )=35,5 26 Железо 55,847 56 А r( Fe )=56 29 Медь 63,546 64 А r( Cu )=64 Вопросы и задания