Первый слайд презентации
1 Лекция "Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц." Кафедра общей и медицинской химии
Слайд 3: Коллоидная химия
Коллоидная химия- раздел физической химии, занимающийся изучением дисперсных систем и их поверхностных явлений. 3 "Человек – бродячий коллоид" Коллоидная химия изучает физико- химические свойства высокодисперсных гетерогенных систем и гомогенных (разбавленных) растворов ВМС
Слайд 4
4 Дисперсные системы – гетерогенные системы, состоящие из дисперсионной среды, дисперсной фазы и стабилизатора.
Слайд 5
5 Дисперсная фаза –мелкораздробленные частицы, равномерно распределённые в дисперсной системе. Дисперсионная среда –однородная непрерывная фаза, в которой распределены частицы дисперсной фазы. Стабилизатор – необходим, чтобы система была устойчивой
Слайд 6
6 Можно смело сказать, что весь человек – это ходячий коллоид, а все органы и системы организма дисперсная система в их связи с поверхностными явлениями. Кости – это коллаген, насыщенный кальцием и фосфором, мигрирующими в присутствии витамина Д. Кровь – это дисперсная система, в которой ферментные элементы эритроциты, тромбоциты, лейкоциты являются фазой, а плазма – дисперсионной средой.
Слайд 7
7 Немного истории Итальянский учёный Франческо Сельми в 40-х годах IX века обратил внимание на аномальные свойства некоторых растворов, являющихся согласно современным представлениям, типичными коллоидными системами. Эти растворы рассеивают свет, растворённые в них вещества выпадают в осадок от прибавления к ним даже небольших количеств солей и т.д. Он назвал их « псевдорастворами», а позднее они получили название золей.
Слайд 8
8 20.12.1805 г. – 11.09 1869 г. Томас Грэм (иногда Грэхем) – английский химик, один из основоположников коллоидной химии. Во второй половине IX века ангийский учёный Томас Грэм подробно исследовал свойства растворов, заинтересовавших Сельми. Он назвал эти растворы, а также вещества, которые их образуют, коллоидами, т.к. думал, что клей, называемый по гречески «колла», является их типичным представителем.
Слайд 9
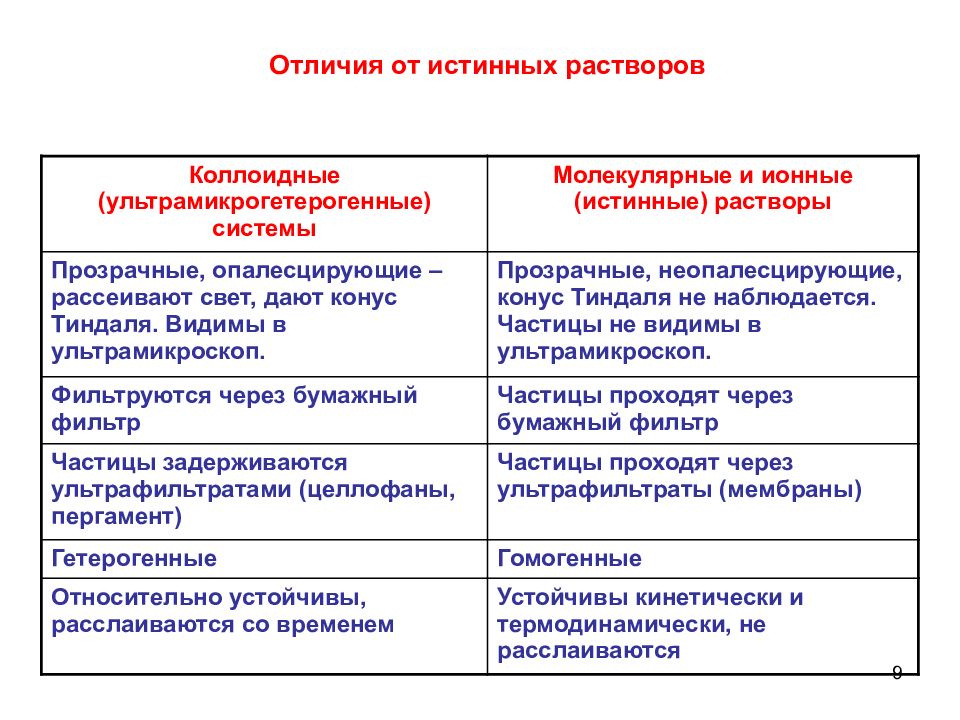
9 Коллоидные (ультрамикрогетерогенные) системы Молекулярные и ионные (истинные) растворы Прозрачные, опалесцирующие – рассеивают свет, дают конус Тиндаля. Видимы в ультрамикроскоп. Прозрачные, неопалесцирующие, конус Тиндаля не наблюдается. Частицы не видимы в ультрамикроскоп. Фильтруются через бумажный фильтр Частицы проходят через бумажный фильтр Частицы задерживаются ультрафильтратами (целлофаны, пергамент) Частицы проходят через ультрафильтраты (мембраны) Гетерогенные Гомогенные Относительно устойчивы, расслаиваются со временем Устойчивы кинетически и термодинамически, не расслаиваются Отличия от истинных растворов
Слайд 10
10 Зигмонди Рихард Адольф 1.06.1865 – 23.09.1929 Разработал (1898) методику получения и ультрафильтрации коллоидных растворов. Сконструировал (1903) ультрамикроскоп для наблюдения броуновского движения. Исследовал свойства и коагуляцию коллоидных растворов. Предложил классификацию коллоидных частиц по их размерам и взаимодействию с дисперсионной средой. Изучал (1911) структуру гелей. Разработал способы получения цветного стекла, в том числе матового. Нобелевская премия (1925г) « за установление гетерогенной природы коллоидных растворов и за разработанные в этой связи методы, имеющие фундаментальное значение в современной коллоидной химии»
Слайд 11
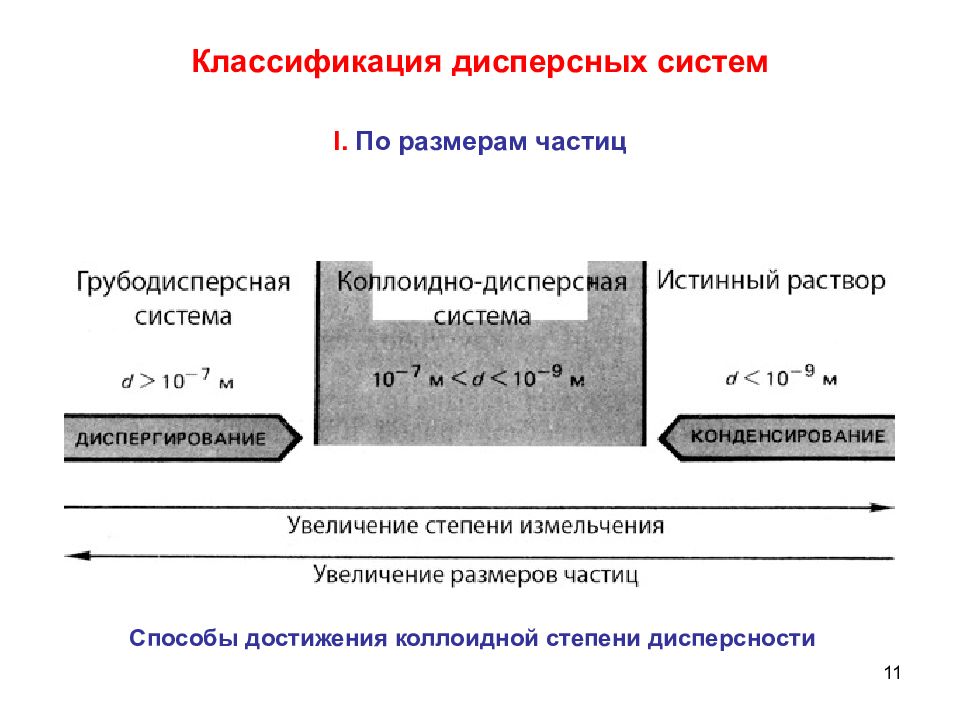
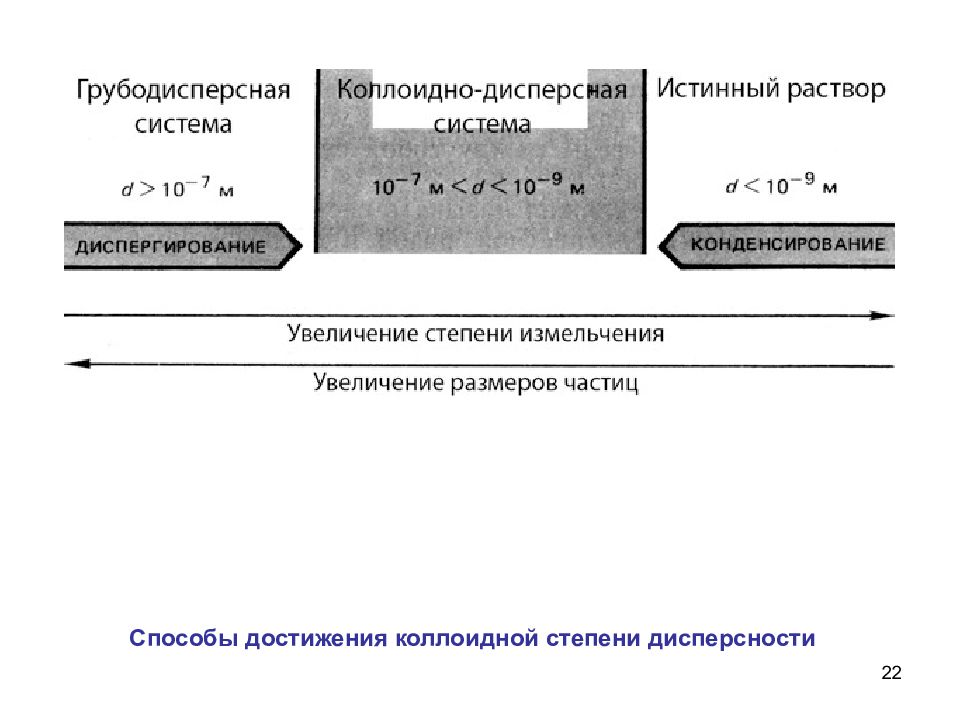
11 Классификация дисперсных систем I. По размерам частиц Способы достижения коллоидной степени дисперсности
Слайд 12
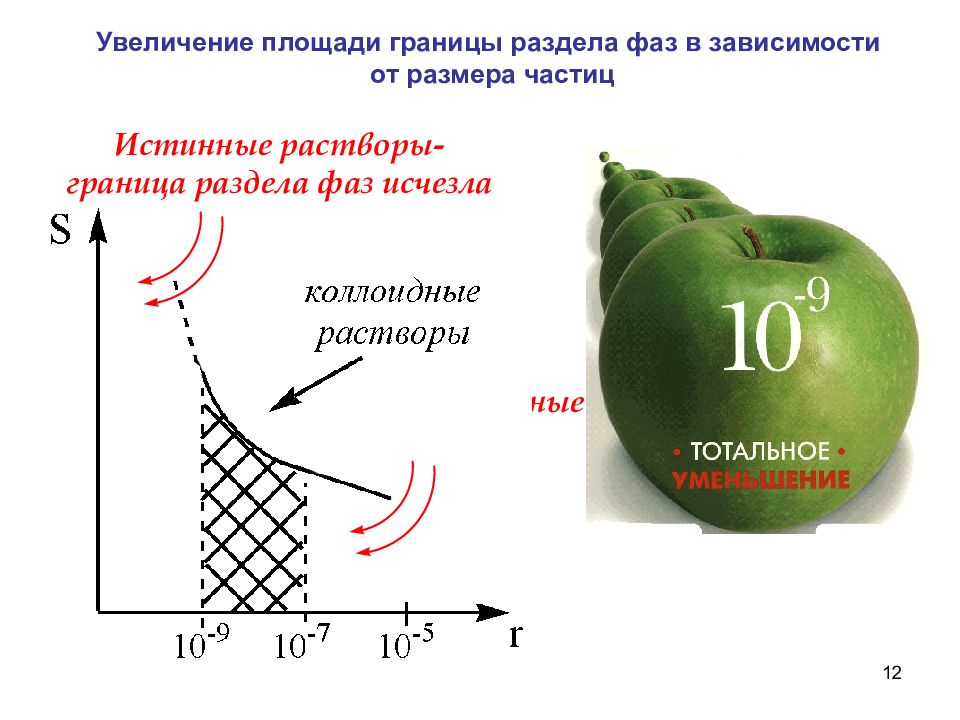
12 Увеличение площади границы раздела фаз в зависимости от размера частиц грубодисперсные системы Истинные растворы-граница раздела фаз исчезла
Слайд 13
13 Фаза Среда Газ Жидкость Твердое вещество Газ ---- Аэрозоли, туман, облака, жидких лекарств Пыль, дым, аэрозоли твердых лекарств Жидкость Мыльная и морская пена, газовые эмульсии Молоко, лекарственные эмульсии, мази Суспензии, коллоидные растворы, нерастворимые в воде лекарства Твердое вещество Хлеб, пемза, активированный уголь, силикагель Жемчуг, почва, слизь, гели, гелевые лекарства Цветные стекла, рубин, минералы, сплавы, драгоценные камни 2. По агрегатному состоянию (границе раздела фаз)
Слайд 16
16 Среда – твердая, фаза – жидкая жемчуг Среда - твердая, фаза – твердая рубин, сапфир
Слайд 18
18 Среда – жидкая, фаза – твердая суспензии, коллоидные растворы Среда - жидкая, фаза – жидкая Эмульсии, молоко, сливки
Слайд 20
20 3. По характеру взаимодействия дисперсной фазы с дисперсионной средой: Лиофобные системы: коллоидные растворы со стабилизатором (золи), суспензии, эмульсии, пены, аэрозоли (протаргол, преднизолон, красители, фибриноген) Лиофильные системы: коллоидные растворы ПАВ и ВМС (белки, мыла, глины, крахмал) Слабое взаимодействие между дисперсной фазой и дисперсионной средой ( гидратная оболочка -тонкая) Сильное взаимодействие между дисперсной фазой и дисперсионной средой (большая гидратная оболочка) Образуются за счет затраты энергии извне Образуются самопроизвольно Эндэргонический процесс образования Экзэргонический процесс образования Термодинамически неустойчивы Термодинамически устойчивы Необходим стабилизатор Стабилизатор не требуется
Слайд 21
21 4. По структурно-механическим свойствам Свободнодисперсные системы, обладают свойством текучести: лиозоли, суспензии, эмульсии, кровь, биологические мембраны, аэрозоли - туманы, дым, пыль Связнодисперсные системы, потеря текучести: лиогели, студни, волокнистые и пористые капиллярные системы (костная ткань, биологические мембраны, студни) Дисперсная фаза подвижна. Представлена отдельными не связанными между собой частицами, относительно равномерно распределенными в объеме дисперсионной среды Дисперсная фаза практически неподвижна, так как образует сплошную структуру (сетку, каркас), внутри которой заключена дисперсионная среда 5. По природе дисперсионной среды Жидкая - лиозоли Воздух - аэрозоли Твердая - солидозоли
Слайд 23
23 Способы получения золей I. Дисперсионные - из грубодисперсных систем ( измельчение) a) Механическое дробление - осуществляют с помощью шаровых и коллоидных мельниц в присутствии жидкой дисперсионной среды и стабилизатора. Схема коллоидной мельницы Схемы диспергаторов: а) – шаровая мельница; б) – коллоидная мельница
Слайд 24
24 б ) Электрическое диспергирование - используют для получения золей металлов. При получении органозолей (дисперсионная среда – органический растворитель) применяют высокочастотный искровой заряд. Теодор Сведберг (30.08.1884-25.021971) Его исследования были посвящены получению гидрозолей металлов с помощью распыления электрической искрой. Определил коэффициент диффузии коллоидных растворов, блестяще подтвердив теорию Эйнштейна-Смолуховского. Усовершенствовал ультрацентрифугу. Сфотографировал путь коллоидных частиц через ультрамикроскоп. Нобелевская премия (1926) «за работы в области дисперсных систем»
Слайд 25
25 в ) Измельчение с помощью ультразвука (дробление почечных камней) Почечный камень (в центре - урат, снаружи - скорлупа из фосфата) При диспергировании ультразвуком работают примерно с теми же частотами, которые используются в радиотехнике, т.е. сотни тысяч и миллионы герц.
Слайд 26
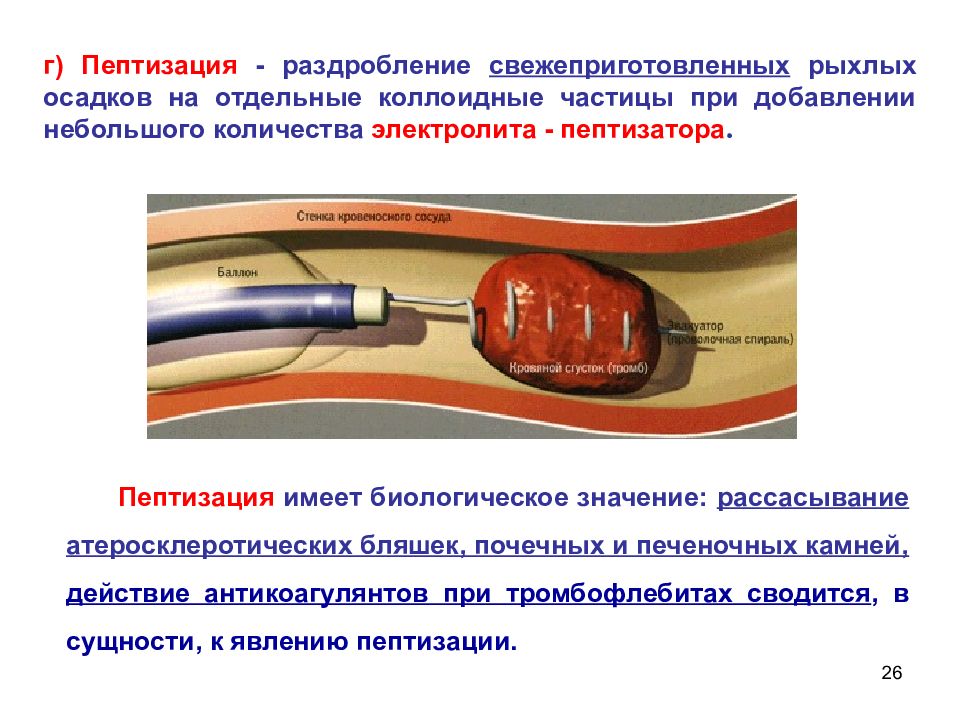
26 г ) Пептизация - раздробление свежеприготовленных рыхлых осадков на отдельные коллоидные частицы при добавлении небольшого количества электролита - пептизатора. Пептизация имеет биологическое значение: рассасывание атеросклеротических бляшек, почечных и печеночных камней, действие антикоагулянтов при тромбофлебитах сводится, в сущности, к явлению пептизации.
Слайд 27
27 II. Конденсационные – из истинных растворов (укрупнение ). а ) Физические - метод замены растворителя. Раствор вещества прибавляют к жидкости, в которой растворенное вещество мало растворимо и выделяется в виде высокодисперсной фазы. Золи серы, холестерина и канифоли получают добавлением спиртовых растворов этих веществ к воде. б) Химические 1 ) Реакции восстановления Формула мицеллы золя золота
Слайд 28
28 Реакции восстановления мицелла MnO 2 (при электрофорезе движется к аноду)
Слайд 29
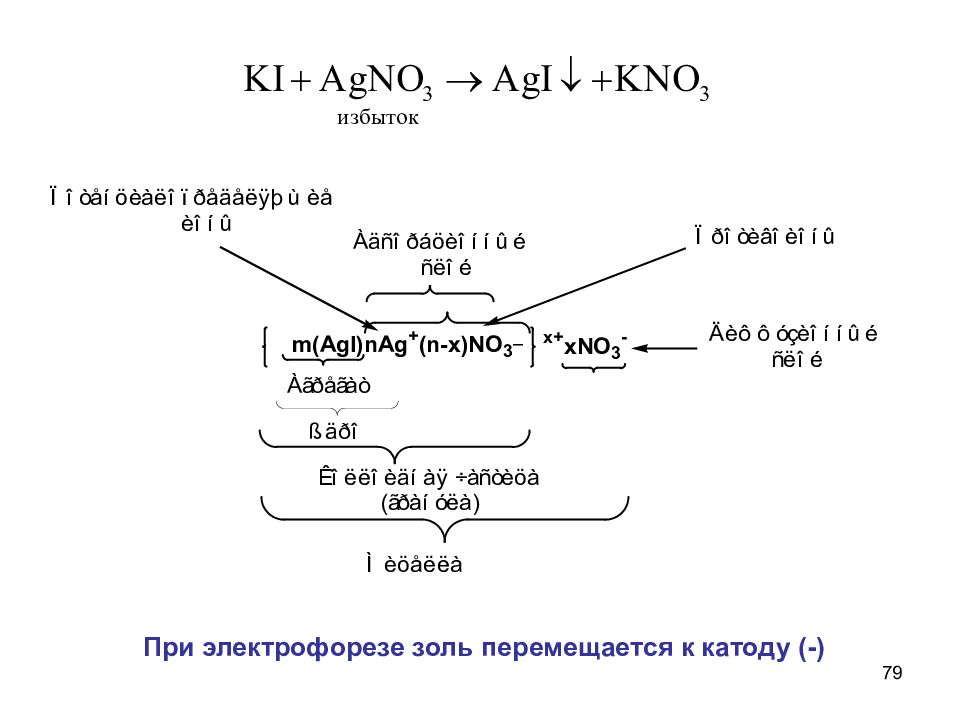
29 2) Реакции двойного обмена избыток избыток движется к аноду движется к катоду
Слайд 30
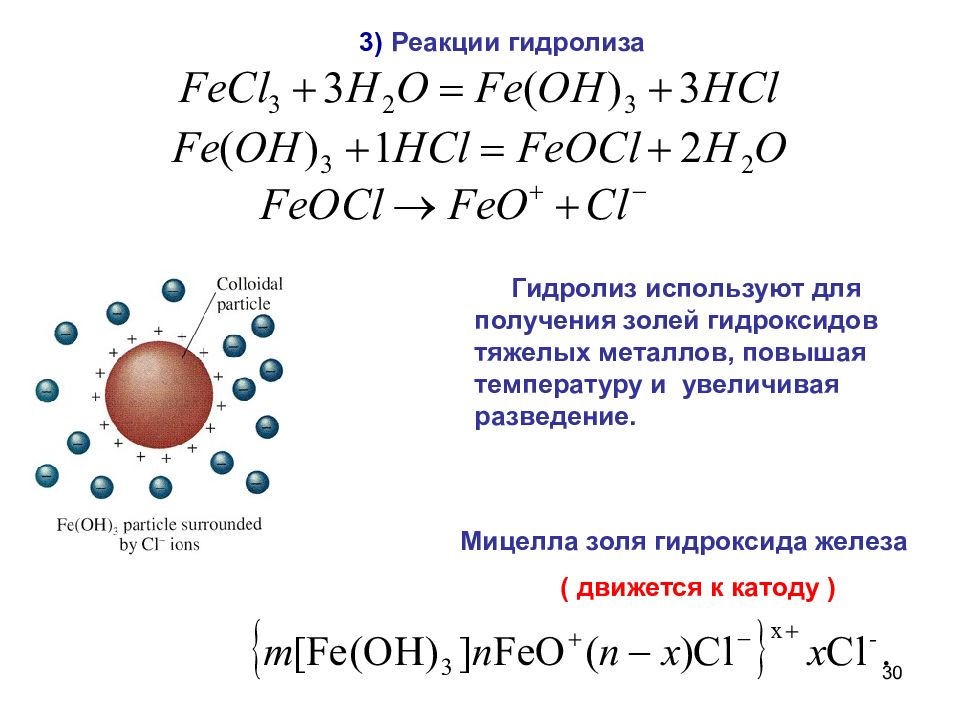
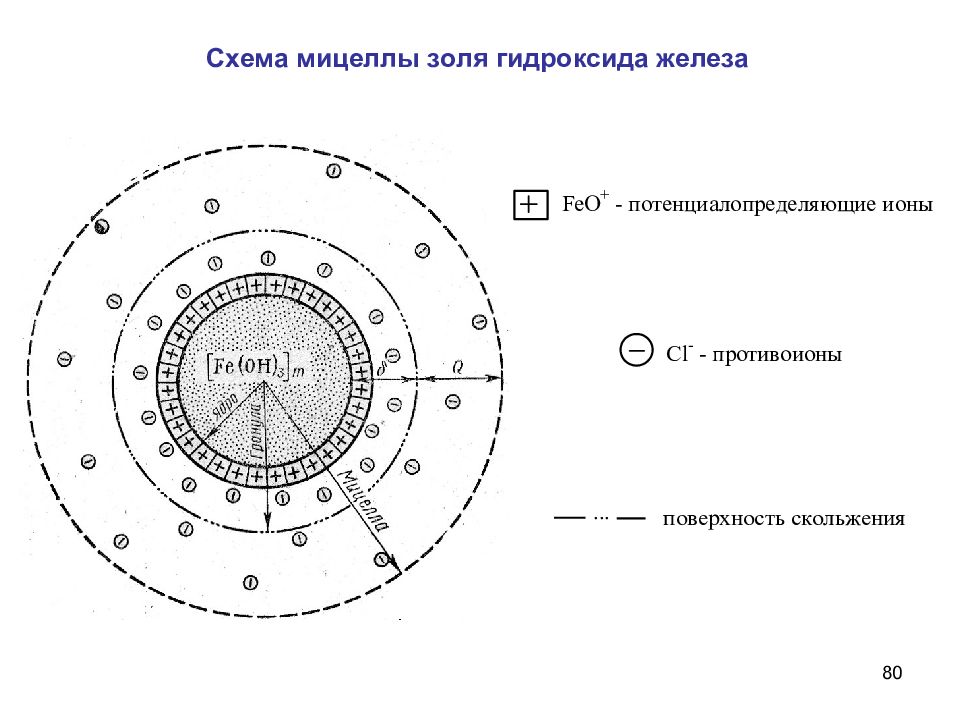
30 3 ) Реакции гидролиза Мицелла золя гидроксида железа Гидролиз используют для получения золей гидроксидов тяжелых металлов, повышая температуру и увеличивая разведение. ( движется к катоду )
Слайд 31
31 1. Обычная фильтрация Методы очистки коллоидных растворов (от низкомолекулярных веществ - электролитов) Фильтрацию используют для очистки коллоидных растворов от примесей грубодисперсных частиц. Фильтрация (от лат. filtrum – войлок) основана на способности коллоидных частиц проходить через поры обычных фильтров. При этом более крупные частицы задерживаются.
Слайд 32
32 Ультрафильтрация — это процесс мембранного разделения, а также фракционирования и концентрирования веществ, осуществляемые путем фильтрования жидкости под действием разности давлений до и после мембраны. Размер пор ультрафильтрационных мембран варьируется от 0,01-0,1 мкм. 2. Ультрафильтрация
Слайд 33
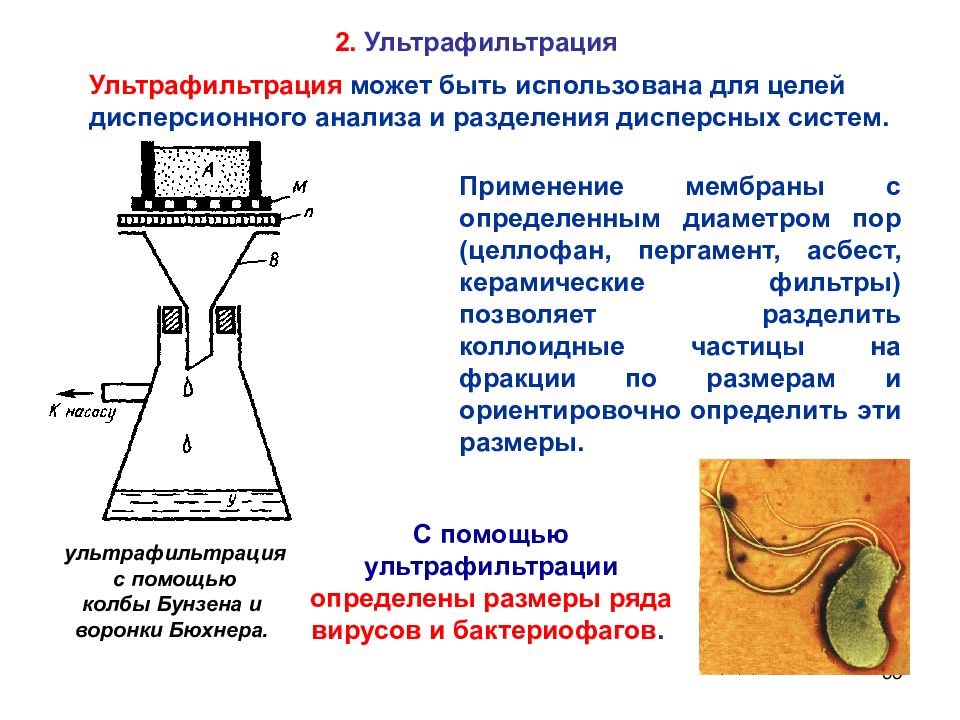
33 2. Ультрафильтрация Применение мембраны с определенным диаметром пор (целлофан, пергамент, асбест, керамические фильтры) позволяет разделить коллоидные частицы на фракции по размерам и ориентировочно определить эти размеры. ультрафильтрация с помощью колбы Бунзена и воронки Бюхнера. Ультрафильтрация может быть использована для целей дисперсионного анализа и разделения дисперсных систем. С помощью ультрафильтрации определены размеры ряда вирусов и бактериофагов.
Слайд 35
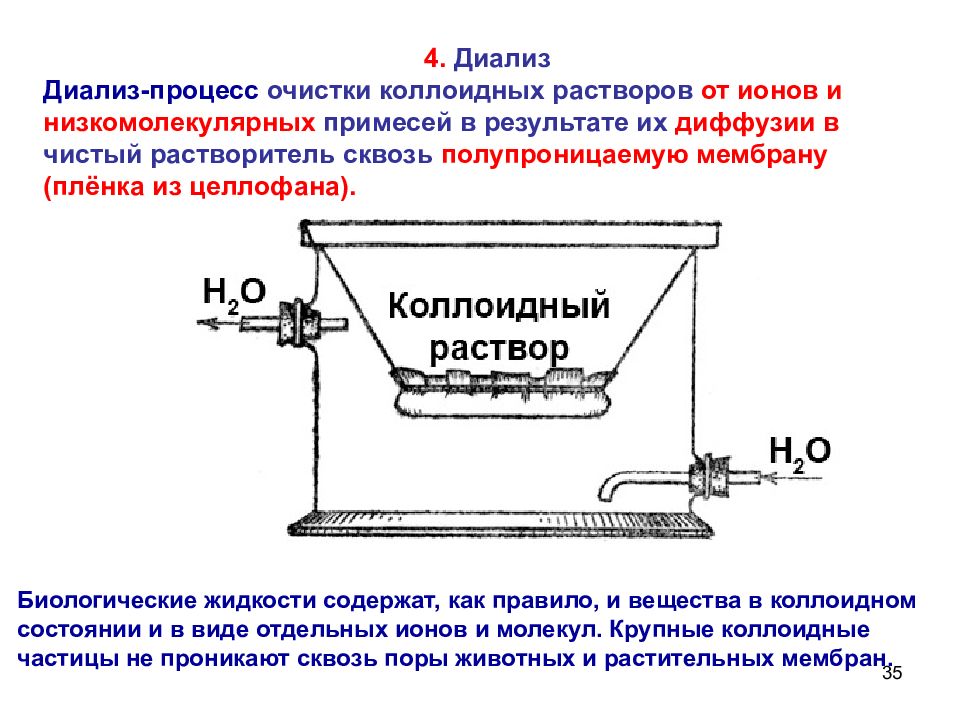
35 4. Диализ Диализ-процесс очистки коллоидных растворов от ионов и низкомолекулярных примесей в результате их диффузии в чистый растворитель сквозь полупроницаемую мембрану (плёнка из целлофана). Биологические жидкости содержат, как правило, и вещества в коллоидном состоянии и в виде отдельных ионов и молекул. Крупные коллоидные частицы не проникают сквозь поры животных и растительных мембран.
Слайд 36
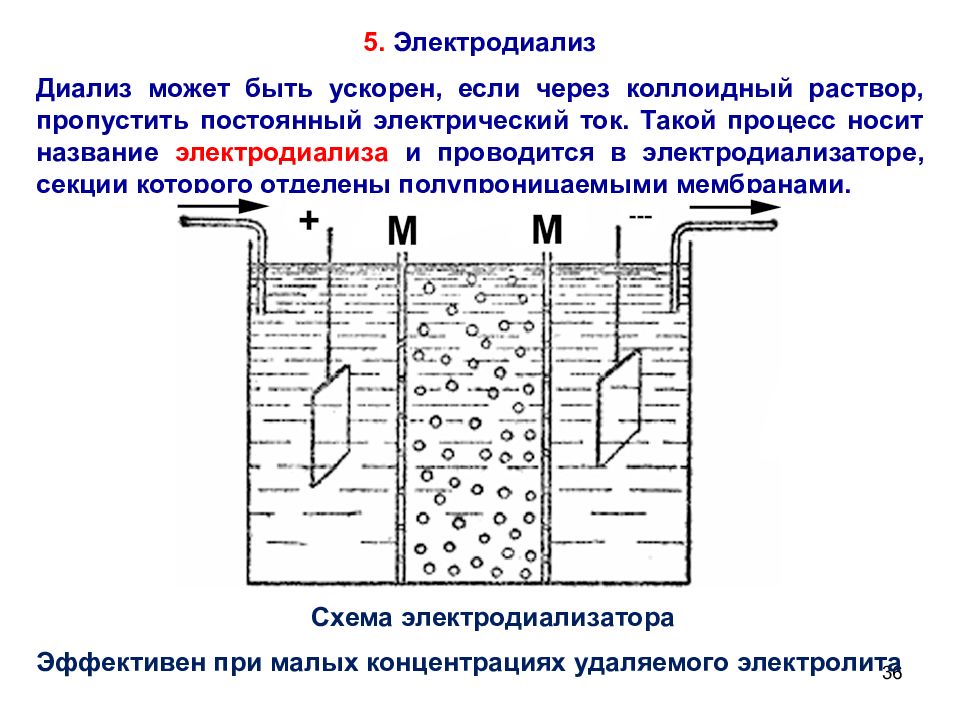
36 5. Электродиализ Диализ может быть ускорен, если через коллоидный раствор, пропустить постоянный электрический ток. Такой процесс носит название электродиализа и проводится в электродиализаторе, секции которого отделены полупроницаемыми мембранами. Схема электродиализатора Эффективен при малых концентрациях удаляемого электролита
Слайд 37
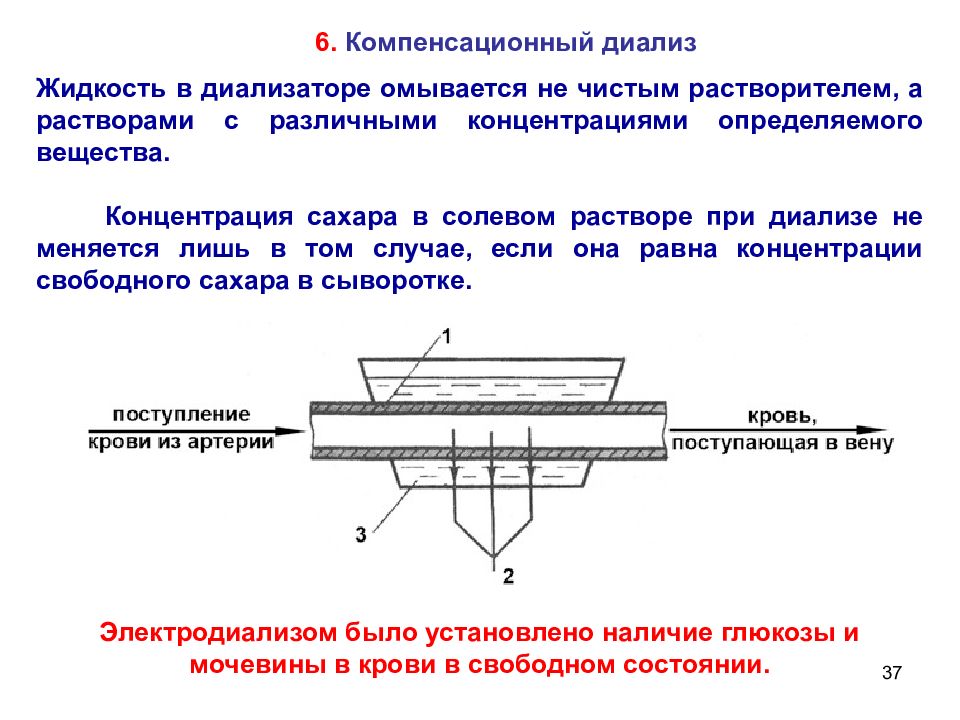
37 6. Компенсационный диализ Жидкость в диализаторе омывается не чистым растворителем, а растворами с различными концентрациями определяемого вещества. Концентрация сахара в солевом растворе при диализе не меняется лишь в том случае, если она равна концентрации свободного сахара в сыворотке. Электродиализом было установлено наличие глюкозы и мочевины в крови в свободном состоянии.
Слайд 38
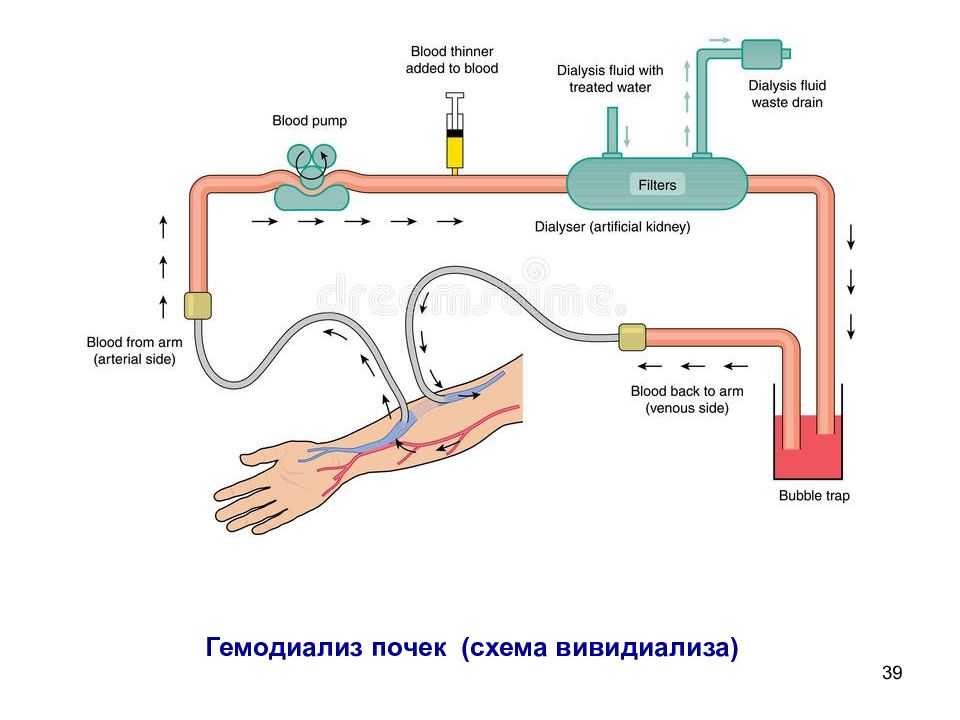
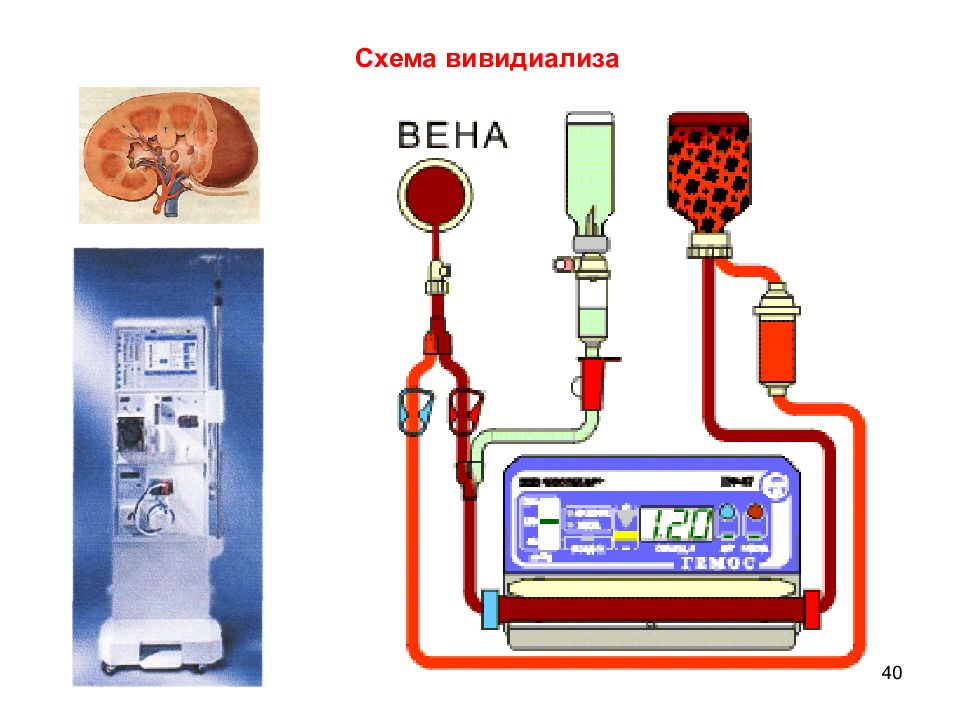
38 7. Вивидиализ (принцип аппарата «искусственная почка») Благодаря большой рабочей площади мембран (до 1.5 м 2 ) из крови достаточно быстро (за 3-4 часа) удаляются «шлаки» - продукты обмена и распада тканей (мочевина, креатинин, ионы калия) Показаниями к применению «искусственной почки» является острая почечная недостаточность при отравлениях сулемой, сульфаниламидными препаратами, при уремии после переливания крови, при тяжелых ожогах, токсикозе беременност и. Диализирующий раствор содержит одинаковые с кровью концентрации веществ, которые необходимо сохранить в крови. Схема аппарата для вивидиффузии
Слайд 41
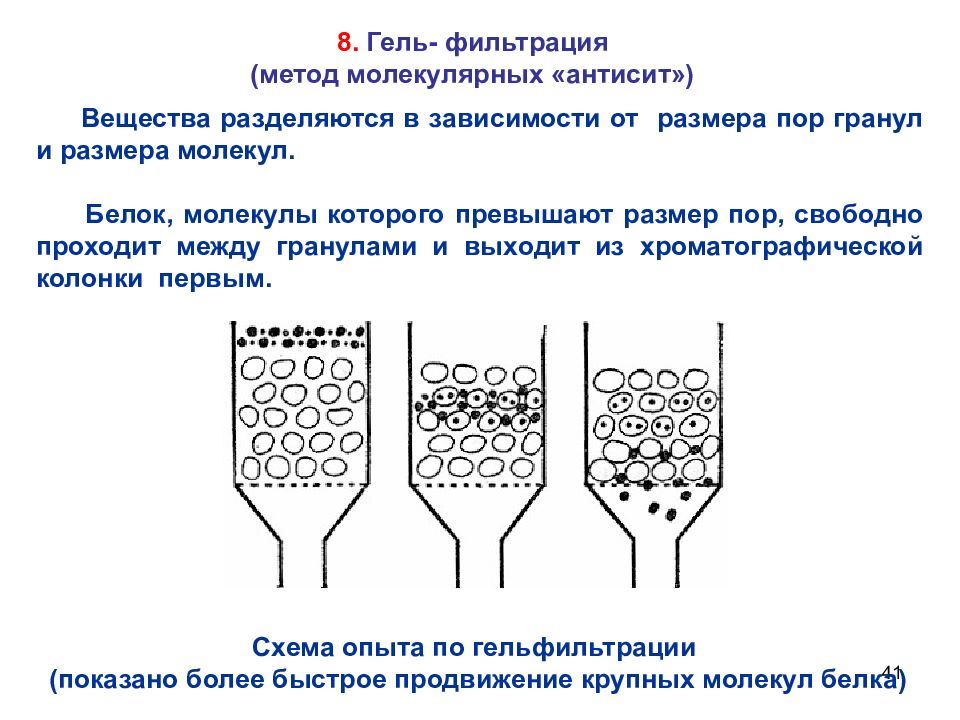
41 8. Гель- фильтрация (метод молекулярных «антисит») Вещества разделяются в зависимости от размера пор гранул и размера молекул. Белок, молекулы которого превышают размер пор, свободно проходит между гранулами и выходит из хроматографической колонки первым. Схема опыта по гельфильтрации (показано более быстрое продвижение крупных молекул белка)
Слайд 42
42 Свойства дисперсных систем Молекулярно-кинетические свойства а)Броуновское движение б) Диффузия в) Осмотическое давление г) Седиментация 2 Оптические свойства. 3. Электрокинетические свойства 4. Поверхностные явления.Адсорбция
Слайд 43
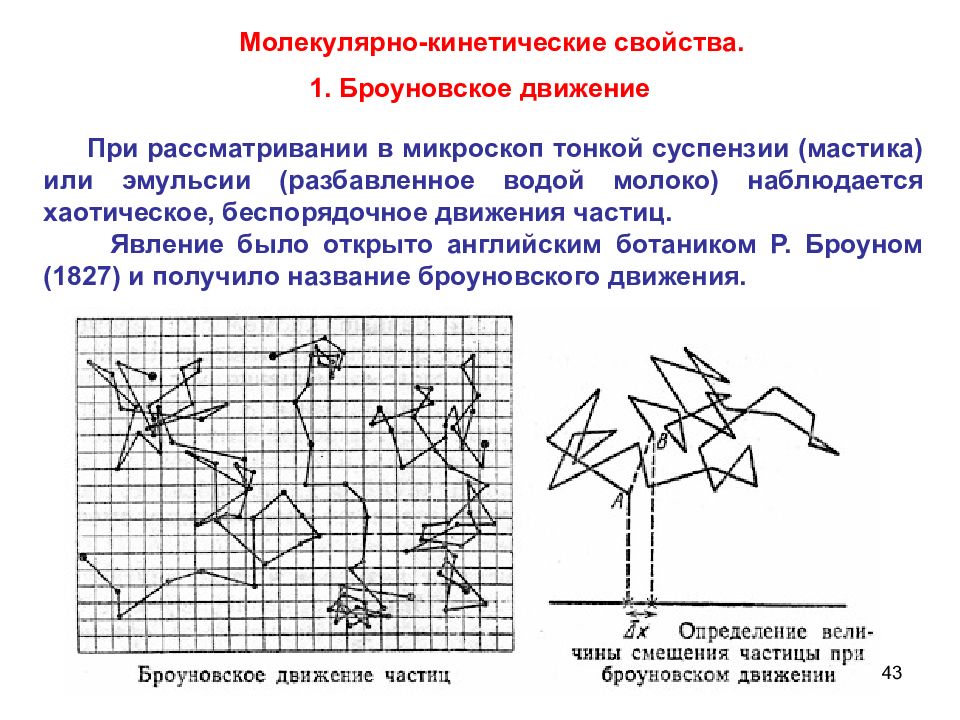
43 Молекулярно-кинетические свойства. 1. Броуновское движение При рассматривании в микроскоп тонкой суспензии (мастика) или эмульсии (разбавленное водой молоко) наблюдается хаотическое, беспорядочное движения частиц. Явление было открыто английским ботаником Р. Броуном (1827) и получило название броуновского движения.
Слайд 44
44 Броуновское движение в коллоидах отражает характер и законы теплового движения обычных молекул и описывается уравнением А.Эйнштейна - М.Смолуховского (1906): ─
Слайд 45
45 Мариан Смолуховский (1872-1917) Внес существенный вклад в кинетическую теорию материи, развив статистические идеи Больцмана. Предложил количественную теорию броуновского движения, объяснив его тепловым движением. Проводил теоретические исследования эмульсий и работал над теорией коагуляции. где D - коэффициент диффузии, м 2 /с. ─
Слайд 46
46 2. Диффузия – процесс направленного движения вещества из области б ó льших концентраций в область меньших.
Слайд 47
47 Формула Стокса-Эйнштейна Определение коэффициента диффузии ( D ) - один из основных методов определения размеров коллоидных частиц и величины макромолекул Закон Фика Масса диффундирующего вещества прямо пропорциональна коэффициенту диффузии, площади поперечного сечения, градиенту концентрации и времени. ─
Слайд 48
48 3. Седиментация Седиментация – процесс оседания частиц дисперсной фазы в жидкой или газообразной среде под действием силы тяжести Для сферических частиц скорость седиментации определяется уравнением Стокса : g= 9.8 (м / сек), d и ρ –плотность фазы и среды соответственно (кг / м 3 ) η –вязкость среды Закон Стокса Зная скорость седиментации V, можно вычислить радиус r дисперсной частицы. Седиментация в золях мала, ей препятствует броуновское движение, которое стремится распределить частицы равномерно по объёму.
Слайд 49
49 В результате устанавливается равновесие, которое называется седиментационным. Устойчивость дисперсных систем – это способность сохранять равномерное распределение частиц в объёме и их степень дисперности. В дисперсных системах существует два вида устойчивости 1. Седиментационная устойчивость – способность сохранять равномерное распределение частиц в объёме и не оседать под действием силы тяжести. 2. Агрегативная устойчивость – способность сохранять степень дисперсности. Золи седиментационно устойчивы Фактором устойчивости является броуновское движение Седиментация
Слайд 50
50 Исследование седиментационного равновесия проводят в ультрацентрифугах, которые позволяют превышать ускорение силы тяжести в сотни тысяч раз. 3. Седиментация В Нобелевской лекции (1927) Сведберг описал большое потенциальное значение, какое, по его мнению будет иметь ультрацентрифуга для прогресса во многих областях, включая медицину, физику, химию и промышленность. Теодор Сведберг 30.08.1884 -26.02.1971
Слайд 51
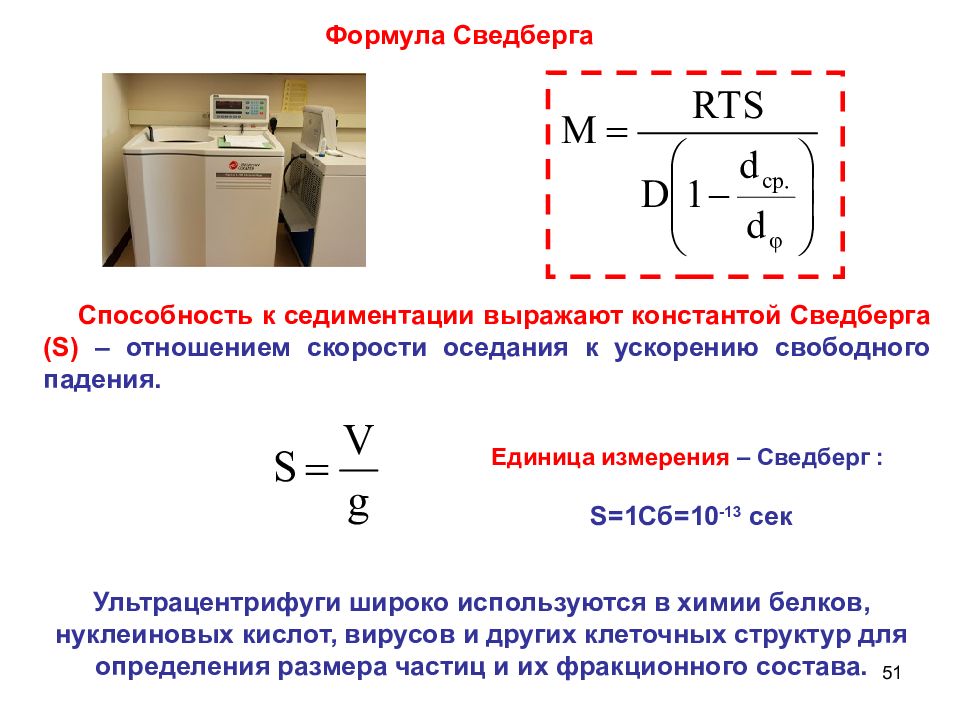
51 Формула Сведберга Ультрацентрифуги широко используются в химии белков, нуклеиновых кислот, вирусов и других клеточных структур для определения размера частиц и их фракционного состава. Способность к седиментации выражают константой Сведберга ( S ) – отношением скорости оседания к ускорению свободного падения. Единица измерения – Сведберг : S= 1Сб=10 -13 сек
Слайд 52
52 Разделение бактерий в ультрацентрифуге Современные центрифуги (Optima L-90K) способны вращать ротор с ускорением до 800000 g или скоростью до 100000 оборотов в минуту!!!
Слайд 53
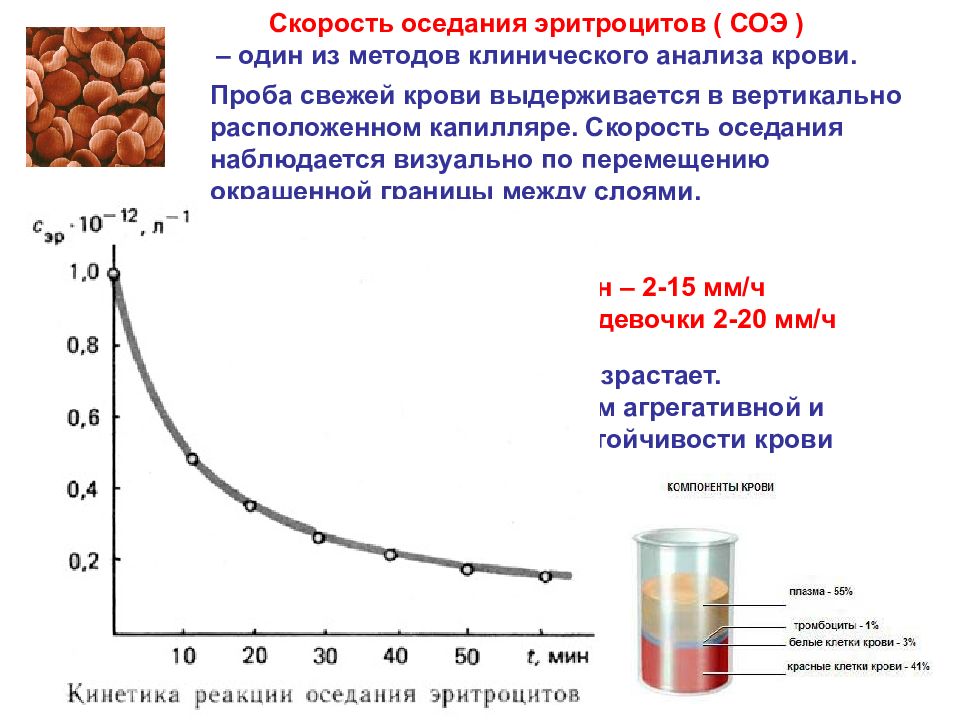
53 Проба свежей крови выдерживается в вертикально расположенном капилляре. Скорость оседания наблюдается визуально по перемещению окрашенной границы между слоями. В норме СОЭ составляет у мужчин 1-10 мм/ч, у женщин – 2-15 мм/ч у детей: мальчики 1-15 мм/ч, девочки 2-20 мм/ч Скорость оседания эритроцитов ( СОЭ ) – один из методов клинического анализа крови. При патологии СОЭ возрастает. в связи с уменьшением агрегативной и седиментационной устойчивости крови
Слайд 54
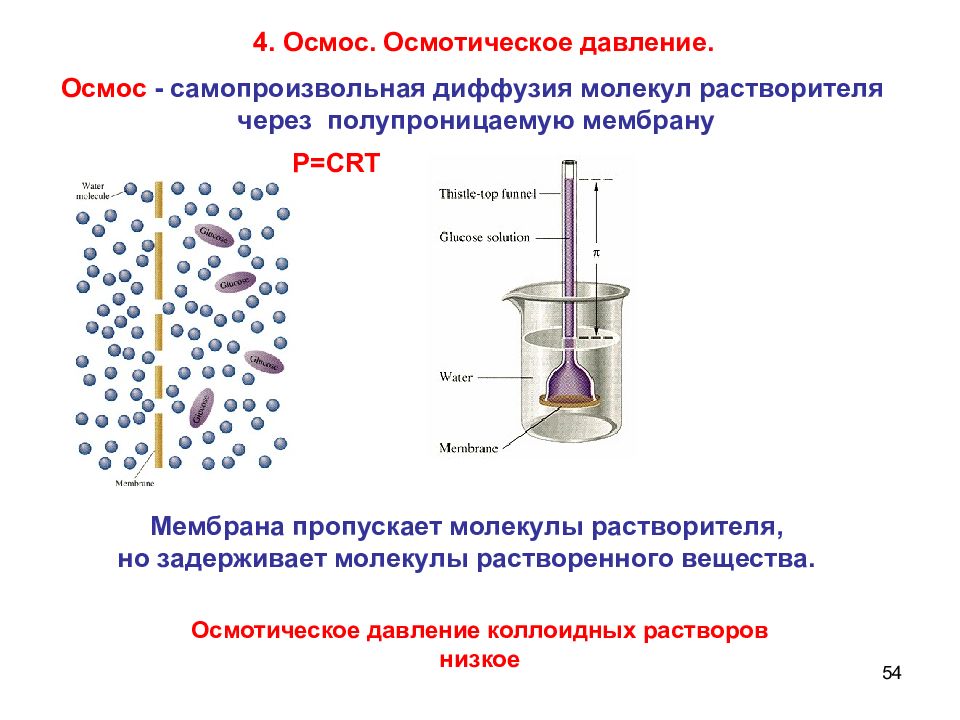
54 4. Осмос. Осмотическое давление. Осмос - самопроизвольная диффузия молекул растворителя через полупроницаемую мембрану Мембрана пропускает молекулы растворителя, но задерживает молекулы растворенного вещества. Р=С RT Осмотическое давление коллоидных растворов низкое
Слайд 56
56 Закон Рэлея Джон Уильям Стретт, третий барон Рэлей (12.11.1842 – 30.06.1919 ) Изучал световые и звуковые волны электромагнетизм, механику, капиллярность, термодинамику. Нобелевская премия (1904) «за исследования плотностей наиболее распространенных газов и за открытие аргона в ходе этих исследований».
Слайд 57
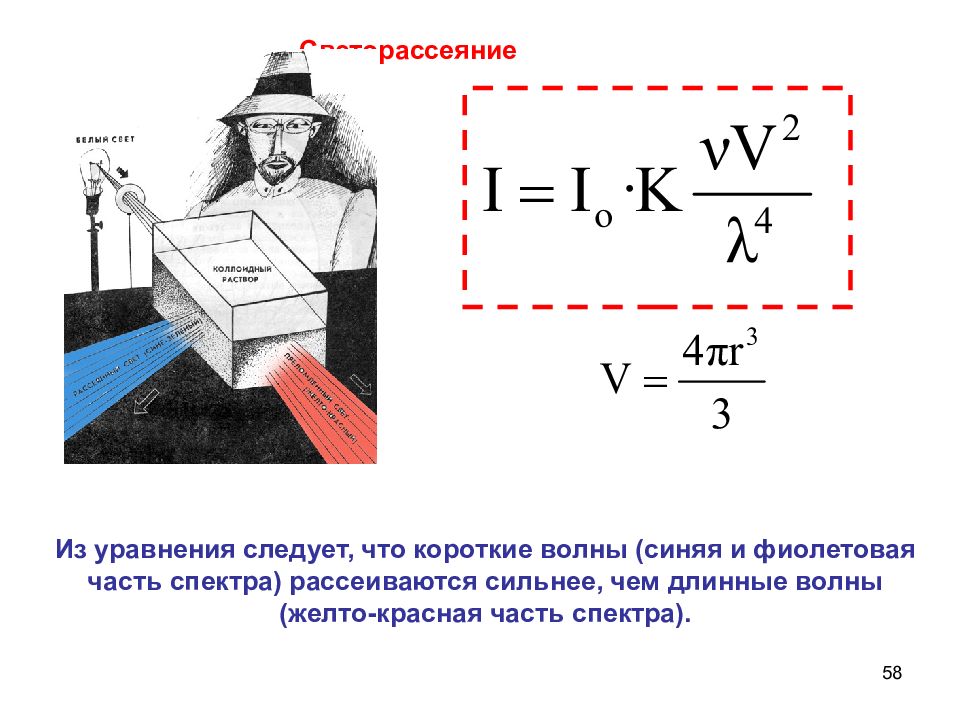
57 Закон Рэлея I и I 0 - интенсивности рассеянного и падающего света, v - число частиц в 1 м 3 золя V - объем отдельной частицы, К - константа, зависящая от коэффициентов преломления фазы и среды. Светорассеяние. ( r<0.1 λ )
Слайд 58
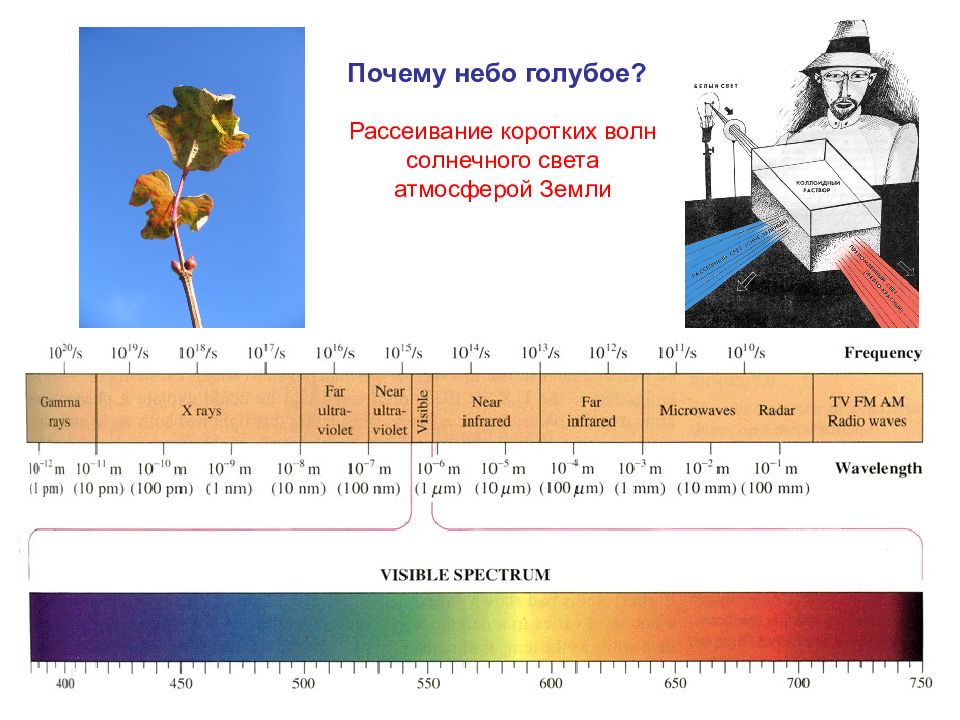
58 Из уравнения следует, что короткие волны (синяя и фиолетовая часть спектра) рассеиваются сильнее, чем длинные волны (желто-красная часть спектра). Светорассеяние
Слайд 59
59 Почему небо голубое? Рассеивание коротких волн солнечного света атмосферой Земли
Слайд 61
61 Почему мигающие устройства в скорых и милицейских автомобилях синего цвета, а запрещающий сигнал светофора – красный ?
Слайд 62
62 Опалесценция белого опала Опалесценция - явление рассеяния света мутной средой, обусловленное её оптической неоднородностью. Наблюдается матовое свечение (чаще всего голубоватых оттенков) при освещении большинства коллоидных растворов. Опалесценция коллоидных частиц хлорида серебра.
Слайд 63
63 Джон Тиндаль (1820 –1893) Исследовал явления магнетизма, рассеяние света в мутных растворах, строение и движение ледников в Альпах. Прославился как блестящий лектор, экспериментатор. Автор книги «Фарадей как исследователь». Джон Тиндаль родился в 1820 году к югу от Дублина, в графстве Карлоу. Затем он переехал в Англию, а потом — в Германию, которая в то время считалась лидером по части экспериментальных наук. Среди его учителей был великий химик Роберт Бунзен.
Слайд 64
64 В основе эффекта лежит рассеяние видимого света коллоидными частицами, которое связано с размерами коллоидных частиц и длиной волны падающего света. Конус Тиндаля
Слайд 65
65 Частицы, размеры которых соизмеримы с длиной полуволны r =1/2λ, а именно такими являются коллоидные частицы, рассеивают свет во все стороны: световые волны, наталкиваясь на подобные частицы, огибают их, и луч отклоняется от прямой линии (явление дифракции света). Аппарат Джона Тиндаля.
Слайд 66
66 Конус Тиндаля тем ярче, чем выше концентрация и больше размер частиц. Интенсивность светорассеяния резко увеличивается с уменьшением длины световой волны. Высокодисперсные системы рассеивают более короткие световые волны и поэтому имеют голубоватую окраску.
Слайд 67
67 Путем несложного эксперимента легко установить, является ли раствор коллоидным или истинным - молекулярным, ионным.
Слайд 68
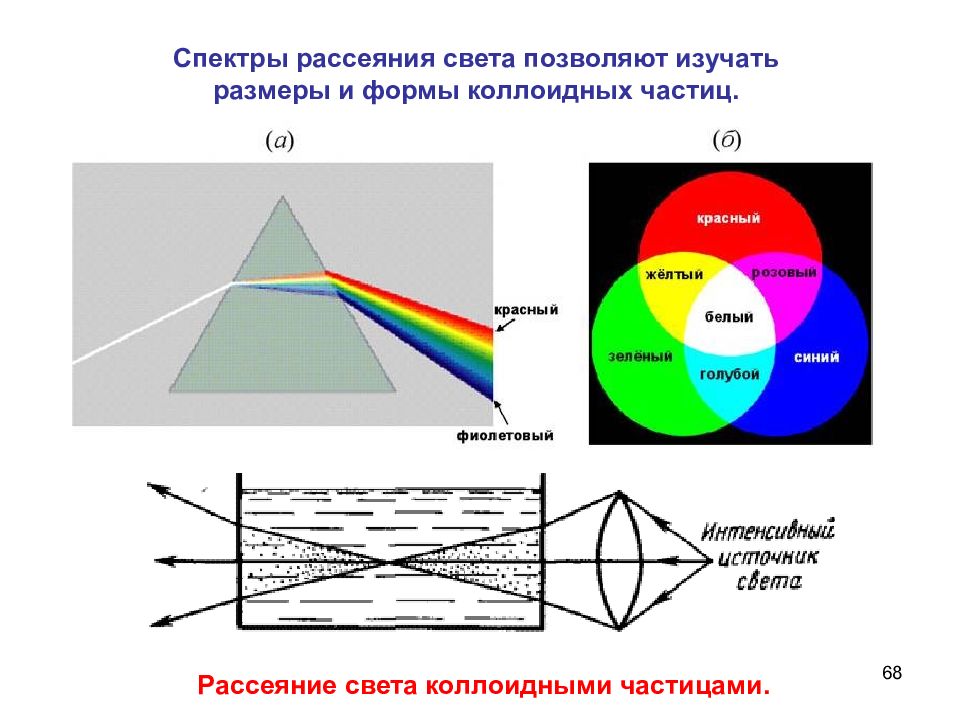
68 Спектры рассеяния света позволяют изучать размеры и формы коллоидных частиц. Рассеяние света коллоидными частицами.
Слайд 69
69 Джон Маклюр Гамильтон. Портрет Джона Тиндаля (дата создания неизвестна). Тиндаль первым продемонстрировал, что атмосферные газы по-разному поглощают тепло. Иными словами, он открыл молекулярные основы парникового эффекта.
Слайд 70
70 Научные круги признали заслуги Тиндаля. Британский Центр по исследованию климатических изменений носит его имя, в Ирландии есть Национальный институт им. Тиндаля. Британский Центр по исследованию климатических изменений Ученые из Национального института имени Тиндаля (Ирландия) объявили о создании транзистора, в котором применена «революционная» технология, которая позволит делать транзисторы размером в несколько атомов.
Слайд 72
72 А вот общественное мнение не принимает Тиндаля. По сей день обыватель не верит в то, что выбросы двуокиси углерода и других газов могут влиять на глобальную температуру, — ведь они так малы!..
Слайд 74
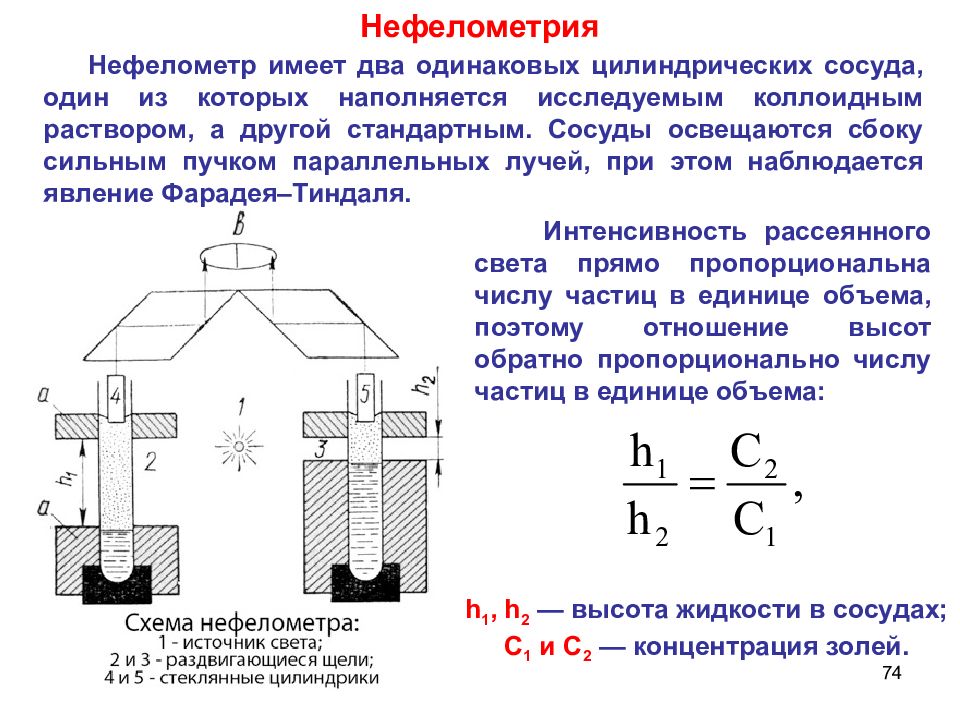
74 Нефелометрия Нефелометр имеет два одинаковых цилиндрических сосуда, один из которых наполняется исследуемым коллоидным раствором, а другой стандартным. Сосуды освещаются сбоку сильным пучком параллельных лучей, при этом наблюдается явление Фарадея–Тиндаля. h 1, h 2 — высота жидкости в сосудах; С 1 и С 2 — концентрация золей. Интенсивность рассеянного света прямо пропорциональна числу частиц в единице объема, поэтому отношение высот обратно пропорционально числу частиц в единице объема:
Слайд 75
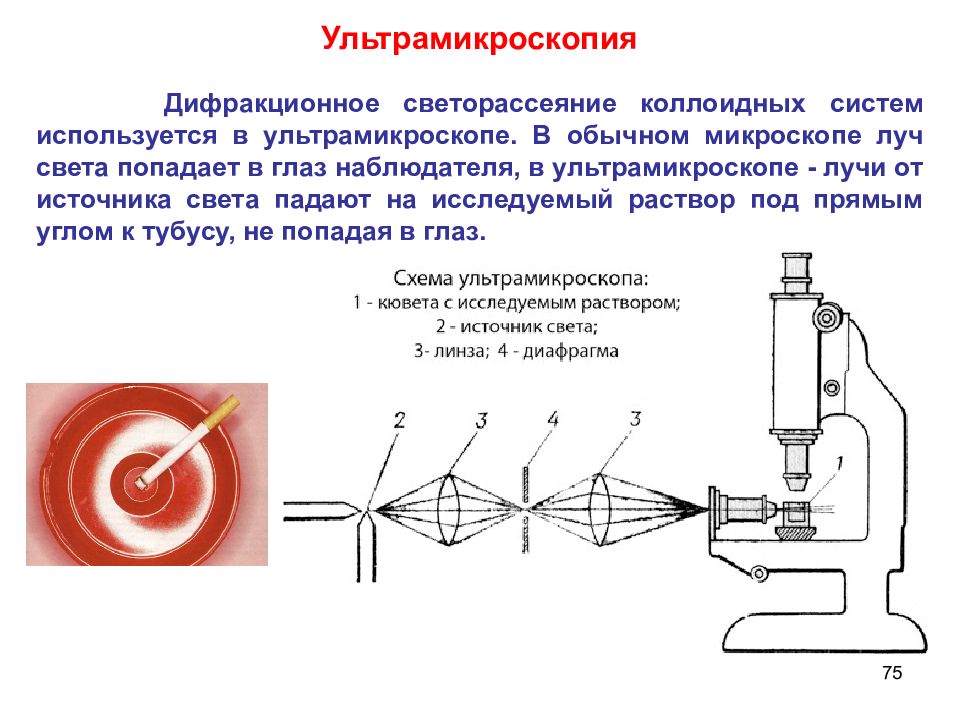
75 Ультрамикроскопия Дифракционное светорассеяние коллоидных систем используется в ультрамикроскопе. В обычном микроскопе луч света попадает в глаз наблюдателя, в ультрамикроскопе - лучи от источника света падают на исследуемый раствор под прямым углом к тубусу, не попадая в глаз.
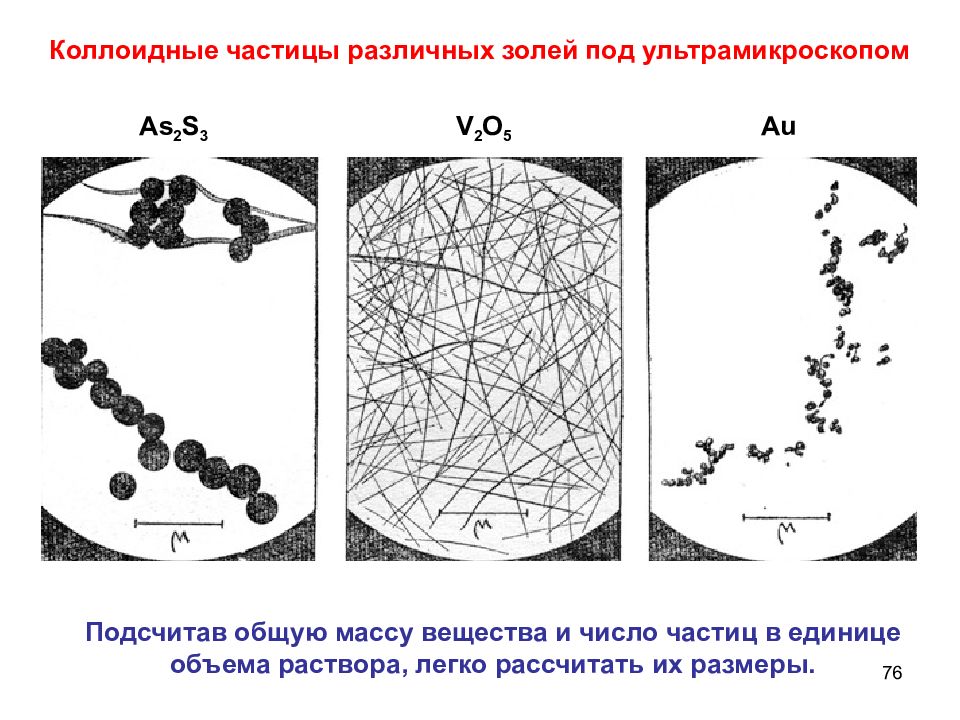
Слайд 76
76 Подсчитав общую массу вещества и число частиц в единице объема раствора, легко рассчитать их размеры. Коллоидные частицы различных золей под ультрамикроскопом As 2 S 3 V 2 O 5 Au
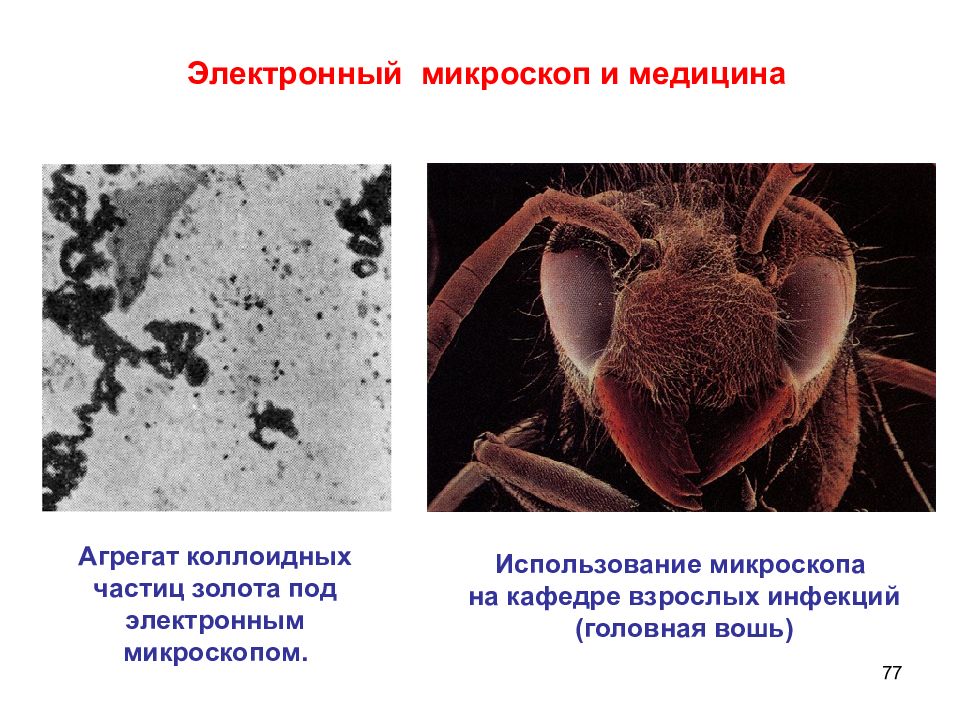
Слайд 77
77 Использование микроскопа на кафедре взрослых инфекций (головная вошь) Агрегат коллоидных частиц золота под электронным микроскопом. Электронный микроскоп и медицина
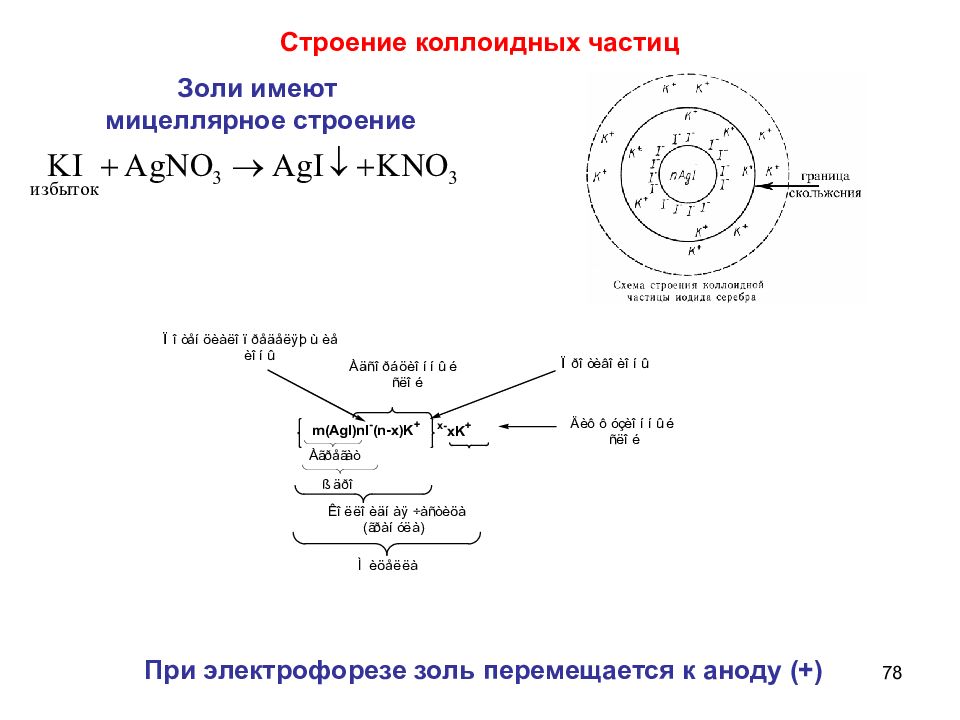
Слайд 78
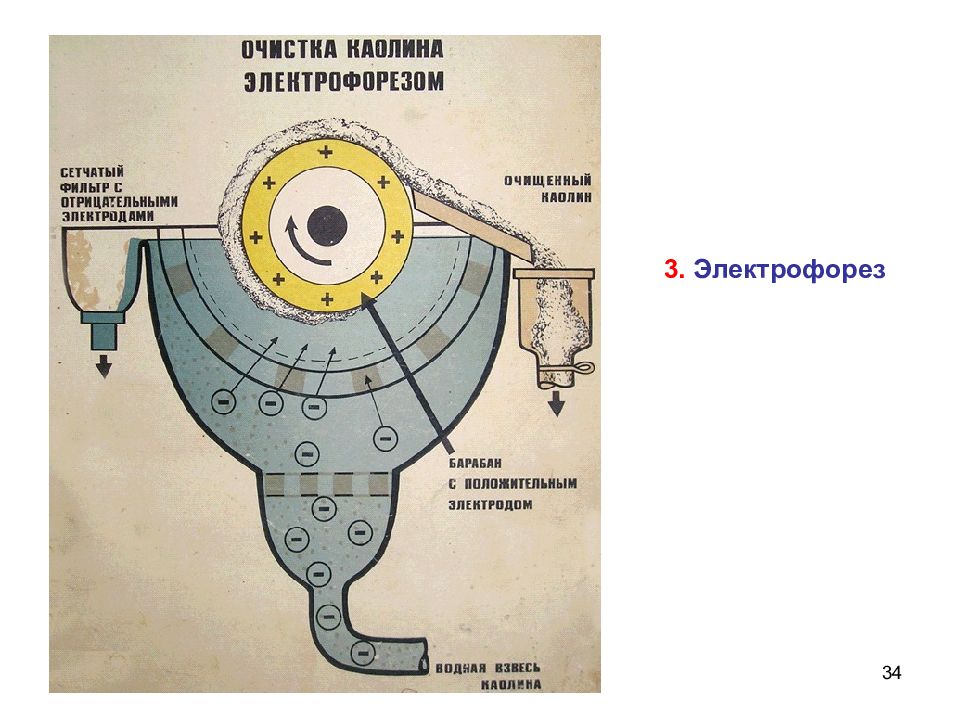
78 Строение коллоидных частиц Золи имеют мицеллярное строение При электрофорезе золь перемещается к аноду (+)
Слайд 84
84 Значение коллоидных растворов Не случайно Оствальд назвал коллоидные системы «миром обойденных величин» — в его время коллоидные растворы были мало изучены и плохо использовались человеком. В широком смысле слова коллоидами являются все живые и растительные организмы. Большую часть пищи мы принимаем в коллоидном состоянии.
Слайд 85
85 Коллоиды — это разнообразные строительные материалы, многие лекарства, краски. Штамповка печатной краской, которая представляет собой коллоидную систему.
Слайд 86
86 Использование коллоидов в промышленности: пищевой, текстильной, резиновой, кожевенной, лакокрасочной, керамической, строительных материалов (цемент, бетон, пенобетон, вяжущие растворы), угольной, торфяной, горнорудной и нефтяной (брикеты угольной и торфяной пыли, суспензии и пены на обогатительных фабриках, нефтяные эмульсии и промывочные растворы при бурении скважин). Обогащение полезных ископаемых (процессы дробления и измельчения, флотации )
Слайд 88
88 В технологии фотографических процессов, искусственного волокна, пластических масс, смазочных и горючих материалов При приготовлении дезинфицирующих растворов. При образовании дымовых завес, распылении химикатов токсичных дымов и туманов При очистке воздуха (построена на закономерностях, установленных при исследовании аэрозолей)
Слайд 89
89 При механической и термической обработке металлов и их сплавов. При очистке питьевой воды (основана на процессах адсорбции и взаимной коагуляции)
Слайд 92
92 Медико-биологическое значение 1. Коллоидные растворы способствуют усвоению пищи Хлеб, молоко, масло - коллоидные системы. Тонко раздробленный жир в молоке и сливочном масле усваивается организмом лучше, чем жир в сплошной массе, например, сало.
Слайд 93
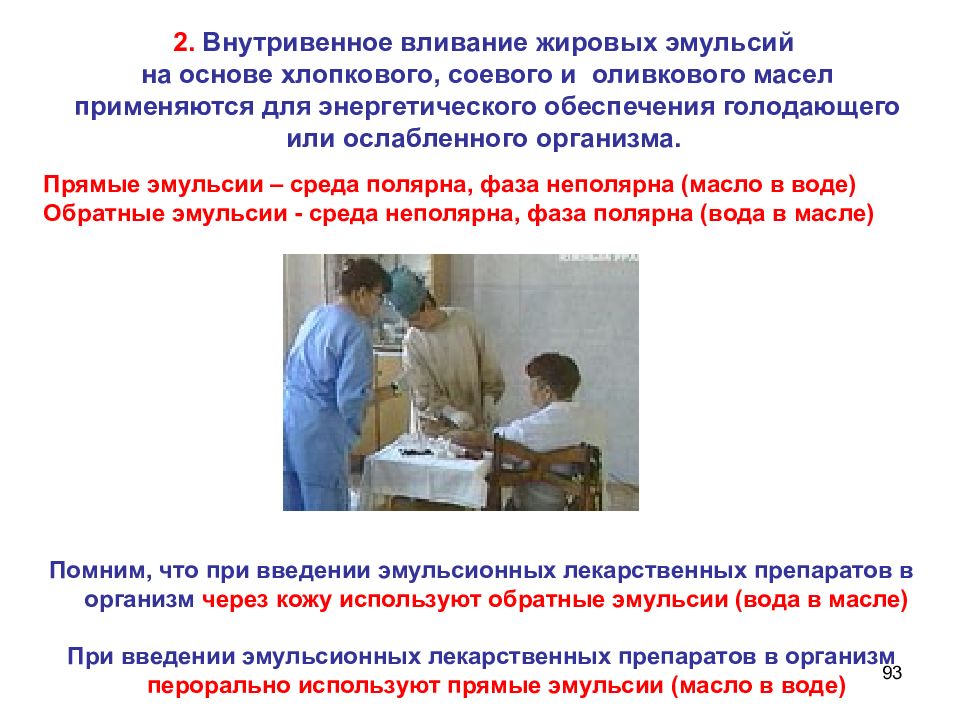
93 2. Внутривенное вливание жировых эмульсий на основе хлопкового, соевого и оливкового масел применяются для энергетического обеспечения голодающего или ослабленного организма. Помним, что при введении эмульсионных лекарственных препаратов в организм через кожу используют обратные эмульсии (вода в масле) При введении эмульсионных лекарственных препаратов в организм перорально используют прямые эмульсии (масло в воде) Прямые эмульсии – среда полярна, фаза неполярна (масло в воде) Обратные эмульсии - среда неполярна, фаза полярна (вода в масле)
Слайд 94
94 4. Использование лекарственных веществ в виде суспензий, эмульсий, мазей, кремов, паст. Сильно раздробленные вещества легче проникают через поры кожи, эффективнее действуют на организм 3. Применение антибиотиков в качестве аэрозолей при лечении инфекционных и аллергических заболеваний дыхательных путей и легких.
Слайд 95
95 5. Реконструкция поврежденных костей Пористый биокерамический стержень (гидроксиапатит) с введенными в него стволовыми клетками превращается в нормальную костную ткань
Слайд 96
96 "Человек – бродячий коллоид" 6. Биологические жидкости- кровь, плазма, лимфа, спинномозговая жидкость представляют собой коллоидные системы, в которых ряд веществ - белки, холестерин, гликоген и многие другие находятся в коллоидном состоянии.