Первый слайд презентации: Кафедра патологической физиологии с курсом клинической патофизиологии им. проф. В.В. Иванова
Тема: Воспаление. Этиопатогенез синдрома системного воспалительного ответа. Практическое занятие № 1 для студентов 4 курса по дисциплине «Клиническая патофизиология». Красноярск,201 7 д.м.н., проф. Зайцева О.И.
Слайд 2: Вопросы занятия
Воспаление: понятие, классификация, этиология Механизмы развития воспаления: альтерация расстройства микроциркуляции экссудация эмиграция фагоцитоз Пролиферация Клиническая оценка воспаления Синдром системного воспалительного ответа
Слайд 3: Тесты исходного уровня
1. К внутренним кардинальным признакам воспаления относится: 1) повышение температуры; 2) припухлость; 3) расстройство микроциркуляции; 4) лейкоцитоз. 2. Общие признаки воспаления: изменение иммунологичекой реактивности; нарушение функций органа; гипертермия; альтерация.
Слайд 4
3. К клеточным модуляторам воспаления в стадию альтерации относят: кинины; комплемент; тромбопластин; экойзаноиды. 4. Внутренней причиной воспаления является: лучевая энергия; вирус герпеса; гематома; отравление барбитуратами; термический ожог.
Слайд 5
5. Какое количество белка может содержать транссудат? больше 3%; от 3% до 8%; до 2%; до 5%; не должен содержать белок. 6. Основной клеточный элемент ответственный за репарацию в очаге воспаления: нейтрофил; макрофаг; фибробласт; эндотелиальные клетки.
Слайд 6
7. К симптомам острой фазы воспаления относят: 1) замедление СОЭ; 2) снижение АД; 3) лейкоцитоз; 4) анизоцитоз. . 8. Комменсализм – это… один из видов инфекционного процесса; свойство возбудителя; способность микроорганизма выделять эндотоксин; форма симбиоза макро- и микроорганизма.
Слайд 7
9. Макрофагами являются: тучные клетки; базофилы; нейтрофилы; моноциты; лимфоциты. 10. Клиническая триада, сопровождающая начало развития SIRS : тахикардия, тахипноэ, гипертония; тахикардия, тахипноэ, гипертермия; брадикардия, гипотония, гипотермия. гипертония, судорожный синдром, аритмия.
Слайд 8: ВОСПАЛЕНИЕ
ТПП, направленный на уничтожение, инактивацию или ликвидацию повреждающего агента и восстановление поврежденной ткани Воспалительный агент- флогоген ПРИЧИНЫ ВОСПАЛЕНИЯ: Физические факторы (ультрафиолетовое излучение, ионизирующая радиация, термические воздействия) Химические факторы (кислоты, щелочи, соли) Биологические агенты (вирусы, грибы, опухолевые клетки, токсины насекомых)
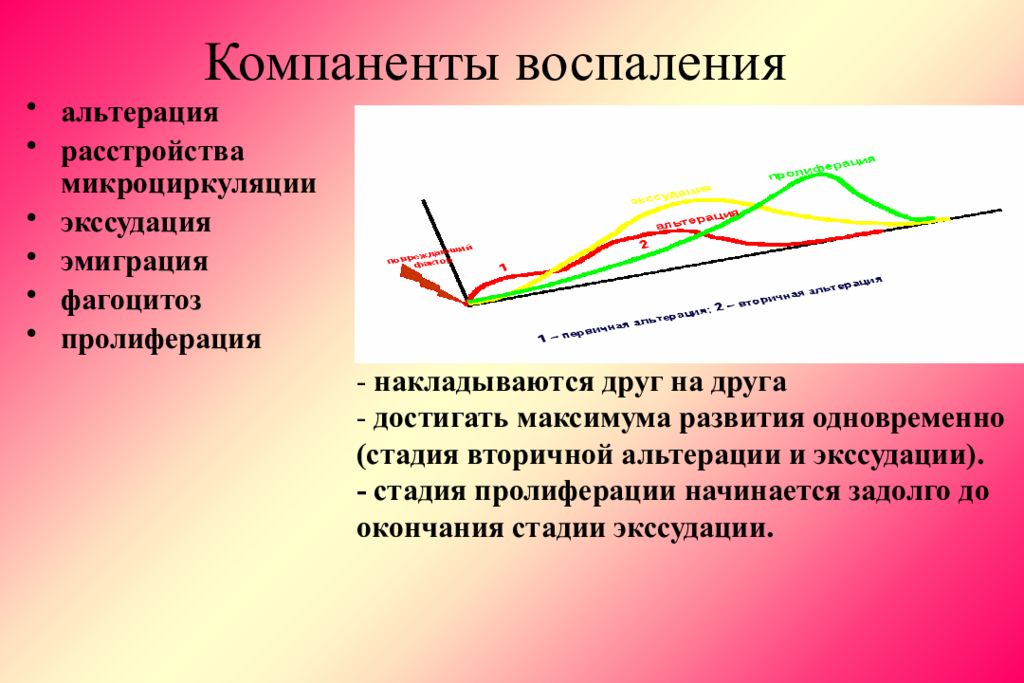
Слайд 9: Компаненты воспаления
альтерация расстройства микроциркуляции экссудация эмиграция фагоцитоз пролиферация - накладываются друг на друга - достигать максимума развития одновременно (стадия вторичной альтерации и экссудации). - стадия пролиферации начинается задолго до окончания стадии экссудации.
Слайд 10: АЛЬТЕРАЦИЯ- повреждение ткани:
нарушение трофики, обмена веществ, структуры, функции. Первичная альтерация – результат повреждающего воздействия самого воспалительного агента Вторичная альтерация – вызывается продуктами первичной альтерации (высвободившиеся во внеклеточное пространство лизосомальные ферменты и активные метаболиты кислорода).
Слайд 11: Изменения обмена веществ в стадию альтерации
Преобладают реакции катаболизма: Углеводный обмен ↑гликогенолиз, ↑гликолиз, ↑ выработки АТФ Разобщители ДЦ → выделение АТФ в виде тепла ↑анаэробный гликолиз - ↑лактата, пирувата→ метаболический ацидоз
Слайд 12: Изменения обмена веществ в стадию альтерации
Липидный обмен: ↑ липолиз → ↑ВЖК, ↑ СПОЛ ↑ кетокислот → метаболический ацидоз, вторичная альтерация Арахидоновая кислота → ↑ ПГ, тромбоксаны, ЛТ
Слайд 13: Изменения обмена веществ в стадию альтерации
Белковый и водно-минеральный обмены: ↑ протеолиз Активация иммунных реакций Нарушение селективного (избирательного) переноса ионов Нарушение вне- и внутриклеточного соотношения между ионами (Са ++, Na +, K +, Mg ++ ) ↑P осм
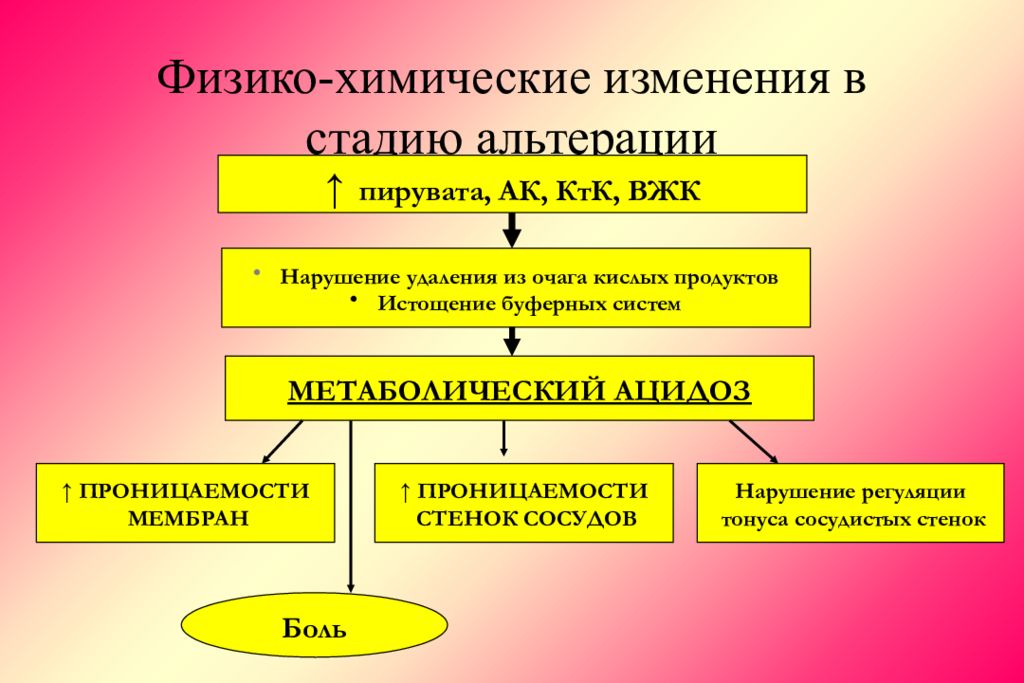
Слайд 14: Физико-химические изменения в стадию альтерации
↑ пирувата, АК, КтК, ВЖК Нарушение удаления из очага кислых продуктов Истощение буферных систем МЕТАБОЛИЧЕСКИЙ АЦИДОЗ ↑ ПРОНИЦАЕМОСТИ МЕМБРАН ↑ ПРОНИЦАЕМОСТИ СТЕНОК СОСУДОВ Боль Нарушение регуляции тонуса сосудистых стенок
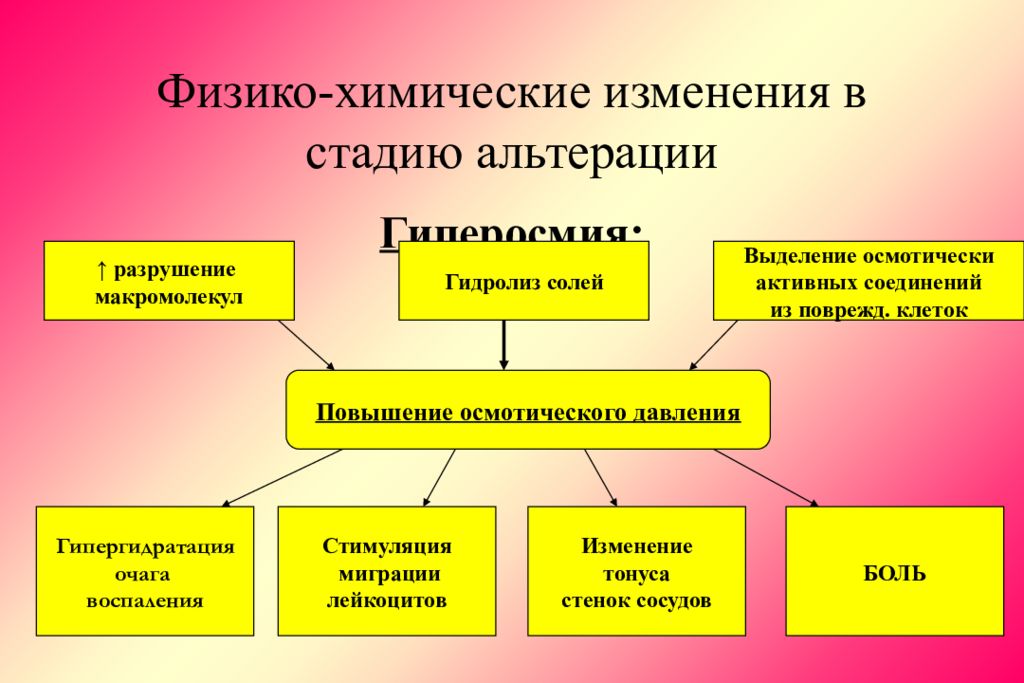
Слайд 15: Физико-химические изменения в стадию альтерации
Гиперосмия: ↑ разрушение макромолекул Гидролиз солей Выделение осмотически активных соединений из поврежд. клеток Повышение осмотического давления Гипергидратация очага воспаления Стимуляция миграции лейкоцитов Изменение тонуса стенок сосудов БОЛЬ
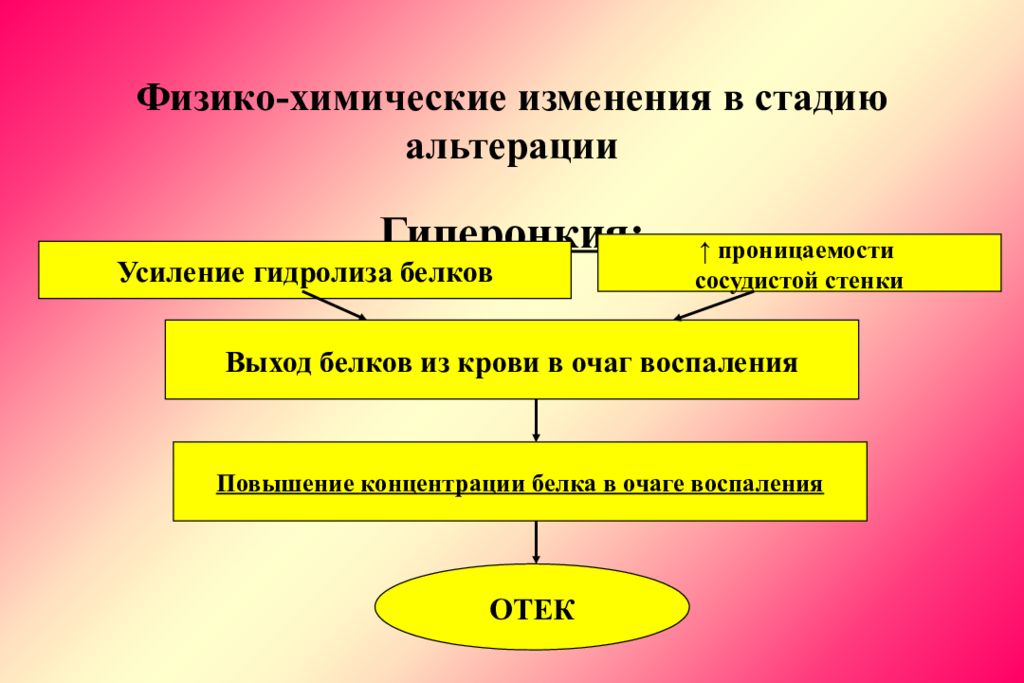
Слайд 16: Физико-химические изменения в стадию альтерации
Гиперонкия: Усиление гидролиза белков Выход белков из крови в очаг воспаления ↑ проницаемости сосудистой стенки Повышение концентрации белка в очаге воспаления ОТЕК
Слайд 17: Медиаторы воспаления
Биологически активные вещества, ответственные за возникновение или поддержание воспалительных явлений Флогогенный раздражитель ПОВРЕЖДАЮЩИЙ ЭФФЕКТ СИНТЕЗ, ВЫДЕЛЕНИЕ, АКТИВАЦИЯ МЕДИАТОРОВ ВОСПАЛЕНИЯ Плазменные Клеточные
Слайд 18: Источники медиаторов
Полиморфноядерные лейкоциты Тучные клетки Тромбоциты Ретикулоциты Клетки паренхиматозных органов, подвергшихся повреждению
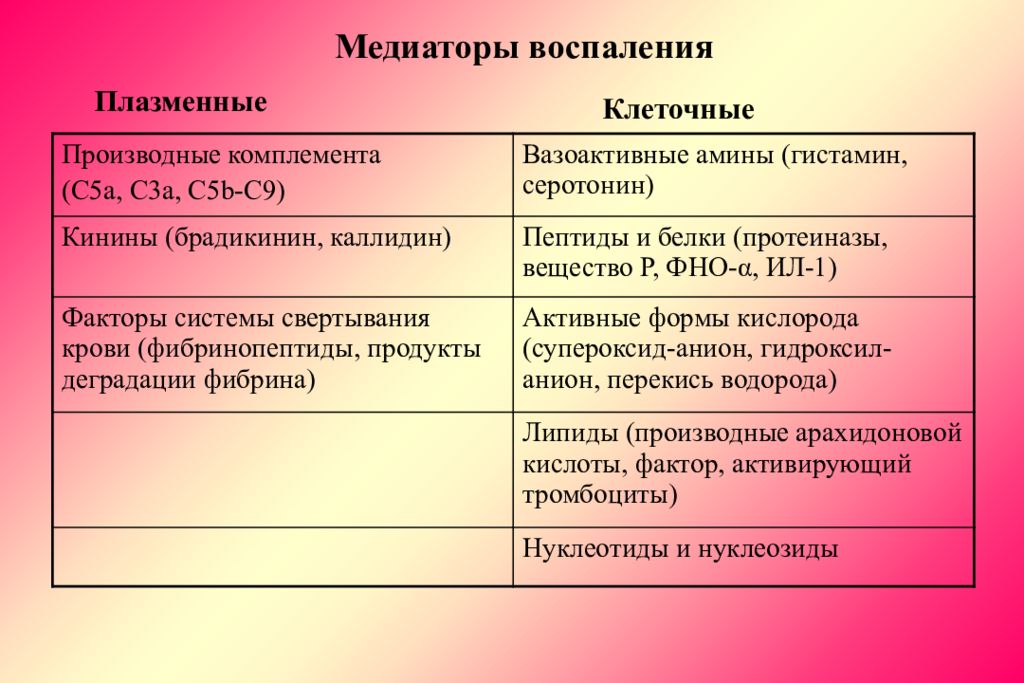
Слайд 19: Медиаторы воспаления
Плазменные Клеточные Производные комплемента (С5а, С3а, С5 b-C9) Вазоактивные амины (гистамин, серотонин) Кинины (брадикинин, каллидин) Пептиды и белки (протеиназы, вещество Р, ФНО- α, ИЛ-1) Факторы системы свертывания крови (фибринопептиды, продукты деградации фибрина) Активные формы кислорода (супероксид-анион, гидроксил-анион, перекись водорода) Липиды (производные арахидоновой кислоты, фактор, активирующий тромбоциты) Нуклеотиды и нуклеозиды
Слайд 20: Эффекты медиаторов
Местные Дистантные Вазомоторные реакции ↑ проницаемости мембраны Опсонизирующее действие Хемоаттрактивное действие Ноцицептивное действие Митогенное действие Антитоксическое действие Лейкопоэтическое действие Иммуномодулирующее действие Пирогенное действие Влияние на систему гемостаза
Слайд 21: Системы кининов
Кинины - пептидные факторы, образующиеся в результате активация сывороточных и тканевых факторов, осуществляемая по каскадному механизму. Эффекты кининов: 1. расширяют артериолы и венулы в очаге воспаления, 2. повышают проницаемость сосудов, 3.усиливают экссудацию, 4. стимулируют образование эйкозаноидов, 5. вызывают ощущение боли.
Слайд 22: Система комплемента
1. Индукция воспаления 2. Активация хемотаксиса фагоцитов в очаг воспаления 3. Опсонизация – обеспечение прикрепления антигенов к фагоцитам 4. Лизис грамотрицательных бактерий и клеток человека, имеющих чужеродные эпитопы 5. Удаление вредных иммунных комплексов из организма группа сывороточных белков, последовательно активирующих друг друга по каскадному принципу. Функции активированной системы комплемента:
Слайд 23: Эйкозаноиды
производные арахидоновой кислоты, которая входит в состав клеточных мембран и отщепляется от липидных молекул под влиянием фермента фосфолипазы А2. Эффекты: сосудистая реакция эмиграции лейкоцитов в очаг воспаления.
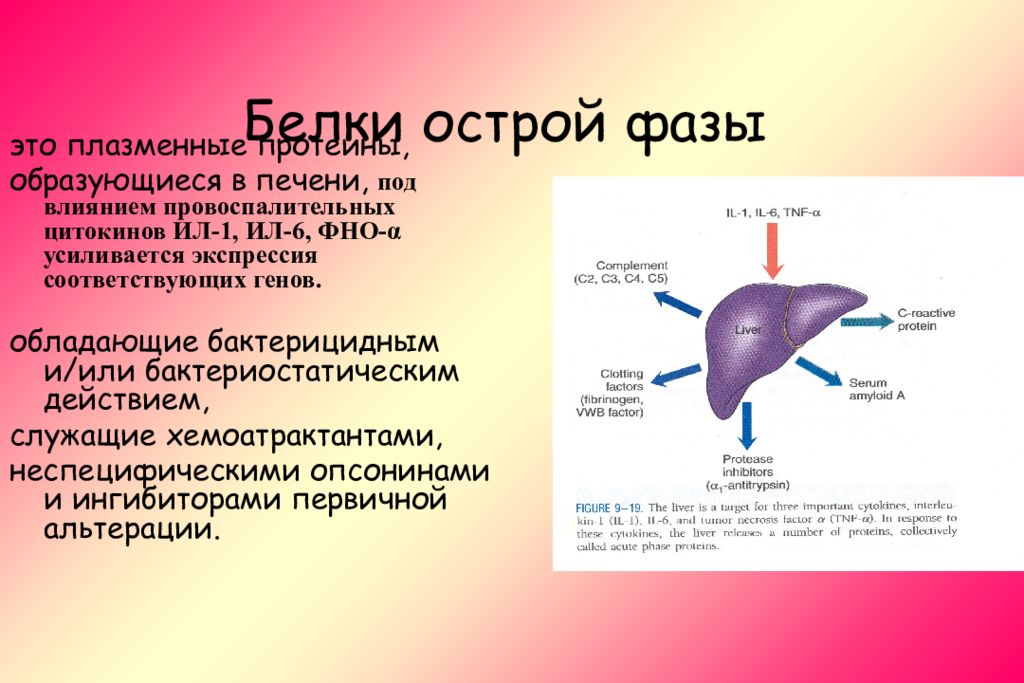
Слайд 24: Белки острой фазы
это плазменные протеины, образующиеся в печени, под влиянием провоспалительных цитокинов ИЛ-1, ИЛ-6, ФНО-α усиливается экспрессия соответствующих генов. обладающие бактерицидным и/или бактериостатическим действием, служащие хемоатрактантами, неспецифическими опсонинами и ингибиторами первичной альтерации.
Слайд 25: С-реактивный белок
Функции СРБ: Элиминация патогенных микроорганизмов, старых и погибших клеток Нейтрализация бактериальных токсинов Опсонизация и разрушение иммунных комплексов Блокада аутоиммунных реакций Повышение СРБ: Хр. воспалительные процессы, инфекционные заболевания Курение Ожирение Сахарный диабет Повышение уровня триглицеридов, холестерина
Слайд 26: СРБ - специфичный и чувствительный клинико-лабораторный индикатор воспаления
при воспалении концентрация СРБ в плазме крови увеличивается - в 10 –100 раз и есть прямая связь между изменением уровня СРБ и тяжестью и динамикой клинических проявлений воспаления. Выше концентрация СРБ - выше тяжесть воспалительного процесса, и наоборот. Измерение концентрации СРБ широко применяется для мониторинга и контроля эффективности терапии воспалительных заболеваний. Разные причины воспалительных процессов по-разному повышают уровни СРБ.
Слайд 27: Цитокины
низкомолекулярные белки (полипептиды или гликополипептиды с молекулярным весом 5-30 кДа), лишенные антигенной специфичности. Эффекты: посредники межклеточных взаимоотношений при воспалении, в формировании иммунного ответа организма, гемопоэзе
Слайд 28: Общие признаки цитокинов
функциональная взаимозаменяемость. способность к синергuзму uлu к антагонизму. цитокины могут индуцировать синтез других цитокинов, активируя для этого соответствующие клетки иммунной системы. короткий период действия.
Слайд 29: Классификация цитокинов
Интерлейкuны (IL): описано 18 видов (от IL-1 до IL-18). Колонuестuмулuрующuе факторы (CSFs): являются факторами роста гемопоэза (лимфопоэза, монопоэза, гранулопоэза). Интерфероны (IFNs): активируют естественные клетки-киллеры, ингибируют репродукцию вирусов и участвуют в генерации других цитокинов, активируя соответствующие клетки иммунной системы. Факторы некроза опухолей (TNFs): способны противостоять инфекционному началу и обладание противоопухолевой активностью. Хемокuны: стимуляция хемотаксиса всех клеток иммунной системы.
Слайд 30: Цитокины и воспаление
Две группы цитокинов: 1 группа обладает провоспалuтельным действuем, 2 группа - протuвовоспалuтельным. Провоспалuтельным действuем обладают : интерлейкины 1, 6, 8, 12, 17, 18, гамма-интерферон, факторы некроза опухолей альфа и бета, фактор гемопоэза GM-CSF. Протuвовоспалuтельным действuем обладают: инги6итор интерлейкина 1 - IL-1ra, интерлейкин 10, трансформирующий фактор роста - бета (TGFb), интерфероны альфа, бета и дельта.
Слайд 31: Провоспалительные цитокины
белки, секретируемые макрофагами и др. клетками (эндотелиальные клетки, нейтрофилы, дендритные клетки, В-лимфоциты, клетки глии, фибробласты) в ответ на их активацию микроорганизмами, их продуктами, а также собственно цитокинами. Основная роль – активировать клетки иммунной системы: способствовать их дифференцировке, стимулировать выработку иммуноглобулинов, обеспечивать адгезию и хемотаксис фагоцитов воспаления. Чрезмерная активность провоспалительных цитокинов приводит к деструкции тканей, росту альтерации. Неблагоприятна роль провоспалительных цитокинов и при развитии хронического воспаления. Расширение (генерализация) воспалительного процесса приводит к расширению и функций цитокинов. Воздействие на центральную нервную систему приводит к повышению температуры тела (лихорадке): (интерлейкины 1 и 6, фактор некроза опухолей альфа, гамма-интерферон) являются эндогенными пирогенами.
Слайд 32: Провоспалительные цитокины
Синтезируется практически всеми клетками Интерлейкин-1 (ИЛ-1) – собирательное обозначение семейства белков, включающего более 10 цитокинов. Системные эффекты ИЛ-1: стимулирует выработку гепатоцитами белков острой фазы, обуславливает развитие лихорадки при действии на центр терморегуляции гипоталамуса, стимулирует выброс из костного мозга лейкоцитов, в том числе не достигших зрелости, что является причиной появления при воспалении лейкоцитоза и сдвига лейкоцитарной формулы влево!
Слайд 33
Фактор некроза опухолей- α : Стимулирует катаболические процессы; Активирует клетки эндотелия и все виды лейкоцитов Способствует выработке печенью белков острой фазы ИЛ-6: Является индуктором белков острой фазы ИЛ-8: Обеспечивает краевое стояние лейкоцитов, хемотаксис Интерфероны (α, β, γ): Потенцируют ответ острой фазы Препятствуют репликации и сборке вирусов Провоспалительные цитокины
Слайд 34: Противовоспалительные цитокины
Эффекты: прекращение воспалительной реакции после подавления возбудителей заболевания и дезактивация активированных клеток. IL-10 (продуцируется моноцитами/макрофагами, В-клетками); основное действие – замедление воспаления, TGF-бета (транформирующийся фактор роста; продуцируется моноцитами, Т-клетками; основное действие – подавление воспаления).
Слайд 35: Расстройства кровообращения и микроциркуляции (фаза альтерации)
Активация вазодилататоров, метаболический ацидоз и гиперкалиемия артериальной гиперемии. Дестабилизация лизосом, высвобождение лизосомальных ферментов приводит к разрушению адвентиции микроциркуляторного русла и развитию диффузной «капиллярной» гиперемии. сдавление венозных и лимфатических сосудов экссудатом вызывают венозную гиперемии с развитием престаза и стаза.
Слайд 36: Экссудация
– процесс выхода плазмы и форменных элементов крови из сосудов микроциркуляторного русла в ткани. Экссудат - жидкость, образующаяся при воспалении и содержащая большое количество белка и форменные элементы крови. Механизм экссудации : 1. Повышение проницаемости сосудов в результате воздействия медиаторов воспаления, а в ряде случае самого воспалительного агента. 2. Увеличение кровяного (фильтрационного) давления в сосудах очага воспаления в результате гиперемии 3. Возрастание осмотического и онкотического давления в воспаленной ткани в результате альтерации и начавшейся экссудации.
Слайд 37
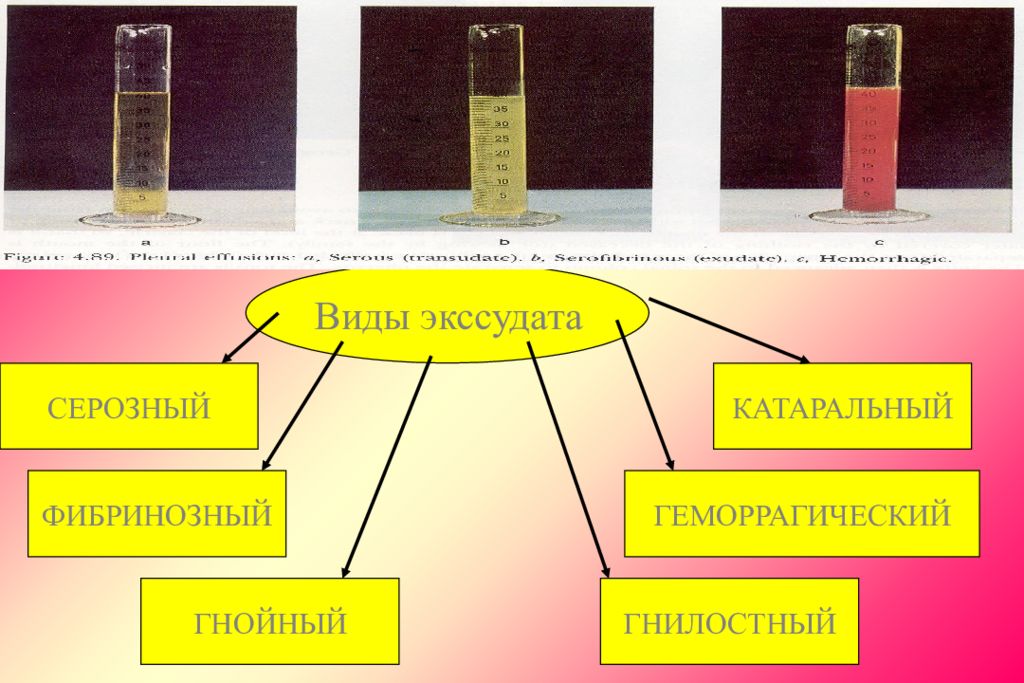
Виды экссудата СЕРОЗНЫЙ ФИБРИНОЗНЫЙ ГНОЙНЫЙ ГНИЛОСТНЫЙ ГЕМОРРАГИЧЕСКИЙ КАТАРАЛЬНЫЙ
Слайд 38: Виды экссудата
Серозный экссудат - белка мало (3-5 %), на ранних этапах воспаления, при асептическом воспалении серозных полостей, кроме воды содержит, альбумин (лучевой ожог). Катаральный экссудат, при воспалении слизистых оболочек, содержит: альбумин, мукополисахариды, секреторные IgA -антитела, лизоцим (астматический бронхит у детей). фибринозный отличается высоким содержанием фибриногена (при высокой проницаемости сосудов). Если пленка фибрина на слизистых расположена рыхло, легко отделяется, воспаление называется крупозным. Если плотно спаяна, не отделяется — это дифтеритическое воспаление; гнойный — содержит много лейкоцитов, обычно погибших и разрушенных, ферментов, продуктов аутолиза тканей (зеленоватый, мутный); гнилостный — наличие продуктов гнилостного разложения тканей (дурной запах); геморрагический — большое содержание эритроцитов (розовый). Геморрагический характер может принять любой вид воспаления (серозный, фибринозный, гнойный). смешанные
Слайд 39: Эмиграция лейкоцитов в очаг воспаления
выход из кровяного русла и миграция в очаг воспаления, что является ключевым событием патогенеза воспаления. Условия эмиграции лейкоцитов: Изменения адгезивных свойств эндотелия сосудов и лейкоцитов Повышение проницаемости мелких сосудов Активация хемотаксиса в направлении очага воспаления
Слайд 40: ФАГОЦИТОЗ
- Кислородзависимый механизм ( респираторный взрыв) - Кислороднезависимый механизм ( действие лизосомальных ферментов) Выделение ими секретов (БАВ) во внеклеточную среду Фагоцитоз – активный биологический процесс, заключающийся в распознавании, поглощении внутриклеточной деструкции чужеродного материала фагоцитами ПЯЛ и макрофагами :
Слайд 41
Продвижение псевдоподий фагоцита в сторону бактерии Макрофаг во время захвата бактерий – начальная стадия фагоцитоза
Слайд 42: Причины недостаточности фагоцитоза
Уменьшение количества фагоцитов Неэффективный гранулоцитопоэз (качественные изменения нейтрофилов) - нарушение подвижности фагоцитов - нарушения образования фаголизосом - нарушение инактивации и разрушения объектов фагоцитоза Нарушение распознавания объектов фагоцитоза Нарушения нейрогормональной регуляции фагоцитоза
Слайд 43: Стадия пролиферации
Увеличение числа стромальных и паренхиматозных клеток, образование межклеточного вещества в очаге воспаления
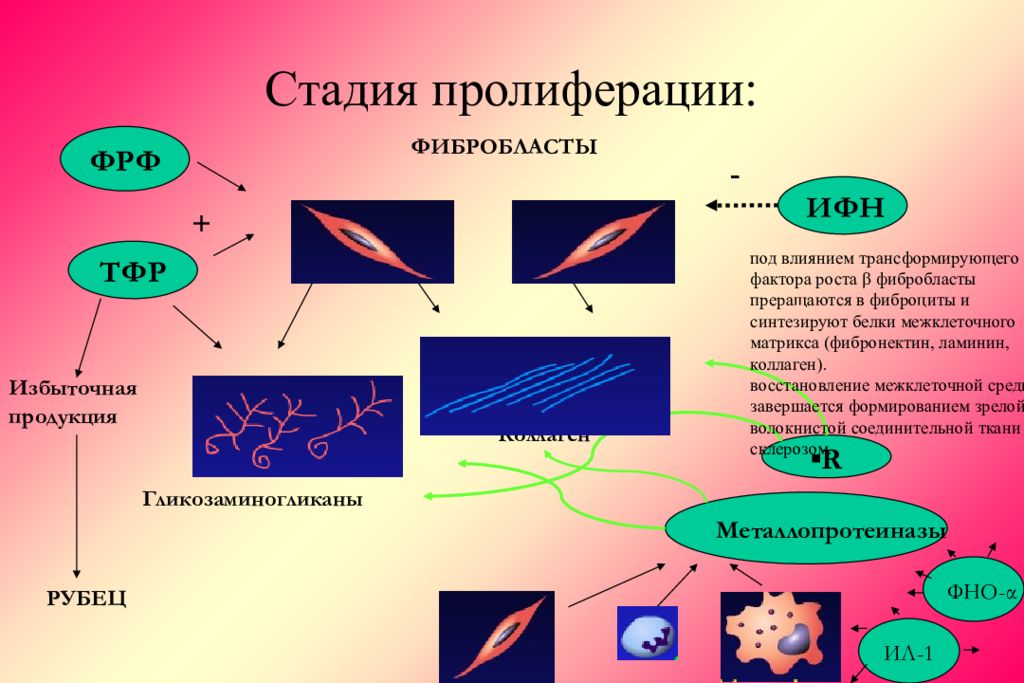
Слайд 44: Стадия пролиферации:
Коллаген ФИБРОБЛАСТЫ ТФР ФРФ ИФН - + Гликозаминогликаны Избыточная продукция РУБЕЦ Металлопротеиназы ▪ R ФНО- α ИЛ-1 под влиянием трансформирующего фактора роста β фибробласты преращаются в фиброциты и синтезируют белки межклеточного матрикса (фибронектин, ламинин, коллаген). восстановление межклеточной среды завершается формированием зрелой волокнистой соединительной ткани и склерозом.
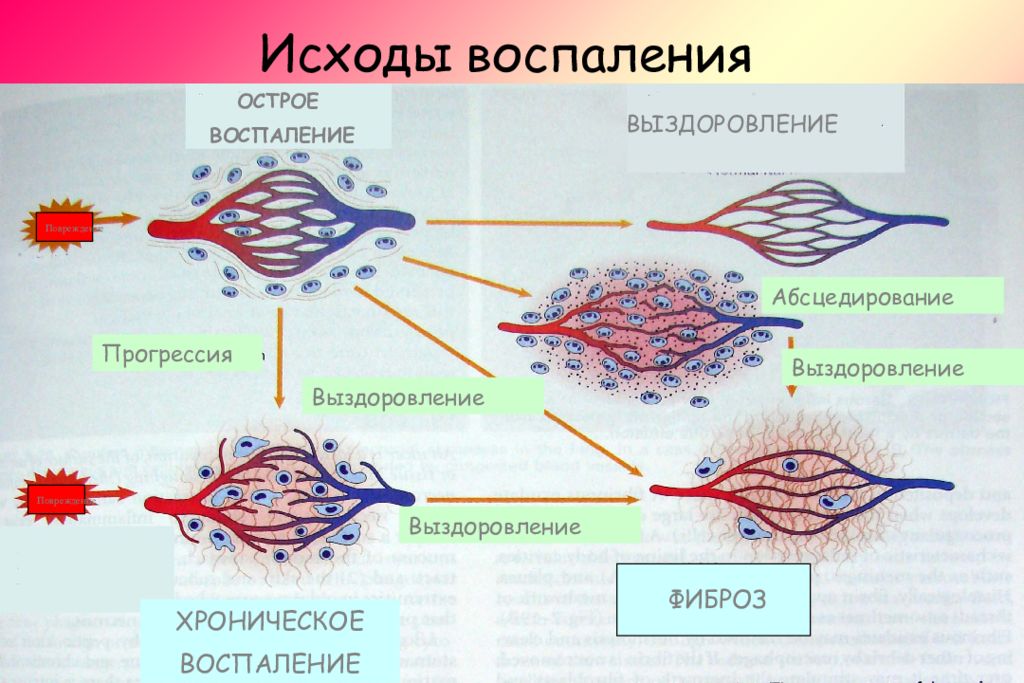
Слайд 45: Исходы воспаления
ОСТРОЕ ВОСПАЛЕНИЕ ВЫЗДОРОВЛЕНИЕ Прогрессия ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ ФИБРОЗ Выздоровление Выздоровление Выздоровление Абсцедирование Повреждение Повреждение
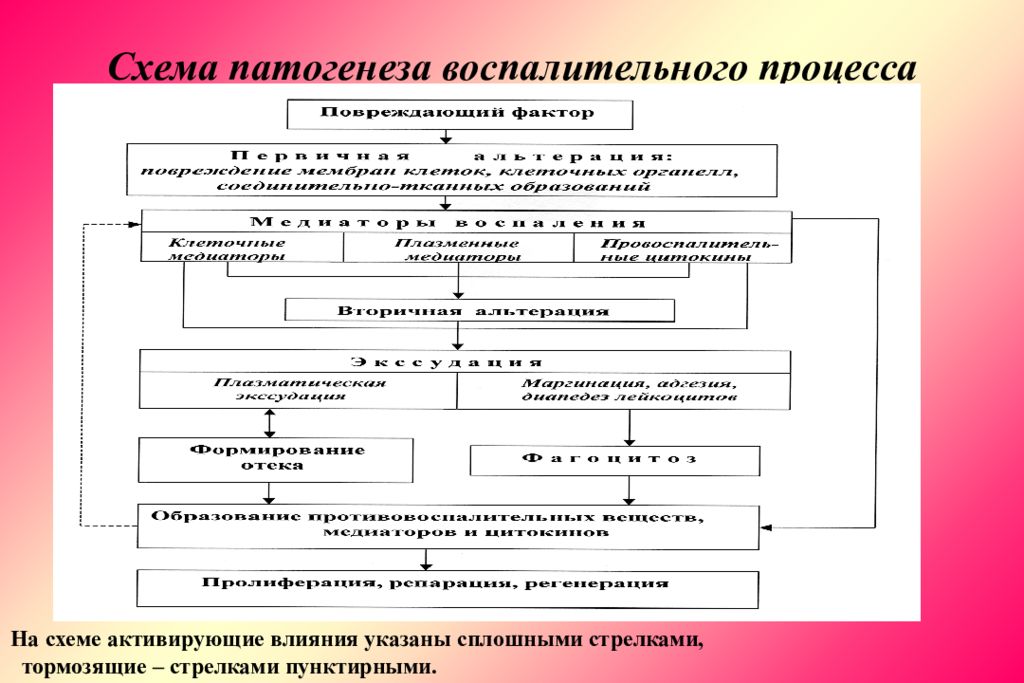
Слайд 46: Схема патогенеза воспалительного процесса
На схеме активирующие влияния указаны сплошными стрелками, тормозящие – стрелками пунктирными.
Слайд 47: Временные параметры событий при остром воспалении:
Активация медиаторов воспаления – секунды Изменения сосудов Миграция нейтрофилов – до 48 часов Хемотаксис, фагоцитоз, дегрануляция Миграция моноцитов – через 48 часов Образование макрофагов Фагоцитоз и выделение цитокинов
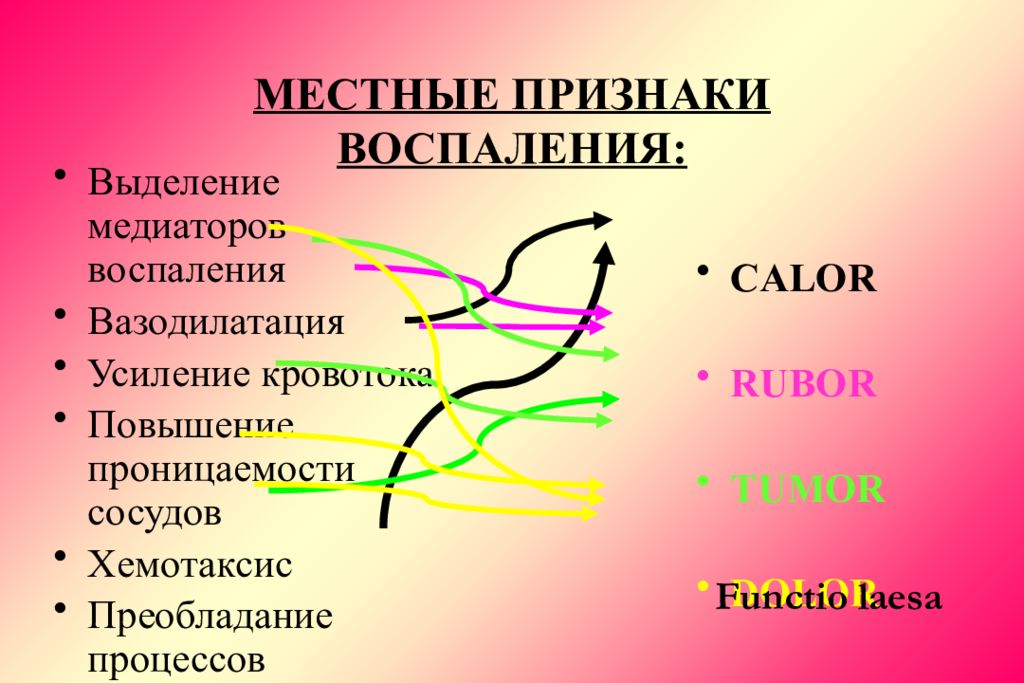
Слайд 49: МЕСТНЫЕ ПРИЗНАКИ ВОСПАЛЕНИЯ:
Выделение медиаторов воспаления Вазодилатация Усиление кровотока Повышение проницаемости сосудов Хемотаксис Преобладание процессов катаболизма C А LOR RUBOR TUMOR DOLOR Functio laesa
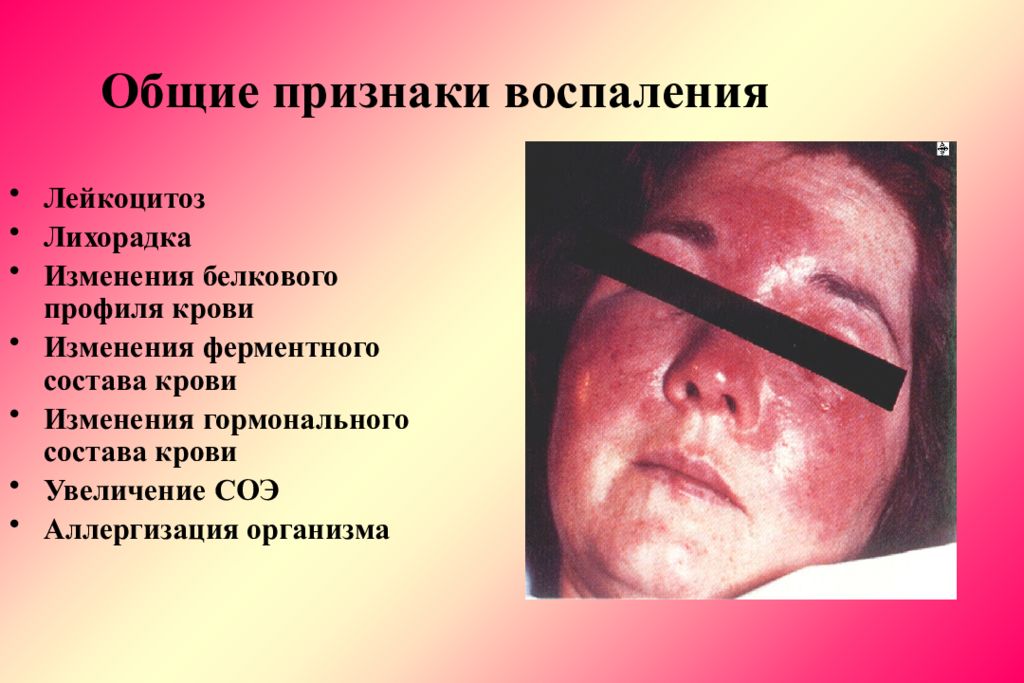
Слайд 50: Общие признаки воспаления
Лейкоцитоз Лихорадка Изменения белкового профиля крови Изменения ферментного состава крови Изменения гормонального состава крови Увеличение СОЭ Аллергизация организма
Слайд 51: Защитно-приспособительное значение воспаления
Локализация очага повреждения Инактивация патогенных (флогогенных) факторов Дренирование (очищение) очага повреждения Мобилизация саногенетических механизмов организма Репарация поврежденной ткани
Слайд 52: Патогенное значение воспаления
Воспаление может быть: Источником генерализации инфекции; Источником патологических рефлексов (аритмия сердца при гастрите, аппендиците, холецистите); Причиной тяжелых повреждений тканей (альтеративно-некротическое воспаление).
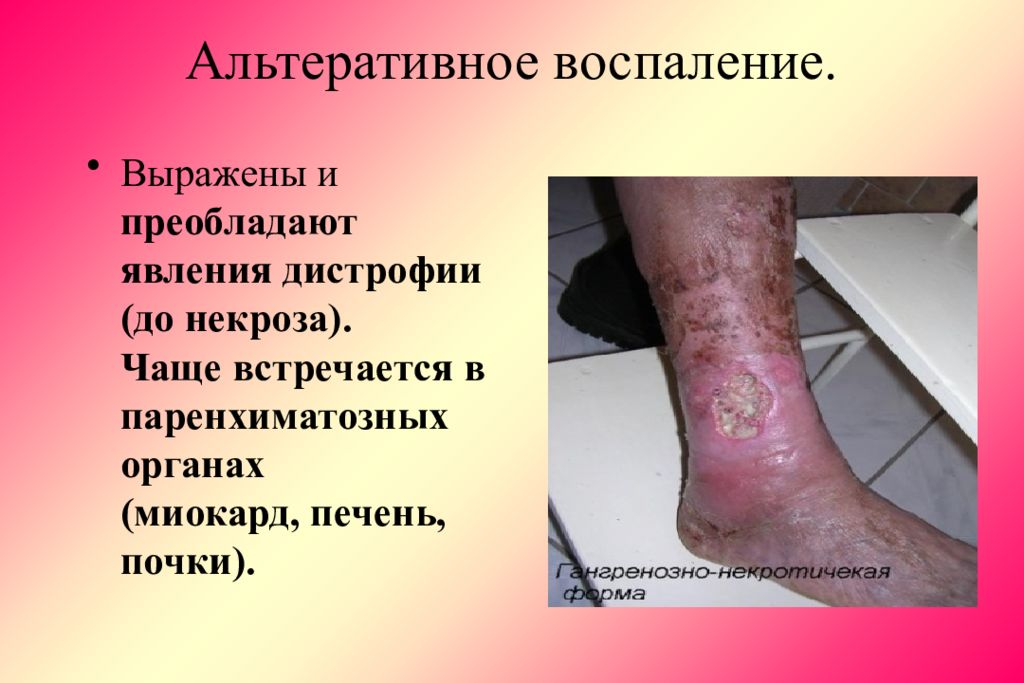
Слайд 54: Альтеративное воспаление
Выражены и преобладают явления дистрофии (до некроза). Чаще встречается в паренхиматозных органах (миокард, печень, почки).
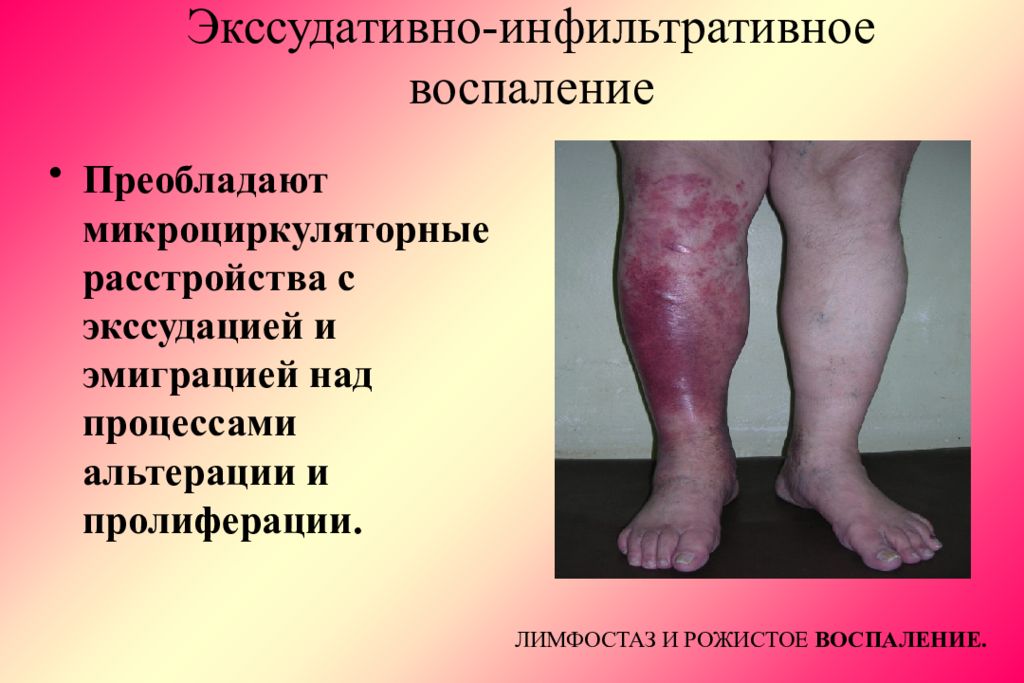
Слайд 55: Экссудативно-инфильтративное воспаление
Преобладают микроциркуляторные расстройства с экссудацией и эмиграцией над процессами альтерации и пролиферации. ЛИМФОСТАЗ И РОЖИСТОЕ ВОСПАЛЕНИЕ.
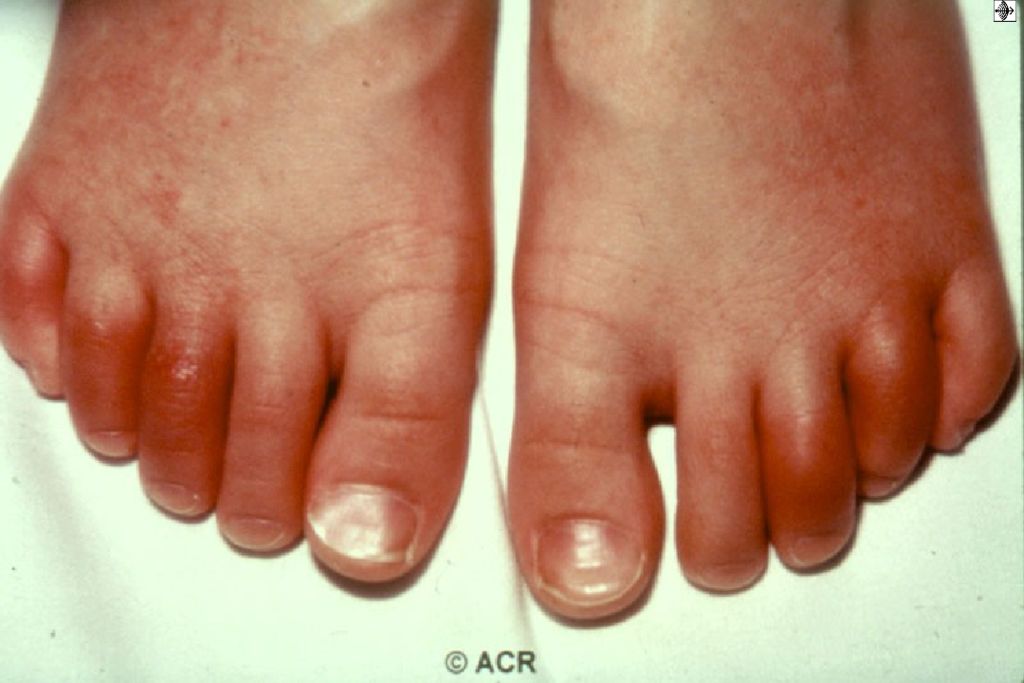
Слайд 56: ОСТРЫЙ РЕАКТИВНЫЙ АРТРИТ (при хламидиозе. C индром Рейтера)
© П.Ф.Литвицкий, 2004 © ГЭОТАР-МЕД, 2004
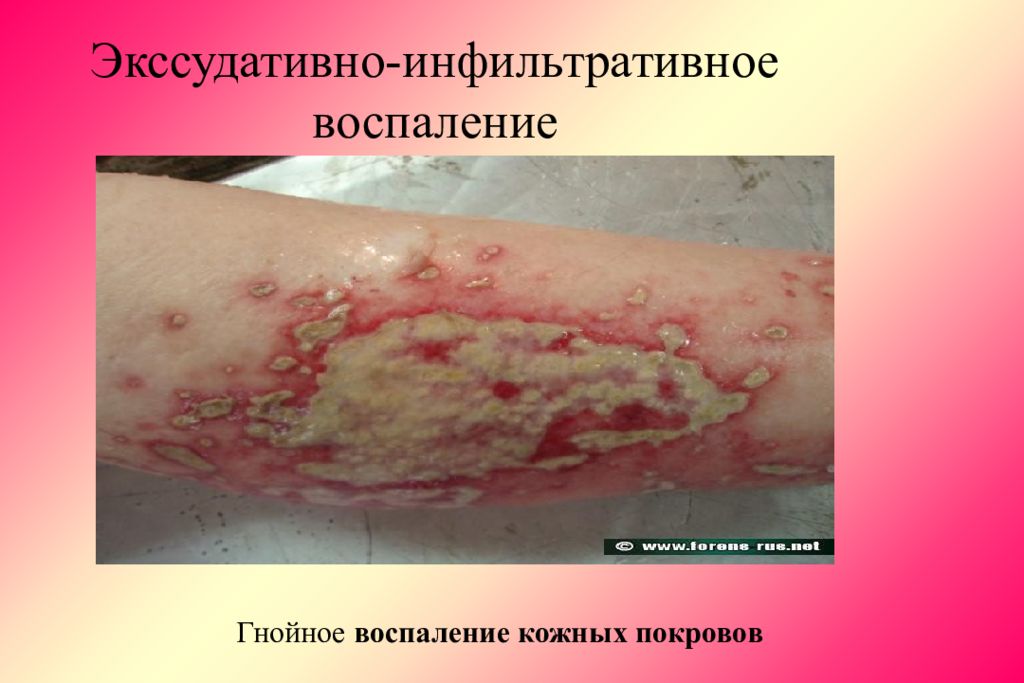
Слайд 57: Экссудативно-инфильтративное воспаление
Гнойное воспаление кожных покровов
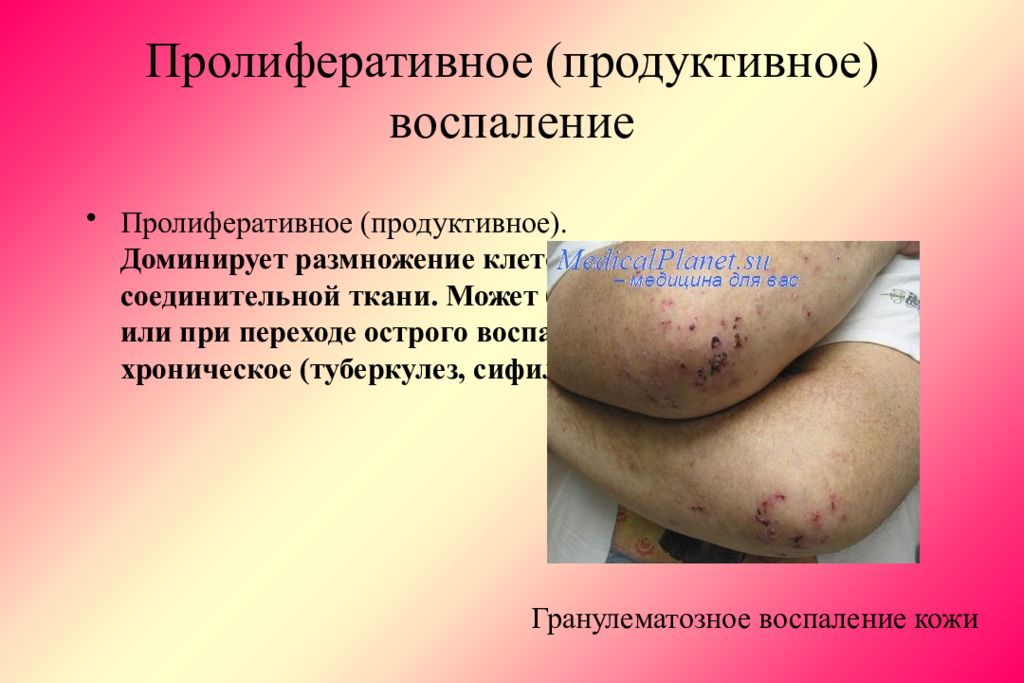
Слайд 58: Пролиферативное (продуктивное) воспаление
Пролиферативное (продуктивное). Доминирует размножение клеток и разрастание соединительной ткани. Может быть первичным или при переходе острого воспаления в хроническое (туберкулез, сифилис, ревматизм). Гранулематозное воспаление кожи
Слайд 59: Клиническая оценка воспаления у больного
Зависит от конкретных обстоятельств возникновения и развития ТПП: Причины развития (асептическое или инфекционное) Локализация очага воспаления (кожа, мозг) Распространенности (чем более местно протекает воспаление, тем благоприятнее его исход) Интенсивности (нормо-.гипо-, гиперергическое) Качества (классическое, некротическое, экссудативное, пролиферативное) Реактивности организма (до развития человек был здоров или болен ? Чем болен?)
Слайд 60: СИНДРОМ СИСТЕМНОГО ВОСПАЛИТЕЛЬНОГО ОТВЕТА SIRS (ССВО)
представляет собой симптомокомплекс, характеризующий выраженность воспалительной реакции в системе эндотелиоцитов и направленность генерализованного воспалительного ответа на повреждение.
Слайд 61: Этиология SIRS
В 90% случаев – результат инфекционной атаки на организм: инфекцией поражен организм с ослабленной иммунной системой; инфекция поражает представителя популяции, ранее не встречавшегося с этой инфекцией (сифилис, туберкулез, корь) среди представителей индейских племен в Северной Америке. (сепсис) развивается благодаря многократному поступлению в системный кровоток антигенных структур микроорганизмов, их экзо- и эндотоксинов. 10% случаев: массивная механическая травма, массивная кровопотеря, обширные ожоги.
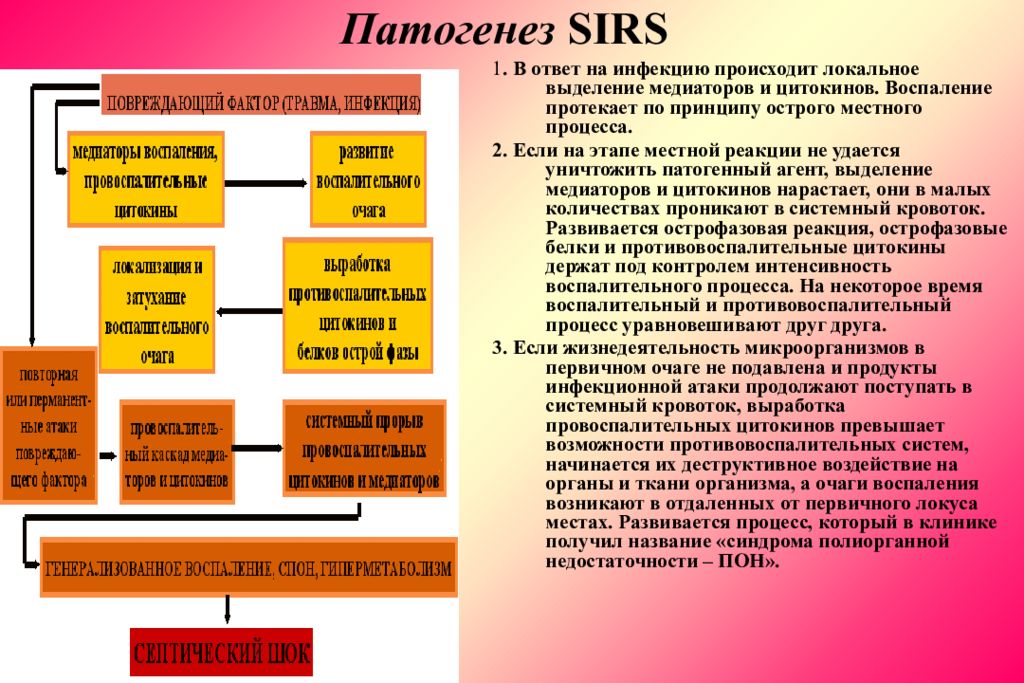
Слайд 62: Патогенез SIRS
1. В ответ на инфекцию происходит локальное выделение медиаторов и цитокинов. Воспаление протекает по принципу острого местного процесса. 2. Если на этапе местной реакции не удается уничтожить патогенный агент, выделение медиаторов и цитокинов нарастает, они в малых количествах проникают в системный кровоток. Развивается острофазовая реакция, острофазовые белки и противовоспалительные цитокины держат под контролем интенсивность воспалительного процесса. На некоторое время воспалительный и противовоспалительный процесс уравновешивают друг друга. 3. Если жизнедеятельность микроорганизмов в первичном очаге не подавлена и продукты инфекционной атаки продолжают поступать в системный кровоток, выработка провоспалительных цитокинов превышает возможности противовоспалительных систем, начинается их деструктивное воздействие на органы и ткани организма, а очаги воспаления возникают в отдаленных от первичного локуса местах. Развивается процесс, который в клинике получил название «синдрома полиорганной недостаточности – ПОН».
Слайд 63: Стадии развития (SIRS)
: Стадия 1 - Локальная продукция цитокинов в ответ на травму или инфекцию. Цитокины способны выполнять ряд защитных функций, участвуя в процессах заживления ран и защиты клеток организма от патогенных микроорганизмов. Стадия 2 - Выброс малого количества цитокинов в системный кровоток. Медиаторы способны активизировать макрофаги, тромбоциты, продукцию гормона роста. Развивающаяся острофазовая реакция контролируется провоспалительными медиаторами и их эндогенными антагонистами: антагонисты интерлейкина-1, 10, 13; фактор некроза опухоли. За счет баланса между цитокинами, антагонистами медиаторных рецепторов и антителами в нормальных условиях создаются предпосылки для заживления ран, уничтожения патогенных микроорганизмов, поддержания гомеостаза. Стадия 3 - Генерализация воспалительной реакции. Регулирующие системы не способны поддерживать гомеостаз и доминируют деструктивные эффекты цитокинов и других медиаторов, что приводит к нарушению проницаемости и функции эндотелия капилляров, формированию отдаленных очагов системного воспаления, развитию моно- и полиорганной дисфункции.
Слайд 64: Клинические критерии развития SIRS
: • температура тела больше 38оС или менее 36оС •частота сердечных сокращений более 90 в минуту •частота дыханий более 20 в минуту или артериальная гипокапния менее 32 мм рт. ст •лейкоцитоз более 12 000 в мл или лейкопения менее 4 000 мл, или наличие более 10% незрелых форм нейтрофилов
Слайд 65: Выводы
Воспаление- типовой патологический процесс В основе воспаления лежат патофизиологические механизмы: альтерация расстройства микроциркуляции экссудация эмиграция фагоцитоз Пролиферация В основе развития синдрома системного воспалительного ответа лежат суммарные эффекты, оказываемые медиаторами повреждения.
Слайд 66: Рекомендуемая литература
Основная Литвицкий П.Ф. Патофизиология. ГЭОТАР-Медиа, 2008 Войнов В.А. Атлас по патофизиологии: Учебное пособие. – М.: Медицинское информационное агентство, 2004. – 218с. Дополнительная 4.Долгих В.Т. Общая патофизиология: учебное пособие.-Р-на-Дону: Феникс, 2007. 5.Ефремов А.А. Патофизиология. Основные понятия: учебное пособие.- М.: ГЭОТАР-Медиа, 2008. 6.Патофизиология: руководство к практическим занятиям: учебное пособие /ред. В.В.Новицкий.- М.: ГЭОТАР-Медиа, 2011. Электронные ресурсы 1.Фролов В.А. Общая патофизиология: Электронный курс по патофизиологии: учебное пособие.- М.: МИА, 2006. 2.Электронный каталог КрасГМУ
Слайд 68: ЭЛАМ эндотелиально-лейкоцитарные адгезивные молекулы
Ключевым этапом аккумуляции лейкоцитов в очаге остроый воспалительной реакции является адгезия (лат. adgesio — прилипание) лейкоцитов к эндотелиальным клеткам. Адгезия зависит от появления и содержания на поверхности эндотелиальных клеток и нейтрофилов эндотелиально-лейкоцитарных адгезивных молекул (ЭЛАМ). При этом определенная эндотелиально-лейкоцитарная адгезивная молекула на поверхности эндотелио-цита представляет собой лиганду к рецептору на наружной мембране нейтрофила в виде комплементарной ЭЛАМ, и наоборот. В частности к ЭЛАМ относят селектины. Выделяют два вида селектинов, L- и Е-селектины, которые присутствуют на плазматической мембране нейтрофилов и других фагоцитов. Функция селектинов эндотелиоцитов — это распознавание и связывание углеводных соединений (гликоконъюгатов) на поверхности нейтрофилов. Вторая разновидность ЭЛАМ на поверхности нейтрофилов — это сходные по строению с иммуноглобулинами молекулы (эндотелиальные межклеточные адгезивные молекулы 1 и 2). Общее название для второго после селектинов вида поверхностных рецепторов нейтрофила, ответственных за их адгезивные свойства, — интегрины. Идентифицировано пять видов интегринов.
Последний слайд презентации: Кафедра патологической физиологии с курсом клинической патофизиологии им. проф: ЭЛАМ
Рост содержания цитокинов в циркулирующей крови (фактор некроза опухолей, интерлейкины и др.) вследствие патогенной системной активации мононук-леарных фагоцитов и иммунокомпетентных клеток при сепсисе и системной воспалительной реакции (СВР) вызывает экспрессию ЭЛАМ на поверхности эндотелиальных клеток и на наружной мембране нейтрофилов и моноцитов. При нарушениях микроциркуляции как неизбежном элементе СВР, тяжелых травматической и раневых болезней, при которых гиперцитокинемия выступает звеном патогенеза системного патологического раневого процесса, экпрессия ЭЛАМ приводит к адгезии лейкоцитов циркулирующей крови к эндотелиальным клеткам. Адгезия активирует эндотелиоциты как клеточные эффекторы воспаления. Они высвобождают флогогены-хемоаттрактанты и вместе с активированными лейкоцитами запускают острую воспалительную реакцию в органах и тканях, удаленных от первичного локуса воспаления. Такое лишенное защитного значения воспаление приобретает чисто патогенный характер и служит одной из причин множественной системной недостаточности.