Первый слайд презентации
Лекция № 9-11 Кристаллизация. Кривые охлаждения. Построение диаграмм состояния.
Слайд 2
Кристаллизация металлов Различают первичную и вторичную кристаллизацию. Переход из жидкого состояния в твердое называется первичной кристаллизацией. Вторичная кристаллизация (перекристаллизация) происходит в твердом состоянии. Рассмотрим процесс первичной кристаллизации более подробно и построим кривую охлаждения.
Слайд 3: Кривые охлаждения
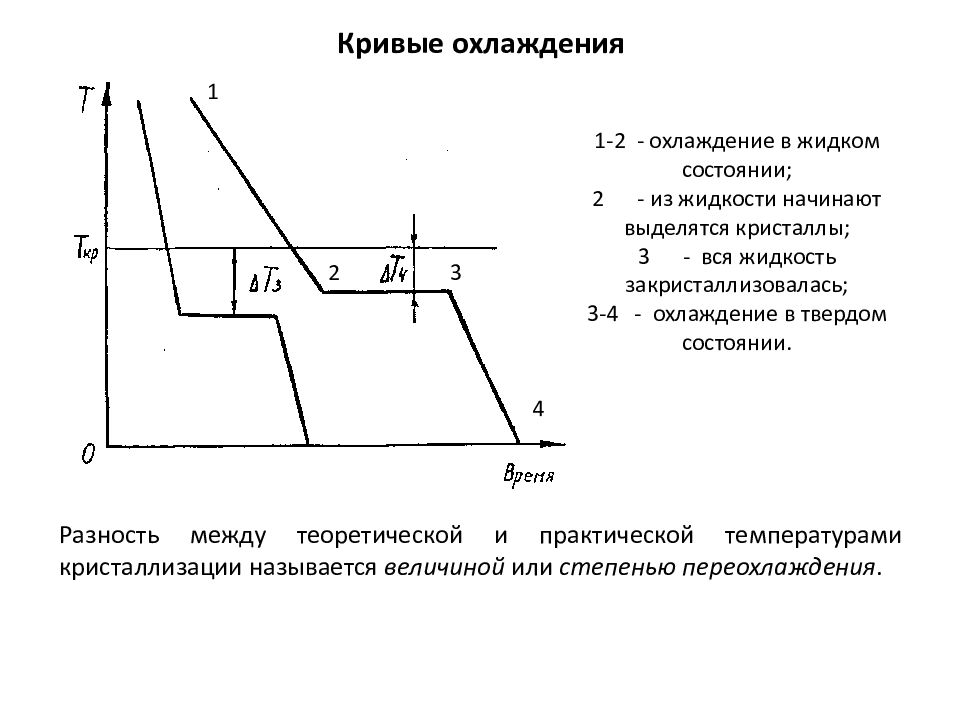
Разность между теоретической и практической температурами кристаллизации называется величиной или степенью переохлаждения. 1 2 3 4 1-2 - охлаждение в жидком состоянии; 2 - из жидкости начинают выделятся кристаллы; 3 - вся жидкость закристаллизовалась; 3-4 - охлаждение в твердом состоянии.
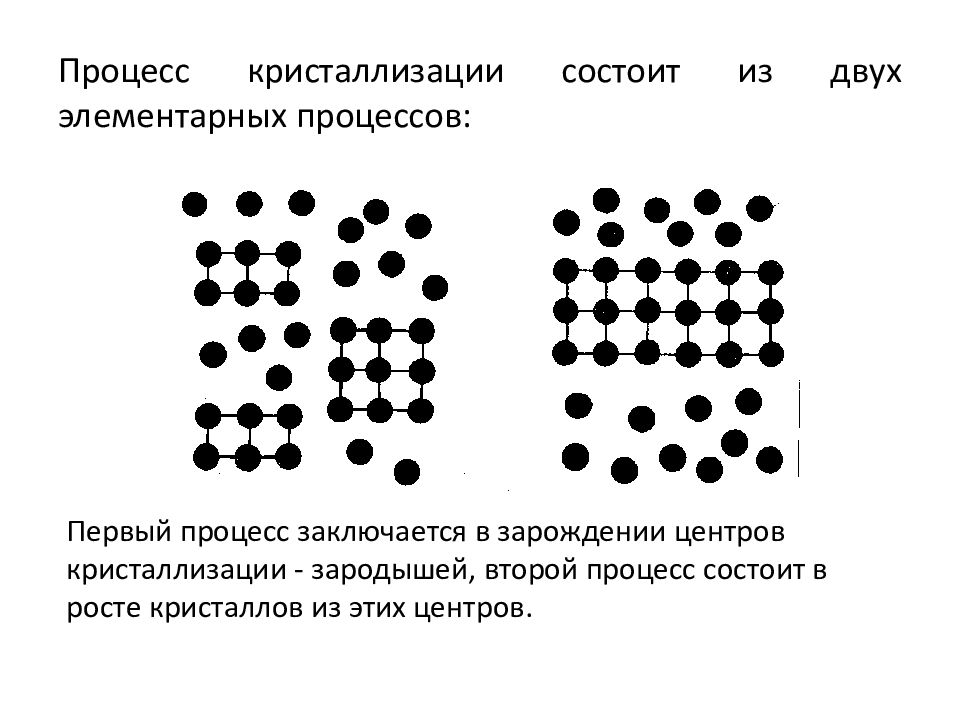
Первый процесс заключается в зарождении центров кристаллизации - зародышей, второй процесс состоит в росте кристаллов из этих центров.
Слайд 7
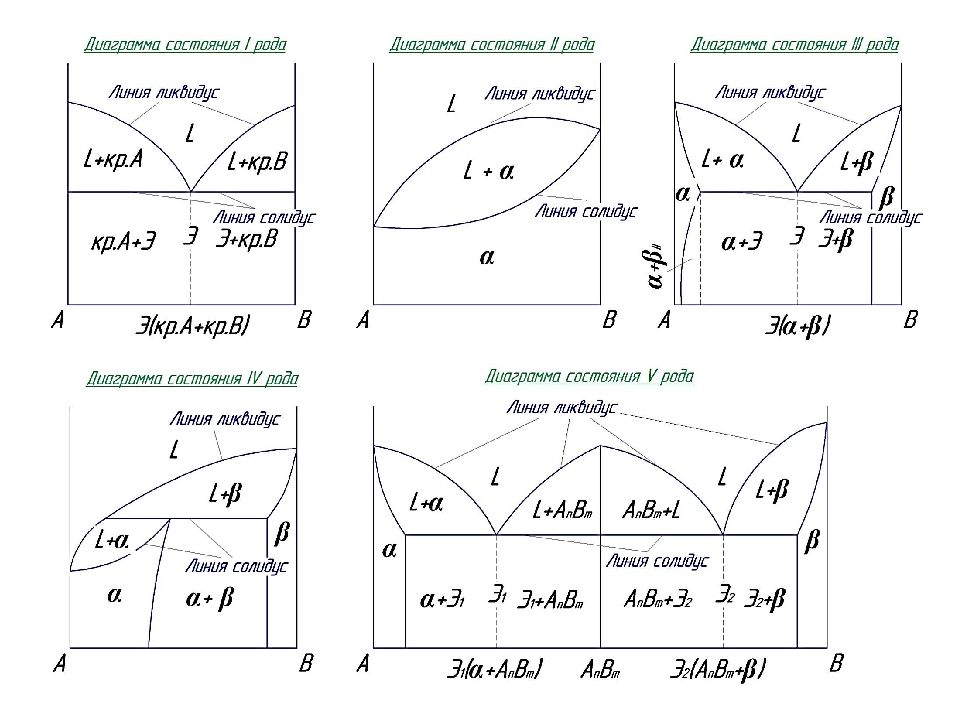
Тип диаграммы состояния двойной системы определяется взаимодействием ее компонентов в жидком и твердом состояниях, а также наличием полиморфных превращений компонентов. Выделяют 5 типов диаграмм состояния.
Слайд 8
Диаграмма состояния представляет собой графическое изображение состояния сплава, т.е. мы можем узнать из каких фаз состоит сплав. (жидкая фаза, твердый раствор, хим.соединение, механическая смесь) Выделяют 5 типов диаграмм состояния: I рода: компоненты А и В неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом (т.е. в сплаве распределены кристаллы А и кристаллы В), а также не образуют химических соединений; I I рода: компоненты А и В образуют неограниченные твердые растворы ; I I I рода: компоненты А и В образуют ограниченные твердые растворы и на диаграмме присутствует эвтектическое превращение, при котором из жидкости ( L ) при постоянной температуре образуется механическая смесь двух фаз ( эвтектика ) : L → Э ( α + β ). IV рода: компоненты А и В образуют ограниченные твердые растворы и на диаграмме присутствует перитектическое превращение L + β → α : жидкость ( L ) реагирует с ранее выпавшими твердыми кристаллами ( β ) и образуется новый вид кристаллов – твердый раствор ( α ). V рода: компоненты А и В образуют химические соединения. Диаграммы состояния двухкомпонентных сплавов
Слайд 10
Линия ликвидус – выше этой линии сплавы в жидком состоянии. Линия солидус - ниже этой линии сплавы в твердом состоянии. Между линиями ними сплав находится в твердо-жидком состоянии. Обозначения структурных составляющих на диаграммах I-IV рода: L - жидкость; кр. А - кристаллы компонента А в чистом виде; кр. В - кристаллы компонента В в чистом виде; α - твердый раствор компонента В в компоненте А ; β – твердый раствор компонента А в компоненте В ; Э – эвтектика – механическая эвтектическая смесь двух фаз: на диагр. 1: кр.А + кр.В ; на диагр. 3: α + β. Обозначения структурных составляющих на диаграмме V рода: L - жидкость; α - твердый раствор А n B m в компоненте А ; β – твердый раствор компонента А n B m в компоненте В ; А n B m – химическое соединение компонентов А и В; Э 1 – эвтектика состава: α + А n B m ; Э 2 – эвтектика состава: А n B m + β.
Слайд 12
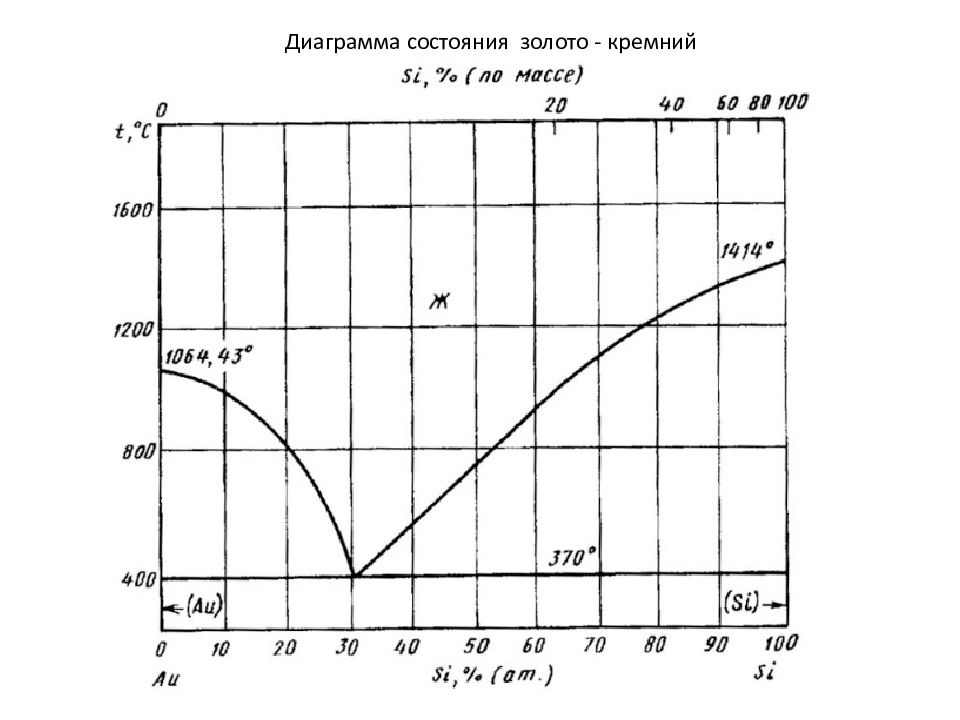
Диаграммы состояния первого типа относятся к сплавам, компоненты которых А и В неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом (т.е. в сплаве распределены кристаллы А и кристаллы В), а также не образуют химических соединений.
Слайд 14
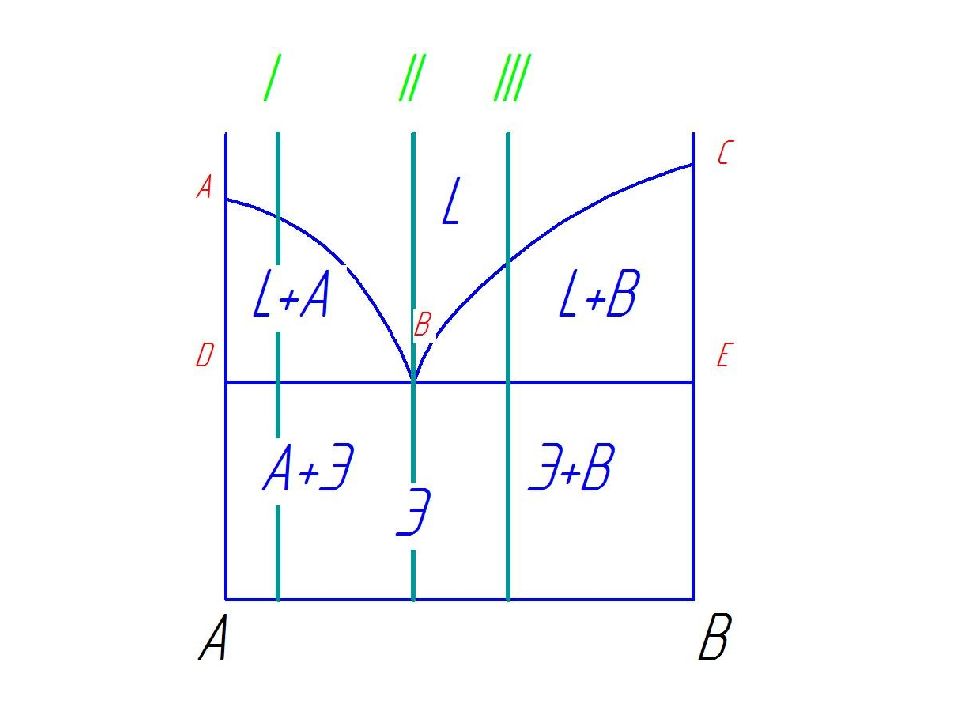
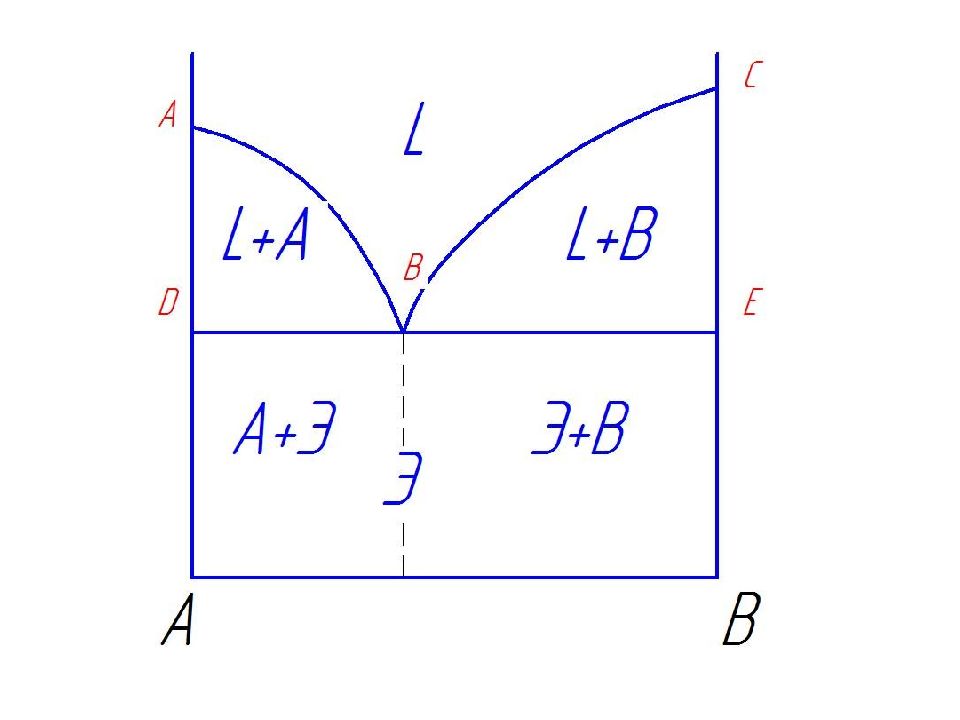
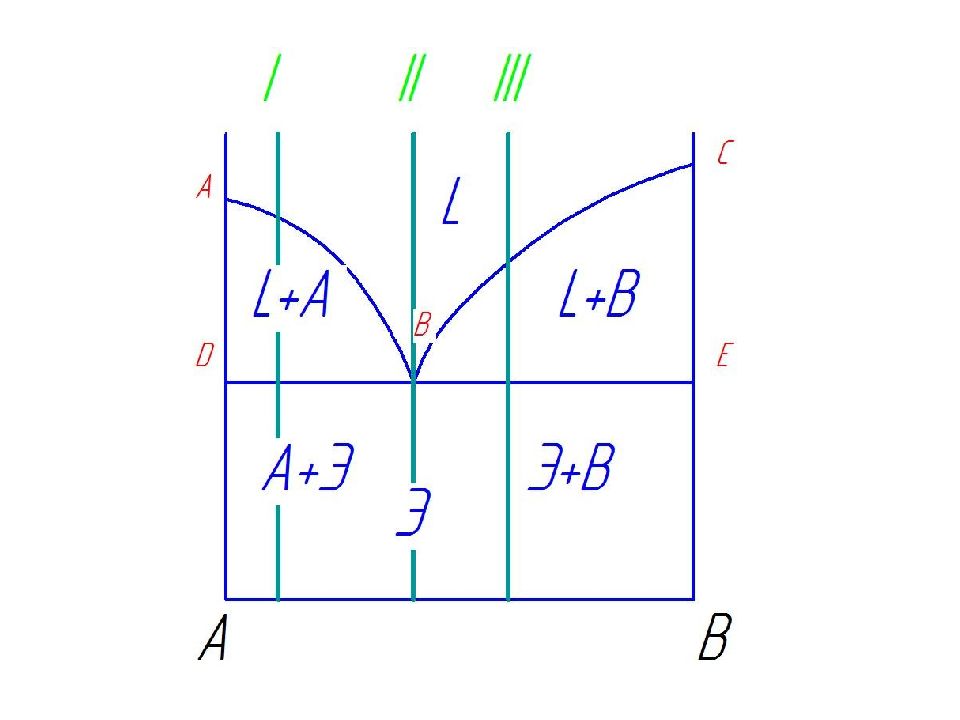
Линия АВС – называется «линия ликвидус », т.к. выше нее сплавы находятся в жидком состоянии (жидкость на диаграмме может обозначатся буквой Ж или L - в разных книгах по разному). Линия DBE – называется «линия солидус », т.к. ниже нее все сплавы твердые (и разные сплавы могут включать просто кристаллы компонентов А и В, твердые растворы (тогда на диаграмме будет буква - α ), механические смеси – например, эвтектика – буква Э и т.д.). Между линиями АВС и DBE сплав находится в твердо-жидком состоянии (т.е. L +А или L +В ) Эвтектика – это механическая смесь двух твердых фаз - кристаллов А и кристаллов В. Жидкость кристаллизуется с образованием 2 - х твердых фаз кристаллов А и В – это называется « Эвтектическое превращение »: Ж → Э ( кр.А + кр.В )
Слайд 17
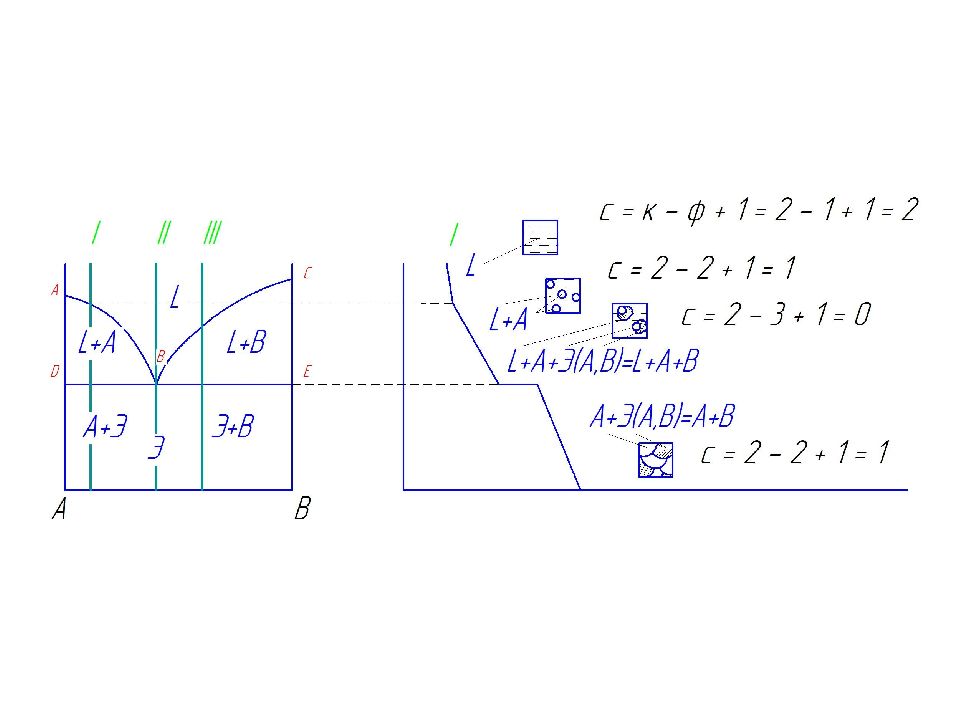
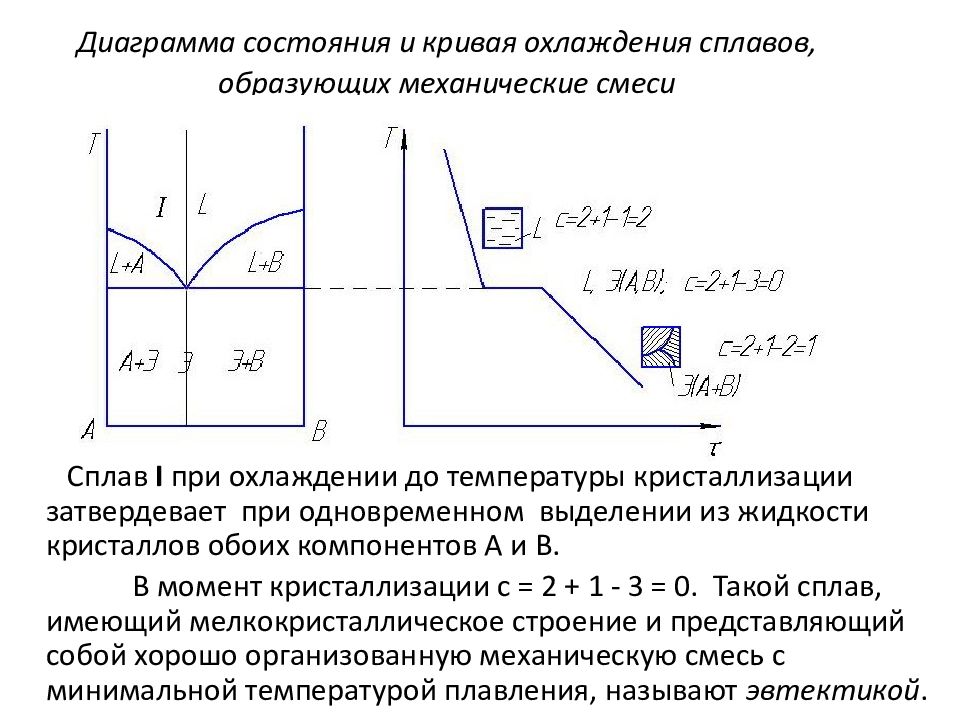
Диаграмма состояния и кривая охлаждения сплавов, образующих механические смеси из чистых компонентов Сплав І при охлаждении до температуры кристаллизации затвердевает при одновременном выделении из жидкости кристаллов обоих компонентов А и В. В момент кристаллизации с = 2 + 1 - 3 = 0. Такой сплав, имеющий мелкокристаллическое строение и представляющий собой хорошо организованную механическую смесь с минимальной температурой плавления, называют эвтектикой.
Слайд 20
Правило фаз Гиббса (закон фаз) Фазовый анализ кривых охлаждения проводят, используя правило фаз: « число равновесно существующих в какой либо системе фаз не может быть больше числа, образующих эти фазы компонентов + 2 ». Это правило связывает число существующих фаз Ф, число компонентов сплава К и число степеней свободы С в одно уравнение: С = К – Ф + 2 Степенями свободы системы называются такие независимые параметры (температура, давление, концентрация) при изменении которых число фаз, находящихся в равновесии не меняется. Цифра « 2 » в уравнении отражает допущение, что фазовое состояние системы определяется двумя параметрами – температурой и давлением.
Слайд 21
Для металлических систем, рассматриваемых при постоянном давлении, равном атмосферному, закон фаз принимает вид: С = К – Ф + 1; где С – число степеней свободы (вариантность), т.е. число внешних и внутренних факторов, которое может изменяться без изменения числа фаз в системе ; К – количество компонентов (веществ, образующих систему ); 1 – число внешних и внутренних факторов ( температура), воздействующих на систему ; Ф – число фаз ; фаза – это однородная часть системы, отделенная от других частей системы поверхностью раздела, при переходе через которую свойства изменяются скачкообразно.
Слайд 22
Правило отрезков (правило рычага): Для того, чтобы определить концентрации компонентов в фазах через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область, проекции точек пересечения на ось концентраций укажут на содержание компонентов в фазах. Для того чтобы определить количественное соотношение фаз в сплаве через заданную точку проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область, отрезки этой линии между заданной точкой ( т.О ) и точками пересечения ( т.В и т.С ), определяющими составы фаз обратно пропорциональны количествам этих фаз.
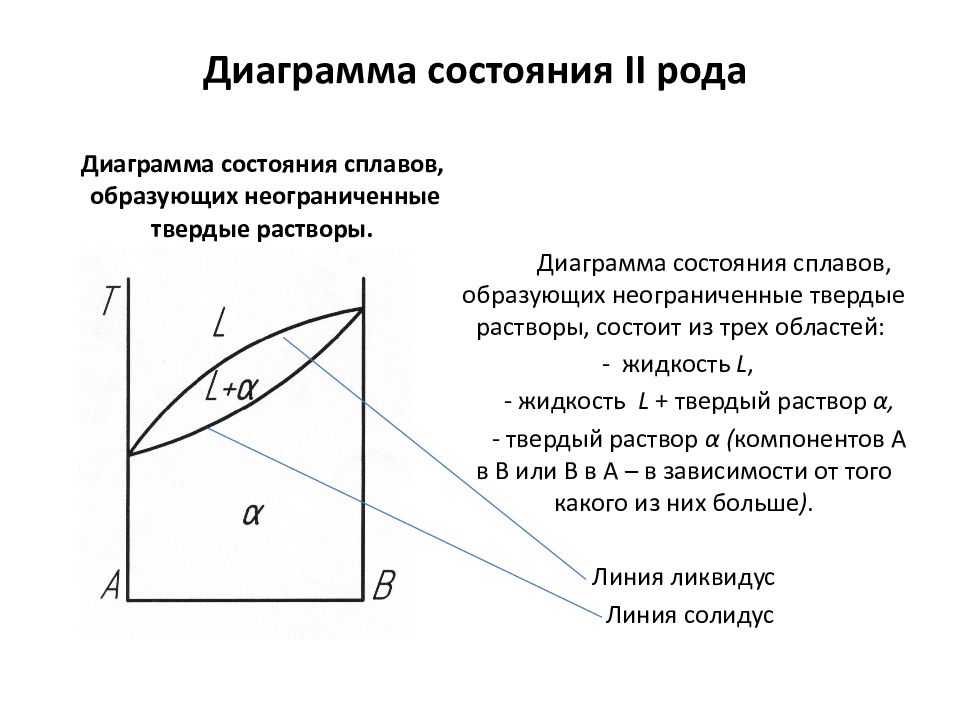
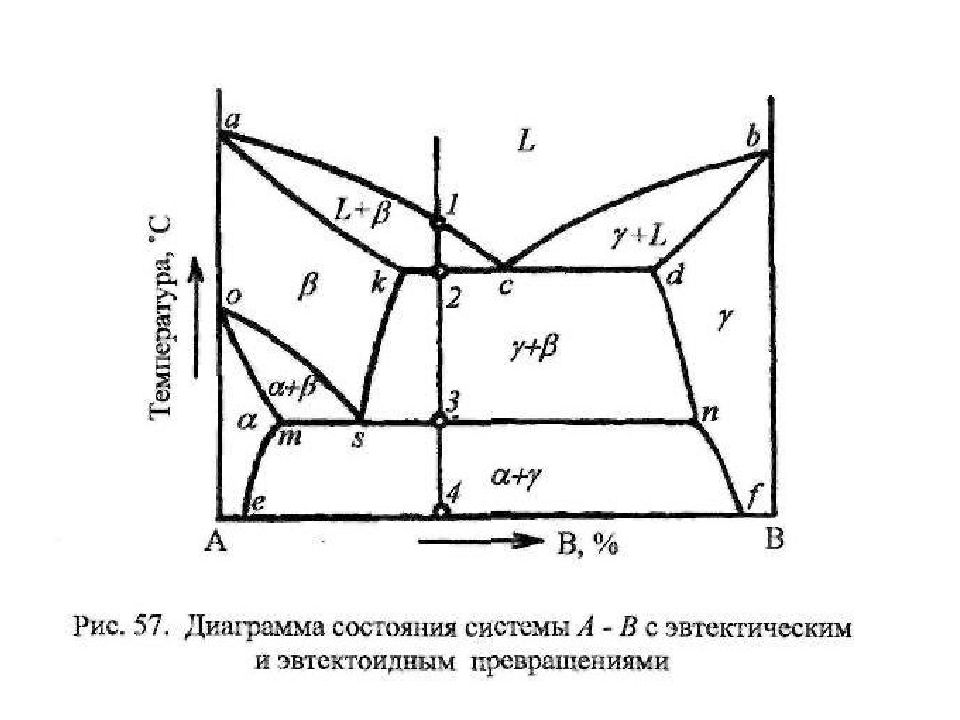
Слайд 23: Диаграмма состояния II рода
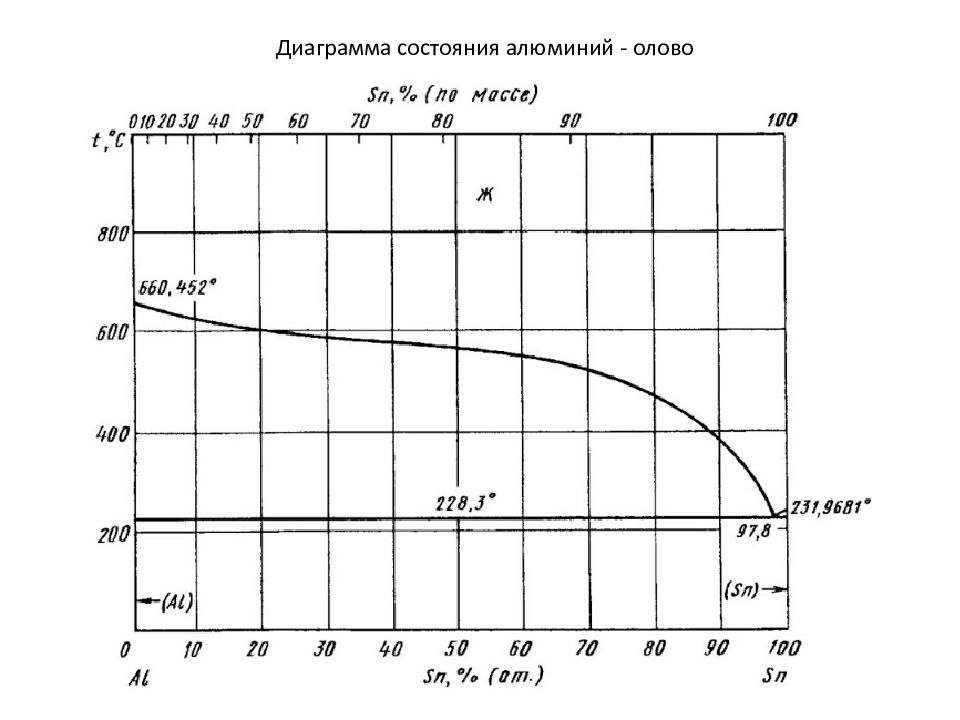
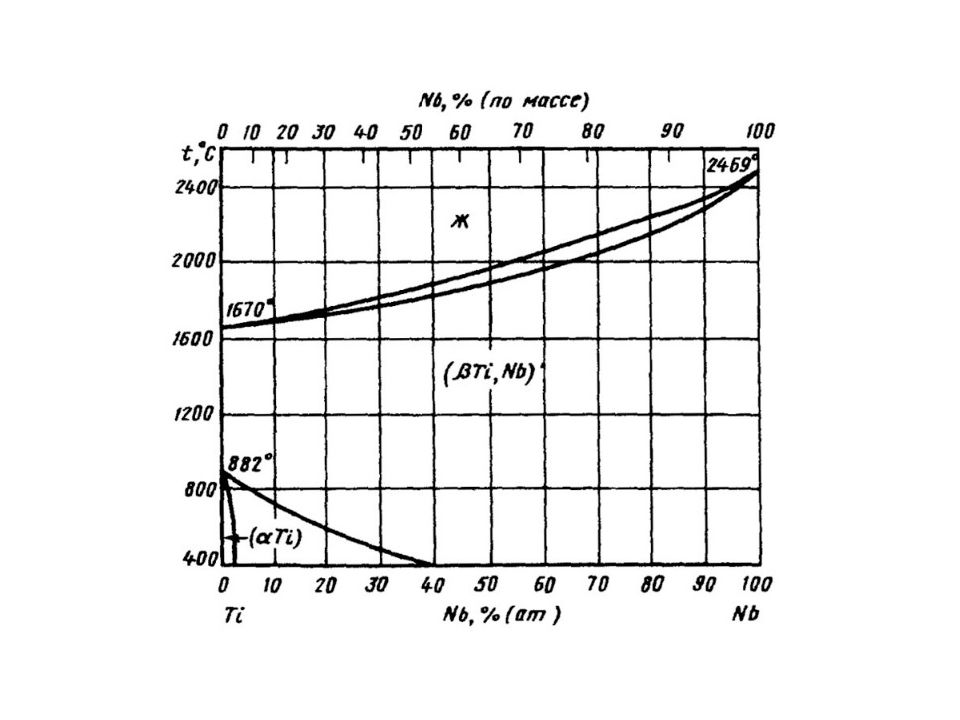
Диаграмма состояния сплавов, образующих неограниченные твердые растворы. Диаграмма состояния сплавов, образующих неограниченные твердые растворы, состоит из трех областей: - жидкость L, - жидкость L + твердый раствор α, - твердый раствор α ( компонентов А в В или В в А – в зависимости от того какого из них больше ). Линия ликвидус Линия солидус
Слайд 25: Диаграмма состояния сплавов, образующих ограниченные твердые растворы – это диаграмм ы состояния III и IV рода
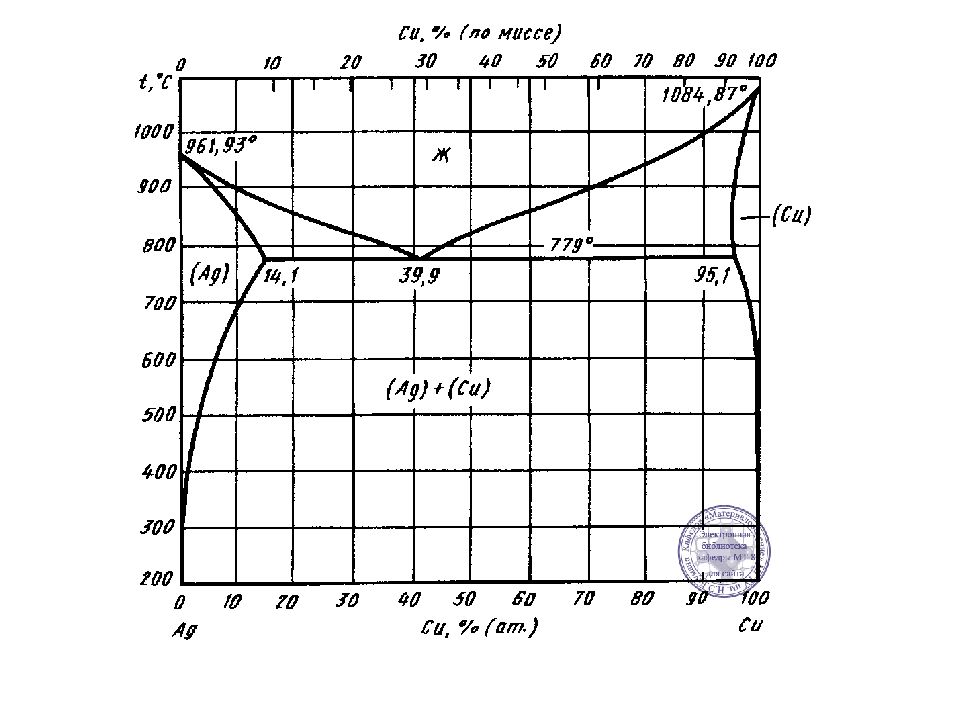
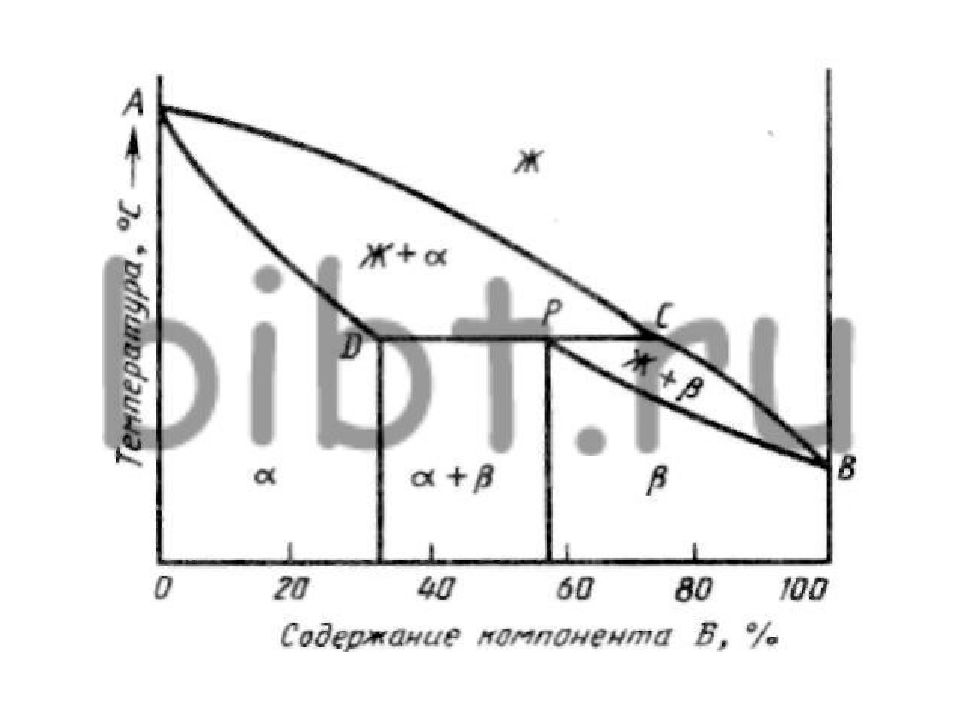
Оба компонента неограниченно растворимы в жидком состоянии, ограниченно в твердом и не образуют химических соединений. В сплавах такого рода возможно существование: жидкой фазы L, жидкого раствора компонента В в А, который будет называться α -раствором, и (или) твердого раствора компонента А в В, который обозначается через β. В этих сплавах возможно равновесие при одновременном сосуществовании трех фаз: L, α и β. В зависимости от того, какая реакция протекает в условиях существования трех фаз, могут быть два вида диаграмм: диаграмма с эвтектическим превращением ( III рода), - диаграмма с перитектическим превращением (IV рода ).
Слайд 26
Диаграмма состояния III рода ABC - линия ликвидус; ADBE и DBEC - линия солидус. Обозначения фаз и структурных составляющих на диаграмме: α – твердый раствор компонента В в компоненте А; Э – эвтектика (механическая смесь фаз) состава α + В; В – кристаллы компонента В; L - жидкость. На диаграмме присутствует эвтектическое превращение, при котором из жидкости ( L ) при постоянной температуре образуется механическая смесь (эвтектика) двух фаз: твердый раствор α + кристаллы В. L → Э ( α + кр.В )
Слайд 27
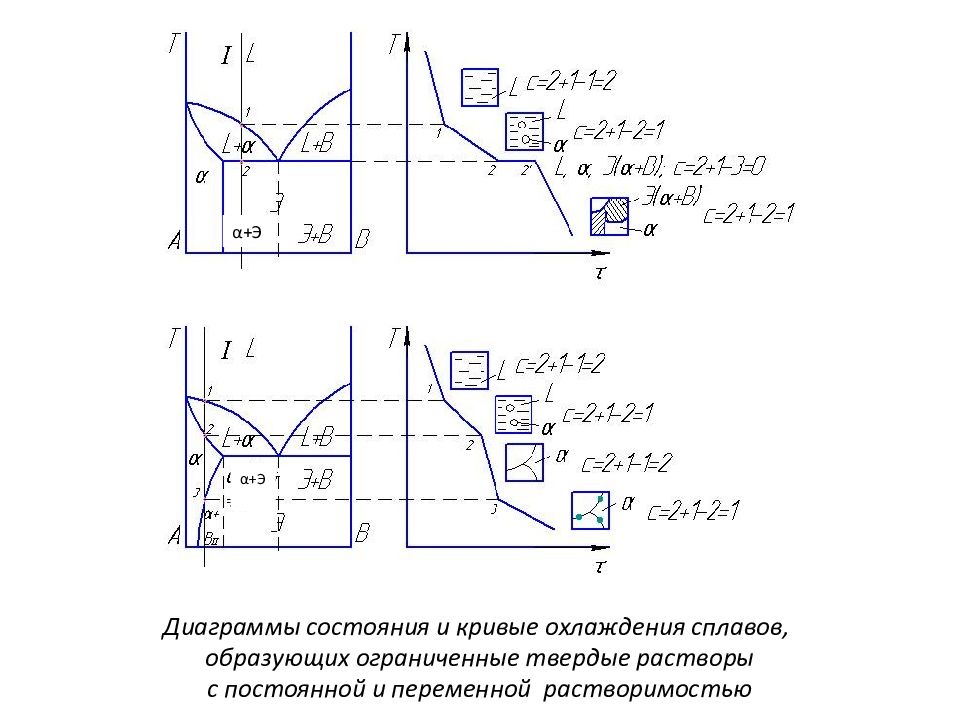
Диаграммы состояния и кривые охлаждения сплавов, образующих ограниченные твердые растворы с постоянной и переменной растворимостью α +Э α +Э
Слайд 28
В отличие от первой диаграммы, на диаграмме, представленной сбоку, видно, что растворимость В в А с понижением температуры уменьшается. Это приводит к пересыщению раствора І, и из него должен выделиться избыточный компонент В. Кристаллы В, выделяющиеся из твердого раствора, называют вторичными кристаллами и часто обозначают символом, имеющим индекс ІІ: в данном случае ВІІ. Процесс выделения вторичных кристаллов из твердой фазы носит название вторичной кристаллизации. Если компонент В также как и А может являться растворителем (т.е. растворять какое-то количество компонента А ), тогда на диаграмме этот раствор обозначим β – твердый раствор компонента А в компоненте В. И диаграмма будет иметь вид…….
Слайд 31
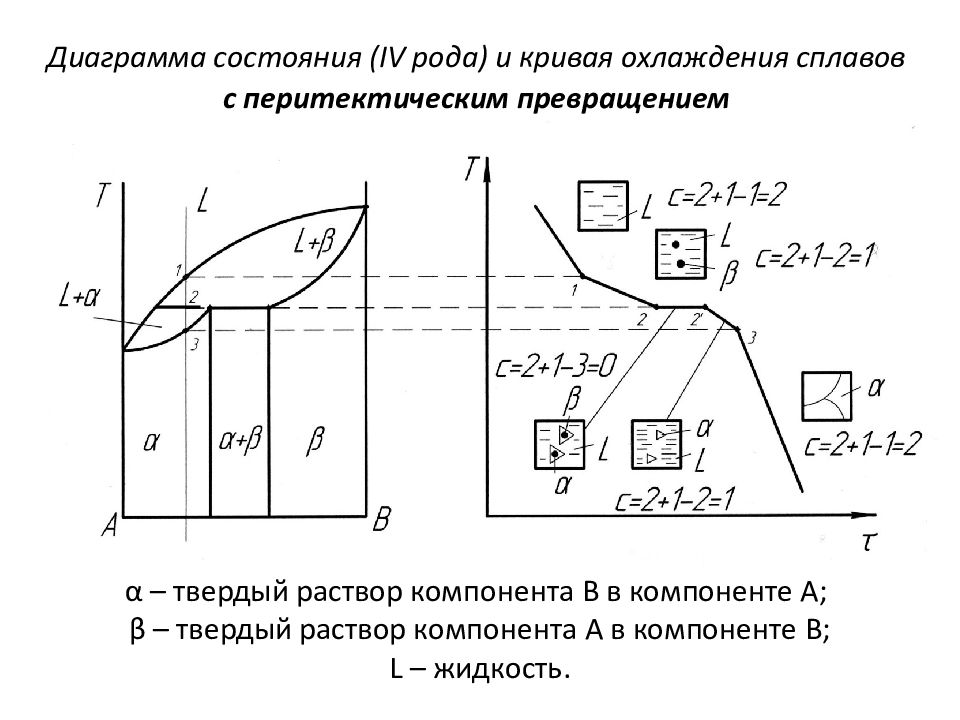
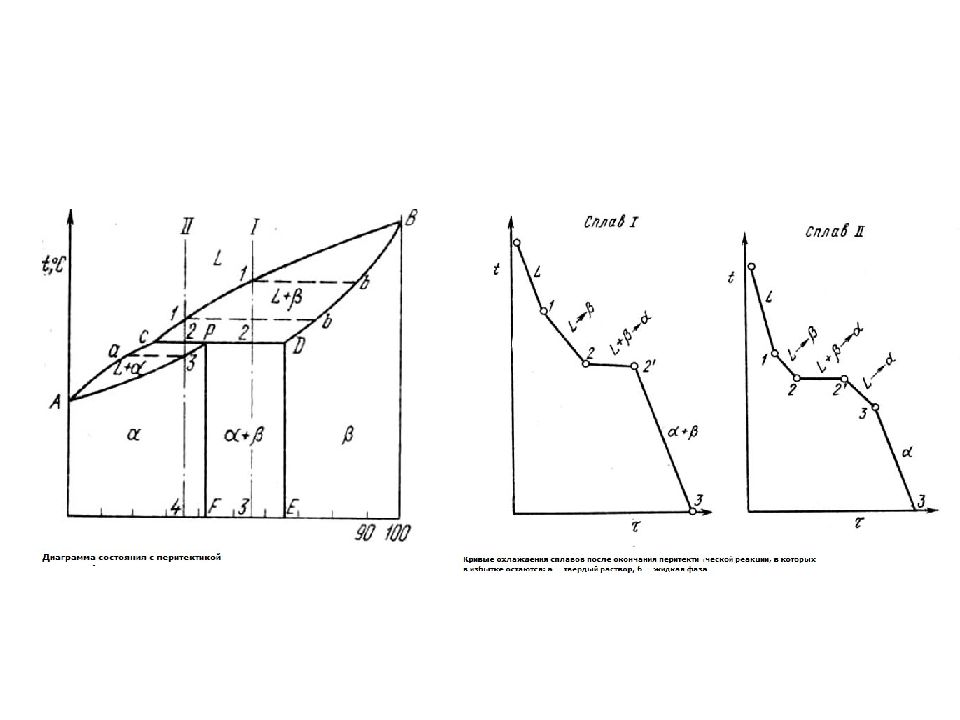
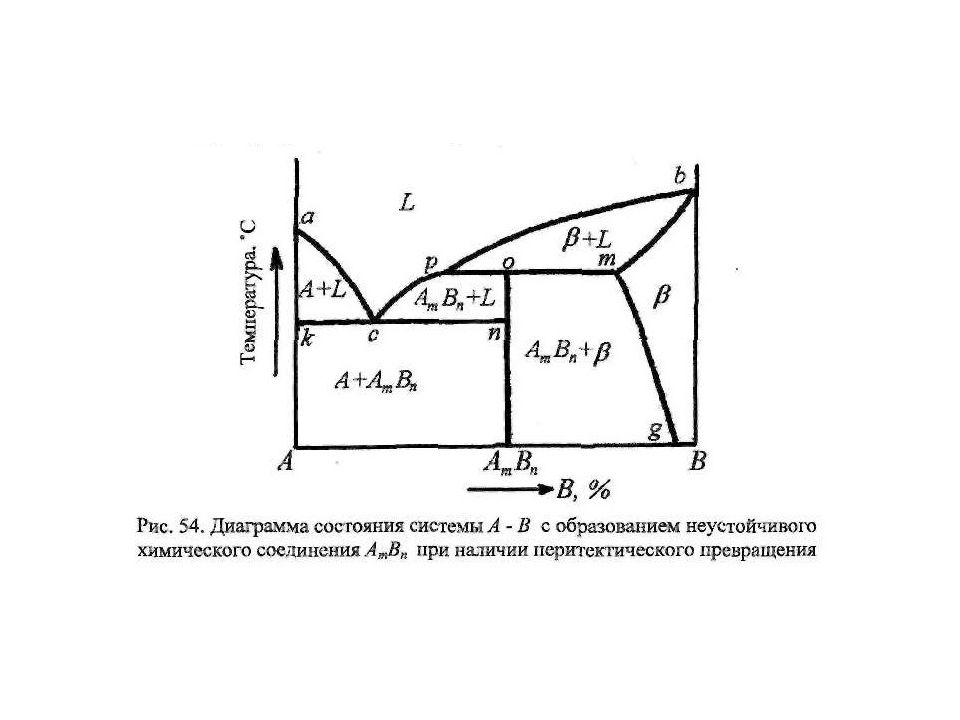
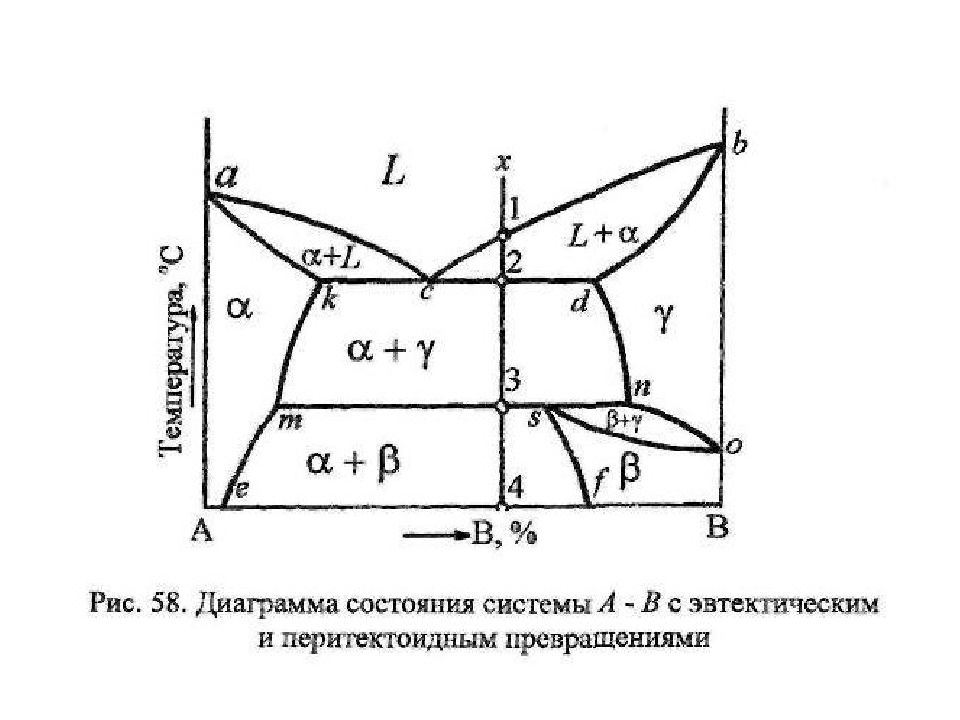
Диаграмма состояния ( I V рода) и кривая охлаждения сплавов с перитектическим превращением α – твердый раствор компонента В в компоненте А; β – твердый раствор компонента А в компоненте В; L – жидкость.
Слайд 32
В рассмотренном ранее эвтектическом превращении жидкость кристаллизуется с образованием двух твердых фаз. Возможен и другой тип превращения, когда жидкость ( L ) реагирует с ранее выпавшими твердыми кристаллами ( β ) и образуется новый вид кристаллов – твердый раствор ( α ). Реакция подобного типа называется перитектической : L + β → α
Слайд 36: Диаграмма состояния сплавов, образующих химические соединения ( V рода)
Слайд 37
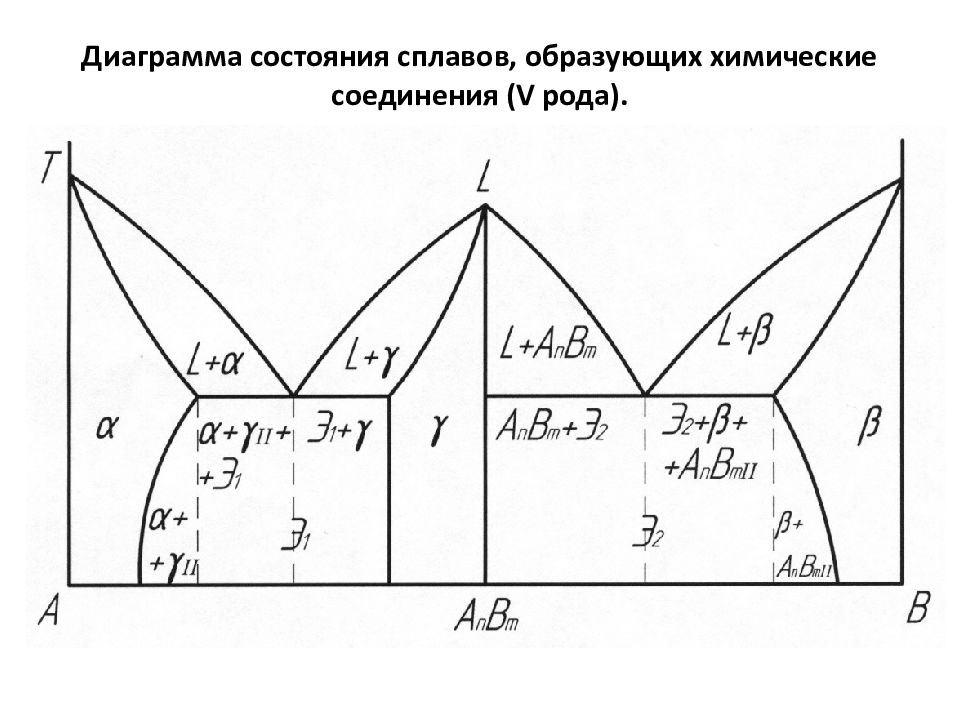
L – жидкость (жидкий раствор компонентов А в В или В в А – в зависимости от того какого из них больше). α - твердый раствор А n В m в компоненте А, γ - твердый раствор компонента А в химическом соединении А n В m, Э 1 (эвтектика состава 1) – механическая смесь твердых растворов α + γ; β – твердый раствор А n В m в компоненте В, Э 2 (эвтектика состава 2) – механическая смесь А n В m + β.
Слайд 38
Химическое соединение А nBm устойчиво, поэтому может быть нагрето без разложения до своей температуры плавления. Химическое соединение А nBm плавится при постоянной температуре и можно рассматривать как однокомпонентную смесь. Кристаллизация сплавов по этой диаграмме происходит совершенно аналогично кристаллизации сплавов, образующих диаграммы с ограниченной растворимостью. Отличие состоит в том, что кроме выделения кристаллов чистых компонентов А и В и кристаллов твердых растворов, происходит еще образование кристаллов химического соединения.
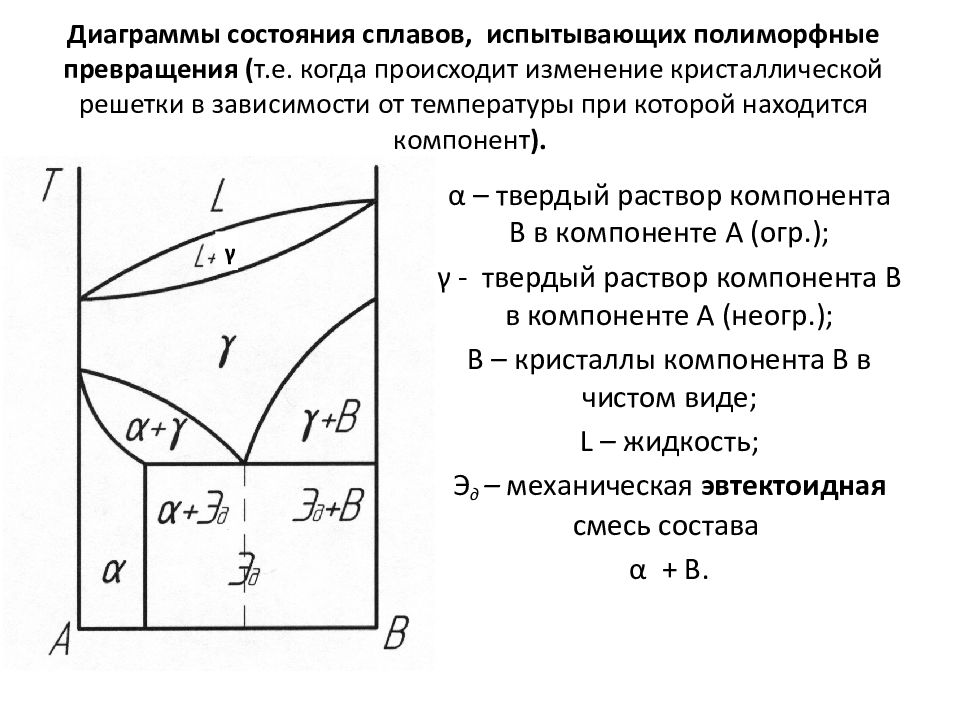
Слайд 41: Диаграммы состояния сплавов, испытывающих полиморфные превращения ( т.е. когда происходит изменение кристаллической решетки в зависимости от температуры при которой находится компонент )
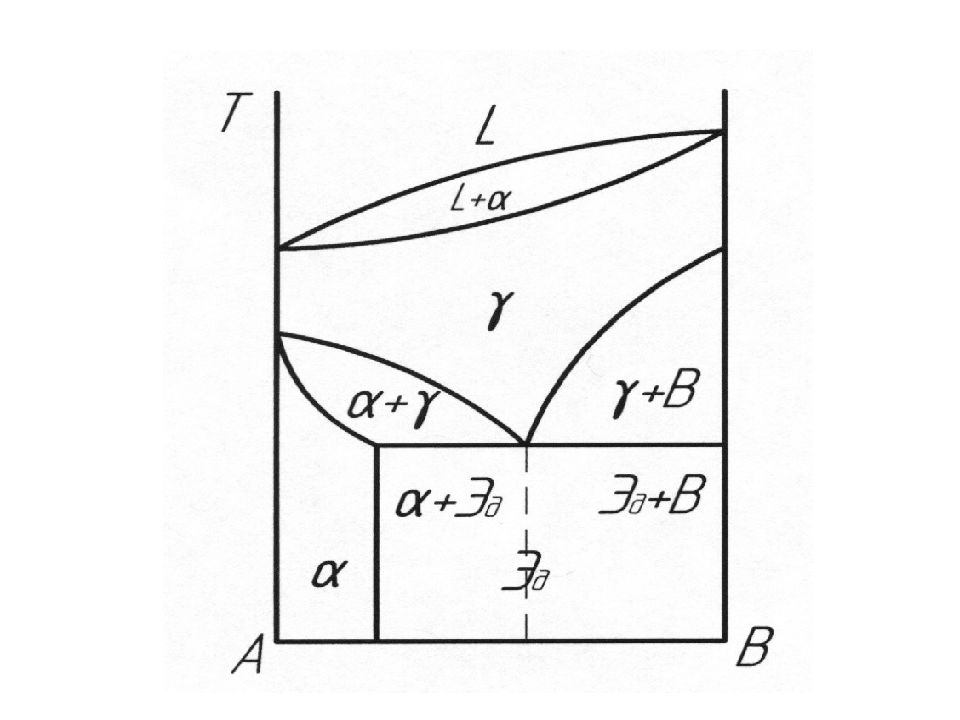
α – твердый раствор компонента В в компоненте А ( огр.); γ - твердый раствор компонента В в компоненте А ( неогр.); В – кристаллы компонента В в чистом виде; L – жидкость; Э д – механическая эвтектоидная смесь состава α + В. γ
Слайд 42
Вид диаграммы состояния зависит от соединений, образующихся между аллотропическими формами обоих компонентов. Если полиморфизм присущ обоим компонентам, и высокотемпературные модификации неограниченно растворимы друг в друге, а низкотемпературные - нерастворимы, то диаграмма состояния имеет такой вид. Ниже некоторой температуры образовавшийся твердый раствор γ распадается в механическую смесь, которая подобна эвтектике, но образуется не из жидкой фазы, а из твердого раствора и называется эвтектоидом. В данном случае Э д = α +В.