Первый слайд презентации
Закон постоянства состава веществ. Химические формулы. Тема урока:
Слайд 2
ЦЕЛЬ УРОКА: сформировать представление о законе постоянства состава веществ, рассмотреть понятие химические формулы. ЗАДАЧИ УРОКА: - сформировать понятие о постоянстве состава веществ; -показать, что постоянный состав характерен только для веществ, имеющих молекулярное строение; сформировать понятия о химической формуле, индексе, коэффициенте. продолжать развивать общеучебные умения и навыки, логическое мышление, умение анализировать, делать вывод.
Слайд 3
(справедлив только для веществ молекулярного строения) Жозеф Луи Пруст (1754-1826) Каждое химически чистое вещество независимо от места нахождения и способа получения имеет один и тот же постоянный состав ЗАКОН ПОСТОЯНСТВА СОСТАВА ВЕЩЕСТВ
Слайд 4
Вода может быть получена в результате следующих химических реакций: 2Н 2 + O 2 = 2Н 2 O Cu(OH) = H 2 O + CuO Са(ОН) 2 + H 2 SO 4 = CaSO 4 + 2Н 2 O
Слайд 5
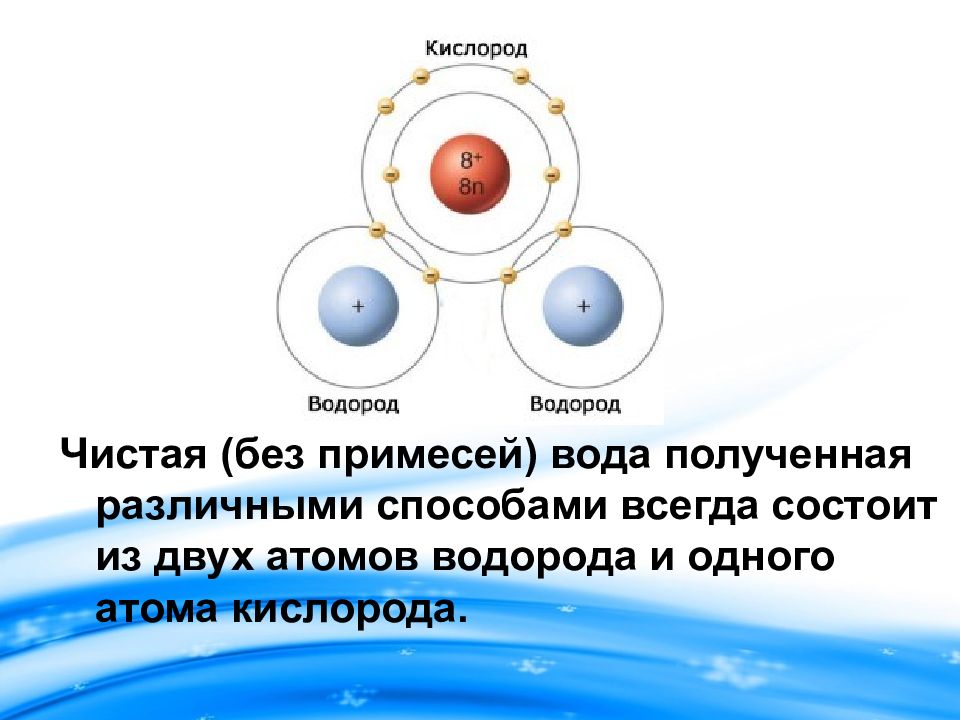
Чистая (без примесей) вода полученная различными способами всегда состоит из двух атомов водорода и одного атома кислорода.
Слайд 6
Из каких атомов состоит это вещество? FeS Найдите в ПСХЭ значение относительных атомных масс железа и серы. Вычислите соотношение масс железа и серы. Расчёты на основе закона постоянства состава веществ
Слайд 7
Ar (Fe) = 56 Ar (S) = 32 Соотношение масс: Ar (Fe) : Ar(S) = 56 : 32 = 7 : 4 Вывод: Чтобы получить сульфид железа надо смешать железо и серу в массовых соотношениях 7 : 4 Если порошка железа взять 9 г, а серы 4 г, химическая реакция произойдет, избыточные 2 г железа в реакцию не вступят.
Слайд 9: Практикум
Известно вещество, в котором на 2 атома меди приходится 1 атом серы. В каких массовых отношениях нужно взять медь и серу, чтобы оба вещества полностью вступили в реакцию?
Слайд 10: Находим:
2 Ar(Cu) = 64 х 2 = 128 Ar(S) = 32 Медь и серу необходимо смешать в соотношении 128 : 32 или 4 : 1
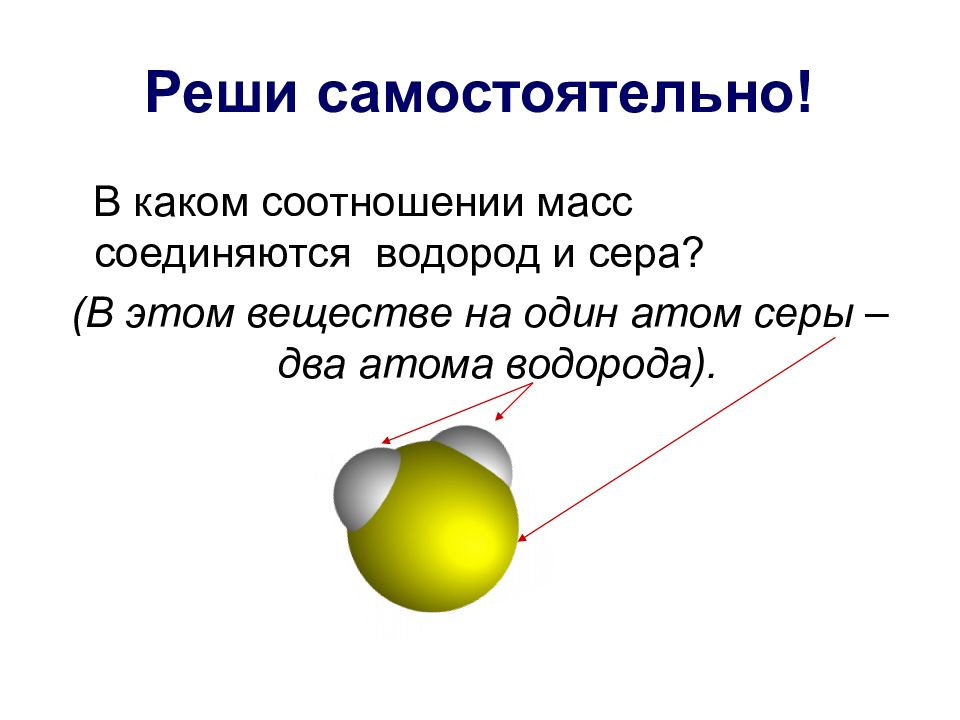
Слайд 11: Реши самостоятельно!
В каком соотношении масс соединяются водород и сера? (В этом веществе на один атом серы – два атома водорода).
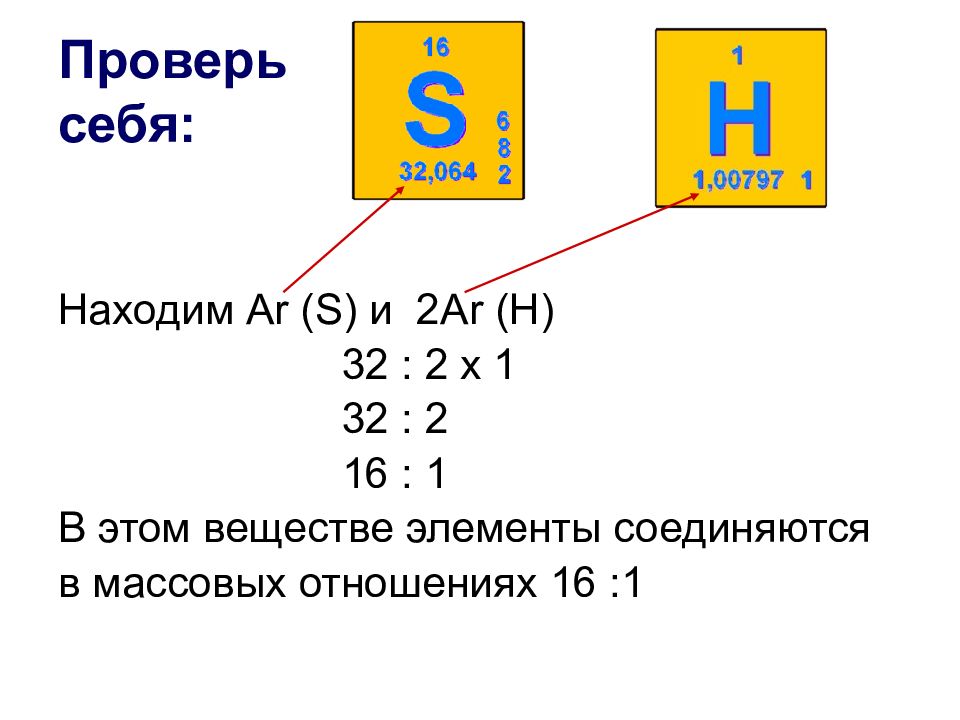
Слайд 12: Проверь себя:
Находим Ar (S) и 2 Ar (H) 32 : 2 х 1 32 : 2 16 : 1 В этом веществе элементы соединяются в массовых отношениях 16 :1
Слайд 13
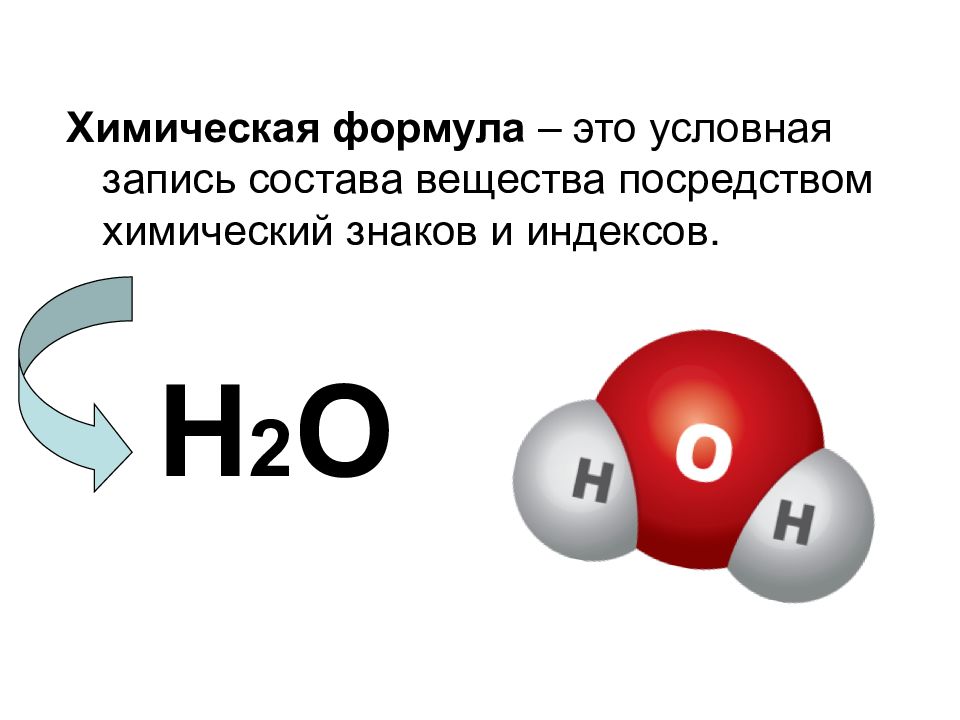
Химическая формула – это условная запись состава вещества посредством химический знаков и индексов. Н 2 О
Слайд 14: ХИМИЧЕСКАЯ ФОРМУЛА ВОДЫ
Н 2 О Индекс 2 (обозначает 2 атома водорода в составе молекулы воды). Индекс 1 не пишут (обозначает 1 атом кислорода в составе молекулы воды). Индекс обозначает число атомов элемента, входящих в состав данного вещества.
Слайд 15: ХИМИЧЕСКАЯ ФОРМУЛА ВОДЫ
2 Н 2 О Коэффициент 2 (показывает 2 молекулы воды). Коэффициент обозначает число молекул (или отдельных атомов)
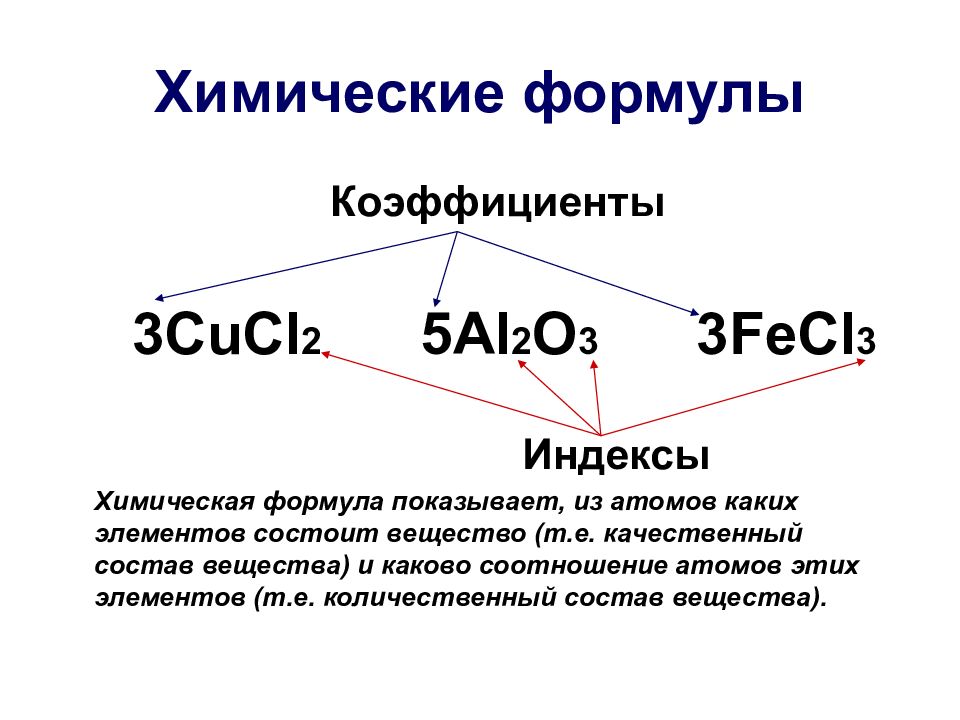
Слайд 16: Химические формулы
Коэффициенты 3CuCl 2 5Al 2 O 3 3FeCl 3 Индексы Химическая формула показывает, из атомов каких элементов состоит вещество (т.е. качественный состав вещества) и каково соотношение атомов этих элементов (т.е. количественный состав вещества).
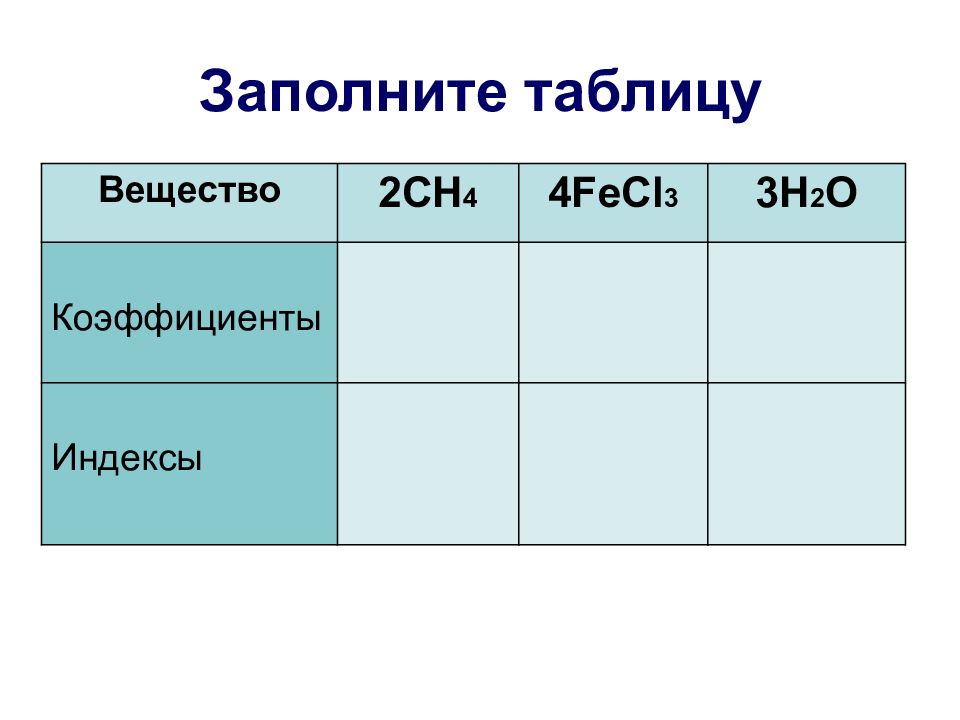
Слайд 17: Подумай, выполни, ответь…
Что означают формулы? 3Н 2 О 5 Fe Как читаются эти записи? Напишите следующую формулу : пять молекул воды образованны десятью атомами водорода и пятью атомами кислорода.