Первый слайд презентации: Занятие 2. Электронная микроскопия
Доронина Татьяна Валерьевна 2019 год Московский государственный университет имени М.В. Ломоносова Биологический факультет Кафедра клеточной биологии и гистологии
Слайд 2
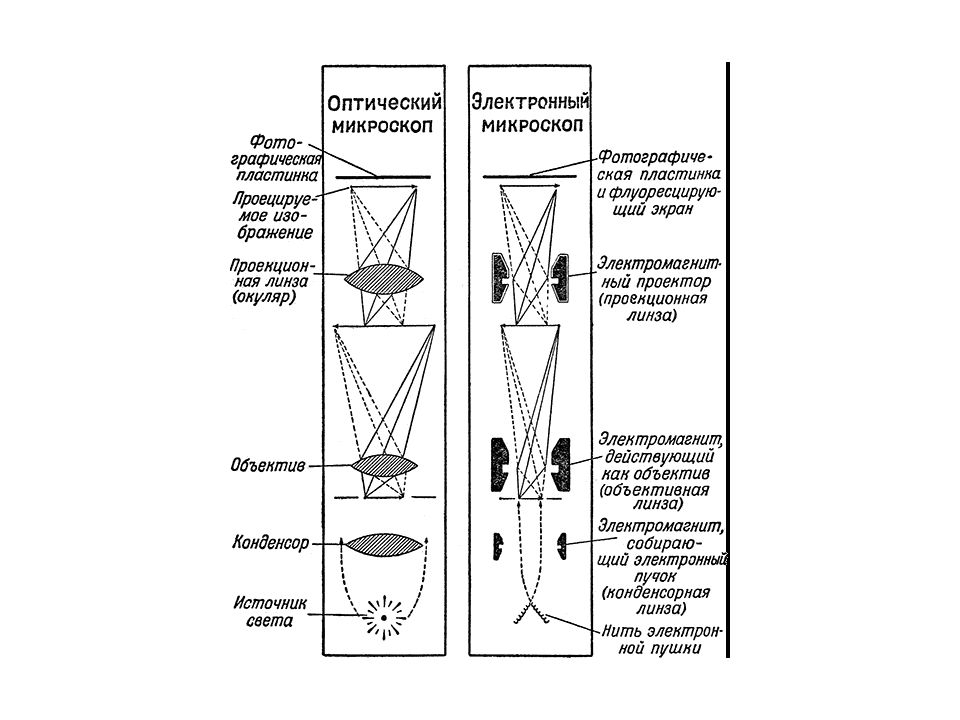
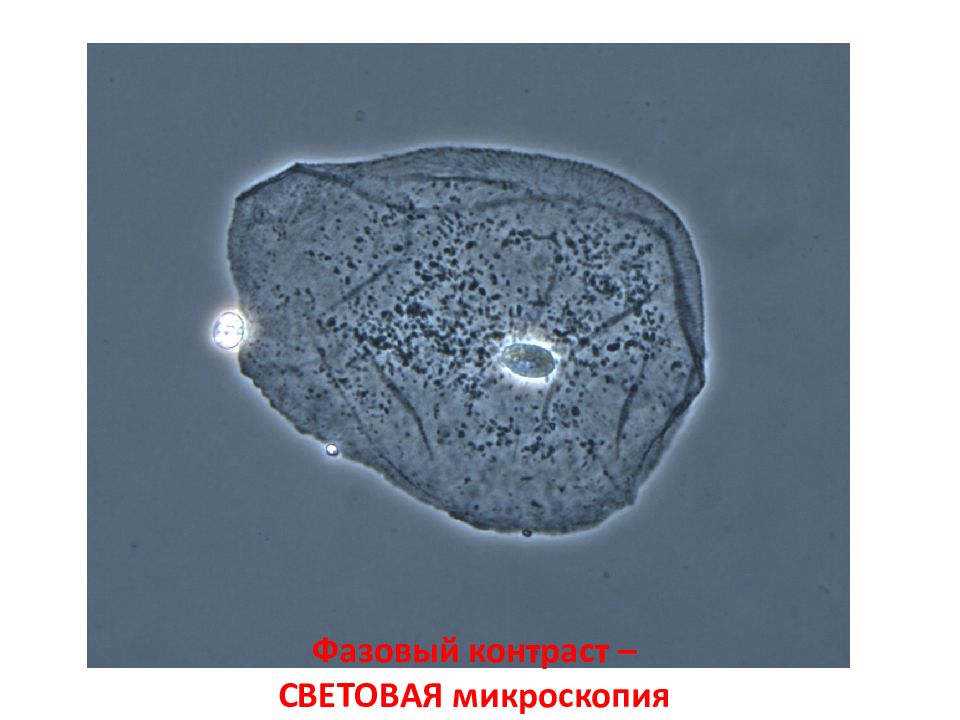
Предел разрешения светового микроскопа: 200-300 нм (0,2 – 0,3 мкм) 130-140 нм (0,13 – 0,14 мкм) – при использовании УФ света Предел разрешения электронного микроскопа : 1 Å (0,1 нм ) 1 мкм = 10 −6 м ; 1 нм = 10 −9 м; 1 Å = 10 −10 м
Слайд 5
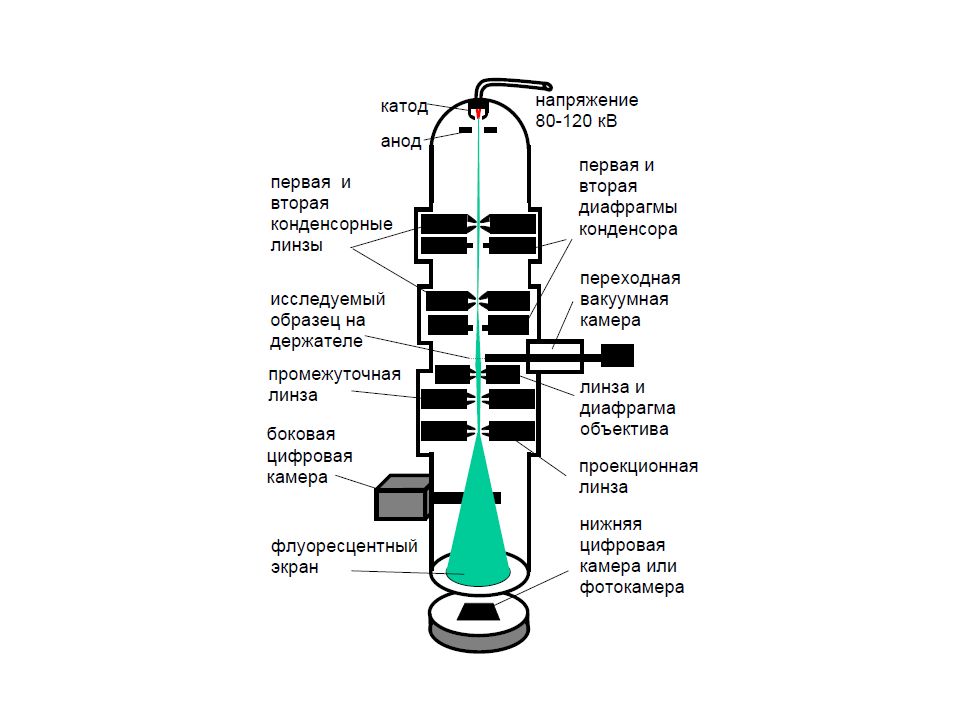
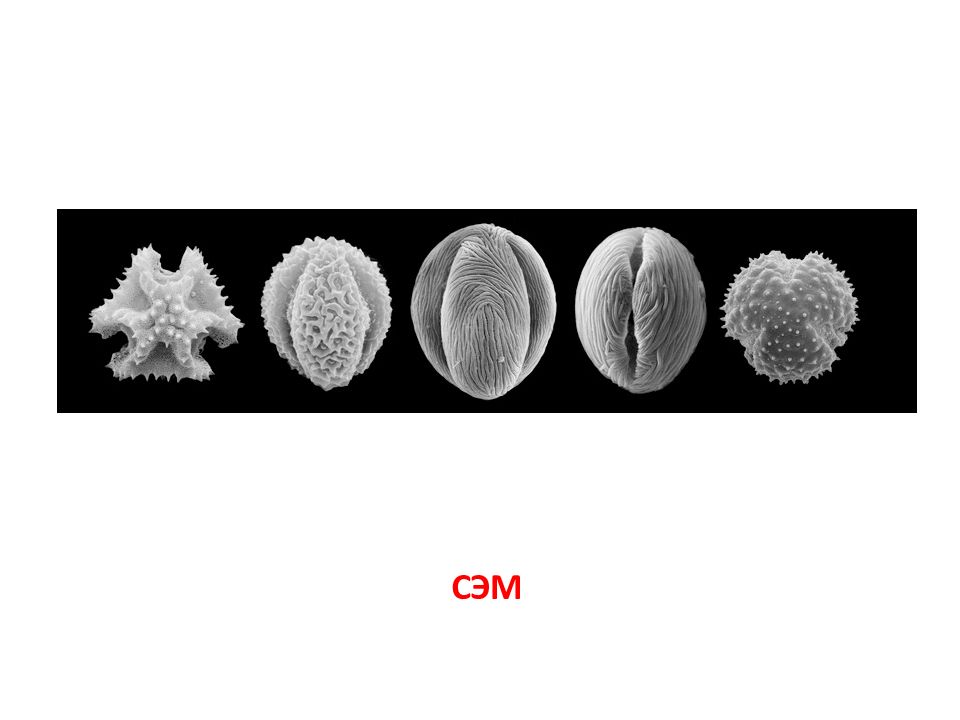
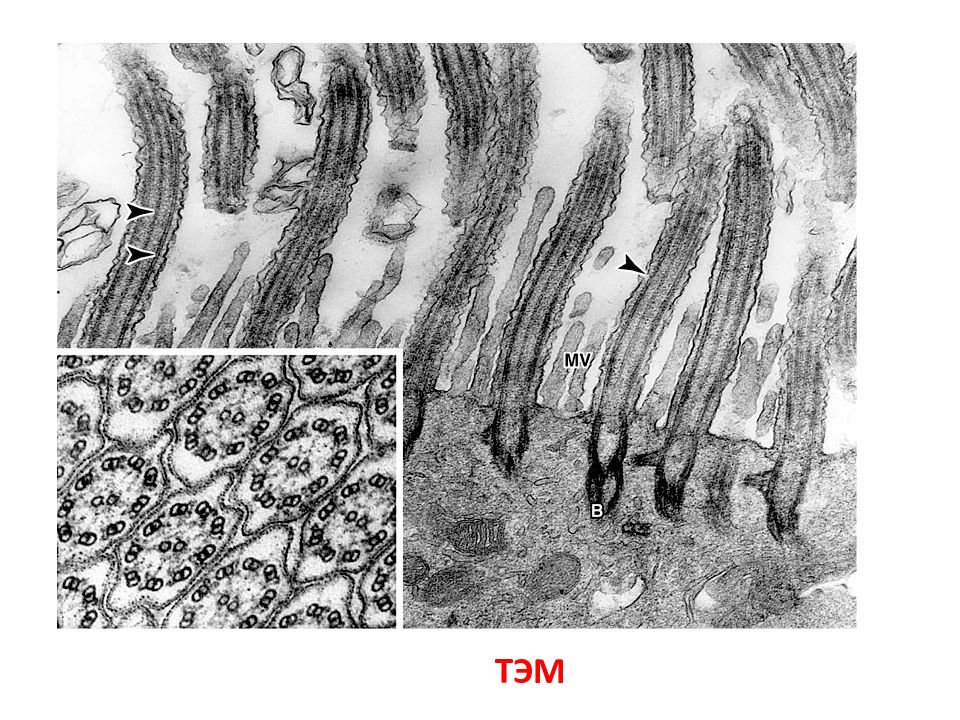
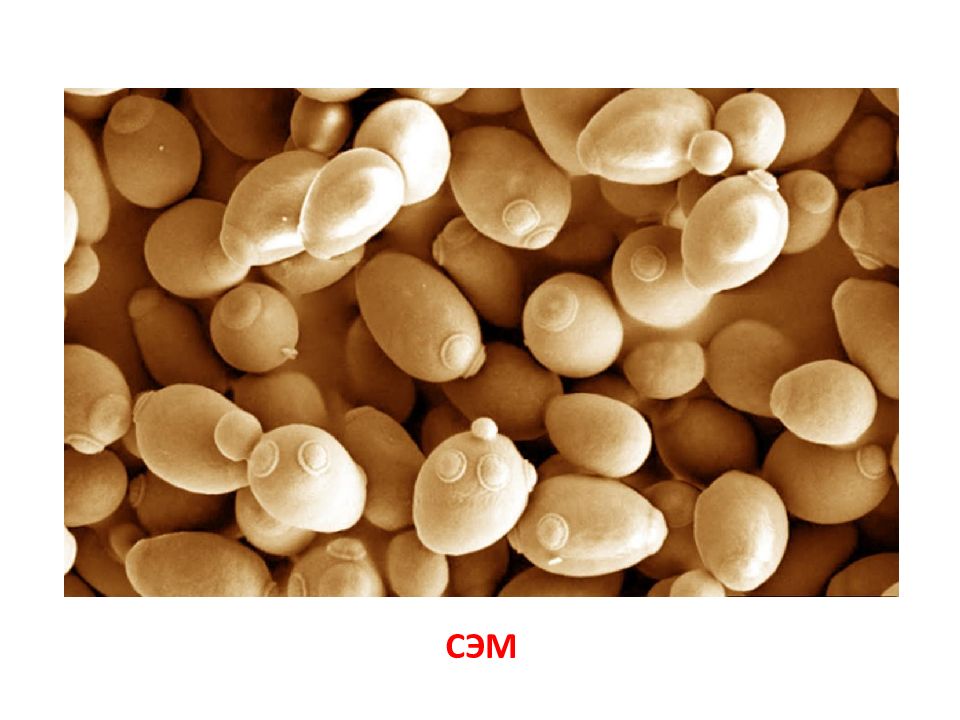
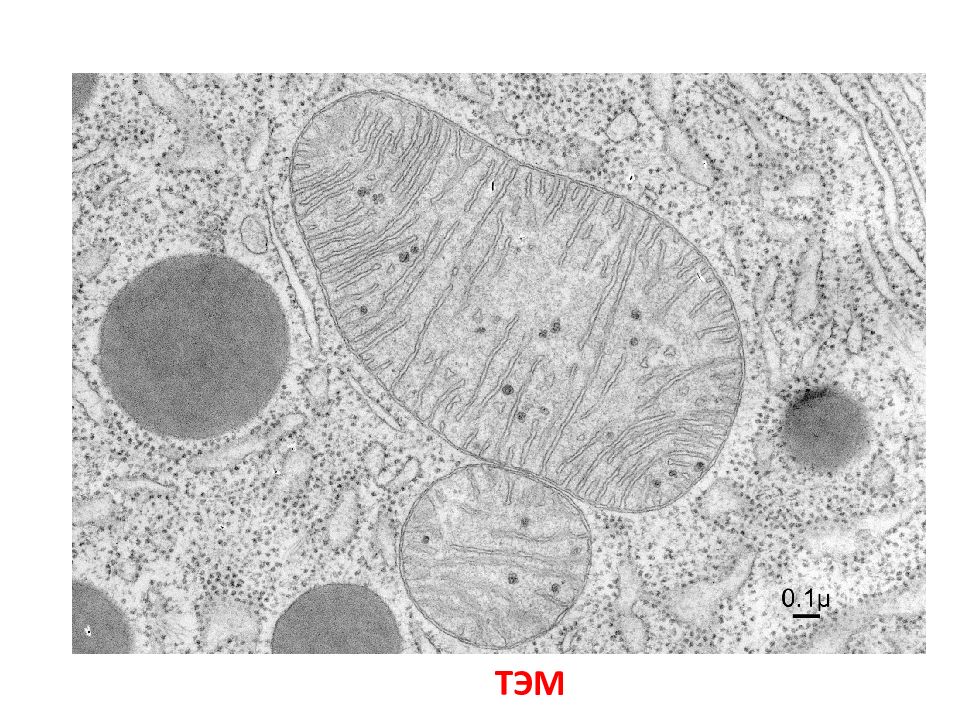
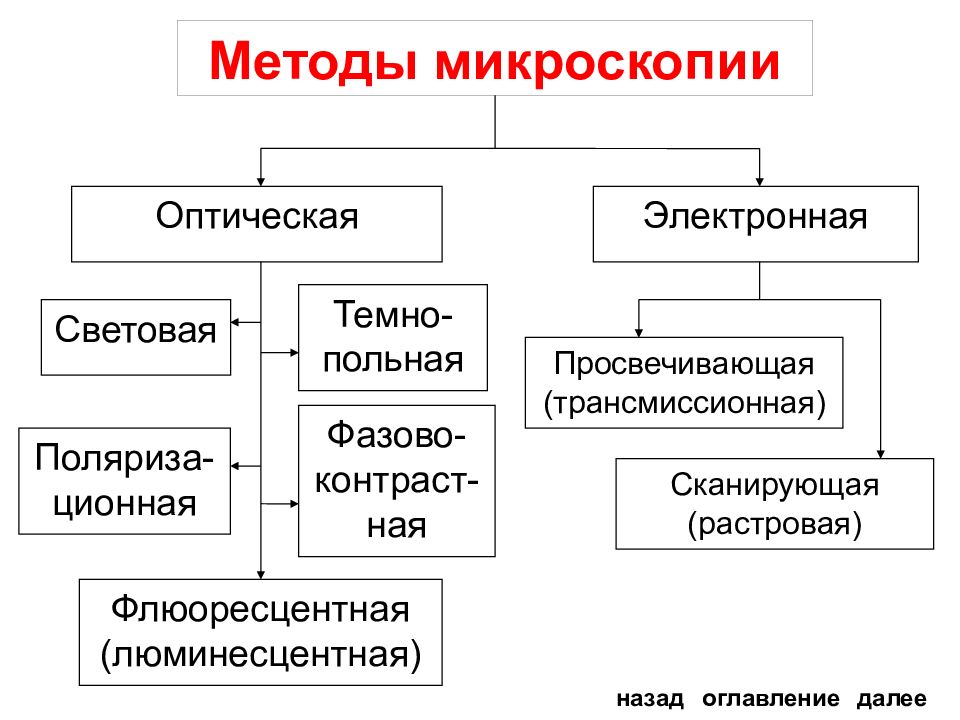
ЭЛЕКТРОННАЯ МИКРОСКОПИЯ ТРАНСМИССИОННАЯ МИКРОСКОПИЯ СКАНИРУЮЩАЯ МИКРОСКОПИЯ
Слайд 6
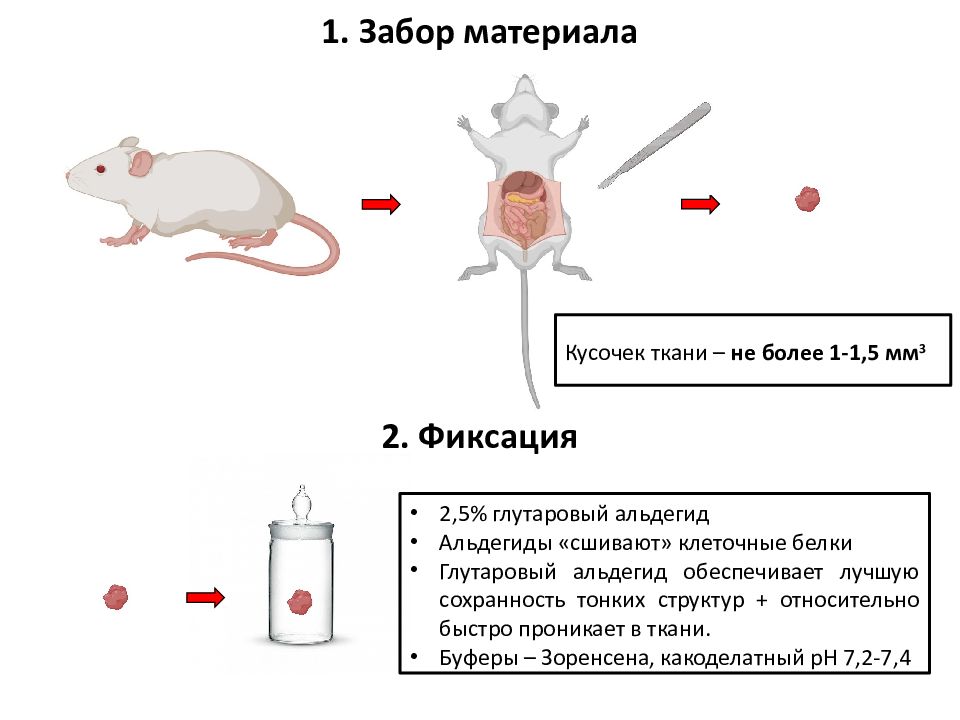
1. Забор материала 2. Фиксация Кусочек ткани – не более 1-1,5 мм 3 2,5% глутаровый альдегид Альдегиды «сшивают» клеточные белки Глутаровый альдегид обеспечивает лучшую сохранность тонких структур + относительно быстро проникает в ткани. Буферы – Зоренсена, какоделатный pH 7,2-7,4
Слайд 7
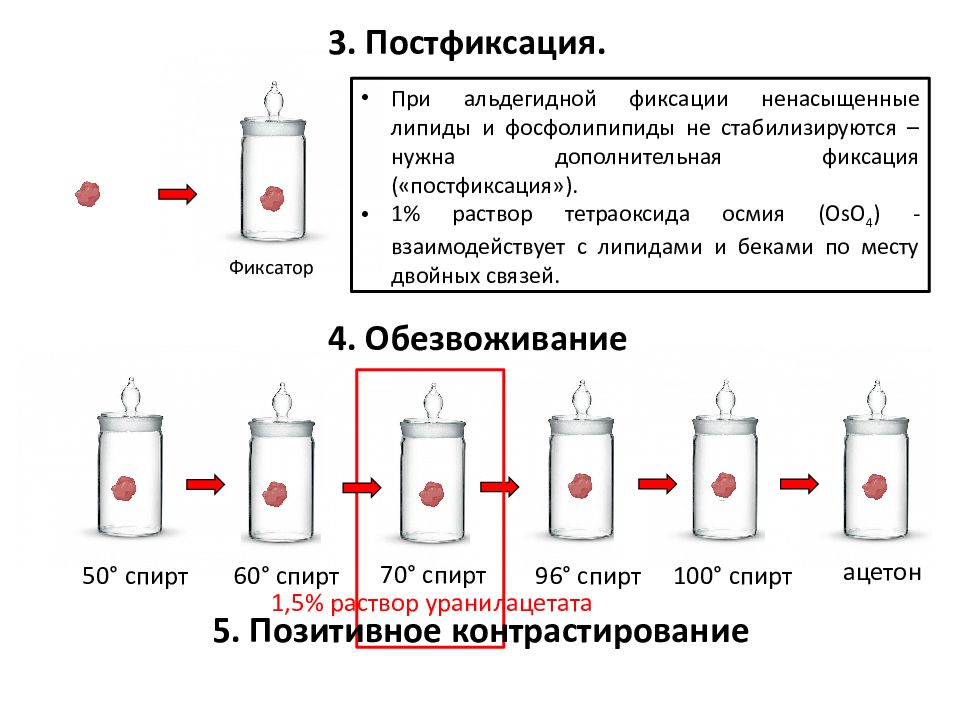
70 ° спирт 96 ° спирт 100 ° спирт ацетон Фиксатор 3. Постфиксация. При альдегидной фиксации ненасыщенные липиды и фосфолипипиды не стабилизируются – нужна дополнительная фиксация (« постфиксация »). 1 % раствор тетраоксида осмия ( OsO 4 ) - взаимодействует с липидами и беками по месту двойных связей. 6 0 ° спирт 50 ° спирт 1,5% раствор уранилацетата 5. Позитивное контрастирование 4. Обезвоживание
Слайд 8
6. Пропитывание ткани заливочной смесью ацетон/ эпон =3:1→ ацетон/ эпон =1:1 → ацетон/ эпон =1:3 7. Заливка материала Эпоксидные смолы, эпон капсулы с заливочным эпоном → термостат 37° С → термостат в 60 ° С (полимеризация)
Слайд 9
8. Резка материала на ультратоме электронный пучок не проникает сквозь срезы, толщина которых значительно превышает 100 нм ; в толстом срезе компоненты перекрывают друг друга и видны менее четко. → тонкие срезы 50-100 нм
Слайд 10
сеточки бленды Помещение срезов на сеточки и бленды 9. Контрастирование ( уранилацетат, затем цитрат свинца по методу Рейнольдса )
Слайд 11
Трансмиссионная электронная микроскопия фиксация глутаровым альдегидом – дает отличную сохранность тканей; промывка буфером; дофиксация четырехокисью осмия (+контрастирование ); 50 ° спирт; 60 ° спирт; 70 ° спирт с уранилацетатом ; 80 ° спирт; 96 ° спирт; 100 ° спирт; ацетон; ацетон:эпон =3:1; ацетон:эпон =1:1; ацетон:эпон =1:3; эпон (эпоксидная смола); 37 ° ; 60 ° ; затачивание пирамидки; изготовление ультратонких срезов 60-80 нм на ультрамикротоме; помещение срезов на бленды или сеточки с формваром ; контрастирование ( уранилацетат, затем цитрат свинца).
Слайд 12
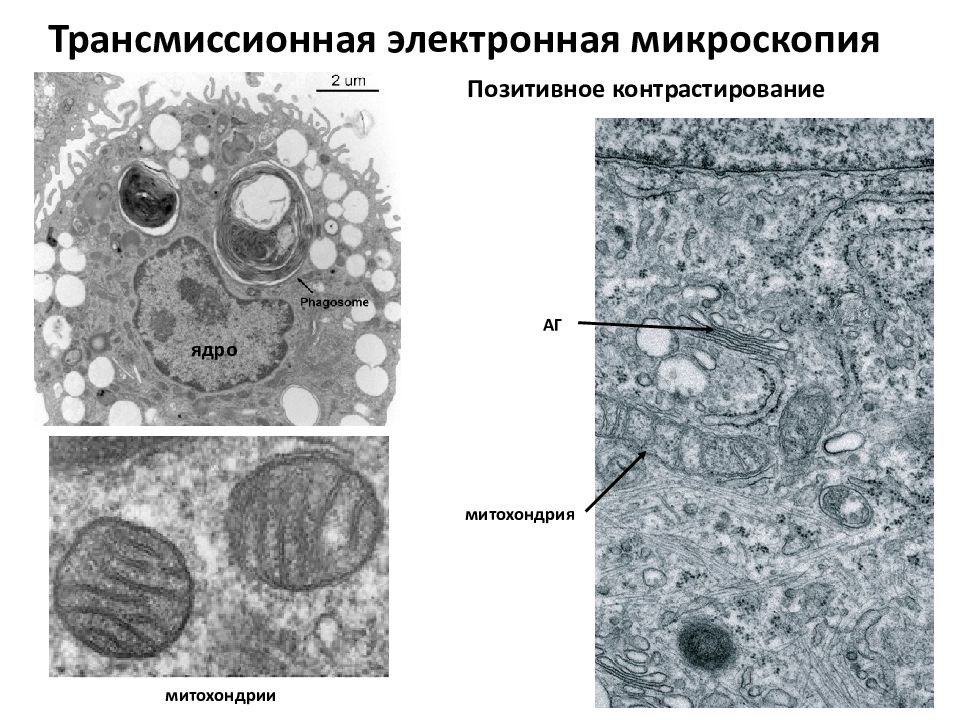
Трансмиссионная электронная микроскопия митохондрии митохондрия АГ ядро Позитивное контрастирование
Слайд 13
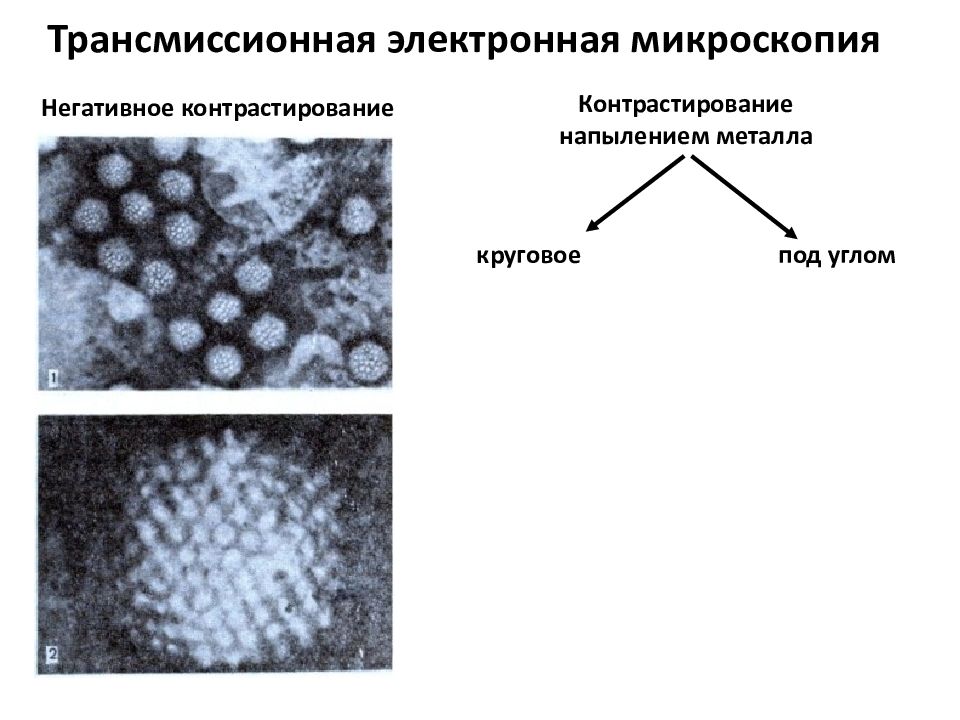
Трансмиссионная электронная микроскопия Негативное контрастирование Контрастирование напылением металла круговое под углом
Слайд 15
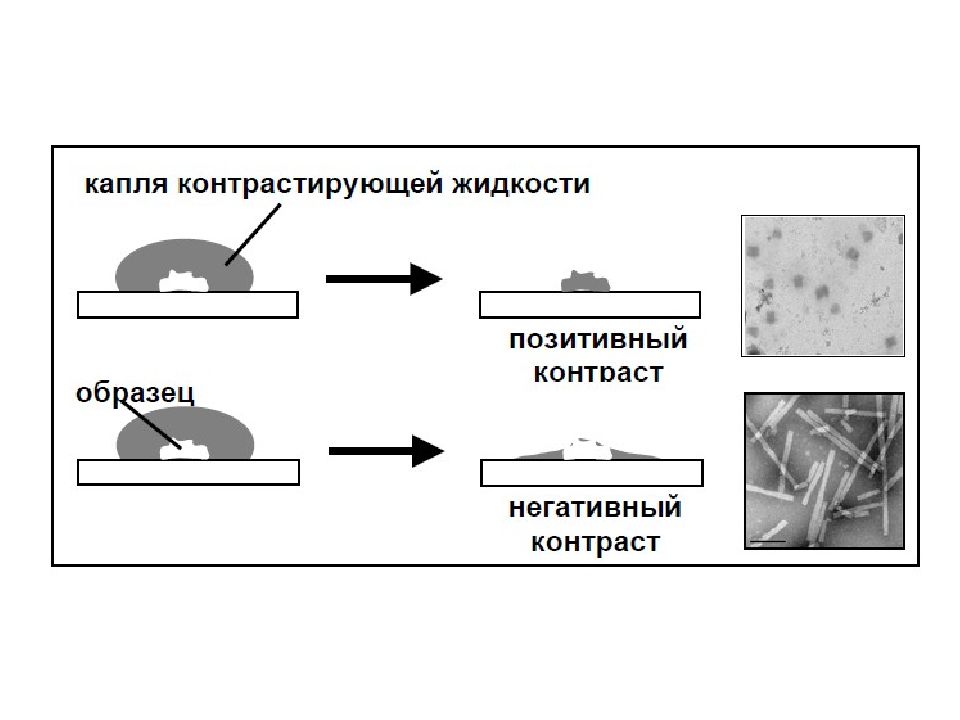
Негативное контрастирование Используют растворы солей тяжелых металлов ( уранилацетата, молибденокислый аммоний, фосфорно-вольфрамовая кислота – электронноплотные вещества) Объекты выглядят светлыми пятнами на темном фоне Плюсы Можно проникать вглубь объекта, выявлять дополнительные детали Минусы Плохо выявляются нитчатые молекулы из-за малой толщины
Слайд 16
Метод напыления Для напыления используют металлы, характеризующиеся низкой степенью окисления, и их сплавы (золото, медь, алюминий, платина). Напыление производят в специальной вакуумной камере путем нагрева и испарения металла в вакууме или «выбивания» атомов металла в результате действия ионов инертного газа. Атомы испаряющегося металла покрывают тонкой пленкой поверхность образца. Если объект имеет сложную конфигурацию, и металл не поникает во все углубления, контрастирование производят путем напыления углерода. Напыленный на ткань металл называется репликой.
Слайд 18
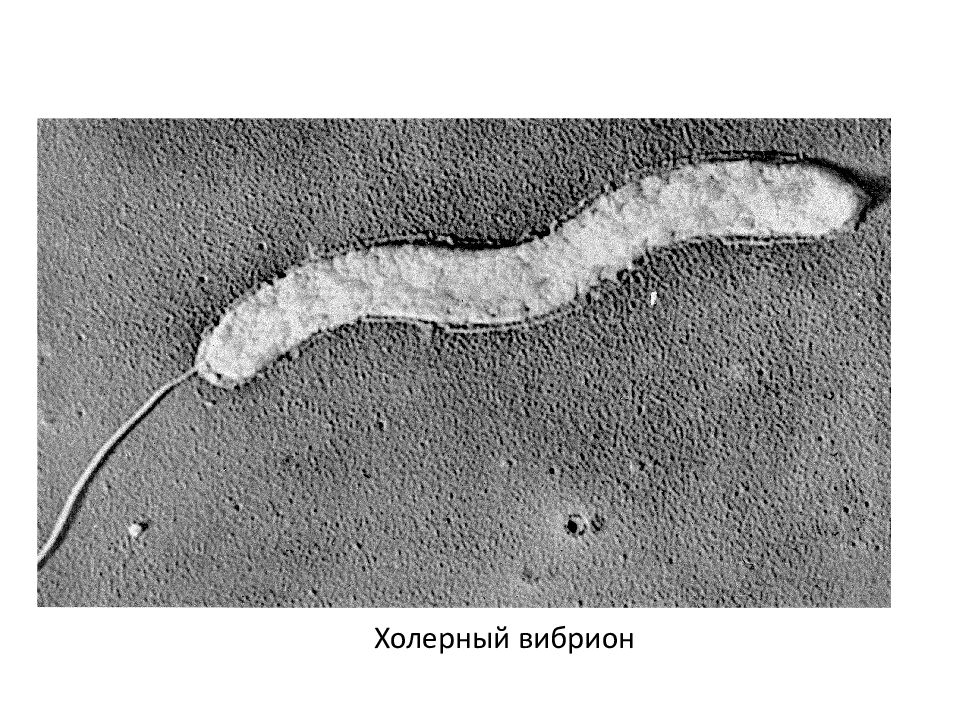
Оттенение металлами К онтраст реплике можно создать, напыляя под острым углом электронноплотное вещество, например, тяжелый металл. Термическое испарение металла металла Атомы металла встречаются с объектом и осаждаются на нем в виде слоя Там, где объект экранирует пучок частиц – «тень» Минусы: Увеличение размеров объекта на толщину напыленного слоя Дает представление только о внешнем виде и форме частиц h = lxtgθ θ - угол напыления, l - длина тени, h - высота объекта
Слайд 21
Сканирующая электронная микроскопия фиксация глутаровым альдегидом ; промывка буфером; 30 ° спирт; 50 ° спирт; 70 ° спирт; 80 ° спирт; 96 ° спирт; 100 ° спирт; 96 ° спирт:ацетон =3:1; 96 ° спирт:ацетон =1:1; 96 ° спирт:ацетон =1:3; ацетон; высушивание в критической точке; приклеивание образца к металлическому столику (лаком для ногтей); напыление (смесью Au - Pd (золото – палладий)).
Слайд 22
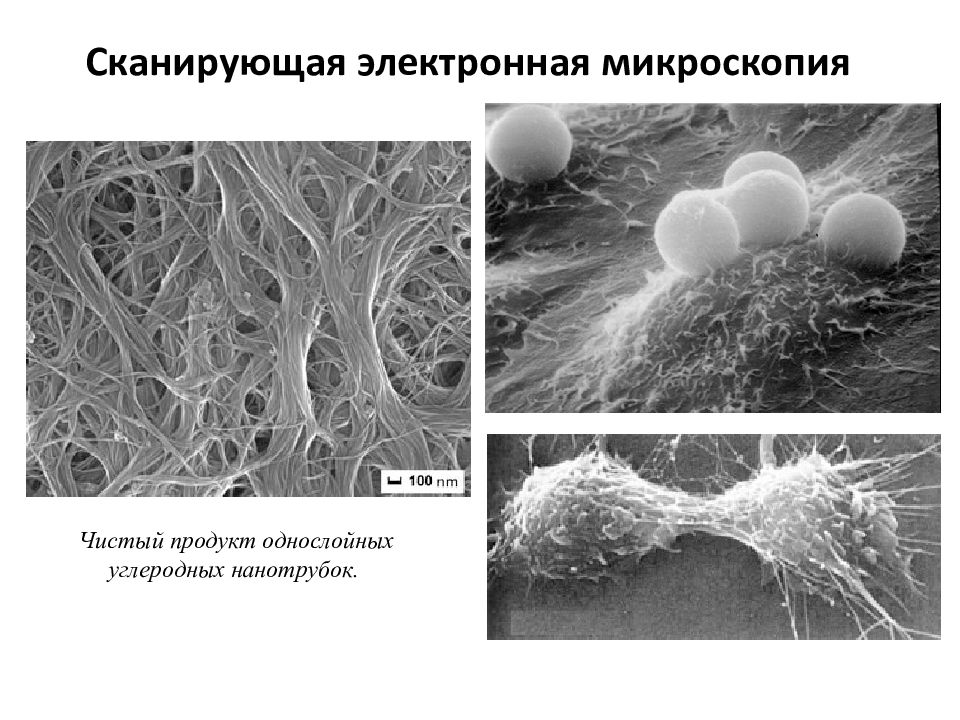
Сканирующая электронная микроскопия Чистый продукт однослойных углеродных нанотрубок.
Слайд 23
Замораживание-скалывание (травление) Пропитывание ткани криопротектором ( глицерин, ацетон, спирт, диметилсульфоксид, сахара, поливинилпирролидон, полиэтиленоксид ) Т кань подвергается быстрому замораживанию жидким азотом (-196°С ) Скол охлажденным ножом в специальной вакуумной установке В вакууме часть воды, перешедшей в стекловидную форму, возгоняется («травление»), а поверхность скола покрывается тонким слоем углерода, а затем металла ( Au, Cu, Pd ) При комнатном температуре ткань растворяют в кислотах, а реплика остается, ее смотрят в СЭМ