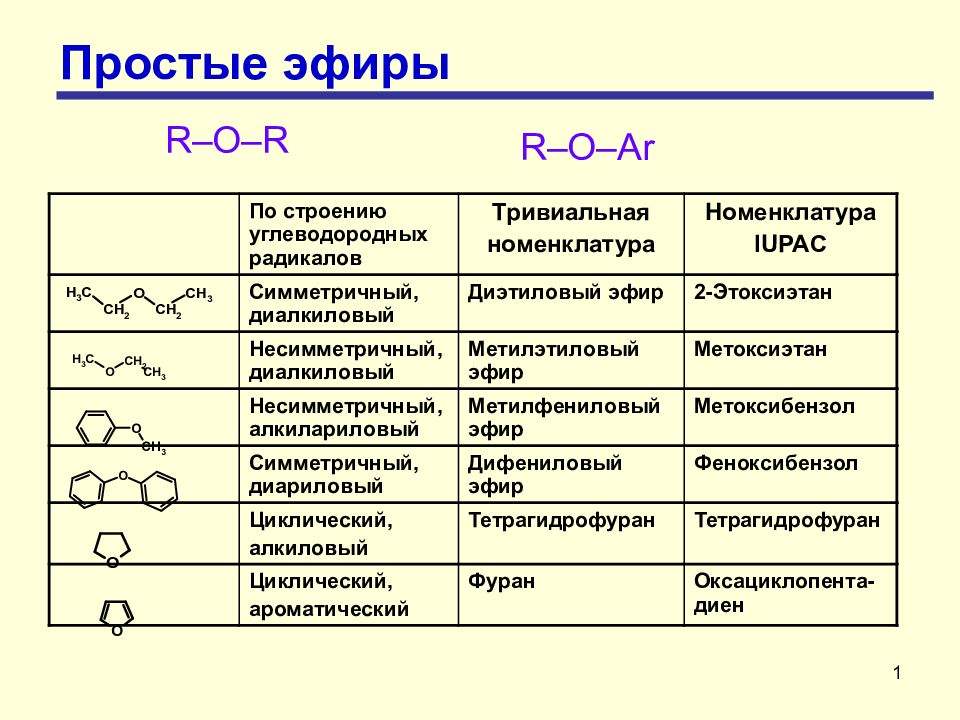
Слайд 3: Формирование углеродного скелета
Слайд 4: Формирование углеродного скелета
Реакции наращивания и укорочения углеродной цепи молекулы Формирование циклов
Слайд 5: Методы создания новых углерод-углеродных связей
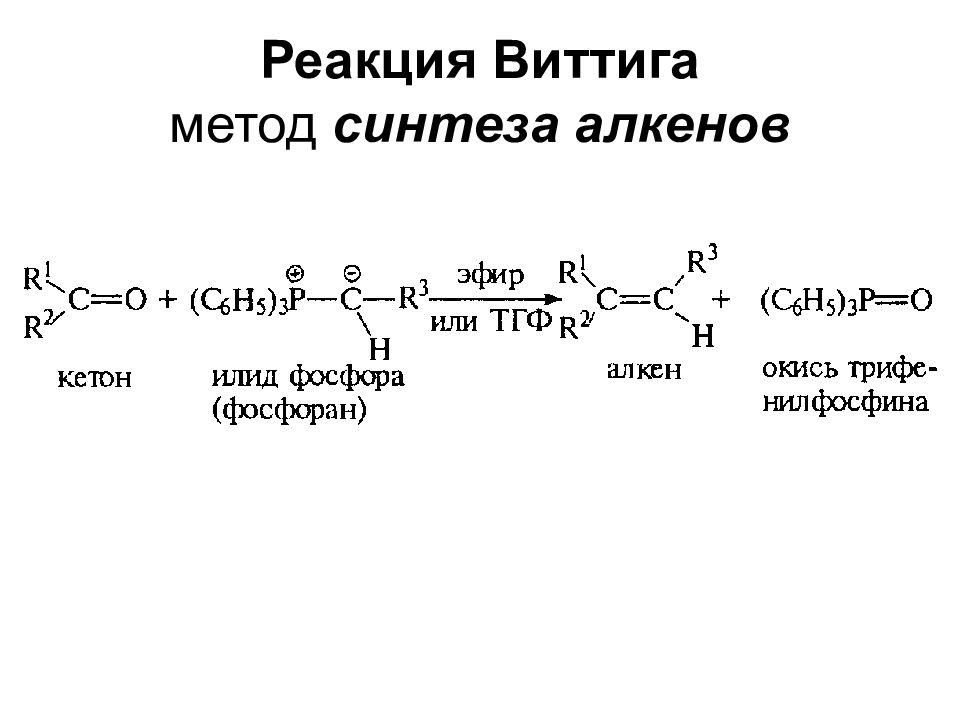
1) на базе металлоорганических соединений 2) на базе различных конденсаций 3) на базе перегруппировок 4) реакции циклоприсоединения
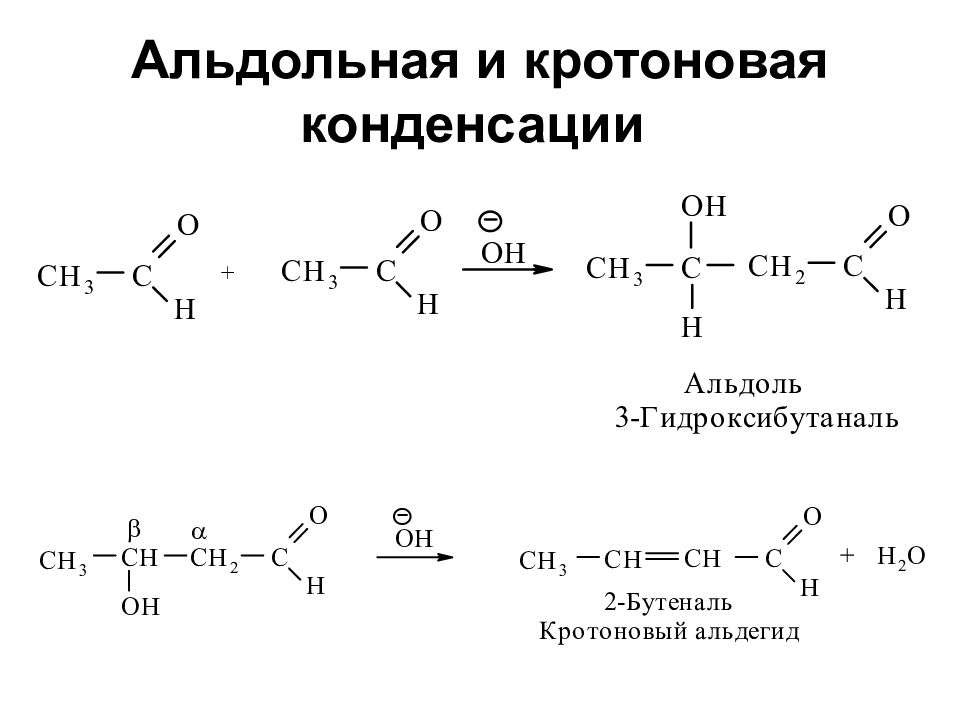
Слайд 6: Альдольная и кротоновая конденсации
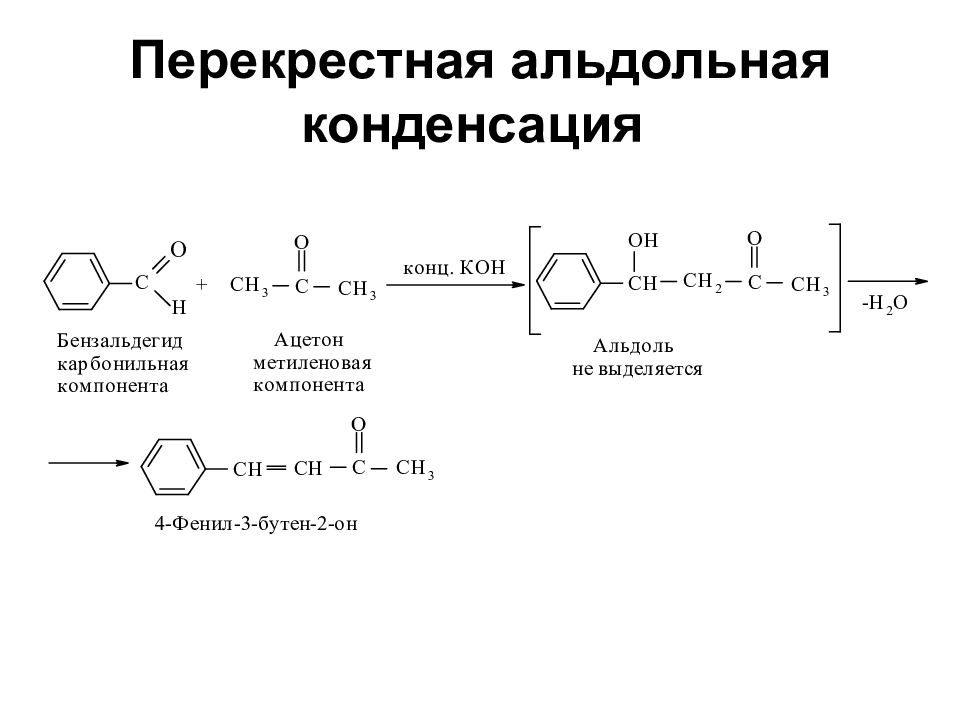
Слайд 7: Перекрестная альдольная конденсация
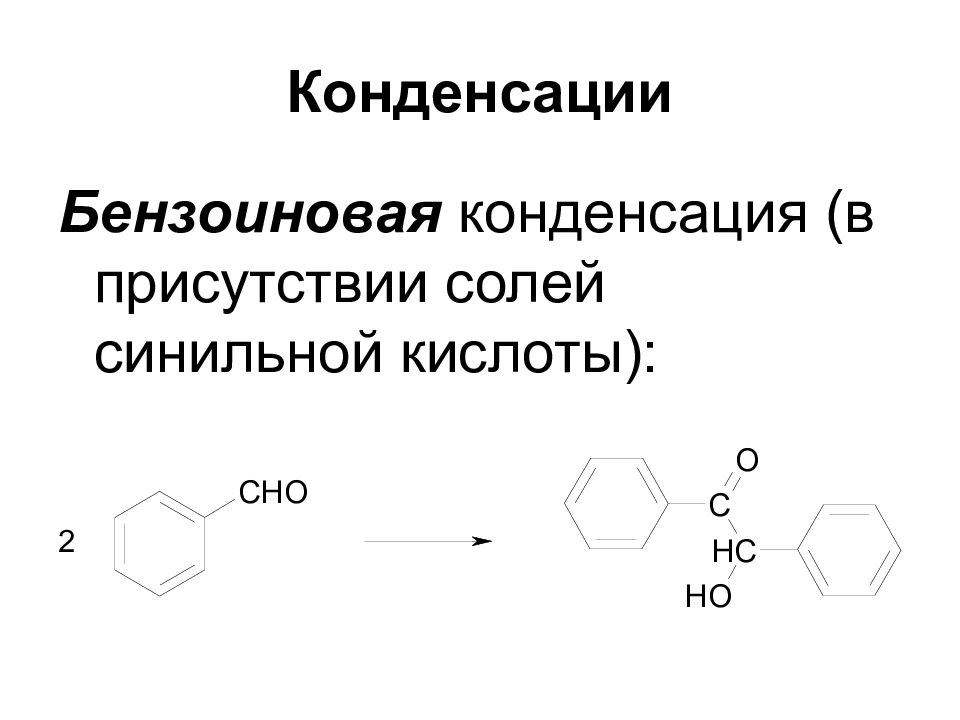
Слайд 8: Конденсации
Бензоиновая конденсация (в присутствии солей синильной кислоты):
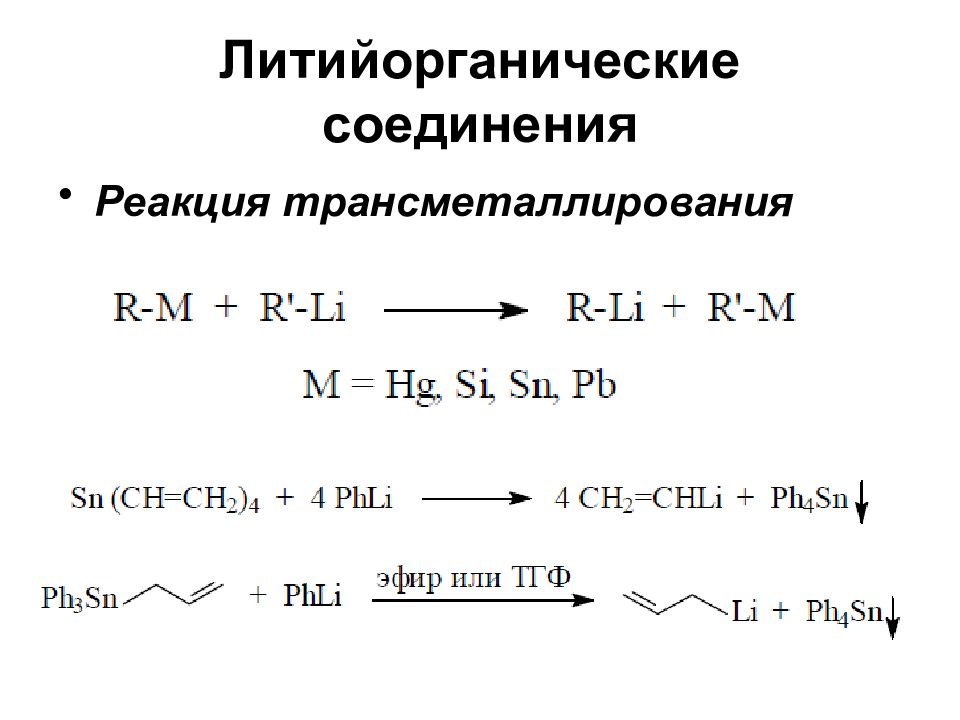
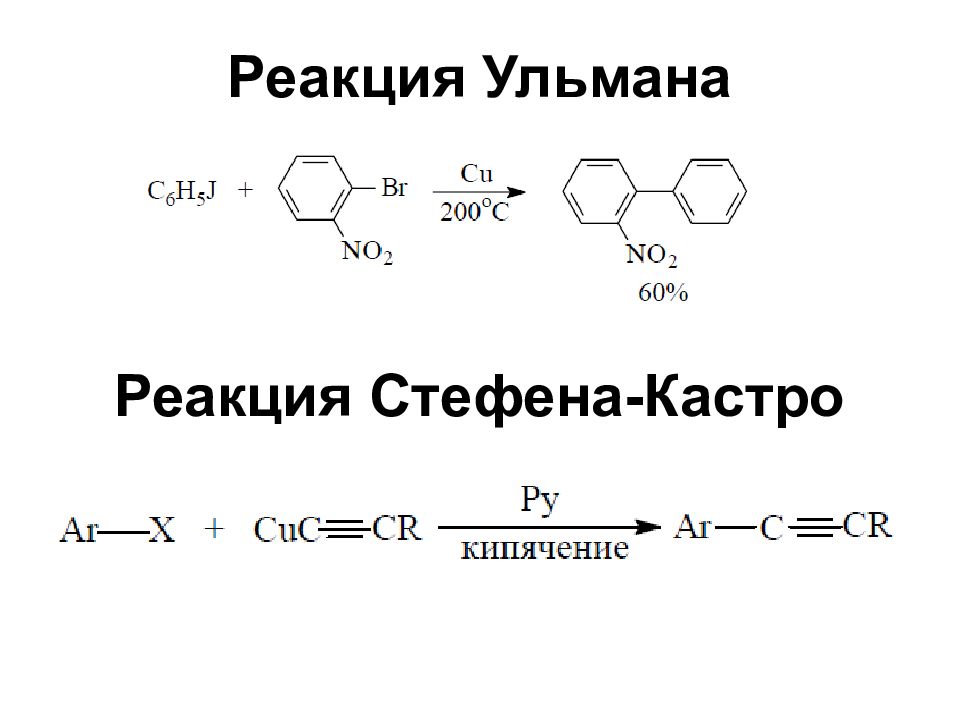
Слайд 11: Металлоорганические соединения
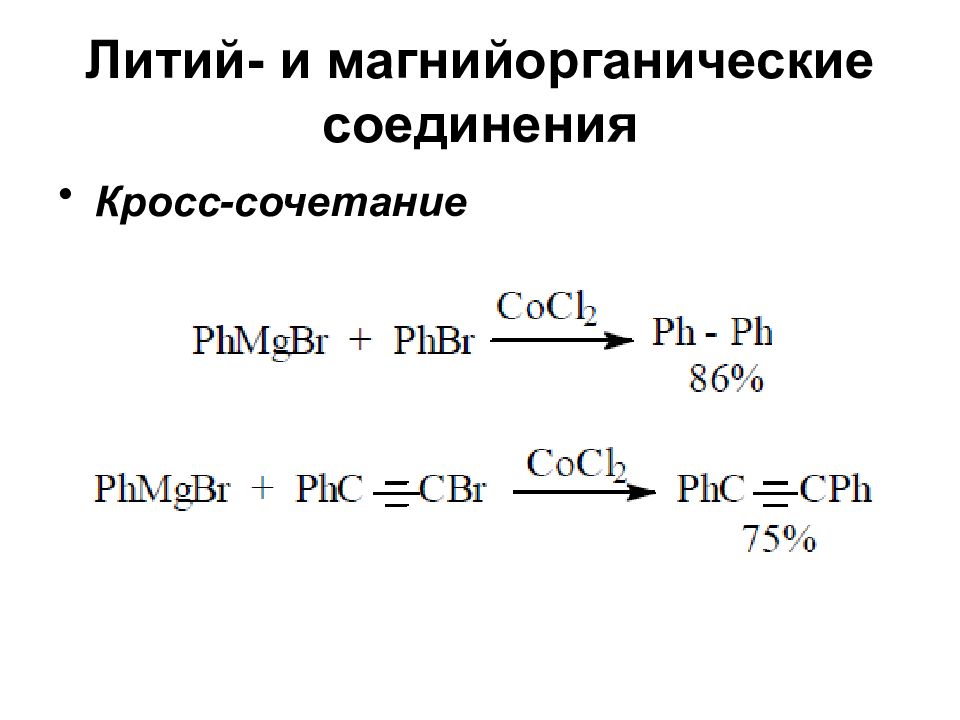
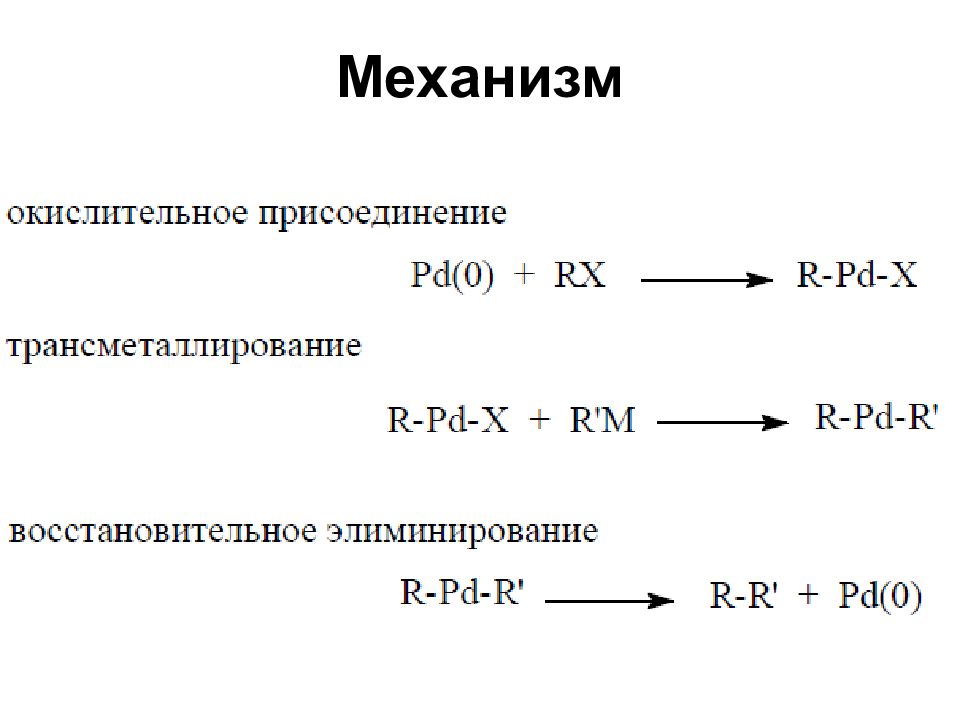
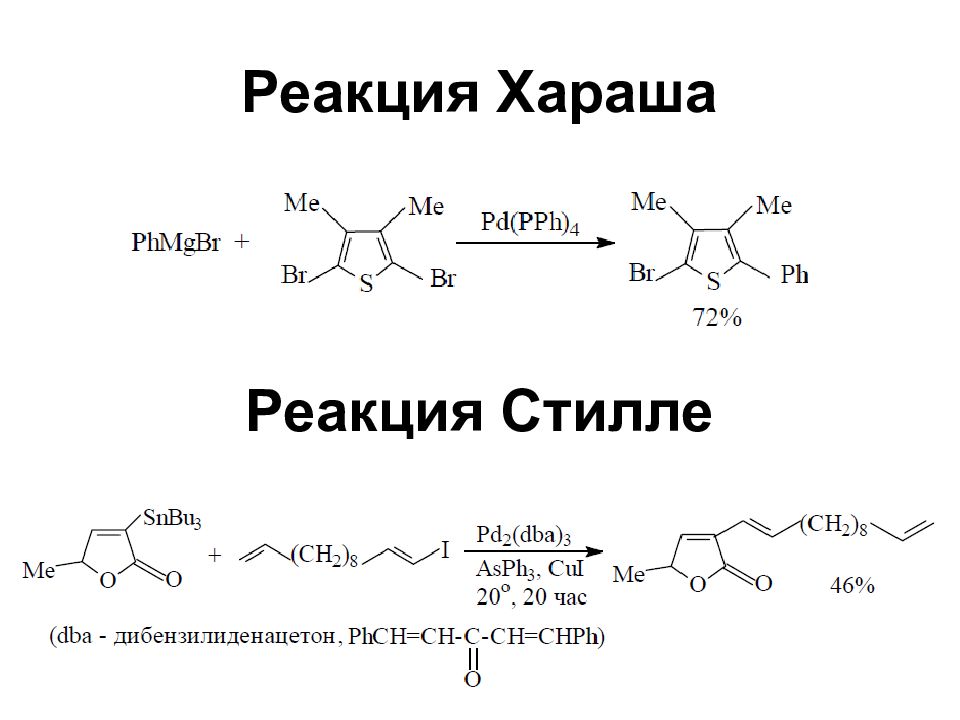
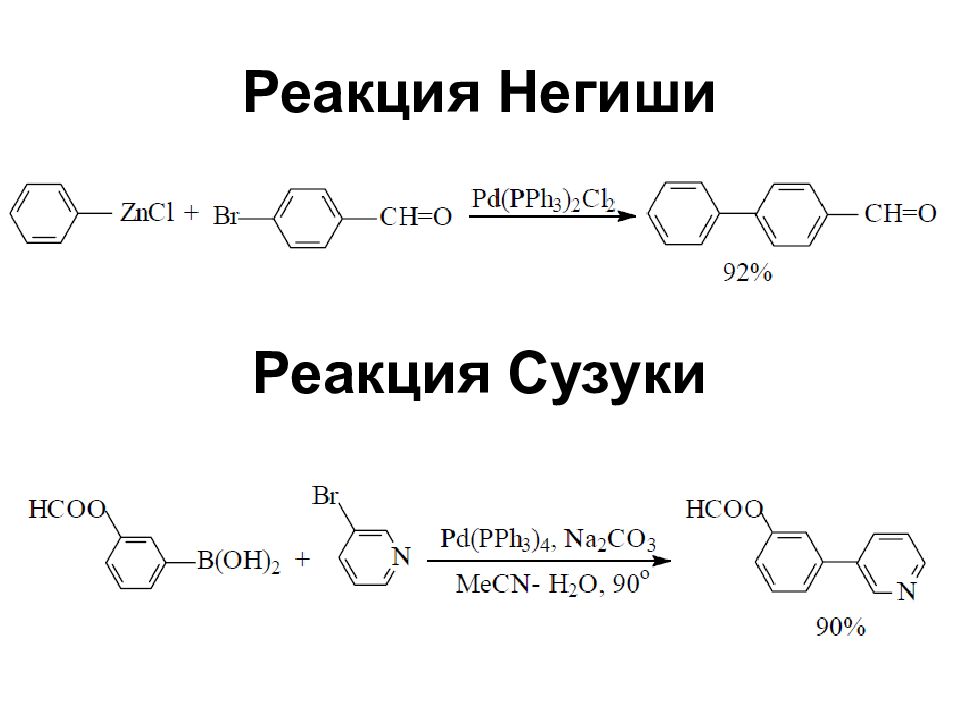
Литий-, магний-, медь-, титаноорганические соединения Реакции кросс-сочетания, катализируемые комплексами палладия
Слайд 12: Реакция Вюрца
Удовлетворительные результаты только для первичных алкилгалогенидов, третичные - продукты элиминирования
Слайд 14: Магнийорганические соединения
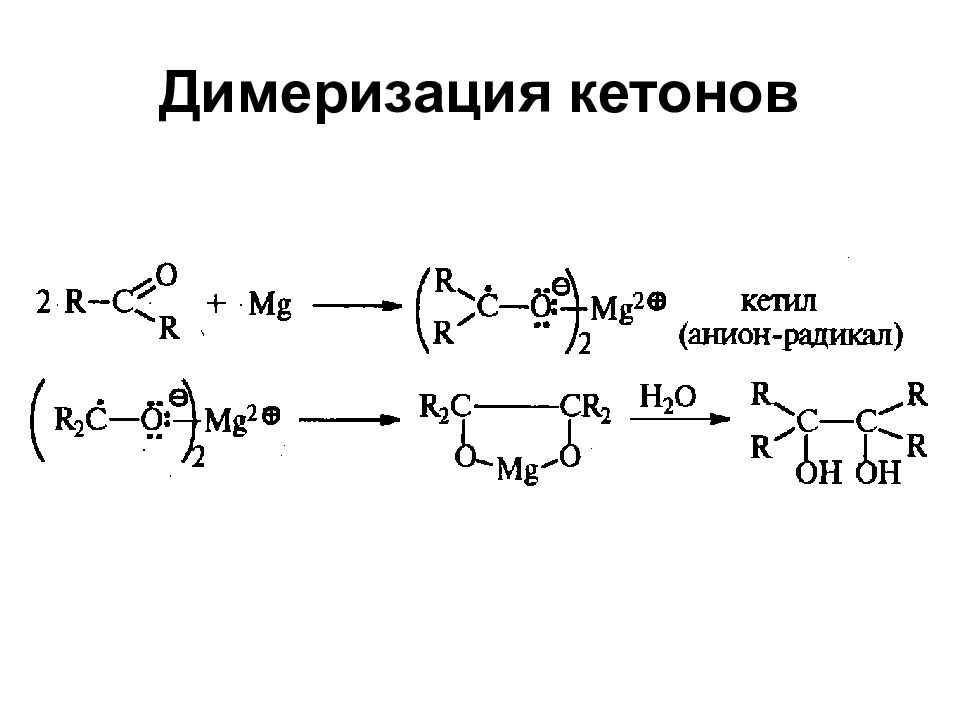
Две стадии : 1) взаимодействие алкилгалогенида с металлическим магнием в эфире 2) действие полученного магниевого реагента на карбонильное соединение
Слайд 16: Магнийорганические соединения
Первое сообщение о таком варианте проведения реакции появилось в 1900 году В.Гриньяр показал, что этот метод имеет общее значение Реакция получила название реакции Гриньяра, а ее автор был удостоен Нобелевской премии по химии в 1912 году
Слайд 17: Магнийорганические соединения
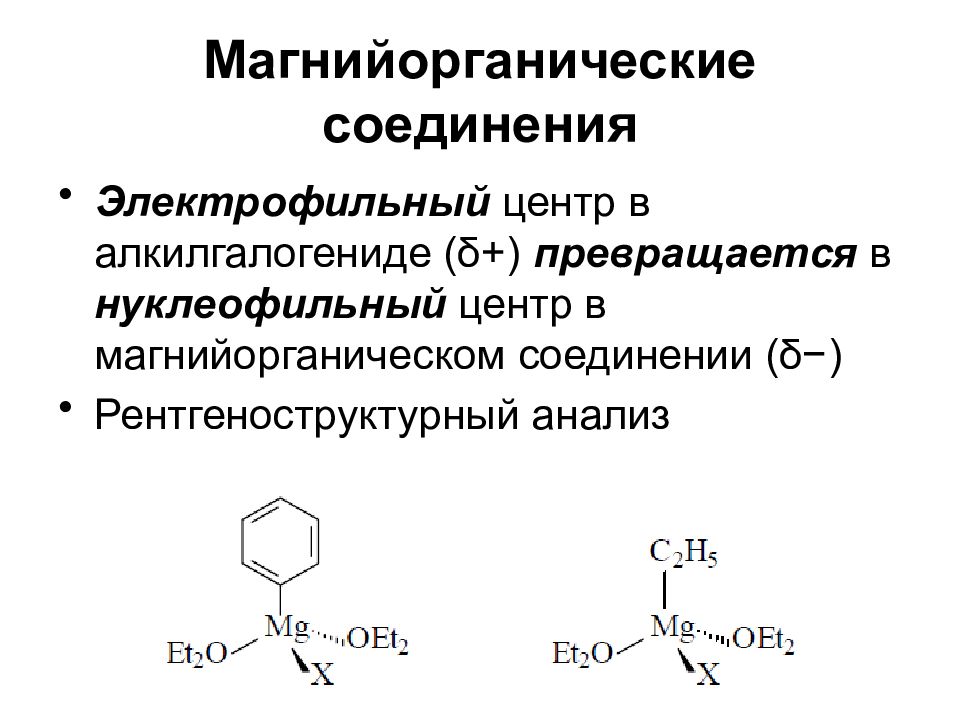
Электрофильный центр в алкилгалогениде (δ+) превращается в нуклеофильный центр в магнийорганическом соединении (δ−) Рентгеноструктурный анализ
Слайд 18: Магнийорганические соединения
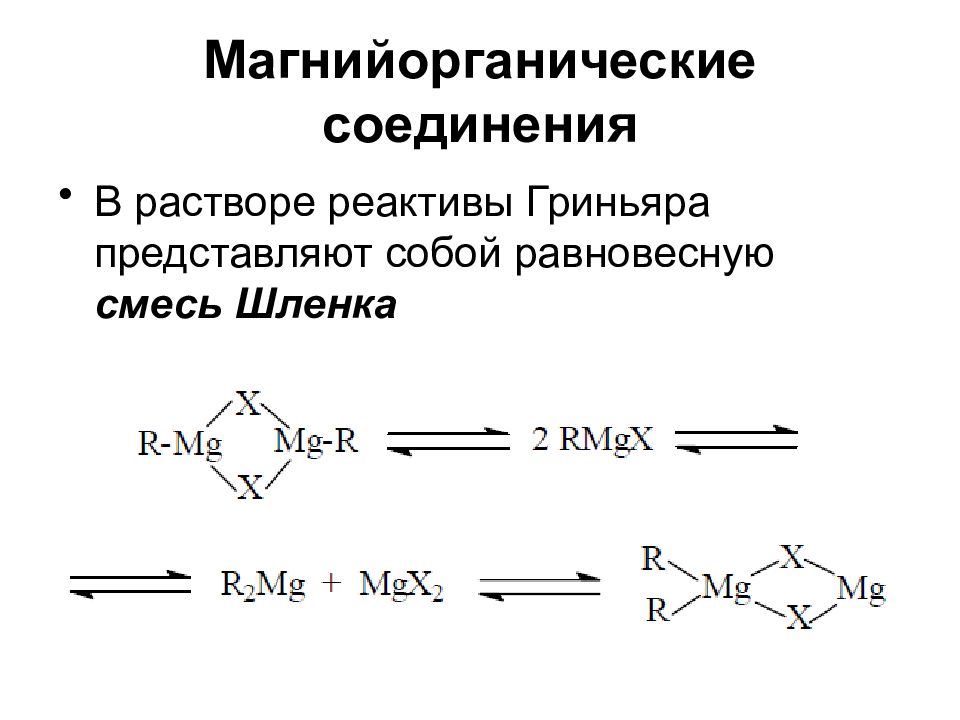
В растворе реактивы Гриньяра представляют собой равновесную смесь Шленка
Слайд 19: Магнийорганические соединения
Реактивы Гриньяра можно получить, исходя из первичных, вторичных и третичных алкилгалогенидов, а также из арилгалогенидов Для получения RMgX чаще всего используются бромиды R-Br, ArBr и иодиды RI, ArI, но могут быть использованы и хлориды RCl, ArCl
Слайд 20: Магнийорганические соединения
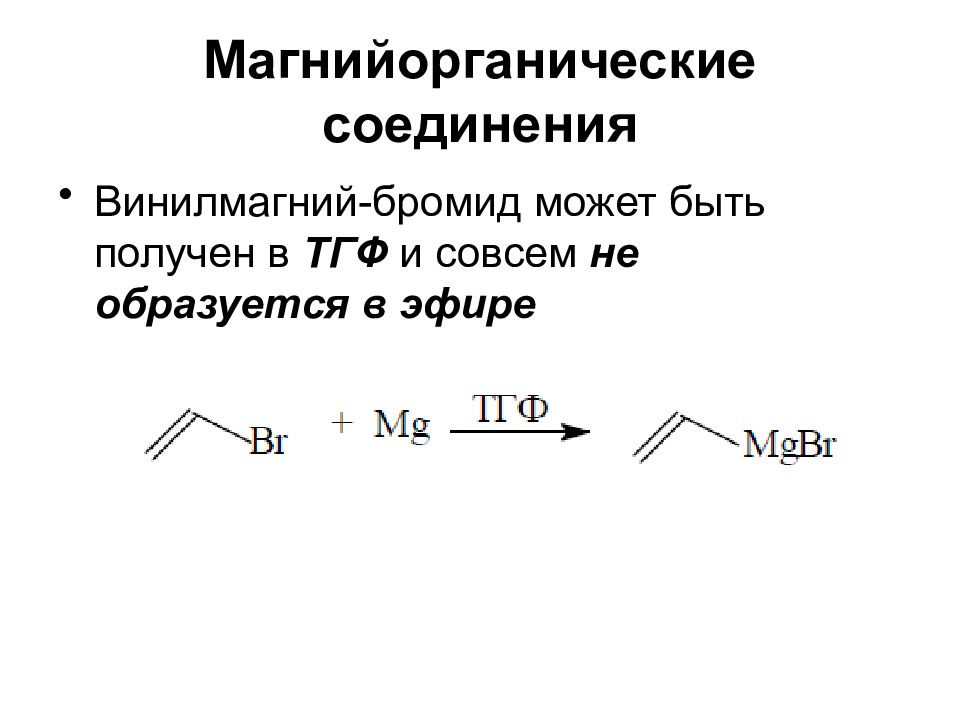
Винилмагний-бромид может быть получен в ТГФ и совсем не образуется в эфире
Слайд 21: Магнийорганические соединения
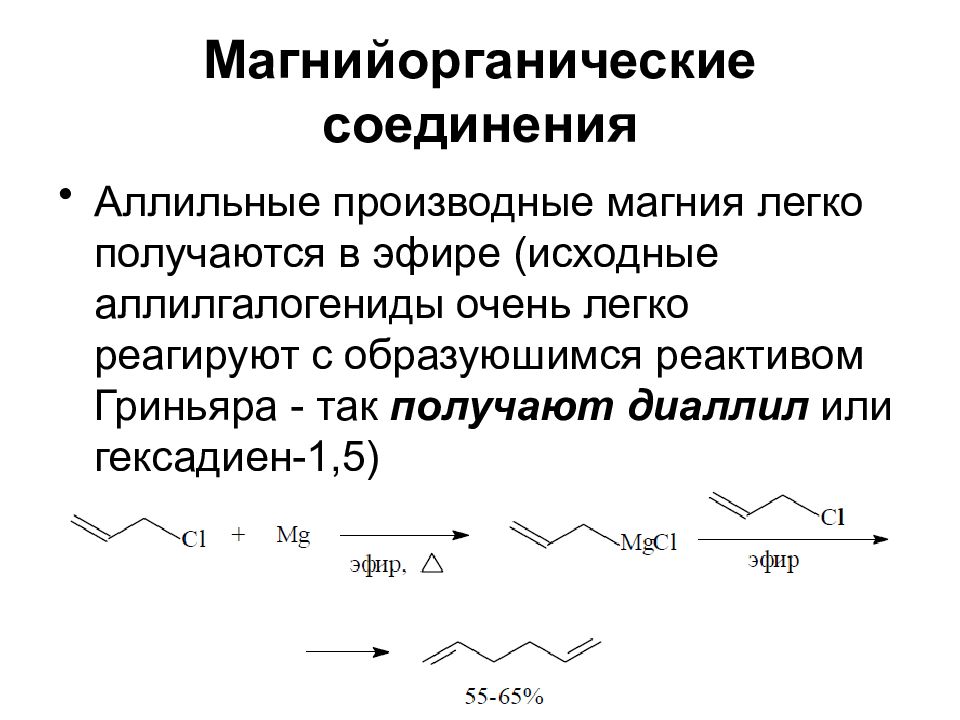
Аллильные производные магния легко получаются в эфире (исходные аллилгалогениды очень легко реагируют с образуюшимся реактивом Гриньяра - так получают диаллил или гексадиен-1,5)
Слайд 22: Магнийорганические соединения
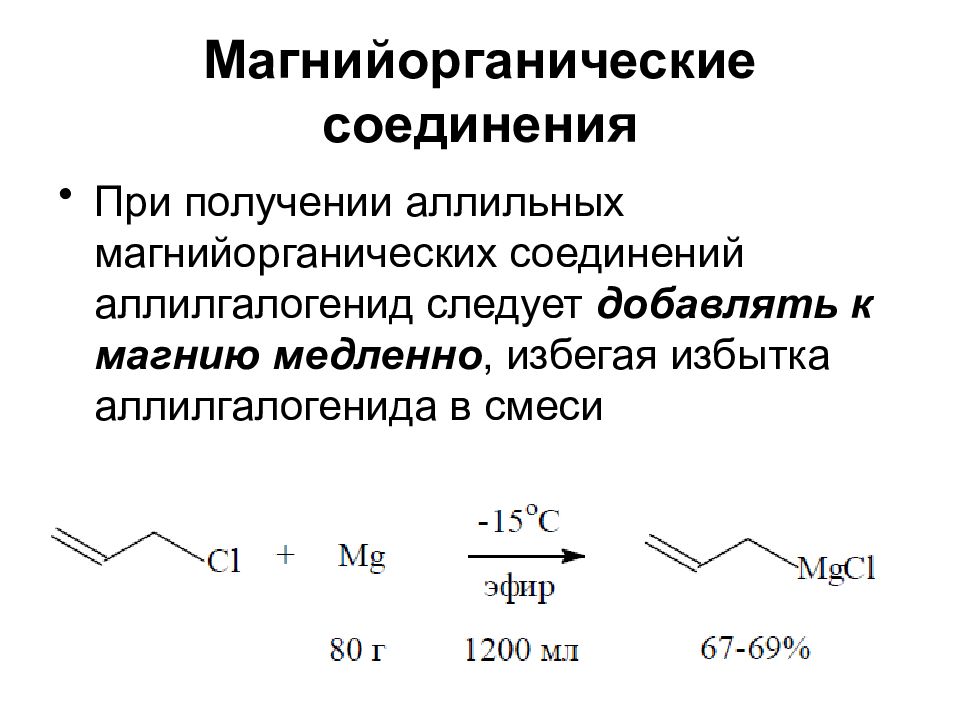
При получении аллильных магнийорганических соединений аллилгалогенид следует добавлять к магнию медленно, избегая избытка аллилгалогенида в смеси
Слайд 23: Магнийорганические соединения
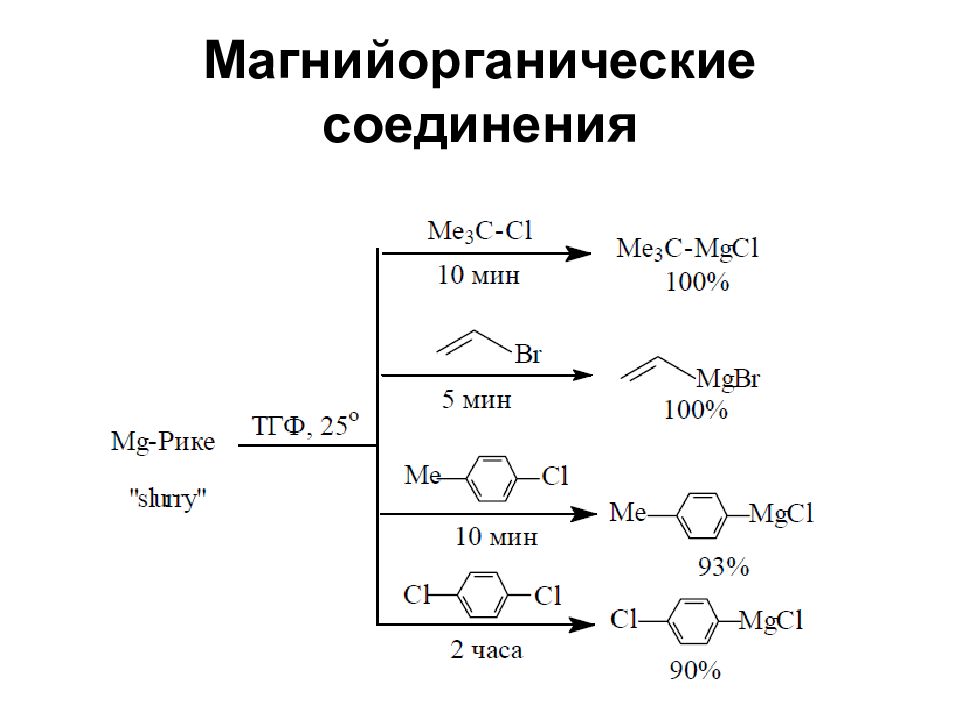
Если органогалогенид мало реакционноспособен, целесообразно использовать высоко реакционноспособный магний (магний Рике ), который получают
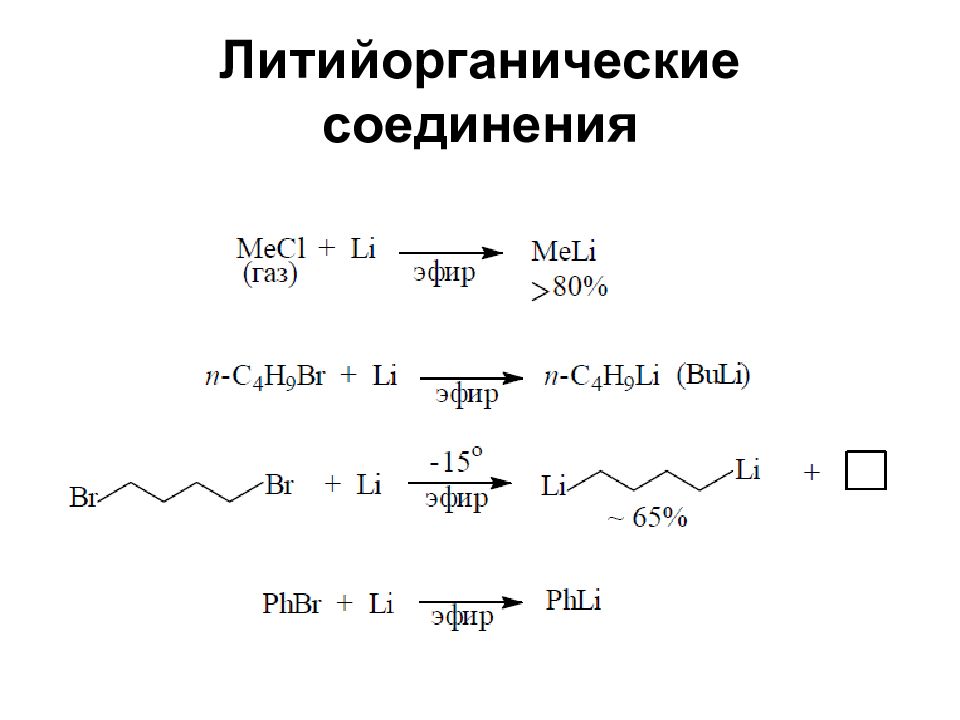
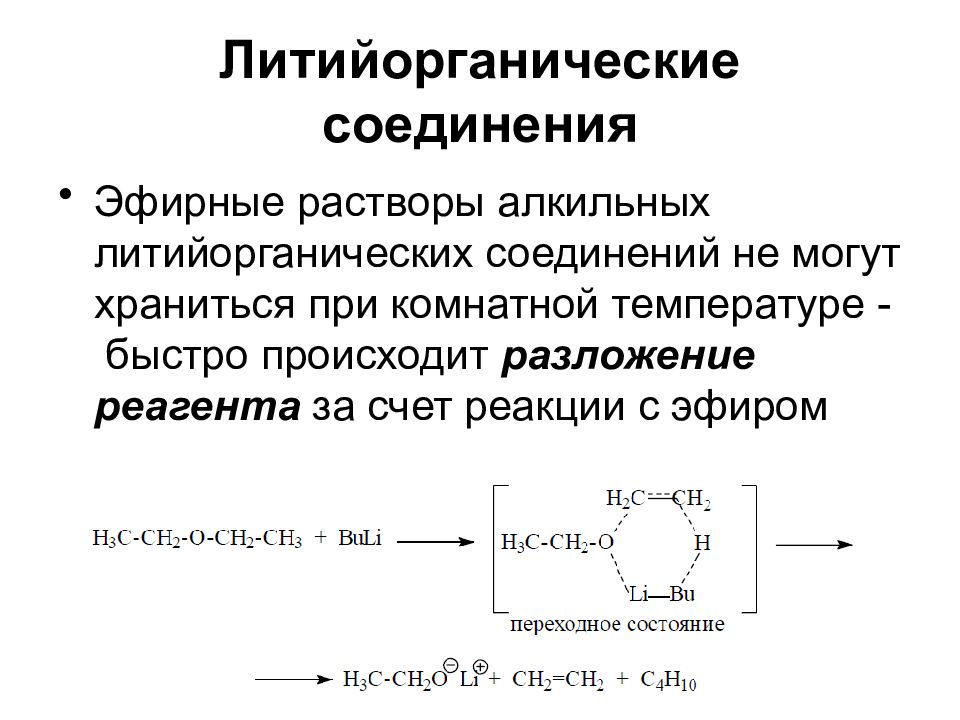
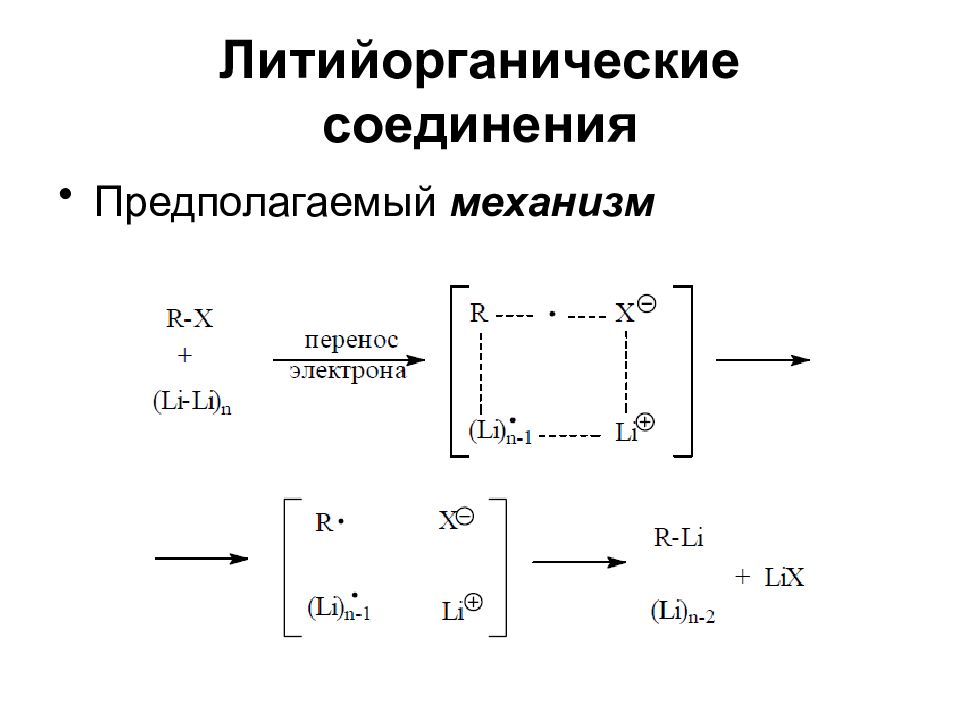
Слайд 26: Литийорганические соединения
Эфирные растворы алкильных литийорганических соединений не могут храниться при комнатной температуре - быстро происходит разложение реагента за счет реакции с эфиром
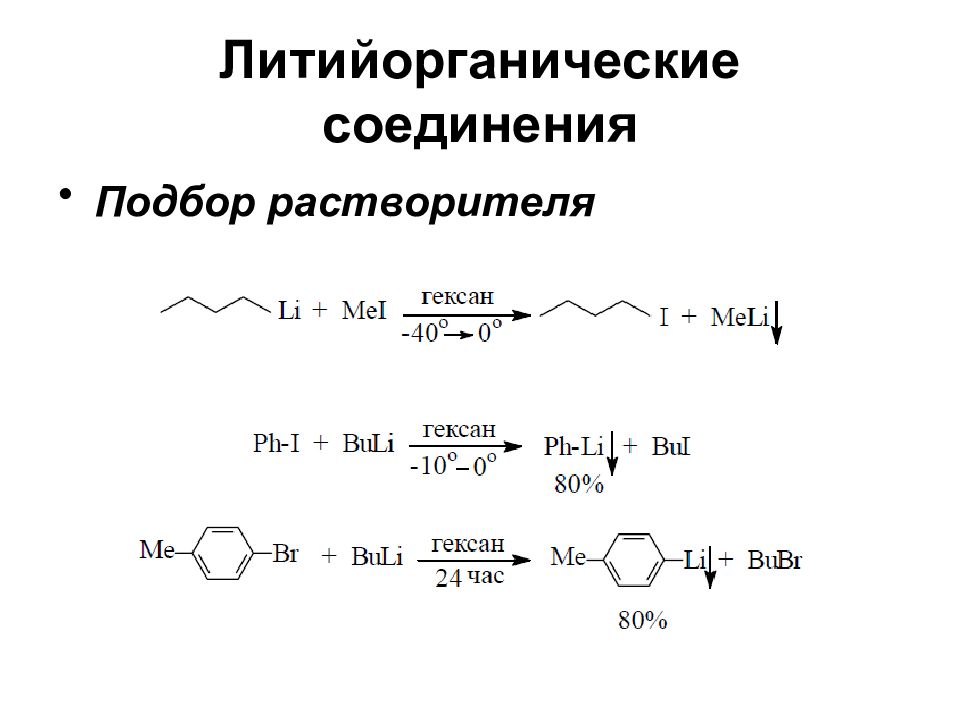
Слайд 27: Литийорганические соединения
Синтез алкиллитиевых соединений с успехом можно вести, используя в качестве растворителей алканы
Слайд 29: Литийорганические соединения
Широко используемый метод синтеза литийорганических соединений
Слайд 31: Литийорганические соединения
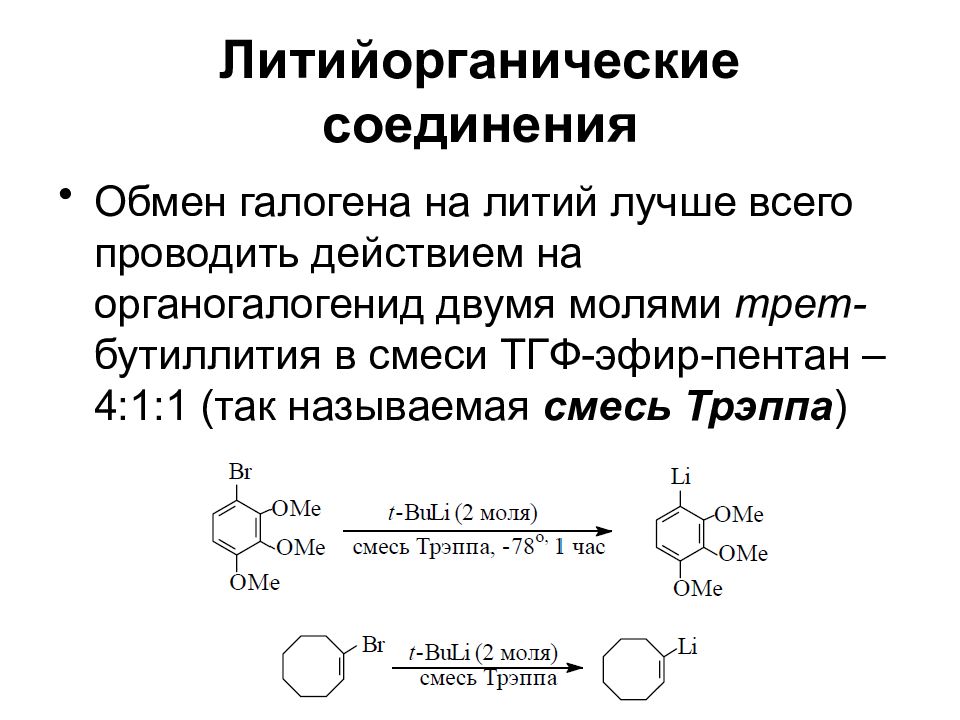
Обмен галогена на литий лучше всего проводить действием на органогалогенид двумя молями трет- бутиллития в смеси ТГФ-эфир-пентан – 4:1:1 (так называемая смесь Трэппа )
Слайд 32: Литийорганические соединения
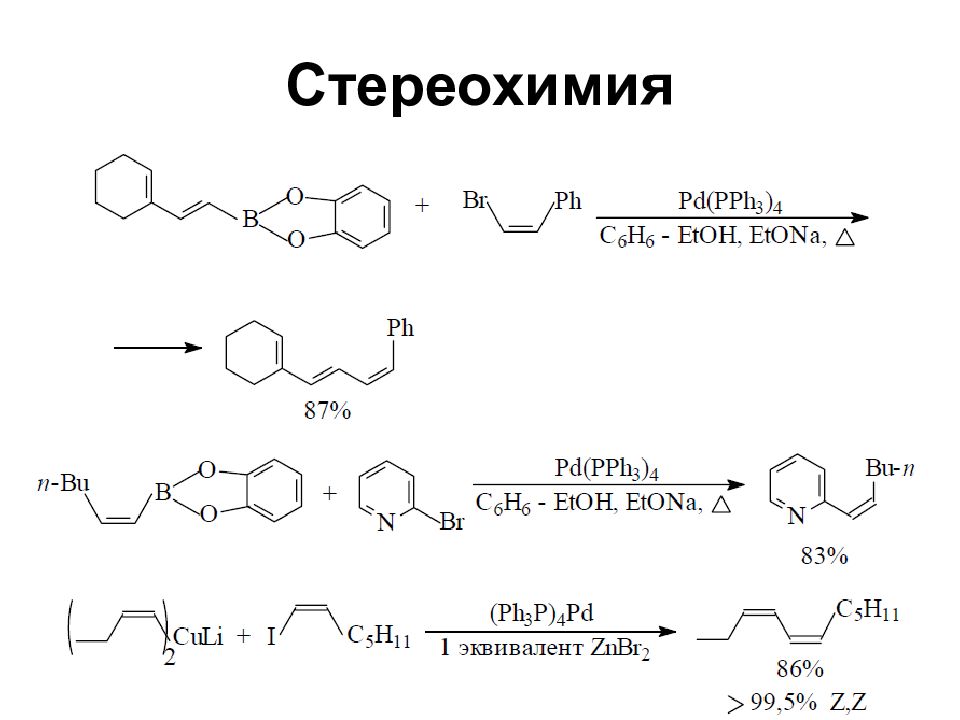
При получении винильных литийорганических соединений таким путем важным моментом является сохранение стереохимической конфигурации двойной связи
Слайд 34: Литийорганические соединения
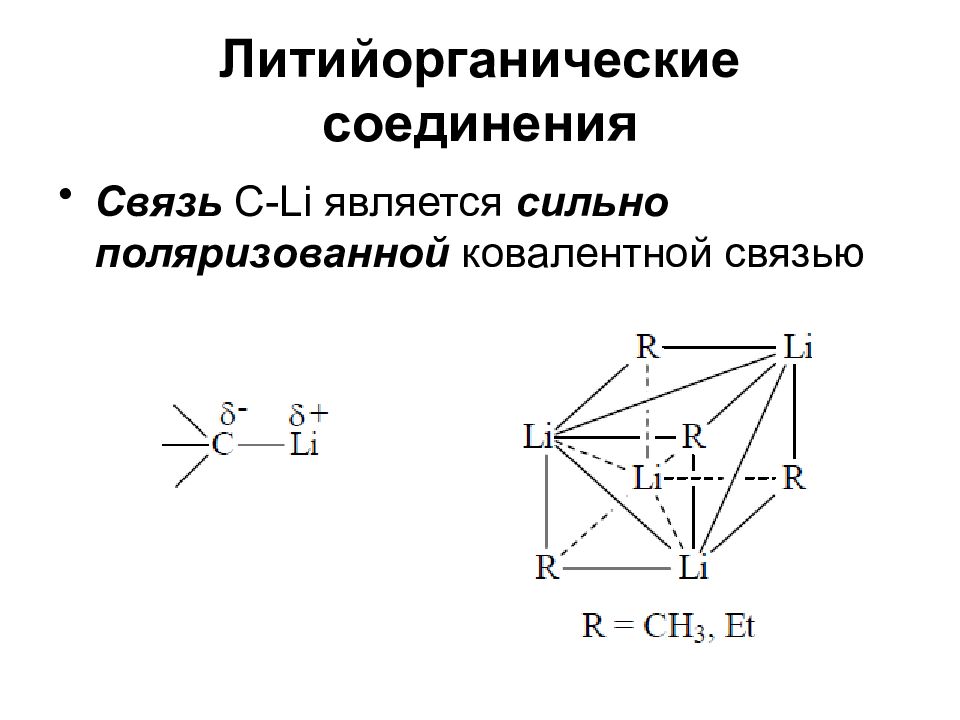
Связь C-Li является сильно поляризованной ковалентной связью
Слайд 35: Литийорганические соединения
Чем больше донорная способность растворителя, тем меньше степень ассоциации RLi: этиллитий гексамерный в гексане в эфире образует димеры Степень ассоциации RLi меняется при добавлении лигандов, способных давать хелаты с атомом Li
Слайд 36: Литийорганические соединения
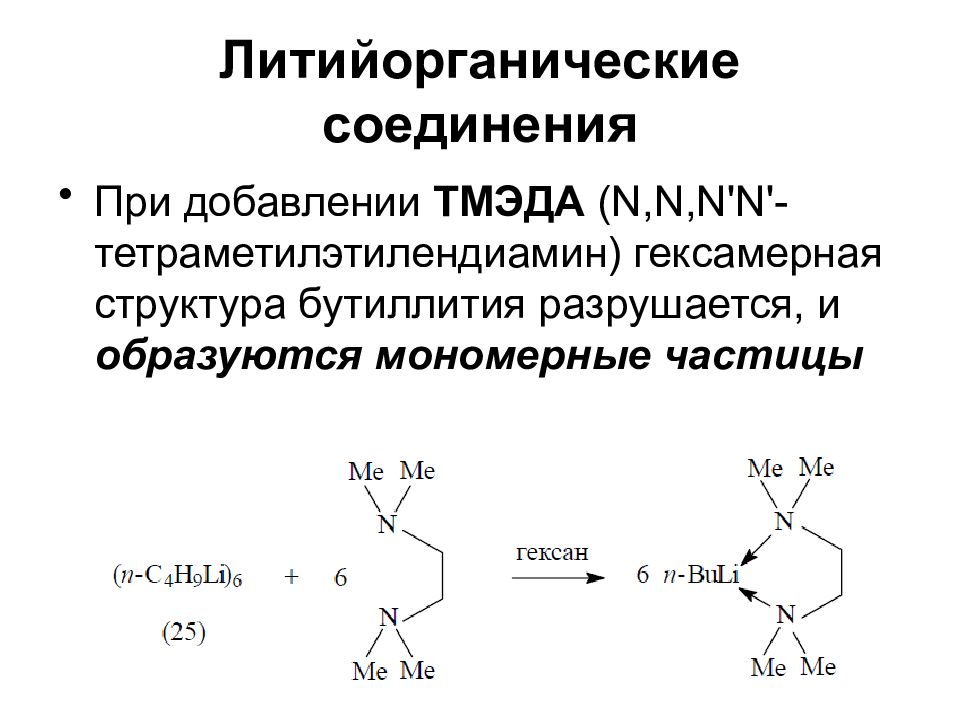
При добавлении ТМЭДА (N,N,N'N'-тетраметилэтилендиамин) гексамерная структура бутиллития разрушается, и образуются мономерные частицы
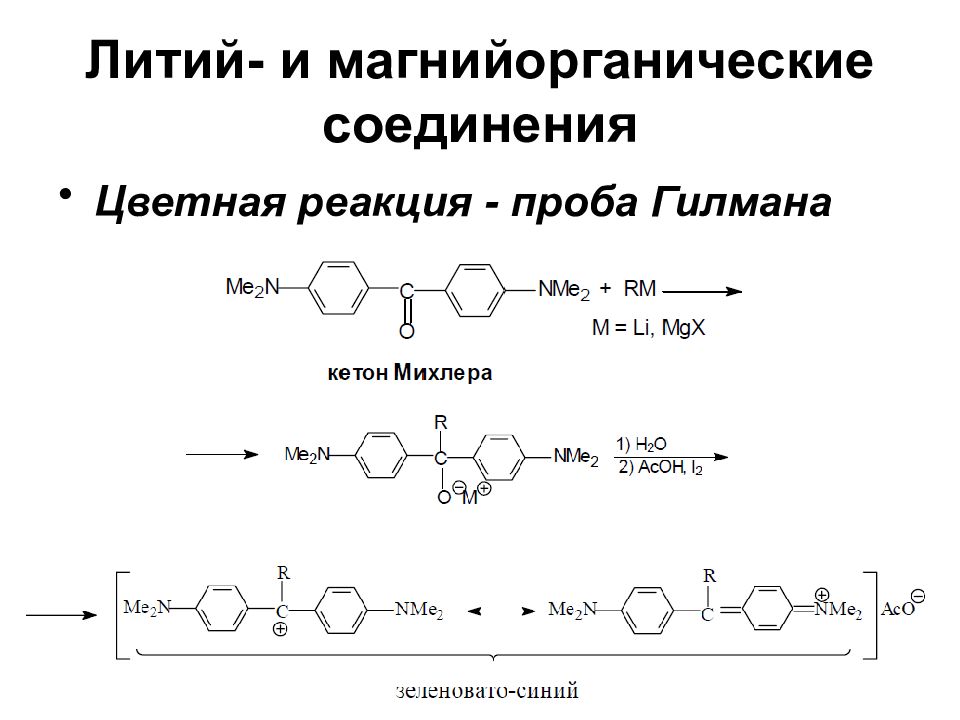
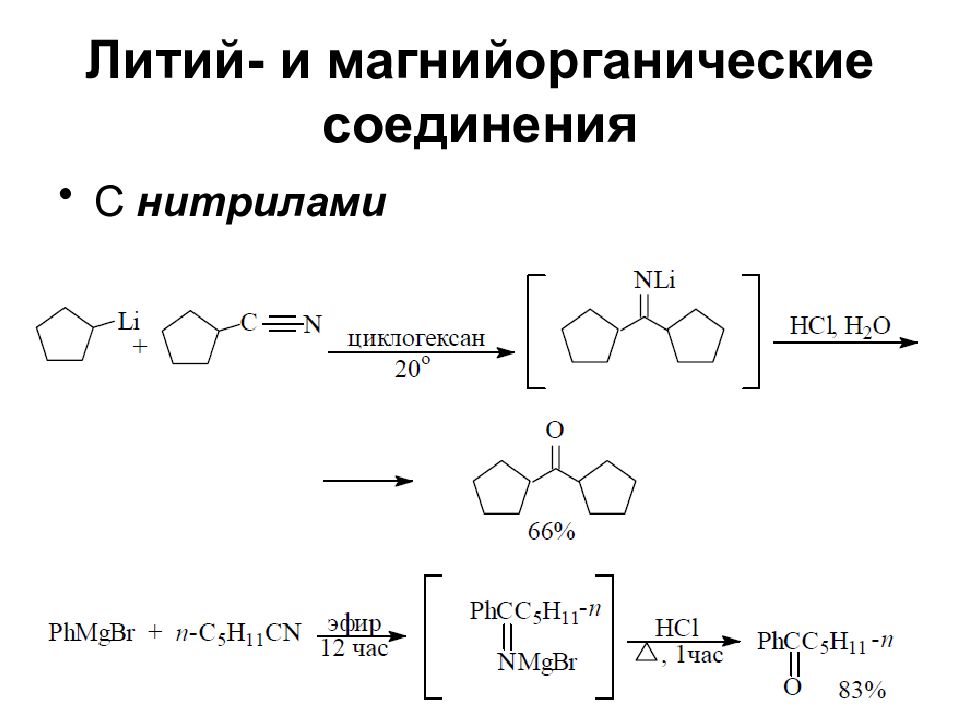
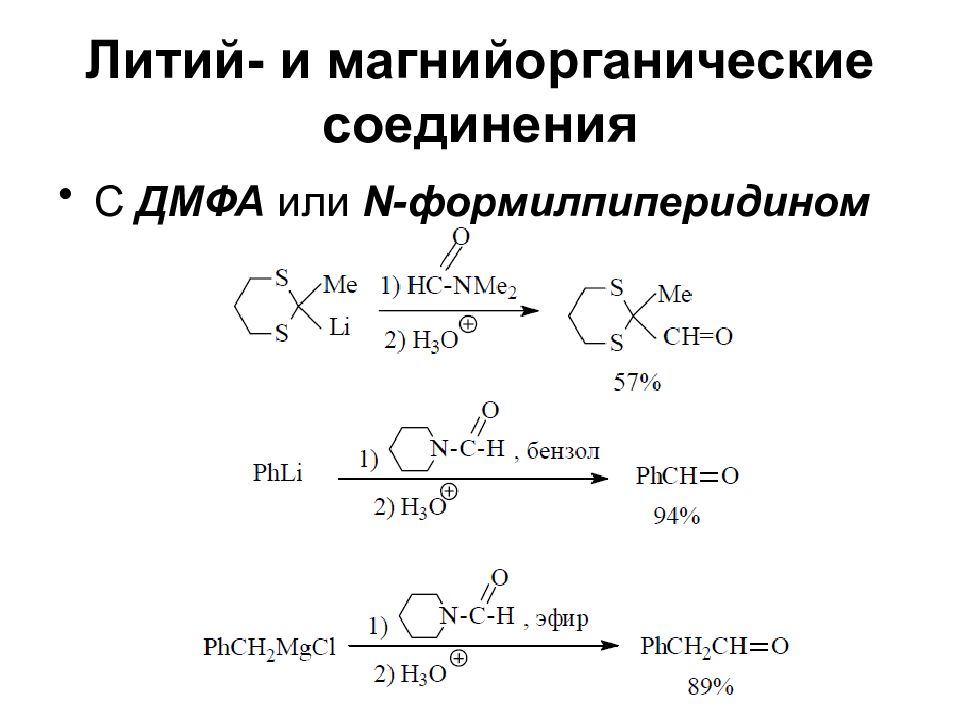
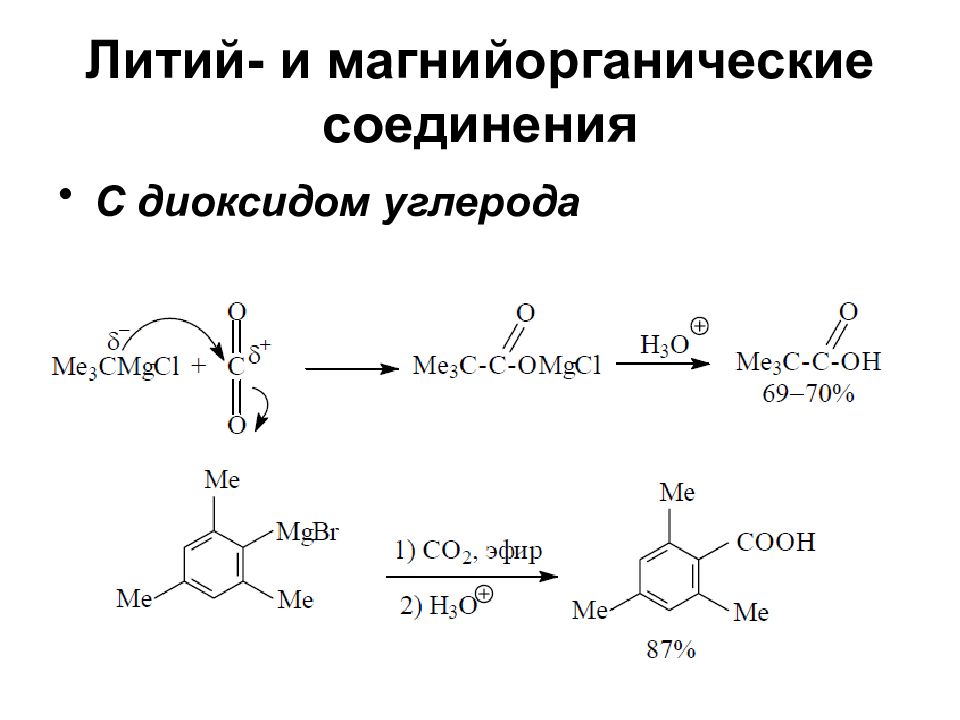
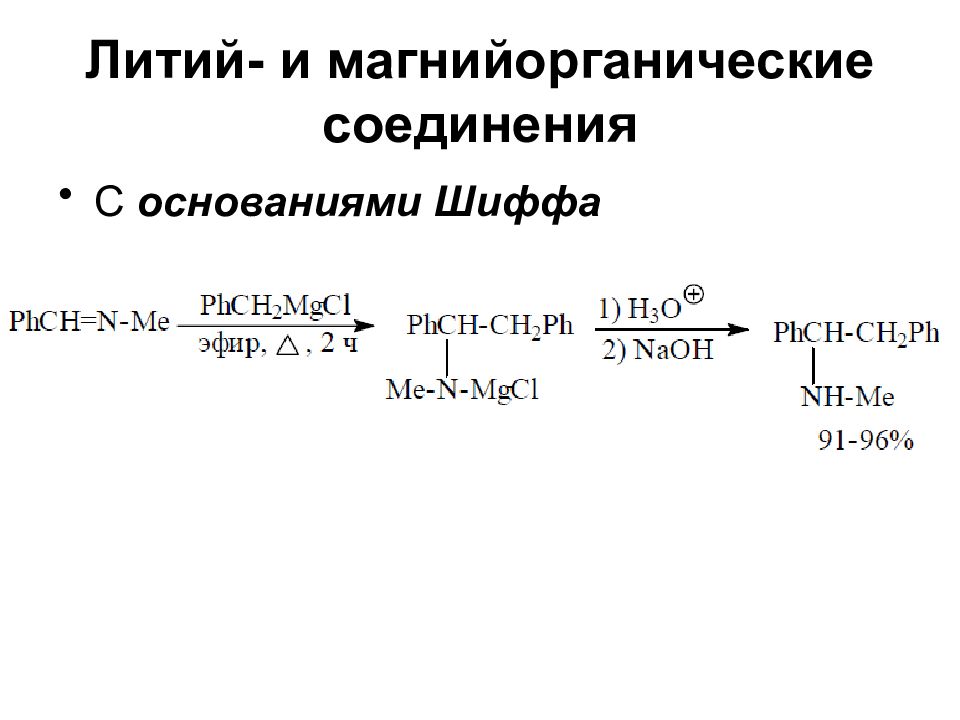
Слайд 37: Литий- и магнийорганические соединения
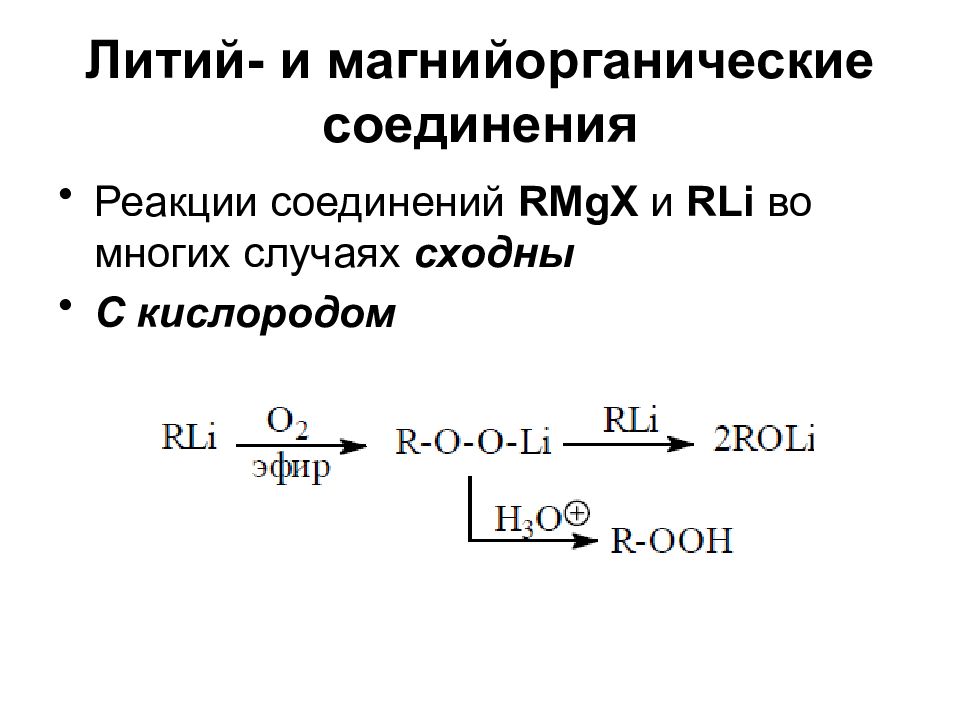
Реакции соединений RMgX и RLi во многих случаях сходны С кислородом
Слайд 38: Литий- и магнийорганические соединения
Особенно чувствителен к кислороду трет-бутиллитий: на воздухе его растворы самовоспламеняются Все манипуляции с литийорганическими соединениями следует проводить в атмосфере инертного газа (азота или аргона)
Слайд 39: Литий- и магнийорганические соединения
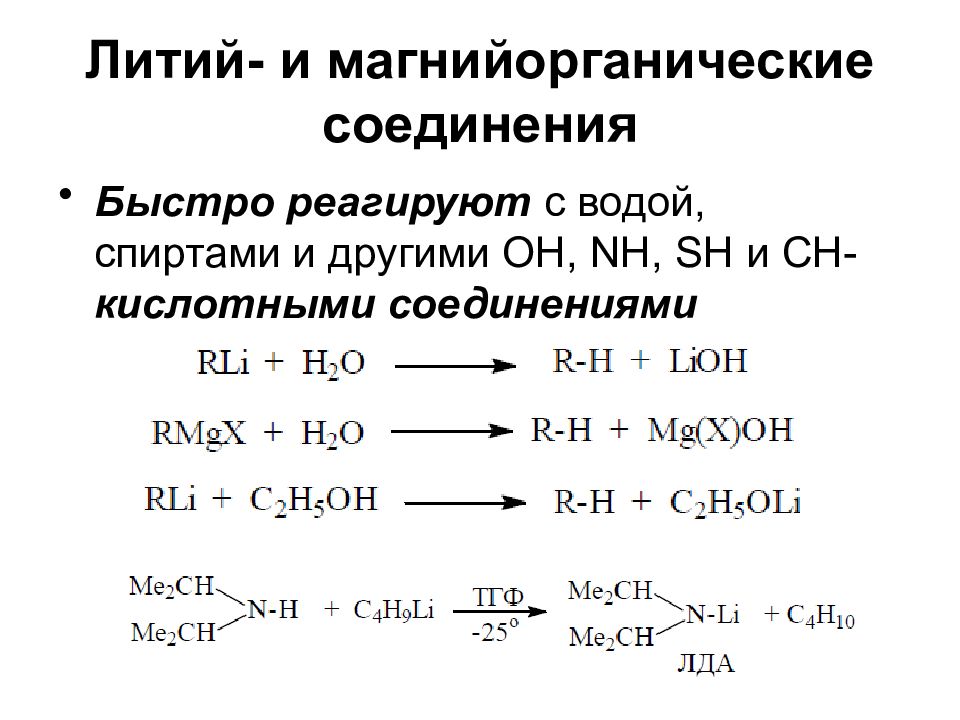
Быстро реагируют с водой, спиртами и другими OH, NH, SH и CH- кислотными соединениями
Слайд 40: Литий- и магнийорганические соединения
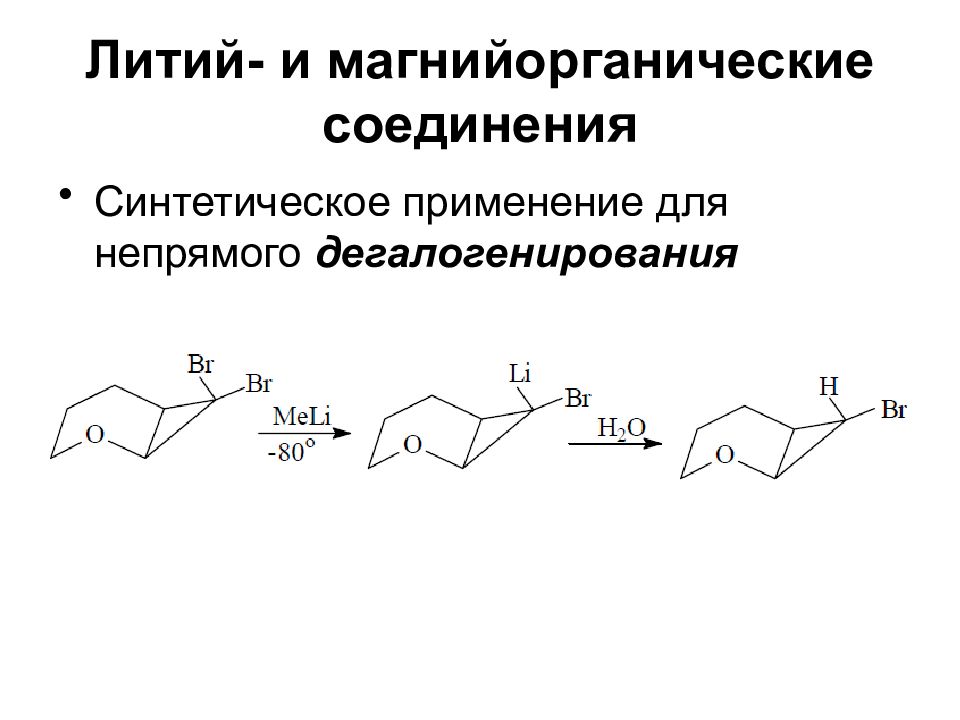
Синтетическое применение для непрямого дегалогенирования
Слайд 41: Литий- и магнийорганические соединения
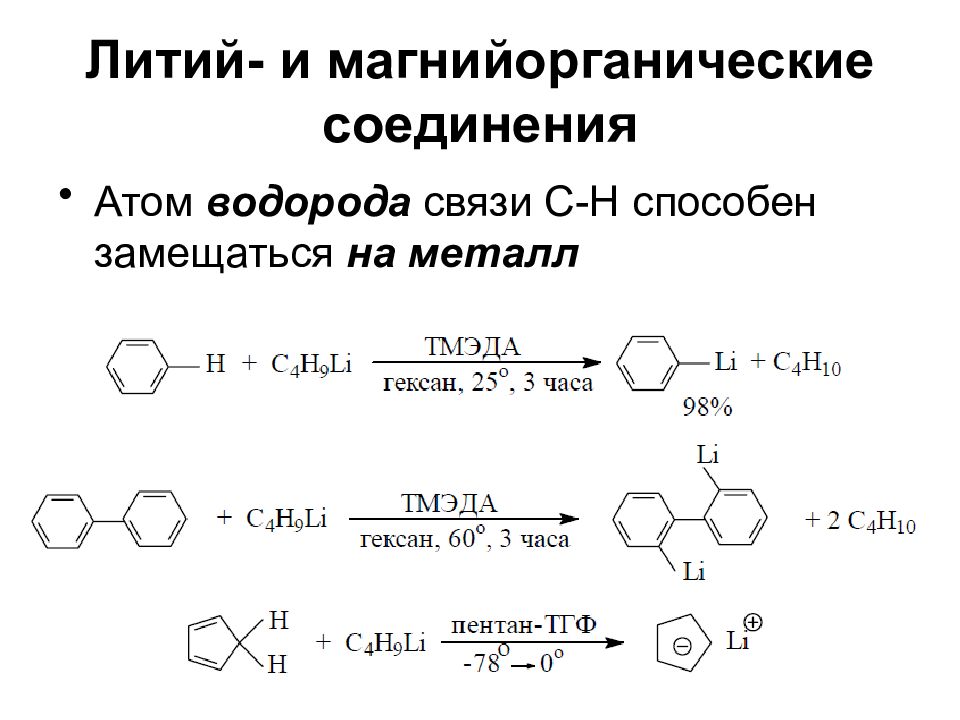
Атом водорода связи С-H способен замещаться на металл
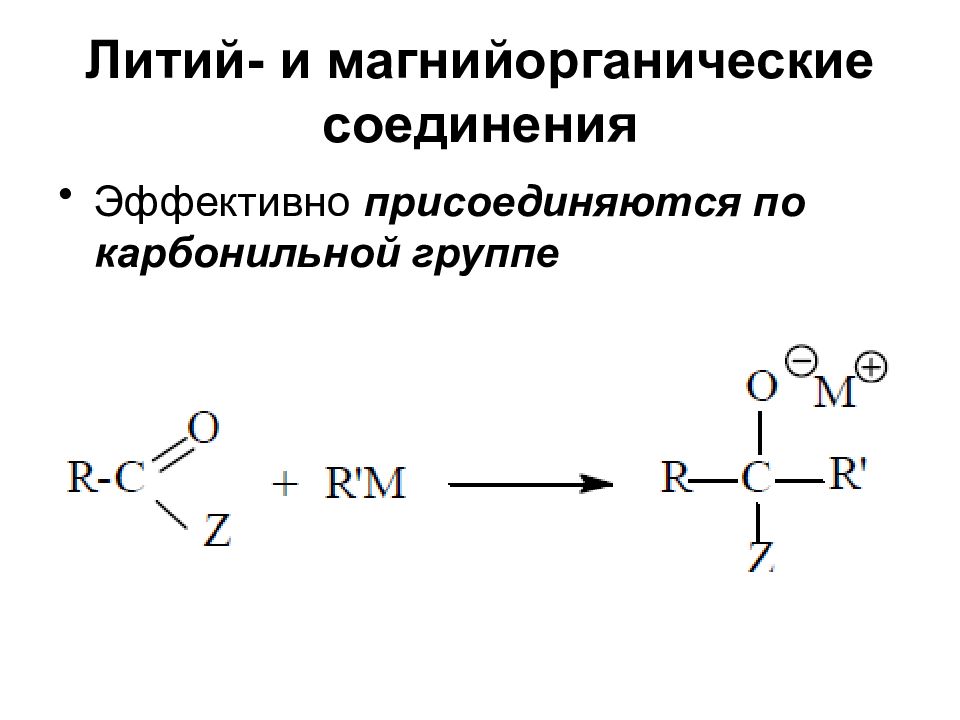
Слайд 42: Литий- и магнийорганические соединения
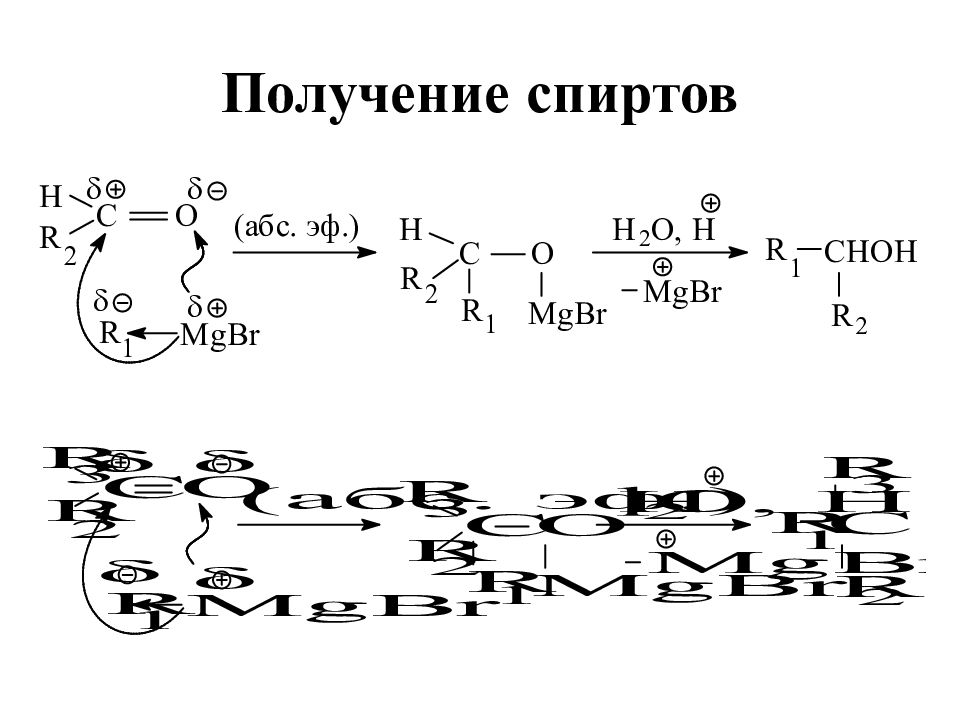
Эффективно присоединяются по карбонильной группе
Слайд 44: Литий- и магнийорганические соединения
С α,β-непредельными альдегидами дают продукты 1,2-присоединения с кетонами - смеси
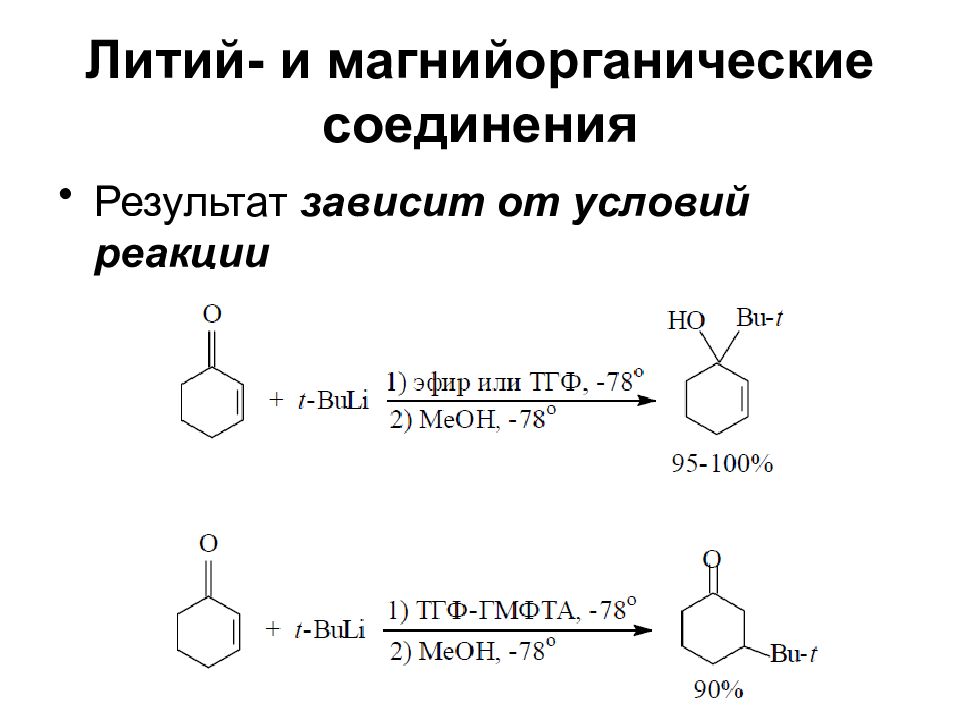
Слайд 45: Литий- и магнийорганические соединения
Результат зависит от условий реакции
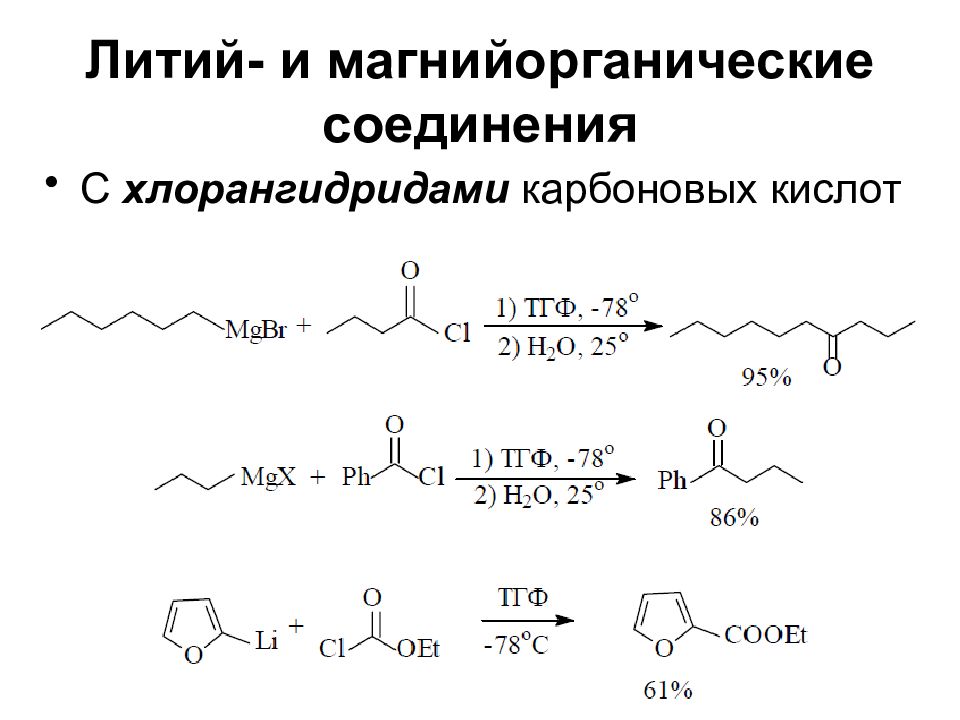
Слайд 47: Литий- и магнийорганические соединения
С хлорангидридами карбоновых кислот
Слайд 52: Литий- и магнийорганические соединения
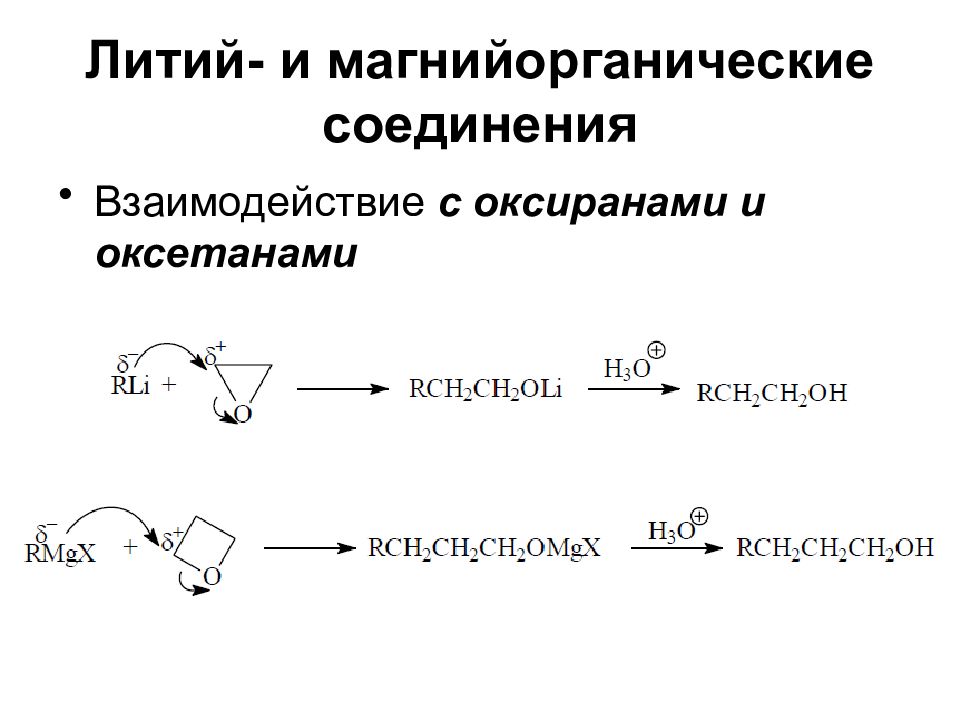
Взаимодействие с оксиранами и оксетанами
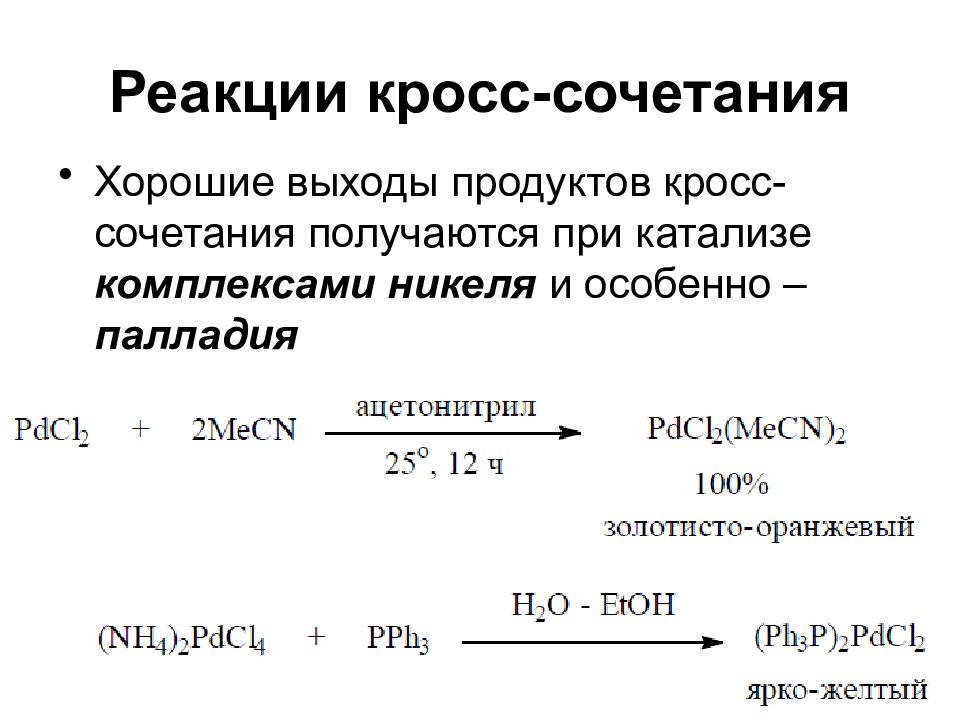
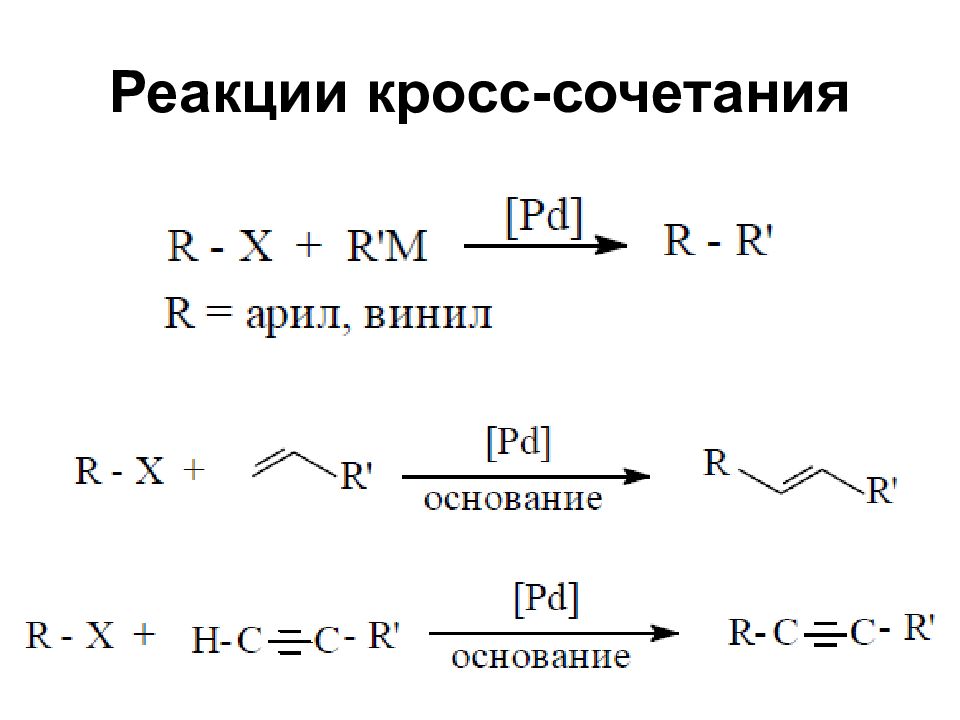
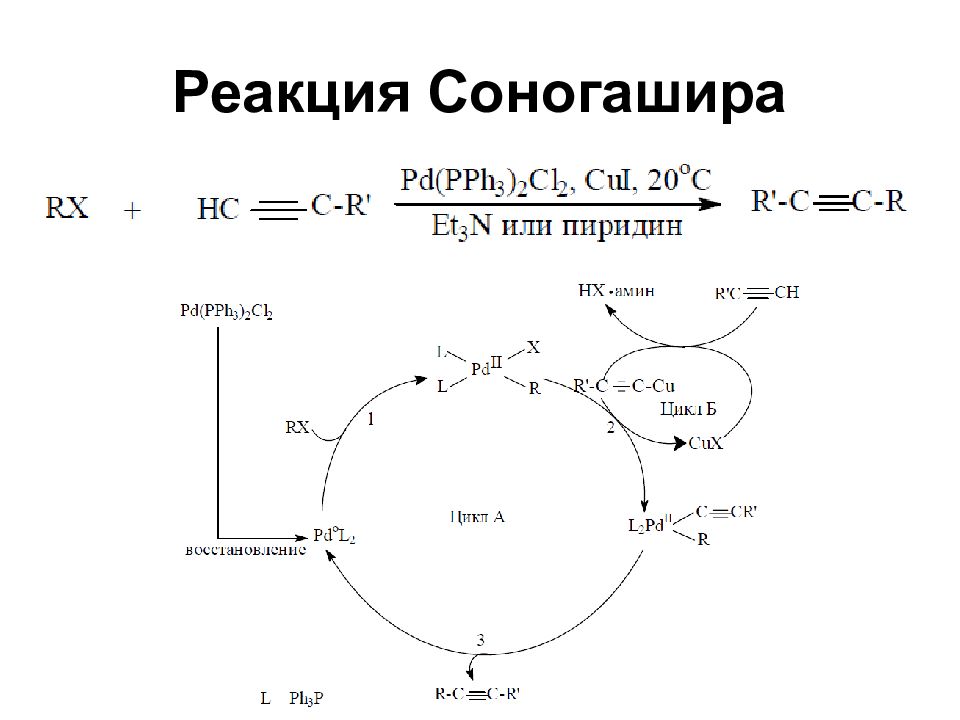
Слайд 54: Реакции кросс-сочетания
Хорошие выходы продуктов кросс-сочетания получаются при катализе комплексами никеля и особенно – палладия
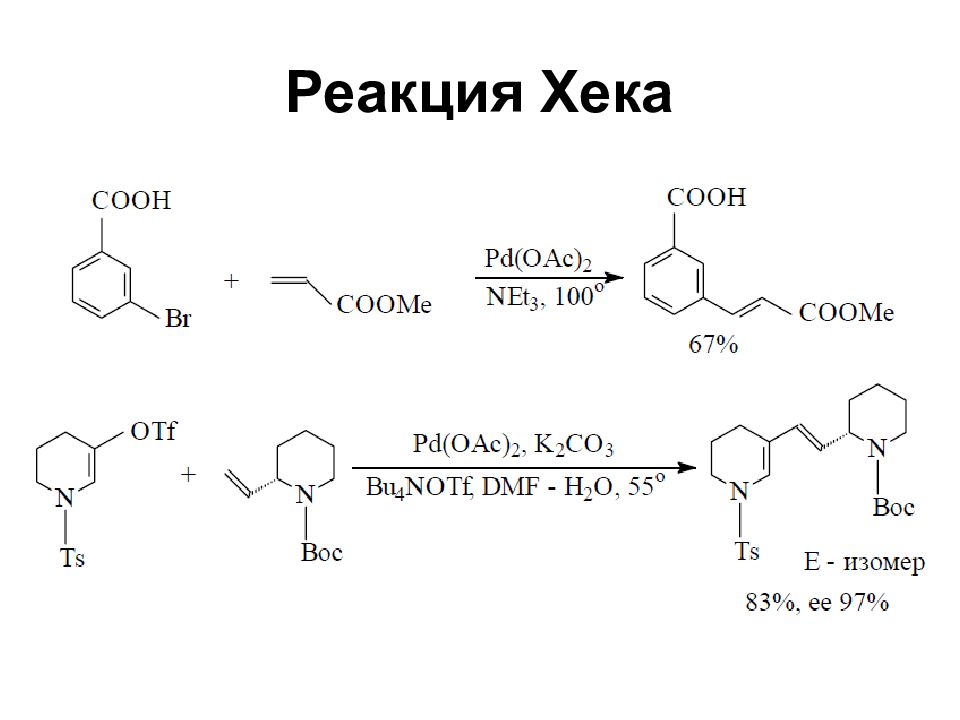
Слайд 60: Реакция Хека
Открыта в 1968 году В настоящее время ртутьорганические соединения не используют в реакции Хека, а ключевой интермедиат – RPdX (R – арил, винил) получают in situ путём окислительного присоединения RX к комплексу Pd(0)
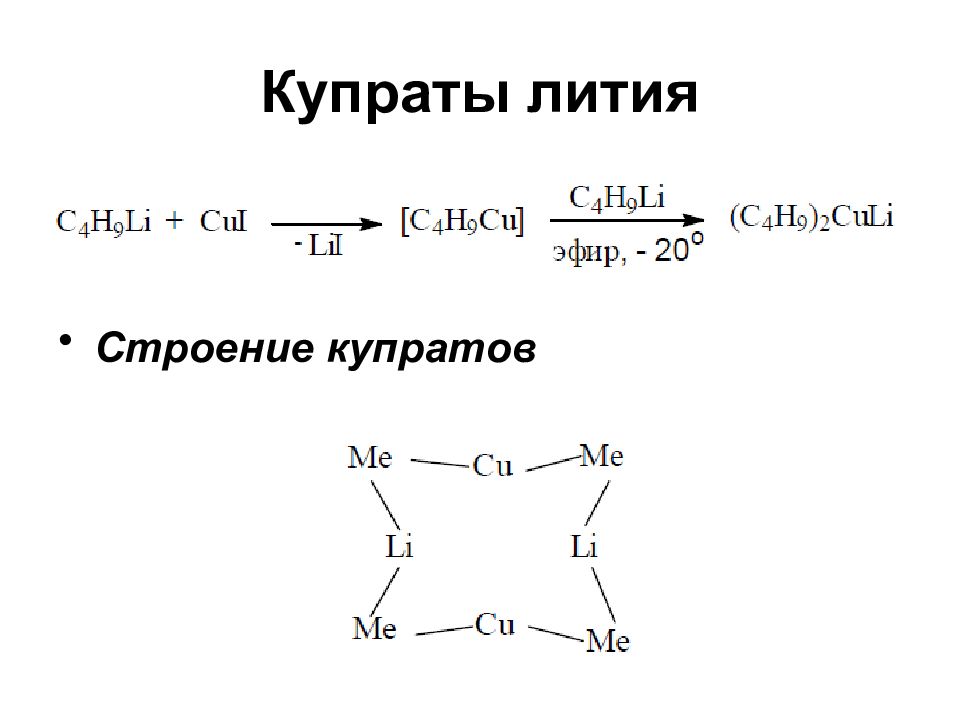
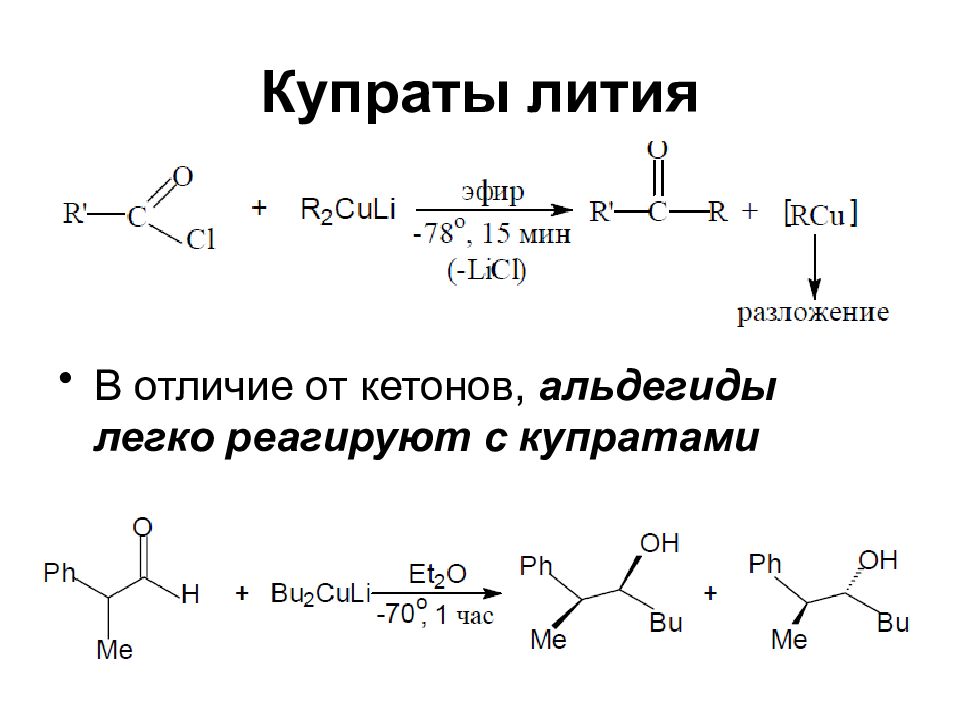
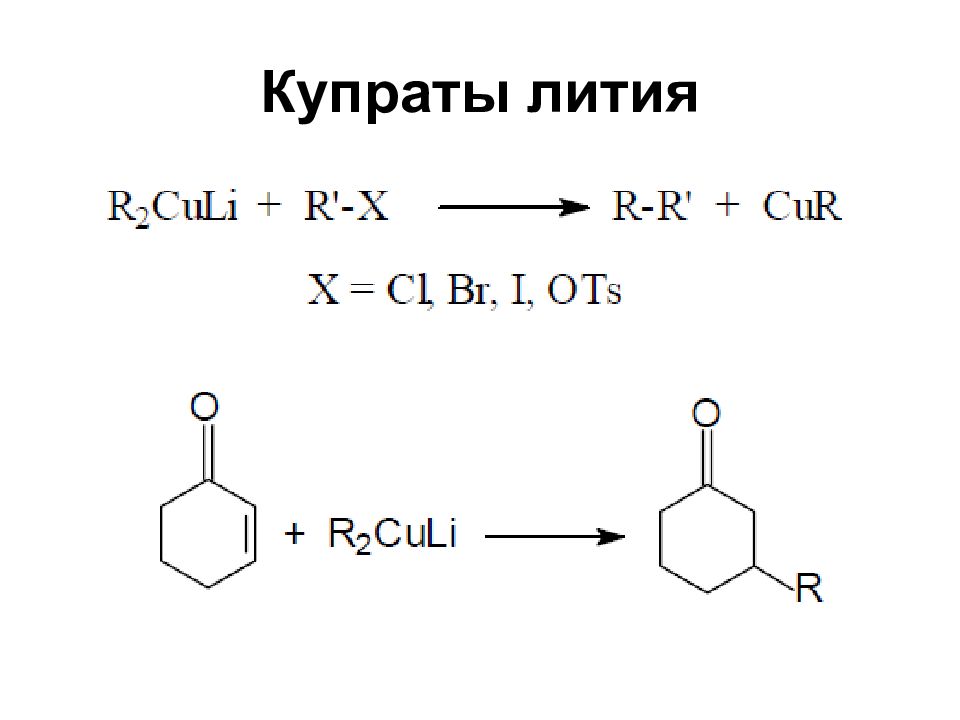
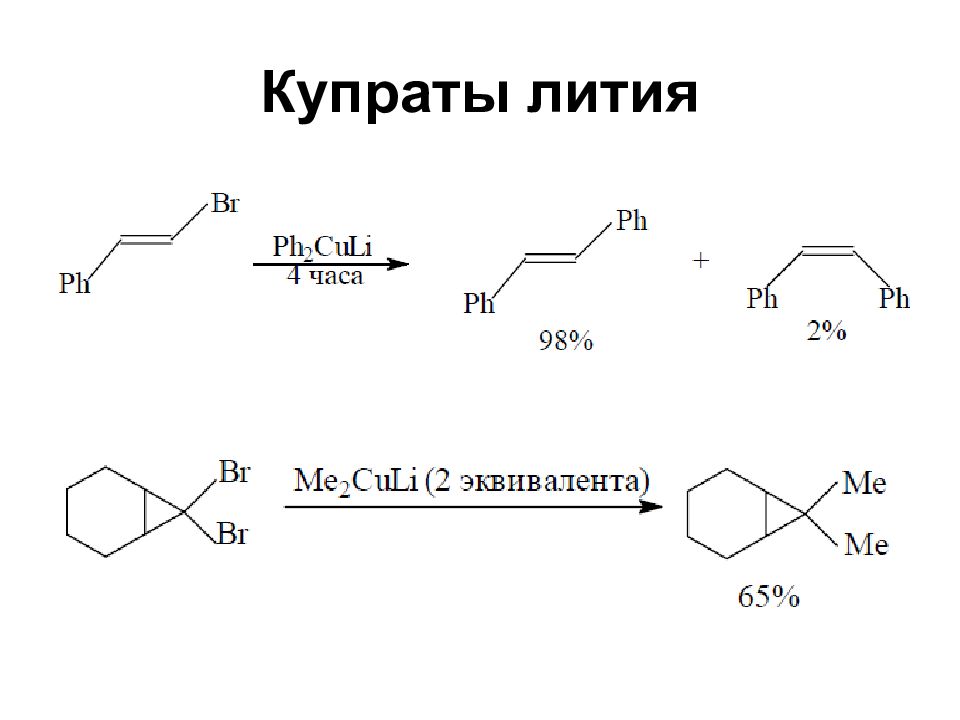
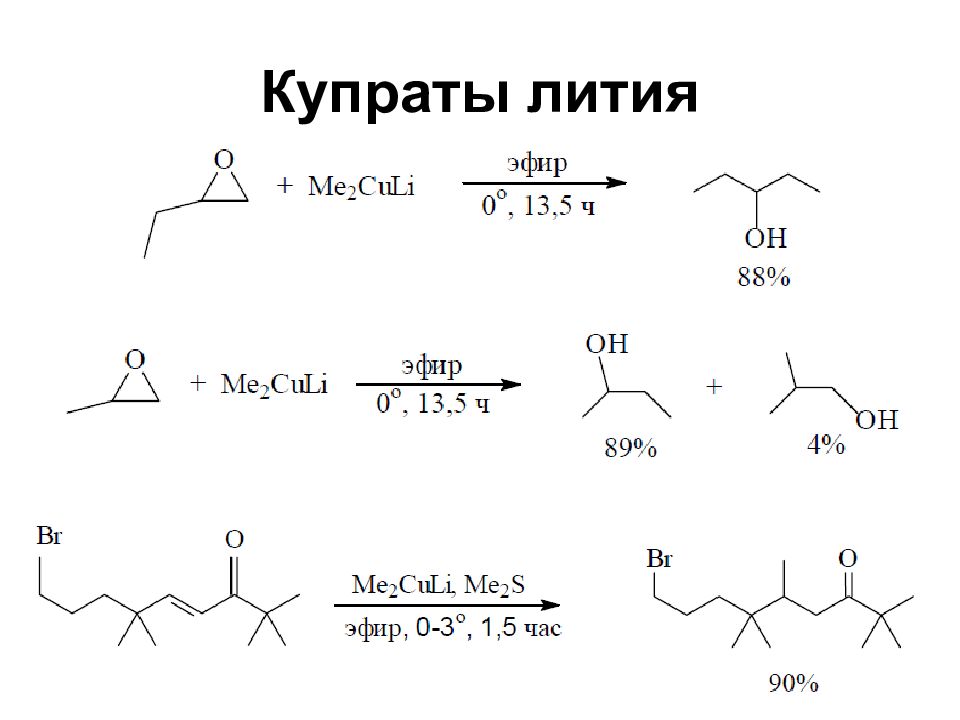
Слайд 66: Купраты лития
В отличие от кетонов, альдегиды легко реагируют с купратами
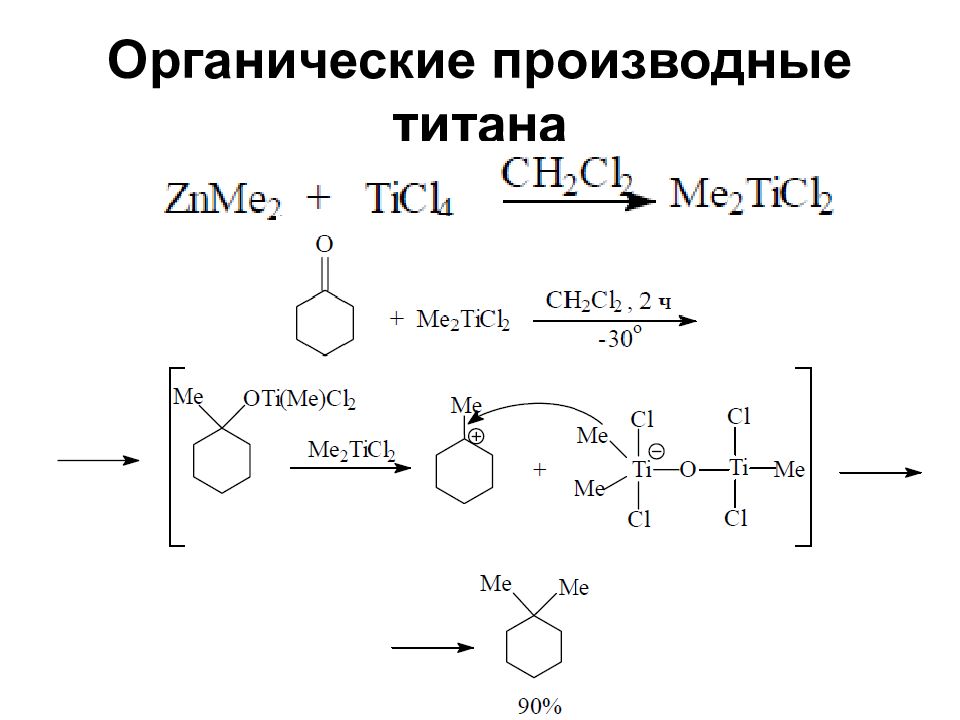
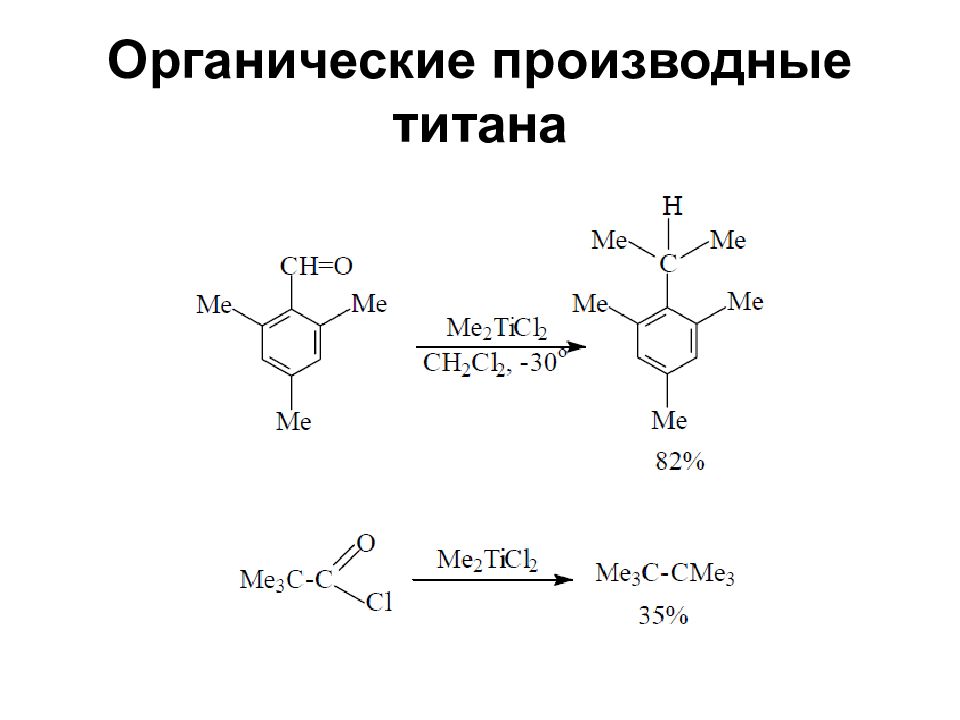
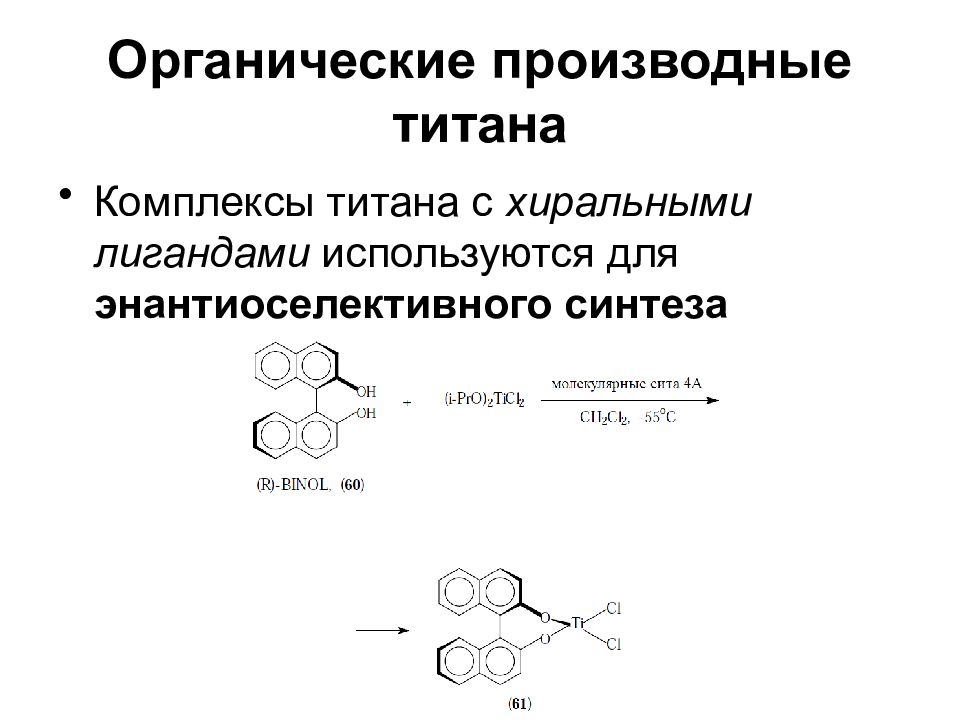
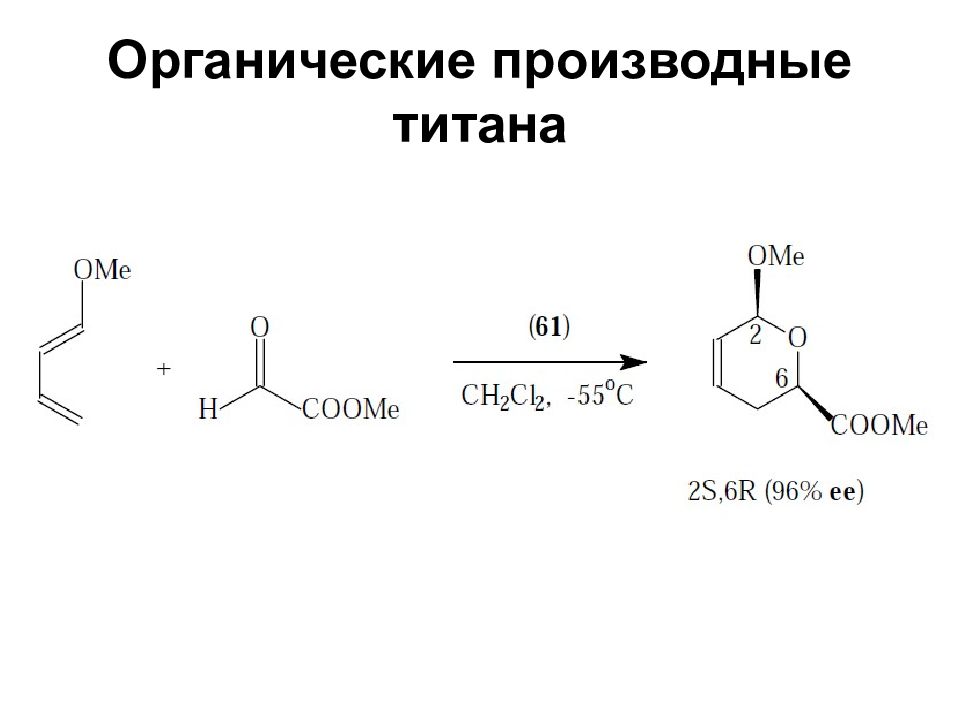
Слайд 72: Органические производные титана
Комплексы титана с хиральными лигандами используются для энантиоселективного синтеза
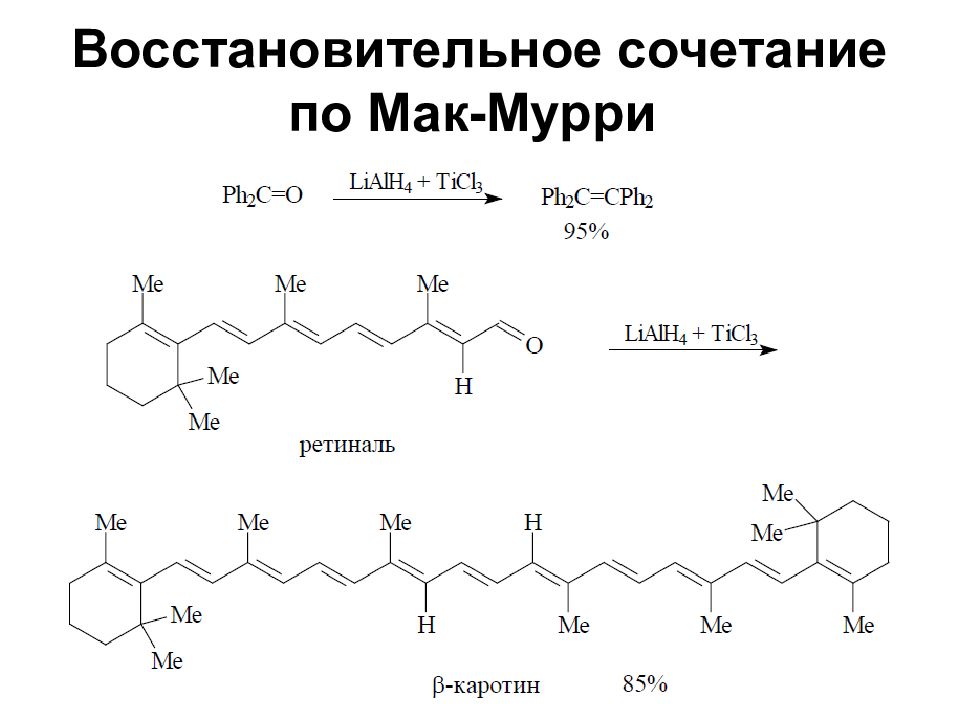
Слайд 74: Восстановительное сочетание по Мак-Мурри
При действии на альдегиды и кетоны соединениями титана в низших степенях окисления