Первый слайд презентации: Классификация химических реакций в неорганической и органической химии
Слайд 2: Хими́ческая реа́кция
— это превращение одного или нескольких исходных веществ (реагентов) в продукты реакции, которые отличаются по химическому составу или строению. Хими́ческая реа́кция
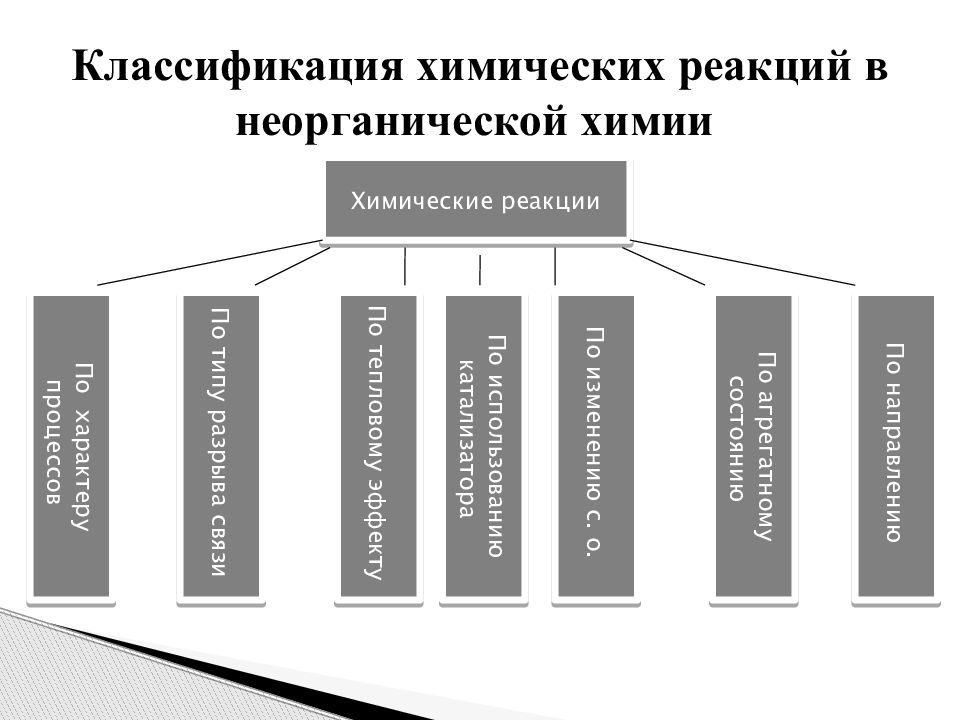
Химические реакции По направлению По агрегатному состоянию По изменению с. о. По использованию катализатора По тепловому эффекту По типу разрыва связи По характеру процессов
По характеру процесса. Реакции разложения Реакции соединения СаСО 3 → СаО + СО 2 2FеСl 2 + Сl 2 → 2FеСl 3 Реакции замещения Реакции обмена Zn + 2HCl → Zn Cl 2 + H 2 AgNO 3 + КВr → Аg Вr+К NO 3 Классификация химических реакций в неорганической химии
Слайд 5: Классификация химических реакций в неорганической химии
По типу разрыва связи Гомолитические (равный разрыв, каждый атом получает по одному электрону). CH 4 свет → CH 3 ∙ + ∙ H Гетеролитические ( неравный разрыв – одному достается пара электронов). CH 3 Сl → CH 3 + + : Cl - Классификация химических реакций в неорганической химии
Слайд 6: Классификация химических реакций в неорганической химии
По тепловому эффекту экзотермические (выделение тепла) СН 4 + 2О 2 → СО 2 + 2Н 2 О + Q эндотермические (поглощение тепла) CaCO 3 → CaO +CO 2 – Q Классификация химических реакций в неорганической химии
Слайд 7: Классификация химических реакций в неорганической химии
Катализатор – это вещество, которое увеличивает скорость химической реакции. По использованию катализатора Каталитические. 2 KClO 3 → t, MnO 2 2 KCl +3 O 2 ↑ Некаталитические. 2Al+6HCl→ t 2AlCl 3 +3H 2 ↑ Классификация химических реакций в неорганической химии
Слайд 8: Классификация химических реакций в неорганической химии
По изменению степени окисления Окислительно-восстановительные - идут с изменением степени окисления элементов: 2KN +5 O 3 +C 0 →2KN +3 O 2 + С +4 O 2 Кислотно-основные - идут без изменения степени окисления элементов. KOH + HBr → KBr + H 2 O Классификация химических реакций в неорганической химии
Слайд 9: Классификация химических реакций в неорганической химии
По направлению Обратимые способные протекать как в прямом, так и в обратном направлении 3H 2 + N 2 ⇆ 2NH 3 Необратимыми реакции, при протекании которых: 1) продукты выпадают в виде осадка, выделяются в виде газа. ВаСl2 + Н 2SО 4 →ВаSО4↓ + 2НСl 2) образуется малодиссоциированное соединение. НСl + NаОН → Н2О + NаСl 3) образуется комплексная соль: СuSO4 + 4NНз = [ Сu ( NНз )4]SO4 Классификация химических реакций в неорганической химии
Слайд 10: Классификация химических реакций в неорганической химии
По агрегатному состоянию фаз Гомогенные реакция проходит в одной фазе, без границ раздела; реакции в газах или в растворах. NaOH ( p - p ) + HCl ( p - p ) → NaCl + H 2 O Гетерогенные реакции содержат разные фазы и проходят на границе раздела фаз. Zn (тв)+ 2 HCl (р-р) → ZnCl 2 + H 2↑ Классификация химических реакций в неорганической химии
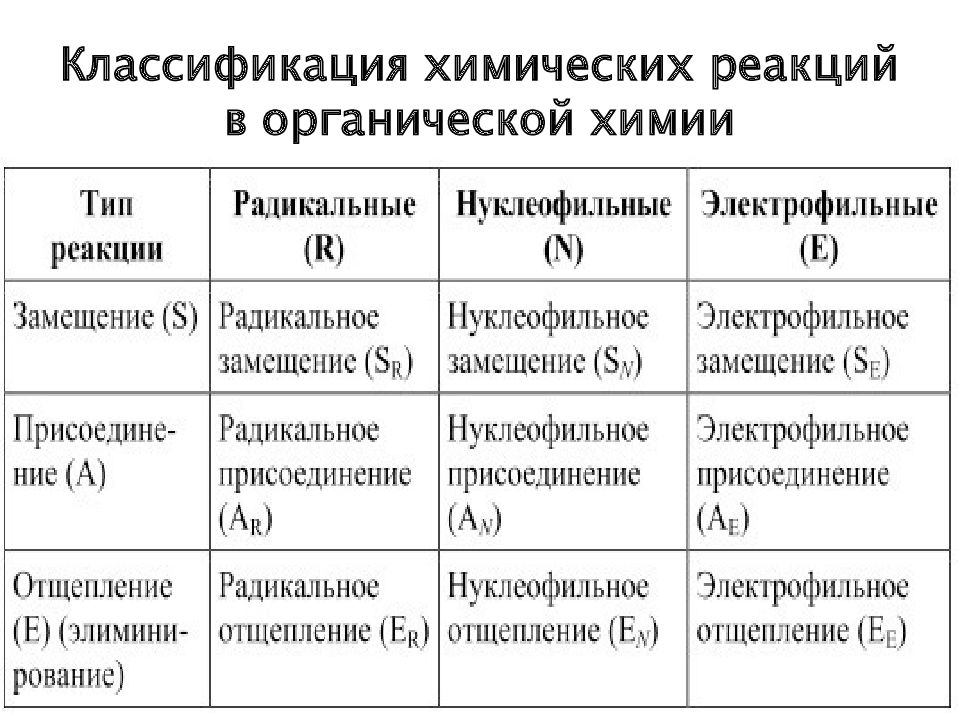
Слайд 12: Классификация химических реакций в органической химии
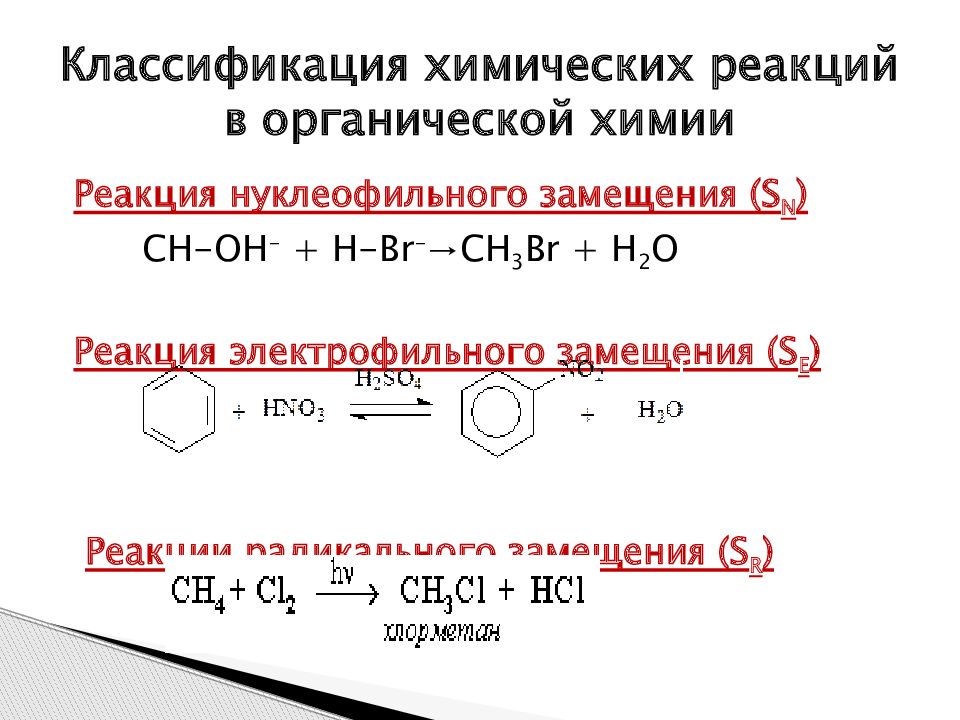
Реакция нуклеофильного замещения (S N ) СН-ОН - + Н-Br - →СН 3 Br + H 2 O Реакция электрофильного замещения ( S Е ) Реакции радикального замещения (S R ) Классификация химических реакций в органической химии
Слайд 13: Классификация химических реакций в органической химии
Реакции электрофильного присоединения (А Е ) Н 2 С = СН 2 + Н + С l – → СН 3 – СН 2 С l Реакции нуклеофильного присоединения (А N ) Реакция радикального присоединения ( A R ) Классификация химических реакций в органической химии
Последний слайд презентации: Классификация химических реакций в неорганической и органической химии: Классификация химических реакций в органической химии
Реакции отщепления(элиминирования) - э то реакции, которые приводят к образованию кратных связей. CH 3 -CH(Cl)-CH 2 -CH 3 + KOH →CH 3 -CH=CH-CH 3 + HCl Элиминирование при действии нуклеофилов (оснований ) Элиминирование при действии электрофилов (кислот) Классификация химических реакций в органической химии