Первый слайд презентации
Количественные методы анализа. Химические методы анализа: Гравиметрический анализ
Слайд 3
Гравиметрический анализ ( гравиметрия, весовой анализ) (от лат. « gravis » - тяжелый) - метод количественного химического анализа, основанный на точном измерении массы определяемого вещества или его составных частей, выделяемых в виде соединений точно известного постоянного состава.
Слайд 4
1. Классификация гравиметрических методов 1. Метод выделения основан на выделении из сложного вещества определяемого компонента, с последующим взвешиванием и расчетом. Например, определение зольности продукта, золота или меди в сплаве и др. Содержание выделенного компонента в исходном объекте, %: m(x) – масса выделенного компонента; m н – масса навески
Слайд 7
Расчет влаги (влажности) по непрямому методу отгонки В методах отгонки определяемый компонент выделяют в виде летучего соединения действием кислоты или высокой температуры m ост. – масса вещества, оставшегося после отделения определяемого летучего компонента.
Слайд 8
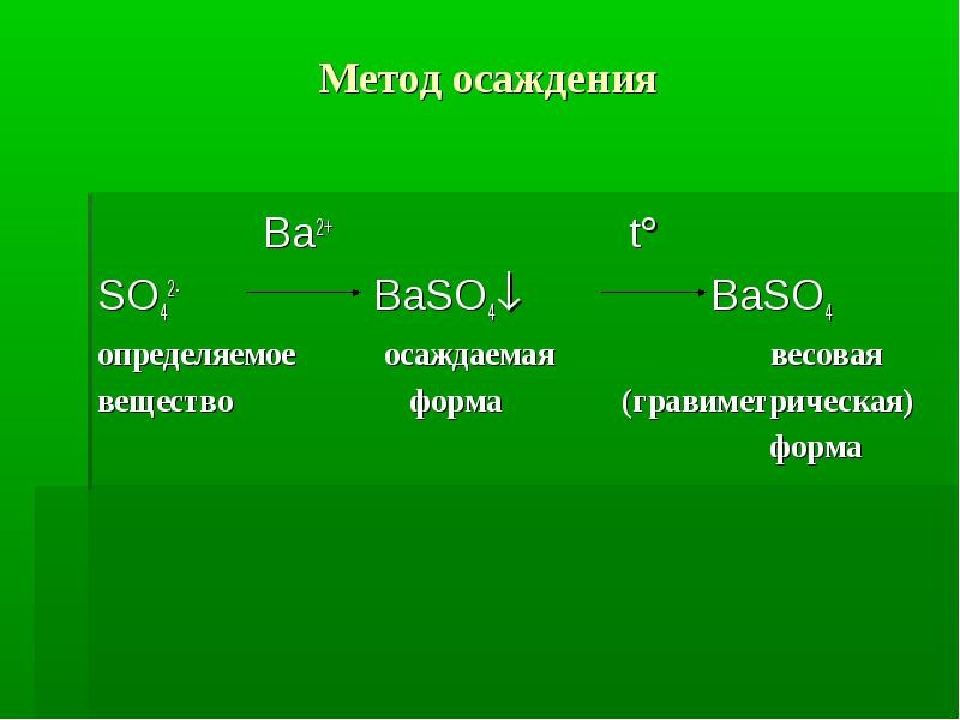
3. Метод осаждения основан на осаждении определяемого компонента в виде малорастворимого химического соединения, фильтровании, прокаливании до постоянной массы и последующем определении массы полученного вещества. Методы осаждения — наиболее распространённые методы гравиметрического анализа
Слайд 11
2.1 Метод осаждения. Основные этапы: • расчет массы навески определяемого вещества; • взятие навески (взвешивание) из аналитической пробы; • растворение навески в воде или другом растворителе (при необходимости устранение мешающих компонентов, упаривание раствора, создание определенного значения рН) • выбор осадителя и расчет его количества; • проведение реакции осаждения; • фильтрование образовавшегося осадка; • промывание осадка; • прокаливание или высушивание осадка; • взвешивание; • расчет содержания.
Слайд 12
При выполнении гравиметрического анализа методом осаждения обычно требуется следующая химическая посуда: - стеклянные бюксы, часовые стекла для взвешивания твердых и жидких веществ : - фарфоровые тигли для прокаливания осадков:
Слайд 13
- тонкостенные химические стаканы объемом 100, 200 и 400 мл для осаждения, растворения веществ и т.п.; - воронки для фильтрования и промывания осадков;
Слайд 14
- обеззоленные фильтры - фильтрующие тигли (тигли Гуча ) - фильтрующие воронки
Слайд 15
- эксикатор с осушителем для охлаждения и хранения осадков. Кроме того, необходимы электрическая плитка, сушильный шкаф и муфельная печь для термической обработки, сушки и прокаливания продуктов анализа.
Слайд 16
2.2 Осаждаемая и гравиметрическая формы Осаждаемая форма – тот осадок, который получается в результате химической реакции между осаждаемым ионом и осадителем. Например : Ba 2+ + SO 4 2– → BaSO 4
Слайд 17
Требования, предъявляемые к осадку (осаждаемой форме). Осадок должен: 1. быть практически нерастворимым. Определяемый компонент должен выделяться в осадок количественно, при этом его концентрация в растворе после осаждения не должна превышать 10 -6 моль/л; 2. выделяться в форме, удобной для его отделения от раствора и промывания, и по возможности быть крупнокристаллическим, если он кристаллический, или хорошо скоагулированным, если он аморфен. 3. быть чистым, т.е. не содержать посторонних примесей. 4. количественно переходить в процессе термообработки в гравиметрическую форму.
Слайд 18
Гравиметрическая (весовая) форма – то вещество, которое получается после прокаливания осаждаемой формы. В некоторых случаях осаждаемая и гравиметрическая формы одинаковы ( например, BaSO 4 ).
Слайд 20
В других случаях их состав отличается друг от друга: Осаждаемая форма Гравиметрическая форма CaCO 3 CaO Fe (OH) 3 Fe 2 O 3 Al (OH) 3 Al 2 O 3
Слайд 22
Для более полного выделения осаждаемого компонента вводят избыток осадителя. Количество осадителя определяется растворимостью, осаждаемой формой и летучестью осадителя. 2.3 Условия получения осадка
Слайд 23
Условия осаждения кристаллических осадков • осаждение ведут, как правило, из горячих разбавленных растворов ; • раствор осадителя добавляют медленно, при интенсивном непрерывном перемешивании ; • перед осаждением в раствор иногда добавляют вещества, несколько повышающие растворимость осадка. Данные условия позволяют уменьшить скорость образования центров кристаллизации и получить более чистый крупнокристаллический осадок.
Слайд 24
Условия осаждения аморфных осадков • осаждение ведут, как правило, из концентрированных растворов добавлением концентрированных растворов осадителей ; • осаждение ведут из горячих растворов; • раствор осадителя добавляют быстро, порциями, при перемешивании; • перед осаждением добавляют электролиты-коагулянты для образования более плотного осадка; • по окончании осаждения к раствору с осадком приливают около 100 мл горячей воды, в результате чего часть посторонних адсорбированных ионов переходит в раствор, и осадок становится более чистым.
Слайд 25
Созревание осадков Улучшение кристаллических осадков с точки зрения упрощения процесса фильтрования и получения более чистого осадка достигают, выдерживая его под маточным раствором (при нагревании или на холоде). Происходит созревание осадка, сопровождающееся укрупнением кристаллов, уменьшением их поверхности и уменьшением концентрации соосаждающихся примесей. Аморфный осадок фильтруют сразу после разбавления раствора, т.к. при стоянии загрязненность осадка адсорбированными примесями растет.
Слайд 26
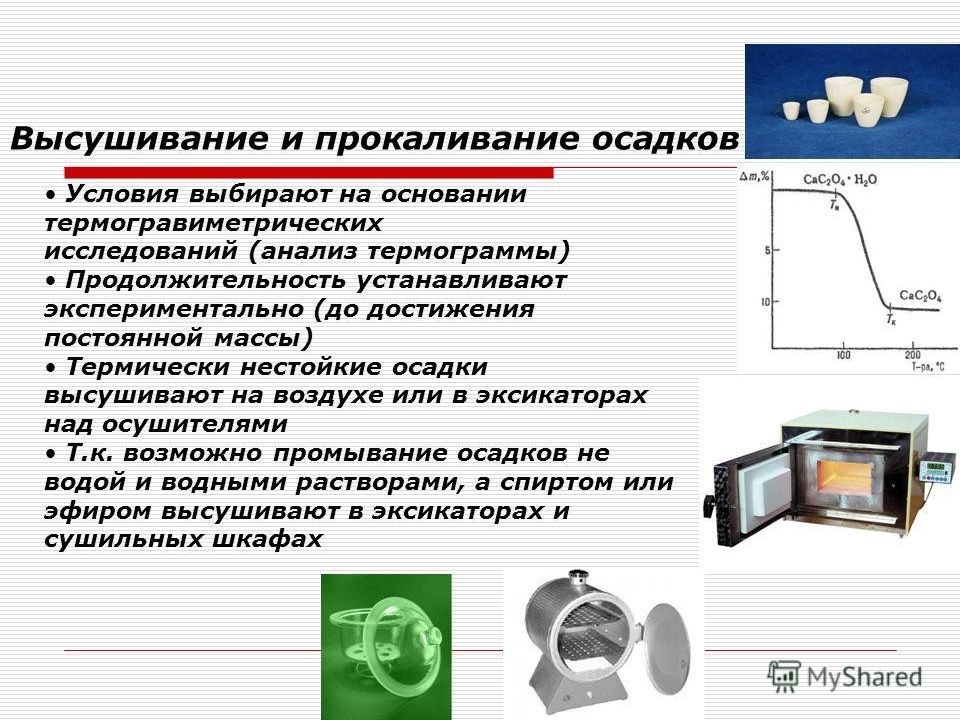
2.4 Фильтрование, промывание и прокаливание осадка Для фильтрования используют: 1. бумажные фильтры 2. фильтрующие тигли 3. воронки с пористым дном Фильтрование позволяет: отделить осадок от раствора, отмыть его от остатков маточного раствора и сорбированных примесей. Промывание осадка ведут для удаления маточного раствора из пор осадка и сорбированных примесей с поверхности осадка и фильтра.
Для методов выделения и отгонки она должна быть такая, чтобы выделяемая или удаляемая определяемая составная часть имела массу 0,1 г. В методе осаждения, навеска должна быть такой величины, чтобы из нее образовались следующие количества осаждаемой формы: если осадок аморфный легкий (оксиды, гидроксиды ) – 0,1 г; осадок кристаллический, легкий (большинство солей) – 0,15 – 0,2 г ; тяжелый кристаллический - 0,4 г ; очень тяжелый - 0,5 г.
Слайд 30
Массовую долю определяемого компонента или массу навески можно посчитать, используя гравиметрический фактор F : в % в долях F - гравиметрический фактор (фактор пересчета, аналитический множитель )
Слайд 31
ν 1 и ν 2 – стехиометрические коэффициенты в уравнении реакции, по которой из определяемого вещества образуется гравиметрическая форма. F - гравиметрический фактор ( фактор пересчета, аналитический множитель ) - отношение молярной массы определяемого компонента к молярной массе гравиметрической формы с учетом стехиометрических коэффициентов.
Слайд 32
Например, если определяемым веществом является Fe 3 O 4, а гравиметрической формой Fe 2 O 3, гравиметрический фактор будет равен Ч исло атомов определяемого компонента в числителе и знаменателе дроби должно быть одинаковым
Слайд 33
Пример: При определении Fe в препарате сульфата железа (III) взвешивали BaSO 4. Написать выражение для гравиметрического фактора. Решение: Между Fe и BaSO 4 существует стехиометрическое соотношение 2М Fe → 1М ( Fe 2 (SO 4 ) 3 )→ 3M ( SO 4 2- ) → 3 М (BaSO 4 ) F
Слайд 34
Навеска анализируемого вещества (если вещество без примесей): Если известна (приблизительно) степень чистоты анализируемого вещества в %:
Последний слайд презентации: Количественные методы анализа. Химические методы анализа: Гравиметрический
Расчет объема раствора реактива- осадителя ( Vр ) где 1,5- const - коэффициент избытка осадителя, найденный практическим путем; М о - молекулярная масса осадителя, г/моль; М ов - молекулярная масса определяемого вещества, г/моль; - навеска определяемого вещества, г; ω - массовая доля осадителя в растворе, %; Ρ - плотность раствора осадителя ; г/см 3 ; x, y – стехиометрические коэффициенты в уравнении реакции осаждения V р =