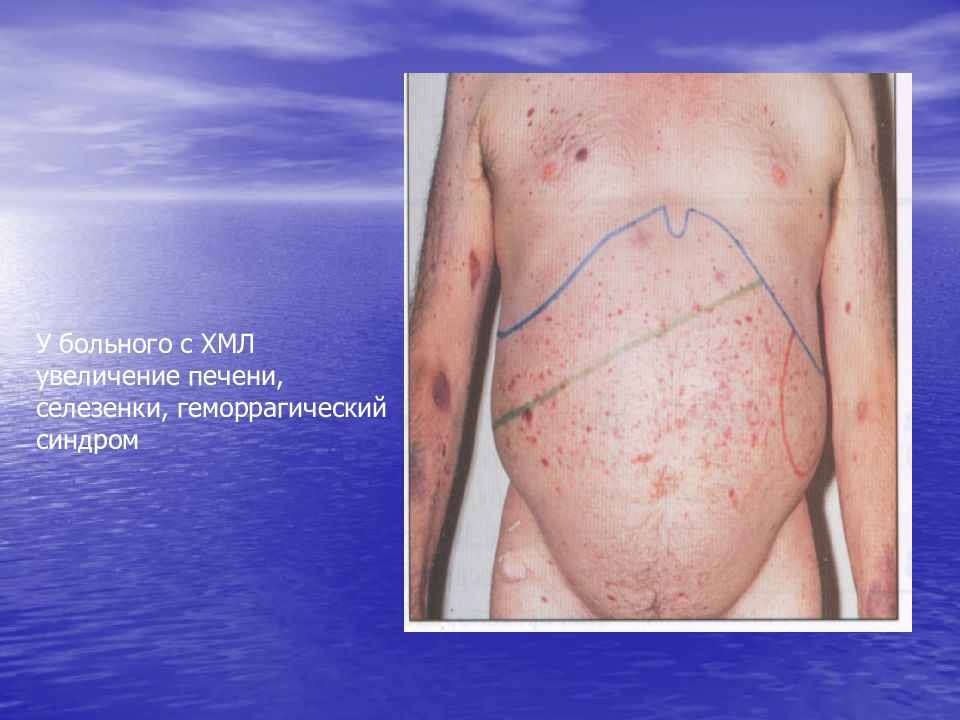
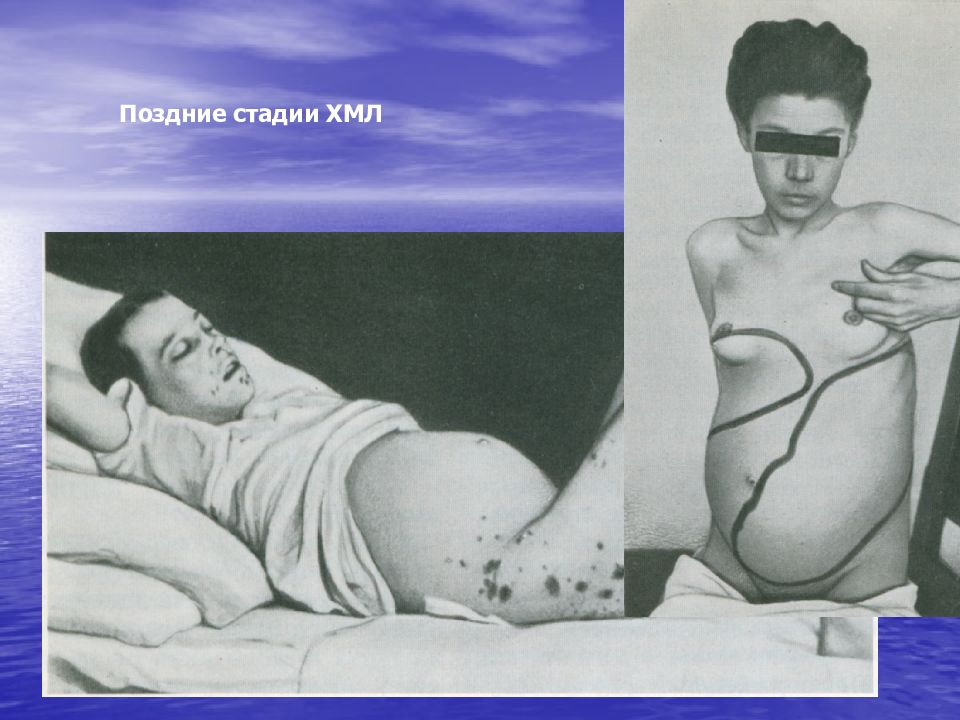
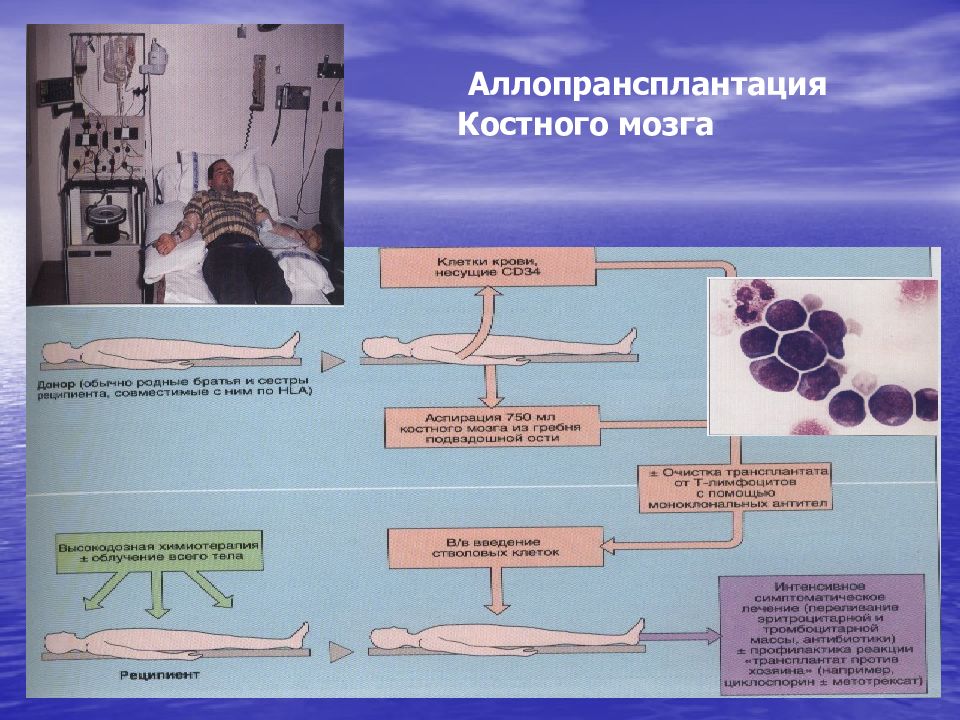
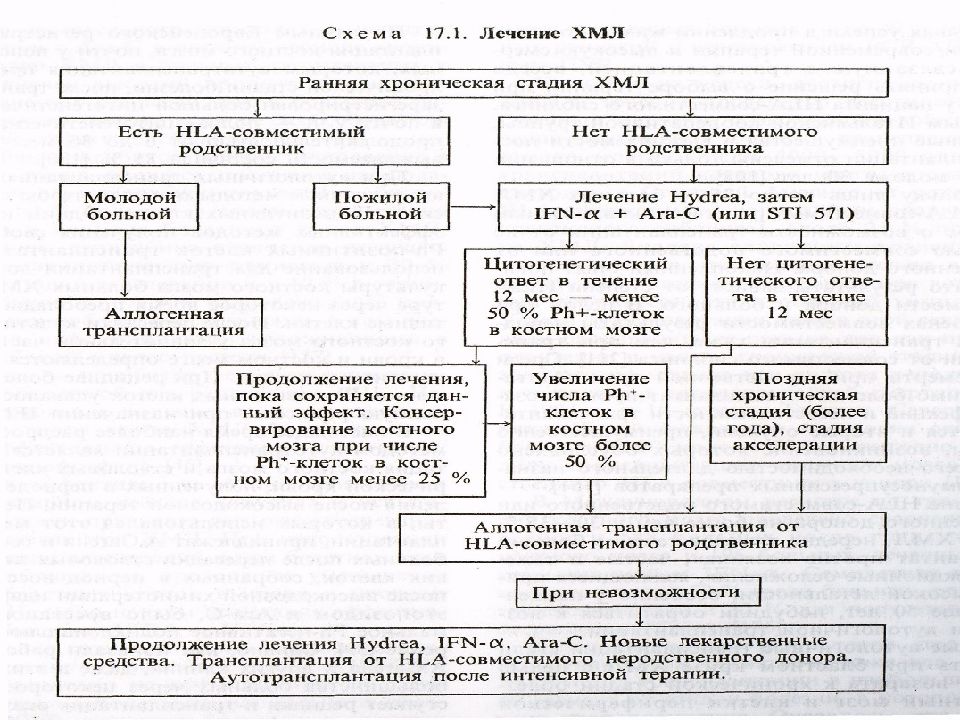
Первый слайд презентации
Лекция для 5 курса 4 факультета ФПВ на тему: « Острые лейкозы » Лектор- доцент кафедры ВМТ Шарова Н.В.
Слайд 2
Онкогематологические заболевания ( гемобластозы ) – злокачественные новообразования, морфологическим субстратом которых являются неопластически трансформированные кроветворные клетки . Гемобластозы, при которых костный мозг первично повсеместно заселен опухолевыми клетками, называют лейкозами Термин “лейкемия ” принадлежит R. Virchow (в 1845 описал ХМЛ)
- острые миелоидные лейкозы - хронические миелопролиферативные заболевания (хронический миелолейкоз, истинная полицитемия, сублейкемический миелоз, эссециальная тромбоцитемия) - В-клеточные опухоли (острый В-клеточный - лимфобластный лейкоз, хронический лимфолейкоз, множественная миелома и др. - Опухоли из Т- и NK -клеток (острый Т-клеточный лимфобластный лейкоз и др.) - Лимфома Ходжкина (лимфогранулематоз) - Неходжкинские лимфомы (НХЛ) - миелодиспластические синдромы
Слайд 4
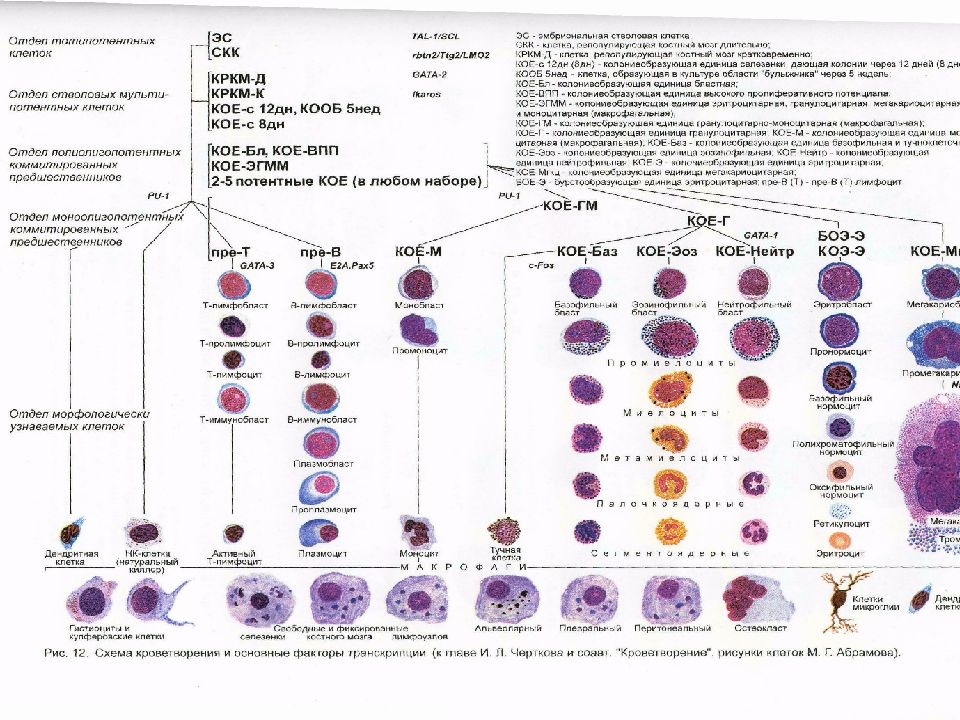
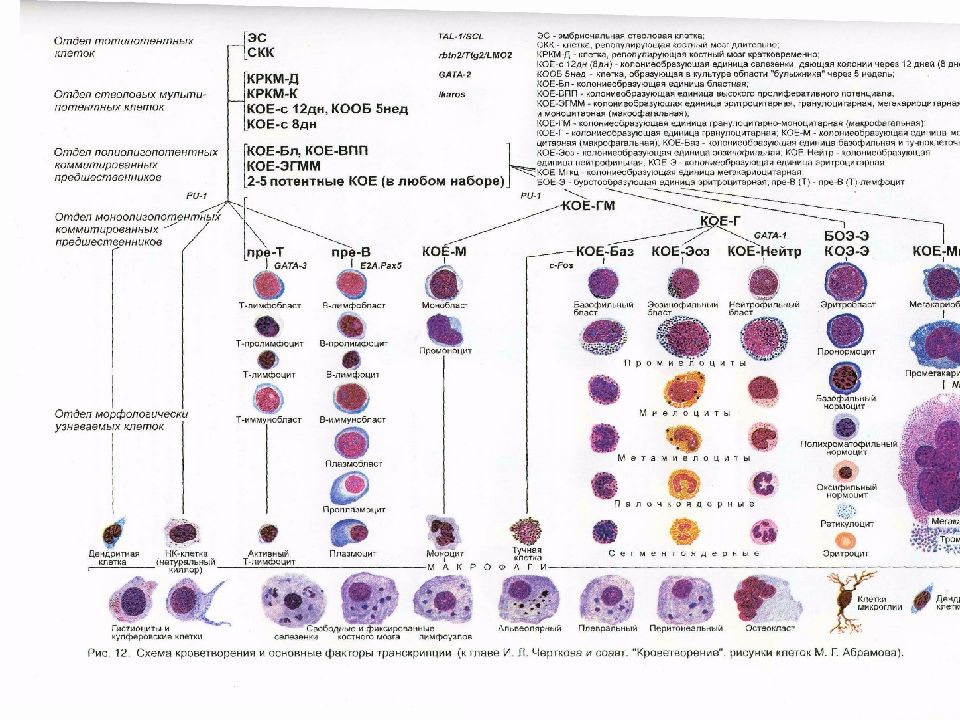
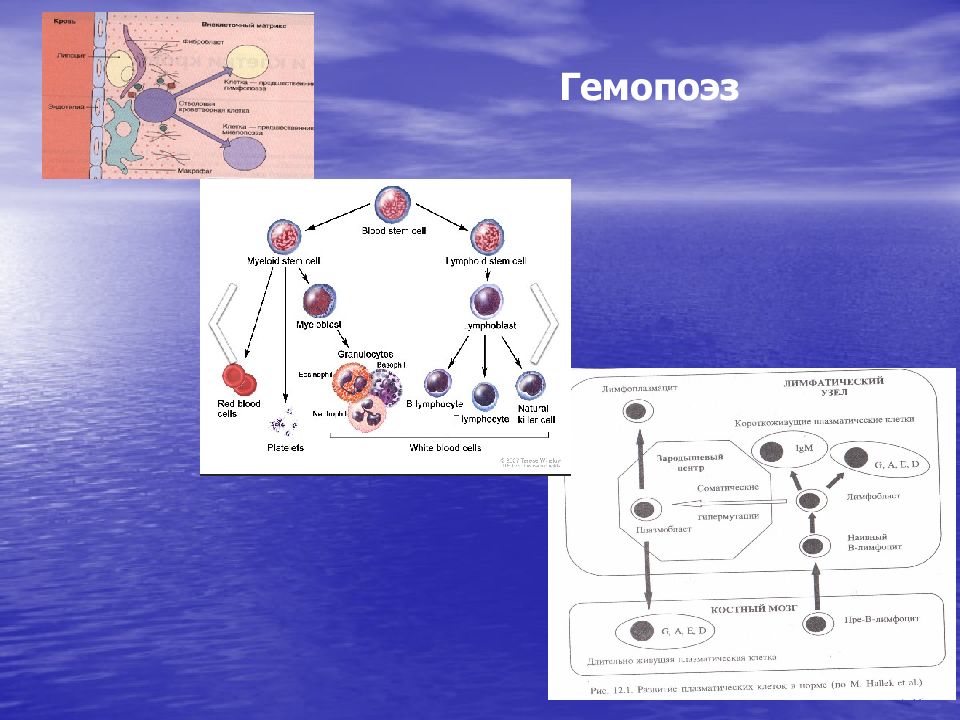
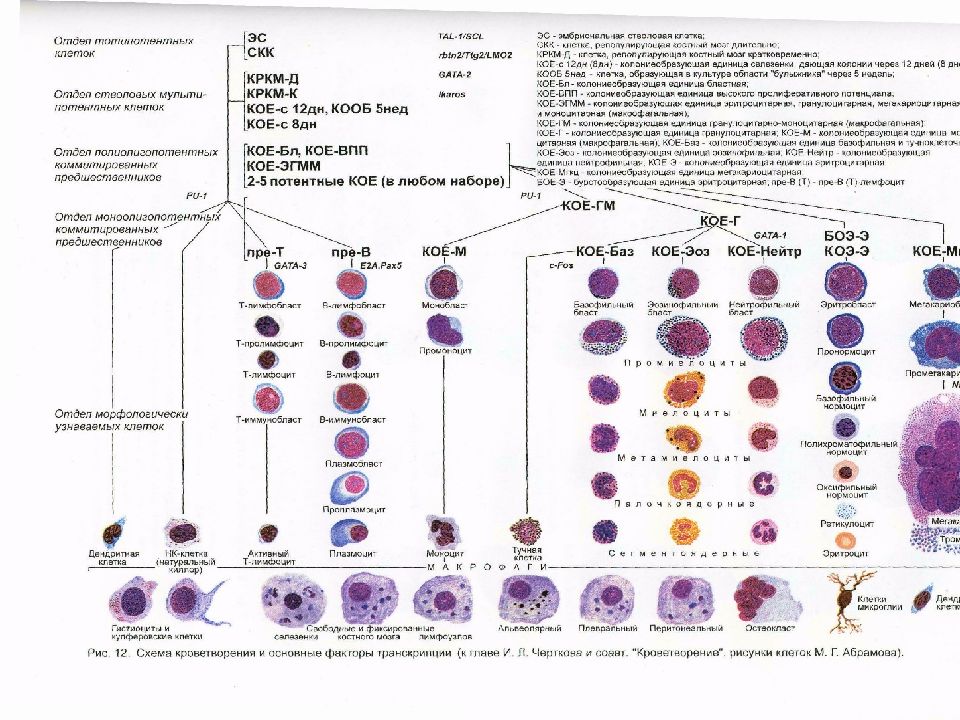
Максимов А.А. в 1908г впервые высказал представление о наличии единой клетки-предшественницы для всех ростков кроветворения – впоследствии СКК – стволовая клетка крови.
Слайд 6: Клеточный состав костного мозга %
Клеточный состав костного мозга – 50 – 250 кл в 1 мкл Мегакариоциты - 0,2-0,6 Бласты – 0,1 -1,6% Миелобласты – 0,2-1,7 Лимфоциты- 4,3-13,7 Промиелоциты – 1,0-4,1 Моноциты – 0,7-3,1 Миелоциты – 7,0 – 12,2 Метамиелоциты – 8,0- 15,0 Палочкоядерные – 12,8-23,7 Сегментоядерные 13,1-24,1 Всего нейтрофильного ряда- 52,7-68,9 Эозинофилы – 0,5-5,8 Базофилы – 0-0,5 Эритробласты - 0,2-1,1 Пронормоциты - 0,1-1,2 Нормоциты базофильные -1,4-4,6 Нормоциты полихроматофильные 8,9-16,9 Нормоциты оксифильные - 0,8-5,6 Всего клеток эритроидного ряда – 14,5 – 26,5 ЛЭС – 2,1 – 4,5
Слайд 7: Распространенность гемобластозов
Суммарная частота гемобластозов : 25–30 случаев на 100 000 населения в год Наиболее распространены неходжкинские лимфомы (10–12 случаев ). В последние 20–30 лет частота неходжкинских лимфом постоянно увеличивается, заболеваемость другими гемобластозами находится на стабильном уровне.
Слайд 8: Распределение гемобластозов
Все онкогематологические заболевания, за исключением острого лимфобластного лейкоза, лимфобластной лимфомы и лимфомы Беркитта, значительно чаще возникают у взрослых Некоторые нозологические формы (хронический лимфолейкоз, множественная миелома, истинная полицитемия, сублейкемический миелоз ) развиваются только в пожилом возрасте. Острый лейкоз основное злокачественное заболевание у детей. Большинство гемобластозов, особенно лимфопролиферативные заболевания, достоверно чаще возникают у европеоидов (прежде всего у семитов – арабов и евреев), существенно реже – у негроидов и крайне редко – у лиц азиатского происхождения
Слайд 9: Этиологические (предрасполагающие) факторы гемобластозов
В основе - первичная мутации кроветворной клетки-предшественницы под действием мутагенов – хромосомные поломки. Ионизирующая радиация. Химические соединения. Генетические заболевания (7% всех опухолевых больных, в семьях с ОЛ заболеваемость выше в 3-4 раза). Связь с аутоиммунными заболеваниями, наследственными и приобретенными иммунодифицитами. Вирусы. Длительное воздействие бактериальных Аг + Возрастное истощение противоопухолевого иммунитета (гена 53, ответственного за апоптоз ). предшествующие заболевания системы кроветворения (рефрактерные формы анемий, пароксизмальная ночная гемоглобинурия, так называемые миелодисплазии ).
Слайд 10: Патогенез онкогематологических заболеваний
Гемобластозы возникают вследствие мутации клетки-предшественницы, приводящей к клональной неопластической пролиферации злокачественно трансформированных кроветворных клеток на любом уровне их дифференцировки ( полипотентность )!!, характеризующихся: 1) блокадой дифференцировки; 2) способностью к неограниченному делению – увеличенное количество митозов . 3) большей продолжительностью жизни, поэтому они быстро накапливаются в организме
Слайд 11: Патогенез онкогематологических заболеваний ( продолжени е)
При лабораторных признаках лейкозов в организме больного имеется около 10 11 бластных клеток, при развитии клинических симптомов – 10 12 бластов (1кг ). При злокачественных лимфомах клинические симптомы (прежде всего – лимфоаденопатия ) появляются при значительно меньшем объеме опухолевой массы Развитие большинства клинико-лабораторных проявлений (анемия, геморрагический синдром, лихорадка, увеличение размеров лимфатических узлов, селезенки) обусловлено “вытеснением” нормальной гемопоэтической ткани опухолевыми клетками или выделением факторов, тормозящих эритро - и тромбоцитопоэз.
Слайд 12: Патогенез онкогематологических заболеваний (окончание)
Для гемобластозов характерна опухолевая прогрессия: по мере развития заболевания появляются клоны более злокачественных клеток с новыми свойствами (морфологическими, цитохимическими, иммунологическими и т.д.), что объясняет развитие резистентности к ранее эффективному лечению. Злокачественные клетки активно метастазируют за пределы органов кроветворения, что приводит к развитию опухолевой инфильтрации внутренних органов, лимфатической ткани, кожи, слизистых оболочек, оболочек и вещества головного и спинного мозга и может сопровождаться органомегалией, функциональной недостаточностью внутренних органов, лимфоаденопатией, гиперпластическим гингивитом, лейкемидами кожи, нейролейкозом и т.д.
Слайд 13
Острые лейкозы – группа клональных заболеваний системы крови, первично поражающих костный мозг, морфологическим субстратом которых являются злокачественно трансформированные бластные клетки, неспособные к нормальной дифференцировке до зрелых клеточных форм, с вытеснением ими нормальных элементов и инфильтрацией ими различных органов и тканей.
Слайд 14
Все острые лейкозы возникают из одной мутировавшей клетки, которая может относиться как к очень ранним, так и коммитированным в направлении различных линий кроветворения. Клиническое течение острого лейкоза, терапия, эффективность лечения и прогноз заболевания определяются: 1) принадлежностью бластных клеток к той или иной линии кроветворения, 2) степенью их дифференцировки, 3) степенью вытеснения нормальных ростков кроветворения обуславливают
Слайд 15
Острые лейкозы – отдельная группа онкогематологических заболеваний, которые никогда не трансформируются в хронические лейкозы. Острый лейкоз – прежде всего диагноз морфологический. Острый лейкоз может быть первичным и вторичным ( после цитостатической или лучевой терапии ). Острый лейкоз составляет 3% всех злокачественных опухолей человека. Частота острых лейкозов в среднем составляет 7,7-13,0 случаев на 100 000 населения в год и приблизительно одинакова в различных регионах. Соотношение М:Ж при ОЛ = 13,2 : 7,7
Слайд 16
Выделяют два вида заболевания, которые различаются по морфологии, течению, характеру проводимой химиотерапии и результатам лечения: 1) Ос трый лимфобластный лейкоз (80–90% в структуре лейкозов детей) 2) острые ( нелимфобластные, миелобластные ) лейкозы (в 80% случаев развиваются у взрослых) Среднее соотношение ОМЛ : ОЛЛ = 6:1
Слайд 17: FAB - классификация острых лейкозов
В 1976 году группой экспертов Франции, США и Великобритании ( FAB ) была предложена классификация ОЛ, которая основана на 1) морфологических, 2) цитохимических особенностях, 3) иммунофенотипировании бластных клеток В соответствии с FAB - классификацией 8 типов ОМЛ (М0–М7) и 3 типа ОЛЛ ( L 1– L 3). Классификация ВОЗ 1991г учитывает цитогенетические и молекулярно-генетические показатели, основана на меньшем количестве клеток, позволяет выделить ряд подтипов, биологических подгрупп, тем самым индивидуализировать лечение больных.
Слайд 18
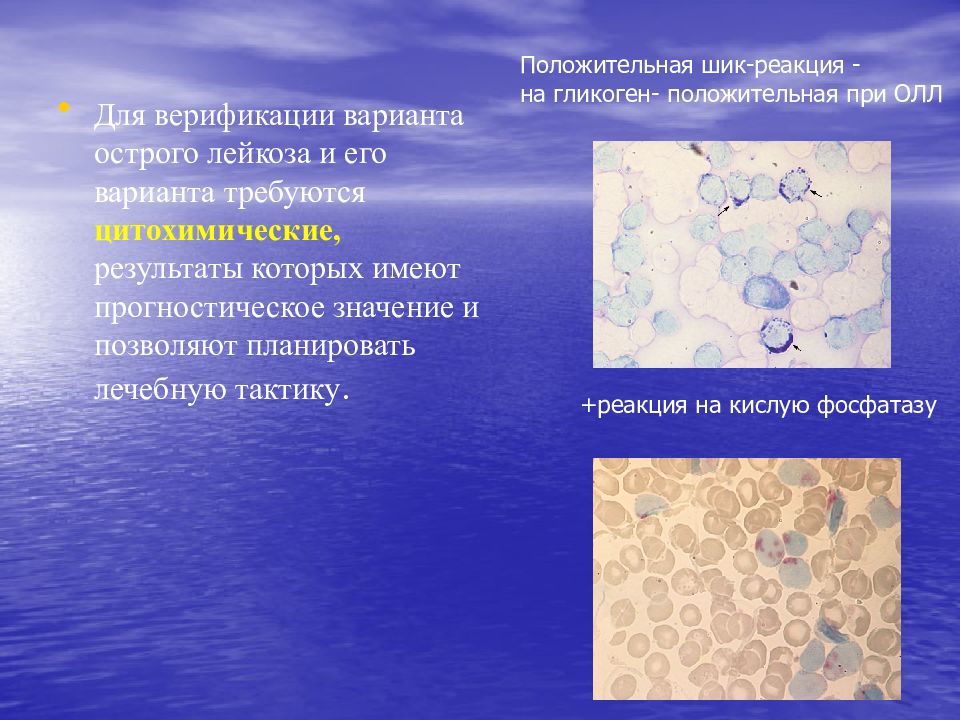
Для верификации варианта острого лейкоза и его варианта требуются цитохимические, результаты которых имеют прогностическое значение и позволяют планировать лечебную тактику. Положительная шик-реакция - на гликоген- положительная при ОЛЛ +реакция на кислую фосфатазу
Слайд 19: Иммунофенотипирование
Внедрение в практику моноклональных антител позволило идентифицировать специфические рецепторы, антигены и другие молекулы (маркеры) на мембране и/или в цитоплазме бластных клеток. В настоящее время идентифицировано более 200 маркеров, получивших название кластеров дифференцировки ( CD ). Иммунофенотипирование необходимо для 1) подтверждение диагноза 2) установление диагноза при сомнительных морфологических и цитохимических результатах 3) мониторинг для выделения новых более злокачественных клеток; 4) разделение ОЛ на различные прогностические группы Пример: острый недифференцированный лейкоз - HLA-DR +, CD15+|-, CD13+\-, CD33+\-
Слайд 20: Иммунофенотипическая характеристика ОМЛ
Иммуноподвариант лейкоза Клеточный фенотип частота М0- малодифференцированный лейкоз HLA-DR+, CD15+|-, CD13+\-, CD33+\- М1-миелобластный лейкоз без созревания HLA-DR+\-, CD38+|-, CD11a+\-, RFB1+\- CD53 М2-миелобластный лейкоз с созреванием HLA-DR+\-CD72+,CD38+\-,CD53+ М3-промиелоцитарный лейкоз CD53+,RFB1+\-,CD11b+\- М4- миеломонобластный HLA-DR+,CD15+,CD38-, М5-монобластный HLA-DR+,CD11b+,CD15 М6-эритромиелоз HLA=DR+\-,CD38-, М7-мегакариобластный CD38+,CD41+,HLA-DR+\-
Слайд 21: Иммунологические и цитогенетические варианты острых лимфобластных лейкозов
Тип и частота Иммунофенотип Цитогенетические нарушения Пре- преВ -ОЛЛ (ранний пре- преВ 5-10% и Common 45% HLA-DR,TdT+, CD34+, CD10+\-,CD19+,cIg-,sIg-,CD20-\+,CD24+\- T(12,21)d 20-25%,t(9,22),11g23 Пре-В-ОЛЛ – 20% HLA-DR, CD19,CD20+\-,CD24,CD9,CD10,CD34- T(1,19) В-ОЛЛ – 4-5% HLA-DR,CD19,CD20,CD22,CD24 T(8,14),t(2,8),t(8,22) Т-ОЛЛ -20-31% HLA-DR+\-,CD1,CD2,CD3,CD5,CD7, T(1,14)d 15-25%
Слайд 22: Цитогенетическое исследование
У 90% больных ОЛ находят генетические поломки ( транслокации, делеции, инверсии, гиперплоидию …). При ОЛЛ транслокация (9;22) или (4;11) – фактор неблагоприятного прогноза. Гиперплоидия характерна для благоприятного течения ОЛ (часто у детей с ОЛЛ).
Слайд 23: Основные клинические синдромы при ОЛ
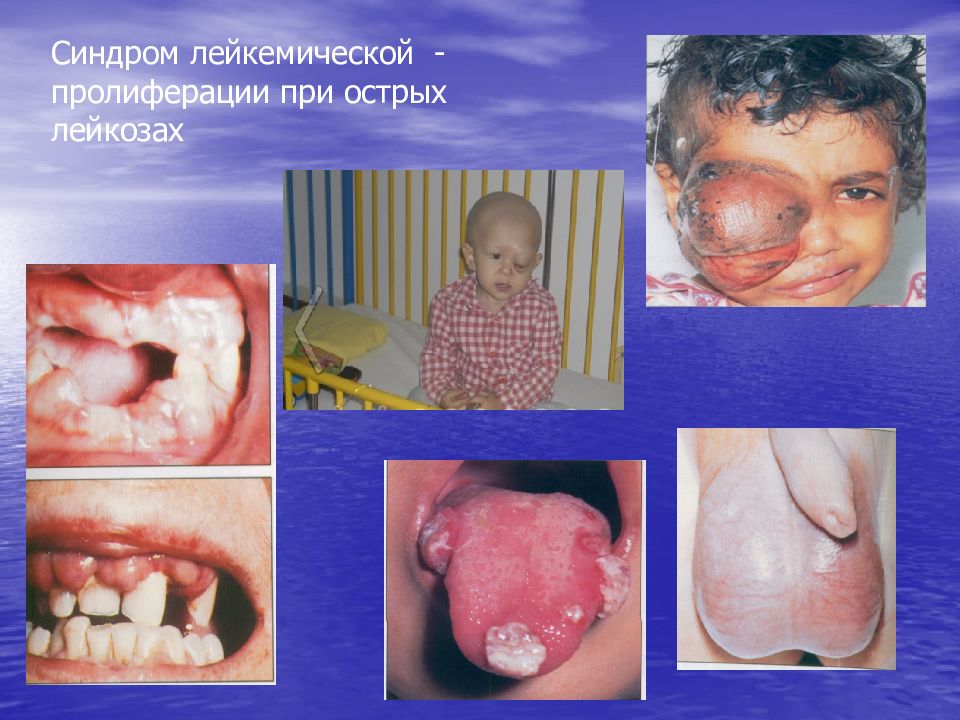
Синдром лейкемической пролиферации: лимфоаденопатия, гепатоспленомегалия, расширение средостения; инфильтрация десен и яичек, лейкемиды кожи; поражение мозговых оболочек и черепно-мозговых нервов ( нейролейкоз – чаще при ОЛЛ) Синдром опухолевой интоксикации (снижение массы тела, общая слабость, усиленная потливость, повышение Т тела, болезненность костей) Анемический синдром (бледность, тахикардия, одышка) Геморрагический синдром ( экхимозы, петехии, внутренние кровотечения), ДВС-синдром Синдром инфекционных осложнений (стоматит, некротизирующая ангина пневмония, сепсис, абсцессы)
Слайд 25
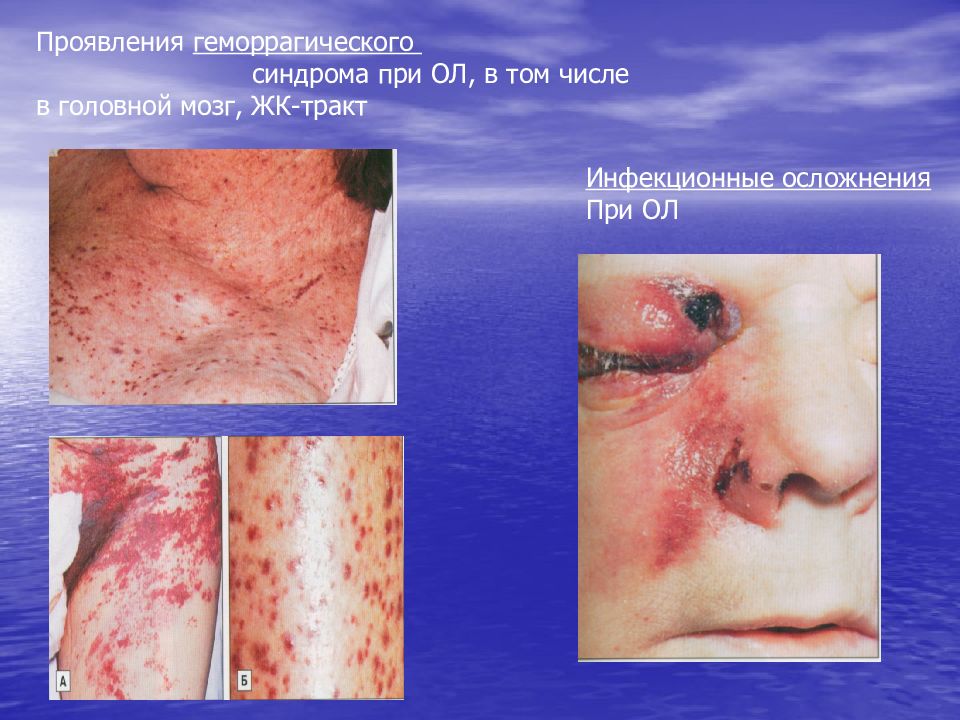
Проявления геморрагического c индрома при ОЛ, в том числе в головной мозг, ЖК-тракт Инфекционные осложнения При ОЛ
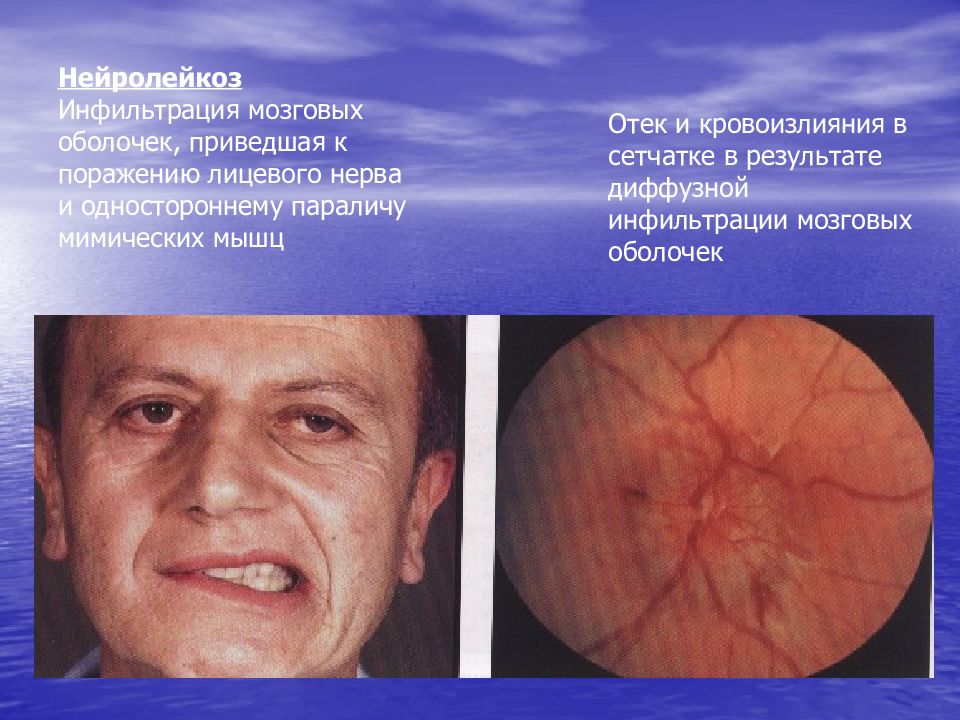
Слайд 26: Нейролейкоз Инфильтрация мозговых оболочек, приведшая к поражению лицевого нерва и одностороннему параличу мимических мышц
Отек и кровоизлияния в сетчатке в результате диффузной инфильтрации мозговых оболочек
Слайд 27: Варианты начала острого лейкоза
- примерно у 50% больных начинается остро с клиники ангины, пневмонии, инфекции мочевыделительных путей ; - у 25-30% больных постепенное начало, проявляющееся слабостью, повышенной утомляемостью, нарастанием кардиальных проявлений (анемическим синдромом), ноющими болями в суставах и мышцах ; - в 10% случаях заболевание манифестирует геморрагическими проявлениями ; - увеличение периферических лимфоузлов, селезенки, печени; - реже дебютом могут быть стоматит, мигрирующий тромбофлебит, специфические кожные проявления, внезапные параличи или парезы. - 5% (до 52 %) - выявляется при случайном исследовании крови.
Слайд 28: Особенности течения некоторых форм ОМЛ
О недифференцированный лейкоз (М0): частота его уменьшается в связи появляющимися дополнительными маркерами ОЛ при иммунофенотипировании. О. миелобластный лейкоз (М1+М2)- 50-60% всех случаев ОЛ. Заболевание чаще встречается у лиц старше 40 лет; характеризуется быстрым развитием всех синдромов: интоксикационного, анемического, геморрагического синдрома. О. Промиелоцитарный лейкоз (М3)- встречается у 5% больных. Характерно развитие тяжелого ГЕМОРРАГИЧЕСКОГО СИНДРОМА, ДВС-синдрома, при адекватной терапии которого прогноз б- го = ОЛЛ О. миеломонобластный лейкоз (М4) -15%, течение более агрессивное, чем М1. Нередко развиваются экстрамедуллярные очаги ( нейролейкз, лейкемиды кожи, гипертрофический гингивит).
Слайд 29
О. монобластный лейкоз (М5) – 10%, клиника схожа с М4, экстрамедуллярные очаги встречаются еще чаще- до 30%. . О. Эритромиелоз (М6)- 5%. –острый эритробластый лейкоз – болезнь Ди Гульельмо. Начальным проявлением может быть анемия. В костном мозге картина напоминает В12-дефицитную анемию. Помогает диагностике увеличение % бластных клеток. Нередко встречаются «ревматические» симптомы: серозиты, артралгии; лечение менее эффективно. О. Мегакариоцитарный лейкоз (М7) – наиболее редкая форма острого лейкоза, характерно развитие миелофиброза, затрудняющее получение костного мозга. Нередко развивается гипертромбоцитоз.
Слайд 30
О. Лимфобластный лейкоз – 10-15% (до 25%) взрослых больных ОЛ, (85% детей). Характено частое развитие синдрома лейкемической пролиферации и нейролейкоза. Интоксикационный, анемический, геморрагический и синдром инфекционных осложнений встречаются значительно реже. Более чем у 50% больных встречаются изменения кариотипа: при этом гиперплоидия сопровождается хорошим ответом на терапию. Особенно неблагоприятно течение при наличии филадельфийской хромосомы. Лечение ОЛЛ проводится по другим программам химиотерапии, поэтому д/д между ними строго обязателен.
Слайд 31: Клинический анализ крови
Количество лейкоцитов периферической крови чаще остается на сублейкемическом уровне и не превышает 20–30х10 9 /л (может варьировать в очень широких пределах (от 1х10 9 /л до 200х10 9 /л ) - т ромбоцитопения (менее 50х10 9 /л) - у 25-50% больных - нормохромная нормоцитарная анемия на момент диагностики заболевания имеется у большинства больных
Слайд 32: Пример клинического анализа крови больного ОЛ
Гемоглобин – 79г/л; эритроциты – 2,8 × 10.12; цветовой показатель- 0,9; лейкоциты – 10.0 × 10.9; Базофилы – 0%; эозинофилы – 0%; Бласты – 37%; Промиелоциты – 0% Миелоциты – 0% Метамиелоциты – 0% нейтрофилы палочкоядерные - 1%; сегментоядерные – 12%; (1300), лимфоциты -45%; моноциты – 5%. Тромбоциты – 30.000 “лейкемический провал” - hiatus leukaemicus
Слайд 33
В типичных случаях между бластами и зрелыми гранулоцитами отсутствуют промежуточные формы клеток нейтрофильного ряда (“лейкемический провал” или hiatus leukaemicus ). При уровне лейкоцитов свыше 100х10 9 /л резко повышается риск развития лейкостатических осложнений ( неврологические нарушения, острый респираторный дистресс -синдром, у мужчин – приапизм ). Биохимическое исследование: повышение уровня ЛДГ, мочевой кислоты.
Слайд 34: Клинический анализ крови- ( морфологическое исследование)
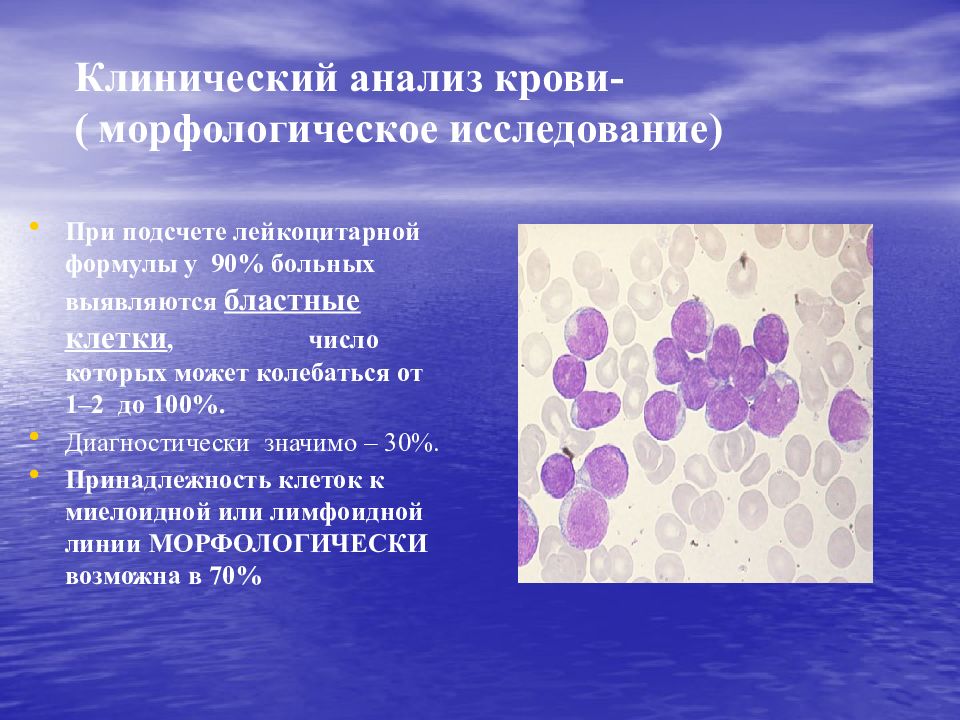
При подсчете лейкоцитарной формулы у 90% больных выявляются бластные клетки, число которых может колебаться от 1–2 до 100 %. Диагностически значимо – 30%. Принадлежность клеток к миелоидной или лимфоидной линии МОРФОЛОГИЧЕСКИ возможна в 70%
Слайд 35: Проведение костномозговой пункции обязательно!!!
Иглы для проведения пункции: Игла Кассирского Современные иглы
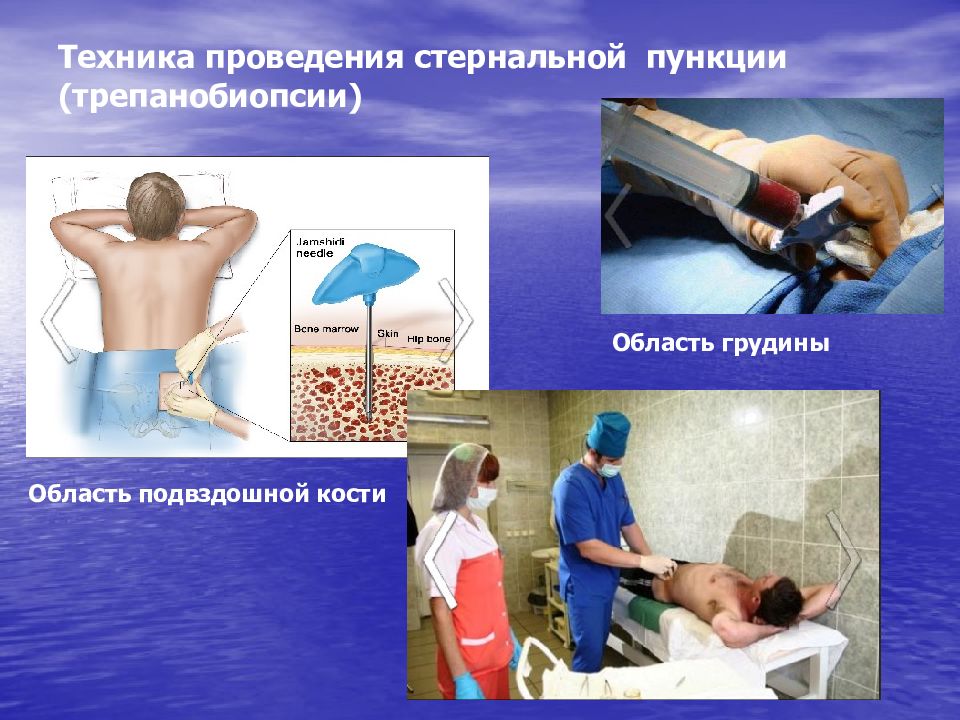
Слайд 36: Техника проведения стернальной пункции ( трепанобиопсии )
Область грудины Область подвздошной кости
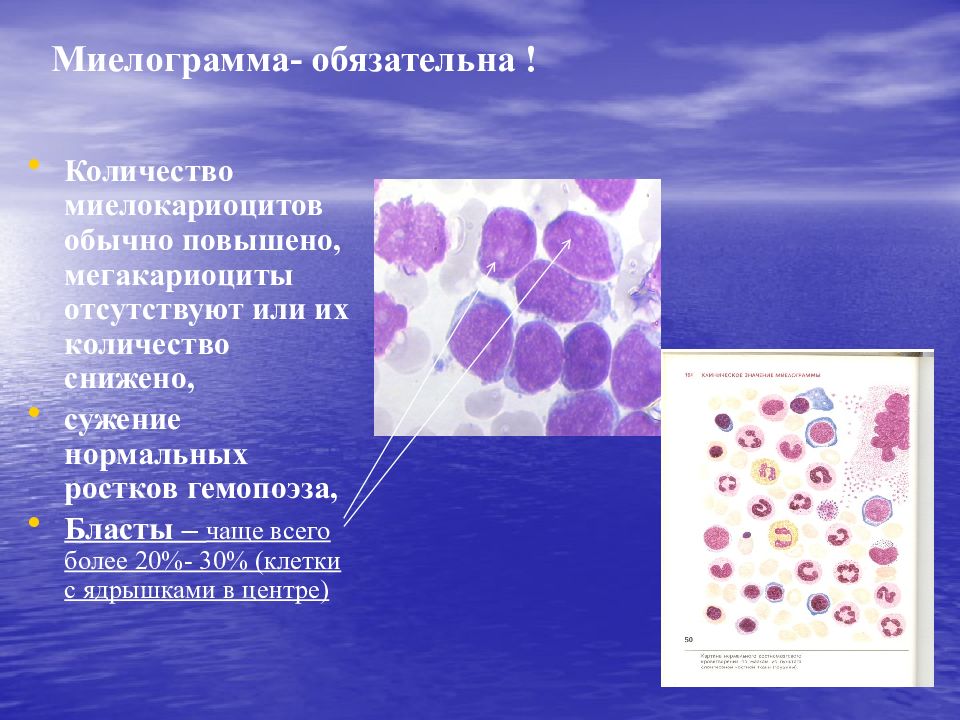
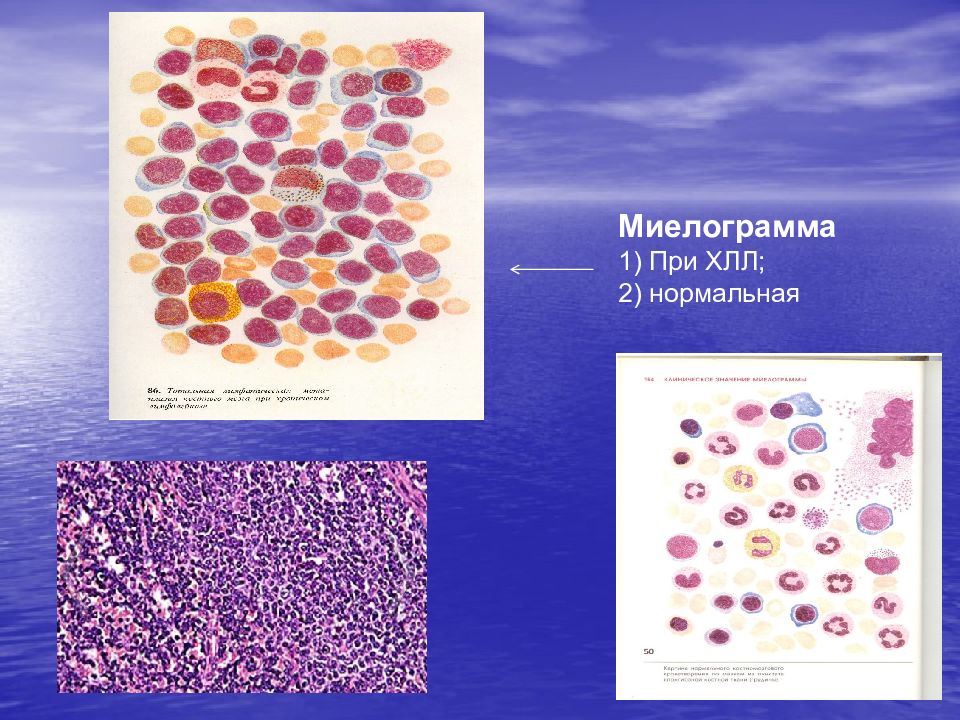
Слайд 37: Миелограмма - обязательна !
Количество миелокариоцитов обычно повышено, мегакариоциты отсутствуют или их количество снижено, сужение нормальных ростков гемопоэза, Бласты – чаще всего более 20%- 30 % (клетки с ядрышками в центре)
Слайд 38: Для проведения морфологического исследования используются:
1 Клетки периферической крови 2 Мазки-отпечатки лимфоузла (опухоли) на предметном стекле 3 Пункционная аспирационная биопсия лимфоузла или тотальная биопсия 4 Цитологическое исследование костного мозга: миелограмма, трепанобиопсия с иммунофенотипированием клеток, 5 Цитологическое исследование биожидкостей (спинно-мозговой ликвор, плевральная жидкость)
Слайд 39
Существует правило: необходимо в течение всей жизни больного ОЛ хранить пунктаты костного мозга и мазки периферической крови, так как под влиянием проводимой цитостатической терапии картина крови и костного мозга становится нетипичной для ОЛ (в препаратах появляются так называемые терапевтические бласты с более грубым ядром и их практически нельзя отличить от лимфоцитов). При повторных обращениях больного в другие лечебные учреждения диагноз ОЛ может быть подтвержден лишь при изучении первичных препаратов.
Слайд 40: Стадии острого лейкоза
I. Первая атака (первый острый период) – время от первых проявлений заболевания до определения результатов индукционной химиотерапии. II. Полная ремиссия – ≥ 4-х недель отсутствуют клинические и гематологические признаки ОЛ: а) без очагов экстрамедуллярного лейкемического роста; б) в периферической крови отсутствуют бластные клетки, количество нейтрофилов > 1,5х109/л, тромбоцитов > 100х109/л; в) имеется достаточная клеточность костного мозга (>20% по данным трепанобиопсии ); г) в миелограмме бластов <5%, представлены все ростки кроветворения с нормальным созреванием.
Слайд 41: Стадии острого лейкоза ( окончание )
III. Рецидив – появление клинических и гематологических признаков ОЛ после полной ремиссии различной длительности. - снижение количества нормальных клеток или появление бластов в периферической крови; - изолированный экстрамедуллярный рецидив ( нейролейкоз, лейкозная инфильтрация яичка и др.). При бластозе костного мозга >5% диагностируется костномозговой рецидив. Выделяют ранний (длительность полной ремиссии <12 месяцев) и поздний (продолжительность полной ремиссии >18 месяцев) рецидив. IV. Терминальная стадия – полная резистентность к проводимой терапии с ближайшим неблагоприятным исходом.
Слайд 42: Дифференциальный диагноз ОЛ
1 - заболевания, не являющимися гемобластозами : инфекционный мононуклеоз, Апластическая анемия, В12-дефицитная анемия. 2 - Гемобластозы : Хронический лейкоз в стадии бластного криза, Миелодиспластический синдром Неходжкинские лимфомы в ст. лейкемизации Лейкемоидные реакции Солидные опухоли через 2-3 года после ЛТ или ХТ 3. Метастазы в костный мозг
Слайд 43
Прогностические факторы при острых миелоидных лейкозах: 1) Значимые: - возраст более 60 лет – неблагоприятный прогноз; - хромосомные нарушения: т(8,12) – высокая частота полных ремиссий, длительная выживаемость; - вторичные лейкозы – прогноз неблагоприятный. 2) Менее значимые: другие FAB – варианты лейкоза (М4-М7) – неблагоприятный прогноз.; - общесоматический статус (более 50% - благоприятный прогноз) - лейкоциты более 50 в микролитре – благоприятный; - наличие палочек Ауэра – благоприятный прогноз.
Слайд 44
Прогностически неблагоприятные факторы при остром лимфобластном лейкозе: - возраст более 35 лет; - лейкоцитоз более 300 в 1 микролитре; - достижение ремиссии более чем за 4 недели; - хромосомные аномалии (т9;22) и т (4;11); - В-иммунологический вариант лейкоза.
Слайд 45: Лечение острого лейкоза
1 исторический этап – 19 – начало 20 века – определение нозологической формы и отсутствие какого-либо лечения. Длительность жизни больных – около 3 месяцев !! 2 этап – с начала 40-х годов 20 века начали использовать гемотрансфузии, достигали отдельных клинических ремиссий. 3 этап – 1948 год, первое клиническое применение аминоптерина – цитостатика, антагониста фолиевой кислоты – привело к первой полной клинико-гематологической ремиссии. В настоящее время – программная (протокольная) система использования химиотерапевтических препаратов. Заслуга во внедрении программной терапии ОЛ принадлежит академику АМН Воробьеву АИ
Слайд 46: Принципы химиотерапии острых лейкозов
1. Лечение необходимо начинать сразу же после установления диагноза, ( не только морфологического, но по результатам иммунофенотипирования, цитогенетики, молекулярно-биологического исследования) поскольку при отсутствии терапии продолжительность жизни пациентов не превышает трех месяцев. 2. Терапия должна проводиться в специализированном гематологическом стационаре, оснащенном асептическими палатами. Лечение больных острым лейкозом в терапевтическом отделении недопустимо!!!
Слайд 47
3. Выбор схемы лечения определяется морфологическим, цитохимическим и иммунофенотипическим, цитогенетическим вариантом острого лейкоза. 4. В большинстве случаев используется ПХТ: так как цитостатики действуют на определенные стадии клеточного митотического цикла, изменение протокола проведения схемы недопустимо!
Слайд 48: Основные методы лечения ОЛ
1 Цитостатическая терапия – уничтожение лейкозного клона ; - восстановление нормального кроветворения 2 Трансплантация костного мозга 3 Сопроводительная терапия ( для уменьшения риска осложнений ) 4 Лейкоферез
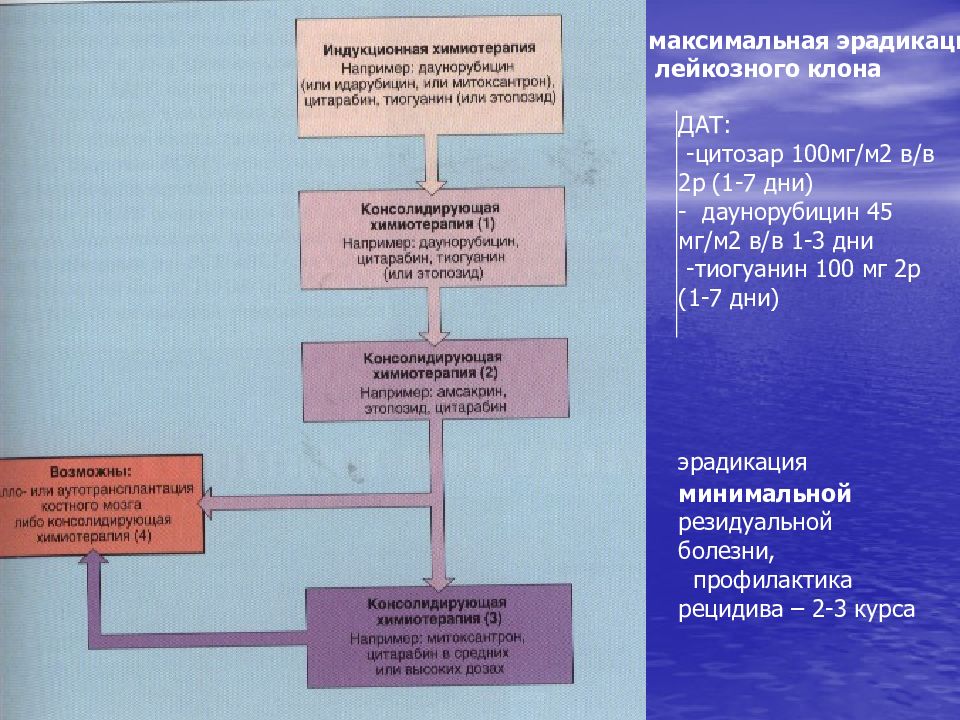
Слайд 49
максимальная эрадикация лейкозного клона эрадикация минимальной резидуальной болезни, профилактика рецидива – 2-3 курса ДАТ: -цитозар 100мг/м2 в/в 2р (1-7 дни) - даунорубицин 45 мг/м2 в/в 1-3 дни -тиогуанин 100 мг 2р (1-7 дни)
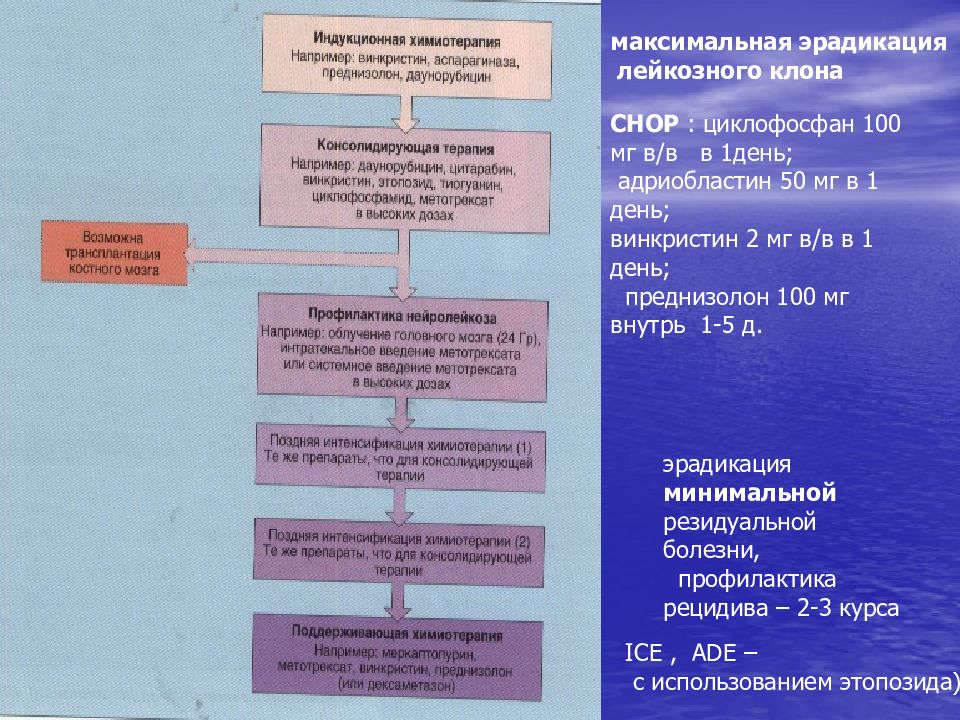
Слайд 50
максимальная эрадикация лейкозного клона эрадикация минимальной резидуальной болезни, профилактика рецидива – 2-3 курса CHOP : циклофосфан 100 мг в/в в 1день; адриобластин 50 мг в 1 день; винкристин 2 мг в/в в 1 день; преднизолон 100 мг внутрь 1-5 д. ICE, ADE – с использованием этопозида)
Слайд 51: Сопроводительная терапия лейкозов:
1 – Дезинтоксикационная терапия (физиологический раствор, полиглюкин, форсированный диурез и др.) 2 – Гемокомпонентная терапия ( переливание тромбоцитарной массы, эритроцитарной массы, очень редко лейкоцитов) 3 – Коррекция метаболических нарушений ( плазмоферез, гемосорбция и др.) 4 – Лечение инфекционных осложнений (антибактериальные, противогрибковые, противовирусные средства ) 5 – Аллопуринол для лечения антилейкоцитозного синдрома. Антиэметическая терапия
Слайд 52: Осложнения острых лейкозов
1. Инфекционные осложнения (у 70% больных определяют летальные исходы). Для их профилактики за 1-2 дня до начала ХТ назначают противогрибковые препараты; - с момента начала ХТ начинают неадсорбируемый а/б: бисептол, офлоксацин, канамицин. - поводом для начала комбинированной а/б терапии является подъем Т тела до 38 градусов, отмеченная 2 или более раз в сутки, при исключении других причин для ее развития.
Слайд 53
2 Геморрагический синдром - выраженная тромбоцитопения – у 1\2 больных - летальность от ГС – 5-10% - кровоизлияния в головной мозг, желудочно-кишечный тракт, легочные кровотечения. - Показания для переливания тромбомассы : а) при наличии признаков кровотечения на фоне тромбоцитопении, б) при уровне ТР - 30 × 10.9 + инфекционные осложнения, В) при уровне ТР до 10 × 10.9 без признаков инфекции и повышенной кровоточивости.
Слайд 54
3 Анемический синдром - анемия встречается у всех больных ОЛ, - основной метод лечения – переливание эритроконцентрата или отмытых эритроцитов. - Показания к переливанию эритромассы : - снижение Нв ниже 70 г/л и гематокрита 14-30% ; - снижение Нв ниже 45 г/л и Нт менее 14% требует неотложной гемотрансфузии!
Слайд 55
4 Энтеропатия Состояние, характеризующееся поражением слизистой ЖКТ, возникающее на фоне миелотоксического агранулоцитоза и проявляющееся болями в животе, вздутием живота, частым жидким стулом. - частота энтеропатии – 10%. 5 Синдром лизиса опухоли - имеет место при гиперлейкоцитозе более 100тыс и органомегалии. -быстрый лизис опухоли выбрасывает в кровь мочевую кислоту и биогенные амины, блокирующих микроциркуляцию и повреждающих мембраны клеток, в результате развиваются ОПН, дистресс -синдром, мозговая кома. - больным перед ПХТ проводят гидратацию, - назначают аллопуринол, лазикс, - с помощью гидроксимочевины снижают лейкоцитоз до 20.000 до начала ПХТ.
Слайд 56
6 Нейролейкоз - частота при ОЛЛ – 30-50%; при ОНЛЛ- 5%. Клинические варианты: а) менингеальные симптомы – 70%, б) очаговое поражение головного мозга -5%, в) изолированное поражение черепно-мозговых нервов – 20%, г) полирадикулоневрит – 5%. - основной критерий нейролейкоза – повышенный цитоз спинномозговой жидкости за счет бластоза. - развитие нейролейкоза ухудшает прогноз ОЛ.
Слайд 57
Современная химиотерапия позволяет получить полные ремиссии у 50–95% взрослых больных В большинстве случаев через 3-4 года развивается рецидив. 5-летняя безрецидивная выживаемость при химиотерапии составляет 20–25% для ОМЛ, 30% для ОЛЛ. У больных после лечения острого лейкоза значительно чаще возникают соматические опухоли.
Слайд 58
Выписка из истории болезни Николаева Л.Г, 74г, пенсионерка Доставлена в НИИ Скорой помощи июнь 2007г бригадой СП в связи с учащением приступов стенокардии. Диагноз: Острый коронарный синдром
Слайд 59: Жалобы при поступлении:
- боли в области сердца, сжимающего характера, возникающие при спокойной ходьбе через 100-200м, уменьшающиеся после приема валидола или нитроглицерина, которые участились до 10 раз в сутки; - выраженная общая слабость; - головокружения при попытке выполнить какую- либо нагрузку; - отсутствие аппетита, снижение настроения, плохой сон. Анамнез заболевания : описанные жалобы беспокоят больную последний месяц, прогрессивно нарастают. К врачам не обращалась. В анамнезе в 2004 году – мастэктомия с последующим курсом пероральной цитостатической терапии.
Слайд 60
Состояние больной при поступлении средней степени тяжести: Субфебриллитет ; Астенизирована, несколько заторможена. Кожа бледная, единичные мелкоточечные геморрагические высыпания на коже нижних конечностей, синячки разной степени давности и размеров. Пастозность голеней. Периферические лимфоузлы не увеличены. Пульс 108 в минуту, единичные экстрасистолы АД 140 и 100 мм рт ст. Тоны сердца приглушены. Печень + 2,0см; селезенка не увеличена. Признаки дисциркуляторной энцефалопатии 2 ст. Грубой очаговой неврологической симптоматики не выявляется. Состояние после правосторонней мастэктомии, рубец без особенностей. ЭКГ- распространенная субэпикардиальная ишемия в области левого желудочка.
Слайд 61
Анализ крови клинический : Нв – 65 г/л ; Эритроциты – 2,0 × 10 12 ; цв.п. – 0,97; Лейкоциты – 0,45 × 10 9 ; Бласты – 37%; Промиелоциты – 0% Миелоциты – 0% Метамиелоциты – 0% нейтрофилы палочкоядерные -3 %; сегментоядерные – 20% = 0,096 × 10 9 ; лимфоциты 30%; Моноциты – 10% тромбоциты - 34 × 10 9 ; СОЭ - 73 мм/час Больная переводится для дальнейшего лечения в гематологическое отделение Александровской больницы.
Слайд 62: Клеточный состав костного мозга %
Клеточный состав костного мозга – 50 В 1 мкл Мегакариоциты - 0,2-0,6 1/259 Бласты – 0,1 -1,6% Миелобласты –( 0,2-1,7) - 5 7,6 % Лимфоциты- 4,3% Единичные палочки Ауэра Промиелоциты – 1,0-4,1 1,2 Моноциты – 0,7-3,1 Миелоциты – 7,0 – 12,22,6 2,6 Метамиелоциты – 8,0- 15,0 2,2 Палочкоядерные – 12,8-23,7 3,4 Сегментоядерные 13,1-24,1 2,8 Всего нейтрофильного ряда- 52,7-68,9 - 12,2% Эозинофилы – 0,5-5,8 Базофилы – 0-0,5 Эритробласты- 0,2-1,1 Пронормоциты- 0,1-1,2 0,6 Нормоциты базофильные -1,4-4,6 5,4 Нормоциты полихроматофильные 8,9-16,9 Нормоциты оксифильные - 0,8-5,6 Всего клеток эритроидного ряда – 14,5 – 26,5 -- 7,7% ЛЭС – 5,1
Слайд 63
1) Цитохимическое исследование бластных клеток: Реакция на гликоген ++++, на липиды + миелопероксидазу 100т характерно для PAS - реакция слабо + клеток миелоидного ряда 2) По данным иммунофенотипирования бластных клеток выявлена популяция трансформированных клеток с общим фенотипом CD7, CD13, CD15, CD33, CD34, CD38, HLA-DR, что более всего соответствует ОМЛ, вариант М1-М2. 3) При цитогенетическом исследовании выявлены множественные хромосомные поломки
Слайд 64: Диагноз больной Николаевой Л.Г
Острый миелобластный лейкоз (вариант М1-М2), вторичный, первый острый период. Прогностический индекс – неблагоприятный Общесоматический статус менее 50% Вторичные острые лейкозы чаще миелобластные. Острый миелобластный лейкоз (М1+М2) составляет 50-60% всех случаев ОЛ. Заболевание чаще встречается у лиц старше 40 лет; характеризуется быстрым развитием интоксикационного, анемического, геморрагического синдрома. Прогноз – неблагоприятный.
Слайд 65
Прогностические факторы при острых миелоидных лейкозах: 1) Значимые: - возраст более 60 лет – неблагоприятный прогноз; - хромосомные нарушения: т(8,12) – высокая частота полных ремиссий, длительная выживаемость; и другие … - вторичные лейкозы – прогноз неблагоприятный. 2) Менее значимые: другие FAB – варианты лейкоза (М4-М7) – неблагоприятный прогноз.; - общесоматический статус (менее 50% - неблагоприятный прогноз) - лейкоциты более 50 в микролитре – благоприятный; - наличие палочек Ауэра – благоприятный прогноз.
Слайд 66
В гематологическом стационаре больной проводится необходимое обследование для уточнения диагноза и сопроводительная терапия: переливание тромбо - и эритромассы, антибактериальная терапия, кардиальная терапия (нитраты, бетаблокаторы, метаболическая терапия, мочегонные препараты). На 5 сутки пребывания в стационаре у больной развивается тяжелый ангинозный приступ с ЭКГ-картиной острого распространенного инфаркта миокарда, сложных нарушений сердечного ритма, от которых больная умирает. На вскрытии : множественные кровоизлияния во внутренние органы, в том числе в миокард, перикард с небольшим количеством крови в перикарде, отек легких. Посмертное исследование костного мозга подтвердило диагноз.
Слайд 67
Лекция для 5 курса 4 факультета ФПВ на тему: « Хронические лейкозы » Лектор- доцент кафедры ВМТ Шарова Н.В.
Слайд 68: Хронические лейкозы – гетерогенная группа опухолевых заболеваний крови, морфологическим субстратом которых является неопластически трансформированная клетка костного мозга, сохраняющая определенную способность к делению, при этом длительно сохраняется нормальный гемопоэз. Вторично может происходить метастазирование опухолевых клеток из костного мозга в периферические органы (лимфоузлы, печень, селезенка и другие органы )
Слайд 69: Хронический лимфолейкоз ( хронический лимфоцитарный лейкоз - клональное лимфопролиферативное заболевание, первично локализующееся в костном мозге, субстратом которого являются зрелые лимфоциты. ( Наряду с костным мозгом вторично поражаются лимфоузлы, селезенка, печень, нервная система и другие органы)
Слайд 72: Эпидемиология
Составляет более 30% всех лейкозов в Северной Америке и Европе Ежегодная заболеваемость в этих регионах составляет 3-4 случая на 100 000 населения, а среди лиц старше 65 лет − 20 на 100 000 населения в год Средний возраст к началу заболевания составляет 55 лет, однако около 10% пациентов моложе 40 лет М:Ж = 2:1 В Европе и Северной Америке В-клеточный иммунофенотип встречается у 95-98% больных, у 2-5%− Т-клеточный · В странах Азии преобладает Т-клеточный хронический лимфолейкоз
Слайд 73: Этиология ХЛЛ
Для ХЛЛ не доказана этиологическая роль ионизирующего облучения. Для ХЛЛ животных доказана этиологическая роль вирусов. Болезнь нередко носит наследственный характер. Отмечается увеличение частоты ХЛЛ в семьях с лимфопролиферативными заболеваниями (ХЛЛ- фактор риска у родственников 1 поколения) .
Слайд 74
ХЛЛ СД 5 Клетка-предшественница лимфопоэза Костный мозг СД19 СД23,24 Патогенез ХЛЛ
Слайд 75
Патогенетические особенности ХЛЛ: - пролиферация клона трансформированных «зрелых» лимфоцитов ; в иммунофенотипе - CD 19, СД23, СД24, СД5+; - характеризуется уменьшением числа мембранных Ig, - наличием кластера СД5+, который ассоциируется с аутоиммунными феноменами (гемолитическая анемия, тромбоцитопения, тиреоидит..); - вытеснение нормального кроветворения с развитием анемии и тромбоцитопении; - в финале болезни может развиваться трансформация ХЛЛ в лимфосаркому (синдром Рихтера ); - нарушение противоопухолевого иммунитета часто приводит к развитию второй опухоли.
Слайд 76: Клиническая картина
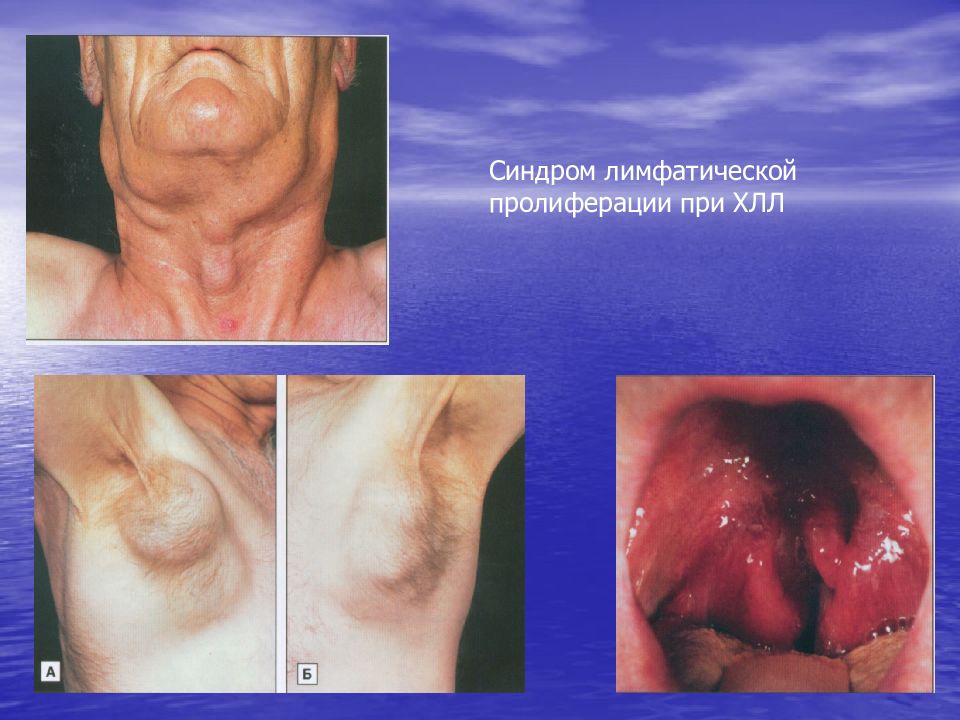
В 70% случаев заболевание начинается постепенно и характеризуется лишь абсолютным лимфоцитозом в периферической крови Основные клинические синдромы: 1. Синдром лейкемической пролиферации: - - Лимфаденопатия : - периферические лимфатические узлы имеют тестоватую консистенцию, безболезненные, не спаянные с кожей, клетчаткой и между собой, не образующие свищей; - висцеральные лимфоузлы ; - позднее появляется увеличение размеров селезенки и печени.
Слайд 78
2 Симптомы опухолевой интоксикации : истощение, боли в костях, повышение температуры тела. 3 Аутоиммунные осложнения : гемолитическая анемия в 25% и тромбоцитопения в 15%/, возможно сочетание с СКВ. 4 Инфекционные осложнения : бронхиты, пневмонии, сепсис, опоясывающий лишай, выраженная инфильтрация при укусе насекомых – 70 %. 5 Возможна трансформация в более агрессивную лимфому (синдром Рихтера), продолжительность жизни < 6 месяцев 30% ХЛЛ имеет индолентное течение.
Слайд 79: Лабораторные данные
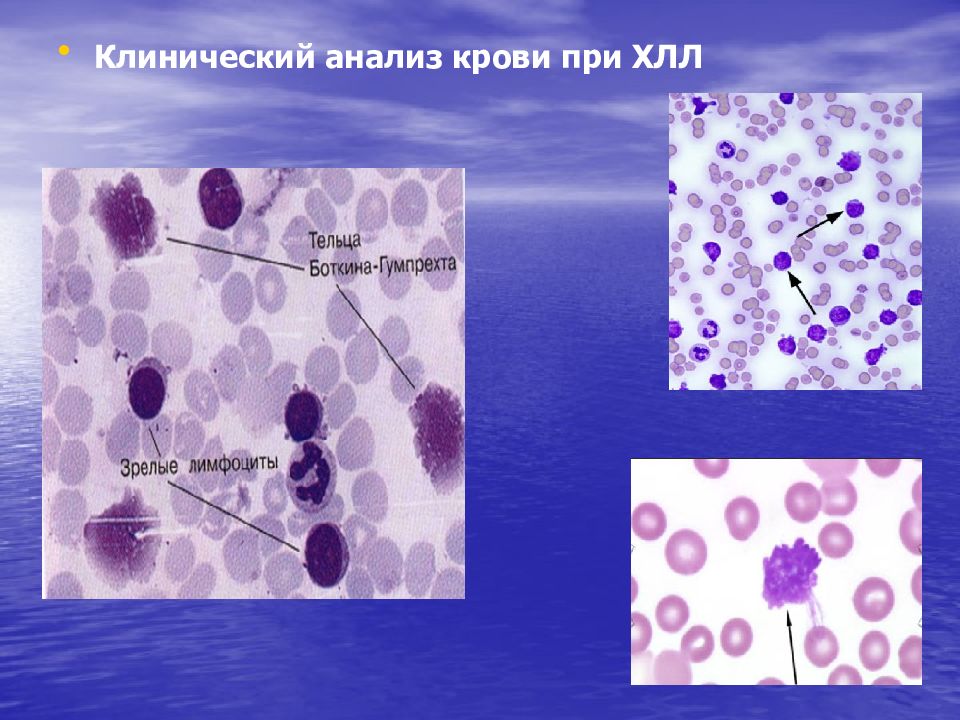
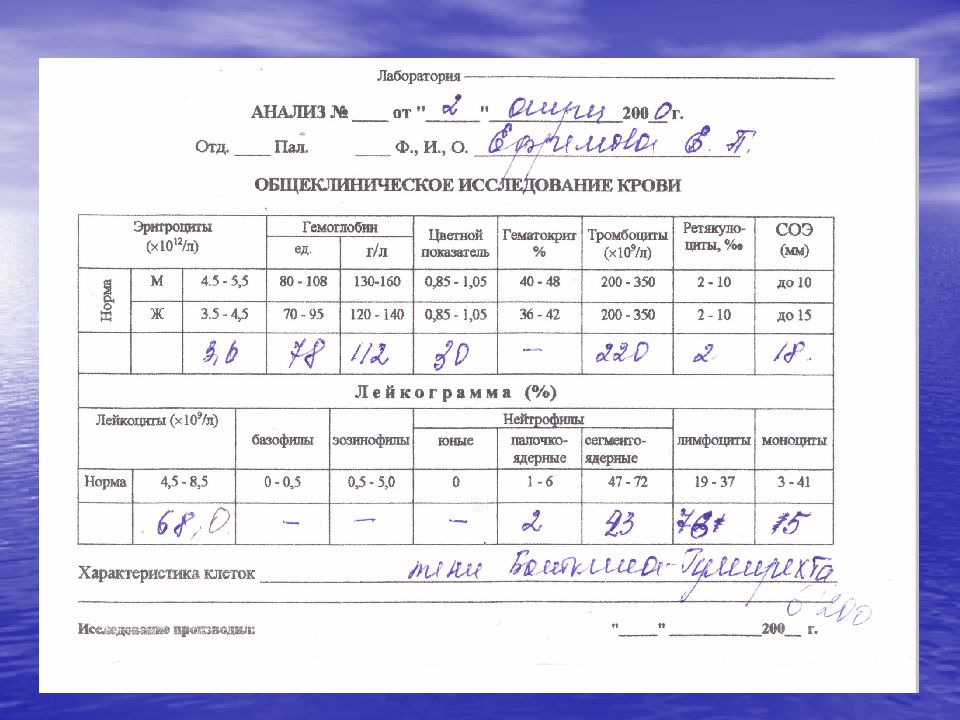
Лейкоцитоз с абсолютным ( более 5 × 10 9 / л ) и относительным лимфоцитозом; Морфологически лимфоциты не отличаются от нормальных; В ряде случаев встречаются пролимфоциты (обычно менее 10 %); Характерно наличие в мазке крови клеток Боткина- Гумпрехта (полуразрушенные ядра лимфоцитов – артефакт, образующийся при приготовлении мазка ); Снижение уровня иммуноглобулинов G, A, M. По мере прогрессирования развиваются анемия и тромбоцитопения
Слайд 80
Нормальные показатели клинического анализа крови Показатель Мужчины Женщины Лимфоциты, % 19 37 19 37 Лимфоциты, х 10 9 /л 1,5 3,5 1,5 3,5 Моноциты, % 2 10 2 10 Моноциты, х 10 9 /л 0,02 0,8 0,02 0,8 СОЭ, мм/час 1 10 2 15 Ретикулоциты, %о 2 15 2 15 Тромбоциты, х 10 9 /л 170 350 170 350
Слайд 84: Критерии диагноза
Абсолютный лимфоцитоз более 5 (10) 10 9 / л Нормальная морфология лимфоцитов при световой микроскопии Более 30% лимфоцитов в аспирате костного мозга ( миелограмме ) Лимфоидная метаплазия костного мозга в трепанобиоптате. Характерный иммунофенотип ( CD19+, CD20+, CD24+, CD5+, CD 23+, слабая экспрессия SIg, CD79b )
Слайд 85: Классификация Rai
Стадия Характеристика Медиана выживаемости O Только лимфоцитоз более 15х10 9 / л в крови, более 40% в костном мозге Как в популяции- 15 лет I Лимфоцитоз + увеличение лимфатических узлов 9 лет II Лимфоцитоз + спленомегалия и / или гепатомегалия независимо от увеличение лимфатических узлов 6 лет III Лимфоцитоз + уровень гемоглобина ниже 110 г / л независимо от увеличения лимфатических узлов и органов 1, 5 года IV Лимфоцитоз + количество тромбоцитов ниже 100х10 9 / л независимо от увеличения лимфатических узлов и органов < 1,5 года
Слайд 87: Критерии для начала лечения
( Рано начатое лечение не увеличивает продолжительность жизни больных !!!) Симптомы интоксикации (потливость, снижение веса) Анемия или тромбоцитопения в связи с инфильтрацией костного мозга Аутоиммунная анемия или тромбоцитопения Симптомы компрессии в связи с массивной лимфаденопатией или спленомегалией Удвоение абсолютного лимфоцитоза менее, чем за 12 месяцев Лимфоцитоз периферии более 150 х10 9 / л. Повышенная частота инфекций Продвинутая стадия заболевания ( C по классификации Binet, III-IV по классификации Rai )
Слайд 88: Принципы лечения
Хлорбутин или циклофосфан При неэффективности − полихимиотерапия (программы COP, CHOP и др.) Преднизолон при аутоиммунной гемолитической анемии или тромбоцитопении Пуриновые аналоги ( флюдарабин по 25 мг / м 2 ) 5 дней подряд каждые 28 дней Анти CD 20 моноклональные антитела ( ритуксимаб, мабтера ) α -интерферон Трансплантация аллогенных стволовых кроветворных клеток (у молодых пациентов)
Слайд 89
В ряде случаев у больных ХЛЛ используются паллиативные методы: лучевая терапия, спленэктомия, лейкацитоферез. Лучевая терапия применяется при наличии выраженной спленомегалии или конгломерата лимфатических узлов с признаками компрессии окружающих органов. Особое значение придается профилактике и лечению инфекционных осложнений. Больные ХЛЛ должны избегать укусов пчел и комаров.
Слайд 90
Темпы прогрессирования хронического лимфолейкоза широко варьируют: продолжительность жизни колеблется от 2-3 до 30 лет и более Средняя продолжительность жизни составляет 5-7 лет
Слайд 91
«В течение последних двух десятилетий ХЛЛ из неизлечимого заболевания превратился в заболевание, которое в большинстве случаев при своевременном начале можно успешно лечить, продлевая жизнь и соматическое благополучие больных, и которое в настоящее время стало принципиально излечимым».
Слайд 93
Диагноз: хронический лимфолейкоз, 1 стадия по Rai, доброкачественная форма. Тактика ведения больного выжидательная. С 2005 года у больного рецидивируют простудные заболевания (3-4 раза в год); появились слабость, потливость. При очередном осмотре больного размеры периферических лимфоузлов увеличились до 3-5 см в диаметре, пальпируется увеличенная селезенка ниже края левой реберной дуги на 3 см (при УЗИ =15,0см). В анализе крови лейкоцитоз 80,5 х10 9 / л, 88% лимфоцитов; гемоглобин – 103г/л, проба Кумбса+. В трепанобиоптате – пролиферация лимфоцитарного ростка.
Слайд 94
ДИАГНОЗ : хронический лимфолейкоз, 3 стадия по Rai, прогрессирующее течение, аутоиммунная гемолитическая анемия. Начата терапия преднизолоном в дозе 40 мг в сутки. Лимфоузлы уменьшились в размерах, количество лейкоцитов в периферической крови снизилось до 48,5 х10 9 / л, 82% лимфоцитов; гемоглобин – 119г/л Наблюдается гематологом ЦП ВМА.
Слайд 95: Хронический миелоидный лейкоз – клональное миелопролиферативное заболевание, характеризующееся -- поражением гемопоэза на уровне стволовой кроветворной клетки, -- увеличением продукции гранулоцитов в костном мозге и периферической крови --и наличием филадельфийской ( Ph ) хромосомы и/или химерного гена BCR / ABL
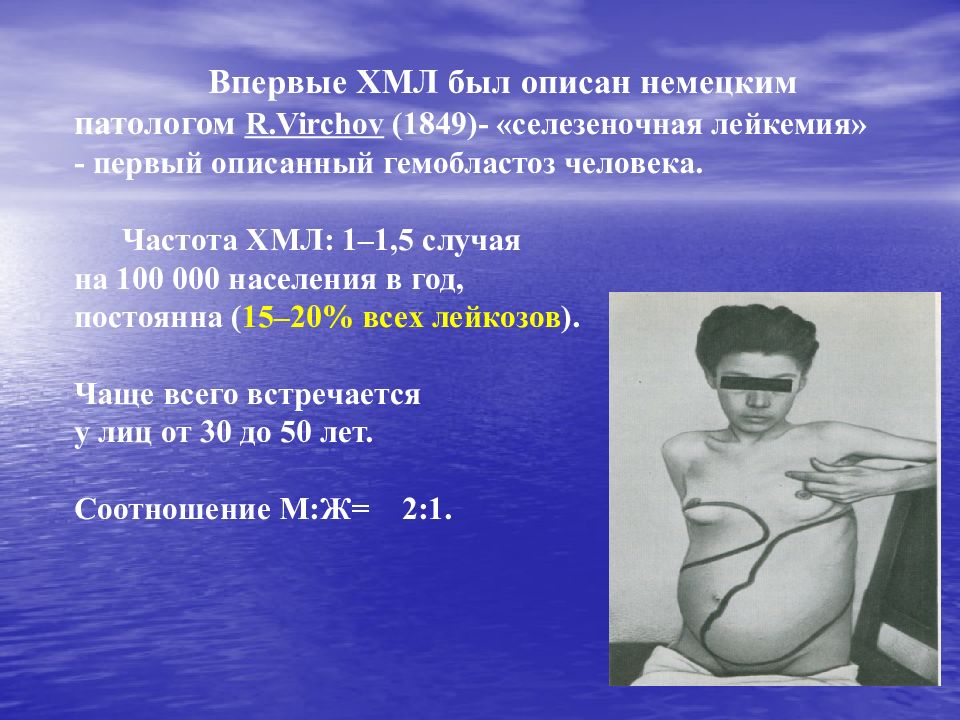
Слайд 96: Впервые ХМЛ был описан немецким патологом R.Virchov (1849)- «селезеночная лейкемия» - первый описанный гемобластоз человека. Частота ХМЛ: 1–1,5 случая на 100 000 населения в год, постоянна ( 15–20% всех лейкозов ). Чаще всего встречается у лиц от 30 до 50 лет. Соотношение М:Ж= 2:1
Слайд 98: Клеточный состав костного мозга %
Клеточный состав костного мозга – 50 – 250 кл в 1 мкл Мегакариоциты - 0,2-0,6 Бласты – 0,1 -1,6% Миелобласты – 0,2-1,7 Лимфоциты- 4,3-13,7 Промиелоциты – 1,0-4,1 Моноциты – 0,7-3,1 Миелоциты – 7,0 – 12,2 Метамиелоциты – 8,0- 15,0 Палочкоядерные – 12,8-23,7 Сегментоядерные 13,1-24,1 Всего нейтрофильного ряда- 52,7-68,9 Эозинофилы – 0,5-5,8 Базофилы – 0-0,5 Эритробласты - 0,2-1,1 Пронормоциты - 0,1-1,2 Нормоциты базофильные -1,4-4,6 Нормоциты полихроматофильные 8,9-16,9 Нормоциты оксифильные - 0,8-5,6 Всего клеток эритроидного ряда – 14,5 – 26,5 ЛЭС – 2,1 – 4,5
Слайд 99: Этиология
· - ионизирующая радиация ( в том числе индуцированная рентгенотерапией), - воздействие бензола. Патогенез У 95–97% больных ХМЛ во всех опухолевых клетках выявляется Ph -хромосома (22 аутосома с укороченным длинным плечом). При этом происходит реципрокная транслокация 9 и 22 хромосом: t (9;22) (q34; q11), в которой участвуют 2 клеточных протоонкогена – ABL ( Abelson leukemia ) и BCR ( breakpoint claster region ), расположенных соответственно на 9 и 22 хромосомах. · На 22 хромосоме образуется химерный ген BCR/ABL, кодирующий белок Р210, обладающий тирозинкиназной активностью, что приводит к : 1) увеличению пролиферации миелоидных клеток-предшественниц с нарушением их дифференцировки; 2) блокаде апоптоза. 3) подавляется нормальное кроветворение. ·
Слайд 100: Клинические стадии ХМЛ – этапы лейкозного процесса
1 - Хроническая – развернутая (ранняя и поздняя) 2 - Прогрессирующую (акселерации) 3 - Терминальная - бластный криз
Слайд 101: Хроническая = развернутая фаза ХМЛ
Начальная стадия У большинства пациентов ХМЛ диагностируется в хронической стадии, в 40-50% случаев – при отсутствии каких-либо жалоб - по анализу крови, - поводом к исследованию анализа крови могла быть спленомегалия.
Слайд 102
Основные симптомы: Признаки гиперметаболизма (снижение массы тела, потливость, анорексия ); Спленомегалия и ощущения дискомфорта в левом подреберье; Нарастание частоты инфекционных заболеваний; Анемический синдром (общая слабость, повышенная утомляемость, одышка при привычной физической нагрузке, тахикардия, учащение стенокардии ); вторичная подагра; Геморрагический синдром; симптомы, обусловленные нарушением микроциркуляции на фоне гиперлейкоцитоза
Слайд 105: Клинический анализ крови
Лейкоцитоз - в среднем более 50х10 9 /л (возможен и низкий уровень лейкоцитов – 15–20х10 9 /л ); Сдвиг “влево” за счет палочкоядерных нейтрофилов, метамиелоцитов, миелоцитов, редко – промиелоцитов ; Могут выявляться единичные бластные клетки ( прогностически неблагоприятный признак) ; Характерна эозинофильно- базофильная ассоциация; В 30% случаев – нормохромная, нормоцитарная анемия легкой степени; У 30% больных – тромбоцитоз; реже тромбоцитопения (неблагоприятный признак)
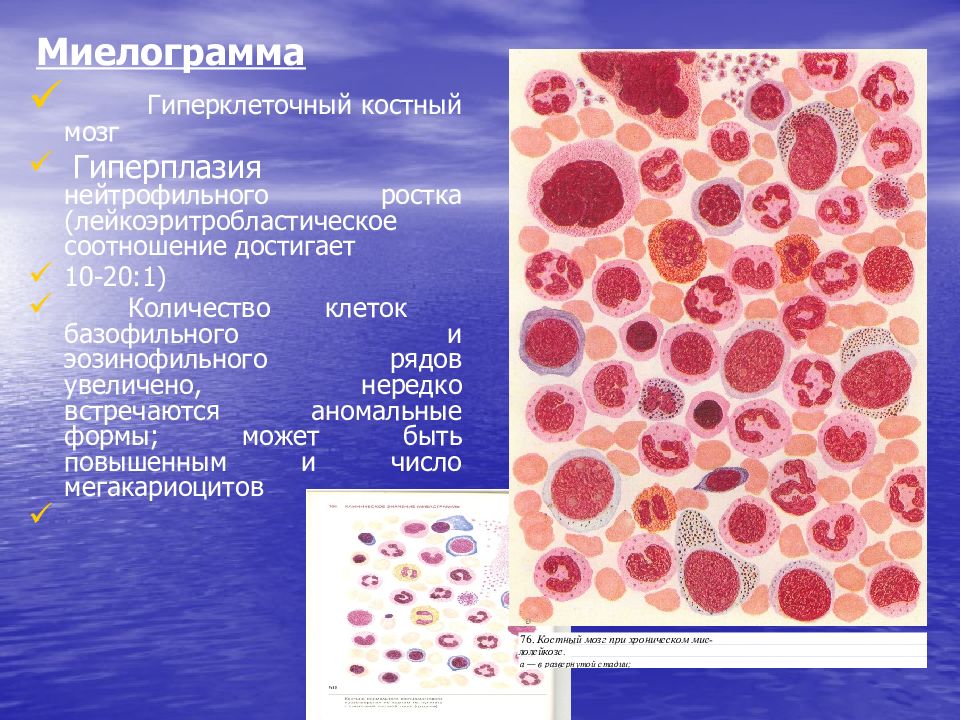
Слайд 106: Миелограмма
Гиперклеточный костный мозг Гиперплазия нейтрофильного ростка ( лейкоэритробластическое соотношение достигает 10-20:1) Количество клеток базофильного и эозинофильного рядов увеличено, нередко встречаются аномальные формы; может быть повышенным и число мегакариоцитов
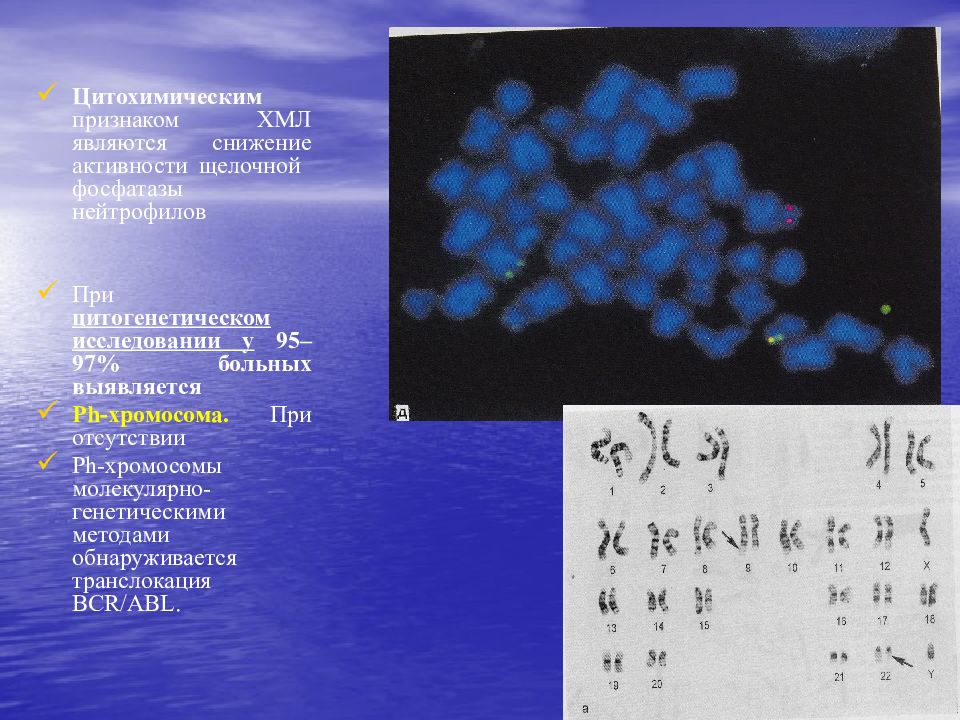
Слайд 107
Цитохимическим признаком ХМЛ являются снижение активности щелочной фосфатазы нейтрофилов При цитогенетическом исследовании у 95 – 97% больных выявляется Ph -хромосома. При отсутствии Ph -хромосомы молекулярно-генетическими методами обнаруживается транслокация BCR/ABL.
Слайд 108
На фоне адекватной химиотерапии практически у всех пациентов симптомы исчезают : - значительно уменьшается в размерах или перестает определяться селезенка, - количество лейкоцитов и лейкоцитарная формула приближаются к норме (при лечении миелосаном ) или нормализуются (при лечении препаратами гидроксимочевины ).
Слайд 109: фаза акселерации ХМЛ
В среднем через 3 года, несмотря на продолжающееся лечение цитостатиками, происходит трансформация заболевания – опухолевая прогрессия). У 2/3 пациентов развивается фаза акселерации, которая характеризуется прогрессирующей спленомегалией с возможными инфарктами селезенки, гепатомегалией ; геморрагическим синдромом, нарастанием количества гранулоцитов, нарастанием анемии, тромбоцитоза или тромбоцитопении, резистентностью к ранее эффективной терапии. Продолжительность фазы акселерации составляет 0,5–1 год.
Слайд 110: Основной лабораторный признак фазы акселерации и бластного криза – прогрессирующее увеличение количества промиелоцитов и бластов в периферической крови и костном мозге. При цитохимическом исследовании бластов у 70% пациентов определяется миелоидный тип бластного криза, у 30% – лимфоидный
Слайд 111: Терминальная фаза ХМЛ
Обычно терминальная фаза протекает в форме бластного криза В редких случаях ХМЛ впервые выявляется в период бластного криза Клиника бластного криза сходна с острым лейкозом. C наличием большого количества бластов в костном мозге и определенной клинической картиной. У 10% пациентов в терминальной стадии развиваются экстрамедуллярные очаги, состоящие из бластных клеток. Лабораторные признаки бластного криза при этом могут отсутствовать (так называемая гранулоцитарная саркома). Медиана выживаемости больных в этой фазе ХМЛ – 3 месяца
Слайд 112: Критерии диагноза ХМЛ:
Лейкоцитоз со сдвигом лейкоцитарной формулы влево Наличие промежуточных форм нейтрофилов Наличие спленомегалии Эозинофильно- базофильная ассоциация Усиленный миелопоэз в костном мозге Низкий уровень щелочной фосфатазы в нейтрофилах Обнаружение Ph - хромосомы ( гена BCR|ABL)
Слайд 113: Дифференциальный диагноз ХМЛ проводится с
- лейкемоидными реакциями, - острыми нелимфобластными лейкозами, - септическим процессом, - инфекционным (постинфекционным) лейкоцитозом, - агранулоцитозами, - нейтропениями, - инфекционным мононуклеозом, - ВИЧ-инфекцией.
Слайд 114: Принципы лечения ХМЛ
· 1. трансплантация аллогенных стволовых кроветворных клеток · 2. Химиотерапия : миелосан ( бусульфан ), препаратами гидроксимочевины ( литалир, гидреа ), · интерферон-α 3. Гливек ( иматиниб ) На стадии бластного криза лечение проводится по программе лечения острых лейкозов.
Слайд 115: Трансплантация аллогенных стволовых кроветворных клеток при ХМЛ
Аллогенная миелотрансплантация в настоящее время является единственной реальной возможностью излечить больного ХМЛ. После проведения трансплантации HLA-совместимого костного мозга в хронической фазе заболевания пятилетняя безрецидивная выживаемость отмечается у 50–70% больных. При выполнении миелотрансплантации в более далеко зашедших стадиях ХМЛ результаты заметно хуже (в фазе акселерации пятилетняя безрецидивная выживаемость < 20%, при бластном кризе – < 10%).
Слайд 117: Принципы лечения препаратами гидроксимочевины
· Задача врача – снизить и поддерживать уровень лейкоцитов в пределах 5–15х10 9 /л
Слайд 118: Гливек ( иматиниб ) специфически ингибирует протеинкиназу, продуцируемую химерным геном BCR - ABL, что приводит к блокаде пролиферации и индукции апоптоза в Ph -позитивных клетках · Гливек показан для лечения больных ХМЛ во всех фазах болезни. · Полная или частичная цитогенетическая ремиссия достигается у 50% больных в хронической фазе (при резистентности к интерферону- ), 25% пациентов в фазе акселерации и 15% – при бластном кризе ·
Слайд 120: Прогноз при хроническом миелолейкозе
Медиана выживаемости больных ХМЛ при стандартной химиотерапии составляет 3,5–4 года. Основные неблагоприятные прогностические факторы в хронической фазе: возраст в момент постановки диагноза > 60 лет наличие бластных клеток в крови ( > 3 %) и/или костном мозге ( > 5%) базофилия в крови ( > 7 %) и/или костном мозге ( > 3%) тромбоцитоз > 700х10 9 /л. Развитие фазы акселерации, а тем более бластного криза резко ухудшает прогноз
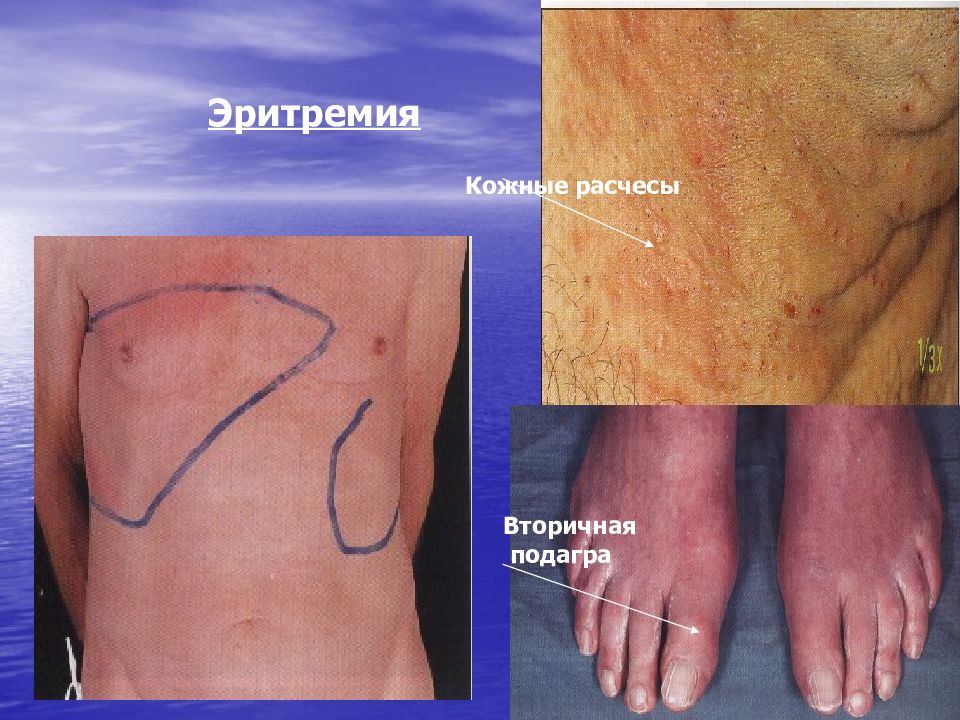
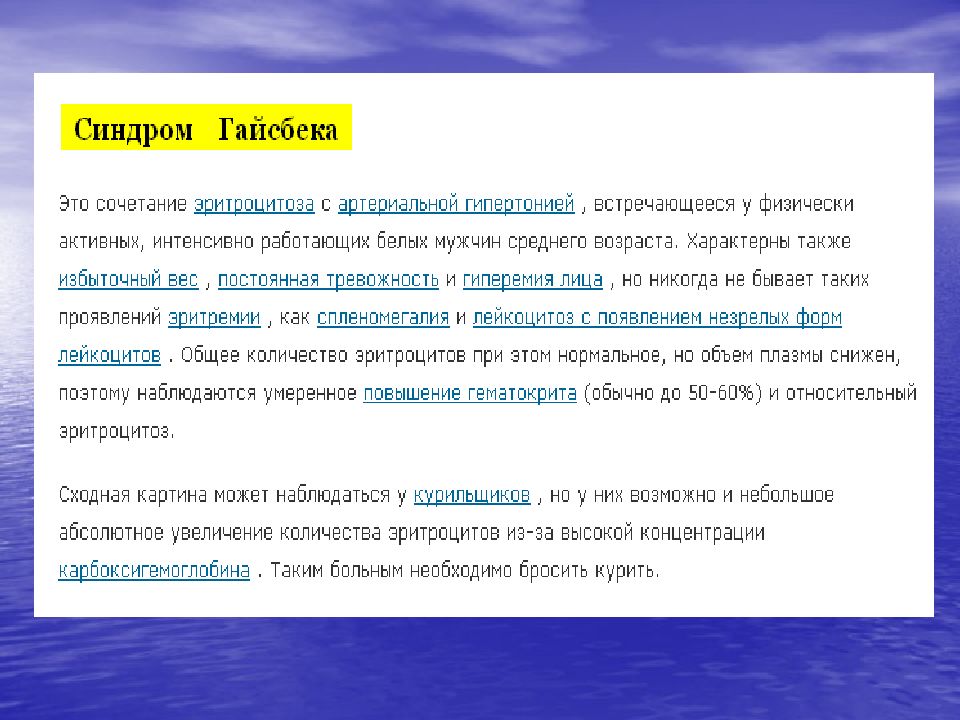
Слайд 121: Истинная полицитемия (эритремия) (болезнь Вакеза, polycythemia vera )
- доброкачественная опухоль из клетки-предшественницы миелопоэза, сохранившей способность дифференцироваться по 3 росткам кроветворения, характеризующаяся повышенной продукцией (неограниченной пролиферацией) клеток красной крови, а также лейкоцитов и тромбоцитов.
Слайд 122
Частота заболевания – 0,6 на 100 тыс населения. Преимущественно болезнь людей старше 50 лет. С одинаковой частотой болеют мужчины и женщины. У лиц еврейской национальности заболевание встречается в 3 раза чаще. Этиология болезни неясна, среди причин выделяют генетические факторы. Основа патогенеза – хромосомные поломки (в 9 хромосоме), сходные во всей группе хронических миелопролиферативных заболеваний ( JAK2 -мутации), проявляющиеся мутацией гена, приводящая к клональной пролиферации трансформированной стволовой клетки с повышенной чувствительностью к эритропоэтину и неконтролируемому их росту, вызывающие: панмиелоз, нарушение микроциркуляции, тромбозы, геморрагические осложнения. .
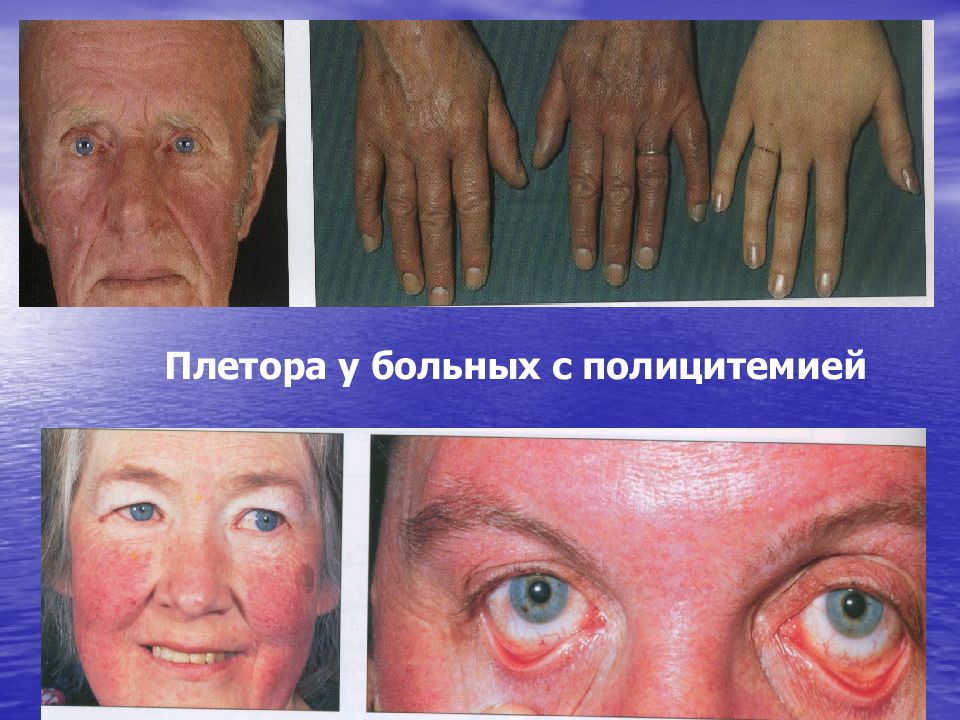
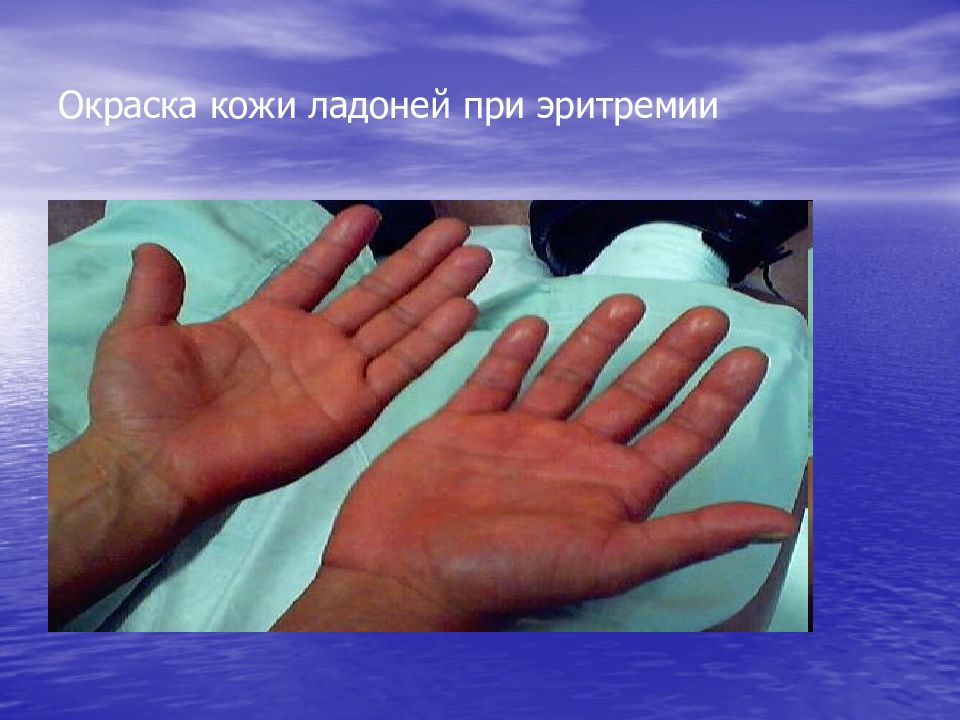
Слайд 123: Основные клинические синдромы истинной полицитемии
1) плеторический синдром; 2) генерализованный кожный зуд у 50% больных; эритроцианоз кожи; 3) спленомегалия, особенно выраженная при вторичном миелофиброзе; 4) тромбозы и тромбэмболии – причина летальных исходов у 30-40% больных; раннее прогрессирование ИБС; 5) геморрагический синдром у 30-40% больных (наклонность к носовым кровотечениям; кровоточивость десен на фоне лечения зубов); 6) неврологические нарушения в 50-60% 7)поражение периферических сосудов (эритромелалгия).
Слайд 128
СТАДИИ ИСТИННОЙ ПОЛИЦИТЕМИИ: 1 – начальная : умеренный эритроцитоз, панмиелоз в костном мозге, небольшое увеличение селезенки. Длительность – 5лет 2 – пролиферативная : выраженная плетора, сплено - и гепатомегалия, рецидивирующие тромбозы, тотальная гиперплазия костного мозга. 3 – анемическая : истощение больных, нарастающая спленомегалия, нарастает панцитопения, в костном мозге прогрессирует постэритремический фиброз. У 20-30% больных развивается вторичный острый лейкоз. Длительность жизни - 10-15 лет.
Слайд 129: Лабораторные и инструментальные методы
Анализ крови: повышение гематокрита > 55% у М, > 47% у Ж; Нв > 175г/л у М, > 155 г/л у Ж, эритроцитов > 6,0 у М, > 5,5 × 10.12; лейкоцитоз, тромбоцитоз, снижение СОЭ до 0 мм/час, дакриоцитоз (каплевидные эритроциты). Повышение активности щелочной фосфатазы Н. Увеличение концентрации витамина В12 сыворотки крови. Миелограмма : 1) в пролиферативной стадии – гиперплазия 3 ростков кроветворения, отсутствие отложения железа, признаки начинающегося фиброза; 2) в стадии истощения – неэффективный гемопоэз, фиброз, скопление мегакариоцитов.
Слайд 130: Лабораторные данные (продолжение)
Трепанобиопсия ( гиперклеточный костный мозг – 60-100%, при сочетании эритроидной гиперплазии с увеличением мегакариоцитов) Концентрация эритропоэтина в норме. рО2 не изменено. Цитогенетическое исследование – наличие «филадельфийской» хромосомы или других хромосомных поломок (9 хромосома) УЗИ для исключения эритропоэтинсекретирующих опухолей. Радиологическое исследование циркулирующей массы эритроцитов (увеличена).
Слайд 131: Современные критерии диагностики истинной полицитемии
А1.Увеличение массы циркулирующих эритроцитов более чем на 25% или повышение гемоглобина более 185 г / л для мужчин и 165 г / л для женщин А2. Отсутствие причин для вторичного эритроцитоза: - отсутствие семейного эритроцитоза - отсутствие повышение уровня эритропоэтина вследствие: а) гипоксии (артериальное рО 2 менее 92%); б) неадекватной продукции опухолью А3.Спленомегалия. А4. Клональные цитогенетические аномалии (кроме Ph -хромосомы или химерного гена BCR/ABL ) А5. Формирование эндогенных эритроидных колоний in vitro
Слайд 132: Критерии диагностики истинной полицитемии (окончание)
В1. Тромбоцитоз свыше 400 х 10 9 / л В2. Количество лейкоцитов свыше 12 х 10 9 / л В3. При трепанобиопсии обнаруживается панмиелоз с повышенной эритроидной и мегакариоцитарной пролиферацией В4. Низкий уровень эндогенного эритропоэтина. В5 Увеличение щелочной фосфатазы нейтрофилов. Диагноз истинной полицитемии правомочен: 1) при наличии критериев А1+А2 в сочетании с любым другим критерием категории А; 2) при наличии критериев А1+А2 в сочетании с любыми двумя критериями категории В.
Слайд 135: Лечение истинной полицитемии
Начинают стационарно !! 1 Уменьшение объема циркулирующей крови с помощью кровопусканий (250-500мл ч/д) 2-3 раза в неделю и поддержание Нт на уровне 42-45%, тромбоцитов ниже 400 × 10.9 2 Профилактика тромбозов – назначение дезаггрегантов (аспирин, клопидогрель, тромбо -асс, курантил ) 3 При гиперурикемии назначение аллопуринола 4 При кожном зуде – антагонисты Н1-Н2рецепторов гистамина, холестерамин, псорален 5 При необходимости проведения срочных операций – предварительная флеботомия и эритроцит аферез
Слайд 136: Лечение истинной полицитемии
Цитостатики показаны больным пожилого возраста с тяжелыми сердечно-сосудистыми осложнениями, выраженной спленомегалией, лейкоцитозом выше 15000/ мкл, тромбоцитозом более 1 000 000/ мкл. Используются гидроксимочевина ( гидреа ), интерферон-альфа, анагрелид (преимущественно угнетает опухолевый рост в мегакариоцитарном ростке), имифос, миелосан. Лечение радиоактивным фосфором.
Слайд 137
Профилактика полицитемии: исключение стрессовых нагрузок, антиаггреганты, малые дозы цитостатиков. Прогноз: продолжительность жизни при адекватном лечении составляет 7-15 лет. (при отсутствии лечения – 18 месяцев). В 20% случаев – переход в постэритремический миелофиброз (высвобождение тромбоцитарного ростового фактора). У 20-30% больных ИП в терминальной стадии развивается острый миелоидный лейкоз Причины летальных исходов: - тромбозы и тромбэмболии – 30-40%, - геморрагические осложнения – 5-10%, - неврологические расстройства – 60%, - развитие вторичного острого лейкоза – 20-30%.
Последний слайд презентации: Лекция для 5 курса 4 факультета ФПВ на тему: « Острые лейкозы » Лектор- доцент
К пункту «а» относятся злокачественные заболевания лимфоидной, кроветворной и родственных им тканей, когда эффект от проводимого лечения отсутствует или носит временный характер. К пункту «б» относятся заболевания с медленно прогрессирующим течением, длительным положительным эффектом от лечения, частотой обострений, не превышающих 1 раза в год, с сохранением способности исполнять обязанности военной службы. К пункту «в» относятся состояния после лучевой и цитостатической терапии по поводу злокачественных заболеваний. Заключение о необходимости предоставления отпуска по болезни выносится после первого курса лучевой или цитостатической терапии. Военнослужащим, проходящим военную службу по контракту и освидетельствующимся в связи с увольнением в запас, заключение выносится по пункту «а», независимо от локализации, стадии и распространенности злок процесса и времени его начала.